Спосіб лікування мезотеліоми з використанням інгібітора hdac – субероїланілідгідроксамінової кислоти (saha)
Номер патенту: 83065
Опубліковано: 10.06.2008
Автори: Чіао Джуді Х., Річон Вікторія М., Бакопулос Ніколас Дж., Міллер Томас А., Перадайз Керолін М.
Формула / Реферат
1. Спосіб лікування злоякісної пухлини у пацієнта, де пухлина являє собою мезотеліому, і де вказаний спосіб містить у собі стадію перорального введення пацієнту ефективної кількості фармацевтичної композиції, що містить субероїланілідгідроксамінову кислоту (SAHA), представлену структурою:
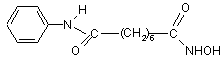 ,
,
або її фармацевтично прийнятну сіль або гідрат і фармацевтично прийнятний носій або розріджувач.
2. Спосіб за п. 1, де зазначену композицію вводять двічі на день у дозі 300 мг у розрахунку за масою SAHA періодично.
3. Спосіб за п. 2, де зазначену композицію вводять від трьох до п’яти днів на тиждень.
4. Спосіб за п. 2, де зазначену композицію вводять три дні на тиждень.
5. Спосіб за п. 1, де зазначену композицію вводять один раз на день у дозі 400 мг за масою SAHA.
6. Спосіб за п. 5, де зазначену композицію вводять протягом 14 днів з наступною перервою в 7 днів без введення.
7. Спосіб за п. 1, де зазначену композицію вводять один раз на день у дозі 300 мг із розрахунку за масою SAHA.
8. Спосіб за п. 7, де зазначену композицію вводять протягом 14 днів з наступною перервою в 7 днів без введення.
9. Спосіб за будь-яким із пп. 1-8, де SAHA є діючою речовиною.
10. Фармацевтична композиція для перорального введення, що містить субероїланілідгідроксамінову кислоту (SAHA), представлену структурою:
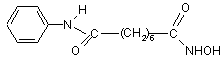 ,
,
або її фармацевтично прийнятну сіль або гідрат у кількості, ефективній для перорального лікування злоякісної пухлини, де пухлина являє собою мезотеліому, і фармацевтично прийнятний носій або розріджувач.
11. Набір, який включає в себе принаймні одне фармацевтично ефективне одиничне дозування SAHA, де фармацевтично ефективне одиничне дозування становить приблизно 300 мг, та інструкцію з лікування мезотеліоми шляхом перорального введення три дні на тиждень 300 мг SAHA двічі на день.
Текст
1. Спосіб лікування злоякісної пухлини у пацієнта, де пухлина являє собою мезотеліому, і де вказаний спосіб містить у собі стадію перорального введення пацієнту ефективної кількості фармацевтичної композиції, що містить субероїланілідгідроксамінову кислоту (SAHA), представлену структурою: O H N (CH 2)6 C C O NHOH , 2 (19) 1 3 83065 4 Даний винахід стосується способів лікування томи перитонеальної мезотеліоми можуть включазлоякісних пухлин, наприклад, мезотеліоми або ти в себе кишкову обструкцію, порушення зсілості лімфоми. Більш конкретно, - даний винахід стосукрові, анемію і лихоманку. У тому випадку, якщо ється способів лікування мезотеліоми, дифузної злоякісна пухлина поширилася за межами мезотевеликоклітинної В-клітинної лімфоми (DLBCL) або лію до інших частин тіла, симптоми можуть вклюінших видів раку або пухлин, шляхом введення чати в себе біль, порушення ковтання або припухфармацевтичних композицій, що містять інгібітори лість шиї або обличчя. HDAC (деацетилаз гістонів), наприклад, субероїПрогноз для мезотеліоми несприятливий, зі ланілід-гідроксамінову кислоту (SAHA). Фармацевслабкою реакцією на радикальне хірургічне втрутичні композиції для перорального застосування чання, існуючу в цей час хіміотерапію, променеву мають сприятливі фармакокінетичні профілі, такі терапію і комбіноване лікування. Мікроскопічне як висока біодоступність, і несподівано приводять поширення пухлинних клітин у стінку грудної клітки до високих рівнів активних сполук у крові протягом і діафрагму зустрічається часто, навіть коли таке тривалого періоду часу. поширення не може бути визначене звичайними За текстом опису різні публікації позначені тестами. арабськими цифрами в дужках. Повні посилання Лімфома являє собою рак лімфатичної систена ці публікації знаходяться в кінці опису безпосеми, сітки лімфатичних вузлів, органів (включаючи редньо перед формулою винаходу. Описи цих селезінку, тимус і піднебінні мигдалики), і судин, публікацій в їх повному обсязі включені сюди шляякі є частиною імунної системи. Існує багато різних хом посилання для більш повного опису рівня техтипів лімфом, та їх можна розділити на дві категоніки, до якого відноситься даний винахід. рії: хвороба Ходжкіна (HD) і неходжкінська лімфоРак являє собою захворювання, при якому пома (NHL). Основною відмінністю між цими двома пуляція клітин стала, у різній мірі, несприйнятликатегоріями є тип клітин, залучених до цього завою до механізмів контролю, які звичайно регулюхворювання. ють проліферацію і диференціювання. Лімфатична система с частиною імунної сисМезотеліома являє собою рідкісну форму ратеми організму і допомагає в боротьбі з інфекцією. ку, при якій злоякісні (ракові) клітини знаходяться в Це складна система, що складається з кісткового мезотелії, захисній капсулі, що покриває більшість мозку, тимуса і селезінки, і лімфатичних вузлів внутрішніх органів організму. Мезотелій являє со(або лімфатичних залоз), які сполучені сіткою дрібою оболонку, яка покриває і захищає більшість бних лімфатичних судин. Лімфатичні вузли знаховнутрішніх органів організму. Він складається з дяться в організмі всюди. двох шарів клітин: один шар безпосередньо оточує Лімфоцити являють собою лейкоцити, які цирорган; інший утворює навколо нього капсулу. Мекулюють у лімфатичній системі; вони є істотними зотелій продукує змащувальну рідину, яка вивількомпонентами імунної системи організму. Існує няється між цими шарами, даючи можливість руху два основних типи лімфоцитів: В-клітини і Торганів (такому як биття серця та розширення і клітини. Більшість лімфоцитів беруть початок із стиснення легень) для полегшення плавного руху кісткового мозку. В-клітини продовжують розвиток відносно сусідніх стр уктур. у кістковому мозку, тоді як T-клітини переміщаютьМезотелій має різні назви, у залежності від йося з кісткового мозку у вилочкову залозу і там дого локалізації в організмі. Очеревина являє собою зрівають. Після дозрівання і В-клітини, і Т-клітини мезотеліальну тканину, яка покриває більшість допомагають організму боротися з інфекцією. органів у черевній порожнині. Плевра являє собою Існує більше ніж 20 різних типів неходжкінсьоболонку, що оточує легені та вистилає стінку груких лімфом. Дифузна великоклітинна В-клітинна дної порожнини. Перикард покриває і захищає лімфома є широко розповсюдженим типом, що серце. Мезотеліальна тканина, що оточує чоловічі складає близько 40% усіх випадків. Ця злоякісна внутрішні репродуктивні органи, називається піхпухлина являє собоюпухлин у з B-лімфоцитів. Дивовою оболонкою яєчка. Серозна оболонка матки фузна В-клітинна лімфома може зустрічатися у покриває внутрішні репродуктивні органи у жінок. У будь-якому віці від юнацького до літнього. Трохи більшості випадків мезотеліома виникає в плеврі частіше зустрічається в чоловіків, ніж у жінок. або очеревині. Злоякісні пухлини, виникаючі з плеНеходжкінські лімфоми також діляться на дві врального мезотелію, тісно пов'язані зі впливом групи: низького ступеня злоякісності та високого азбесту. ступеня злоякісності. Лімфоми низького ступеня Хоча повідомлялося, що за останні 20 років злоякісності звичайно є повільно зростаючими, а збільшилася частота випадків, мезотеліома заливисокого ступеня злоякісності мають тенденцію до шається порівняно рідкісним видом раку. Майже більш швидкого росту. Дифузна великоклітинна В2000 нових випадків мезотеліоми діагностують у клітинна лімфома являє собою лімфому високого Сполучених Штата х кожний рік. Мезотеліома часступеня злоякісності та потребує негайного лікутіше зустрічається у чоловіків, ніж у жінок і ризик вання. зростає з віком, але це захворювання може з'явиОсновним лікуванням дифузної великоклітинтися як у чоловіків, так і в жінок у будь-якому віці. ної В-клітинної лімфоми є хіміотерапія. Вид хіміоЗадишка і біль у грудях унаслідок накопичення терапії залежить від ступеня розповсюдження лірідини в плеврі є частими симптомами плевральмфоми та інших чинників, таких як вік і загальний ної мезотеліоми. Симптоми перитонеальної мезостан здоров'я. Два лікарських засоби, якими звителіоми включають у себе втрату ваги і біль у чечайно лікують дифузну великоклітинну В-клітинну ревній порожнині, а також набрякання унаслідок лімфому, називаються доксорубіцин і циклофосутворення рідини в черевній порожнині. Інші симпфомід. Звичайно їх призначають разом з іншими 5 83065 6 протираковими лікарськими засобами. У цей час рвинні експлантати пухлин людини для представкомбінація, що найбільш широко використовуєтьлення більш диференційованих характеристик. ся, називається "CHOP" режим. Ця комбінація Проведені раніше дослідження встановили включає в себе лікарські засоби вінкристин і предряд полярних сполук, які були ефективними індукнізолон, а також доксорубіцин і циклофосфомід. торами диференціювання ряду трансформованих Хіміотерапію звичайно проводять амбулаторно в клітинних ліній (8, 9). Із них найбільш ефективним стаціонарі та продовжують протягом чотирьох індуктором була комбінована полярна/неполярна шести місяців. сполука N,N'-гексаметиленбісацетамід (HMBA) (9). Крім того, хіміотерапія у високій дозі з інфузіяЗастосування цієї полярної/неполярної сполуки ми кісткового мозку або стовбурових клітин була для індукції еритроїдного диференціювання еритефективною в деяких пацієнтів із рецидивом лімролейкемічних клітин миші (MELC) зі супресією фоми. Цей тип лікування включає в себе високоінонкогенних властивостей обґрунтувало застосутенсивну хіміотерапію та іноді променеву терапію. вання моделі для вивчення індукторОскільки побічні ефекти можуть бути важкими, опосередкованого диференціювання трансформодеякі типи трансплантата не застосовують у люваних клітин (5, 7-9). Кінцеве диференціювання дей старших 45-50 років, а інші можна застосовуMELC, індуковане з використанням HMBA, є багавати у людей до 65 років, які є достатньо підготовтоетапним процесом. При додаванні HMBA до леними для одержання лікування. Інтенсивність MELC (745A-DS19) у культурі існує латентний пелікування збільшує ризик серйозних побічних еферіод від 10 до 12 годин до встановлення комітуктів у людей старших за цей вік. вання. Комітування визначають як здатність клітин Променеву терапію також можна використати досягати кінцевої стадії диференціювання, незвав тих випадках, коли клітини лімфоми знаходяться жаючи на видалення індуктора (25). При продовв одній або двох ділянках лімфатичних вузлів у тій женні впливу HMBA відбувається прогресивний же частині тіла (стадія 1 або 2). Також можна зарекрутинг диференціювання клітин. Автори даного стосовувати в доповнення до хіміотерапії. винаходу представили дані про те, що клітинні Пробували застосовувати інше лікування, яке лінії MELC, стійкі до порівняно низьких рівнів вінкявляє собою моноклональне антитіло, що називаристину, стають значно більш чутли вими до індується ритуксимаб. куючої дії HMBA і можуть бути індуковані до дифеПротягом багатьох років існувало дві принциренціювання з невеликим латентним періодом або пові стратегії хіміотерапевтичного лікування раку: без нього (26). 1) інгібування гормонально-залежної проліферації HMBA здатний індукувати фенотипічпі зміни пухлинних клітин шляхом пригнічення продукції відповідно диференціюванню у великій різноманіабо периферичної дії статевих гормонів; і 2) безтності клітинних ліній (5). Характеристики ефектів, посереднє знищення ракових клітин шляхом вплиіндукованих даним лікарським засобом, були найву на них цитотоксичими речовинами, які ушкобільш вивчені в системі еритролейкемічних клітин джують як пухлинні, так і нормальні клітинні миші (MELC) (5, 25, 27, 28). Індукція диференціюпопуляції. вання MELC залежить як від часу, так і від конценНезважаючи на великі успіхи в галузі онкології, трації. Мінімальна концентрація, необхідна для більшість солідних пухлин залишаються невилікодемонстрації ефекту in vitro в більшості штамів, вними на пізніх стадіях. У більшості випадків заскладає від 2 до 3мМ; мінімальна тривалість безстосовують цитотоксичне лікування, однак воно перервного впливу, в основному необхідна для часто є дуже болючим для пацієнта, не надаючи індукції диференціювання значної частини (>20%) істотного клінічного ефекту. Необхідні менш токсипопуляції без безперервного впливу лікарського чні та більш специфічні засоби для лікування і конзасобу, становить приблизно 36 годин. тролювання злоякісних пухлин на пізніх стадіях. Первинна мішень дії HMBA невідома. Існує доАльтернативним підходом хіміотерапії раку є каз того, що протеїнкіназа C залучена до шляху індукція кінцевої стадії диференціювання пухлиндиференціювання, опосередкованого індуктором них клітин (1). На моделях клітинної культури ди(29). Дослідження, проведені in vitro, були основою ференціювання описували при впливі на клітини для оцінки потенційних можливостей HMBA як різних стимулюючи х речовин, у тому числі: циклічзасобу для клітинного диференціювання при лікуного АМФ і ретиноєвої кислоти (2, 3), акларубіцину ванні злоякісних пухлин людини (30). Була заверта інших антрациклінів (4). шена окрема І фаза клінічних досліджувань із виЄ численні вказівки на те, що пухлинна транскористанням HMBA (31-36). Клінічні досліджування формація необов'язково знищує здатність ракових показали, що ця сполука може викликати терапевклітин до диференціювання (1, 5, 6). Існує багато тичну відповідь у пацієнтів зі злоякісною пухлиною прикладів пухлинних клітин, які не реагують на (35, 36). Однак у І фазі ці клінічні досліджування нормальні регулятори проліферації і, мабуть, блотакож показали, що потенційна ефективність кують експресію своєї програми диференціювання, HMBA обмежена, зокрема, токсичністю, пов'язаі ще можуть бути індуковані до диференціювання і ною з дозою, яка перешкоджає досягненню оптиприпинення реплікації. Різні засоби, у тому числі мальних рівнів у крові та необхідністю внутрішньодеякі порівняно прості полярні сполуки (5, 7-9), венного введення величезних кількостей даного похідні вітаміну D і ретиноєвої кислоти (10-12), засобу протягом тривалих періодів часу. стероїдні гормони (13), фактори росту (6, 14), проПовідомлялося, що ряд сполук, споріднених теази (15, 16), пухлинні промотори (17, 18) та інгіHMBA, із полярними групами, розділеними непобітори синтезу ДНК або PHK (4, 19-24), можуть лярними зв'язками, на молярній основі є такими ж індукувати різні трансформовані клітинні лінії і пеактивними (37) або в 100 разів більш активними, 7 83065 8 ніж HMBA (38). Як клас, однак, було виявлено, що культурі інгібіторами HDAC, демонструють постійсиметричні димери, такі як HMBA і споріднені спону індукцію інгібітора циклін-залежної кінази р21 луки, не є найкращими засобами диференціюван(44). Цей білок відіграє важливу роль у затримці ня клітин. клітинного циклу. Вважають, що інгібітори HDAC Несподівано було виявлено, що найкращі спозбільшують швидкість транскрипції р21, передаюлуки містять дві полярні кінцеві групи, розділені чи гіперацетильований стан гістонів у ділянці гена гнучким ланцюгом метиленових груп, де одна або р21, що тим самим робить даний ген доступним обидві полярні кінцеві групи являють собою великі механізму транскрипції. Гени, експресію яких не гідрофобні групи. Переважно, полярні кінцеві групи зачіпають інгібітори HDAC, не виявляють змін ацеє різними, і тільки одна являє собою велику гідротилювання регіональних асоційованих гістонів фобну гр упу. Ці сполуки несподівано є в тисячу (45). разів більш активними, ніж сполуки, споріднені У декількох прикладах було показано, що поHMBA. рушення активності HAT або HDAC залучене до Інгібітори деацетилаз гістонів, такі як субсроїрозвитку злоякісного фенотипу. Наприклад, при ланілід-гідроксамінова кислота (SAHA), належать гострому промієлоцитарному лейкозі, онкобілок, до цього класу засобів, що мають здатність індукущо продукується злиттям PML і RAR альфа, мавати пригнічення росту пухлинних клітин, диферебуть, пригнічує специфічну генну транскрипцію нціювання і/або апоптоз (39). Ці сполуки націлені через рекрутинг HDACs (46). Таким чином, пухна механізми, перешкоджаючі переродженню пухлинна клітина не здатна завершити диференціюлинних клітин у злоякісні, оскільки вони, мабуть, не вання, що є причиною надмірної проліферації лінії мають токсичності в дозах, ефективних для прилейкозних клітин. гнічення пухлинного росту в тварин (40). Існує деУ [патентах США №№ 5369108, 5932616, кілька ліній доказів того, що ацетилювання гістонів 5700811, 6087367 і 6511990], виданих на ім'я деі деацетилювапня являють собою механізми, за яких авторів даного винаходу, описані сполуки, допомогою яких здійснюється регуляція транскриефективні для селективної індукції кінцевого дипції в клітині (41). Вважають, що ці ефекти здійсференціювання пухлинних клітин, ці сполуки манюються через зміну структури хроматину шляхом ють дві полярні кінцеві групи, розділені гнучким зміни афінності гістонових білків до спіральної ланцюгом метиленових груп або жорсткою феніДНК у н уклеосомі. льною групою, де одна або обидві полярні кінцеві Було ідентифіковано п'ять типів гістонів (погрупи являють собою велику гідрофобну гр упу. значені H1, Н2А, Н2В, Н3 і Н4). Гістони Н2А, Н2В, Деякі з цих сполук мають додаткову велику гідроН3 і Н4 виявлені в нуклеосомах, a H1 являє собою фобну груп у на тому ж кінці молекули, що і перша лінкер, розташований між нуклеосомами. Кожна гідрофобна група, яка додатково збільшує активнуклеосома у своєму ядрі містить два гістони кожність диференціювання приблизно в 100 разів у ного типу, за винятком H1, який знаходиться окреферментативному аналізі та приблизно в 50 разів мо тільки в зовнішній частині структури нуклеосоу дослідженні клітинного диференціювання. Споми. Вважається, що коли гістонові білки є соби синтезу даних сполук, що використовуються гіпоацетильованими, має місце більш висока в способах і фармацевтичних композиціях за даафінність гістону до фосфатного скелета ДНК. ним винаходом, повністю описані в наведених виТака афінність приводить до більш міцного зв'язку ще патентах, повні тексти яких включені тут як ДНК із гістоном і робить ДНК недоступною для посилання. регуляторних елементів транскрипції та механізКрім їхньої біологічної активності як протипухмів. линних засобів, недавно було встановлено, що Регуляція станів ацетилювання відбувається сполуки, описані в наведених вище патентах, є шляхом урівноваження активності між двома ферефективними для лікування або профілактики шиментативними комплексами, ацетилтрансферазою рокого ряду захворювань і станів, опосередковагістонів (HAT) і деацетилазою гістонів (HDAC). них тіоредоксином (TRX), таких як запальні захвоВважають, що стан гіпоацетилювання інгібує рювання, алергічні захворювання, аутоімунні транскрипцію асоційованої ДНК. Цей гіпоацетизахворювання, захворювання, пов'язані з окисним льований стан каталізується великими мультипростресом при захворюваннях, що характеризуються теїновими комплексами, які включають у себе фегіперпроліферацією клітин, [заявка США рменти HDAC. Зокрема, було показано, що №10/369,094, подана 15 лютого 2003]. Крім того, деацетилази гістонів (HDACs) каталізують видабуло встановлено, що ці сполуки є ефективними лення ацетильних груп із гістонів ядра хроматину. для лікування захворювань центральної нервової Вважається, що інгібування HDAC під дією системи (ЦНС), таких як нейродегенеративні заSAH A відбувається шляхом прямої взаємодії з хворювання, і для лікування злоякісної пухлини каталітичним сайтом ферменту, як показано в доголовного мозку [див. заявку США №10273401, слідженнях за допомогою рентгеноструктурної подану 16 жовтня 2002]. кристалографії (42). Думають, що в результаті Наведені вище патенти не описують особливі інгібування HDAC не відбувається генералізованокомпозиції інгібіторів HDAC для перорального го впливу на геном, а швидше, тільки зачіпає малу прийому або особливі режими дозування згаданих субодиницю геному (43). Доказ, представлений сполук, які є ефективними для лікування раку, намікроматрицями ДНК із використанням ліній злоприклад, мезотеліоми або лімфоми. Важливо, наякісних клітин, культивованих з інгібітором, покаведені вище патенти не описують пероральні комзує, що є обмежена кількість (1-2%) генів, продукти позиції, які мають сприятливі фармакокінетичні яких пошкоджені. Наприклад, клітини, оброблені в профілі, такі як висока біодоступність, яка приво 9 83065 10 дить до високих рівнів активних сполук у крові проликоклітинна лімфома" являє собою лімфому, що тягом тривалого періоду часу. характеризується незвичайно великими клітинами. Існує гостра потреба у встановленні відповідІнгібітори HDAC, придатні для застосування в них доз і режимів дозування цих сполук і розробці даному винаході, включають у себе, але не тільки, фармацевтичних композицій, переважно перорапохідні гідроксамової кислоти, жирні кислоти з кольних фармацевтичних композицій, які приводять ротким ланцюгом (SCFAs), циклічні тетрапептиди, до стабільних, терапевтично ефективних рівнів похідні бензаміду або похідні електрофільних кеактивних сполук у крові протягом тривалого перітонів, як визначено тут. Окремими необмежувальоду часу та які є ефективними для лікування раку. ними прикладами інгібіторів HDAC, придатних для Даний винахід стосується способів лікування застосування в способах за даним винаходом, є: злоякісних пухлин, наприклад, мезотеліоми або А) По хідні гідроксамової кислоти, вибрані з біслімфоми. Більш конкретно, - даний винахід стосугідроксаміду м-карбоксицинамової кислоти ється способів лікування мезотеліоми або дифуз(CBHA), трихостатину A (TSA), три хостатин у C, ної великоклітинної В-клітинної лімфоми (DLBCL), саліцилгідроксамової кислоти, азелаїншляхом введення фармацевтичних композицій, бісгідроксамової кислоти (ABHA), азелаїн-1що містять інгібітори HDAC, наприклад, субероїгідроксамат-9-аніліду (AAHA), 6-(3ланілід-гідроксамінову кислоту (SAH A). В окремих хлорфенілуреїдо) капронової гідроксамової кислоаспектах способи даного винаходу застосовують ти (3Cl-UCHA), оксамфлатину, А-161906, скриптаїдля лікування мезотеліоми. В інших аспектах споду, PXD-101, LAQ-824, CHAP, MW2796 і MW2996; соби даного винаходу використовують для лікуB) Циклічні тетрапептиди, вибрані з трапоксивання лімфоми, наприклад DLBCL. ну А (ТРХ)-циклічний тетрапептид (цикло-(LПероральні форми даних фармацевтичних фенілаланіл-L-фенілаланіл-D-піпеколініл-L-2композицій мають сприятливі фармакокінетичні аміно-8-оксо-9,10-епоксидеканоїл); FR901228 (FK профілі, наприклад, високу біодоступність, і не228, депсипептид); FR225497 циклічного тетрапепсподівано приводять до високих рівнів активних тиду; циклічного тетрапептиду апіцидину [цикло(Nсполук у крові протягом тривалого періоду часу. О-метил-L-триптофаніл-L-ізолейциніл-DДодатково, даний винахід стосується безпечного піпеколініл-L-2-аміно-8-оксодеканоїл)]; апіцидину щоденного режиму дозування цих фармацевтичIa, апіцидину Ib, апіцидину Ic, апіцидину IIа та апіних композицій, який легко дотримувати, що в рецидину IIb; CHAP, циклічного тетрапептиду НСзультаті приводить до терапевтично ефективної токсину; циклічного WF27082; і хламідоцину; кількості інгібіторів HDAC in vivo. C) Жирні кислоти з коротким ланцюгом В одному варіанті здійснення даний винахід (SCFAs), вибрані з бутирату натрію, ізовалерату, стосується способу лікування мезотеліоми або валерату, 4-фенілбутирату (4-РВА), фенілбутирату DLBCL у пацієнта, потребуючого цього, шляхом (PB), пропіонату, бутираміду, ізобутираміду, фенівведення пацієнту фармацевтичної композиції, що лацетату, 3-бромпропіонату, трибутирину, вальпмістить ефективну кількість субероїланілідроєвої кислоти і вальпроату і піванексу; гідроксамінової кислоти (SAHA) або її фармацевD) Похідні бензаміду, вибрані з СІ-994, MS-27тично прийнятної солі або гідрату, як описано тут. 275 (MS-275) [N-(2-амінофеніл)-4-[N-(піридин-3Загальна доза SAHA, яку можна вводити щодня, ілметоксикарбоніл)амінометил]бензамід] і 3'аміно складає до 800мг, переважно перорально, однопохідного MS-27-275; разово, двічі або три рази на день, безперервно E) Похідні електрофільних кетонів, вибрані з (кожний день) або періодично (наприклад, 3-5 днів трифторметилкетону і а-кетоаміду, як, наприклад, на тиждень). N-метил-a-кетоамід; і Перорально SAHA з успіхом призначали в І F) Різні інгібітори HDAC, у тому числі природні фазі клінічних досліджувань пацієнтам, страждаюпродукти, псамапліни і депудецин. чим на мезотеліому або DLBCL. Специфічні інгібітори HDAC включають у себе, Крім того, даний винахід стосується способу наприклад: субероїланілід-гідроксамінову кислоту лікування мезотеліоми або DLBCL у пацієнта, по(SAH A), представлену такою структурною формутребуючого цього, шляхом введення пацієнту фалою: рмацевтичної композиції, що містить ефективну кількість інгібітора HDAC, як описано тут, або його фармацевтично прийнятної солі або гідрату. Інгібітор HDAC можна вводити в загальній добовій дозі до 800мг, переважно, перорально, один, два або три рази на день, безперервно (тобто кожний день) або періодично (наприклад, 3-5 днів на тиждень). Піроксамід, представлений такою структурною Інгібітори HDAC і способи за даним винаходом формулою: ефективні при лікуванні різних видів раку, наприклад, лімфоми, у тому числі хвороби Ходжкіна (HD) і неходжкінської лімфоми (NHL). В одному варіанті здійснення інгібітори HDAC ефективні для лікування мезотеліоми або великоклітинної лімфоми, у тому числі дифузної великоклітинної Вклітинної лімфоми (DLBCL). Як визначено тут, "ве 11 83065 Бісгідроксамід м-карбоксицинамової кислоти (CBHA), представлений структурною формулою: Інші необмежувальні приклади інгібіторів HDAC, придатних для використання у способах за даним винаходом, являють собою: Сполуку, представлену стр уктурою: де R3 і R4 незалежно являють собою заміщену або незаміщену, розгалужену або нерозгалужену алкільну, алкенільну, циклоалкільну, арильну, алкілокси, арилокси, арилалкілокси або піридинову груп у, циклоалкільну, арильну, арилокси, арилалкілокси або піридинову груп у, або R3 і R4 зв'язані разом з утворенням піперидинової групи; R2 являє собою гідроксиламіногрупу; і n являє собою ціле число від 5 до 8. Сполуку, представлену стр уктурою: де R являє собою заміщений або незаміщений феніл, піперидин, тіазол, 2-піридин, 3-піридин або 4-піридин, а n являє собою ціле число від 4 до 8. Сполуку, представлену стр уктурою: де А являє собою амідну частин у молекули, R1 і R2 кожен вибраний із заміщеного або незаміщеного арилу, арилалкілу, нафтилу, піридинаміно, 9пурин-6-аміно, тіазоламіно, арилокси, арилалкілокси, піридилу, хінолінілу або ізохінолінілу; R4 являє собою водень, галоген, фенільну або циклоалкільну частину молекули, а n являє собою ціле число від 3 до 10. 13 12 В одному варіанті здійснення фармацевтичні композиції, що містять інгібітор HDAC, вводять перорально, наприклад, у желатиновій капсулі. Ще в одному варіанті здійснення фармацевтичні композиції додатково містять мікрокристалічну целюлозу, кроскармелозу натрію і стеарат магнію. Інгібітори HDAC можна вводити в загальній добовій дозі, яка варіює від пацієнта до пацієнта, і може бути введена в різних режимах. Придатними дозами є загальні добові дози приблизно, 254000мг/м 2, що вводяться перорально одноразово, двічі на день або три рази на день, безперервно (кожний день) або періодично (наприклад, 3-5 днів на тиждень). Крім того, дані композиції можна вводити циклами, із перервами між циклами (наприклад, лікування протягом від двох до восьми тижнів із перервою до тижня між лікуванням). В одному варіанті здійснення дану композицію вводять один раз на день у дозі приблизно 200600мг. В іншому варіанті здійснення дану композицію вводять два рази на день у дозі приблизно 200-400мг. В іншому варіанті здійснення дану композицію вводять два рази на день у дозі приблизно 200-400мг періодично, наприклад, три, чотири або п'я ть днів на тиждень. В іншому варіанті здійснення дану композицію вводять три рази на день у дозі приблизно 100-250мг. В одному варіанті здійснення добова доза становить 200мг, яку можна вводити один раз на день, двічі на день або три рази на день. В одному варіанті здійснення добова доза становить 300мг, яку можна вводити один раз на день або двічі на день. В одному варіанті здійснення добова доза становить 400мг, яку можна вводити один раз на день або двічі на день. Даний винахід також стосується способів селективної індукції кінцевого диференціювання, затримки клітинного росту і/або апоптозу пухлинних клітин, наприклад, клітин лімфоми, у пацієнта, тим самим інгібуючи проліферацію цих клітин у зазначеного пацієнта, шляхом введення пацієнту фармацевтичної композиції, що містить ефективну кількість інгібітора HDAC, наприклад, SAHA, або його фармацевтично прийнятної солі або гідрату, і фармацевтично прийнятний носій або розріджувач. Ефективна кількість інгібітора HDAC у даному винаході може складати до 800мг загальної добової дози. Даний винахід також стосується способів інгібування активності деацетилази гістонів у пацієнта шляхом введення пацієнту фармацевтичної композиції, що містить ефективну кількість інгібітора HDAC, наприклад, SAHA, або його фармацевтично прийнятної солі або гідрату, і фармацевтично прийнятний носій або розріджувач. Ефективна кількість інгібітора HDAC у даному винаході може складати до 800мг загальної добової дози. Даний винахід також стосується in-vitro способів селективної індукції кінцевого диференціювання, затримки клітинного росту і/або апоптозу пухлинних клітин, наприклад, клітин лімфоми, тим самим інгібуючи проліферацію таких клітин, шляхом взаємодії зазначених клітин з ефективною кількістю інгібітора HDAC, наприклад, SAHA, або його фармацевтично прийнятної солі або гідрату. 13 83065 14 Даний винахід також стосується in-vitro спосоєнтів після пероральної або внутрішньовенної (IV) бів інгібування активності деацетилази гістонів, дози SAHA. IV SAHA вводили інфузійно 400мг шляхом взаємодії деацетилази гістонів з ефективпротягом двох годин. Перорально SAHA вводили в ною кількістю інгібітора HDAC, наприклад, SAHA, одній капсулі 400мг. Кількість a-АсН4 показана в або його фармацевтично прийнятної-солі або гідзазначені часові точки. Експеримент представлерату. ний тричі (Фіг.5А і В). Нижні панелі: забарвлювання Даний винахід додатково стосується безпечблакитним Кумасі. ного щоденного режиму дозування лікарської суНа Фіг.6 представлене Вестерн-блот зобраміші фармацевтичної композиції, що містить інгібіження (верхні панелі), що показує кількість ацетор HDAC, який легко дотримувати і якого легко тильованого гістону-3 (a-АсН3) у плазмі крові пацідотримуватися. Ці фармацевтичні композиції підєнтів зі солідною пухлиною, після пероральної або ходять для перорального введення і ефективні внутрішньовенної (IV) дози SAHA. IV і перорально для лікування раку, наприклад, мезотеліоми, лімSAH A вводили, як на Фіг.5. Кількість a-АсН3 покафоми або інших видів раку або пухлин, шляхом зана в зазначені часові точки. Нижня панель: заселективної індукції кінцевого диференціювання, барвлювання блакитним Кумасі. затримки клітинного росту і/або апоптозу пухлинНа Фіг.7 представлене Вестерн-блот зобраних клітин, і/або шляхом інгібування деацетилази ження (верхні панелі), що показує кількість ацегістонів (HDAC). тильованого гістону-3 (a-АсН3) у плазмі крові паціЗгадані вище й інші об'єкти, істотні ознаки і пеєнтів зі солідною пухлиною, після пероральної або реваги даного винаходу будуть очевидні з наступвнутрішньовенної (IV) дози SAH A, на 1 день і на 21 ного більш докладного опису переважних варіантів день. IV і пероралыю SAHA вводили, як на Фіг.4. здійснення даного винаходу, як показано на кресКількість a-АсН4 або a-АсН3 показана в зазначені леннях, що додаються, на яких одне і те ж посичасові точки. Експеримент представлений тричі лальне позначення стосується всіх ілюстрацій. (Фіг.7А-С). Нижні панелі: забарвлювання блакитМасштаб фігур не є обов'язковим, вони ілюструним Кумасі. ють принципи даного винаходу. На Фіг.8 представлене Вестерн-блот зобраНа Фіг.1 представлене Вестерн-блот зображення (верхні панелі), що показує кількість ацеження (верхня панель), що показує кількість ацетильованого гістону-3 (a-АсН3) у плазмі крові пацітильованого гістону-4 (a-АсН4) у плазмі крові пацієнтів після пероральної або внутрішньовенної(ІУ) єнтів після пероральної або внутрішньовенної (IV) дози SAHA. IV і перорально SAHA вводили, як на дози SAHA. IV SAHA вводили 200мг інфузійно Фіг.5. Кількість a-АсН3 показана в зазначені часові протягом двох годин. Перорально SAHA вводили точки. Нижні панелі: забарвлювання блакитним 200мг в одній капсулі. Кількість a-АсН4 показана у Кумасі. зазначені часові точки. Нижня панель: забарвлюНа Фіг.9A-C представлені графіки середньої вання блакитним Кумасі. концентрації SAH A у плазмі (нг/мл) у зазначені На Фіг.2 представлене Вестерн-блот зобрачасові точки після введення. Фіг.9А: Пероральна ження (верхні панелі), що показує кількість ацедоза (200мг і 400мг) натщесерце на 8 день. Фіг.9В: тильованого гістону-4 (a-АсН4) у плазмі крові паціпероральна доза (200мг і 400мг) з їжею на 9 день. єнтів зі солідною пухлиною, після пероральної або Фіг.9С: IV доза на 1 день. внутрішньовенної (IV) дози SAHA. IV і перорально На Фіг.10 показаний період напівжиття 200мг і SAH A вводили, як на Фіг.1. Кількість a-АсН4 пока400мг пероральної дози SAHA, що спостерігаєтьзана у зазначені часові точки. Експеримент покася, на 8, 9 і 22 день. заний двічі (Фіг.2А і Фіг.2В). Нижні панелі: забарвНа Фіг.11 показана AUC (нг/мл/годину) 200мг і лювання блакитним Кумасі. 400мг пероральної дози SAHA на 8, 9 і 22 день. На Фіг.3 представлене Вестерн-блот зобраНа Фіг.12 показана біодоступність SAHA після ження (верхні панелі), що показує кількість аце200мг і 400мг пероральної дози на 8, 9 і 22 день. тильованого гістону-4 (a-АсН4) (Фіг.3А) і ацетильоНа Фіг.13 представлений KT зріз (зображення ваного гістону-3 (a-АсН3) (Фіг.3В-Е) у плазмі крові комп'ютерної томографії) мезотеліоми пацієнта до пацієнтів після пероральної або внутрішньовенної (зліва) і після (праворуч) шести місяців лікування з (IV) дози SAHA, на 1 день і на 21 день. IV і перовикористанням SAHA у дозі 300мг, двічі на день, 3 рально SAHA вводили, як на Фіг.1. Кількість aдні на тиждень. На Фіг.14 представлений KT зріз, одержаний у АсН4 або a-АсН3 показано у зазначені часові точпацієнта з дифузною великоклітинною лімфомою, ки. Нижні панелі: забарвлювання блакитним Кумадо лікування (А) і після 2 місяців лікування (В), із сі. використанням SAHA у дозі 400мг BID протягом 1 На Фіг.4 представлене Вестерн-блот зобрамісяця, у подальшому 400мг QD (щодня) протягом ження (верхні панелі), що показує кількість аце1 місяця. тильованого гістону-3 (a-АсН3) у плазмі крові паціНа Фіг.15 зображений PET зріз (зображення єнтів зі солідною пухлиною, після пероральної або позитронної емісійної томографії), одержаний у внутрішньовенної (IV) дози SAHA. IV і перорально пацієнта з дифузною великоклітинною лімфомою, SAH A вводили, як на Фіг.1. Кількість a-АсН3 покадо лікування (А) і після 2 місяців лікування (В), із зана в зазначені часові точки. Нижня панель: завикористанням SAHA у дозі 400мг BID протягом 1 барвлювання блакитним Кумасі. місяця, у подальшому 400мг QD протягом одного На Фіг.5 представлене Вестерн-блот зобрамісяця. ження (верхні панелі), що показує кількість ацеНа Фіг.16 представлений KT зріз, одержаний у тильованого гістону-3 (a-АсН3) у плазмі крові паціпацієнта з дифузною великоклітинною лімфомою 15 83065 16 до лікування (А) і після 1 місяця лікування (В) із SAH A можна вводити в загальній добовій дозі до використанням SAHA у дозі 600мг QD. 800мг, переважно перорально, одноразово, двічі На Фіг.17 представлений PET зріз, одержаний або три рази на день, безперервно (кожний день) у пацієнта з дифузною великоклітинною лімфомою або періодично (наприклад, 3-5 днів на тиждень). до лікування (А) і після 2 місяців лікування (В) із SAH A представлена такою структурою: використанням SAHA у дозі 200мг BID. Даний винахід стосується способів лікування раку, наприклад, мезотеліоми або лімфоми. Більш конкретно, - даний винахід стосується способів лікування мезотеліоми або дифузної великоклітинної В-клітинної лімфоми (DLBCL) шляхом введення фармацевтичних композицій, що містять інгібітори HDAC, наприклад, субероїланілідгідроксамінову кислоту (SAHA). В окремих аспекВ іншому конкретному варіанті здійснення датах способи даного винаходу застосовують для ний винахід стосується способу лікування мезотелікування мезотеліоми. В інших аспектах способи ліоми або DLBCL у пацієнта, що включає стадію даного винаходу застосовують для лікування лімвведення зазначеному пацієнту ефективної кільфоми, у тому числі DLBCL. кості фармацевтичної композиції, що містить інгібіПероральні форми фармацевтичних композитор деацетилази гістонів (HDAC), представлений цій даного винаходу мають сприятливі фармакокібудь-якою зі структур, описаною тут формулами 1нетичні профілі, наприклад, високу біодоступність, 51, або його фармацевтично прийнятну сіль або і несподівано приводять до високих рівнів активгідрати, і фармацевтично прийнятний носій або них сполук у крові протягом тривалого періоду розріджувач, де зазначена кількість інгібітора деачасу. Таким чином, даний винахід додатково стоцетилази гістонів є ефективною для лікування месується безпечного щоденного режиму дозування зотеліоми або DLBCL у пацієнта. цих фармацевтичних композицій, який легко доТермін "лікування" у різних граматичних фортримувати і який у результаті приводить до ефекмах відносно даного винаходу стосується профітивної кількості інгібіторів HDAC in vivo. лактики (тобто хіміопрофілактики), лікування, реВідповідно, в одному варіанті здійснення даверсії, ослаблення, полегшення, мінімізації, ний винахід стосується способу лікування мезотепригнічення або зупинки негативних впливів хволіоми або DLBCL у пацієнта, потребуючого цього, робливого стану, прогресування захворювання, шляхом введення пацієнту фармацевтичної кометіологічного фактора (наприклад, бактерій або позиції, що містить ефективну кількість інгібітора вірусів) або іншого аномального стану. Наприклад, HDAC, як описано тут, або його фармацевтично лікування може включати в себе полегшення симприйнятної солі або гідрату. Інгібітор HDAC можна птому (тобто необов'язково всіх симптомів) захвовводити в загальній добовій дозі до 800мг, перерювання або зменшення прогресування захворюважно перорально, один, два або три рази на вання. Оскільки деякі зі способів винаходу день, безперервно (тобто кожний день) або перівключають у себе фізичне видалення етіологічноодично (наприклад, 3-5 днів на тиждень). го фактора, фахівцеві в даній галузі буде зрозуміВ одному варіанті здійснення інгібітор HDAC лим, що вони однаково ефективні в ситуаціях, коявляє собою субероїланілід-гідроксамінову кислоли сполуки за винаходом вводять до або ту (SAH A). В іншому варіанті здійснення інгібітор одночасно з впливом на етіологічний фактор HDAC являє собою похідне гідроксамової кислоти, (профілактичне лікування), і в ситуаціях, коли спояк описано тут. В іншому варіанті здійснення інгібілуки за винаходом вводять після (навіть значно тор HDAC представлений однією з описаних тут пізніше) впливу на етіологічний фактор. структурних формул 1-51. В іншому варіанті здійсЛікування раку, що використовується тут, стонення інгібітор HDAC являє собою описане тут сується часткового або повного інгібування, запохідне бензаміду. В іншому варіанті здійснення тримки або запобігання прогресуванню раку, у інгібітор HDAC являє собою описаний тут циклічтому числі метастазування, інгібування, затримки ний тетрапептид. В іншому варіанті здійснення або запобігання рецидиву раку, у тому числі метаінгібітор HDAC являє собою описану тут жирну стазування; або запобігання виникненню або розкислоту з коротким ланцюгом (SCFA). В іншому витку раку (хіміопрофілактика) у ссавця, наприваріанті здійснення інгібітор HDAC являє собою клад людини. описаний тут електрофільний кетон. В іншому ваТермін "терапевтично ефективна кількість", що ріанті здійснення інгібітор HDAC являє собою детут використовується, охоплює будь-яку кількість, пудецин. В іншому варіанті здійснення інгібітор при якій досягається бажана біологічна відповідь. HDAC являє собою природний продукт. В іншому У даному винаході бажаною біологічною відповідваріанті здійснення інгібітор HDAC являє собою дю є часткове або повне інгібування, затримка або псамаплін. профілактика прогресування раку, у тому числі В одному конкретному варіанті здійснення даметастазування; інгібування, затримка або профіний винахід стосується способу лікування мезотелактика виникнення або розвитку раку (хіміопроліоми або DLBCL у пацієнта, потребуючого цього, філактика) у ссавця, наприклад людини. шляхом введення пацієнту фармацевтичної комСпосіб за даним винаходом призначений для позиції, що містить ефективну кількість описаної лікування або хіміопрофілактики людей, страждатут субероїланілід-гідроксамінової кислоти (SAHA) ючих на злоякісне захворювання. Однак також або її фармацевтично прийнятної солі або гідрату. 17 83065 18 імовірно, що даний спосіб буде ефективним при Аналізи накопичення ацетильованих гістонів лікуванні раку в інши х ссавців. добре відомі в літературі. Деацетилази гістонів та інгібітори деацетилаз [Див., наприклад, Marks, Р.A. ct al., J. Natl. гістонів Cancer Inst., 92:1210-1215, 2000, Butler, L.M. et al., Деацетилази гістонів (HDACs), як термін, що Cancer Res. 60:5165-5170 (2000), Richon, V.M. et тут використовується, являють собою ферменти, al., Proc. Natl. Acad. ScL, USA, 95:3003-3007, 1998, які каталізують видалення ацетильних груп із заі Yoshida, M. et al. J. Biol. Chem., 265:17174-17179, лишків лізину в амінокінцевих хвостах гістонів нук1990]. леосомного ядра. По суті, HDACs разом з ацетилНаприклад, ферментативний аналіз для витрансферазами гістонів (HATs) регулюють статус значення активності сполуки, що інгібує HDAC, ацетилювання гістонів. Ацетилювання гістонів може бути виконаний таким чином. Стисло, дію впливає на експресію гена та інгібітори HDACs, сполуки, що інгібує HDAC, на афінність очищеного такі як гібридна полярна сполука на основі гідроепітоп-міченого (Flag) HDACl людини можна проксамової кислоти - субероїланілід-гідроксамінової аналізувати шля хом інкубації ферментативного кислоти (SAHA), викликають затримку росту, дипрепарату у відсутності субстрату на льоду приференціювання і/або апоптоз трансформованих близно протягом 20 хвилин із зазначеною кількісклітин in vitro та інгібують ріст пухлини in vivo. Ha тю сполуки інгібітора. Можна додати субстрат ([3H] підставі структурної гомології HDACs можна роздіацетил-міченого гістону з еритролейкемічних клілити на три класи. HDACs І класу (HDACs 1, 2, 3 і тин миші), і зразок можна інкубувати протягом 20 8) мають подібність із білком RPD3 дріжджів, розхвилин при 37°С у загальному об'ємі 30мкл. Потім ташовані в ядрі та знаходяться в комплексах, асореакцію можна зупинити і можна екстрагувати виційованих із транскрипційними корепресорами. I вільнений ацетат, а кількість радіоактивної мітки, IDACs II класу (HDACs 4, 5, 6, 7 і 9) подібні з білщо вивільнилася, визначають сцинтиляційним ком HDAl дріжджів і мають як ядерну, так і циторахунком. Альтернативний аналіз, придатний для плазматичну локалізацію. HDACs і І, і II класів інгівизначення активності сполуки, що інгібує HDAC, буються інгібіторами HDAC на основі являє собою "Аналіз флуоресцентної активності гідроксамової кислоти, такими як SAHA. HDACs III HDAC; Drug Discovery Kit-AK-500", доступний від класу утворюють стр уктурно віддалений клас NADфірми BIOMOLS Research Laboratories, Inc., залежних ферментів, які відносяться до білків Plymouth Meeting, PA. SIR2 дріжджів і не інгібуються інгібіторами HDAC Дослідження in vivo можна провести таким чина основі гідроксамової кислоти. ном. Тваринам, наприклад мишам, внутрішньоІнгібітори деацетилаз гістонів або інгібітори очеревинно вводять сполуку інгібітора HDAC. ВиHDAC, як термін, що тут використовується, являбрані тканини, наприклад, головний мозок, ють собою сполуки, здатні інгібувати деацетилюселезінку, печінку і т.д. можна виділити в заздалевання гістонів in vivo і/або in vitro. По суті, HD AC гідь визначені проміжки часу після введення. Гіінгібітори пригнічують активність принаймні однієї стони можна виділити з тканин, в основному, як деацетилази гістону. У результаті інгібування деаописано [Yoshida et al., J. Biol. Chem. 265:17174цетилювання принаймні одного гістону, відбува17179, 1990]. Рівні кількості гістонів (близько 1мкг) ється збільшення ацетильованих гістонів, і накоможуть бути піддані електрофорезу на 15% SDSпичення ацетильованих гістонів є відповідним поліакриламідних гелях і перенесені на фільтри біологічним маркером для оцінки активності інгібі(одержані від Amersham). Фільтри можуть бути торів HDAC. Отже, методи аналізу накопичення блоковані 3% молоком і можуть бути зондовані ацетильованих гістонів можуть бути використані очищеним поліклональним кролячим антитілом до для визначення інгібуючої активності сполук, що ацетильованого гістону Н4 (a-Ас-Н4) і антитілом цікавлять, відносно HDAC. Зрозуміло, що сполуки, до ацетильованого гістону Н3 (a-Ас-Н3) (Upstate які можуть інгібувати активність деацетилаз гістоBiotechnology, Inc.). Рівні ацетильованих гістонів нів, також можуть зв'язуватися з іншими субстраможуть бути візуалізовані з використанням козячотами, і, по суті, можуть інгібувати інші біологічно го антикролячого антитіла, кон'югованого з перокактивні молекули, такі як ферменти. Також зрозусидазою хріну (1:5000) і хемілюмінесцентного субміло, що сполуки за даним винаходом здатні інгістрату SuperSignal (Pierce). Як навантажувальний бувати будь-які деацетилази гістонів, згадані виконтроль для гістонового білка можна використати ще, або будь-які інші деацетилази гістонів. паралельні гелі та забарвити блакитним Кумасі Наприклад, у пацієнтів, що одержують інгібіто(CB). ри HDAC, накопичення ацетильованих гістонів у 22 периферичних мононуклеарних клітинах, а також і Крім того, було показано, що інгібітори HDAC в тканинах, оброблених інгібіторами HDAC, може на основі гідроксамової кислоти активують експребути визначено в порівнянні з придатним контросію гена p21WAFI. Білок p21WAFI індукується протялем. гом 2 годин культивування з інгібіторами HDAC у Інгібуюча активність конкретної сполуки віднорізних трансформованих клітинах із використансно HDAC може бути визначена in vitro з викорисням стандартних методів. Індукція гена p21WAFI танням, наприклад, ферментативних аналізів, які пов'язана з накопиченням ацетильованих гістонів у показують інгібування принаймні однієї деацетиділянці хроматину цього гена. Таким чином, індуклази гістонів. Крім того, визначення накопичення цію p21WAFI можна розпізнати як залучення до заацетильованих гістонів у клітинах, оброблених тримки клітинного циклу Gl, викликану інгібіторами конкретною композицією, може бути встановленHDAC у трансформованих клітинах. ням інгібуючої активності сполуки відносно HDAC. 19 83065 20 Звичайно інгібітори HDAC діляться на п'ять PCT WO 98/48825]; і хламідоцин [Bosch et al., виосновних класів: 1) похідні гідроксамової кислоти; ще]. 2) коротколанцюгові жирні кислоти (SCFAs); 3) C. Похідні жирних кислот із коротким ланцюциклічні тетрапептиди; 4) бензаміди; і 5) електрогом, такі як: бутират натрію [Cousens et al., J. Biol. фільні кетони. Chem. 254, 1716-1723 (1979)]; ізовалерат [McBain Таким чином, даний винахід включає в себе et al., Biochem. Pharm. 53:1357-1368 (1997)]; валешироке коло композицій, що містять інгібітори рат [McBain et al., ви ще]; 4-фенілбутират (4-РВА) HDAC, які являють собою 1) похідні гідроксамової [Lea і Tulsyan, Anticancer Research, 15, 879-873 кислоти; 2) коротколанцюгові жирні кислоти (1995)]; фенілбутират (PB) [Wang et al., Cancer (SCFAs); 3) циклічні тетрапептиди; 4) бензаміди; 5) Research, 59, 2766-2799(1999)]; пропіонат [McBain електрофільні кетони; і/або будь-який інший клас et al., вище]; бутирамід [Lea і Tulsyan, вище]; ізобусполук, здатних інгібувати деацетилази гістонів, тирамід [Lea і Tulsyan, вище]; фенілацетат [Lea і що використовуються для інгібування деацетилаз Tulsyan, вище]; 3-бромпропіонат [Lea і Tulsyan, гістонів, індукції кінцевого диференціювання, завище]; трибутирин [Guan et al., Cancer Research, тримки клітинного росту і/або для апоптозу пух60, 749-755 (2000)]; вальпроєва кислота, вальпролинних клітин, і/або індукції диференціювання, ат і PivanexÔ . затримки клітинного росту і/або апоптозу пухлинD. Похідні бензаміду, такі як СІ-994; MS-275 [Nних клітин у п ухлині. (2-амінофеніл)-4-[N-(піридин-3Необмежувальні приклади таких інгібіторів ілметоксикарбоніл)амінометил]бензамід] [Saito et HDAC наведені нижче. Зрозуміло, що даний винаal., Proc. Natl. Acad. Sci. USA 96, 4592-4597 (1999)]; хід включає в себе будь-які солі, кристалічні струкі 3'-аміно похідне сполуки MS-275 [Saito et al., витури, некристалічні структури, гідрати, похідні, меще]. таболіти, стереоізомери, структурні ізомери і E. Похідні електрофільних кетонів, такі як проліки описаних тут інгібіторів HDAC. трифторметилкетони [Frey et al, Bioorganic & Med. А. Похідні гідроксамової кислоти, такі як субChem. Lett. (2002), 12, 3443-3447; US 6511990] і aероїланілід-гідроксамова кислота (SAHA) [Richon кетоаміди, такі як N-метил-a-кетоаміди. et al, Proc. Natl. Acad. ScL USA 95,3003F. Інші інгібітори HDAC, наприклад, природні 3007(1998)]; бісгідроксамід м-карбоксицинамової продукти, псамапліни і депудецин [Kwon et al. кислоти (CBHA) [Richon et al., вище]; піроксамід; 1998. PNAS 95:3356-3361]. аналоги трихостатину, такі як трихостатин A (TSA) Переважними інгібіторами HDAC па основі гіді трихостатин C [Koghe et al. 1998. Biochem. роксамової кислоти є субероїланілідPharmacol. 56: 1359-1364]; саліцилгідроксамова гідроксамінова кислота (SAHA), бісгідроксамід мкислота [Andrews et al., International J. Parasitology карбоксицинамової кислоти (CBHA) і піроксамід. 30, 761-768 (2000)]; субероїл-бісгідроксамова кисБуло показано, що SAH A прямо зв'язується з калота (SBHA) [патент США №5608108]; азелаїнталітичним карманом деацетилази гістону. SAHA бісгідроксамова кислота (ABHA) [Andrews et al., індукує затримку клітинного циклу, диференціювище]; азелаїн-1-гідроксамат-9-анілід (AAHA) [Qiu вання і/або апоптоз трансформованих клітин у et al., МоI. Biol. Cell 11, 2069-2083 (2000)]; 6-(3культурі та інгібує ріст пухлини у гризунів. SAHA хлорфенілуреїдо)капронова гідроксамова кислота ефективна при індукції цих ефектів як при солідних (3C1-UCHA); оксамфлатин[(2Е)-5-[3пухлинах, так і при злоякісних пухлинах кровотво[(фенілсульфоіііл)амінолфеніл]-ііент-2-ен-4рної системи. Було показано, що SAHA є е фективіногідроксамова кислота] [Kim et al. Oncogene, 18: ною при інгібуванні пухлинного росту у тварин без 2461 2470 (1999)]; A-161906, Scriptaid [Su et al. вияву токсичності для цієї тварини. Інгібування 2000 Cancer Research, 60: 3137-3142]; PXD-101 пухлинного росту, що індукується дією SAH A, по(Prolifix); LAQ-824; CHAP; MW2796 [Andrews et al., в'язане з накопиченням у пухлині ацетильованих вище]; MW2996 [Andrews et al., вище]; або будьгістонів. SAHA ефективна для пригнічення розвитяка з гідроксамових кислот, описаних у [патентах ку і безперервного росту індукованих канцерогеСША № 5369108, 5932616, 5700811, 6087367 і ном (N-метилнітрозосечовиною) пухлин молочних 6511990]. залоз щурів. SAHA вводили щурам у харчовий B. Циклічні тетрапептиди, такі як трапоксин А раціон протягом 130 днів дослідження. Таким чи(ТРХ)-циклічний тетрапептид (цикло-(Lном, SAHA є нетоксичним, активним при перорафенілаланіл-L-фенілаланіл-D-піпеколініл-L-2льному введенні противоопухлинним засобом, аміно-8-оксо-9,10-епокси деканоїл)) [Kijima et al., J механізм дії якого включає в себе інгібування акBiol. Chem. 268,22429-22435(1993)]; FR901228 тивності деацетилаз гістонів. (FK228, депсипептид) [Nakajima et al., Ex. Cell Res. Переважними інгібіторами HDAC є сполуки, 241,126-133 (1998)]; FR225497 циклічний тетрапеописані в [патентах США № 5369108, 5932616, птид [H. Mori et al., Заявка PCT WO 00/08048 (17 5700811, 6087367 і 6511990], виданих деяким із лютого 2000)]; циклічний тетрапептид апіцидин авторів даного винаходу, повний зміст яких вклю[цикло(N-О-метил-L-триптофаніл-L-ізолейциніл-Dчений тут як посилання, не обмежуючі приклади піпеколініл-L-2-аміно-8-оксодеканоїл)] [Darkinяких наведені нижче. Rattray et al., Proc. Natl. Acad. Sci. USA 93, 13143В одному варіанті здійснення інгібітор HDAC, 13147 (1996)]; апіцидин Ia, апіцидин Ib, апіцидин Ic, що використовується у способах за даним винахоапіцидин IIа та апіцидин IIb [P. Dulski et al., заявка дом, представлений структурою формули 1 або PCT WO 97/11366]; CHAP, циклічний тетрапептид фармацевтично прийнятною сіллю або гідратом, і НС-токсину [Boschet al., Plant Cell 7, 1941-1950 фармацевтично прийнятним носієм або ексципієн(1995)]; WF27082 циклічний тетрапептид [заявка том. 21 83065 22 або R3 і R4 зв'язані разом з утворенням піперидинової групи; R2 являє собою гідроксиламіно, гідроксильну, аміно, алкіламіно або алкілокси групу; n являє собою ціле число від 5 до 7; a R3-N-R4 і R2 є різними. В іншому конкретному варіанті здійснення у формулі 2 n дорівнює 6. Ще в одному варіанті здійснення у формулі 2 R4 являє собою атом водню, R3 являє собою заміщений або незаміщений феніл, а n дорівнює 6. Ще в одному варіанті здійсде R1 і R2 можуть бути однаковими або різнинення у формулі 2 R4 являє собою атом водню, R3 ми; у тому випадку, коли R1 і R2 однакові, кожен являє собою заміщений феніл, а n дорівнює 6, де являє собою заміщену або незаміщену ариламіно, зазначений замісник фенілу вибраний із групи, яка циклоалкіламіно, піридинаміно, піперидино, 9складається з метальної, ціано, нітро, трифтормепурин-6-амін або тіазоламіно групу; у тому випадтильної, аміно, амінокарбонільної, метилціано, ку, коли R1 і R2 різні, R1=R3-N-R4, де кожен із R3 і R4 хлор, фтор, бром, йод, 2,3-дифтор, 2,4-дифтор, незалежно є однаковими або відрізняються один 2,5-дифтор, 3,4-дифтор, 3,5-ди фтор, 2,6-дифтор, від одного та являють собою атом водню, гідро1,2,3-трифтор, 2,3,6-трифтор, 2,4,6-трифтор, 3,4,5ксильну груп у, заміщену або незаміщену, розгалутрифтор, 2,3,5,6-тетрафтор, 2,3,4,5,6-пентафтор, жену або нерозгалужену алкільну, алкенільну, циазидо, гексил, трет-бутильної, фенільної, карбокклоалкільну, арильну, алкілокси, арилокси, сильної, гідроксильної, метокси, фенілокси, бензиарилалкілокси або піридинову гр упу, або R3 і R4 локси, феніламіноокси, феніламінокарбонільної, зв'язані разом з утворенням піперидинової групи, метоксикарбонільної, метиламінокарбонільної, R2 являє собою гідроксиламіно, гідроксильну, амідиметиламіно, диметиламінокарбонільної або гідно, алкіламіно, діалкіламіно або алкілокси групу, а роксиламінокарбонільної групи. n являє собою ціле число від приблизно 4 до приВ іншому варіанті здійснення у формулі 2 n близно 8. дорівнює 6, R4 являє собою атом водню, a R3 явУ конкретному варіанті здійснення у формулі ляє собою циклогексильну гр упу. В іншому варіанті 1, R1 і R2 є однаковими та являють собою заміщездійснення у формулі 2 n дорівнює 6, R4 являє ну або незаміщену тіазоламіно групу; і n являє собою атом водню, a R3 являє собою метокси грусобою ціле число від приблизно 4 до приблизно 8. пу. В іншому варіанті здійснення у формулі 2 n В одному варіанті здійснення інгібітор HDAC, дорівнює 6, a R3 і R4 зв'язані разом з утворенням що використовується у способах за даним винахопіперидинової групи. В іншому варіанті здійснення, дом, представлений структурою формули 2, або у формулі 2, n дорівнює 6, R4 являє собою атом фармацевтично прийнятною сіллю або гідратом, і водню, a R3 являє собою бензилокси групу. В інфармацевтично прийнятним носієм або ексципієншому варіанті здійснення, у формулі 2, R4 являє том. собою атом водню, і R3 являє собою g-піридинову груп у. В іншому варіанті здійснення, у формулі 2, R4 являє собою атом водню, і R3 являє собою bпіридинову груп у. В іншому варіанті здійснення, у формулі 2, R4 являє собою атом водню, і R3 являє собою a-піридинову груп у. В іншому варіанті здійснення, у формулі 2, n дорівнює 6, а обидва - R3 і R4 являють собою метильні групи. В іншому варіанті здійснення, у формулі 2, n дорівнює 6, R4 являє собою метильну груп у, a R3 являє собою фенільну груп у. В одному варіанті здійснення інгібітор HDAC, де кожен із R3 і R4 незалежно є однаковими що використовується у способах за даним винахоабо відрізняються один від одного, і являють содом, представлений структурою формули 3, або бою атом водню, гідроксильну групу, заміщену або фармацевтично прийнятною сіллю або гідратом, і незаміщену, розгалужену або нерозгалужену алкіфармацевтично прийнятним носієм або ексципіснльну, алкенільну, циклоалкільну, арилалкілокси, том. арилокси, арилалкілокси або піридинову гр упу, або R3 і R4 зв'язані разом з утворенням піперидинової групи, R2 являє собою гідроксиламіно, гідроксил, аміно, алкіламіно, діалкіламіно або алкілокси груп у, і n являє собою ціле число від приблизно 4 до приблизно 8. У конкретному варіанті здійснення у формулі 2 кожен із R3 і R4 незалежно є однаковими або відрізняються один від іншого та являють собою атом водню, гідроксильну групу, заміщену або незаміщену, розгалужену або нерозгалужену алкільну, алкенільну, циклоалкільну, арильну, алкілокси, де n являє собою ціле число від 5 до приблизарилокси, арилалкілокси, або піридинову гр упу, но 8. 23 83065 24 У переважному варіанті здійснення у формулі В одному варіанті здійснення інгібітор HDAC, 3 n дорівнює 6. Відповідно до цього варіанту здійщо використовується у способах за даним винахоснення, інгібітор HDAC являє собою SAHA (4), або дом, представлений структурою формули 8, або її фармацевтично прийнятну сіль або гідрати, і фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятний носій або ексципієнт. фармацевтично прийнятним носієм або ексципієнSAH A може бути представлена такою структурною том. формулою: В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 5, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 6 (піроксамід), або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носісм або ексципієнтом. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 7, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 9, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 10, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де R3 являє собою водень, і R4 циклоалкільну, арильну, арилокси, арилалкілокси або піридинову груп у, або R3 і R4 зв'язані разом з утворенням піперидинової групи; R2 являє собою гідроксиламіногрупу; і n являє собою ціле число від 5 до приблизно 8. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 11, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. 25 83065 26 міщену або незаміщену алкілокси, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу; кожен із R1 і R2 незалежно є однаковими або відрізняються один від одного і являють собою атом водню, гідроксильну груп у, заміщену або незаміщену алкільну, арильну, алкілокси або арилокси групу; і кожен із m, n і о незалежно є однаковими або відрізняються один від одного, і кожен являє собою ціле число приде R3 і R4 незалежно являють собою заміщену близно від приблизно 0 до приблизно 8. або незаміщену, розгалужену або нерозгалужену В одному конкретному варіанті здійснення у алкільну, алкенільну, циклоалкільну, арильну, алформулі 13 кожен із X і Y являє собою гідроксилькілокси, арилокси, арилалкілокси або піридинову ну груп у, і кожен із R1 і R2 являє собою метильну груп у, циклоалкільну, арильну, арилокси, арилалгруп у. В іншому конкретному варіанті здійснення у кілокси або піридинову груп у, або R3 і R4 зв'язані формулі 13 кожен із X і Y являє собою гідроксильразом з утворенням піперидинової групи; R2 являє ну груп у, кожен із R1 і R2 являє собою метильну собою гідроксиламіногрупу; і n являє собою ціле груп у, кожен із n і о дорівнює 6, і m дорівнює 2. число від 5 до приблизно 8. В одному варіанті здійснення інгібітор HDAC, В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винахощо використовується у способах за даним винаходом, представлений структурою формули 14, або дом, представлений структурою формули 12, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнфармацевтично прийнятним носієм або ексципієнтом. том. де кожен із X і Y незалежно є однаковими або відрізняються один від одного та являють собою гідроксильну, аміно або гідроксиламіно групу, заміщену або незаміщену алкілокси, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу; R являє собою атом водню, гідроксильну групу, заміщену або незаміщену алкільну, арилалкілокси або арилокси групу; і кожен із m і n незалежно є однаковими або відрізняються один від одного, і кожен являє собою ціле число від приблизно 0 до приблизно 8. У конкретному варіанті здійснення інгібітор HDAC являє собою сполуки формули 12, де X, Y і R кожен являє собою гідроксил, і обидва - m і n дорівнюють 5. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 13, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де кожен із X і Y незалежно є однаковими або відрізняються один від одного і являють собою гідроксильну, аміно або гідроксиламіно групу, за де кожен із X і Y незалежно є однаковими або відрізняються один від одного і являють собою гідроксильну, аміно або гідроксиламіно групу, заміщену або незаміщену алкілокси, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу; кожен із R1 і R2 незалежно є однаковими або відрізняються один від одного і являють собою атом водню, гідроксильну груп у, заміщену або незаміщену алкільну, арильну, алкілокси або арилокси групу; і кожен із m і n незалежно є однаковими або відрізняються один від одного і кожен являє собою ціле число від приблизно 0 до приблизно 8. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 15, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де кожен із X і Y незалежно є однаковими або відрізняються один від одного і являють собою гідроксильну, аміно або гідроксиламіно групу, заміщену або незаміщену алкілокси, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу; і кожен із m і n незалежно є однаковими або відрізняються один від одно 27 83065 28 го, і кожен являє собою ціле число від приблизно 0 дом, представлений структурою формули 18, або до приблизно 8. фармацевтично прийнятною сіллю або гідратом, і В одному конкретному варіанті здійснення у фармацевтично прийнятним носієм або ексципієнформулі 15 кожен із X і Y являє собою гідроксильтом. ну гр уп у, і кожен із m і n дорівнює 5. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 16, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де кожен із X і Y незалежно є однаковими або відрізняються один від одного і являють собою гідроксильну, аміно або гідроксиламіно групу, заміщену або незаміщену алкілокси, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу; R1 і R2 незалежно є однаковими або відрізняються один від одного і являють собою атом водню, гідроксильну груп у, заміщену або незаміщену алкільну, арилалкілокси або арилокси групу; і кожен із m і n незалежно є однаковими або відрізняються один від одного, і кожен являє собою ціле число від приблизно 0 до приблизно 8. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 17, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де кожен із X і Y незалежно є однаковими або відрізняються один від одного і являють собою гідроксильну, аміно або гідроксиламіно групу, заміщену або незаміщену алкілокси, алкіламіно, діалкіламіно, ариламіно, алкілариламіно або арилоксіалкіламіно групу; і n являє собою ціле число від приблизно 0 до приблизно 8. В одному конкретному варіанті здійснення у формулі 17 кожен із X і Y являє собою гідроксиламіногрупу; R1 являє собою метильну групу, R2 являє собою атом водню; і кожен із m і n дорівнює 2. В іншому конкретному варіанті здійснення у формулі 17 кожен із X і Y являє собою гідроксиламіногруп у; R1 являє собою карбонілгідроксиламіно групу, R2 являє собою атом водню; і кожен із m і n дорівнює 5. В іншому конкретному варіанті здійснення у формулі 17, кожен із X і Y являє собою гідроксиламіногрупу; кожен із R1 і R2 являє собою фтор-гр упу; і кожен із m і n дорівнює 2. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винахо де кожен із X і Y незалежно є однаковими або відрізняються один від одного і являють собою гідроксильну, аміно або гідроксиламіно групу, заміщену або незаміщену алкілокси, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу; кожен із R1 і R2 незалежно є однаковими або відрізняються один від одного і являють собою атом водню, гідроксильну груп у, заміщену або незаміщену алкільну, арильну, алкілокси, арилокси, карбонілгідроксиламіно або фтор-груп у; і кожен із m і n незалежно є однаковими або відрізняються один від одного, і кожен являє собою ціле число від приблизно 0 до приблизно 8. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 19, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де кожен із R1 і R2 незалежно є однаковими або відрізняються один від одного, і являють собою гідроксильну, алкілокси, аміно, гідроксиламіно, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу. У конкретному варіанті здійснення інгібітор HDAC являє собою сполуку стр уктурної формули 19, де обидва R1 і R2 являють собою гідроксиламіно. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 20, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. 29 83065 30 пентафтор групою; і n являє собою ціле число від 4 до 8. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 23 (бісгідроксамід м-карбоксицинамової кислоти - CBHA), або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де кожен із R1 і R2 незалежно є однаковими або відрізняються один від одного, і являють собою гідроксильну, алкілокси, аміно, гідроксиламіно, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу. У конкретному варіанті здійснення інгібітор HDAC являє собою сполуку стр уктурної формули 20, де обидва R1 і R2 являють собою гідроксиламіно. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винахоВ одному варіанті здійснення інгібітор HDAC, дом, представлений структурою формули 21, або що використовується у способах за даним винахофармацевтично прийнятною сіллю або гідратом, і дом, представлений структурою формули 24, або фармацевтично прийнятним носієм або ексципієнфармацевтично прийнятною сіллю або гідратом, і том. фармацевтично прийнятним носієм або ексципієнтом. де кожен із R1 і R2 незалежно є однаковими або відрізняються один від одного і являють собою гідроксильну, алкілокси, аміно, гідроксиламіно, алкіламіно, діалкіламіно, ариламіно, алкілариламіно, алкілоксіаміно, арилоксіаміно, алкілоксіалкіламіно або арилоксіалкіламіно групу. У конкретному варіанті здійснення інгібітор HDAC являє собою сполуку стр уктурної формули 21, де обидва R1 і R2 являють собою гідроксиламіно. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 22, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де R являє собою феніламіно групу, заміщену ціано, метилціано, нітро, карбоксильною, амінокарбонільною, метиламінокарбонільною, диметиламінокарбонільною, трифторметильною, гідроксиламінокарбонільною, Nгідроксиламінокарбонільною, метоксикарбонільною, хлор, фтор, метильною, метокси, 2,3-дифтор, 2,4-дифтор, 2,5-дифтор, 2,6-ди фтор, 3,5-дифтор, 2,3,6-трифтор, 2,4,6-трифтор, 1,2,3-трифтор, 3,4,5трифтор, 2,3,4,5-тетрафтор або 2,3,4,5,6 В одному варіанті здійснення, інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 25, або фармацевтично прийнятною сіллю або гідратом, і фармацевтично прийнятним носієм або ексципієнтом. де R являє собою заміщений або незаміщений феніл, піперидин, тіазол, 2-піридин, 3-піридин або 4-піридин, і n являє собою ціле число від приблизно 4 до приблизно 8. В одному конкретному варіанті здійснення у формулі 25 R являє собою заміщену фенільну груп у. В іншому конкретному варіанті здійснення у формулі 25 R являє собою заміщену фенільну груп у, де замісник вибраний із групи, яка складається з метальної, ціано, нітро, тіо, трифторметильної, аміно, амінокарбонільної, метилціано, хлор, фтор, бром, йод, 2,3-дифтор, 2,4-дифтор, 2,5дифтор, 3,4-дифтор, 3,5-дифтор, 2,6-дифтор, 1,2,3-трифтор, 2,3,6-трифтор, 2,4,6-трифтор, 3,4,5трифтор, 2,3,5,6-тетрафтор, 2,3,4,5,6-пентафтор, азидо, гексильної, трет-бутильної, фенільної, карбоксильної, гідроксильної, метилокси, фенілокси, 31 83065 32 бензилокси, феніламіноокси, феніламінокарбоніде кожен із R1 і R2 приєднаний безпосередньо льної, метилоксикарбонільної, метиламінокарбоніабо через лінкер і являє собою заміщений або льної, диметиламінo, диметиламінокарбонільної незаміщений арил (наприклад, феніл), арилалкіл або гідроксиламінокарбонільної групи. (наприклад, бензил), нафтил, циклоалкіл, циклоаВ іншому конкретному варіанті здійснення у лкіламіно, піридинаміно, піперидино, 9-пурин-6формулі 25 R являє собою заміщену або незаміаміно, тіазоламіно, гідроксил, розгалужений або щену 2-піридин, 3-піридин або 4-ніридин, і n являє нерозгалужений алкіл, алкеніл, алкілокси, арилоксобою ціле число від приблизно 0 до приблизно 8. си, арилалкілокси, піридил, або хінолініл або ізохіВ одному варіанті здійснення інгібітор HDAC, нолініл; n являє собою ціле число від приблизно 3 що використовується у способах за даним винаходо приблизно 10, і R3 являє собою гідроксамову дом, представлений структурою формули 26, або кислоту, гідроксиламіно, гідроксильну, аміно, алкіфармацевтично прийнятною сіллю або гідратом, і ламіно або алкілокси групу. Лінкер може являти фармацевтично прийнятним носієм або ексципієнсобою, наприклад, амідну частину молекули, О-, том. S-, -NH-, NR 5, -CH2-, -(CH2) m-, -(CH=CH)-, фенілен, циклоалкілен або будь-яку їх комбінацію, де R5 являє собою заміщений або незаміщений C1-C5 алкіл. У певних варіантах здійснення у формулі 27 R1 являє собою -NH-R4, де R4 являє собою заміщений або незаміщений арил (наприклад, феніл), арилалкіл (наприклад, бензил), нафтил, циклоалкіл, циклоалкіламіно, піридинаміно, піперидино, 9-пуринде R являє собою заміщену або незаміщену 6-аміно, тіазоламіно, гідроксил, розгалужений або фенільну, піридинову, піперидинову або тіазольну нерозгалужений алкіл, алкеніл, алкілокси, арилокгруп у, і n являє собою ціле число від приблизно 4 си, арилалкілокси, піридил, хінолініл або ізохінолідо приблизно 8, або їх фармацевтично прийнятні ніл. солі. В одному варіанті здійснення інгібітор HDAC, У конкретному варіанті здійснення у формулі що використовується у способах за даним винахо26 R являє собою заміщену фенільну груп у. В індом, представлений структурою формули 28, або шому конкретному варіанті здійснення у формулі фармацевтично прийнятною сіллю або гідратом, і 26 R являє собою заміщену фенільну груп у, де фармацевтично прийнятним носієм або ексципієнзамісник вибраний із групи, яка складається з метом. тальної, ціано, нітро, тіо, трифторметильної, аміно, амінокарбонільної, метилціано, хлор, фтор, бром, йод, 2,3-дифтор, 2,4-дифтор, 2,5-дифтор, 3,4дифтор, 3,5-дифтор, 2,6-дифтор, 1,2,3-трифтор, 2,3,6-трифтор, 2,4,6-трифтор, 3,4,5-трифтор, 2,3,5,6-тетрафтор, 2,3,4,5,6-пентафтор, азидо, гексильної, трет-бутильної, фенільної, карбоксильної, гідроксильної, метокси, фенілокси, бензилокси, феніламіноокси, феніламінокарбонільної, метилоксикарбонільної, метиламінокарбонільної, диметиламіно, диметиламінокарбонільної або гідде кожен із R1 і R2 являє собою заміщений або роксиламінокарбонільної групи. незаміщений арил (наприклад, феніл), арилалкіл В іншому конкретному варіанті здійснення у (наприклад, бензил), нафтил, циклоалкіл, циклоаформулі 26 R являє собою феніл, і n дорівнює 5. В лкіламіно, піридинаміно, піперидино, 9-пурин-6іншому варіанті здійснення n дорівнює 5, і R являє аміно, тіазоламіно, гідроксил, розгалужений або собою 3-хлорофеніл. нерозгалужений алкіл, алкеніл, алкілокси, арилокВ одному варіанті здійснення інгібітор HDAC, си, арилалкілокси, піридил, хінолініл або ізохіноліщо використовується у способах за даним винахоніл; R3 являє собою гідроксамову кислоту, гідродом, представлений структурою формули 27, або ксиламіно, гідроксильну, аміно, алкіламіно або фармацевтично прийнятною сіллю або гідратом, і алкілокси групу; R4 являє собою водень, галоген, фармацевтично прийнятним носієм або ексципієнфенільну або циклоалкільну частину молекули; і А том. можуть бути однаковими або різними і представляють амідну частину молекули, О-, -S-, -NH-, NR 5, -CH2-, -(CH2)m-, -(CH=CH)-, фенілен, циклоалкілен або будь-яку їх комбінацію, де R5 являє собою заміщений або незаміщений C1-C5 алкіл; а n і m кожен являє собою ціле число від 3 до 10. Ще в одному конкретному варіанті здійснення сполуки, що мають більш специфічну структур у в обсязі сполук 27 або 28, представляють наступне: В одному варіанті здійснення інгібітор HDAC, який використовується у способах за даним винаходом представлений структурою формули 29: 33 83065 34 аміно, тіазоламіно, арилокси, арилалкілокси, піридилу, хінолінілу або ізохінолінілу; n являє собою ціле число від 3 до 10, і Y вибраний із: де А являє собою амідну частин у молекули, R1 і R2 кожен вибраний із заміщеного або незаміщеного арилу (наприклад, фенілу), арилалкілу (наприклад, бензилу), нафтилу, піридинаміно, 9пурин-6-аміно, тіазоламіно, арилокси, арилалкілокси, піридилу, хінолінілу або ізохінолінілу; і n являє собою ціле число від 3 до 10. Наприклад, сполука формули 29 може мати структур у 30 або 31: В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 33: де n являє собою ціле число від 3 до 10, Y вибраний із де R1, R2, і n мають значення формули 29. В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 32: і R7' вибраний із де R7 вибраний із заміщеного або незаміщеного арилу (наприклад, фенілу), арилалкілу (наприклад, бензилу), нафтилу, піридинаміно, 9-пурин-6 35 83065 36 собою водень, галоген, фенільну або циклоалкільну частин у молекули, і n являє собою ціле число від 3 до 10. Наприклад, сполука формули 35 може мати структур у 36 або 37: В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 34: де Y вибраний із заміщеного або незаміщеного арилу (наприклад, фенілу), арилалкілу (наприклад, бензилу), нафтилу, піридинаміно, 9-пурин-6аміно, тіазоламіно, арилокси, арилалкілокси, піридилу, хінолінілу або ізохінолінілу; n являє собою ціле число від 3 до 10, і R7' вибраний із В одному варіанті здійснення інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 35: де А являє собою амідну частин у молекули, R1 і R2 кожен вибраний із заміщеного або незаміщеного арилу (наприклад, фенілу), арилалкілу (наприклад, бензилу), нафтилу, піридинаміно, 9пурин-6-аміно, тіазоламіно, арилокси, арилалкілокси, піридилу, хінолінілу або ізохінолінілу; R4 являє де R1, R2, R4, і n мають значення формули 35. В одному варіанті здійснення, інгібітор HDAC, що використовується у способах за даним винаходом, представлений структурою формули 38: де L являє собою лінкер, вибраний із групи, яка складається з амідної частини, О-, -S-, -NH-, NR5, -CH2-, (СН2)m-, -(CH=CH)-, фенілену, циклоалкілену або будь-якої їхньої комбінації, R5 являє собою заміщений або незаміщений C1-C5 алкіл; і де кожен із R7 і R8 незалежно являє собою заміщений або незаміщений арил (наприклад, феніл), арилалкіл (наприклад, бензил), нафтил, піридинаміно, 9-пурин-6-аміно, тіазоламіно, арилокси, арилалкілокси, піридил, хінолініл або ізохінолініл; n являє собою ціле число від 3 до 10, і m являє собою ціле число від 0 до 10. Наприклад, сполука формули 38 може бути представлене структурною формулою (39): 37 83065 38 Сполука, представлена структурою: Інші інгібітори HDAC, придатні для використання у способах даного винаходу, включають у себе інгібітори HDAC, зображені на наступних більш конкретних формулах: Сполука, представлена структурою: де n являє собою ціле число від 3 до 10, або її енантіомер. У конкретному варіанті здійснення у формулі 42 n=5. Сполука, представлена структурою: де n являє собою ціле число від 3 до 10, або її енантіомер. У конкретному варіанті здійснення у формулі 40 n=5. Сполука, представлена структурою: де n являє собою ціле число від 3 до 10, або її енантіомер. У конкретному варіанті здійснення у формулі 43 n=5. Сполука, представлена структурою: де n являє собою ціле число від 3 до 10, або її енантіомер. У конкретному варіанті здійснення у формулі 41 n=5. 39 83065 де n являє собою ціле число від 3 до 10, або її енантіомер. У конкретному варіанті здійснення у формулі 44 n=5. Сполука, представлена структурою: де n являє собою ціле число від 3 до 10, або її енантіомер. У конкретному варіанті здійснення у формулі 45 n=5. де n являє собою ціле число від 3 до 10, або її енантіомер. У конкретному варіанті здійснення у формулі 46 n=5. Сполука, представлена структурою: 40 де n являє собою ціле число від 3 до 10, або її енантіомер. В одному конкретному варіанті здійснення у формулі 47 n=5. Сполука, представлена структурою: де n являє собою ціле число від 3 до 10, або її енантіомер. В одному конкретному варіанті здійснення у формулі 48 n=5. Сполука, представлена структурою: 41 83065 42 (3), 931-934; Suzuki, T., et al., J. Med. Chem. 42 де n являє собою ціле число від 3 до 10, або її (15), 3001-3003 (1999); опублікованій заявці PCT енантіомер. В одному конкретному варіанті здійсWO 01/18171 публікація 15 березня, 2001 на адренення у формулі 49 n=5. су Sloan-Kettering Institute для Cancer Research і Сполука, представлена структурою: довірених осіб Колумбійського університету; опублікованій заявці PCT WO 02/246144 на адресу Hoffmann-La Roche; опублікованій заявці PCT WO 02/22577 на адресу Novartis; опублікованій заявці PCT WO 02/30879 на адресу Prolifix; опублікованих заявках PCT WO 01/38322 (публікація 31 травня 2001), WO 01/70675 (публікація 27 вересня 2001) і WO 00/71703 (публікація 30 листопада 2000) все на адресу Methylgene, Inc.; опублікованій заявці PCT WO 00/21979 публікація 8 жовтня 1999 на адресу Fujisawa Pharmaceutical Co., Ltd.; опублікованій заявці PCT WO 98/40080 публікація 11 березня 1998 на адресу Beacon Laboratories, L.L.C; і Curtin M. ("Current patent status of HDAC inhibitors" Expert Opina. Ther. Patents (2002) 12 (9): 1375-1384 і посиланнях, що тут цитуються)]. SAH A, або будь-який інший із HDACs, може бути синтезована відповідно до способів, викладених у Experimental Details Section, або відповідно до способу, викладеному в [патентах США №№ 5369108, 5700811, 5932616 і 6511990], змісти яких включені тут як посилання в повному обсязі, або де n являє собою ціле число від 3 до 10, або її відповідно до іншого способу, відомого фахівцеві у енантіомер. В одному конкретному варіанті здійсданій галузі. нення у формулі 50 n=5. Окремі необмежувальні приклади інгібіторів Сполука, представлена структурою: HDAC представлені в Таблиці, наведеній нижче. Потрібно зазначити, що даний винахід охоплює будь-які сполуки, які мають структурну подібність зі сполуками, наведеними нижче, і які мають здатність інгібувати деацетилази гістонів. де n являє собою ціле число від 3 до 10, або її енантіомер. В одному конкретному варіанті здійснення у формулі 51 n=5. Інші приклади таких сполук та інших інгібіторів HDAC можна знайти в [патенті США №5369108, виданому 29 листопада 1994, патенті США №5700811, виданому 23 грудня 1997, патенті США №5773474, виданому 30 червня 1998, патенті США №5932616, виданому 3 серпня 1999 і патенті США №6511990 виданому 28 січня 2003, все на ім'я Breslow et al.; у патенті США №5055608, виданому 8 жовтня 1991, патенті США №5175191 виданому 29 грудня 1992 і патенті США №5608108, виданому 4 березня 1997, все на ім'я Marks et al.; а також Yoshida, M., et al., Bioassays 17, 423-430 (1995); Saito, A., et al., PN AS USA 96, 4592-4597, (1999); Furamai, R. et al., PNAS USA 98 (1), 87-92 (2001); Komatsu, Y., et al., Cancer Res. 61 (11), 4459-4466 (2001); Su, G.H., et al., Cancer Res. 60, 3137-3142 (2000); Lee, B.I. et al., Cancer Res. 61 43 83065 44 алкільні групи з прямим або розгалуженим ланцюгом. Приклади включають у себе метил, етил, нпропіл, ізо-пропіл, н-бутил, втор-бутил і третбутил. "Ароматична група" (що також називають "арильною групою"), як використовується тут, включає в себе карбоциклічні ароматичні групи, гетероциклічні ароматичні групи (що також називають "гетероарил") і конденсовані поліциклічні ароматичні кільцеві системи, визначені тут. "Карбоциклічна ароматична група" являє собою ароматичне кільце з 5-14 атомів вуглецю, і включає в себе карбоциклічну ароматичну гр упу, конденсовану з 5- або 6-членною циклоалкільною групою, такою як індан. Приклади карбоциклічних ароматичних груп включають у себе, але не обмежуються, феніл, нафтил, наприклад, 1-нафтил і 2нафтил; антраценіл, наприклад, 1-антраценіл, 2антраценіл; фенантреніл; флуореноніл, наприклад, 9-флуореноніл, інданіл та інші. Карбоциклічна ароматична група необов'язково заміщена певною кількістю замісників, описаних нижче. "Гетероциклічна ароматична група" (або "гетероарил") являє собою моноциклічне, біциклічне або трициклічне ароматичне кільце від 5 до 14 атомів вуглецю і від одного до чотирьох гетероатомів, вибраних з O, N або S. Приклади гетероарилу включають у себе, але не обмежуються, піридил, наприклад, 2-піридил (що також називають a-піридил), 3-піридил (що також називають bпіридил) і 4-піридил (що також називають gпіридил); тієніл, наприклад, 2-тієніл і 3-тієніл; фураніл, наприклад, 2-фураніл і 3-фураиіл; піримідил, наприклад, 2-піримідил і 4-піримідил; імідазоліл, наприклад, 2-імідазоліл; піраніл, наприклад, 2піраніл і 3-піраніл; піразоліл, наприклад, 4піразоліл і 5-піразоліл; тіазоліл, наприклад, 2тіазоліл, 4-тіазоліл і 5-тіазоліл; тіадіазоліл; ізотіазоліл; оксазоліл, наприклад, 2-оксазоліл, 4оксазоліл і 5-оксазоліл; ізоксазоліл; піроліл; піридазиніл; піразиніл та інші. Гетероциклічна ароматична група (або гетероарил), визначена вище, може бути необов'язково заміщена певною кількістю замісників, описаних нижче для ароматичних груп. Сполуки за даним винаходом с застосовними "Конденсована поліциклічна ароматична" кільдля селективної індукції кінцевого диференціюцева система являє собою карбоциклічну аромавання, затримки клітинного росту і/або апоптозу тичну груп у або гетероарил, конденсований з одпухлинних клітин і, отже, ефективні при лікуванні ним або більше гетероарильним або раку в пацієнтів, як детально описано тут. неароматичним гетероциклічним кільцем. ПриклаХімічні визначення ди включають у себе хінолініл та ізохінолініл, на"Алі фтична гр упа" є неароматичною, складаприклад, 2-хінолініл, 3-хінолініл, 4-хінолініл, 5ється тільки з вуглецю і водню і необов'язково мохінолініл, 6-хінолініл, 7-хінолініл і 8-хінолініл, 1же містити одну або більше одиниць ненасиченосізохінолініл, 3-хінолініл, 4-ізохінолініл, 5ті, наприклад, подвійні і/або потрійні зв'язки. ізохінолініл, 6-ізохінолініл, 7-ізохінолініл і 8Алі фатична група може бути з прямим ланцюгом, ізохінолініл; бензофураніл, наприклад, 2розгалуженим або циклічною. У разі прямого або бензофураніл і 3-бензофураніл; дибензофураніл, розгалуженого ланцюга аліфатична група звичайнаприклад, 2,3-дигідробензофураніл; дибензотіоно містить від приблизно 1 до приблизно 12 атомів феніл; бензотієніл, наприклад, 2-бензотієніл і 3вуглецю, частіше від приблизно 1 до приблизно 6 бензотієніл; індоліл, наприклад, 2-індоліл і 3атомів вуглецю. Циклічна аліфатична група звиіндоліл; бензотіазоліл, наприклад, 2-бензотіазоліл; чайно містить від приблизно 3 до приблизно 10 бензоксазоліл, наприклад, 2-бензоксазоліл; бензіатомів вуглецю, частіше від приблизно 3 до примідазоліл, наприклад, 2-бензімідазоліл; ізоіндоліл, близно 7 атомів вуглецю. Аліфатичні гр упи перенаприклад, 1-ізоіндоліл і 3-ізоіндоліл; бензотриаважно являють собою C1-C12 алкільні групи з прязоліл; пуриніл; трианафтеніл та інші. Конденсовані мим або розгалуженим ланцюгом (тобто повністю поліциклічні ароматичні кільцеві системи необов'янасичені аліфатичні групи), більш переважно C1-C6 45 83065 46 зково можуть бути заміщені певною кількістю замісвітла даною сполукою, при цьому (-) або 1 познасників, описаних тут. чає, що дана сполука є лівообертальною. Сполука "Аралкільна група" (арилалкіл) являє собою з префіксом (+) або d є правообертальною. Для алкільну гр упу, заміщену ароматичною групою, даної хімічної структури ці сполуки, що називаютьпереважно, фенільною групою. Переважною арался стереоізомерами, є ідентичними, за винятком кільною групою є бензильна група. Тут описані того, що вони є дзеркальними відображеннями придатні ароматичні групи і придатні алкільні груодин одного, що не накладаються. пи. Придатні замісники для аралкільної групи опиСпецифічний стереоізомер також може назисані тут. ватися енантіомером, і суміш таких ізомерів часто "Арилоксигрупа" являє собою арильну групу, називають енантіомерною сумішшю. Суміш енанприєднану до сполуки через кисень (наприклад, тіомерів 50:50 називається рацемічною сумішшю. фенокси). Більшість описаних тут сполук може мати один "Алкоксигрупа" (алкілокси), як використовуєтьабо більше хіральних центрів і, отже, ці сполуки ся тут, являє собою C1-C12 алкільну гр упу з прямим можуть існувати в різних енантіомерних формах. або розгалуженим ланцюгом або C3-C12 циклічну Якщо потрібно, хіральний атом вуглецю може бути алкільну гр упу, яка зв'язана зі сполукою через позначений зірочкою (*). У тих випадках, коли у атом кисню. Приклади алкокси груп включають у формулах даного винаходу зв'язки із хіральним себе, але не тільки, метокси, етокси і пропокси. атомом вуглецю зображені у вигляді прямих ліній, "Арилалкокси група" (арилалкілокси) являє созрозуміло, що обидві конфігурації (R) і (S) можуть бою арилалкільну групу, яка приєднана до сполуки мати місце відносно хірального атома вуглецю, і, через кисень на алкільній частині арилалкілу (наотже, обидва енантіомера та їх суміші містяться в приклад, фенілметокси). даній формулі. Як прийнято в даній галузі, коли "Ариламіногрупа", як використовується тут, треба точно зазначити абсолютну конфігурацію являє собою арильну групу, приєднану до сполуки біля хірального атома вуглецю, один зі зв'язків із через азот. хіральним атомом вуглецю можна зобразити у Як використовується тут, "арилалкіламіногрувигляді клина (зв'язки з атомами біля площини), а па" являє собою арилалкільну групу, приєднану до інший можна зобразити у вигляді ряду або клина сполуки через азот на алкільній частині арилалкікоротких паралельних ліній (зв'язки з атомами лу. нижче площини). Для визначення (R) або (S) конЯк використовується тут, багато які частини фігурації відносно хірального атома може бути молекули або групи, називаються "заміщеними використана система "Cahn-Inglod-Prelog". або незаміщеними". Коли частину молекули назиУ тих випадках, коли інгібітори HDAC за даним вають заміщеною, це означає, що будь-яка частивинаходом містять один хіральний центр, дані на функціональної групи, відома фахівцеві в даній сполуки існують у дво х енантіомерних формах, і галузі, доступна для заміщення, може бути заміданий винахід включає в себе і енантіомери, і сущена. Наприклад, заміщуваною групою може бути міші енантіомерів, як наприклад, специфічна суміш атом водню, заміщуваний групою, відмінною від 50:50, що називається рацемічною сумішшю. Енаводню (тобто заміщувана група). Можуть існувати нтіомери можуть бути розділені способами, відомножинні заміщувані групи. Коли присутні мномими фахівцям у даній галузі, наприклад, шляхом жинні замісники, замісники можуть бути однаковиутворення діастереоізомерних солей, які можуть ми або різними, і заміщення може відбуватися у бути розділені, наприклад, кристалізацією [див. будь-яких сайтах заміщення. Такі способи заміCRC Handbook of Optical Resolutions via щення добре відомі на рівні техніки. Із метою ілюсDiastereomeric Salt Formation під ред. David Kozma трації, яка не обмежує обсяг даного винаходу, де(CRC Press, 2001)]; утворенням діастереоізомерякі приклади груп, що є замісниками, являють них похідних або комплексів, які можуть бути розсобою: алкільні групи (які також можуть бути заміділені, наприклад, кристалізацією, газовощені одним або більш замісниками, такими як рідинною або рідинною хроматографією; селектиCF3), алкокси групи (які можуть бути заміщеними, вною реакцією одного енантіомера з енантіомернаприклад, OCF3), галоген або галогрупа (F, Cl, Br, специфічним реактивом, наприклад, ферментатиІ), гідрокси, нітро, оксо, -CN, -СОН, -COOH, аміно, вною етерифікацією; або газово-рідинною або ріазидо, N-алкіламіно або N,N-діалкіламіно (в яких динною хроматографією в хіральному оточенні, алкільні групи також можуть бути заміщеними), наприклад, на хіральній підкладці, наприклад, складні ефіри (-C(O)-OR, де R може бути групою, двоокису кремнію зі зв'язаним хіральним лігандом такою як алкіл, арил і т.д., яка може бути заміщеабо у присутності хірального розчинника. Буде ною), арил (найбільш переважним є феніл, який зрозумілим, що в тих випадках, коли бажаний енаможе бути заміщеним), арилалкіл (який може бути нтіомер перетворюють в інший хімічний структурзаміщеним), і арилокси. ний елемент із допомогою однієї з описаних ви ще Стереохімія методик розділення, наступний етап є необхідним Багато органічних сполук існують в оптично для виділення бажаної енантіомерної форми. Альактивних формах, здатних обертати площину плотернативно, окремі енантіомери можуть бути синско-поляризованого світла. При описі оптично актезовані шляхом асиметричного синтезу з викоритивних сполук префікси D і L або R і S використостанням оптично активних реактивів, субстратів, вують для позначення абсолютної конфігурації каталізаторів або розчинників, або шляхом перемолекули біля її хірального центра (центрів). Претворення одного енантіомера в інший шляхом фікси d і 1 або (+) і (-) використовують для познаасиметричної трансформації. чення напрямку обертання плоско-поляризованого 47 83065 48 Зрозуміло, що зазначення певної абсолютної ми кислотами, наприклад, кислотно-адитивні солі, конфігурації біля хірального атома вуглецю сполук якими, наприклад, можуть бути соляна кислота, за даним винаходом означає, що зазначена енапсірчана кислота, метансульфонова кислота, футіомерна форма даних сполук знаходиться в енанмарова кислота, малеїнова кислота, бурштинова тіомерному надлишку (eн) або, інакше кажучи, є по кислота, оцтова кислота, бензойна кислота, щавсуті вільною від іншого енантіомера. Наприклад, лева кислота, винна кислота, вугільна кислота, "R" форми даних сполук є по суті вільними від "S" фосфорна кислота та інші. Фармацевтично прийнформ сполук і, отже, знаходяться в енантіомерноятні солі також можуть бути одержані шляхом обму надлишку відносно "S" форм. Навпаки, "S" форобки неорганічними основами, наприклад, гідрорми сполук є по суті вільними від "R" форм сполук ксидами натрію, калію, амонію, кальцію або заліза, і, отже, знаходяться в енантіомерному надлишку і такими органічними основами, як ізопропіламін, відносно "R" форм. Як використовується тут, енантриметиламін, 2-етиламіноетанол, гістидин, прокатіомерний надлишок являє собою наявність більїн і подібними. ше ніж 50% конкретного енантіомера. Наприклад, Даний винахід також охоплює фармацевтичні енантіомерний надлишок може складати близько композиції, що містять гідрати інгібіторів HDAC. 60% або більше, наприклад, близько 70% або біТермін "гідрат" включає в себе, але не тільки, нальше, наприклад, близько 80% або більше, наприпівгідрат, моногідрат, дигідрат, тригідрат та інші. клад, близько 90% або більше. У конкретному ваДаний винахід також охоплює фармацевтичні ріанті здійснення, коли визначена специфічна композиції, що містять SAHA у твердій або рідкій абсолютна конфігурація, енантіомерний надлишок фізичній формі, або будь-який інший інгібітор представлених сполук складає принаймні близько HDAC. Наприклад, інгібітори HDAC можуть бути в 90%. У більш конкретному варіанті здійснення кристалічній формі, у некристалічній формі та маенантіомерний надлишок сполук складає, принайти будь-який розмір частинок. Частки інгібітора мні, близько 95%, наприклад, принаймні, близько HDAC можуть бути мікронізовані або можуть бути 97,5%, наприклад, принаймні 99% енантіомерний агломеровані, у вигляді подрібнених гранул, понадлишок. рошків, масел, масляних суспензій або інших твеКоли сполука за даним винаходом має два або рдих або рідких фізичних форм. більше хіральних атомів вуглецю, вона може мати Терапевтичні застосування інгібіторів HDAC більше двох оптичних ізомерів і може існувати в 1. Лікування раку діастереоізомерних формах. Наприклад, коли маЯк представлено тут, інгібітори HDAC за дають місце два хіральних атоми вуглецю, дана споним винаходом є ефективними для лікування раку. лука може мати до 4 оптичних ізомерів і 2 пари Відповідно до цього, в одному варіанті здійснення енантіомерів ((S, S)/(R, R) і (R, S)/(S, R)). Пари даний винахід стосується способу лікування раку в енантіомерів (наприклад, (S, S)/(R, R)) є дзеркальпацієнта, потребуючого лікування, що включає в ними відображеннями стереоізомерів один одного. себе введення зазначеному пацієнту терапевтичСтереоізомери, які не є дзеркальними відобрано ефективної кількості описаного тут інгібітора женнями (наприклад, (S, R) і (R, S)) являють содеацетилази гістонів. бою діастереомери. Діастереоізомерні пари можна Термін "рак" стосується будь-якого типу раку, розділити способами, відомими фахівцям у даній викликаного проліферацією пухлинних клітин, нагалузі, наприклад, хроматографією або кристаліприклад, солідних пухлин, новоутворень, карцизацією, а індивідуальні енантіомери в межах кожном, сарком, лейкозу, мезотеліом, лімфом і подібної пари можуть бути розділені, як описано вище. них. Наприклад, типи раку включають у себе, але Даний винахід включає в себе кожен діастереоізоне тільки: мезотеліоми, наприклад, мезотеліому мер таких сполук та їх суміші. плеври, перитонеальну мезотеліому і доброякісну У контексті даного опису, якщо не зазначено фіброзну мезотеліому; лейкоз, у тому числі гостособливо, однина і множина для визначення террий лейкоз і хронічний лейкоз, наприклад гострий мінів взаємозамінні. Так, наприклад, позначення лімфолейкоз (ALL), гострий нелімфоцитарний лей"активний агент" або "фармакологічно активний коз, гострий мієлоїдний лейкоз (AML), хронічний агент" передбачає як одну сполуку, так і два і білімфолейкоз (CLL), хронічний мієлоїдний лейкоз льше різних активних об'єктів у комбінації, позна(CML) і волосатоклітинний лейкоз; лімфоми, начення "носій" може передбачати як суміш двох і приклад Т-клітинні лімфоми шкіри (CTCL), нешкірні більше речовини, так і один носій, і т.ін. периферичні Т-клітинні лімфоми, лімфоми, асоціДаний винахід також охоплює проліки описайовані з Т-клітинним лімфотропним вірусом людиних тут інгібіторів HDAC. Проліки будь-якої зі спони (HTLV), наприклад Т-клітинний лейкоз дорослук можуть бути одержані з використанням добре лих/лімфома (ATLL), хвороба Ходжкіна і відомих фармакологічних методик. неходжкінські лімфоми, великоклітинні лімфоми, Даний винахід, крім перерахованих вище сподифузна великоклітинна В-клітинна лімфома лук, о хоплює застосування гомологів і аналогів цих (DLBCL); лімфома Беркітта; первинна лімфома сполук. У даному контексті гомологи являють соцентральної нервової системи (WYC); множинна бою молекули, що мають істотні структурні подібмієлома; дитячі солідні пухлини, наприклад пухлиності з описаними вище сполуками, а аналоги явни головного мозку, нейробластома, ретинобласляють собою молекули, що мають істотні біологічні тома, пухлина Вільмса, пухлини кісткової тканини і подібності незалежно від структурних подібностей. саркоми м'яких тканин, широко розповсюджені Даний винахід також охоплює фармацевтичні солідні пухлини дорослих, наприклад ділянки гокомпозиції, що містять фармацевтично прийнятні лови і шиї (наприклад, рак ротової порожнини, рак солі інгібіторів HDAC з органічними і неорганічнигортані, рак стравоходу), рак сечостатевої системи 49 83065 50 (наприклад, рак простати, рак сечового міхура, рак у кістковому мозку. В-клітини продовжують розвинирки, рак матки, рак яєчника, тестикулярний рак, ток у кістковому мозку, тоді як Т-клітини перемірак прямої кишки і рак товстої кишки), рак легень, щуються з кісткового мозку в тимус і дозрівають рак молочної залози, рак підшлункової залози, там. Після того, як клітини дозрівають, і В-клітини, і меланома та інші типи раку шкіри, рак шлунка, T-клітини допомагають організму боротися з інфепухлини головного мозку, рак печінки і рак щитокціями. видної залози. Існує більше ніж 20 різних типів неходжкінської 2. Лікування мезотеліоми і лімфоми лімфоми. Дифузна великоклітинна В-клітинна ліЯк показано тут, інгібітори HDAC є ефективмфома є загальнопоширеним типом, що складає ними при лікуванні мезотеліоми і різних форм ліблизько 40% всіх випадків. Вона являє собою зломфоми, у тому числі дифузної великоклітинної Вякісну пухлину з В-лімфоцитів. Дифузна В-клітинна клітинної лімфоми (DLBCL). лімфома може зустрічатися в будь-який час від Існують різні типи мезотеліом. Плевральні та юнацького до старечого віку. Вона зустрічається перитонеальні (злоякісні) мезотеліоми включають трохи часті ше в чоловіків, ніж у жінок. Великокліу себе пухлини мезотеліальної тканини, пов'язані з тинна лімфома являє собою лімфому, яка хараквпливом азбесту. Гістологічно ці пухлини складатеризується наявністю надзвичайно великих кліються з епітеліоїдних, саркомоподібних або фібротин. зних, або клітин змішаних типів (що також називаІ хвороба Ходжкіна і NHL (неходжкінська лімються двофазним типом). Доброякісна фіброзна фома) класифікуються за однаковими характерисмезотеліома являє собою рідкісну солідну пухлину тиками стадій. Більшість лімфом у ВІЛ-позитивних плеври, яка викликає біль у грудя х, задишку, жар і людей включає в себе В-клітини, у протилежність гіпертрофічну остеоартропатію. Т-клітинам. Однією із систем, що застосовуються для опиСтадія лімфоми є дуже важливою і може досу мезотеліоми, є система Бутчарта (Butchart). Ця помогти визначити прогноз і курс лікування. Чотисистема обґрунтована, головним чином, на розмірі ри стадії наступні: первинної злоякісної пухлини, і підрозділяє мезоСтадія І: У наявності є одне вогнище злоякістеліоми на стадії з І по IV. ного новоутворення. Немає залучення до процесу Стадія І: Мезотеліома знаходиться тільки на кісткового мозку. одному боці грудної клітки і не проростає в грудну Стадія II: У наявності є два вогнища; обидва стінку. знаходяться або вище, або нижче діафрагми. НеСтадія II: Мезотеліома проростає в грудн у стімає залучення до процесу кісткового мозку. нку або зачіпає стравохід (травний шлях, що з'єдСтадія III: У наявності є вогнища вище і нижче нує глотку і шлунок), серце, або проросла у плевру діафрагми. Немає залучення до процесу кістковона інший бік грудей. Також у процес можуть бути го мозку. залучені грудні лімфатичні вузли. Стадія IV: Уражений кістковий мозок або пухСтадія III: Мезотеліома проросла через діафлинні клітини поширилися за межі лімфатичної рагму в очеревину (вистилає черевну порожнину) системи. або поширилася на лімфатичні вузли за межами При хворобі Ходжкіна стадії захворювання грудної клітки. класифікують таким чином: Стадія IV: Мезотеліома поширилася через Класифікація хвороби Ходжкіна кровотік на інші органи (метастази). А: відсутність жару, втрати ваги або нічної пітІнша система для визначення стадії мезотеліливості оми недавно була розроблена International В: наявність жару, втрата ваги або нічна пітлиMesothelioma Interest Group. У цій системі інфорвість мація про пухлину, лімфатичні вузли і метастази E: захворювання поширене на органи поза ліоб'єднана у процедуру, що називається групуванмфатичною системою. ня за стадіями. Класифікація Стадія І: Захворювання обмежене сумкою паЗ практичною метою неходжкінські лімфоми рієтальної плеври: іпсілатеральна плевра, легеня, також поділяють на дві групи: низького і високого перикард і діафрагма. ступеню злоякісності. Лімфоми низького ступеню Стадія II: всі ознаки стадії І із позитивними (N1 злоякісності звичайно ростуть повільно, а лімфоми або N2) внутрішньогрудними лімфатичними вузвисокого ступеню злоякісності мають тенденцію до лами. більш швидкого росту. Дифузна великоклітинна ВСтадія III: Місцеве поширення пухлини на такі клітинна лімфома стосується лімфом високого органи: грудна стінка або середостіння; серце або ступеню злоякісності. через діафрагму, очеревина; із залученням або Як передбачається тут, інгібітори HDAC за дабез залучення загруднинних або контралатеральним винаходом ефективні при лікуванні мезотеліних лімфатичних вузлів (N3). ом і лімфом на всіх стадіях розвитку, тобто на стаСтадія IV: Віддалене метастазування. діях І, II, III і IV, визначених ви ще, а також на Існує бага то різних типів лімфоми, і вони мостадіях А, В і E хвороби Ходжкіна. Крім того, інгібіжуть бути розділені на дві категорії: хвороба Ходжтори HDAC ефективні при лікуванні лімфом низькіна (HD) і неходжкінська лімфома (NHL). Голокого і високого ступеню злоякісності. вною відмінністю між цими двома категоріями є Як показано тут, інгібітори HDAC за даним витип клітин, залучених до патологічного процесу. находом, зокрема, ефективні при лікуванні мезоІснує два основних типи лімфоцитів: В-клітини теліоми і дифузної великоклітинної В-клітинної і Т-клітини. Більшість лімфоцитів починає розвиток лімфоми (DLBCL). 51 83065 52 3. Інші галузі застосування інгібіторів HDAC склерозом, синдромом Шегрена, поліоміозитом Інгібітори HDAC ефективні при лікуванні широабо дерматоміозитом); системну анафілактичну кого спектра захворювань, що характеризуються реакцію або реакцію гіперчутливості, лікарську проліферацією новоутворень, такихяк будь-які з алергію (наприклад на пеніцилін, цефалоспорини), описаних вище типів раку. Однак терапевтичне алергічну реакцію на укус комахи та інші. застосування інгібіторів HDAC не обмежується Наприклад, було виявлено, що інгібітори лікуванням раку. Навпаки, було виявлено, що існує HDAC, зокрема SAHA, є е фективними при лікуширокий ряд захворювань, при яких ефективні ванні різноманітних нейродегенеративних захвоінгібітори HDAC. рювань, неповний список яких наступний: Наприклад, було виявлено, що інгібітори I. Захворювання, що характеризуються проHDAC, зокрема SAH A, е фективні при лікуванні гресуючим недоумством за відсутності інших помірізних гострих і хронічних запальних захворювань, тних неврологічних ознак, наприклад хвороба аутоімунних захворювань, алергічних захворюАльцгеймера; старече недоумство альцгеймеріввань, захворювань, пов'язаних із окисним стресом, ськоготипу; і хвороба Піка (лобарна атрофія). і захворювань, що характеризуються гіперпроліII. Синдроми, що об'єднують прогресуюче неферацією клітин. Необмежувальними прикладами доумство з іншими помітними неврологічними є запальні стани суглоба, у тому числі ревматоїдрозладами, як, наприклад, А) синдроми, що з'явний артрит (RA) і псоріатичний артрит; запальні ляються головним чином у дорослих (наприклад, захворювання кишечнику, такі як хвороба Крона і хвороба Хантінгтона, мультисистемна атрофія, що виразковий коліт; спондилоартропатії; склеродерпоєднує недоумство з атаксією і/або проявами мія; псоріаз (включаючи псоріаз, опосередкований хвороби Паркінсона, прогресуючий супрануклеарТ-клітинами) і запальні дерматози, такі як дерманий параліч (синдром Стіл-Річардсонтит, екзема, атопічний дерматит, алергічний контаОльжевського), хвороба дифузних тілець Леві та ктний дерматит, кропивниця; васкуліт (наприклад, кортикодентатонігральна дегенерація); і В) синднекротичний, шкірний і гіперчутливий васкуліт); роми, що з'являються головним чином у дітей або еозинофільний міозит, еозинофільний фасцит; рак молодих людей (наприклад хвороба Халлерворіз лейкоцитарною інфільтрацією шкіри або органів, дена-Шпатца і сімейна прогресуюча міоклонічна ішемічне ушкодження, у тому числі ішемія голоепілепсія). вного мозку (наприклад ушкодження головного III. Синдроми поступового розвитку порушення мозку внаслідок травми, епілепсії, крововиливу пози і руху, наприклад тремтючий параліч (хвороабо інсульту, кожне з яких приводить до нейродеба Паркінсона), прогресуюча стріатонігральна дегенерації); ВІЛ, серцева недостатність, хронічне, генерація, супрануклеарний параліч, торзійна дисгостре або злоякісне захворювання печінки, аутоітонія (торзійний спазм; дистонія musculorum мунний тиреоїдит; системний червоний вовчак, deformans), спастична кривошия та інші дискінезії, синдром Шегрена, захворювання легень (наприсімейний тремор і синдром Жиля де ла Туретта. клад ARDS); гострий панкреатит; бічний аміотроIV. Синдроми прогресуючої атаксії, наприклад фічний склероз (ALS); хвороба Альцгеймера; кахемозочкові дегенерації (наприклад, дегенерація ксія/анорексія; астма; атеросклероз; синдром кори мозочка та оливомостомозочкова атрофія хронічної втоми, лихоманка; діабет (наприклад (OPCA)); і спинномозочкова дегенерація (спадкова інсулінозалежний діабет або юнацький діабет); атаксія Фрідрейха і суп утні захворювання). гломерулонефрит; реакція "трансплантат проти V. Синдром порушення центральної і вегетагосподаря" (наприклад при трансплантації); гемотивної нервової системи (синдром Шай-Драгера). рагічний шок; гіпералгезія: запальне захворювання VI. Синдроми м'язової слабкості та знесилення кишечнику; розсіяний склероз; міопатії (наприклад без сенсорних змін (захворювання мотонейрона, метаболізм м'язового білка, особливо при сепсисі); наприклад бічний аміотрофічний склероз, спінальостеопороз; хвороба Паркінсона; біль; передчасні на м'язова атрофія (наприклад, дитяча спінальна пологи; псоріаз; ушкодження при реперфузії; цитом'язова атрофія (Вердніга-Гофмана), юнацька спікініндукована токсичність (наприклад септичний нальна м'язова атрофія (Вохлфарт-Кугельбергашок, ендотоксичний шок); побічні ефекти променеВеландера) та інші форми сімейної спінальної вої терапії, захворювання скроневом'язової атрофії), первинний латеральний склероз нижньощелепового суглоба, п ухлинне метастазуі спадкова спастична параплегія.) вання; або запальний стан, викликаний розтягненVII. Синдроми, що поєднують м'язову слабням, вивихом, ушкодженням хряща, травмою, накість і знесилення із сенсорними змінами (прогреприкладопіком, ортопедичною хірургією, суюча нейром'язова атрофія; хронічні сімейні поінфекцією або іншими хворобливими процесами. лінейропатії), наприклад перонеальна м'язова Алергічні хвороби і стани включають у себе, але атрофія (синдром Шарко-Марі-Туса), гіпертрофічне тільки, респіраторні алергічні захворювання, на інтерстиціальна полінейропатія (синдром Детакі як астма, алергічний риніт, захворювання, пожеріна-Соттаса) і змішані форми хронічної прогрев'язані з гіперчутливістю легень, гіперчутливий суючої нейропатії. пневмоніт, еозинофільні пневмонії (наприклад VIII. Синдроми прогресуючої втрати зору, насиндром Леффлера, хронічна еозинофільна пневприклад пігментна дегенерація сітківки (пігментний монія), гіперчутливість уповільненого типу, інтерретиніт), і спадкова атрофія зорового нерва (хвостиціальні захворювання легень (ILD) (наприклад роба Лебера). ідіопатичний фіброз легень або ILD, асоційовані з Комбінована терапія ревматоїдним артритом, системним червоним воСпособи за даним винаходом також можуть вчаком, анкілозивним спондилітом, системним включати в себе спочатку введення пацієнту про 53 83065 54 типухлинного засобу, так щоб п улинні клітини стадень у дозі приблизно 200-400мг періодично, нали резистентними до протипухлинного засобу, і приклад, три, чотири або п'ять днів на тиждень. подальше введення ефективної кількості будь-якої В іншому варіанті здійснення композицію ввоз композицій за даним винаходом, ефективної для дять три рази на день у дозі приблизно 100-250мг. селективної індукції кінцевого диференціювання, В одному варіанті здійснення добова доза затримки клітинного росту і/або апоптозу таких становить 200мг, яку вводять одноразово, двічі на клітин, або для лікування раку або забезпечення день або три рази на день. В одному варіанті здійхіміопрофілактики. снення добова доза становить 300мг, яку можна Протипухлинним засобом може бути будьвводити одноразово, двічі на день або три рази на який із численних хіміотерапевтичних засобів, надень. В одному варіанті здійснення добова доза приклад, алкілуючий агент, антиметаболіт, гормостановить 400мг, яку можна вводити одноразово нальний засіб, антибіотик, колхіцин, алкалоїд барабо двічі на день. В одному варіанті здійснення вінку, L-аспарагіназа, прокарбозин, добова доза становить 150мг, яку можна вводити гідроксисечовина, мітотан, нітрозосечовини або двічі на день або три рази на день. імідазол-карбоксамід. Придатними є засоби, які Крім того, введення може бути безперервним, сприяють деполяризація тубуліну. Переважним тобто кожний день або періодичним. Терміни "пепротипухлинним засобом є колхіцин або алкалоїд ріодичне" або "періодично", що використовуються барвінку; особливо переважним є вінбластин і вінтут, означають припинення і початок або з регулякристин. У варіантах здійснення, в яких протипухрними, або з нерегулярними інтервалами. Наприлинним засобом є вінкристин, клітини переважно клад, періодичним введенням інгібітора HDAC мообробляють таким чином, щоб вони були резистеже бути введення від одного до шести днів на нтними до вінкристину в концентрації приблизно 5 тиждень або це може означати введення циклами мг/мл. Обробку клітин для надання їм резистент(наприклад, щоденне введення протягом від двох ності до протипухлинного засобу можна здійснити до восьми тижнів підряд, потім перерва до тижня взаємодією клітин із зазначеним засобом протягом без введення), або може означати введення через періоду часу принаймні від 3 до 5 днів. Контактудень. вання одержаних унаслідок клітин з однією зі споSAH A або будь-який з інгібіторів HDAC можна лук, представлених вище, проводять, як описано вводити пацієнту в загальній добовій дозі від 25 до раніше. Крім наведених вище хіміотерапевтичних 4000мг/м". засобів, дані сполуки можна застосовувати разом У цей час переважний лікувальний протокол із променевою терапією. включає в себе безперервне введення (тобто кожДози і схеми дозування ний день), один, два або три рази на день у загаСхема дозування з використанням інгібіторів льній добовій дозі в інтервалі від приблизно 200мг HDAC може бути вибрана відповідно до різних до приблизно 600мг. чинників, у тому числі типу, видів, віку, маси тіла, Інший переважний у цей час лікувальний простаті і тип у раку, який піддають лікуванню; тяжкості токол включає в себе періодичне введення від (тобто стадії) раку, який піддають лікуванню; шлятрьох до п'яти разів на тиждень, один, два або три ху введення, стану функції нирок і печінки пацієнта рази на день у загальній добовій дозі в інтервалі і конкретної сполуки або солі, що використовуєтьвід приблизно 200мг до приблизно 600мг. ся. Лікуючий лікар або ветеринар легко може виВ одному конкретному варіанті здійснення інгізначити і призначити ефективну кількість лікарсьбітор HDAC вводять безперервно один раз на кого засобу, необхідну для лікування, наприклад, день у дозі 400мг або двічі на день у дозі 200мг. для профілактики, інгібування (повного або частВ іншому конкретному варіанті здійснення інгікового) або затримки прогресування даного захвобітор HDAC вводять періодично три дні на тижрювання. день, один раз на день у дозі 400мг або двічі на Придатні дози складають загальну добову додень у дозі 200мг. зу приблизно від 25 до 4000мг/м 2, що вводиться В іншому конкретному варіанті здійснення інгіперорально один раз на день, двічі на день або бітор HDAC вводять періодично чотири дні на титри рази на день, безперервно (кожний день) або ждень, один раз на день у дозі 400мг або двічі на періодично (наприклад, 3-5 днів на тиждень). Надень у дозі 200мг. приклад, SAHA або будь-який інший з інгібіторів В іншому конкретному варіанті здійснення інгіHDAC можна вводити в загальній добовій дозі аж бітор HDAC вводять періодично п'ять днів на тиждо 800мг. Інгібітор HDAC можна вводити один раз день, один раз на день у дозі 400мг або двічі на на день (QD) або розділити на багаторазові щодень у дозі 200мг. денні дози, наприклад, двічі на день (BID) і три В одному конкретному варіанті здійснення, інрази на день (TID). Інгібітор HDAC можна вводити гібітор HDAC вводять безперервно один раз на в загальній добовій дозі аж до 800мг, наприклад, день у дозі 600мг, двічі на день у дозі 300мг, або 150мг, 200мг, 300мг, 400мг, 600мг або 800мг, яку три рази на день у дозі 200мг. можна вводити в одній добовій дозі або розділити В іншому конкретному варіанті здійснення інгіна багаторазові добові дози, як описано вище. бітор HDAC вводять періодично три рази на тижПереважним є пероральне введення. день, один раз на день у дозі 600мг, двічі на день у В одному варіанті здійснення композицію вводозі 300мг, або три рази на день у дозі 200мг. дять один раз на день у дозі приблизно 200-600мг. В іншому конкретному варіанті здійснення інгіВ іншому варіанті здійснення композицію вводять бітор HDAC вводять періодично чотири дні на тидвічі на день у дозі приблизно 200-400мг. В іншому ждень, один раз на день у дозі 600мг, двічі на день варіанті здійснення композицію вводять двічі на у дозі 300мг, або три рази на день у дозі 200мг. 55 83065 56 В іншому конкретному варіанті здійснення інгіго засобу або будь-якої їхньої комбінації. Більш бітор HDAC вводять періодично п'ять днів на тижтого композиції за даним винаходом можуть бути у день, один раз на день у дозі 600мг, двічі на день у формі контрольованого вивільнення або фармадозі 300мг, або три рази на день у дозі 200мг. цевтичних сумішей негайного вивільнення. Крім того, інгібітор HDAC можна вводити відОдним варіантом здійснення є фармацевтична повідно до будь-якої, описаної вище схеми, декікомпозиція для перорального введення, що міслька тижнів підряд, із подальшою перервою. Натить інгібітор HDAC або його фармацевтично приприклад, інгібітор HDAC можна вводити відповідно йнятну сіль або гідрат, мікрокристалічну целюлозу, до будь-якої описаної вище схеми від двох до вокроскармелозу натрію і стеарат магнію. В іншому сьми тижнів, із подальшою перервою на один тижваріанті здійснення як інгібітор HDAC використодень, або двічі на день у дозі 300мг протягом від вують SAH A. Ін ший варіант здійснення включає в трьох до п'яти днів на тиждень. В іншому конкретсебе 50-70% за масою інгібітора HDAC або його ному варіанті здійснення інгібітор HDAC вводять фармацевтично прийнятної солі або гідрату, 20три рази на день протягом двох тижнів підряд, із 40% за масою мікрокристалічної целюлози, 5-15% подальшою однотижневою перервою. за масою кроскармелози натрію і 0,1-5% за масою Фахівцеві в даній галузі буде зрозумілим, що стеарату магнію. Інший варіант здійснення вклюрізні дози і схеми дозування, описані тут, тільки чає в себе близько 50-200мг інгібітора HDAC. викладають окремі варіанти здійснення і не обмеВ одному варіанті здійснення фармацевтичні жують обсяг даного винаходу. Будь-які зміни, варікомпозиції вводять перорально, і, отже, їх одеранти і комбінації зазначених доз і схем дозування жують у формі, придатній для перорального ввевключені в обсяг даного винаходу. дення, тобто у вигляді твердого або рідкого препаДаний винахід пропонує безпечний щоденний рату. Придатні тверді пероральні лікарські суміші режим дозування цих лікарських сумішей, якому включають у себе таблетки, капсули, пілюлі, гралегко слідувати і якого легко дотримуватися. Фарнули, облатки та інше. Придатні рідкі пероральні мацевтичні композиції за даним винаходом, таким суміші включають у себе розчини, суспензії, дисчином, є застосовними для селективної індукції персії, емульсії, олії та інше. В одному варіанті кінцевого диференціювання, затримки клітинного здійснення даного винаходу композицію одержуросту і/або апоптозу пухлинних клітин і, отже, доють у вигляді капсули. Відповідно до даного варіапомагають при лікуванні пухлин у пацієнтів. нту здійснення, композиції за даним винаходом Фармацевтичні композиції включають у себе крім активної сполуки інгібітора Композиції за даним винаходом і похідні, фраHDAC та інертного носія або розріджувача, тверду гменти, аналоги, гомологи, їх фармацевтично прижелатинову капсулу. йнятні солі або гідрат, можуть бути включені у фаВикористовуваний тут "фармацевтично прийнрмацевтичні композиції, придатні для ятний носій" включає в себе будь-який і всі розперорального введення, разом із фармацевтично чинники, дисперсійні середовища, покриття, антиприйнятним носієм або ексципієнтом. Такі компобактеріальні та протигрибкові засоби, ізотонічні зиції звичайно містять терапевтично активну кільагенти і засоби, що сповільнюють абсорбцію, та кість будь-якої з перерахованих ви ще сполук і фаінші, сумісні з фармацевтичним застосуванням, рмацевтично прийнятного носія. Переважно, наприклад, стерильна апірогенна вода. Придатні ефективною кількістю є кількість, ефективна для носії описані в більшості останніх редакцій селективної індукції кінцевого диференціювання Remington's Pharmaceutical Sciences, стандартний відповідних пухлинних клітин і менша, ніж кільдовідковий текст у даній галузі, який включений кість, що викликає токсичність у пацієнта. тут як посилання. Переважні приклади таких носіїв Композиції за даним винаходом можуть бути або розріджувачів включають у себе, але не тільодержані в будь-якій одиничній дозованій формі ки, воду, фізіологічний розчин, розчини Рінгера, (рідкій або твердій), придатній для перорального розчин декстрози і 5% сироватковий альбумін люзастосування, наприклад, у формі облатки, табледини. Також можуть бути використані ліпосоми і тки, покритої таблетки, капсули, желатинової капневодні носії, наприклад, фіксовані в олії. Застосусули, розчину, суспензії або дисперсії. У цей час у вання таких середовищ і агентів для фармацевтипереважному варіанті здійснення дана композиція чно активних речовин добре відоме в даній галузі. знаходиться у формі желатинової капсули. У даних композиціях розглядається застосування Будь-який інертний ексципієнт, який звичайно будь-якого традиційного середовища або агента, використовують як носій або розріджувач, може за винятком несумісних з активною сполукою. У бути використаний у композиціях даного винаходу, композиції також можуть бути включені додаткові як наприклад, камедь, крохмаль, цукор, целюлозактивні сполуки. ний матеріал, акрилат або їх суміші. Переважним Тверді носії/розріджувачі включають у себе, розріджувачем є мікрокристалічна целюлоза. Комале не тільки, камедь, крохмаль (наприклад, кукупозиції додатково можуть містити дезінтегрант рудзяний крохмаль, пептизований крохмаль), цу(наприклад, кроскармелозу натрію) і лубрикант кор (наприклад, лактозу, маніт, сахарозу, декстро(наприклад, стеарат магнію), і, крім того, можуть зу), целюлозний матеріал (наприклад, містити одну або більше допоміжних речовин, вимікрокристалічну целюлозу), акрилат (наприклад, браних із зв'язувальних речовин, буфера, інгібітополіметилакрилат), карбонат кальцію, оксид магра протеаз, поверхнево-активної речовини, солюнію, тальк або їх суміші. білізатора, пластифікатора, емульгатора, Для рідких лікарських сумішей, фармацевтичстабілізатора, речовини, що підвищує в'язкість, но прийнятними носіями можуть бути водні або підсолоджувальних речовин, плівкоутворювальноневодні розчини, суспензії, емульсії або олії. При 57 83065 58 кладами неводних розчинників є пропіленгліколь, В одному варіанті здійснення активні сполуки поліетиленгліколь і органічні складні ефіри, що готують із носіями, які будуть захищати сполуки вводяться шляхом ін'єкцій, такі як етилолеат. Водвід швидкої елімінаціїї з організму, наприклад, суні носії включають у себе воду, водно-спиртові міші з контрольованим вивільненням, у тому числі розчини, емульсії або суспензії, у тому числі фізіоімплантати і мікроінкапсульовані системи доставки логічний розчин і буферні середовища. Прикладалікарського засобу. Можуть бути використані біоми масел є нафтові масла, тваринні, рослинні або сумісні полімери, що піддаються біорозкладу, такі масла синтетичного походження, наприклад, араяк етиленвінілацетат, поліангідриди, полігліколева хісова олія, соєва олія, мінеральне масло, оливкокислота, колаген, поліортоефіри і полімолочна ва олія, соняшникова олія і риб'ячий жир. Розчини кислота. Способи одержання таких сумішей будуть або суспензії також можуть включати в себе такі очевидні для фахівців у даній галузі. Дані матеріакомпоненти: стерильний розріджувач, такий як ли також можуть бути одержані комерційним шлявода для ін'єкцій, фізіологічний розчин, нелеткі хом від фірм Alza Corporation і Nova масла, поліетиленгліколі, гліцерин, пропіленгліPharmaceuticals, Inc. Ліпосомні суспензії (у тому коль або інші синтетичні розчинники; антибактерічислі ліпосоми, націлені на інфіковані клітини з альні засоби, такі як бензиловий спирт або метилмоноклональними антитілами до вірусних антигепарабени; антиоксиданти, такі як аскорбінова нів) також можуть бути використані як фармацевкислота або бісульфіт натрію; хелатоутворюючі тично прийнятні носії. Вони можуть бути одержані агенти, такі як етилендіамінтетраоцтова кислота відповідно до способів, відомих фа хівцям у даній (EDTA); буфери, такі як ацетатні, цитратні або фогалузі, наприклад, як описано в [патенті США сфатні, і агенти для встановлення тонічності, такі №4522811]. як хлорид натрію або декстроза. рН може бути Особливо переважно одержувати пероральні встановлений кислотами або основами, такими як композиції в одиничній дозованій формі для легкосоляна кислота або гідроксид натрію. го застосування і рівномірного дозування. Як викоКрім того, дані композиції можуть додатково ристовується тут, одинична дозована форма стомістити зв'язувальні речовини (наприклад, камедь, сується фізично дискретних одиниць, придатних як кукурудзяний крохмаль, желатин, карбомер, етилодиничні дози для пацієнта, що одержує лікуванцелюлозу, гуарову камедь, гідроксипропілцелюлоня; кожна одиниця містить заздалегідь визначену зу, гідроксипропілметилцелюлозу, повідон), дезінкількість активної сполуки, розраховану для одертегранти (наприклад, кукурудзяний крохмаль, жання бажаного терапевтичного ефекту, спільно з картопляний крохмаль, альгінову кислоту, діоксид необхідним фармацевтичним носієм. Характерискремнію, кроскармелозу натрію, кросповідон, гуатика одиничних дозованих форм за даним винахорову камедь, гліколят натрієвого крохмаля, Прімодом визначається і прямо залежить від особливих гель), буфери (наприклад, трис-НСІ, ацетатний, властивостей активної сполуки і конкретного терафосфа тний) із різними рН та іонною силою, добавпевтичного ефекту, що досягається, і обмежень, ки, такі як альбумін або желатин для запобігання характерних для галузі одержання такої активної абсорбції до поверхонь, детергенти (наприклад, сполуки для лікування окремих осіб. Твін 20, Твін 80, Плуронік F68, солі жовчних кисФармацевтичні композиції можуть бути поклалот), інгібітори протеаз, поверхнево-активні речодені в контейнер, упаковку або дозатор разом з вини (наприклад, лаурилсульфат натрію), підсиінструкціями із застосування. лювачі проникності, солюбілізуючі агенти Щоденне введення можна повторювати без(наприклад, гліцерин, поліетиленгліколь), глідант перервно протягом періоду від декількох днів до (наприклад, колоїдний діоксид кремнію), антиоксидекількох років. Пероральне лікування може проданти (наприклад, аскорбінову кислоту, метабісудовжуватися від одного тижня до довічного. Перельфіт натрію, бутильований гваякол), стабілізатоважно введення проводять протягом п'яти днів ри (наприклад, гідроксипропіл целюлозу, підряд, після закінчення цього часу для пацієнта гідроксипропілметилцелюлозу), агенти, що збільвизначають необхідність додаткового введення. шують в'язкість (наприклад, карбомер, колоїдний Введення може бути безперервним або періодичдіоксид кремнію, етилцелюлозу, гуарову камедь), ним, тобто лікування протягом декількох днів підподсолоджувальні речовини (наприклад, сахарозу, ряд із подальшою перервою. аспартам, лимонну кислоту), смакові добавки (наСполуки за даним винаходом можна вводити приклад, м'яту перцеву, метилсаліцилат або апевнутрішньовенно в перший день лікування, із пельсиновий ароматизатор), консерванти (наприроральним введенням на другий день і всі наступклад, Тімеросал, бензиловий спирт, парабени), ні дні підряд. лубриканти (наприклад, стеаринову кислоту, стеаСполуки за даним винаходом можна вводити рат магнію, поліетиленгліколь, лаурилсульфат для профілактики прогресування захворювання натрію), гліданти (наприклад, колоїдний діоксид або для стабілізації пухлинного росту. кремнію), пластифікатори (наприклад, діетилфтаОдержання фармацевтичних композицій, що лат, три етил цитрат), емульгатори (наприклад, містять активний компонент, добре відоме на рівні карбомер, гідроксипропілцелюлозу, лаурилсультехніки, наприклад, за допомогою процесів змішуфат натрію), полімерні покриття (наприклад, половання, гранулювання або таблетування. Терапевксамери або полоксаміни), покриття і плівкоутвотично активний компонент звичайно змішують із рювальні агенти (наприклад, етилцелюлозу, ексципієнтами, які є фармацевтично прийнятними і акрилати, поліметакрилати) і/або допоміжні засосумісними з активним інгредієнтом. Для пероральби. ного введення активні агенти змішують із добавками, загальноприйнятими для цієї мети, такими 59 83065 60 як носії, стабілізатори або інертні розріджувачі, і містить приблизно 50-200мг інгібітора HDAC (наперетворюють за допомогою прийнятих методів у приклад, 50мг, 100мг і 200мг інгібітора HDAC, наформи, придатні для застосування, такі як таблетприклад, SAHA). В особливо переважному варіанті ки, покриті таблетки, тверді або м'які желатинові здійснення дана композиція знаходиться у формі капсули, водні, спиртові або олійні розчини та інші, желатинової капсули. описані вище. На сьогоднішній день переважним варіантом Кількість сполуки, що вводиться пацієнту, є здійснення є 200мг твердої SAHA з 89,5мг мікроменшою ніж кількість, яка викликала б токсичність кристалічної целюлози, 9мг кроскармелози натрію у пацієнта. В окремих варіантах здійснення кільі 1,5мг стеарату магнію, що містяться в желатинокість сполуки, що вводиться пацієнту, є меншою вій капсулі. ніж кількість, яка приводить до концентрації сполуIn vitro методи: ки у плазмі пацієнта, що дорівнює або перевищує Даний винахід також стосується in vitro метотоксичний рівень даної сполуки. Переважно, кондів селективної індукції кінцевого диференціюванцентрацію сполуки у плазмі пацієнта підтримують ня, затримки клітинного росту і/або апоптозу пухна рівні приблизно 10нМ. В іншому варіанті здійслинних клітин, наприклад, клітин лімфоми, тим нення концентрацію сполуки у плазмі пацієнта самим інгібуючи проліферацію таких клітин, шляпідтримують на рівні приблизно 25нМ. В іншому хом контактування зазначених клітин з ефективваріанті здійснення концентрацію сполуки у плазмі ною кількістю інгібітора HDAC, наприклад, SAHA, пацієнта підтримують на рівні приблизно 50нМ. В або його фармацевтично прийнятної солі або гідіншому варіанті здійснення концентрацію сполуки рату. у плазмі пацієнта підтримують на рівні приблизно Даний винахід також стосується in vitro мето100нМ. В іншому варіанті здійснення концентрацію дів інгібування активності деацетилази гістонів, сполуки у плазмі пацієнта підтримують на рівні шляхом взаємодії деацетилази гістонів з ефективприблизно 500нМ. В іншому варіанті здійснення ною кількістю інгібітора HDAC, наприклад, SAHA, концентрацію сполуки у плазмі пацієнта підтримуабо його фармацевтично прийнятної солі або гідють на рівні приблизно 1000нМ. В іншому варіанті рату. здійснення концентрацію сполуки у плазмі пацієнХоча способи даного винаходу можуть бути та підтримують на рівні приблизно 2500нМ. В інздійснені in vitro, передбачається, що переважний шому варіанті здійснення концентрацію сполуки у варіант здійснення для способів селективної індуплазмі пацієнта підтримують на рівні приблизно кції кінцевого диференціювання, затримки клітин5000нМ. ного росту і/або апоптозу пухлинних клітин, та інгіБуло встановлено з HMBA, що введення спобування HDAC буде включати в себе взаємодію луки в кількості від приблизно 5г/м 2/день до приклітин in vivo, тобто шляхом введення даних споблизно 30г/м 2/день, зокрема близько 20г/м 2/день, є лук пацієнту, що має скупчення неопластичних ефективним без виявлення токсичної дії на пацієклітин або пухлинних клітин, які необхідно піддати нта. Оптимальна кількість сполуки, яку потрібно лікуванню. вводити пацієнту при здійсненні даного винаходу, Таким чином, даний винахід також стосується буде залежати від конкретної сполуки, що викориспособів селективної індукції кінцевого диференстовується і типу раку, що піддають лікуванню. ціювання, затримки клітинного росту і/або апоптоНа сьогоднішній день, у переважному варіанті зу пухлинних клітин, наприклад, клітин лімфоми у здійснення даного винаходу, фармацевтична компацієнта, тим самимінгібуючи проліферацію таких позиція містить інгібітор деацетилаз гістонів клітин у зазначеного пацієнта, шляхом введення (HDAC); мікрокристалічну целюлозу як носій або пацієнту фармацевтичної композиції, що містить розріджувач; кроскармелозу натрію як дезінтегефективну кількість інгібітора HDAC, наприклад, рант; і стеарат магнію як змащувальну речовину. В SAH A, або його фармацевтично прийнятної солі іншому переважному варіанті здійснення інгібітор або гідрату, і фармацевтично прийнятний носій HDAC являє собою субероїланілід-гідроксамінову або розріджувач. Ефективна кількість інгібітора кислоту (SAH A). Інший переважний варіант здійсHDAC у даному винаході може складати до 800 мг нення даного винаходу являє собою тверду лікарзагальної добової дози. ську суміш SAH A з мікрокристалічною целюлозою, Даний винахід також стосується способів інгіNF (Avicel Ph 101), кроскармелозою натрію, NF бування активності деацетилаз гістонів у пацієнта, (AC-Di-SoI) і стеаратом магнію, NF, що міститься в шляхом введення зазначеному пацієнту фармацежелатиновій капсулі. втичної композиції, що містить ефективну кількість Відсоткове співвідношення активного інгредієінгібітора HDAC, наприклад, SAHA, або його фарнта і різних ексципієнтів у фармацевтичних компомацевтично прийнятної солі або гідрату, і фармазиціях може варіювати. Наприклад, дана композицевтично прийнятний носій або розріджувач. Ефеція може містити від 20 до 90%, переважно 50-70% ктивна кількість інгібітора HDAC у даному винаході за масою інгібіторів деацетилаз гістонів (HDAC). може складати до 800мг загальної добової дози. Крім того, композиція може містити від 10 до 70%, Приклади переважно 20-40% за масою мікрокристалічної Даний винахід ілюструється наведеними ниж целюлози як носія або розріджувача. Крім того, че прикладами. Даний розділ представлений для композиція може містити від 1 до 30%, переважно кращого розуміння даного винаходу, але не при5-15% за масою кроскармелози натрію як дезінтезначений для обмеження яким-небудь чином дагранта. Крім того, композиція може містити 0,1-5% ного винаходу, викладеного у формулі винаходу, за масою стеарату магнію як лубриканта. В іншому що наведена далі. переважному варіанті здійснення дана композиція Приклад 1
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for treating mesothelioma with the use of hdac inhibitors - suberoylanilide hydroxamic acid (saha)
Автори англійськоюBacopulos Nicolas J., Chiao Judy H., Miller Thomas A., Peradais Kerolin M., Ricon Victoria M.
Назва патенту російськоюСпособ лечения мезотелиомы с использованием ингибитора hdac - субероиланилидгидроксаминовой кислоты (saha)
Автори російськоюБакопулос Николас Дж., Чиао Джуди Х., Миллер Томас A., Перадайз Керолин М., Ричон Виктория М.
МПК / Мітки
МПК: A61P 35/00, A61K 31/185
Мітки: лікування, saha, субероїланілідгідроксамінової, використанням, спосіб, мезотеліоми, кислоти, інгібітора
Код посилання
<a href="https://ua.patents.su/44-83065-sposib-likuvannya-mezoteliomi-z-vikoristannyam-ingibitora-hdac-suberolanilidgidroksaminovo-kisloti-saha.html" target="_blank" rel="follow" title="База патентів України">Спосіб лікування мезотеліоми з використанням інгібітора hdac – субероїланілідгідроксамінової кислоти (saha)</a>
Попередній патент: Пристрій для водоструминної обробки поверхонь матеріалів
Наступний патент: Установка заглибна для електрогідроімпульсного руйнування монолітних об’єктів
Випадковий патент: Спосіб кількісного визначення вмісту компонентів у препараті протикашлевої дії












