Продукт твердої дисперсії, що містить сполуки на основі n-арилсечовини
Формула / Реферат
1. Продукт твердої дисперсії, що містить щонайменше один фармацевтично активний агент, приготований:
a) одержанням рідкої суміші, що містить щонайменше один активний агент, щонайменше один фармацевтично прийнятний матрицеутворюючий агент, щонайменше одну фармацевтично прийнятну речовину і щонайменше один розчинник, і
b) видаленням розчинника(ів) з рідкої суміші з одержанням продукту твердої дисперсії,
де активним агентом є щонайменше одна сполука формули (І)
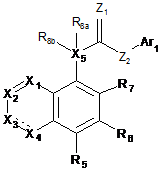 (I)
(I)
або її фармацевтично прийнятна сіль або проліки, де
![]() відсутній або є одинарним зв'язком;
відсутній або є одинарним зв'язком;
Х2 є N або CR2;
Х3 є N, NR3 або CR3;
Х4 є зв'язком, N або CR4;
Х5 є N або С; за умови, що щонайменше один з Х1, Х 2, Х3 і Х4 є N;
Z1 є О, NH або S;
Z2 є зв'язком, NH або О;
Аr1 вибирають із групи, що включає
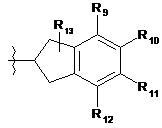 , (II)
, (II)
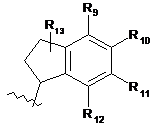 , (III)
, (III)
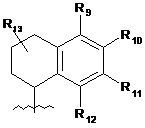 , (IV)
, (IV)
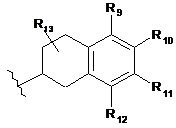 , (V)
, (V)
і R1, R3, R5, R6 і R7 кожний незалежно вибирають із групи, що включає водень, алкеніл, алкокси, алкоксіалкокси, алкоксіалкіл, алкоксикарбоніл, алкоксикарбонілалкіл, алкіл, алкілкарбоніл, алкілкарбонілалкіл, алкілкарбонілокси, алкілтіо, алкініл, карбокси, карбоксіалкіл, ціано, ціаноалкіл, циклоалкіл, циклоалкілалкіл, форміл, формілалкіл, галоалкокси, галоалкіл, галоалкілтіо, галоген, гідрокси, гідроксіалкіл, меркапто, меркаптоалкіл, нітро, (CF3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2, RBO(SO)2, ZAZBN-, (ZAZBN)алкіл, (ZAZBN)карбоніл, (ZAZBN)карбонілалкіл і (ZAZBN)сульфоніл;
R2 і R4 кожний незалежно вибирають із групи, що включає водень, алкеніл, алкокси, алкоксіалкокси, алкоксіалкіл, алкоксикарбоніл, алкоксикарбонілалкіл, алкіл, алкілкарбоніл, алкілкарбонілалкіл, алкілкарбонілокси, алкілтіо, алкініл, карбокси, карбоксіалкіл, ціано, ціаноалкіл, циклоалкіл, циклоалкілалкіл, форміл, формілалкіл, галоалкокси, галоалкіл, галоалкілтіо, галоген, гідрокси, гідроксіалкіл, меркапто, меркаптоалкіл, нітро, (CF3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2, R6O(SO)2, ZAZBN-, (ZАZВN)алкіл, (ZAZBN)алкілкарбоніл, (ZAZBN)карбоніл, (ZАZB)карбонілалкіл, (ZАZBN)сульфоніл, (ZAZBN)C(=NH)-, (ZAZBN)C(=NCN)NH- і (ZAZBN)C(=NH)NH-;
R8a є воднем або алкілом;
R8b відсутній або є воднем, алкокси, алкоксикарбонілалкілом, алкілом, алкілкарбонілокси, алкілсульфонілокси, галогеном або гідрокси;
R9, R10, R11 і R12 кожний окремо вибирають із групи, що включає водень, алкеніл, алкокси, алкоксіалкокси, алкоксіалкіл, алкоксикарбоніл, алкоксикарбонілалкіл, алкіл, алкілкарбоніл, алкілкарбонілалкіл, алкілкарбонілокси, алкілтіо, алкініл, арил, карбокси, карбоксіалкіл, ціано, ціаноалкіл, форміл, формілалкіл, галоалкокси, галоалкіл, галоалкілтіо, галоген, гетероарил, гетероцикл, гідрокси, гідроксіалкіл, меркапто, меркаптоалкіл, нітро, (CF3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2, R6O(SO)2, ZAZBN-, (ZAZBN)алкіл, (ZAZBN)карбоніл, (ZAZвN)кapбoнiлaлкiл і (ZAZBN)сульфоніл, де ZA і ZB кожний незалежно є воднем, алкілом, алкілкарбонілом, формілом, арилом або арилалкілом, за умови, що щонайменше один з R9, R10, R11 або R12, який не є воднем, або R10 і R11 разом з атомами, до яких вони приєднані, утворюють циклоалкільне, циклоалкенільне або гетероциклічне кільце;
R13 вибирають із групи, що включає водень, алкіл, арил, гетероарил і галоген;
RA є воднем або алкілом; і
RB є алкілом, арилом або арилалкілом;
за умови, що R8b відсутній, якщо Х5 є N.
2. Продукт твердої дисперсії за п. 1, де фармацевтично прийнятний матрицеутворюючий агент вибирають із групи, що включає циклодекстрини, фармацевтично прийнятні полімери, жири або комбінації двох або більше із них.
3. Продукт твердої дисперсії за п. 1, де вказаний фармацевтично прийнятний матрицеутворюючий агент вибирають із групи, що включає складні ефіри целюлози, прості ефіри целюлози, прості-складні ефіри целюлози, мальтодекстрини, гомополімери N-вінілпіролідону, співполімери N-вінілпіролідону і комбінації двох або більше із них.
4. Продукт твердої дисперсії за п. 1, де фармацевтично прийнятну поверхнево-активну речовину вибирають із групи, що включає складні ефіри жирної кислоти багатоатомного спирту, складні ефіри жирної кислоти поліалкоксилованого багатоатомного спирту, сполуки токоферилу або комбінації двох або більше із них.
5. Продукт твердої дисперсії за п. 1, де фармацевтично прийнятна поверхнево-активна речовина містить щонайменше одну поверхнево-активну речовину, що має значення HLB 10 або більше.
6. Продукт твердої дисперсії за п. 1, де комбінація фармацевтично прийнятних поверхнево-активних речовин містить (і) щонайменше одну сполуку токоферилу, що має групу поліалкіленгліколю і (іі) щонайменше один складний ефір жирної кислоти поліалкоксилованого багатоатомного спирту.
7. Продукт твердої дисперсії за п. 6, де складним ефіром жирної кислоти поліалкоксилованого багатоатомного спирту є поліалкоксилований гліцерид.
8. Продукт твердої дисперсії за п. 1, де активний агент вибирають із групи, що включає 1-((R)-5-трет-бутиліндан-1-іл)-3-(1Н-індазол-4-іл)сечовину (АВТ102) і її солі або гідрати, або сольвати.
9. Продукт твердої дисперсії за п. 1, де активний агент вибирають із групи, що включає
N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-5-ізохінолінілсечовину;
N-(5-трет-бутил-2,3-дигідро-1H-інден-1-іл)-N'-(3-метил-5-ізохінолініл)сечовину;
(+) N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-(3-метил-5-ізохінолініл)сечовину;
(-) N-(5-трет-бутил-2,3-дигідро-1H-інден-1-іл)-N'-(3-метил-5-ізохінолініл)сечовину;
(-) (5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-5-ізохінолінілсечовину;
(+) N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-5-ізохінолінілсечовину;
N-(5-бром-2,3-дигідро-1Н-інден-1-іл)-N'-5-ізохінолінілсечовину;
метил-4-({[(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Н-індазол-1-карбоксилат;
N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-1Н-індазол-4-ілсечовину (АВТ-102);
метил 4-[({[(1S)-5-трет-бутил-2,3-дигідро-1H-інден-1-іл]аміно}карбоніл)аміно]-1H-індазол-1-карбоксилат;
метил-4-[({[(1R)-5-трет-бутил-2,3-дигідро-1Н-інден-1-іл]аміно}карбоніл)аміно]-1Н-індазол-1-карбоксилат;
N-[(1S)-5-трет-бутил-2,3-дигідро-1Н-інден-1-іл]-N'-1Н-індазол-4-ілсечовину;
N-[(1S)-5-трет-бутил-2,3-дигідро-1H-інден-1-іл]-N'-1Н-індазол-4-ілсечовину;
метил-4-[({[5-(трифторметил)-2,3-дигідро-1H-інден-1-іл]аміно}карбоніл)аміно]-1H-індазол-1-карбоксилат;
N-1Н-індазол-4-іл-N'-[5-(трифторметил)-2,3-дигідро-1Н-інден-1-іл]сечовину;
метил-4-({[(5-піперидин-1-іл-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Н-індазол-1-карбоксилат;
N-1Н-індазол-4-іл-N'-(5-піперидин-1-іл-2,3-дигідро-1Н-інден-1-іл)сечовину;
метил-4-({[(5-гексагідро-1Н-азепін-1-іл-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1H-індазол-1-карбоксилат;
N-(5-гексагідро-1Н-азепін-1-іл-2,3-дигідро-1Н-інден-1-іл)-N'-1Н-індазол-4-ілсечовину;
N-1Н-індазол-4-іл-N'-[(1R)-5-піперидин-1-іл-2,3-дигідро-1Н-інден-1-іл]сечовину;
N-1Н-індазол-4-іл-N'-[(1S)-5-піперидин-1-іл-2,3-дигідро-1Н-інден-1-іл]сечовину;
ізопропіл-4-({[(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Н-індазол-1-карбоксилат; і
ізобутил-4-({[(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Н-індазол-1-карбоксилат;
N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-1Н-індазол-4-ілсечовину;
N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-(4R)-6-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-6-фтор-3,3',4,4'-тетрагідро-2'Н-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-6-фтор-3,3',4,4'-тетрагідро-2'Н-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-6-фтор-3,3',4,4'-тетрагідро-2'Н-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-1Н-індазол-4-ілсечовину;
N-[(4R)-6-фтор-3,3',4,4'-тетрагідро-2'Н-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-[(7S)-7-пдрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4S)-6-фтор-3,3',4,4'-тетрагідро-2'Н-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4S)-6-фтор-3,3',4,4'-тетрагідро-2'Н-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1H-індазол-4-іл)сечовину;
N-[(4R)-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-6-фтop-3,4-дигiдpo-2H-xpoмeн-4-iл]-N'-[(7S)-7-гiдpoкcи-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-іл сечовину;
N-(4R)-7-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-1H-індазол-4-ілсечовину;
N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-1Н-індазол-4-ілсечовину;
N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-(3-метилізохінолін-5-іл)сечовину;
N-[(4R)-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-8-ілсечовину;
N-[(4R)-2,2-диметил-7-(трифторметокси)-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-2,2-диметил-7-(трифторметокси)-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-1H-індазол-4-ілсечовину;
N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-8-ілсечовину;
N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-1Н-індазол-4-ілсечовину;
N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1H-індазол-4-іл)сечовину;
N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-2,2-діетил-7-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-2,2-діетил-7-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-2,2-діетил-8-(трифторметокси)-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1H-індазол-4-іл)сечовину;
N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-(3-метилізохінолін-5-іл)сечовину;
N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-ізохінолін-5-ілсечовину;
N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-1Н-індазол-4-ілсечовину;
N-(1-метил-1Н-індазол-4-іл)-N'-[(4R)-8-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]сечовину;
N-[(4R)-2,2-діетил-6,8-дифтор-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1H-індазол-4-іл)сечовину;
N-[(4R)-6-фтор-2,2-дипропіл-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2Н-хромен-4-іл]-N'-(3-метилізохінолін-5-іл)сечовину;
N-1H-індазол-4-іл-N'-[(4R)-8-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]сечовину;
N-ізохінолін-5-іл-N'-[(4R)-8-(трифторметил)-3,4-дигідро-2Н-хромен-4-іл]сечовину;
5N-[(4R)-8-фтор-2,2-дипропіл-3,4-дигідро-2Н-хромен-4-іл]-N'-(1-метил-1Н-індазол-4-іл)сечовину;
N-[(4R)-6-фтор-2,2-біс(фторметил)-3,4-дигідро-2Н-хромен-4-іл]-N'-(3-метилізохінолін-5-іл)сечовину;
N-[(4R)-8-фтор-2,2-дипропіл-3,4-дигідро-2Н-хромен-4-іл]-N'-(3-метилізохінолін-5-іл)сечовину;
N-[(4R)-7-хлор-2,2-діетил-3,4-дигідро-2Н-хромен-4-іл]-N-(3-метилізохінолін-5-іл)сечовину;
N-1Н-індазол-4-іл-N-[(4R)-8-(трифторметокси)-3,4-дигідро-2Н-хромен-4-іл]сечовину;
N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2Н-хромен-4-іл]-N-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-(4R)-6-фтор-2,2-дипропіл-3,4-дигідро-2Н-хромен-4-іл]-N-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл] сечовину;
N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2Н-хромен-4-іл]-N-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2Н-хромен-4-іл]-N-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-7-хлор-2,2-діетил-3,4-дигідро-2Н-хромен-4-іл]-N-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
N-[(4R)-7-хлор-2,2-діетил-3,4-дигідро-2Н-хромен-4-іл]-N-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовину;
(R)-1-(3-метилізохінолін-5-іл)-3-[8-(трифторметокси)хроман-4-іл]сечовину;
(R)-1-[6-фтор-2,2-біс(фторметил)хроман-4-іл]-3-(3-метилізохінолін-5-іл)сечовину;
і їх солі або гідрати, або сольвати.
10. Фармацевтична дозована форма, що містить продукт твердої дисперсії за п. 1.
11. Спосіб одержання продукту твердої дисперсії згідно з будь-яким з пп. 1-9, який включає:
a) одержання рідкої суміші, яка містить щонайменше один активний агент, щонайменше один фармацевтично прийнятний матрицеутворюючий агент, щонайменше одну фармацевтично прийнятну речовину і щонайменше один розчинник, і
b) видалення розчинника(ів) з рідкої суміші з одержанням продукту твердої дисперсії.
12. Спосіб за п. 11, де рідку суміш одержують розчиненням фармацевтично прийнятного матрицеутворюючого агента з одержанням розчину матрицеутворюючого агента, і додаванням активного агента й фармацевтично прийнятної поверхнево-активної речовини до розчину.
13. Спосіб за п. 11, де видалення розчинника проводять сушінням розпиленням, барабанним сушінням, сушінням на стрічці, сушінням на лотках або комбінацією двох або більше із них.
14. Спосіб за п. 11, де розчинник вибирають із групи, що включає алканоли, вуглеводні, галогеновані вуглеводні, кетони, складні ефіри, прості ефіри й комбінації двох або більше із них.
15. Спосіб за п. 11, де щонайменше один наповнювач додають у рідкій суміші до видалення розчинника(ів).
Текст
Реферат: Продукт твердої дисперсії, який містить щонайменше один активний агент на основі Nарилсечовин, одержаний а) одержанням рідкої суміші, що містить щонайменше один активний агент, щонайменше один фармацевтично прийнятний матрицеутворюючий агент, щонайменше одну фармацевтично прийнятну речовину і щонайменше один розчинник, і b) видаленням розчинника(ів) з рідкої суміші з одержанням продукту твердої дисперсії. UA 100866 C2 (12) UA 100866 C2 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 Множина сильних лікарських засобів належить до класу N-арилсечовин або сполук споріднених структурних типів. На жаль, кристалічні формі більшості активних агентів на основі N-арилсечовин або сполук споріднених структурних типів відрізняються поганою розчинністю у водних рідинах. Загальновідомо, що лікарські засоби з поганою розчинністю у воді, наприклад, класифіковані як "практично нерозчинні" або "нерозчинні" згідно з Фармакопеєю Сполучених Штатів Америки (USP) 24 (2000), p. 10, тобто, що мають розчинність менше близько 1 частини на 10000 частин води (менше близько 100 мкг/мл), дуже важко складати для перорального застосування. Серед інших проблем, біодоступність таких ліків, при введенні пероральним шляхом, дуже низька. Конкретним ілюстративним лікарським засобом з невеликою молекулою, який погано розчинний у воді, є сполука 1-((R)-5-трет-бутиліндан-1-іл)-3-(1H-індазол-4-іл)сечовина (ABT102), перше в класі антагоністів TRPV1, призначене для лікування болі. ABT-102 має молекулярну масу 348,44 г/моль і описане в патенті США № 7015233 і WO 2004/111009. З множини причин, таких як дотримання хворим режиму й схеми лікування і виправлення смаку лікарського засобу, тверді дозовані формі зазвичай більш переважні в порівнянні з рідкими дозованими формами. У більшості випадків, однак, пероральні тверді дозовані формі мають погану біодоступність у порівнянні з пероральними розчинами лікарського засобу. Все ще залишається необхідність в галузі фармацевтики в нових твердих композиціях активних агентів з поганою розчинністю у воді, таких як ABT-102, які придатні для перорального введення. Більш конкретно і без обмежень, існує необхідність у такій композиції, яка має щонайменше одну з наступних характеристик, переваг або корисностей: прийнятно висока концентрація лікарського засобу; і прийнятна біодоступність при пероральному введенні. Даний винахід належить до продуктів твердої дисперсії, що містять щонайменше один фармацевтично активний агент, одержаний a) одержанням рідкої суміші, що містить щонайменше один активний агент, щонайменше один фармацевтично прийнятний матрицеутворюючий агент, щонайменше одну фармацевтично прийнятну речовину і щонайменше один розчинник, і b) видаленням розчинника з рідкої суміші з одержанням продукту твердої дисперсії. Винахід особливо корисний для нерозчинних у воді або погано розчинних у воді (або "гідрофобних" або "ліпофільних") сполук. Сполуки вважаються нерозчинними у воді або погано розчинними у воді, якщо їх розчинність у воді при 25 °C становить менше 1 г/100 мл, особливо менше 0,1 г/100 мл. У дозованих формах відповідно до даного винаходу активний агент присутній у вигляді твердої дисперсії або, переважно, у вигляді твердого розчину. Термін "тверда дисперсія" визначає систему у твердому стані (на відміну від рідкого або газоподібного стану), що містить щонайменше два компоненти, де один з компонентів рівномірно диспергований в іншому компоненті або компонентах. Наприклад, активний агент або комбінація активних агентів диспергований у матриці, що складається з матрицеутворюючого агента і фармацевтично прийнятної поверхнево-активної речовини. Термін "тверда дисперсія" охоплює системи, що містять дрібні частинки, зазвичай менше 1 мкм у діаметрі, однієї фази, дисперговані в іншій фазі. Якщо вказана дисперсія компонентів така, що система хімічно й фізично однорідна або гомогенна або складається з однієї фази (як визначено в термодинаміці), така тверда дисперсія називається "твердий розчин" або "склоподібний розчин". Склоподібним розчином є гомогенна, склоподібна структура, в якій речовину, що розчиняється, розчиняють у склоподібному розчиннику. Склоподібні розчини й тверді розчини є переважними фізичними системами. Ці системи не містять будь-яку значну кількість активних агентів у їх кристалічнім або мікрокристалічному стані, що підтверджується термоаналізом (DSK) або рентгеноструктурним аналізом (WAXS). В одному варіанті даного винаходу щонайменше один наповнювач додають до рідкої суміші до видалення розчинників. Було виявлено, що введення наповнювача в рідку суміш перед видаленням розчинників підвищує крихкість отриманого продукту твердої дисперсії. Це дозволяє піддавати продукт твердої дисперсії процесу прямого таблетування. Переважно, наповнювач практично не розчинний у рідкій суміші. Вибір наповнювачів практично не обмежений. Наповнювач може бути придатним чином вибраний з неорганічних зернистих матеріалів, таких як двоокис кремнію, карбонат кальцію, фосфати кальцію, двоокис титану; природні й преклейстеризовані крохмалі, такі як кукурудзяний крохмаль, зерновий крохмаль, картопляний крохмаль; або подібні. 1 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 Однак, наповнювач, переважно, розчинний у воді. Корисні наповнювачі на даний момент можуть бути вибрані із цукрів, таких як лактоза, сахароза; цукрових спиртів, таких як маніт, сорбіт, ксиліт; або похідних цукрових спиртів. Відносні кількості активного агента, фармацевтично прийнятного матрицеутворюючого агента й фармацевтично прийнятної поверхнево-активної речовини вибирають, приймаючи до уваги наступні умови: (1) практично весь активний агент повинен бути рівномірно диспергований у матриці, що складається з матрицеутворюючого агента й фармацевтично прийнятної поверхнево-активної речовини. (2) Матриця повинна мати достатню механічну цілісність і стабільність; зокрема, матриця не повинна бути холодотекучою. Зазвичай масове співвідношення активного агента й фармацевтично прийнятного матрицеутворюючого агента становить від 0,01:1 до 1:3, переважно, від 0,05:1 до 0,2:1; загалом, масове співвідношення активного агента й фармацевтично прийнятної поверхнево-активної речовини становить від 0,1:1 до 1:7, переважно, від 1:4 до 1:6,5. Зазвичай, продукт твердої дисперсії містить від близько 1 до 30 % масових, переважно від близько 4 до 15 % мас., вказаного щонайменше фармацевтично активного агента, від близько 15 до 70 % мас., переважно, від близько 20 до 55 % мас., вказаного щонайменше одного фармацевтично прийнятного матрицеутворюючого агента, від близько 2 до 70 % мас., переважно, від близько 5 до 55 % мас., вказаної щонайменше однієї поверхнево-активної речовини, і від близько 0 до 80 % мас., переважно, від близько 0 до 60 % мас., добавок, таких як наповнювачі. Матрицеутворюючим агентом може бути будь-який агент, здатний проникати в активний агент і/або завантажуватися з активним агентом і стабілізувати практично аморфний стан активного агента. Зазвичай, можуть застосовуватися суміші матрицеутворюючих агентів. Фармацевтично прийнятний матрицеутворюючий агент придатним чином вибирають із групи, що включає циклодекстрини, фармацевтично прийнятні полімери, жири або комбінації двох або більше з них. Циклодекстрини для цілей даного винаходу включають циклічні оліго- або полісахариди, наприклад, так звані циклоамілози або циклоллюкани, і аналогічні циклічні вуглеводи, які описані, наприклад, в Angew. Chem. 92 (1980) p. 343 або F. Vogtle, Supramolekulare Chemie, 2nd Edition, (1992). Придатними й переважними є такі циклодекстрини, які мають структури, що придатні для взаємодії з молекулами активного агента, особливо в значенні систем "хазяїнгість". Особливо придатними циклодекстринами є такі, що містять 6, 7, 8 або 9 б-1,4-глікозидно зв'язані глюкозні одиниці, які називають б-, в-, г- або д-циклодекстрини. Більш високі структури, що аналогічні циклодекстринам і складаються з більшої кількості глюкоз і подібних цукрів, також розглядаються й підходять. Також як циклодекстрини можуть підходити модифіковані циклодекстрини, такі як, наприклад, продукти, які можуть бути одержані взаємодією циклодекстринів з алкіленоксидами, алкілгалогенідами, хлорангідридами, епігалогідринами, ізоціанатами або галогенованими карбоновими кислотами. Таким чином придатні приклади включають продукти реакції циклодекстринів з алкіленоксидами, такими як етиленоксид, пропіленоксид, бутиленоксид або оксид стиролу. Одна, більше однієї або всі гідроксильні групи в простих поліефірах циклодекстрину, отриманого таким чином, можуть бути заміщені. Залежно від ступеня заміщення або від довжини ланцюга, середній молярний ступінь заміщення, тобто кількість молів алкіленоксиду, з якими взаємодіє один моль циклодекстрину, зазвичай становить від 3 до 20000, але, в принципі, верхньої межі не існує. Особливо придатними прикладами є продукти взаємодії циклодекстринів з алкілувальними агентами, такими як С 1-C22-алкілгалогеніди, наприклад, метилхлорид, етилхлорид, ізопропілхлорид, нібутилхлорид, ізобутилхлорид, бензилхлорид, лаурилхлорид, стеарилхлорид, метилбромід, етилбромід, нібутилбромід і діалкілсульфатами, такими як, наприклад, диметилсульфат або діетилсульфат. Реакція з алкілувальними реагентами дає прості ефіри циклодекстрину, в яких одна, більше однієї або всі гідроксильні групи заміщені групами простого ефіру алкілу. Для циклодекстринів, що складаються із глюкозних одиниць, середній ступінь етерифікації на глюкозну одиницю зазвичай становить від 0,5 до 3, переважно, в інтервалі від 0,1 до 2,5, і особливо переважно, в інтервалі від 1 до 2. Особлива перевага віддається метильованим, етильованим або пропільованим б-, в, г-циклодекстринам із середнім ступенем етерифікації від 1,5 до 2,2. Також підходять складні ефіри циклодекстрину, які одержують взаємодією циклодекстринів із хлорангідридами, такими як карбонілхлориди або сульфонілхлориди. Особливо переважними є карбонілхлориди, такі як ацетилхлорид, акрилоїлхлорид, метакрилоїлхлорид або бензоїлхлорид. Також придатні модифіковані полімером циклодекстрини, тобто циклодекстрини, які введені в основний ланцюг полімером і/або циклодекстрини, які приєднані до бічних ланцюгів полімерів 2 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 або самі по собі є бічними ланцюгами полімерів. Модифіковані полімер циклодекстрини, в яких циклодекстринові одиниці введені в основний ланцюг полімеру, можуть бути одержані, наприклад, взаємодією циклодекстринів з, або у присутності придатних зв'язувальних або поперечно-зшивних реагентів, наприклад, як описано в Helv. Chim. Acta, Vol. 48, (1965), p. 1225. Модифіковані полімером циклодекстрини, в яких циклодекстринові одиниці є складовими бічних ланцюгів або діють як бічні ланцюги, можуть бути одержані, наприклад, полімеризацією циклодекстринів, модифікованих полімерізованими групами, з іншими співмономерами, наприклад, полімеризацією циклодекстрин(мет)акрилатів у присутності інших етиленненасичених мономерів або вільнорадикальним щепленням циклодекстрин(мет)акрилатів на полімери з вільними гідроксильними групами, такі як, наприклад, полівініловий спирт. Інша можливість одержання модифікованих полімером циклодекстринів із циклодекстриновими одиницями в бічних групах або як бічні групи полімерів, включає взаємодію циклодекстринів, депротонованих циклодекстринів або їх солей лужних металів, з полімерами, які мають додаткові реакційноздатні групи, такі як, наприклад, ангідрид, ізоціанат, галогенангідрид або епоксигрупи або галогени. Переважними циклодекстринами є гідроксіалкілциклодекстрини, такі як гідркосипропіл-вциклодекстрин. Придатні ліпіди можуть бути вибрані з парафінів, три-, ди- і моногліцеридів і фосфоліпідів. Переважними матрицеутворюючими агентами є фармацевтично прийнятні полімери. Фармацевтично прийнятні полімери можуть бути вибрані з водорозчинних полімерів, диспергованих у воді полімерів або полімерів, що розбухають у воді, або будь-яких їхніх сумішей. Полімери вважаються водорозчинними, якщо вони утворюють прозорий гомогенний розчин у воді. При розчиненні при 20 °C у водному розчині при 2 % (мас./об.), водорозчинний полімер, переважно, має гадану в'язкість від 1 до 5000 мпа*с, більш переважно, від 1 до 700 мпа*с, і найбільш переважно, від 5 до 100 мпа*с. Диспергованими у воді полімерами є такі, які при контакті з водою утворюють колоїдні дисперсії, а не прозорий розчин. При контакті з водою або водними розчинами полімери, що розбухають у воді, зазвичай утворюють гумистий гель. Водорозчинні полімери переважні. Переважно, фармацевтично прийнятний полімер, застосовуваний відповідно до даного винаходу, має Tg щонайменше 40 °C, переважно щонайменше +50 °C, найбільше переважно, від 80° до 180 °C. "Tg" означає температуру склування. Способи визначення Tg органічних полімерів описані в "Introduction to Physical Polymer Science", 2nd Edition by L. H. Sperling, published by John Wiley & Sons, Inc., 1992. Значення Tg може бути розраховане як середньозважена сума значень Tg для гомополімерів, одержаних для кожного окремого мономера, i, які становлять полімер: Tg=УW iXi, де W є масовий відсоток мономера i в органічному полімері, і X є значенням Tg для гомополімеру, отриманого з мономера i. Значення Tg для гомополімерів можуть бути взяті з "Polymer Handbook", 2nd Edition by J. Brandrup and E. H. Immergut, Editors, published by John Wiley & Sons, Inc., 1975. Різні добавки, що містяться в продукті твердої дисперсії, або навіть сам активний інгредієнт можуть виявляти пластифікуючу дію на полімер, тим самим знижувати Tg полімеру так, що кінцевий продукт твердої дисперсії буде мати більш низьку Tg, ніж вихідний полімер, застосовуваний для одержання. Загалом, кінцевий продукт твердої дисперсії має Tg 10 °C або вище, переважно, 15 °C або вище, більш переважно, 20 °C або вище, і найбільш переважно, 30 °C або вище. Наприклад, переважні фармацевтично прийнятні полімери можуть бути вибрані із групи, що включає гомополімери і співполімери N-вініллактамів, особливо гомополімерів і співполімерів Nвінілпіролідону, наприклад, полівінілпіролідон (ПВП), співполімери N-вінілпіролідону та вінілацетату або вінілпропіонату, складні ефіри целюлози, прості ефіри целюлози й складні-прості ефіри целюлози, зокрема, метилцелюлоза та етилцелюлоза, гідроксіалкілцелюлоза, зокрема, гідроксипропілцелюлоза, гідроксіалкілалкілцелюлози, зокрема гідроксипропілметилцелюлоза, фталати або сукцинати целюлози, зокрема ацетатфталат целюлози й фталат гідроксипропілметилцелюлози, сукцинат гідроксипропілметилцелюлози або ацетатсукцинат гідроксипропілметилцелюлози; високомолекулярні поліалкіленоксиди, такі як поліетиленоксид і поліпропіленоксид і співполімери етиленоксиду та пропіленоксиду, щеплені співполімери полівінілового спирту-поліетиленгліколю (доступні як Kollicoat® IR від BASF SE, Ludwigshafen, Germany); 3 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 поліакрилати та поліметакрилати, такі як співполімери метакрилової кислоти/етилацетату, співполмери метакрилової кислоти/метилметакрилату, співполімери бутилметакрилату/2диметиламіноетилметакрилату, полі(гідроксіалкілакрилати), полі(гідроксіалкілметакрилати), поліакриламіди, вінілацетатні полімери, такі як співполімери вінілацетату й кротонової кислоти, особливо гідролізований полівінілацетат (що також називається частково омилений "полівініловий спирт), полівініловий спирт, оліго- і полісахариди, такі як карагенани, галактоманани та ксантанова камедь, або суміші одного або більше із них. Серед них переважні гомополмери або співполімери N-вінілпіролідону, зокрема, співполімер N-вінілпіролідону та вінілацетат ацетат. Особливо переважним полімером є співполімер 60 % мас. співполімеру, N-вінілпіролідону, і 40 % мас. співполімеру, вінілацетату. Різні види комерційно доступних гомополімерів N-вінілпіролідону (також позначені як полівінілпіролідо або ПВП) включають ПВП K-12, ПВП K-15, ПВП K-17, ПВП K-20, ПВП K-30, ПВП K-60, ПВП K-90 і ПВП K-120. Значення К, вказане в цій номенклатурі, розраховують за формулою Фікентера з в'язкості ПВП у водному розчині, щодо цього показника для води. Усі вони можуть застосовуватися, але особливо переважні ПВП K-12, ПВП K-15, ПВП K-17, ПВП K-20 і ПВП K-30. Іншим полімером, який може застосовуватися, є Kollidon® SR (від BASF SE, Ludwigshafen, Germany), який містить суміш ПВП і полівінілацетату. Термін "фармацевтично прийнятна поверхнево-активна речовина" у даному описі належить до фармацевтично прийнятної неіонної поверхнево-активної речовини. Поверхнево-активна речовина може виконувати миттєве емульгування активного агента, виділюваного з дозованої формі і/або запобігати осадженню активного інгредієнта у водних рідинах шлунково-кишкового тракту. Може застосовуватися єдина поверхнево-активна речовина або комбінація поверхневоактивних речовин. Відповідно до одного з варіантів даного винаходу, продукт твердої дисперсії містить комбінацію двох або більше фармацевтично прийнятних поверхнево-активних речовин. Переважні поверхнево-активні речовини вибирають зі складних ефірів жирних кислот сорбітану, складних ефірів поліалкоксильованих жирних кислот, таких як, наприклад, поліалкоксильовані гліцериди, поліалкоксильовані складні ефіри жирної кислоти сорбітану або складні ефіри жирних кислот поліалкіленгліколів, поліалкоксильовані прості ефіри жирних спиртів, сполуки токоферилу або суміші двох або більше із них. Ланцюг жирної кислоти в таких сполуках як правило містить від 8 до 22 атомів вуглецю. Поліалкіленоксидні блоки містять у середньому від 4 до 50 одиниць алкіленоксиду, переважно, одиниць етиленоксиду, на молекулу. Придатні складні ефіри жирних кислот сорбітану включають монолаурат сорбітану, монопальмітат сорбітану, моностеарат сорбітану (Span® 60), моноолеат сорбітану (Span® 80), тристеарат сорбітану, триолеат сорбітану, моностеарат сорбітану, монолаурат сорбітану або моноолеат сорбітану. Приклади придатних складних ефірів поліалкоксильованих жирних кислот включають поліоксіетилен (20) монолаурат сорбітану, поліоксіетилен (20) монопальмітат сорбітану, поліоксіетилен (20) моносетарат сорбітану, поліоксіетилен (20) моноолеат сорбітану (Tween® 80), поліоксіетилен (20) тристеарат сорбітану (Tween® 65), поліоксіетилен (20) триолеат сорбітану (Tween® 85), поліоксіетилен (4) моностеарат сорбітану, поліоксіетилен (4) монолаурат сорбітану або поліоксіетилен (4) моноолеат сорбітану. Придатні поліалкоксильовані гліцериди одержують, наприклад, алкоксилюванням природних або гідрованих гліцеридів або трансестерифікацією природних або гідрованих гліцеридів з поліалкіленгліколями. Комерційно доступні приклади включають поліоксіетиленгліцерин рицинолеат 35, поліоксіетиленгліцерин тригідроксистеарат 40 (Cremophor® RH40, BASF SE) і поліалкоксильовані гліцериди, такі, які одержують під торговими марками Gelucire® і Labrafil® від Gattefosse, наприклад, Gelucire® 44/14 (лауроїлмакроголь 32 гліцериди, одержані трансестерифікацією гідрованої пальмовоядерної олії з ПЕГ PEG 1500), Gelucire® 50/13 (стеароїлмакроголь 32 гліцериди, одержані трансестерифікацією гідрованої пальмової масла з ПЕГ 1500) або Labrafil M 1944 CS (олеоїлмакроголь 6 гліцериди, одержані трансефтерифікацією абрикосової олії з ПЕГ 300). Придатними складними ефірами жирних кислот поліалкіленгліколів є, наприклад, ПЕГ 660 гідроксистеаринова кислота (полігліколевий ефір 12-гідроксистеаринової кислоти (70 % моль.) з 30 % мл. етиленгліколю). Придатні поліалкоксильовані прості ефіри жирних спиртів включають, наприклад, ПЕГ (2) стеариловий ефір (Brij® 72), макроголь 6 цетилстеариловий ефір або макроголь 25 цетилсткариловий ефір. 4 UA 100866 C2 Загалом, сполука токоферилу відповідає представленій нижче формулі 5 10 15 20 25 30 35 40 45 , 1 2 де Z є сполучною групою, R і R є, незалежно один від одного, воднем або C1-C4 алкілом і n дорівнює цілому числу від 5 до 100, переважно, від 10 до 50. Зазвичай, Z є залишком аліфатичної двохосновної кислоти, такої як глутарова, бурштинова або адипінова кислоти. 1 2 Переважно, обидва R і R є воднем. Переважною сполукою токоферилу є сукцинат альфа-токоферил поліетиленгліколю, який зазвичай називають вітамін E TPGS. Вітамін E TPGS є розчинною у воді формою природного джерела вітаміну E, отриманою естерифікацією сукцинату d-альфа-токоферилової кислоти з поліетиленгліколем 1000. Вітамін E TPGS доступний від Eastman Chemical Company, Kingsport, TN, USA і вказаний у фармакопеї США (NF). Було виявлено, що поверхнево-активні речовини або комбінації поверхнево-активних речовин, що мають певне значення HLB (гідрофільно-ліпофільного балансу) переважні в порівнянні з іншими солюбілізаторами. th Система HLB (Fiedler, H. B., Encylopedia of Excipients, 5 ed., Aulendorf: ECV-EDITIOCANTOR-VERLAG (2002)) включає множину значень для поверхнево-активних речовин, де ліпофільні речовини одержують більш низькі значення HLB, а гідрофільні речовини одержують більш високі значення HLB. В переважних варіантах, фармацевтично прийнятна поверхнево-активна речовина містить щонайменше одну поверхнево-активну речовину, що має значення HLB 10 або більше. Солюбілізатори, що мають значення HLB 10 або більше, можуть бути вибрані з Gelucire® 44/14 (HLB 14), Cremophor® RH40 (HLB 13), Tween® 65 (HLB 10,5), Tween® 85 (HLB 11). Переважними солюбілізаторами з високим HLB є сполуки токоферилу, що мають поліалкіленгліколевий зв'язок. У переважному варіанті застосовують поєднання солюбілізаторів, яке включає (i) щонайменше одну сполуку токоферилу, яка має поліалкіленгліколеву групу, переважно, сукцинат альфа-токоферил поліетиленгліколю, і (ii) щонайменше один складний ефір жирної кислоти поліалкоксильованого багатоатомного спирту. Сполукою токоферилу, переважно, є сукцинат альфа-токоферил поліетиленгліколю. Складним ефіром жирної кислоти поліалкоксильованого багатоатомного спирту, переважно, є поліалкоксильований гліцерид. Масове співвідношення сполуки токоферилу і складний ефір жирної кислоти поліалкоксильованого багатоатомного спирту, переважно, становить від 0,2:1 до 1:1. В одному варіанті, активним агентом є активний агент на основі N-арилсечовини. Активні агенти на основі N-арилсечовини є біологічно активними сполуками, які містять щонайменше одну групу сечовини в молекулярній структурі, де один або обидва атоми азоту заміщені арильною групою, і які виявляють місцеву фізіологічну дію, а також, виявляють системну дію після перорального введення. Арильною групою може бути карбоциклічна або гетероциклічна ароматична група. Приєднання до атома азоту зазвичай відбувається через атом вуглецю арильної групи. Конденсована ароматична група може бути зв'язана з атомом азоту через ароматичний або не ароматичний атом вуглецю. Арильна група, зазвичай, може бути заміщена іншими замісниками. Зазвичай, активний агент на основі N-арилсечовини представлений загальною формулою , де 1 2 G і G є, незалежно один від одного, карбоциклічним кільцем, вибраним з фенілу, нафтилу, бензоциклобутанілу, дигідронафтилу, тетрагідронафтилу, бензоциклогептанілу, бензоциклогептенілу, інданілу та інденілу; 5 UA 100866 C2 5 10 15 20 25 30 35 системою кілець, вибраною з (дигідро)бензоксазинілу, бензімідазолілу, індазолілу, бензотіазолілу, бензооксазолілу, бензізоксазолілу, бензофуранілу, (дигідро)бензопіранілу, бензодіоксолілу, (дигідро)хіналдинілу, (дигідро)хіназолінілу, (дигідро)хіноксалінілу, (дигідро)ізохінолінілу, (дигідро)хінолінілу, індолілу, ізоіндолілу, індолінілу, пуринілу, тетрагідрохінолініду, індазолілу, імідазопіридиніла, піразолопіридиніла, піразолопіримідиніла, піролопіримідинілу, піролопіридиніла, піридопіразинілу, піридопіримідинілу, піридооксазинілу, піридотіазинілу, піридооксазолілу, піридотіоксазолілу, піримідопіримідину, птеридинілу, цинолінілу й нафтиридинілу; 1 2 де G або G або обидва можуть бути заміщені одним або більше замісниками, наприклад, вибраними із групи, що включає C1-6 розгалужений або нерозгалужений алкіл, C1-6 галоалкіл, C16 розгалужений або нерозгалужений ацил, C 1-6 розгалужений або нерозгалужений алкокси, галоген, C1-6 розгалужений або нерозгалужений алкілоксикарбоніл, гідрокси, аміно, моно- або ді(C1-4 алкіл)аміно, моно- або ді-(C1-4 алкіл)аміно-SO2, ціано, нітро або H2NSO2, Z є 1, 4-феніленом, і n дорівнює 0 або 1, або його фармацевтично прийнятними солями, складними ефірами, ізомерами, гідратами або сольватами. У цій номенклатурі префікс "(дигідро)" позначає або дигідросполуку, або ароматичну сполуку без префікса; в такий спосіб (дигідро)бензоксалініл означає або дигідробензоксалініл, або бензоксалініл, і т.д. В одному варіанті, активним агентом є щонайменше одна сполука формули (I) , або її фармацевтично прийнятна сіль або проліки, де --- відсутній або є одинарним зв'язком; X2 є N або CR2; X3 є N, NR3 або CR3; X4 є зв'язком, N або CR4; X5 є N або C; за умови, що щонайменше один з X1, X2, X3 і X4 є N; Z1 є O, NH або S; Z2 є зв'язком, NH або O; Ar1 вибирають із групи, що включає і ; R1, R3, R5, R6 і R7 кожний незалежно вибирають із групи, що включає водень, алкеніл, алкокси, алкоксіалкокси, алкоксіалкіл, алкоксикарбоніл, алкоксикарбонілалкіл, алкіл, алкілкарбоніл, алкілкарбонілалкіл, алкілкарбонілокси, алкілтіо, алкініл, карбокси, карбоксіалкіл, ціано, ціаноалкіл, циклоалкіл, циклоалкілалкіл, форміл, формілалкіл, галоалкокси, галоалкіл, галоалкілтіо, галоген, гідрокси, гідроксіалкіл, меркапто, меркаптоалкіл, нітро, (CF 3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2-, RBO(SO)2-, ZAZBN-, (ZAZBN)алкіл, (ZAZBN)карбоніл, (ZAZBN)карбонілалкіл і (ZAZBN)сульфоніл; 6 UA 100866 C2 5 10 15 20 25 30 35 40 R2 і R4 кожний незалежно вибирають із групи, що включає водень, алкеніл, алкокси, алкоксіалкокси, алкоксіалкіл, алкоксикарбоніл, алкоксикарбонілалкіл, алкіл, алкілкарбоніл, алкілкарбонілалкіл, алкілкарбонілокси, алкілтіо, алкініл, карбокси, карбоксіалкіл, ціано, ціаноалкіл, циклоалкіл, циклоалкілалкіл, форміл, формілалкіл, галоалкокси, галоалкіл, галоалкілтіо, галоген, гідрокси, гідроксіалкіл, меркапто, меркаптоалкіл, нітро, (CF 3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2-, R6O(SO)2-, ZAZBN-, (ZAZBN)алкіл, (ZAZBN)алкілкарбоніл, (ZAZBN)карбоніл, (ZAZBN)карбонілалкіл, (ZAZBN)сульфоніл, (ZAZBN)C(=NH)-, (ZAZBN)C(=NCN)NH- і (ZAZBN)C(=NH)NH-; R8a є воднем або алкілом; R8b відсутній або є воднем, алкокси, алкоксикарбонілалкілом, алкілом, алкілкарбонілокси, алкілсульфонілокси, галогеном або гідрокси; R9, R10, R11 і R12 кожний окремо вибирають із групи, що включає водень, алкеніл, алкокси, алкоксіалкокси, алкоксіалкіл, алкоксикарбоніл, алкоксикарбонілалкіл, алкіл, алкілкарбоніл, алкілкарбонілалкіл, алкілкарбонілокси, алкілтіо, алкініл, арил, карбокси, карбоксіалкіл, ціано, ціаноалкіл, форміл, формілалкіл, галоалкокси, галоалкіл, галоалкілтіо, галоген, гетероарил, гетероцикл, гідрокси, гідроксіалкіл, меркапто, меркаптоалкіл, нітро, (CF 3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2-, R6O(SO)2-, ZAZBN-, (ZAZBN)алкіл, (ZAZBN)карбоніл, (ZAZBN)карбонілалкіл і (ZAZBN)сульфоніл, де ZA і ZB кожний незалежно є воднем, алкілом, алкілкарбонілом, формілом, арилом або арилалкілом, за умови, що щонайменше один з R 9, R10, R11 або R12 відрізняється від водню, або R10 і R11 разом з атомами, до яких вони приєднані, утворюють циклоалкільне, циклоалкенільне або гетероциклічне кільце; R13 вибирають із групи, що включає водень, алкіл, арил, гетероарил і галоген; RA є воднем або алкілом; і RB є алкілом, арилом або арилалкілом; за умови, що R8b відсутній, якщо X5 є N. В одному варіанті даного винаходу, активним агентом є щонайменше однієї сполуки формули (I), де --- відсутній; X1 є CR1; X2 є N; X3 є NR3; X4 є зв'язком; X5 є N; Z1 є O; Z2 є NH; Ar1 вибирають із групи, що включає і R8b відсутній; і R1, R3, R5, R6, R7, R8a, R9, R10, R11, R12 і R13 такі, як визначені у формулі (I). В іншому варіанті даного винаходу, активним агентом є щонайменше одна сполука формули (I), де --- відсутній; X1 є CR1; X2 є N; X3 є NR3; X4 є зв'язком; X5 є N; Z1 є O; Z2 є NH; Ar1 вибирають із групи, що включає і R1 вибирають із групи, що включає водень, алкіл, галоген і гідроксіалкіл; R 3, R5, R6, R7 і R8a є воднем; R8b відсутній; і R9, R10, R11, R12 і R13 такі, як визначені у формулі (I). В іншому варіанті даного винаходу, активним агентом є щонайменше одна сполука формули (I), де --- відсутній; X1 є CR1; X2 є N; X3 є NR3; X4 є зв'язком; X5 є N; Z1 є O; Z2 є NH; Ar1 вибирають із групи, що включає і 7 UA 100866 C2 5 10 15 R1 вибирають із групи, що включає водень, алкіл і гідроксіалкіл; R3, R5, R6, R7 і R8a є воднем; щонайменше один з R9, R10, R11 і R12 незалежно вибирають із групи, що включає алкіл, алкокси, алкоксіалкіл, арил, ціаноалкіл, галоген, галоалкіл, галоалкокси та гетероцикл; R 8b відсутній; і R13 такий, як визначений у формулі (I). В іншому варіанті даного винаходу, активним агентом є щонайменше одна сполука формули (I) де --- відсутній; X1 є CR1; X2 є N; X3 є NR3; X4 є зв'язком; X5 є N; Z1 є O; Z2 є NH; Ar1 вибирають із групи, що включає і R1 вибирають із групи, що включає водень, алкіл і гідроксіалкіл; R3, R5, R6, R7 і R8a є воднем; щонайменше один з R9, R10, R11 і R12 незалежно вибирають із групи, що включає алкіл, алкокси, алкоксіалкіл, ціаноалкіл, галоген, галоалкіл і галоалкокси; R 3b відсутній; і R13 такий, як визначений у формулі (I). В іншому варіанті, активним агентом є щонайменше одна сполука формули (I), де Ar 1 є R14 і R15 кожний окремо вибирають із групи, що включає водень і алкіл, або R 14 і R15 разом з атомом, до якого вони приєднані, утворюють циклоалкільне кільце, і X1, X2, X3, X4, X5, Z1, Z2, R1, R2, R3, R4, R5, R6, R7, R8a, R8b, R9, R10, R11 і R12 такі, як визначені у формулі (I). В іншому варіанті, активним агентом є щонайменше одна сполука формули (VII), , 20 25 де Ar1 є R14 і R15 кожний окремо вибирають із групи, що включає водень і алкіл, або R14 і R15 взяті разом з атомом, до якого вони приєднані, утворюють циклоалкільне кільце, і X5, Z1, Z2, R1, R2, R3, R4, R5, R6, R7, R8a, R8b, R9, R10, R11 і R12 такі, як визначені у формулі (I). Сполуки, охоплені цим класом, включають: N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)- N'-5-ізохінолінілсечовину; N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-(3-метил-5-ізохінолініл)сечовину; (+) N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-(3-метил-5-ізохінолініл)сечовину; (-) N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-(3-метил-5-ізохінолініл)сечовину; 8 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 (-) N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)- N'-5-ізохінолінілсечовину; (+) N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)- N'-5-ізохінолінілсечовину; N-(5-бром-2,3-дигідро-1Н-інден-1-іл)- N'-5-ізохінолінілсечовину; метил 4-({[(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Н-індазол-1карбоксилат; N-(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)-N'-1Н-індазол-4-ілсечовину (ABT-102); метил 4-[({[(1S)-5-трет-бутил-2,3-дигідро-1Н-інден-1-іл]аміно}карбоніл)аміно]-1Н-індазол-1карбоксилат; метил 4-[({[(1R)-5-трет-бутил-2,3-дигідро-1Н-інден-1-іл]аміно}карбоніл)аміно]-1Н-індазол-1карбоксилат; N-[(1S)-5-трет-бутил-2,3-дигідро-1Н-інден-1-іл]-N'-1Н-індазол-4-ілсечовину; N-[(1R)-5-трет-бутил-2,3-дигідро-1Н-інден-1-іл]-N'-1Н-індазол-4-ілсечовину; метил 4-[({[5-(трифторметил)-2,3-дигідро-1Н-інден-1-іл]аміно}карбоніл)аміно]-1Н-індазол-1карбоксилат; N-1H-індазол-4-іл-N'-[5-(трифторметил)-2,3-дигідро-1Н-інден-1-іл]сечовину; метил 4-({[(5-піперидин-1-іл-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Н-індазол-1карбоксилат; N-1H-індазол-4-іл -N'-(5-піперидин-1-іл -2,3-дигідро-1Н-інден-1-іл)сечовину; метил 4-({[(5-гексагідро-1H-азепін-1-іл-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Ніндазол-1-карбоксилат; N-(5-гексагідро-1H-азепін-1-іл-2,3-дигідро-1Н-інден-1-іл)-N'-1Н-індазол-4-ілсечовину; N-1H-індазол-4-іл-N'-[(1R)-5-піперидин-1-іл-2,3-дигідро-1Н-інден-1-іл]сечовину; N-1H-індазол-4-іл-N'-[(1S)-5-піперидин-1-іл-2,3-дигідро-1Н-інден-1-іл]сечовину; ізопропіл 4-({[(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Н-індазол-1карбоксилат; і ізобутил 4-({[(5-трет-бутил-2,3-дигідро-1Н-інден-1-іл)аміно]карбоніл}аміно)-1Н-індазол-1карбоксилат. Усі ці сполуки були одержані раніше й описані в патенті США № 7015233. Дозовані формі, в яких активним агентом є сполука формули (I) або (VII) або її фармацевтично прийнятна сіль або проліки, можуть застосовуватися для лікування розладу через інгібування підтипу ванілоїдного рецептора. Розлад може бути вибраний з болю, підвищеної активності сечового міхура, нетримання сечі й запальної термічної алодинії. AВ даному описі й формулі винаходу наступний терміни мають наступне значення: Термін "алкеніл" у даному описі означає прямий або розгалужений вуглеводень, що містить від 2 до 10 атомів вуглецю, і що містить щонайменше один подвійний зв'язок вуглець-вуглець, утворений двома атомами водню. Типові приклади алкенілу включають, але не обмежені ними, етеніл, 2-пропеніл, 2-пропеніл, 3-бутеніл, 4-пентеніл, 5-гексеніл, 2-гептеніл, 1-гептеніл і 3деценіл. Термін "алкокси" у даному описі позначає алкільну групу, таку як визначена тут, приєднану до основної молекулярної групи через атом кисню. Типові приклади алкокси включають, але не обмежені ними, метокси, етокси, пропокси, 2-пропокси, бутокси, третбутокси, пентилокси й гексилокси. Термін "алкоксіалкокси" у даному описі, означає алкоксигрупу, таку як визначена тут, приєднану до основної молекулярної групи через алкоксигрупу, таку як визначена тут. Типові приклади алкоксіалкокси включають, але не обмежені ними, метоксиметокси, етоксиметокси та 2-етоксіетокси. Термін "алкоксіалкіл" у даному описі, означає алкоксигрупу, таку, як визначена тут, приєднану до основної молекулярної групи через алкільну групу, таку, як визначена тут. Типові приклади алкоксіалкілу включають, але не обмежені ними, трембутоксиметил, 2-етоксіетил, 2метоксіетил і метоксиметил. Термін "алкоксикарбоніл" у даному описі, означає алкоксигрупу, таку, як визначена тут, приєднану до основної молекулярної групи через карбонільну групу, таку, як визначена тут. Типові приклади алкоксикарбонілу включають, але не обмежені ними, метоксикарбоніл, етоксикарбоніл і трет-бутоксикарбоніл. Термін "алкоксикарбонілалкіл" у даному описі, означає алкоксикарбонільну групу, таку, як визначена тут, приєднану до основної молекулярної групи через алкільну групу, таку, як визначена тут. Типові приклади алкоксикарбонілалкілу включають, але не обмежені ними, 3метоксикарбонілпропіл, 4-етоксикарбонілбутил і трет-бутоксикарбонілетил. Термін "алкіл" у даному описі, означає прямий або розгалужений вуглеводень, що містить від 1 до 10 атомів вуглецю. Типові приклади алкілу включають, але не обмежені ними, метил, 9 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 етил, н-пропіл, с-пропіл, н-бутил, втор-бутил, ізо-бутил, трет-бутил, н-пентил, ізопентил, неопентил, н-гексил, 3-метилгексил, 2,2-диметилпентил, 2,3-диметилпентил, н-гептил, н-октил, н-ноніл і н-децил. Термін "алкілкарбоніл" у даному описі, означає алкільну групу, таку, як визначена тут, приєднану до основної молекулярної групи через карбонільну групу, таку як визначена тут. Типові приклади алкілкарбонілу включають, але не обмежені ними, ацетил, 1-оксопропіл, 2,1оксопропіл, 1-оксобутил і 1-оксопентил. Термін "алкілкарбонілалкіл" у даному описі, означає алкілкарбонільну групу, таку, як визначена тут, приєднану до основної молекулярної групи через алкільну групу, таку, як визначена тут. Типові приклади алкілкарбонілалкілу включають, але не обмежені ними, 2оксопропіл, 3,2-оксопропіл, 3-оксобутил і 3-оксопентил. Термін "алкілкарбонілокси" у даному описі, означає алкілкарбонільну групу, таку, як визначена тут, приєднану до основної молекулярної групи через атом кисню. Типові приклади алкілкарбонілокси включають, але не обмежені ними, ацетилокси, етилкарбонілокси та третбутилкарбонілокси. Термін "алкілсульфоніл" у даному описі, означає алкільну групу, таку, як визначена тут, приєднану до основної молекулярної групи через сульфонільну групу. Типові приклади алкілсульфонілу включають, але не обмежені ними, метилсульфоніл і етилсульфоніл. Термін "алкілтіо" у даному описі, означає алкільну групу, таку, як визначена тут, приєднану до основної молекулярної групи через атом сірки. Типові приклади алкілтіо включають, але не обмежені ними, метилсульфаніл, етилсульфаніл, трефбутилсульфаніл і гексилсульфаніл. Термін "алкініл" у даному описі, означає прямий або розгалужений вуглеводень, що містить від 2 до 10 атомів вуглецю, і що містить щонайменше один потрійний зв'язок вуглець-вуглець. Типові приклади алкінілу включають, але не обмежені ними, ацетиленіл, 1-пропініл, 2-пропініл, 3-бутиніл, 2-пентиніл і 1-бутиніл. Термін "арил" у даному описі, означає фенільну групу, або біциклічну або трициклічну конденсовану систему кілець, де одне або більше із конденсованих кілець є фенільною групою. Біциклічні конденсовані кільцеві системи представлені фенільною групою, конденсованою із циклоалкільною групою, такою, як визначена тут, або іншою фенільною групою. Трициклічні конденсовані системи кілець представлені біциклічними конденсованими системами кілець, конденсованими із циклоалкільною групою, такою, як визначена тут, або іншою фенільною групою. Типові приклади арилу включають, але не обмежені ними, антраценіл, азуленіл, флуореніл, інденіл, нафтил, феніл і тетрагідронафтил. Термін "циклоалкіл" у даному описі, означає насичену моноциклічну систему кілець, що містить від 3 до 8 атомів вуглецю. Приклади циклоалкілу включають циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і циклооктил. Термін "форміл" у даному описі, означає -C(O)H групу. Термін "гало" або "галоген" у даному описі, означає -Cl, -Br, -I або -F. Термін "галоалкокси" у даному описі, означає щонайменше один галоген, такий, як визначений тут, приєднаний до основної молекулярної групи через алкоксигрупу, таку, як визначена тут. Типові приклади галоалкокси включають, але не обмежені ними, хлорметокси, 2фторетокси, трифторметокси, 3-фторпентилокси та пентафторетокси. Термін "галоалкіл" у даному описі, означає щонайменше один галоген, такий, як визначений тут, приєднаний до основної молекулярної групи через алкільну групу, таку, як визначена тут. Типові приклади галоалкілу включають, але не обмежені ними, хлорметил, 2-фторетил, трифторметил, пентафторетил і 3-фторпентил. Термін "гетероцикл" у даному описі, належить до три-, чотири-, п'яти-, шести-, семи- або восьмичленного кільця, що містить один або два гетероатоми, незалежно вибраних із групи, що включає азот, кисень і сірку. Тричленне кільце має нуль подвійних зв'язків. Чотири- і п'ятичленне кільце має нуль або один подвійний зв'язок. Шестичленне кільце має нуль, один або два подвійні зв'язки. Семи- і восьмичленне кільце має нуль, один, два або три подвійні зв'язки. Гетероциклічні групи відповідно до даного винаходу можуть бути приєднані в основній молекулярній групі через атом вуглецю або атом азоту. Типові приклади гетероциклу включають, але не обмежені ними, азабіцикло[2.2.1]гептаніл, азабіцикло[2.2.1.]октаніл, азетидиніл, гексагідро-1H-азепініл, гексагідроазоцин-(2H)-іл, індазоліл, морфолініл, октагідроізохінолін, піперазиніл, піперидиніл, піридиніл, піролідиніл і тіоморфолініл. Термін "меркаптоалкіл" у даному описі означає меркаптогрупу, приєднану до основної молекулярної групи через алкільну групу, таку, як визначена тут. Типові приклади меркаптоалкіл включають, але не обмежені ними, 2-меркаптоетил і 3-меркаптопропіл. 10 UA 100866 C2 В одному варіанті даного винаходу активним агентом є 1-((R)-5-трет-бутиліндан-1-іл)-3-(1Hіндазол-4-іл)-сечовина (ABT102) 5 10 15 20 25 30 35 40 45 50 , або її солі або гідрати або сольвати. В іншому варіанті даного винаходу, активний агент вибирають з однієї з наступних сполук: N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4-ілсечовина; N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-6-фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина; N-[(4R)-6-фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-(1-метил-1Hіндазол-4-іл)сечовина; N-[(4R)-6-фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-1H-індазол-4ілсечовина; N-[(4R)-6-фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-[(7S)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина; N-[(4S)-6-фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-[(7S)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина; N-[(4S)-6-фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина; N-[(4R)-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4-іл)сечовина; N-[(4R)-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1іл]сечовина; N-[(4R)-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1іл]сечовина; N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4-іл)сечовина; N-[(4R)-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4-ілсечовина; N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; 11 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 N-[(4R)-7-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-8-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4-ілсечовина; N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина; N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(3-метилізохінолін-5-іл)сечовина; N-[(4R)-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-8-ілсечовина; N-[(4R)-2,2-диметил-7-(трифторметокси)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол4-іл)сечовина; N-[(4R)-2,2-диметил-7-(трифторметокси)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина; N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4ілсечовина; N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-8ілсечовина; N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина; N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4ілсечовина; N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4-іл)сечовина; N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина; N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-2,2-діетил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4-іл)сечовина; N-[(4R)-2,2-діетил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина; N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина; N-[(4R)-2,2-діетил-8-(трифторметокси)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(3-метилізохінолін-5-іл)сечовина; N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина; N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4-илсечовина; N-(1-метил-1H-індазол-4-ил)-N'-[(4R)-8-(трифторметил)-3,4-дигідро-2H-хромен-4іл]сечовина; N-[(4R)-2,2-діетил-6,8-дифтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-6-фтор-2,2-дипропіл-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина; N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(3-метилізохінолін-5-іл)сечовина; N-1H-індазол-4-іл-N'-[(4R)-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]сечовина; N-ізохінолін-5-ил-N'-[(4R)-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]сечовина. Продукт твердої дисперсії одержують способом, який включає a) одержання рідкої суміші, що містить щонайменше один активний агент, щонайменше один фармацевтично прийнятний матрицеутворюючий агент, щонайменше одну фармацевтично прийнятну поверхнево-активну речовину та щонайменше один розчинник, і b) видалення розчинника(ів) з рідкої суміші з одержанням продукту твердої дисперсії. 12 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 Як описано вище щонайменше один наповнювач може, переважно, бути доданий до рідкої суміші перед видаленням розчинника(ів). Придатними розчинниками є такі, які здатні розчиняти або солюбілізувати матрицеутворюючий агент. Зазвичай застосовують не водні розчинники. Може застосовуватися будь-який такий розчинник, однак, фармацевтично прийнятні розчинники є переважними, тому що сліди розчинника можуть залишатися у висушеному продукті твердої дисперсії. Придатним чином, розчинник може бути вибраний із групи, що включає алканоли, такі як метанол, етанол, ізопропанол, н-пропанол, ізобутанол, н-бутанол; вуглеводні, такі як пентан, гексан, циклогексан, метилциклогексан, толуол, ксилол; галогеновані вуглеводні, такі як дихлорметан, трихлорметан, дихлоретан, хлорбензол; кетони, такі як ацетон; складні ефіри, такі як етилацетат; прості ефіри, такі як діоксан, тетрагідрофуран; і комбінації двох або більше з них. Етанол особливо переважний завдяки його біодоступності, розчинюючій силі і фармацевтичній безпеці. Рідка суміш може бути отримана будь-яким придатним способом взаємодії основних інгредієнтів, тобто фармацевтично прийнятного матрицеутворюючого агента, активного агента, фармацевтично прийнятної поверхнево-активної речовини й розчинники або комбінації розчинників. В одному варіанті, рідку суміш одержують розчиненням фармацевтично прийнятного матрицеутворюючого агента з одержанням розчину матрицеутворюючого агента, і додаванням активного агента й фармацевтично прийнятної поверхнево-активної речовини до розчину. Розчинений матрицеутворюючий агент може виявляти поліпшуюче розчинність дія на активний агент; таким чином, розчинність активного агента в матрицеутворюючому агенті може стати в кілька раз вище, ніж його розчинність у чистому розчиннику. Переважно, активний агент практично повністю розчиняється в рідкій суміші. Рідка суміш містить суху речовину в кількості аж до 90 % мас., наприклад, від 0,5 до 90 % мас., у більшості випадків від 2 до 60 % мас., відносно загальної маси рідкої суміші. Розчинник(і) можуть бути вилучені будь-яким придатним методом, відомим у даній галузі техніки, таким як сушіння розпиленням, барабанне сушіння, сушіння на стрічці, сушіння на лотках, сушіння в псевдорозрідженому шарі або комбінація двох або більше з них. Наприклад, первинний порошок твердої дисперсії, одержаний сушінням розпиленням, може бути далі висушений сушінням на лотках (необов'язково у вакуумі). В одному варіанті, видалення розчинника включає стадію сушіння розпиленням, необов'язково в комбінації з однією або більше стадіями сушіння, що відрізняються від сушіння розпиленням. Залишковий вміст розчинника в кінцевому продукті твердої дисперсії переважно становить 5 % мас. або менше, більш переважно, 1 % мас. або менше. При сушінні розпиленням рідину, що висушується, суспендують у потоці газу, наприклад, повітря, тобто рідину перетворюють на водяний пил (розпилений) що має більшу площу поверхні. Розпилену рідину обробляють потоком гарячого газу в сушильній камері. Волога швидко випаровується, і тверді речовини виділяють у вигляді порошку, що складається із дрібних порожніх сферичних частинок. Температура газу на вході становить аж до 250 °C або навіть вище, через випарювання температура газу дуже швидко знижується до температури від близько 30 до близько 150 °C (температура газу на виході). Принцип барабанної сушарки (вальцьової сушарки) полягає в тому, що плівку з матеріалу наносять на гладку поверхню нагрітого металевого барабана, що безперервно обертається. Плівку висушеного матеріалу безперервно знімають стаціонарним ножем, розташованим навпроти місця нанесення рідкого матеріалу. Сушарка складається з одного барабана або пари барабанів з або без "допоміжних" роликів. Барабан(і) можуть бути поміщені у вакуумну камеру. Придатним чином, пари розчинника збирають, і розчинник відновлюють і рециркулюють. При сушінні на стрічці рідину розпилюють на стрічку, яка проходить над декількома нагрітими пластинами, розташованими під стрічкою. Матеріал нагрівається пластинами, які нагрівають парою або електрикою. Випарювання розчинника додатково може бути посилене інфрачервоними радіаторами або мікрохвильовими радіаторами, розташованими над стрічкою. Сушіння на стрічці може проводитися у вакуумній камері. При сушінні на лотку рідку суміш (або продукт дисперсії, який був попередньо висушений будь-яким іншим методом) розподіляють на множини лотків. Їх поміщають у піч, зазвичай в потік гарячого газу, наприклад, повітря. Додатково може застосовуватися вакуум. Висушений продукт твердої дисперсії потім може бути розмелений і/або класифікований (просіяний). Потім висушений продукт твердої дисперсії може бути засипаний у капсули або може бути спресований. Пресування означає процес, в якому порошкову масу, що містить продукт твердої дисперсії, ущільнюють під високим тиском для одержання брикету з низькою пористістю, 13 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, таблетки. Пресування порошкової маси зазвичай проводять на таблетковому пресі, більш конкретно, у сталевому отворі між двох поршнів, що рухаються. Щонайменше одну добавку вибирають із регуляторів потоку, розпушувачів, наповнювачів і мастильних агентів і, переважно, застосовують при пресуванні гранул. Розпушувачі забезпечують швидке розкладання брикету в шлунку, і зберігають вивільнені гранули окремо одна від одної. Придатні розпушувачі включають поперечно-зшиті полімери, такі як поперечнозшитий полівінілпіролідон і поперечно-зшиту карбоксиметилцелюлозу. Придатні наповнювачі вибирають із лактози, гідрофосфату кальцію, мікрокристалічної целюлози (Avicel®), оксиду магнію, природного або попередньо желатинізованого картопляного або кукурудзяного крохмалю, полівінілового спирту. Придатні регулятори потоку вибирають із високодиспергованого двоокису кремнію (Aerosil®) і тваринних і рослинних жирів або вісків. Мастильний агент переважно застосовують при пресуванні гранул. Придатні мастильні агенти вибирають із поліетиленгліколю (наприклад, що має Мм від 1000 до 6000), стеаратів магнію й кальцію, стеарилфумарату натрію, тальку й подібних. Можуть застосовуватися різні інші добавки, наприклад, барвники, такі як азобарвники, органічні або неорганічні пігменти, такі як оксид алюмінію або оксид титану, або барвники природного походження; стабілізатори, такі як антиоксиданти, світлостабілізатори, акцептори радикалів або стабілізатори проти мікробної атаки. Для того щоб сприяти поглинанню такої дозованої формі ссавцем, переважно давати дозовану форму придатної формі. Великі таблетки, які можуть бути проковтнуті комфортно, тому, переважно, мають витягнуту форму, а не круглу. Плівкове покриття на таблетці ще більше спрощує проковтування. Плівкове покриття також поліпшує смак і надає приємний зовнішній вигляд. При бажанні, плівковим покриттям може бути ентеросолюбільне покриття. Плівкове покриття зазвичай включає полімерний плівкоутворювальний матеріал, такий як гідроксипропілметилцелюлоза, гідроксипропілцелюлоза й співполімери акрилату або метакрилату. Крім плівкоутворювального полімеру, плівка також може включати пластифікатор, наприклад, поліетиленгліколь, поверхнево-активну речовину, наприклад, типу Tween®, і, необов'язково, пігмент, наприклад, двоокис титану або оксиди заліза. Плівкове покриття також може містити тальк як антиадгезив. Плівкове покриття зазвичай становить менше 5 % мас. дозованої формі. Представлені в описі малюнки й приклади служать для ілюстрації винаходу, не обмежуючи його. На Фігурі 1 показані рентгенограми ПРД суміші наповнювача, що містить Kollidon-30, Gelucire 44/14 і Вітамін E-TPGS (Фігура 1, зверху) і кристалічного ABT-102 (Фігура 1, знизу). На Фігурі 2 показані рентгенограми ПРД висушених розпиленням твердих дисперсій після зберігання при температурі 40 °C/ВВ 75 % протягом 4 тижнів (друга зверху з 15 % дозуванням ліків) і 6 тижнів (четверта знизу, з 25 % дозуванням ліків). Приклади ABT 102 одержують від Abbott Laboratories, Illinois, U.S.A. Інші активні агенти одержують, як описано нижче. A. Одержання активних агентів Приклад 1 N-[(4R)-6-фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина Приклад 1A: 6-Фтор-2,2-диметилхроман-4-он В 5000мл круглодонну колбу додають 1-(5-фтор-2-гідроксифеніл)етанон (20,0 г, 130 ммоль, Aldrich Chemical), пропан-2-ону (19,0 мл, 260 ммоль) і піролідин (21,5 мл, 260 ммоль) у метанолі (150 мл) з одержанням оранжевого розчину. Реакційну суміш перемішують при температурі навколишнього середовища протягом 48 год. Реакційну суміш виливають в EtОАc (200 мл) і промивають 1N HСl (50 мл), насиченим NaHCO3 (50 мл) і насиченим розчином солі (50 мл). Органічну частину сушать (Na2SO4), фільтрують і концентрують із одержанням оранжевого залишку, який очищають хроматографією на силікагелі (градієнтне елюювання, 0-20 % EtOAc/гексани) з одержанням вказаної в заголовку сполуки (14,2 г, 73,1 ммоль, 56 %) у вигляді + білої твердої речовини. МС (DCl/NH3) m/z 208 (M+NH4) . Приклад 1B: (S)-6-Фтор-2,2-диметилхроман-4-ол Розчин метил трет-бутилового ефіру (34 мл), (R)-дифеніл(піролідин-2-іл)метанолу (1,10 г, 4,35 ммоль) і комплекс боран-N, N-діетиланілін (18,5 мл, 104 ммоль) нагрівають до 45 °C і додають Приклад 1A (16,9 г, 87,0 ммоль) у метил трелт-бутиловому ефірі (136 мл) протягом 75 хв через краплинну лійку. Після додавання РХМС показує завершення реакції. Через 15 хв додаткового перемішування при 45 °C реакційну суміш охолоджують до 10 °C і обробляють 14 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 МеОН (85 мл) протягом 10 хв., зберігаючи температуру 15 °C (виділення H2). Після перемішування протягом 30 хв. при температурі навколишнього середовища додають 2N HСl (85 мл) і реакційну суміш перемішують протягом 10 хв. Додають метил трет-бутиловий ефір (170 мл), і реакційну суміш розділяють. Органічну частину промивають 2N HСl (85 мл) і насиченим розчином солі (35 мл). Водні екстракти повторно екстрагують метил трет-бутиловим ефіром (85 мл). Об'єднані органічні частини сушать (Na2SO4), фільтрують і концентрують із одержанням Прикладу 1B (17,4 г, 89,0 ммоль). Аналіз аналітичної хіральної ВЕРХ (Chiralcel OJ 4,6Ч25 мм, 20 % ізопропанол/гексан, 23 °C, 0,5 мл/хв.) показує 99 % оі до рацемічного посилання (отриманого, як описано вище, із застосуванням боргідриду натрію як + відновлювального агента). МС (DCl/NH3) m/z 197 (M+H) . Приклад 1C: (R)-6-Фтор-2,2-диметилхроман-4-амін Суміш Прикладу 1B (17,1 г, 87,0 ммоль) у ТГФ (340 мл) охолоджують до -30 °C з наступним додаванням метансульфонового ангідриду (16,7 мл, 131 ммоль). До цієї суміші повільно додають N, N-діізопропілетиламін (21,3 мл, 122 ммоль) (внутрішня температура ≤24 °C). Через 30 хв. ~50 % перетворення бачать за РХ/МС, реакційну суміш нагрівають до -10 °C. Через 20 хв. реакційну суміш нагрівають до 0 °C. Через 20 хв. додають ще Ms2O (3,00 г, 0,2 екв.) і N, Nдіізопропілетиламін (2,8 мл, 0,2 екв.), і реакційну суміш перемішують протягом 20 хв. При 0 °C додають ще N, N-діізопропілетиламін (1,40 мл, 0,1 екв.), реакційну суміш перемішують протягом 10 хв., потім охолоджують до -30 °C і обробляють азидом тетра-N-бутиламонію (49,5 г, 174 ммоль). Отриману суспензію повільно нагрівають до температури навколишнього середовища протягом ночі. Через 14 год. додають метанол (85 мл) з наступним додаванням 2N NaOH (85 мл; незначний екзотерм до 27 °C). Реакційну суміш перемішують протягом 30 хв., потім розбавляють МТБЕ (340 мл) і водою (170 мл). Шари розділяють, і органічний шар промивають водою (85 мл), 2N HСl (2Ч85 мл), водою (85 мл) і насиченим розчином солі (34 мл). Кислі промивання повторно екстрагують МТБЕ (85 мл). Об'єднані органічні частини сушать (Na 2SO4), фільтрують і концентрують із одержанням жовтого залишку, який промивають без подальшого очищення. Неочищений продукт азиду суспендують у ТГФ (305 мл) і воді (34 мл) і обробляють трифенілфосфіном (25,1 г, 96,0 ммоль). Жовтий розчин нагрівають до 60 °C протягом 2,5 год. Реакційнусуміш охолоджують і концентрують для видалення ТГФ. Дихлорметан (170 мл), 2N HСl (85 мл) і воду (425 мл) додають для одержання гомогенної двофазної суміші. Шари розділяють, і водну частину промивають дихлорметаном (85 мл). 2N NaOH (100 мл) додають у водний шар, який потім екстрагують дихлорметаном (585 мл), сушать (Na2SO4), фільтрують і концентрують із одержанням вказаної в заголовку сполуки (12,6 г, 64,3 ммоль, 74 %). Аналітична хіральна ВЕРХ (Chiralcel OJ 4,625 мм, 20 % ізопропанол/гексан, 23 °C, 0,5 мл/хв.) + показала 91 % оі до рацемічного еталонного стандарту. МС (DCl/NH3) m/z 196 (M+H) . Приклад 1D: (R)-6-Фтор-2,2-диметилхроман-4-амін сіль (R)-2-гідрокси-2-фенілоцтової кислоти Приклад 1C (12,6 г, 64,3 ммоль) і ізопропанол (126 мл) нагрівають до 50 °C при додаванні (R)-(-)-мигдальної кислоти (9,79 г, 64,3 ммоль). При 43 °C одержують тверді речовини й нагрівання продовжують до 50 °C. Суміш вистоюють при 50 °C протягом 10 хв., потім додають гексан (126 мл) протягом 45 хв. при 50 °C. Після додавання реакційну суміш поступово охолоджують до температури навколишнього середовища протягом 90 хв., осаджені тверді речовини фільтрують і промивають 1:1 ізопрополом-гексаном. Тверду речовину сушать у печі при 45 °C протягом ночі з повітровідводом, з одержанням вказаної в заголовку сполуки (17,2 г, 49,5 ммоль, 77 %) у вигляді кристалічної твердої речовини. Тверда речовина має не обумовлений незначний ізомер за аналітичною хіральною ВЕРХ (Chiralcel OJ 4,6Ч25 мм, 20 % ізопропанол/гексан, 0,5 мл/хв) і маткова рідина показала ~50 % оі на користь бажаного ізомеру. 1 H ЯМР (300 МГц, ДМСО-d6) 57,44-7,37 (м, 3H), 7,30-7,17 (м, 3H), 7,01 (тд, J=8,5, 3,1 Гц, 1H), 6,78-6,73 (м, 1H), 4,70 (с, 1H), 4,21 (дд, J=11,5, 6,3 Гц, 1H), 2,13 (дд, J=13,2, 6,3 Гц, 1H), 1,65 (т, + J=12,3 Гц, 1H), 1,37 (с, 3H), 1,17 (с, 3H); МС (DCl/NH 3) m/z 179 (M-16) . Приклад 1E: 2-Бром-6-фторбензальдегід 1-Бром-3-фторбензол (17,3 г, 100 ммоль) додають протягом 5 хв. до розчину діізопропіламіду літію (одержують додаванням 40 мл 2,5 N-бутиллітію в гексані до 11,5 г 0,1M діізопропіламіну при 0 °C) у ТГФ при -70 °C. Суміш перемішують холодною протягом 1 год., потім додають ДМФ (8 мл) протягом 10 хв. Суміш перемішують при -70 °C протягом ще 40 хв., потім обробляють оцтовою кислотою (26 г). Суміш нагрівають до температури навколишнього середовища, переносять у суміш МТБЕ (200 мл), води (200 мл) і 4N хлористоводневої кислоти (150 мл). Шари розділяють, і органічну частину концентрують при зниженому тиску з + одержанням вказаної в заголовку сполуки. МС (DCl/NH3) m/z 202 (M+H) . 15 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 1F: 4-Бром-1-метил-1H-індазол Розчин Прикладу 1E (2,00 г, 9,95 ммоль) у ДМСО (3,5 мл) додають до метилгідразину (98 %, 3,20 г 98 % реагенту, 69,6 ммоль). Суміш нагрівають при 85 °C протягом 24 год., потім охолоджують до температури навколишнього середовища й розбавляють водою (50 мл). Розчин екстрагують CH2Cl2 (2Ч50 мл), і об'єднані органічні шари сушать (MgSO4), фільтрують і концентрують при зниженому тиску з одержанням вказаної в заголовку сполуки, яку + застосовують без подальшого очищення. МС (DCl/NH3) m/z 202 (M+H) . Приклад 1G: 1-Метил-1Н-індазол-3-амін Суміш ацетату паладію(II) (82 мг, 2 % моль) і Xantphos (287 мг, 3 % моль) у толуолі (10 мл) перемішують протягом 5 хв. при температурі навколишнього середовища. До розчину додають розчин Прикладу 1F (3,68 г, 17,4 ммоль) і бензофеноніміну (3,00 г, 17,4 ммоль) у толуолі (30 мл). Суміш видаляють і продувають азотом два рази, потім перемішують при температурі навколишнього середовища протягом 15 хв. Додають треобутоксид натрію (1,90 г, 24,4 ммоль), і суміш видаляють і продувають азотом. Суміш нагрівають до температури від близько 80 до 85 °C протягом 2 год., охолоджують до температури навколишнього середовища й розбавляють водою (30 мл). Шари розділяють, і водний шар екстрагують додатковим толуолом (20 мл). Об'єднані органічні шари перемішують із 6N HСl (10 мл) протягом 1 год., потім додають 40 мл води для розчинення твердих речовин. Шар толуолу викидають, і водний шар фільтрують для видалення нерозчинного матеріалу. Водний шар доводять до pН 14 з додаванням 50 % NaOH, і отриману тверду речовину фільтрують і сушать із одержанням вказаної в заголовку сполуки. + МС (DCl/NH3) m/z 202 (M+H) . Приклад 1H: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1Hіндазол-4-іл)сечовина В 100 мл круглодонну колбу додають N, N'-дисукцинілкарбонат (1,38 г, 5,38 ммоль), піридин (0,435 мл, 5,38 ммоль) і Приклад 1G (0,754 г, 5,12 ммоль) в ацетонітрилі (15 мл). Коричневий розчин перемішують при кімнатній температурі протягом 30 хв. і обробляють розчином Прикладу 1D (1,00 г, 5,12 ммоль) в ацетонітрилі (10 мл) з наступним додаванням N, Nдіізопропілетиламіну (2,66 мл, 15,4 ммоль). Реакційну суміш перемішують протягом 1 год., потім виливають в EtOAc (200 мл) і промивають насиченим NaHCO 3 (50 мл) і 1N HСl (50 мл). Розчин сушать (Na2SO4), фільтрують і концентрують. Одержаний залишок очищають хроматографією на силікагелі (градієнтне елюювання, 0-50 % EtOAc/гексан) з одержанням вказаної в заголовку 1 сполуки (1,54 г, 4,18 ммоль, 82 %) у вигляді білуватої твердої речовини. H ЯМР (300 МГц, ДМСО-d6) д 8,76 (с, 1H), 8,05 (д, J=0,9 Гц, 1H), 7,70 (дд, J=7,5, 0,7 Гц, 1H), 7,27 (д, J=7,7 Гц, 1H), 7,18 (дт, J=8,3, 0,8 Гц, 1H), 7,09 (ддд, J=9,4, 3,1, 0,9 Гц, 1H), 7,05-6,97 (м, 1H), 6,78 (дд, J=8,8, 4,8 Гц, 2H), 5,03-4,94 (м, 1H), 4,01 (с, 3H), 2,29-2,16 (м, 1H), 1,77 (дд, J=13,2, 10,9 Гц, 1H), 1,40 (с, + 3H), 1,29 (с, 3H); МС (DCl/NH3) m/z 369 (M+H) . Приклад 2: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4ілсечовина Приклад 2A: 4-Нітро-1H-індазол 3-нітроанілін (20,0 г, 131 ммоль) в оцтовій кислоті (200 мл) обробляють NaNO 2 (20,0 г, 289 ммоль) у воді (50 мл) при 4 °C (механічне перемішування). Реакційну суміш нагрівають при температурі навколишнього середовища й перемішують протягом 16 год. Розчинник видаляють при зниженому тиску, і залишок обробляють водою (700 мл) і фільтрують. Відфільтровану тверду речовину сушать при 45 °C у вакуумній печі протягом 10 год. з одержанням вказаної в заголовку сполуки, яку застосовують без подальшого очищення. Альтернативно, в 4-горлу 5-л круглодонну колбу з подвійними стінками, оснащену механічною мішалкою й термопарою, завантажують 3-нітроанілін (100 г, 658 ммоль) і оцтову кислоту (2000 мл). Розчин охолоджують до 14 °C і обробляють охолодженим (-1 °C; баня лідвода) розчином NaNO2 (100 г, 1450 ммоль) у воді (250 мл), доданим однією порцією. Внутрішню температуру підвищують від 14 °C до 28 °C протягом 5 хв. і суміш залишають при цій температурі протягом 5 хв., потім поступово охолоджують до 15 °C. Суміш перемішують протягом 24 год., потім концентрують при зниженому тиску до приблизного об'єму 500 мл. Залишок повторно суспендують у воді (1800 мл) при температурі навколишнього середовища протягом 21 год. Отриману оранжеву тверду речовину фільтрують, промивають водою (3Ч250 мл) і сушать у вакуумній печі при 70 °C з одержанням 97,0 г вказаної в заголовку сполуки у вигляді яскраво-оранжевої твердої речовини, яку застосовують без подальшого очищення. Приклад 2B: Метил 4-нітро-1H-індазол-1-карбоксилат NaН (300 мг, 12,5 ммоль) в N, N-диметилформаміді (5 мл) обробляють Прикладом 2A (1,33 г, 10,0 ммоль) при 0 °C. Реакційну суміш нагрівають до температури навколишнього середовища й перемішують протягом 1 год. Потім суміш обробляють метилхлорформіатом 16 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 (0,90 мл) і перемішують при кімнатній температурі протягом 3 год. Реакційну суміш гасять водою й фільтрують із одержанням вказаної в заголовку сполуки у вигляді білуватої твердої речовини. Альтернативно, в 3-горлу 2-л круглодонну колбу з подвійними стінками, обладнану механічною мішалкою, термопарою й краплинною лійкою, завантажують Приклад 2A (95,2 г, 716 ммоль) і N, N-диметилформамід (650 мл). Темний розчин охолоджують до 10 °C і додають ДБУ (96,0 г, 788 ммоль) через краплинну лійку так, щоб внутрішня температура не перевищувала 15 °C. Після охолодження суміші до 10 °C додають метилхлорформіат (108 г, 1430 ммоль) через краплинну лійку так, щоб внутрішня температура не перевищувала 25 °C. Через 1 год. перемішування при 10 °C додають водний 10 % фосфат калію дикислоти у воді (500 мл), і суміш перемішують протягом 15 год. Отриману коричневу тверду речовину фільтрують, і посудину з реакційною сумішшю промивають водним 10 % фосфатом калію дикислоти у воді (2Ч150 мл). Промивки додають до твердої речовини на фільтрі. Отриману тверду речовину промивають водним 10 % фосфатом калію дикислоти у воді (2Ч200 мл) і водою (2Ч200 мл), потім сушать у вакуумній печі при 70 °C з одержанням 122 г темно-коричневої твердої речовини. Тверду речовину повторно суспендують в ізопропілацетаті (2000 мл) протягом 2 год. Тверду речовину фільтрують, промивають свіжим ізопропілацетатом (2Ч250 мл) і сушать у вакуумній печі при 70 °C з одержанням вказаної в заголовку сполуки (110 г, 495 ммоль) у вигляді світло-коричневої + твердої речовини. МС (DCl/NH3) m/z 222 (M+H) . Приклад 2C: Метил 4-аміно-1H-індазол-1-карбоксилат Приклад 2B (1,66 г, 7,50 ммоль) і 10 % Pd/C поєднують в етанолі (20 мл) і обробляють газоподібним воднем (тиск 1 атм). Реакційну суміш нагрівають при 80 °C протягом 20 хв., охолоджують до температури навколишнього середовища й фільтрують через Целіт. Фільтрат випарюють із одержанням вказаної в заголовку сполуки (1,22 г, 6,35 ммоль). МС (DCl/NH3) m/z + 192 (M+H) . Приклад 2D: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4ілсечовина В 100 мл круглодонну колбу додають N, N'-дисукцинілкарбонат (1,38 г, 5,38 ммоль), піридин (0,435 мл, 5,38 ммоль) і Приклад 2C (983 мг, 5,12 ммоль) в ацетонітрилі (15 мл). Коричневий розчин перемішують при кімнатній температурі протягом 30 хв. і обробляють розчином Прикладу 1D (1,00 г, 5,12 ммоль) в ацетонітрилі (10 мл) з наступним додаванням N, Nдіізопропілетиламіну (2,66 мл, 15,4 ммоль). Реакційну суміш перемішують протягом 1 год., потім виливають в етилацетат (200 мл) і промивають насиченим Na-НСО3 (50 мл) і 1N HСl (50 мл). Розчин сушать (Na2SO4), фільтрують і концентрують. Одержаний залишок розчиняють у тетрагідрофурані (15 мл) і МеОН (15 мл) з одержанням жовтого розчину. До розчину додають 5N NaOH (4,8 мл), і реакційну суміш перемішують при температурі навколишнього середовища протягом 2 год. Реакційну суміш виливають в EtOAc (200 мл) і промивають насиченим бікарбонатом натрію (50 мл). Органічну частину сушать (Na2SO4), фільтрують і концентрують. Очищають хроматографією на силікагелі (градієнтне елюювання 0-10 % МеОН/CH2Cl2) з одержанням вказаної в заголовку сполуки (1,10 г, 3,11 1 ммоль, 83 %) у вигляді білої аморфної твердої речовини. H ЯМР (300 МГц, ДМСО-d6) д 13,0613,04 (шир.с, 1H), 8,76 (с, 1H), 8,08 (т, J=1,1 Гц, 1H), 7,68 (д, J=7,2 Гц, 1H), 7,23 (д, J=7,76 Гц, 1H), 7,11-6,98 (м, 3H), 6,81-6,76 (м, 2H), 5,04-4,94 (м, 1H), 2,19 (дд, J=13,2, 6,2 Гц, 1H), 1,77 (дд, + 23 J=13,2, 10,9 Гц, 1H), 1,40 (с, 3H), 1,29 (с, 3H). МС (DCl/NH 3) m/z 355 (M+H) ; [б] D=+39,2 (c 1,0, МеОН). Приклад 3 N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Приклад 3A: 8-Аміно-1,2,3,4-тетрагідронафталін-2-ол Етанол (1 л) додають до 2-нафтолу (100 г, 610 ммоль), нікелю Ренея (40 г, зволожений водою) і гідроксиду натрію (4,00 г, 8 % моль водний) у реакторі з перемішуванням. Ректор герметично закривають і продувають воднем. Реакційну суміш перемішують протягом 13 год. при 85 °C, і потім ще 8 год. при 100 °C. Потім суміш фільтрують через шар Целіту. Одержаний розчин обробляють Darco G-60 (35 г) і нагрівають до кипіння зі зворотним холодильником протягом 1 год., потім охолоджують до температури навколишнього середовища й перемішують ще 3 год. Цю суміш фільтрують через Целіт (350 г), і шар промивають EtOAc (1,5 л). Розчинник видаляють у вакуумі й додають метил трет-бутиловий ефір (1 л). Суміш нагрівають протягом 15 хв. при 50 °C, перемішують протягом 1 год. при температурі навколишнього середовища й розчинник видаляють у вакуумі. Приблизно половину отриманої неочищеної твердої речовини очищають хроматографією на силікагелі (градієнтне елюювання, 2-30 % МеОН/CH2Cl2) з 1 одержанням 37 г вказаної в заголовку сполуки у вигляді світло-коричневої твердої речовини. H 17 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 ЯМР (300 МГц, CdСl3) д 6,96 (т, J=7,6 Гц, 1H), 6,55 (дд, J=10,7, 7,6 Гц, 2H), 4,44-4,24 (м, 1H), 2,95-2,80 (м, 3H), 2,38 (дд, J=16,1, 7,6 Гц, 1H), 2,09-1,96 (м, 1H), 1,85-1,70 (м, 1H). Приклад 3B: (2S)-8-Аміно-1,2,3,4-тетрагідронафталін-2-ол Приклад 3A розчиняють в ізопропанолі, завантажують в Chiralpak IC колонку для хіральної ВЕРХ (30 см ВД 250 см) і елююють 32 % ізопропанолом/гексаном при 25 °C зі швидкістю потоку 20 мл/хв. Найраніший пік елюювання (час утримання=16 хв.) збирають, і розчинник випарюють із одержанням вказаної в заголовку сполуки у вигляді білуватої твердої речовини з + + 99,2 % оі. МС (DCl/NH3) m/z 164 (M+H) , 181 (M+NH4) . Приклад 3C: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина До суспензії ди(N-сукцинімідил)карбонату (703 мг, 2,75 ммоль) в ацетонітрилі (5 мл) додають Приклад 3B (427 мг, 2,62 ммоль), розчинений в ацетонітрилі (10 мл) і піридин (0,222 мл, 2,75 ммоль). Реакційну суміш перемішують протягом 20 хв., одночасно додаючи Приклад 1C (510,6 мг, 2,62 ммоль) в ацетонітрилі (10 мл) і N, N-діізопропілетиламін (1,37 мл, 7,85 ммоль). Реакційну суміш перемішують протягом 16 год. при температурі навколишнього середовища. Додають EtOAc (200 мл), і реакційну суміш промивають водою (2Ч200 мл) і насиченим розчином солі (200 мл) і розділяють. Органічну частину сушать (Na 2SO4) і фільтрують. Розчинник випарюють при зниженому тиску й з розчину осаджують тверду речовину. Тверду речовину збирають, розтирають із діетиловим ефіром і фільтрують. Тверду речовину промивають діетиловим ефіром, потім гексаном, і сушать на повітрі з одержанням вказаної в заголовку сполуки (737 мг, 1,92 ммоль, 73 % вихід) у вигляді бежевої твердої 1 речовини. H ЯМР (300 МГц, ДМСО-d6) д 7,70 (д, J=7,9 Гц, 1H), 7,60 (с, 1H), 7,08-6,94 (м, 4H), 6,81-6,71 (м, 2H), 4,93 (дд, J=18,0, 7,2 Гц 1H), 4,86 (д, J=4,2 Гц, 1H), 3,98-3,87 (м, 1H), 2,91-2,63 (м, 3H), 2,37 (дд, J=16,5, 7,7 Гц, 1H), 2,15 (дд, J=13,2, 6,2 Гц, 1H), 1,93-1,83 (м, 1H), 1,69 (дд, + J=13,0, 11,1 Гц, 1H), 1,63-1,52 (м, 1H), 1,39 (с, 3H), 1,26 (с, 3H); МС (ІЕР) m/z 385 (M+H) ; 23 [б] D=+38,0° (c 1,0, CH3OH). Приклад 4: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Приклад 4A: ((2R))-8-Аміно-1,2,3,4-тетрагідронафталін-2-ол Приклад 3A розчиняють в ізопропанолі, завантажують до Chiralpak IC колонку для хіральної ВЕРХ (30 см ВД 250 см) і елююють 32 % ізопропанолом/гексаном при 25 °C зі швидкістю потоку 20 мл/хв. Самий останній елюйований пік (час утримання=19 хв.) збирають, і розчинник випарюють із одержанням вказаної в заголовку сполуки у вигляді білуватої твердої речовини з + + 99,6 % оі. МС (DCl/NH3) m/z 164 (M+H) , 181 (M+NH4) . Приклад 4B: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B. H ЯМР (300 МГц, ДМСО-d6) д 7,69 (д, J=7,9 Гц, 1H), 7,61 (с, 1H), 7,08-6,94 (м, 4H), 6,81-6,71 (м, 2H), 4,99-4,88 (м, 1H), 4,86 (д, J=4,1 Гц, 1H), 4,00-3,88 (м, 1H), 2,90-2,64 (м, 3H), 2,35 (дд, J=16,5, 7,7 Гц, 1H), 2,15 (дд, J=13,2, 6,2 Гц, 1H), 1,93-1,81 (м, 1H), 1,69 (дд, J=13,0, 11,1 + 23 Гц, 1H), 1,64-1,51 (м, 1H), 1,39 (с, 3H), 1,27 (с, 3H); МС (DCl/NH 3) m/z 385 (M+H) ; [б] D=+34,6° (c 1,0, CH3OH). Приклад 5: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина В 5000мл круглодонну колбу додають карбонат N, N'-дисукцинімідилу (1,38 г, 5,38 ммоль), піридин (0,435 мл, 5,38 ммоль) і ізохінолін-5-амін (0,738 г, 5,12 ммоль, Acros) в ацетонітрилі (15 мл) з одержанням коричневого розчину. Реакційну суміш перемішують при температурі навколишнього середовища протягом 30 хв. До цієї суміші додають Приклад 1C (1,00 г, 5,12 ммоль) в ацетонітрилі (10 мл) і N, N-діізопропілетиламін (2,66 мл, 154 ммоль). Реакційну суміш перемішують протягом 90 хв., потім концентрують. Суміш розбавляють EtOAc (300 мл) і промивають насиченим NaHCO3 (100 мл), сушать (Na2SO4), фільтрують і концентрують. Залишок очищають хроматографією на силікагелі (градієнтне елюювання, 0-10 % МеОН/CH2Cl2) з одержанням вказаної в заголовку сполуки (1,12 г, 3,07 ммоль, 60 %) у вигляді білої твердої 1 речовини. H ЯМР (300 МГц, ДМСОd6) д 9,29 (д, J=0,8 Гц, 1H), 8,76 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,34 (дд, J=7,7, 1,1 Гц, 1H), 7,94 (д, J=6,1 Гц, 1H), 7,77 (д, J=8,1 Гц, 1H), 7,64 (т, J=7,9 Гц, 1H), 7,12 (ддд, J=9,4, 3,2, 0,9 Гц, 1H), 7,06-6,98 (м, 2H), 6,79 (дд, J=8,9, 4,9 Гц, 1H), 5,05-4,95 (м, 1H), 2,21 (дд, J=13,2, 6,2 Гц, 1H), 1,78 (дд, J=13,2, 10,9 Гц, 1H), 1,41 (с, 3H), 1,29 (с, 3H); МС (DCl/NH 3) + 23 m/z 366 (M+H) ; [б] D=+32,6 (c 0,65, CH3OH). Приклад 6: N-[(4R)-6-Фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовина 18 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 6A: 6-Фторспіро[хроман-2,1'-циклобутан]-4-он Вказану в заголовку сполуку одержують за методикою Прикладу 1A, із застосуванням 1-(5фтор-2-гідроксифеніл)етанону й заміняючи циклобутаноном пропан-2-он. МС (DCl/NH3) m/z 207 + (M+H) . Приклад 6B: O-метилоксим (E)-6-Фторспіро[хроман-2,1'-циклобутан]-4-ону В 5000мл круглодонну колбу додають Приклад 6A (19,4 г, 94,9 ммоль) і гідрохлорид Oметилгідроксиламіну (8,53 мл, 112 ммоль) у піридині (150 мл) з одержанням жовтого розчину. Реакційну суміш перемішують протягом 54 год. при температурі навколишнього середовища, концентрують, розбавляють EtOAc (1 л) і промивають водою (400 мл). Органічну частину сушать (Na2SO4), фільтрують і концентрують. Одержаний жовтий залишок очищають хроматографією на силікагелі (градієнтне елюювання, 0-30 % EtOAc/гексан) з одержанням вказаної в заголовку сполуки (21,8 г, 94,0 ммоль, 99 %) у вигляді блідо-жовтої твердої речовини. + МС (DCl/NH3) m/z 224 (M+NH4) . Приклад 6C: 6-Фторспіро[хроман-2,1'-циклобутан]-4-амін Приклад 6B (21,8 г, 94,0 ммоль) і нікель Ренея (5,49 г, зволожений водою) перемішують в EtoН, що містить 7M аміак (150 мл). Реактор герметично закривають і продувають воднем. Реакційну суміш перемішують протягом 3 год. при 32 °C, прохолоджують, розбавляють EtOAc (250 мл) і фільтрують через шар Целіту (50 г). Одержаний розчин фільтрують через шар силікагелю (50 г) і фільтрат випарюють із одержанням вказаної в заголовку сполуки (10,8 г, 52,1 + ммоль, 56 %) у вигляді блідого масла. МС (DCl/NH3) m/z 208 (M+H) . Приклад 6D: (R)-6-Фторспіро[хроман-2,1'-циклобутан]-4-амін Приклад 6C розділяють напівпрепаративною хіральною ВЕРХ (Chiralcel OD 5Ч50 см, 5 % ізопропанол/гексан+ 0,1 % діетиламін, 23 °C, 100 мл/хв). Останній їз двох піків елюювання (час утримання=26,0 хв.) збирають, і розчинник випарюють із одержанням вказаної в заголовку сполуки у вигляді білуватої твердої речовини з 99 % оі до рацемічного посилання (отриманого, як описано вище, із застосуванням боргідриду натрію як відновлювального агента). МС + (DCl/NH3) m/z 208 (M+H) . Приклад 6E: сіль фенілоцтової кислоті (R)-6-фторспіро[хроман-2,1'-циклобутан]-4-аміну Вказану в заголовку сполуку одержують за методикою Прикладу 1D, заміняючи Прикладом + 6D Приклад 1C. МС (DCl/NH3) m/z 208 (M+H) . Приклад 6F: N-[(4R)-6-Фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'[(7R)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 6E Приклад 1D, і заміняючи Прикладом 4A Приклад 3B. H ЯМР (300 МГц, ДМСОd6) д 7,70 (д, J=7,8 Гц, 1H), 7,62 (с, 1H), 7,06-6,96 (м, 4H), 6,81 (дд, J=9,6, 4,9 Гц, 1H), 6,74 (д, J=7,4 Гц, 1H), 4,93 (дд, J=14,8, 9,1 Гц 1H), 4,86 (д, J=4,1 Гц, 1H), 3,99-3,88 (м, 1H), 2,91-2,64 (м, 3H), 2,42-2,03 + 23 (м, 6H), 1,93-1,67 (м, 4H), 1,67-1,52 (м, 1H); МС (ІЕР) m/z 397 (M+H) ; [б] D=+62,8° (c 1,0, CH3OH) Приклад 7: N-[(4R)-6-Фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-(1метил-1H-індазол-4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 6E Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,79 (с, 1H), 8,05 (д, J=0,9 Гц, 1H), 7,72 (дд, J=7,5, 0,7 Гц, 1H), 7,28 (д, J=7,7 Гц, 1H), 7,20-7,16 (м, 1H), 7,09-6,99 (м, 2H), 6,83 (дд, J=8,7, 4,7 Гц, 2H), 5,03-4,94 (м, 1H), 4,01 (с, 3H), 2,51-2,38 (м, 1H), 2,36-2,04 (м, 4H), 2,00-1,68 (м, 3H); МС (DCl/NH3) + D m/z 381 (M+H) ; [б] 23=+34,45 (c 0,50, CH3OH). Приклад 8: N-[(4R)-6-Фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'-1Hіндазол-4-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 2D, заміняючи Прикладом 1 6E Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 13,03-13,01 (шир.с, 1H), 8,75 (с, 1H), 8,08 (с, 1H), 7,68 (д, J=7,2 Гц, 1H), 7,22 (д, J=7,8 Гц, 1H), 7,11-6,94 (м, 3H), 6,86-6,81 (м, 2H), 5,03-4,94 (м, 1H), + D 2,45-2,06 (м, 5H), 1,95-1,69 (м, 3H); МС (DCl/NH3) m/z 367 (M+H) ; [б] 23=+24,1 (c 0,70, CH3OH). Приклад 9: N-[(4R)-6-Фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 6E Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,71 (д, J=7,3 Гц, 1H), 7,61 (с, 1H), 7,07-6,95 (м, 4H), 6,86-6,77 (м, 1H), 6,74 (д, J=7,4 Гц, 1H), 4,92 (дд, J=14,5, 9,2 Гц, 1H), 4,85 (д, J=4,3 Гц, 1H), 3,99-3,87 (м, 1H), 2,91-2,64 (м, 3H), 2,42-2,03 (м, 6H), 1,93-1,67 (м, 4H), 1,67-1,52 (м, 1H); МС + 23 (ІЕР) m/z 397 (M+H) ; [б] D=+68,4° (c 1,0, CH3OH). Приклад 10: N-[(4S)-6-Фтор-3,3',4,4'-тетрагідро-2'H-спіро[хромен-2,1'-циклобутан]-4-іл]-N'[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовина Приклад 10A: (S)-6-Фторспіро[хроман-2,1'-циклобутан]-4-амін 19 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 6C розділяють напівпрепаративною хіральною ВЕРХ (Chiralcel OD 5Ч50 см, 5 % ізопропанол/гексан+ 0,1 % діетиламін, 23 °C, 100 мл/хв). Самий ранній із двох піків (час утримання=20,9 хв.) збирають, і розчинник випарюють із одержанням вказаної в заголовку сполуки у вигляді білуватої твердої речовини з 99 % оі до рацемічного посилання (одержують, як описано вище, із застосуванням боргідриду натрію як відновлювального агента). МС + (DCl/NH3) m/z 208 (M+H) . Приклад 10B: N-[(4S)-6-Фтор-3,3',4,4'-тетрагідро-2З-спіро[хромен-2,1'-циклобутан]-4-іл]-N'[(7S)-7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 10A Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,71 (д, J=7,4 Гц, 1H), 7,62 (с, 1H), 7,07-6,96 (м, 4H), 6,81 (дд, J=9,6, 4,8 Гц, 1H), 6,74 (д, J=7,0 Гц, 1H), 4,98-4,89 (м, 1H), 4,87 (д, J=4,1 Гц, 1H), 3,99-3,89 (м, 1H), 2,90-2,64 (м, 3H), 2,41-2,02 (м, 6H), 1,92-1,67 (м, 4H), 1,66-1,51 (м, 1H); МС + 23 (ІЕР) m/z 397 (M+H) ; [] D=-59,5° (c 1,0, CH3OH). Приклад 11: N-[(4S)-6-Фтор-3,3',4,4'-тетрагідро-2З-спіро[хромен-2T-циклобутан]-4-іл]-N'-[(7R)7-гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 10A Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,71 (д, J=7,4 Гц, 1H), 7,61 (с, 1H), 7,06-6,95 (м, 4H), 6,85-6,77 (м, 1H), 6,74 (д, J=7,5 Гц, 1H), 4,92 (дд, J=15,0, 9,1 Гц, 1H), 4,85 (д, J=5,3 Гц, 1H), 3,99-3,87 (м, 1H), 2,90-2,64 (м, 3H), 2,43-2,03 (м, 6H), + 23 1,92-1,66 (м, 4H), 1,66-1,52 (м, 1H); МС (ІЕР) m/z 397 (M+H) ; [б] D=-63,0° (c 1,0, CH3OH). Приклад 12: N-[(4R)-6-Фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина Приклад 12A: 6-Фторхроман-4-он Вказану в заголовку сполуку одержують за методикою Прикладу 1A, заміняючи + параформальдегідом пропан-2-он. МС (DCl/NH3) m/z 183 (M+NH4) . Приклад 12B: (R)-6-Фторхроман-4-амін, сіль (R)-2-гідрокси-2-фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 12A за методиками, описаними у + + Прикладі 1B, Прикладі 1C і Прикладі 1D. МС (DCl/NH3 ) m/z 168 (M+H) . Приклад 12C: N-[(4R)-6-Фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина Вказану в заголовку сполуку одержують за методикою Приклад 1H, заміняючи Прикладом 1 12B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,63 (с, 1H), 8,00 (д, J=0,9 Гц, 1H), 7,70 (д, J=7,5 Гц, 1H), 7,43-7,25 (м, 2H), 7,18-6,79 (м, 5H), 5,01-4,88 (м, 1H), 4,20-4,00 (м, 4H), 2,20-1,84 (м, 2H); + 23 МС (DCl/NH3) m/z 341 (M+H) ; [] D=+37 (c 0,15, МеОН). Приклад 13: N-[(4R)-6-Фтор-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 12B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,28 (с, 1H), 8,62 (с, 1H), 8,54 (д, J=6,0 Гц, 1H), 8,36 (д, J=8,1 Гц, 1H), 7,90 (д, J=6,1 Гц, 1H), 7,76 (д, J=8,1 Гц, 1H), 7,63 (т, J=7,9 Гц, 1H), 7,246,99 (м, 3H), 6,85 (дд, J=9,0, 4,9 Гц, 1H), 4,97-4,90 (м, 1H), 4,33-4,23 (м, 1H), 4,18 (ддд, J=11,3, + 23 8,3, 3,0 Гц, 1H), 2,28-1,96 (м, 2H); МС (DCl/NH3) m/z 338 (M+H) ; [б] D=+29,0 (c 0,25 CH3OH). Приклад 14: N-[(4R)-6-Фтор-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 12B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,73 (д, J=8,0 Гц, 1H), 7,49 (с, 1H), 7,13 (д, J=7,7 Гц, 1H), 7,10-6,96 (м, 3H), 6,82 (дд, J=8,9, 4,9 Гц, 1H), 6,72 (д, J=7,3 Гц, 1H), 4,89-4,82 (м, 2H), 4,26 (ддд, J=10,1, 6,8, 3,2 Гц, 1H), 4,13 (ддд, J=11,2, 8,4, 2,9 Гц, 1H), 3,98-3,87 (м, 1H), 2,88-2,62 (м, 3H), 2,31 (дд, J=16,8, 8,0 Гц, 1H), 2,18-2,04 (м, 1H), + 23 2,01-1,81 (м, 2H), 1,66-1,50 (м, 1H); МС (ІЕР) m/z 357 (M+H) ; [б] D=+66,1° (c 1,0, 1:1 ДМСО:CH3OH). Приклад 15: N-[(4R)-6-Фтор-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Приклад 3C, заміняючи Прикладом 1 12B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,74 (д, J=8,0 Гц, 1H), 7,49 (с, 1H), 7,13 (д, J=7,7 Гц, 1H), 7,10-6,96 (м, 3H), 6,82 (дд, J=8,9, 4,9 Гц, 1H), 6,72 (д, J=7,5 Гц, 1H), 4,90-4,81 (м, 2H), 4,26 (ддд, J=10,2, 6,6, 3,1 Гц, 1H), 4,13 (ддд, J=11,3, 8,4, 2,9 Гц, 1H), 3,98-3,85 (м, 1H), 2,90-2,62 (м, 3H), 2,32 (дд, J=16,5, 7,7 Гц, 1H), 2,17-2,03 (м, 1H), 2,01-1,81 (м, 2H), 1,67-1,50 (м, 1H); МС + 23 (ІЕР) m/z 357 (M+H) ; [б] D=+62,0° (c 1,0, 1:1 ДМСО:CH3OH). Приклад 16: N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1Hіндазол-4-іл)сечовина Приклад 16A: 6,8-дифтор-2,2-диметилхроман-4-он 20 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 Вказану в заголовку сполуку одержують за методикою Приклад 1A, заміняючи 1-(3,5дифтор-2-гідроксифеніл)етаноном 1-(5-фтор-2-гідроксифеніл)етанон. МС (DCl/NH 3) m/z 230 + (M+NH4) . Приклад 16B: (R)-6,8-дифтор-2,2-диметилхроман-4-амін, сіль (R)-2-гідрокси-2-фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 16A за методиками, описаними у + Прикладі 1B, Прикладі 1C і Прикладі 1D. МС (DCl/NH3) m/z 214 (M+H) . Приклад 16C: N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1Hіндазол-4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Приклад 1H, заміняючи Прикладом 1 16B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,80 (с, 1H), 8,05 (д, J=0,9 Гц, 1H), 7,69 (дд, J=7,5, 0,8 Гц, 1H), 7,32-7,15 (м, 3H), 6,99-6,94 (м, 1H), 6,80 (д, J=8,3 Гц, 1H), 5,06-4,96 (м, 1H), 4,01 (с, 3H), 2,23 (дд, J=13,3, 6,2 Гц, 1H), 2,00-1,81 (м, 1H), 1,45 (с, 3H), 1,32 (с, 3H); МС (DCl/NH3) + 23 m/z 387 (M+H) ; [] D=+19,3 (c 0,73, МеОН). Приклад 17: N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 16B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,29 (д, J=0,8 Гц, 1H), 8,77 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,35 (дд, J=7,7, 1,1 Гц, 1H), 7,93 (д, J=6,1 Гц, 1H), 7,77 (д, J=8,1 Гц, 1H), 7,64 (т, J=7,9 Гц, 1H), 7,18-7,07 (м, 2H), 7,04 (д, J=8,4 Гц, 1H), 6,89 (тд, J=7,9, 5,0 Гц, 1H), 5,10-5,01 (м, 1H), 2,24 + (дд, J=13,3, 6,2 Гц, 1H), 2,00-1,81 (м, 1H), 1,46 (с, 3H), 1,33 (с, 3H), МС (DCl/NH 3) m/z 366 (M+H) ; 23 [] D=+26,7 (c 0,70, CH3OH). Приклад 18: N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 16B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,717,61 (м, 2H), 7,17 (ддд, J=11,5, 8,8, 3,0 Гц, 1H), 7,06-6,97 (м, 2H), 6,91 (д, J=9,3 Гц, 1H), 6,75 (д, J=7,2 Гц, 1H), 5,02-4,89 (м, 1H), 4,86 (д, J=4,1 Гц, 1H), 4,00-3,87 (м, 1H), 2,90-2,64 (м, 3H), 2,35 (дд, J=16,5, 7,7 Гц, 1H), 2,19 (дд, J=13,3, 6,2 Гц, 1H), 1,93-1,82 (м, 1H), 1,77 (дд, J=13,2, 11,2 Гц, + 23 1H), 1,68-1,51 (м, 1H), 1,43 (с, 3H), 1,30 (с, 3H); МС (ІЕР) m/z 403 (M+H) ; [] D=+39,4° (c 1,0, CH3OH). Приклад 19: N-[(4R)-6,8-дифтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Приклад 3C, заміняючи Прикладом 1 16B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,72-7,62 (м, 2H), 7,17 (ддд, J=11,4, 8,7, 3,0 Гц, 1H), 7,06-6,97 (м, 2H), 6,91 (д, J=9,3 Гц, 1H), 6,75 (д, J=7,4 Гц, 1H), 5,02-4,88 (м, 1H), 4,86 (д, J=4,1 Гц, 1H), 3,98-3,86 (м, 1H), 2,91-2,61 (м, 3H), 2,37 (дд, J=16,5, 7,8 Гц, 1H), 2,19 (дд, J=13,3, 6,2 Гц, 1H), 1,93-1,82 (м, 1H), 1,77 (дд, J=13,2, 11,3 Гц, 1H), 1,67-1,52 (м, 1H), 1,43 (с, 3H), 1,30 (с, + 23 3H); МС (ІЕР) m/z 403 (M+H) ; [] D=+42,8° (c 1,0, CH3OH). Приклад 20: N-[(4R)-8-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Приклад 20A: 8-Фтор-2,2-диметилхроман-4-он Вказану в заголовку сполуку одержують за методикою Прикладу 1A, заміняючи 1-(3-фтор-2гідроксифеніл)етаноном 1-(5-фтор-2-гідроксифеніл)етанон і застосовуючи пропан-2-он. МС + (DCl/NH3) m/z 212 (M+NH4) . Приклад 20B: (R)-8-Фтор-2,2-диметилхроман-4-амін, соль (R)-2-гідрокси-2-фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 20A за методиками, описаними у + Прикладі 1B, Прикладі 1C і Прикладі 1D. МС (DCl/NH3) m/z 196 (M+H) . Приклад 20C: N-[(4R)-8-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 20B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,70 (д, J=7,4 Гц, 1H), 7,60 (с, 1H), 7,14-6,94 (м, 4H), 6,87 (тд, J=8,0, 5,0 Гц, 1H), 6,74 (д, J=7,1 Гц, 1H), 5,04-4,92 (м, 1H), 4,86 (д, J=4,2 Гц, 1H), 3,99-3,86 (м, 1H), 2,90-2,63 (м, 3H), 2,36 (дд, J=16,6, 7,8 Гц, 1H), 2,18 (дд, J=13,3, 6,2 Гц, 1H), 1,93-1,82 (м, 1H), 1,76 (дд, J=13,3, 10,9 Гц, 1H), 1,67-1,51 (м, + 23 1H), 1,44 (с, 3H), 1,31 (с, 3H); МС (ІЕР) m/z 385 (M+H) ; [б] D=+35,8° (c 1,0, CH3OH). Приклад 21: N-[(4R)-8-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина 21 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 20B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,69 (д, J=7,4 Гц, 1H), 7,60 (с, 1H), 7,14-6,94 (м, 2H), 6,87 (тд, J=8,0, 5,0 Гц, 1H), 6,74 (д, J=7,3 Гц, 1H), 5,04-4,92 (м, 1H), 4,86 (д, J=4,2 Гц, 1H), 3,99-3,87 (м, 1H), 2,89-2,64 (м, 3H), 2,34 (дд, J=16,5, 7,8 Гц, 1H), 2,19 (дд, J=13,4, 6,2 Гц, 1H), 1,93-1,82 (м, 2H), 1,76 (дд, J=13,3, 11,0 Гц, 1H), 1,61 (д, J=5,4 Гц, 1H), 1,44 (с, 3H), 1,31 (с, 3H); + 23 МС (ІЕР) m/z 385 (M+H) ; [б] D=+30,7° (c 1,0, CH3OH). Приклад 22: N-[(4R)-8-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 20B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,29 (д, J=0,9 Гц, 1H), 8,78 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,32 (дд, J=7,7, 1,1 Гц, 1H), 7,94 (д, J=6,1 Гц, 1H), 7,78 (д, J=8,1 Гц, 1H), 7,64 (т, J=7,9 Гц, 1H), 7,20 (ддд, J=11,3, 8,5, 2,9 Гц, 1H), 7,07-6,97 (м, 2H), 5,08-4,91 (м, 1H), 2,31-2,03 (м, 1H), 1,91+ 23 1,82 (м, 1H), 1,45 (с, 3H), 1,32 (с, 3H), МС (DCl/NH3) m/z 384 (M+H) ; [б] D=+32,5 (c 0,63, CH3OH). Приклад 23: N-[(4R)-7-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина Приклад 23A: 7-Фтор-2,2-диметилхроман-4-он Вказану в заголовку сполуку одержують за методикою Прикладу 1A, заміняючи 1-(4-фтор-2+ гідроксифеніл)етаноном 1-(5-фтор-2-гідроксифеніл)етанон. МС (DCl/NH3) m/z 212 (M+NH4) . Приклад 23B: (R)-7-Фтор-2,2-диметилхроман-4-амін, сіль (R)-2-гідрокси-2-фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 23A за методиками, описаними у + Прикладі 1B, Прикладі 1C і Прикладі 1D. МС (DCl/NH3) m/z 196 (M+H) . Приклад 23C: N-[(4R)-7-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 23B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,29 (с, 1H), 8,72 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,35 (д, J=7,7 Гц, 1H), 7,93 (д, J=6,1 Гц, 1H), 7,77 (д, J=8,1 Гц, 1H), 7,63 (т, J=7,9 Гц, 1H), 7,397,34 (м, 1H), 6,98 (д, J=8,3 Гц, 1H), 6,76 (тд, J=8,5, 2,7 Гц, 1H), 6,62 (дд, J=10,6, 2,6 Гц, 1H), 5,054,95 (м, 1H), 2,21 (дд, J=13,3, 6,1 Гц, 1H), 1,79 (дд, J=13,2, 10,7 Гц, 1H), 1,42 (с, 3H), 1,32 (м, 3H), + 23 МС (DCl/NH3) m/z 366 (M+H) ; [б] D=+28,5 (c 0,82, CH3OH). Приклад 24: N-[(4R)-7-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 23B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,74 (с, 1H), 8,04 (с, 1H), 7,71 (д, J=7,5 Гц, 1H), 7,37-7,25 (м, 2H), 7,17 (д, J=8,3 Гц, 1H), 6,76 (дд, J=8,6, 2,7 Гц, 1H), 6,72 (д, J=8,2 Гц, 1H), 6,61 (дд, J=10,6, 2,6 Гц, 1H), 5,03-4,93 (м, 1H), 4,01 (с, 3H), 2,20 (дд, J=13,3, 6,1 Гц, 1H), 2,00-1,73 (м, + 23 1H), 1,42 (с, 3H), 1,31 (с, 3H); МС (DCl/NH3) m/z 369 (M+H) ; [б] D=+11 (c 0,61, CH3OH). Приклад 25: N-[(4R)-8-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 20B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,76 (с, 1H), 8,04 (д, J=0,9 Гц, 1H), 7,70 (дд, J=7,5, 0,8 Гц, 1H), 7,27 (д, J=7,7 Гц, 1H), 7,19-7,06 (м, 3H), 6,88 (тд, J=7,9, 5,0 Гц, 1H), 6,76 (д, J=8,4 Гц, 1H), 5,09-4,99 (м, 1H), 4,01 (с, 3H), 2,22 (дд, J=13,3, 6,2 Гц, 1H), 1,84 (дд, J=13,3, 10,8 + 23 Гц, 1H), 1,45 (с, 3H), 1,33 (с, 3H); МС (DCl/NH3) m/z 369 (M+H) ; [б] D=+13 (c 0,67, CH3OH). Приклад 26: N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина Приклад 26A: 2,2-діетил-6-фторхроман-4-он 1-(5-Фтор-2-гідроксифеніл)етанон (30,2 г, 196 ммоль) і МеОН (300 мл) перемішують при температурі навколишнього середовища й додають 3-пентанон (41,6 мл, 392 ммоль) і піролідин (17,8 мл, 216 ммоль). Суміш нагрівають до 60 °C протягом 62 год., до цього моменту РХМС аналіз показує чітке перетворення продукту. Реакційну суміш прохолоджують, концентрують до мінімального обсягу МеОН, і додають МТБЕ (300 мл). Органічні речовини промивають 2N HСl (150 мл), насиченим розчином солі (60 мл), 2N NaOH (150 мл), і насиченим розчином солі (60 мл). Розчин пропускають через шар силікагелю (30 г), промиваючи МТБЕ (150 мл). Фільтрат концентрують із одержанням вказаної в заголовку сполуки (38,8 г, 175 ммоль, 89 %) у вигляді + світло-коричневого твердого масла. МС (DCl/NH3) m/z 240 (M+NH4) . Приклад 26B: (R)-6-Фтор-2,2-діетилхроман-4-амін, сіль (R)-2-гідрокси-2-фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 26A за методиками, описаними у + Прикладі 1B і Прикладі 1C. МС (DCl/NH3) m/z 224 (M+H) . 22 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 26C: N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 26B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,75 (с, 1H), 8,05 (с, 1H), 7,70 (д, J=7,5 Гц, 1H), 7,28 (т, J=7,9 Гц, 1H), 7,18 (д, J=8,3 Гц, 1H), 7,09 (дд, J=9,4, 3,2 Гц, 1H), 7,01 (тд, J=8,6, 3,2 Гц, 1H), 6,83-6,77 (м, 1H), 6,77 (д, J=8,2 Гц, 1H), 5,01-4,91 (м, 1H), 4,01 (с, 3H), 2,19 (дд, J=13,4, 6,1 + 23 Гц, 1H), 1,76-1,52 (м, 5H), 0,94-0,85 (м, 6H); МС (DCl/NH3) m/z 397 (M+H) ; [б] D=+9,2 (c 0,61, CH3OH). Приклад 27: N-[(4R)-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина Приклад 27A: 2,2-диметилхроман-4-он Вказану в заголовку сполуку одержують за методикою Прикладу 1A, заміняючи 1-(2гідроксифеніл)етаноном 1-(5-фтор-2-гідроксифеніл)етанон і застосовуючи пропан-2-он. МС + (DCl/NH3) m/z 194 (M+NH4) . Приклад 27B: (R)-2,2-диметилхроман-4-амін, сіль (R)-2-гідрокси-2-фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 27A за методиками, описаними у + Прикладі 1B, Прикладі 1C і Прикладі 1D. МС (APCl) m/z 178 (M+H) . Приклад 27C: N-[(4R)-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 27B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,28 (с, 1H), 8,72 (с, 1H), 8,55 (д, J=6,0 Гц, 1H), 8,36 (д, J=8,1 Гц, 1H), 7,94 (д, J=6,1 Гц, 1H), 7,76 (д, J=8,1 Гц, 1H), 7,63 (т, J=7,9 Гц, 1H), 7,34 (д, J=7,8 Гц, 1H), 7,20-7,13 (м, 1H), 7,01-6,88 (м, 2H), 6,76 (дд, J=8,2, 1,2 Гц, 1H), 5,07-4,98 (м, 1H), 2,21 (дд, J=13,2, 6,2 Гц, 1H), 1,86-1,74 (м, 1H), 1,41 (с, 3H), 1,30 (с, 3H), МС (DCl/NH 3) m/z 348 + 23 (M+H) ; [б] D=+34,1 (c 0,65, CH3OH). Приклад 28: N-[(4R)-2,2-діетил-6-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 26B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,29 (д, J=0,8 Гц, 1H), 8,73 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,34 (дд, J=7,7, 1,1 Гц, 1H), 7,94 (д, J=6,1 Гц, 1H), 7,77 (д, J=8,1 Гц, 1H), 7,63 (т, J=7,9 Гц, 1H), 7,09-7,14 (м, 1H), 6,98-7,05 (м, 2H), 6,81 (дд, J=8,9, 4,9 Гц, 1H), 4,93-5,02 (м, 1H), 2,20 (дд, + 23 J=13,4, 6,1 Гц, 1H), 1,52-1,77 (м, 5H), 0,85-0,94 (м, 6H); МС (DCl/NH3) m/z 394 (M+H) ; [] D=+34,1 (c 0,46, CH3OH). Приклад 29: N-[(4R)-7-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 2D, заміняючи Прикладом 1 23B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 13,02 (шир.с, 1H), 8,71 (с, 1H), 8,07 (с, 1H), 7,68 (д, J=7,5 Гц, 1H), 7,37-7,32 (м, 1H), 7,23 (т, J=7,9 Гц, 1H), 7,09 (д, J=8,2 Гц, 1H), 6,79-6,71 (м, 2H), 6,61 (дд, J=10,6, 2,6 Гц, 1H), 5,03-4,93 (м, 1H), 2,20 (дд, J=13,3, 6,1 Гц, 1H), 1,78 (дд, J=13,2, 10,8 + 23 Гц, 1H), 1,42 (с, 3H), 1,31 (с, 3H); МС (DCl/NH3) m/z 355 (M+H) ; [б] D=+34,7 (c 1,0, CH3OH). Приклад 30: N-[(4R)-7-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 23B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,70 (д, J=7,9 Гц, 1H), 7,59 (с, 1H), 7,34-7,25 (м, 1H), 7,01 (т, J=7,8 Гц, 1H), 6,94 (д, J=8,4 Гц, 1H), 6,806,69 (м, 2H), 6,59 (дд, J=10,6, 2,6 Гц, 1H), 4,98-4,88 (м, 1H), 4,86 (д, J=4,1 Гц, 1H), 4,00-3,88 (м, 1H), 2,90-2,63 (м, 3H), 2,34 (дд, J=16,6, 7,7 Гц, 1H), 2,16 (дд, J=13,3, 6,1 Гц, 1H), 1,94-1,81 (м, 1H), 1,70 (дд, J=13,2, 10,9 Гц, 1H), 1,65-1,51 (м, 1H), 1,40 (с, 3H), 1,29 (с, 3H); МС (ІЕР) m/z 385 + 23 (M+H) ; [б] D=+20,2° (c 1,0, CH3OH). Приклад 31: N-[(4R)-7-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 23B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,70 (д, J=7,5 Гц, 1H), 7,58 (с, 1H), 7,35-7,25 (м, 1H), 7,01 (т, J=7,8 Гц, 1H), 6,94 (д, J=8,3 Гц, 1H), 6,79-6,69 (м, 2H), 6,59 (дд, J=10,6, 2,6 Гц, 1H), 4,98-4,88 (м, 1H), 4,86 (д, J=4,1 Гц, 1H), 3,99-3,86 (м, 1H), 2,90-2,63 (м, 3H), 2,35 (дд, J=16,3, 7,5 Гц, 1H), 2,15 (дд, J=13,2, 6,1 Гц, 1H), 1,93-1,82 (м, 1H), 1,70 (дд, J=13,4, 10,9 Гц, 1H), 1,65-1,51 (м, + 23 1H), 1,40 (с, 3H), 1,28 (с, 3H); МС (ІЕР) m/z 385 (M+H) ; [б] D=+26,0° (с 1,0, CH3OH). Приклад 32: N-[(4R)-8-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-1H-індазол-4ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 2D, заміняючи Прикладом 1 20B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 13,02 (шир.с, 1H), 8,74 (с, 1H), 8,08 (с, 1H), 7,67 (д, J=7,5 Гц, 1H), 7,23 (т, J=7,9 Гц, 1H), 7,14 (д, J=7,4 Гц, 1H), 7,11-7,07 (м, 2H), 6,88 (тд, J=8,0, 5,0 Гц, 1H), 6,77 (д, J=8,4 Гц, 1H), 5,09-4,99 (м, 1H), 2,23 (дд, J=13,3, 6,2 Гц, 1H), 1,84 (дд, J=13,3, 23 UA 100866 C2 + 5 10 15 20 25 30 35 40 45 50 55 60 23 10,9 Гц, 1H), 1,46 (с, 3H), 1,33 (с, 3H); МС (DCl/NH 3) m/z 355 (M+H) ; [б] D=+28,7° (c 0,32, CH3OH). Приклад 33: N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил1H-індазол-4-іл)сечовина Приклад 33A: 2,2-диметил-7-(трифторметил)хроман-4-он Розчин гідрокси-4-(трифторметил) бензойної кислоти (10,0 г, 48,5 ммоль) і ТГФ (100 мл) охолоджують до 5 °C (внутрішня температура) і додають метиллітій (95 мл 1,6M розчину в Et2O, 152 ммоль), зберігаючи внутрішню температуру 20 °C (повільним додаванням, утворення метану). Після додавання метиллітію розчин нагрівають до температури навколишнього середовища й перемішують протягом 1 год. Розчин потім повторно охолоджують до 10 °C і обережно обробляють EtOAc (100 мл) і 2N HСl (100 мл). Реакційну суміш далі розбавляють EtOAc (100 мл), потім промивають водою (100 мл) і насиченим розчином солі (20 мл). Органічну частину сушать (Na2SO4), фільтрують і концентрують із одержанням 1-(2-гідрокси-4(трифторметил)феніл)етанону (10,3 г), який застосовують без подальшого очищення. Неочищений 1-[2-гідрокси-4-(трифторметил)феніл]етанон (9,90 г, 48,5 ммоль) з попередньої стадії розчиняють у метанолі (100 мл) і ацетоні (3,56 мл, 48,5 ммоль) і додають піролідин (8,02 мл, 97,0 ммоль). Реакційну суміш перемішують при температурі навколишнього середовища протягом 14 год.; РХМС показує завершення реакції. Реакційну суміш концентрують і розбавляють EtOAc (300 мл), потім промивають водою (100 мл), 2N HСl (2Ч100 мл), водою (50 мл), 2N NaOH (2Ч100 мл), водою (50 мл) і насиченим розчином солі (20 мл). Органічну частину сушать (Na2SO4), фільтрують, концентрують, і залишок очищають хроматографією на силікагелі (градієнтне елюювання, 0-20 % EtOAc/гексан) з одержанням вказаної в заголовку сполуки (8,93 + г, 36,6 ммоль, 75 %) у вигляді білої твердої речовини. МС (ІЕР) m/z 245 (M+H) . Приклад 33B: (R)-7-(Трифторметил)-2,2-диметилхроман-4-амін, сіль (R)-2-гідрокси-2фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 33A за методиками, описаними у + Прикладі 1B, Прикладі 1C і Прикладі 1D. МС (DCl/NH3) m/z 246 (M+H) . Приклад 33C: N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1метил-1H-індазол-4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 33B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,81 (с, 1H), 8,05 (д, J=0,9 Гц, 1H), 7,70 (д, J=7,5 Гц, 1H), 7,54 (д, J=8,1 Гц, 1H), 7,32-7,23 (м, 2H), 7,18 (д, J=8,3 Гц, 1H), 7,07 (д, J=1,7 Гц, 1H), 6,80 (д, J=8,4 Гц, 1H), 5,12-5,03 (м, 1H), 3,28 (с, 3H), 2,23 (дд, J=13,2, 6,2 Гц, 1H), 1,86 (дд, J=13,2, + 23 11,2 Гц, 1H), 1,42 (с, 3H), 1,32 (с, 3H); МС (DCl/NH3) m/z 419 (M+H) ; [б] D=+16° (c 0,78, CH3OH). Приклад 34: N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін5-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 33B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,29 (д, J=0,8 Гц, 1H), 8,78 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,33 (дд, J=7,7, 1,1 Гц, 1H), 7,94 (д, J=6,1 Гц, 1H), 7,78 (д, J=8,1 Гц, 1H), 7,64 (т, J=7,9 Гц, 1H), 7,56 (д, J=8,1 Гц, 1H), 7,26 (дд, J=8,1, 1,8 Гц, 1H), 7,08-7,04 (м, 2H), 5,14-5,04 (м, 1H), 2,25 (дд, J=13,3, 6,2 Гц, 1H), 1,87 (дд, J=13,2, 11,1 Гц, 1H), 1,45 (с, 3H), 1,33 (с, 3H); МС (DCl/NH 3) m/z + 23 416 (M+H) ; [б] D=+26,8° (c 0,50, CH3OH). Приклад 35: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(3-метилізохінолін-5іл)сечовина Приклад 35A: 3-Метил-5-нітроізохінолін В 0 °C розчин 3-метилізохіноліну (3,00 г, 20,9 ммоль) у концентрованій сірчаній кислоті (35 мл) додають твердий нітрат калію (2,33 г, 23,0 ммоль) чотирма порціями. Суміш перемішують 2 год. при 0 °C, потім розбавляють льодом. Цю суміш підлужнюють (pН 10) 50 % водним NaOH, екстрагують CH2Cl2 (60 мл). Органічну фазу промивають насиченим розчином солі (25 мл), сушать (Na2SO4), фільтрують і леткі речовини видаляють у вакуумі. Отриману тверду речовину розтирають із 1:1 EtOAС-гексаном, фільтрують і сушать на повітрі з одержанням вказаної в 1 заголовку сполуки (1,60, 8,78 ммоль, 42 %) у вигляді жовтої твердої речовини. H ЯМР (300 МГц, CdСl3) д 9,30 (с, 1H), 8,53 (дд, J=7,7, 1,1 Гц, 1H), 8,35 (с, 1H), 8,26 (д, J=8,1 Гц, 1H), 7,64 (дд, + J=9,9, 5,9 Гц, 1H), 2,80 (с, 3H); МС (ІЕР) m/z 189 (M+H) . Приклад 35B: 3-Метилізохінолін-5-амін До розчину Прикладу 35A (1,60 г, 8,82 ммоль) в етанолі (45 мл) і ТГФ (45 мл) додають 10 % Pd/C (100 мг). Розчин гідрують в 1 атмосфері водню протягом 16 год. при температурі навколишнього середовища. Суміш фільтрують через шар Целіту, і леткі речовини випарюють у вакуумі. Отриману тверду речовину розтирають із 1:1 CH 2Cl2-гексаном і сушать на повітрі з одержанням вказаної в заголовку сполуки (1,31 г, 8,29 ммоль, 94 % вихід) у вигляді світло 24 UA 100866 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 зеленої твердої речовини. H ЯМР (300 МГц, ДМСО-d6) д 9,00 (с, 1H), 7,78 (д, J=0,6 Гц, 1H), 7,25 (д, J=7,5 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 6,80 (дд, J=7,4, 1,2 Гц, 1H), 5,84 (с, 2H), 2,58 (с, 3H); МС + (ІЕР) m/z 159 (M+H) . Приклад 35C: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-(3-метилізохінолін5-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 35B 5-аміноізохінолін. H ЯМР (300 МГц, ДМСО-d6) д 9,19 (с, 1H), 8,65 (с, 1H), 8,27 (д, J=7,6 Гц, 1H), 7,72 (д, J=8,2 Гц, 1H), 7,53 (т, J=7,9 Гц, 1H), 7,12 (дд, J=9,5, 3,0 Гц, 1H), 7,02 (тд, J=8,4, 3,3 Гц, 2H), 6,79 (дд, J=8,9, 4,9 Гц, 1H), 5,00 (дд, J=17,8, 7,4 Гц, 1H), 2,59 (д, J=14,2 Гц, 3H), 2,20 (дд, J=13,2, 6,2 Гц, 1H), 1,83-1,71 (м, 1H), 1,38 (д, J=19,2 Гц, 3H), 1,30-1,19 (м, 3H); МС (ІЕР) m/z 380 + (M+H) . Приклад 36: N-[(4R)-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 27B Приклад 1D. H ЯМР (300 МГц, ДМСОd6) д 7,71 (д, J=7,8 Гц, 1H), 7,58 (с, 1H), 7,28 (д, J=7,6 Гц, 1H), 7,14 (т, J=7,7 Гц, 1H), 7,01 (т, J=7,8 Гц, 1H), 6,94 (д, J=8,4 Гц, 1H), 6,89 (тд, J=7,6, 1,1 Гц, 1H), 6,77-6,70 (м, 2H), 5,01-4,89 (м, 1H), 4,86 (д, J=4,1 Гц, 1H), 3,99-3,87 (м, 1H), 2,90-2,64 (м, 3H), 2,34 (дд, J=16,5, 7,7 Гц, 1H), 2,15 (дд, J=613,2, 6,2 Гц, 1H), 1,93-1,82 (м, 1H), 1,69 (дд, J=13,2, 10,8 Гц, 1H), 1,63-1,51 (м, 1H), 1,39 (с, 3H), 1,28 (с, 3H); + 23 МС (ІЕР) m/z 367 (M+H) ; [б] D=+28,0° (c 1,0, CH3OH). Приклад 37: N-[(4R)-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-[(7S)-7-гідрокси-5,6,7,8тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 27B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,72 (д, J=7,3 Гц, 1H), 7,57 (с, 1H), 7,28 (д, J=7,6 Гц, 1H), 7,14 (тд, J=7,5, 1,2 Гц, 1H), 7,01 (т, J=7,8 Гц, 1H), 6,96-6,84 (м, 2H), 6,73 (дд, J=8,2, 1,2 Гц, 2H), 5,01-4,89 (м, 1H), 4,85 (д, J=4,2 Гц, 1H), 3,98-3,87 (м, 1H), 2,89-2,64 (м, 3H), 2,35 (дд, J=16,4, 7,7 Гц, 1H), 2,15 (дд, J=13,2, 6,2 Гц, 1H), 1,92-1,82 (м, 1H), 1,69 (дд, J=13,1, 10,9 Гц, 1H), + 23 1,64-1,52 (м, 1H), 1,39 (с, 3H), 1,27 (с, 3H); МС (ІЕР) m/z 367 (M+H) ; [б] D=+33,5° (c 1,0, CH3OH). Приклад 38: N-[(4R)-6-Фтор-2,2-диметил-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-8ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи 81 аміноізохіноліном (Combi-Blocks) 5-аміноізохінолін. H ЯМР (300 МГц, ДМСО-d6) д 9,52 (с, 1H), 9,00 (с, 1H), 8,51 (д, J=5,7 Гц, 1H), 8,18 (дд, J=7,6, 0,8 Гц, 1H), 7,80 (д, J=5,2 Гц, 1H), 7,71 (т, J=7,9 Гц, 1H), 7,60 (д, J=8,1 Гц, 1H), 7,13 (дд, J=9,5, 2,5 Гц, 1H), 7,01 (дд, J=13,4, 3,6 Гц, 1H), 6,79 (дд, J=8,9, 4,9 Гц, 1H), 5,01 (дд, J=17,9, 7,3 Гц, 1H), 2,21 (дд, J=13,2, 6,2 Гц, 1H), 1,79 (дд, J=13,1, 11,0 + Гц, 1H), 1,41 (с, 3H), 1,29 (с, 3H); МС (ІЕР) m/e 366 (M+H) . Приклад 39: N-[(4R)-2,2-диметил-7-(трифторметокси)-3,4-дигідро-2H-хромен-4-іл]-N'-(1метил-1H-індазол-4-іл)сечовина Приклад 39A: 2,2-диметил-7-(трифторметокси)хроман-4-он Реагент Ітона (225 мл) нагрівають до 70 °C і додають 3-метилбут-2-енову кислоту (28,1 г, 281 ммоль) і 3-(трифторметокси)фенол (25,0 г, 140 ммоль). Через 30 хв додають ще 3метилбут-2-енову кислоту (1 екв., 14 г) і нагрівання продовжують. Через 30 хв додають ще реагент Ітона (150 мл) і нагрівання продовжують протягом 35 хв. Темний розчин охолоджують і виливають у лід. Водну суспензію екстрагують Et2O (300 мл), і органічну частину промивають водою (75 мл) і насиченим розчином солі (50 мл). Органічну частину сушать (Na 2SO4), фільтрують, концентрують і очищають хроматографією на силікагелі (градієнтне елюювання, 020 % EtOAc/гексан) з одержанням вказаної в заголовку сполуки (11,7 г, 45,0 ммоль, 32 %) у + вигляді білої твердої речовини. МС (ІЕР) m/z 261 (M+H) . Приклад 39B: (R)-7-(Трифторметокси)-2,2-диметилхроман-4-амін, сіль (R)-2-гідрокси-2фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 39A за методиками, описаними у + Прикладі 1B, Прикладі 1C і Прикладі 1D. МС (DCl/NH3+) m/z 262 (M+H) . Приклад 39C: N-[(4R)-2,2-диметил-7-(трифторметокси)-3,4-дигідро-2H-хромен-4-іл]-N'-(1метил-1H-індазол-4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 39B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,75 (с, 1H), 8,04 (д, J=0,9 Гц, 1H), 7,70 (дд, J=7,5, 0,8 Гц, 1H), 7,43 (дд, J=8,5, 1,0 Гц, 1H), 7,27 (д, J=7,7 Гц, 1H), 7,17 (дт, J=8,4, 0,8 Гц, 1H), 6,91 (ддд, J=8,5, 2,5, 1,2 Гц, 1H), 6,78-6,73 (м, 2H), 5,06-4,97 (м, 1H), 4,01 (с, 3H) 2,28-2,18 (м, 1H), 1,82 (дд, J=13,3, 10,9 Гц, 1H), 1,43 (с, 3H), 1,32 (с, 3H); МС (DCl/NH 3) m/z 435 (M+H)+; 23 [б] D=+6,2° (c 0,53, CH3OH). 25 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 Приклад 40: N-[(4R)-2,2-диметил-7-(трифторметокси)-3,4-дигідро-2H-хромен-4-іл]-N'ізохінолін-5-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 39B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,29 (д, J=0,8 Гц, 1H), 8,78 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,34 (дд, J=7,7, 1,1 Гц, 1H), 7,93 (д, J=6,1 Гц, 1H), 7,77 (д, J=8,1 Гц, 1H), 7,63 (т, J=7,9 Гц, 1H), 7,45 (дд, J=8,5, 1,0 Гц, 1H), 7,02 (д, J=8,3 Гц, 1H), 6,92 (ддд, J=8,5, 2,5, 1,3 Гц, 1H), 6,75 (дд, J=2,5, 1,1 Гц, 1H), 5,08-4,99 (м, 1H), 2,22 (дд, J=13,3, 6,1 Гц, 1H), 1,83 (дд, J=13,3, 10,8 Гц, 1H), + 23 1,45 (с, 3H), 1,33 (с, 3H); МС (DCl/NH3) m/z 432 (M+H) ; [б] D=+7,5° (c 0,45, CH3OH). Приклад 41: N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-1Hіндазол-4-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 2D, заміняючи Прикладом 1 33B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 13,02 (шир.с, 1H), 8,77 (с, 1H), 8,09 (с, 1H), 7,67 (д, J=7,2 Гц, 1H), 7,54 (д, J=8,1 Гц, 1H), 7,24 (т, J=8,0 Гц, 2H), 7,10 (д, J=8,2 Гц, 1H), 7,07 (д, J=1,8 Гц, 1H), 6,81 (д, J=8,4 Гц, 1H), 5,12-5,03 (м, 1H), 2,23 (дд, J=13,2, 6,1 Гц, 1H), 1,90-1,81 (м, 1H), + 23 1,44 (с, 3H), 1,33 (с, 3H); МС (DCl/NH3) m/z 405 (M+H) ; [б] D=+21,4° (c 0,30, CH3OH). Приклад 42: N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил1H-індазол-4-іл)сечовина Приклад 42A: 1-(Метоксиметокси)-2-(трифторметил)бензол Розчин 2-(трифторметил)фенолу (12,0 г, 74,0 ммоль) у дихлорметані (49 мл) охолоджують до 5 °C і по краплях додають N, N-діізопропілетиламін (25,9 мл, 148 ммоль) і метоксиметилхлорид (8,43 мл, 111 ммоль), зберігаючи внутрішню температуру 15 °C. Після перемішування протягом 15 хв при температурі навколишнього середовища реакційну суміш розбавляють МТБЕ (250 мл) і промивають 2N HСl (2Ч50 мл), водою (50 мл), 2N NaOH (2Ч30 мл), водою (30 мл) і насиченим розчином солі (30 мл). Органічну частину сушать (Na 2SO4), фільтрують і концентрують із одержанням вказаної в заголовку сполуки (14,1 г, 68,4 ммоль, + 92 %), яку застосовують без подальшого очищення. МС (DCl/NH3) m/z 207 (M+H) . Приклад 42B: 2-Гідрокси-3-(трифторметил)бензойна кислота Розчин Прикладу 42A (14,1 г, 68,4 ммоль) у ТГФ (68 мл) охолоджують до -20 °C і повільно додають нибутиллітій (30,1 мл 2,5 M розчину в гексані, 75,0 ммоль), зберігаючи температуру 0 °C. Через 70 хв при температурі від -5 до 5 °C реакційну суміш охолоджують до -20 °C, і CO2 газ барботують через коричневу суспензію, зберігаючи температуру ≤-10 °C. Реакційна суміш змінюється від коричневої суспензії до темно-фіолетового розчину, потім до жовтого розчину. Через 10 хв реакційну суміш далі охолоджують до -20 °C і обробляють 2N HСl (68 мл, 140 ммоль). Для сприяння утвору реакційної суміші додають ще HСl (17 мл, усього 5 екв 4M HСl). Через 30 хв додають МТБЕ (70 мл), і органічну частину екстрагують 2N NaOH (70 мл) і водою (70 мл). Водний шар підкисляють 2N HСl (98 мл) і екстрагують дихлорметаном (2Ч140 мл). Органічну частину сушать (Na2SO4), фільтрують і концентрують із одержанням вказаної в заголовку сполуки (14,8 г, 71,8 ммоль, 99 %) у вигляді жовтої твердої речовини, яку + застосовують без подальшого очищення. МС (DCl/NH3) m/z 207 (M+H) . Приклад 42C: 1-(2-Гідрокси-3-(трифторметил)феніл)етанон Розчин Прикладу 42B (14,1 г, 68,4 ммоль) у ТГФ (70 мл) охолоджують до 5 °C і додають метиллітій (133 мл 1,6M розчину в Et2O, 212 ммоль), зберігаючи температуру 20 °C (повільне додавання, утворення метану). Охолоджуючу баню видаляють і через 10 хв підтверджують утворенням реакційної суміші РХМС. Реакційну суміш охолоджують до 10 °C і додають EtOAc (140 мл) і 2N HСl (140 мл). Шари розділяють, і органічну частину промивають водою (70 мл) і насиченим розчином солі (28 мл). Органічну частину сушать (Na 2SO4), фільтрують і концентрують із одержанням вказаної в заголовку сполуки (14,0 г, 68,6 ммоль, 99 %) у вигляді оранжевого масла, яке застосовують без подальшого очищення. МС (DCl/NH 3) m/z 222 + (M+NH4) . Приклад 42D: 2,2-диметил-8-(трифторметил)хроман-4-он Розчин неочищеного Прикладу 42C (13,9 г, 68,4 ммоль), метанолу (140 мл), 2-пропанону (10,1 мл, 137 ммоль) і піролідину (6,22 мл, 75,0 ммоль) перемішують при температурі навколишнього середовища протягом 16 год. Додають EtOAc (430 мл), і розчин промивають водою (140 мл), 2N HСl (2Ч70 мл), водою (70 мл), 2N NaOH (2Ч70 мл), водою (70 мл) і насиченим розчином солі (30 мл). Органічну частину сушать (Na 2SO4), фільтрують і концентрують. Одержаний залишок очищають хроматографією на силікагелі (градієнтне елюювання, 0-25 % EtOAc/гексан) з одержанням вказаної в заголовку сполуки (9,04 г, 37,0 ммоль, 54 % загальний вихід) у вигляді білуватої твердої речовини. МС (DCl/NH 3) m/z 262 + (M+NH4) . 26 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 42E: (R)-8-(Трифторметил)-2,2-диметилхроман-4-амін, сіль (R)-2-гідрокси-2фенілоцтової кислоти Вказану в заголовку сполуку одержують із Прикладу 42D за методиками, описаними у + Прикладі 1B, Прикладі 1C і Прикладі 1D. МС (DCl/NH3+) m/z 246 (M+H) . Приклад 42F: N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1метил-1H-індазол-4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 42E Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д ч./млн. 8,79 (с, 1H), 8,05 (д, J=0,9 Гц, 1H), 7,69 (дд, J=7,5, 0,7 Гц, 1H), 7,59-7,63 (м, 1H), 7,51 (д, J=7,8 Гц, 1H), 7,27 (д, J=7,7 Гц, 1H), 7,19-7,16 (м, 1H), 7,06 (т, J=7,7 Гц, 1H), 6,79 (д, J=8,4 Гц, 1H), 5,11-5,01 (м, 1H), 4,01 (с, 3H), 2,25 (дд, J=13,3, + 6,3 Гц, 1H), 1,90 (дд, J=13,3, 10,8 Гц, 1H), 1,44 (с, 3H), 1,33 (с, 3H); МС (DCl/NH 3) m/z 419 (M+H) ; 23 [] D=+14° (c 0,68, CH3OH). Приклад 43: N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін8-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 33B Приклад 1C, і заміняючи 8-аміноізохіноліном ізохінолін-5-амін. H ЯМР (300 МГц, ДМСО-d6) д 9,52 (с, 1H), 9,04 (с, 1H), 8,51 (д, J=5,7 Гц, 1H), 8,21-8,15 (м, 1H), 7,80 (дд, J=5,7, 0,5 Гц, 1H), 7,71 (т, J=7,9 Гц, 1H), 7,64-7,55 (м, 2H), 7,29-7,23 (м, 1H), 7,06 (д, J=8,5 Гц, 2H), 5,07 (д, J=8,3 Гц, 1H), 2,25 (дд, J=13,3, 6,2 Гц, 1H), 1,94-1,82 (м, 1H), 1,45 (с, 3H), 1,33 (с, 3H); МС (DCl/NH3) m/z + 416 (M+H) . Приклад 44: N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін5-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 42E Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,31 (с, 1H), 8,75 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,33 (д, J=7,7 Гц, 1H), 7,94 (д, J=6,1 Гц, 1H), 7,78 (д, J=8,1 Гц, 1H), 7,60-7,66 (м, 2H), 7,52 (д, J=7,8 Гц, 1H), 7,06 (т, J=8,3 Гц, 2H), 5,13-5,03 (м, 1H), 2,27 (дд, J=13,3, 6,3 Гц, 1H), 2,00-1,86 (м, + 23 1H), 1,44 (с, 3H), 1,33 (с, 3H); МС (DCl/NH3) m/z 416 (M+H) ; [б] D=+23,8° (c 0,65, CH3OH). Приклад 45: N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-1Hіндазол-4-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 2D, заміняючи Прикладом 1 42E Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 13,02 (шир.с, 1H), 8,77 (с, 1H), 8,09 (с, 1H), 7,66 (д, J=7,5 Гц, 1H), 7,63-7,59 (м, 1H), 7,51 (д, J=7,8 Гц, 1H), 7,23 (т, J=7,9 Гц, 1H), 7,16-6,94 (м, 2H), 6,81 (д, J=8,4 Гц, 1H), 5,1 1-5,02 (м, 1H), 2,26 (дд, J=13,3, 6,2 Гц, 1H), 1,90 (дд, J=13,3, 10,9 Гц, + 23 1H), 1,44 (с, 3H), 1,33 (с, 3H); МС (DCl/NH3) m/z 405 (M+H) ; [б] D=+13,8° (c 0,45, CH3OH). Приклад 46: N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина Приклад 46A: 2,2-діетил-7-фторхроман-4-он Вказану в заголовку сполуку одержують за методикою Прикладу 26A, заміняючи 1-(4-фтор+ 2-гідроксифеніл)етаноном 1-(5-фтор-2-гідроксифеніл)етанон. МС (ІЕР) m/z 240 (M+NH4) . Приклад 46B: (R)-2,2-діетил-7-фторхроман-4-амін Вказану в заголовку сполуку одержують із Прикладу 46A за методиками, описаними у + Прикладі 1B і Прикладі 1C. МС (DCl/NH3) m/z 224 (M+H) . Приклад 46C: N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол4-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 46B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,73 (с, 1H), 8,04 (д, J=0,9 Гц, 1H), 7,70 (дд, J=7,5, 0,7 Гц, 1H), 7,37-7,25 (м, 2H), 7,17 (д, J=8,3 Гц, 1H), 6,78-6,70 (м, 2H), 6,63 (дд, J=10,6, 2,6 Гц, 1H), 5,00-4,90 (м, 1H), 4,01 (с, 3H), 2,23-2,14 (м, 1H), 1,77-1,51 (м,5H), 0,99-0,86 (м, 6H); МС + 23 (DCl/NH3) m/z 397 (M+H) ; [б] D=+1,0° (c 0,58, CH3OH). Приклад 47: N-[(4R)-2,2-диметил-8-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 42E Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,69 (д, J=7,8 Гц, 1H), 7,63 (с, 1H), 7,56 (д, J=7,7 Гц, 1H), 7,50 (д, J=7,6 Гц, 1H), 7,10-6,97 (м, 3H), 6,74 (д, J=7,4 Гц, 1H), 5,07-4,94 (м, 1H), 4,86 (д, J=4,2 Гц, 1H), 4,00-3,87 (м, 1H), 2,91-2,64 (м, 3H), 2,35 (дд, J=16,5, 7,7 Гц, 1H), 2,22 (дд, J=13,3, 6,3 Гц, 1H), 1,93-1,75 (м, 2H), 1,67-1,50 (м, 1H), 1,43 (с, + 23 3H), 1,31 (с, 3H); МС (ІЕР) m/z 435 (M+H) ; [б] D=+28,2° (c 1,0, CH3OH). Приклад 48: N-[(4R)-2,2-діетил-7-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5-ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 46B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,28 (д, J=0,8 Гц, 1H), 8,71 (с, 1H), 8,56 (д, J=6,0 27 UA 100866 C2 5 10 15 20 25 30 35 40 45 50 55 Гц, 1H), 8,35 (дд, J=7,7, 1,1 Гц, 1H), 7,93 (д, J=6,1 Гц, 1H), 7,76 (д, J=8,1 Гц, 1H), 7,66-7,57 (м, 1H), 7,39-7,33 (м, 1H), 6,98 (д, J=8,2 Гц, 1H), 6,76 (тд, J=8,5, 2,6 Гц, 1H), 6,66-6,56 (м, 1H), 5,01-4,92 (м, 1H), 2,20 (дд, J=13,5, 6,0 Гц, 1H), 1,79-1,54 (м, 5H), 0,95-0,84 (м, 6H); МС (DCl/NH3) m/z 394 + 23 (M+H) ; [б] D=+8,8° (c 0,25, CH3OH). Приклад 49: N-[(4R)-2,2-діетил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил1H-індазол-4-іл)сечовина Приклад 49A: 2,2-діетил-7-(трифторметил)хроман-4-он Вказану в заголовку сполуку одержують за методикою Прикладу 26A, заміняючи 1-[2гідрокси-4-(трифторметил)феніл]етаноном (отриманим за методикою Прикладу 33A) 1-(5-фтор+ 2-гідроксифеніл)етанон. МС (ІЕР) m/z 273 (M+H) . Приклад 49B: (R)-2,2-діетил-7-(трифторметил)хроман-4-амін Вказану в заголовку сполуку одержують із Прикладу 49A за методиками, описаними у + Прикладі 1B і Прикладі 1C. МС (DCl/NH3) m/z 274 (M+H) . Приклад 49C: N-[(4R)-2,2-діетил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил1Н-індазол-4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 49B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,80 (с, 1H), 8,05 (д, J=0,9 Гц, 1H), 7,70 (д, J=7,5 Гц, 1H), 7,54 (д, J=8,1 Гц, 1H), 7,29 (д, J=8,1 Гц, 1H), 7,27-7,22 (м, 1H), 7,18 (д, J=8,3 Гц, 1H), 7,08 (д, J=1,8 Гц, 1H), 6,80 (д, J=8,4 Гц, 1H), 5,09-4,99 (м, 1H), 4,01 (с, 3H), 2,28-2,19 (м, 1H), 1,85-1,53 + 23 (м, 5H), 0,96-0,87 (м, 6H); МС (DCl/NH3) m/z 447 (M+H) ; [б] D=+8,6° (c 0,57, CH3OH). Приклад 50: N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол-4іл)сечовина Приклад 50A: 2,2-діетил-8-фторхроман-4-он Вказану в заголовку сполуку одержують за методикою Прикладу 26A, заміняючи 1-(3-фтор+ 2-гідроксифеніл)етаноном 1-(5-фтор-2-гідроксифеніл)етанон. МС (DCl/NH3) m/z 240 (M+NH4) . Приклад 50B: (R)-2,2-діетил-8-фторхроман-4-амін Вказану в заголовку сполуку одержують із Прикладу 50A за методиками, описаними у + Прикладі 1B і Прикладі 1C. МС (DCl/NH3+) m/z 224 (M+H) . Приклад 50C: N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-(1-метил-1H-індазол4-іл)сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 1H, заміняючи Прикладом 1 50B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 8,75 (с, 1H), 8,04 (д, J=0,9 Гц, 1H), 7,70 (дд, J=7,5, 0,8 Гц, 1H), 7,27 (д, J=7,7 Гц, 1H), 7,06-7,19 (м, 3H), 6,88 (тд, J=7,9, 5,0 Гц, 1H), 6,76 (д, J=8,3 Гц, 1H), 4,01 (с, 3H), 2,28-2,19 (м, 1H), 1,83-1,58 (м, 6H), 0,96-0,87 (м, 6H); МС (DCl/NH3) + 23 m/z 397 (M+H) ; [] D=+7,2° (c 0,57, CH3OH). Приклад 51: N-[(4R)-2,2-діетил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-ізохінолін-5ілсечовина Вказану в заголовку сполуку одержують за методикою Прикладу 5, заміняючи Прикладом 1 49B Приклад 1C. H ЯМР (300 МГц, ДМСО-d6) д 9,29 (д, J=0,6 Гц, 1H), 8,76 (с, 1H), 8,56 (д, J=6,0 Гц, 1H), 8,33 (дд, J=7,6, 1,0 Гц, 1H), 7,94 (д, J=6,1 Гц, 1H), 7,78 (д, J=8,1 Гц, 1H), 7,68-7,49 (м, 2H), 7,25 (д, J=8,1 Гц, 1H), 7,07 (дд, J=11,8, 4,9 Гц, 2H), 5,04 (с, 1H), 2,24 (дд, J=13,6, 6,2 Гц, 1H), 1,80+ 23 1,50 (м, 5H), 1,00-0,80 (м, 6H); МС (DCl/NH3) m/z 444 (M+H) ; [б] D=+24,3° (c 0,14, CH3OH). Приклад 52: N-[(4R)-2,2-діетил-8-фтор-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7-гідрокси5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 50B Приклад 1D. H ЯМР (300 МГц, ДМСО-d6) д 7,70 (д, J=7,5 Гц, 1H), 7,59 (с, 1H), 7,13-6,95 (м, 4H), 6,86 (дт, J=8,0, 5,0 Гц, 1H), 6,73 (д, J=7,4 Гц, 1H), 5,01-4,88 (м, 1H), 4,86 (д, J=4,2 Гц, 1H), 3,97-3,87 (м, 1H), 2,90-2,65 (м, 3H), 2,34 (дд, J=16,5, 7,6 Гц, 1H), 2,18 (дд, J=13,5, 6,1 Гц, 1H), 1,94-1,81 (м, 1H), 1,78-1,50 (м, 6H), 0,90 (дт, J=12,1, 7,4 Гц, + 23 6H); МС (ІЕР) m/z 413 (M+H) ; [б] D=+22,1° (c 1,0, CH3OH). Приклад 53: N-[(4R)-2,2-диметил-7-(трифторметил)-3,4-дигідро-2H-хромен-4-іл]-N'-[(7R)-7гідрокси-5,6,7,8-тетрагідронафталін-1-іл]сечовина Вказану в заголовку сполуку одержують за методикою Прикладу 3C, заміняючи Прикладом 1 4A Приклад 3B, і заміняючи Прикладом 33B Приклад 1D. H ЯМР (300 МГц, ДМСОd6) д 7,69 (д, J=7,9 Гц, 1H), 7,63 (с, 1H), 7,50 (д, J=8,1 Гц, 1H), 7,24 (дд, J=8,0, 1,2 Гц, 1H), 7,07-6,97 (м, 3H), 6,74 (д, J=7,5 Гц, 1H), 5,08-4,95 (м, 1H), 4,87 (д, J=4,1 Гц, 1H), 4,00-3,86 (м, 1H), 2,91-2,64 (м, 3H), 2,35 (дд, J=16,5, 7,7 Гц, 1H), 2,20 (дд, J=13,3, 6,2 Гц, 1H), 1,93-1,83 (м, 1H), 1,77 (дд, J=13,0, 11,5 + 23 Гц, 1H), 1,67-1,51 (м, 1H), 1,43 (с, 3H), 1,31 (с, 3H); МС (ІЕР) m/z 435 (M+H) ; [] D=+34,8° (c 1,0, CH3OH). 28
ДивитисяДодаткова інформація
Назва патенту англійськоюSolid dispersion product comprising n-aryl urea-based compounds
Автори англійськоюSchroeder, Rudolf, Heitermann, Tanja
Назва патенту російськоюПродукт твердой дисперсии, который содержит соединения на основе n-арилмочевины
Автори російськоюШредер Рудольф, Хайтерманн Танья
МПК / Мітки
МПК: A61K 9/16, A61K 31/337
Мітки: продукт, твердої, дисперсії, містить, основі, сполуки, n-арилсечовини
Код посилання
<a href="https://ua.patents.su/45-100866-produkt-tverdo-dispersi-shho-mistit-spoluki-na-osnovi-n-arilsechovini.html" target="_blank" rel="follow" title="База патентів України">Продукт твердої дисперсії, що містить сполуки на основі n-арилсечовини</a>
Попередній патент: Твердий дисперсний продукт лікарських засобів на основі n-арилсечовини
Наступний патент: Похідна (аза)індолу, заміщена в положенні 5, фармацевтична композиція, що містить її, проміжні сполуки та спосіб їх одержання
Випадковий патент: Спосіб отримання постійної частоти синхронного генератора












