Азолідинонові похідні конденсованих вінілбензолів
Номер патенту: 79793
Опубліковано: 25.07.2007
Автори: Рюкле Томас, Гейяр Паскаль, Черч Денніс, Дзянь Сюлянь, Валлотон Таня
Формула / Реферат
1. Застосування сполуки формули (I)
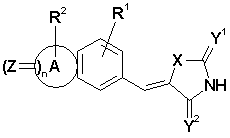 , (I)
, (I)
а також геометричних ізомерів, оптично активних форм, наприклад, енантіомерів, діастереомерів та рацемічних форм, а також фармацевтично прийнятних солей та фармацевтично активних похідних цієї сполуки, де
A є 5-8-членна гетероциклічна або карбоциклічна група, причому згадана карбоциклічна група може бути конденсована з арилом, гетероарилом, циклоалкілом або гетероциклоалкілом;
X – S, O або NH;
кожний з Y1 та Y2 незалежно один від одного є S, O або -NH;
Z – S або O;
R1 є H, CN, карбоксил, ацил, C1-C6-алкоксигрупа, галоген, гідроксил, ацилокси-, C1-C6-алкілкарбокси-, C1-C6-алкілацилокси-, C1-C6-алкілалкоксигрупа, алкоксикарбоніл, C1-C6-алкілалкоксикарбоніл, амінокарбоніл, C1-C6-алкіламінокарбоніл, ациламіно-, C1-C6-алкілациламіно-, уреїдо-, C1-C6-алкілуреїдо-, аміно-, C1-C6-алкіламіногрупа, амоній, сульфонілокси-, C1-C6-алкілсульфонілоксигрупа, сульфоніл, C1-C6-алкілсульфоніл, сульфініл, C1-C6-алкілсульфініл, сульфаніл, C1-C6-алкілсульфаніл, сульфоніламіно-, C1-C6-алкілсульфоніламіногрупа або карбамат;
R2 вибраний з групи, яка складається або до якої входять H, галоген, ацил, аміногрупа, C1-C6-алкіл, C2-C6-алкеніл, C2-C6-алкініл, C1-C6-алкілкарбоксил, C1-C6-алкілацил, C1-C6-алкілалкоксикарбоніл, C1-C6-алкіламінокарбоніл, C1-C6-алкілацилоксигрупа, C1-C6-алкілациламін, C1-C6-алкілуреїдо-, C1-C6-алкіламіно-, C1-C6-алкілалкоксигрупа, C1-C6-алкілсульфаніл, C1-C6-алкілсульфініл, C1-C6-алкілсульфоніл, C1-C6-алкілсульфоніламіноарил, арил, C3-C8-циклоалкіл або гетероциклоалкіл,
C1-C6-алкіларил, C2-C6-алкеніларил, C2-C6-алкініларил, карбокси-, ціаногрупа, гідроксил, C1-C6-алкокси-, нітро-, ациламіно-, уреїдогрупа, C1-C6-алкілкарбамат, сульфоніламіногрупа, сульфаніл та сульфоніл;
n – 0, 1 або 2;
за винятком вказаних нижче сполук:
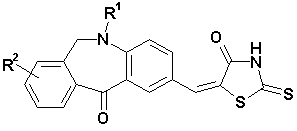 ,
,
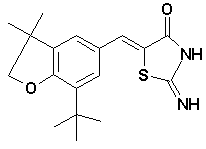 ,
,
(TE)
(JA)
де R1 є нижчий алкіл або аралкіл і R2 є H або галоген,
для виготовлення лікарського засобу для профілактики та/або лікування автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, агрегації тромбоцитів, раку, відторгнення трансплантата або травм легенів.
2. Застосування сполуки за п. 1, причому згадане захворювання вибране з групи, до якої входять розсіяний склероз, псоріаз, ревматоїдний артрит, системний червоний вовчак, запальне захворювання кишок, запалення легенів, тромбоз або інфекційне захворювання чи запалення мозку, наприклад, менінгіт або енцефаліт.
3. Застосування сполуки за п. 1, причому згадане захворювання вибране з групи, до якої входять хвороба Альцгеймера, хорея Гентінгтона, травма центральної нервової системи, інсульт та ішемічні стани.
4. Застосування сполуки за п. 1, причому згадане захворювання вибране з групи, до якої входять атеросклероз, гіпертрофія серця, дисфункція серцевого міоцита, підвищений кров’яний тиск та судинозвуження.
5. Застосування сполуки за п.1, причому згадане захворювання вибране з групи, до якої входять хронічне обструктивне легеневе захворювання, фіброзний анафілактичний шок, псоріаз, алергічні захворювання, астма, інсульт або ішемічні стани, ішемія-реперфузія, агрегація/активація тромбоцитів, атрофія/гіпертрофія скелетного м’яза, рекрутмент лейкоцитів у раковій тканині, панкреатит, множинна недостатність органів, ангіогенез, метастазування пухлин, зокрема, меланоми, саркоми Капоші, гострі та хронічні бактеріальні та вірусні інфекції, сепсис, відторгнення трансплантата, гломерулосклероз, гломерулонефрит, прогресивний нирковий фіброз, ендотеліальні та епітеліальні травми легенів і генералізоване запалення легеневих дихальних шляхів.
6. Застосування за будь-яким із попередніх пунктів, причому кожен з Y1 та Y2 є кисень.
7. Застосування за будь-яким із попередніх пунктів, причому n є 1 або 2 і кожен із R1 та R2 є H.
8. Застосування сполук за будь-яким із попередніх пунктів, причому X є S, кожен з Y1 та Y2 є O, R1 та R2 відповідають вищенаведеним визначенням та n є 0.
9. Застосування за будь-яким із попередніх пунктів, причому згадана тіазолідинонова похідна конденсованого вінілбензолу має формулу (Ia)
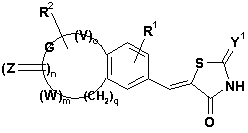 , (Ia)
, (Ia)
де Y1, R1, R2, Z та n відповідають вищенаведеним визначенням;
кожний з V та W незалежно від іншого є O, S або -NR3, де R3 є H або
C1-C6-алкіл;
G є C1-C5-алкіленова або C1-C5-алкеніленова група;
кожний з o та m незалежно від іншого є 0 або 1;
q – ціле число від 0 до 4.
10. Застосування за п. 9, причому згадана тіазолідинонова похідна конденсованого вінілбензолу має формулу (Ib)
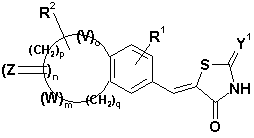 , (Ib)
, (Ib)
де Y1, R1, R2, V, Z, W, m, n, o, q відповідають вищенаведеним визначенням і p – ціле число від 1 до 4.
11. Застосування за будь-яким із п. 9 або п. 10, причому згадана тіазолідинонова похідна конденсованого вінілбензолу має формулу (Ic)
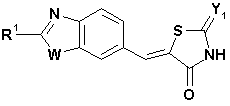 , (Ic)
, (Ic)
де W, а також R1 та Y1 відповідають вищенаведеним визначенням.
12. Застосування за будь-яким із п. 9 або п. 10, причому тіазолідинонова похідна конденсованого вінілбензолу має формулу (Id):
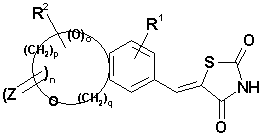 , (Id)
, (Id)
де R1, R2, Z та n відповідають вищенаведеним визначенням; o – 0 або 1;
p – ціле число від 1 до 4 і q – ціле число від 0 до 4.
13. Застосування сполук за будь-яким із п. 9, п. 10 або п. 12, де Z – O, m – 0, n – 1, p – 1 або 2, q – 1, кожний з R1 та R2 відповідає вищенаведеним визначенням.
14. Застосування сполук за будь-яким із п. 9, п. 10 або п. 12, де m – 1, n – 0, p – 1 або 2, q – 0, кожний з R1 та R2 відповідає вищенаведеним визначенням.
15. Застосування за будь-яким із п. 9, п. 10 та пп. 12-14, де m – 0, n – 1, p – 1 або 2, q – 0, кожний з R1 та R2 відповідає визначенню за п. 1.
16. Застосування за будь-яким із п. 9, п. 10 та пп. 12-14, причому R1 є галоген або водень.
17. Застосування за будь-яким із пп. 1-16 для модулювання, зокрема, для пригнічення, активності PI3-кінази.
18. Застосування за п. 17, причому згадана PI3-кіназа є ![]() -кіназою.
-кіназою.
19. Тіазолідинонова похідна конденсованого вінілбензолу формули (II-a)
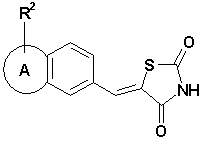 , (II-a)
, (II-a)
де A вибраний з групи, яка складається з діоксолу, діоксину, дигідрофурану, (дигідро)фуранілу, (дигідро)оксазинілу, піридинілу, ізооксазолілу, оксазоліл(дигідро)нафталінілу, піримідинілу, триазолілу, імідазолілу, піразинілу, тіазолідинілу, тіадіазолілу, оксадіазолілу;
R2 вибраний з групи, яка складається або до якої входять H, галоген, ацил, аміногрупа, C1-C6-алкіл, C2-C6-алкеніл, C2-C6-алкініл, C1-C6-алкілкарбоксил, C1-C6-алкілацил, C1-C6-алкілалкоксикарбоніл, C1-C6-алкіламінокарбоніл, C1-C6-алкілацилокси-, C1-C6-алкілациламіно-, C1-C6-алкілуреїдогрупа, C1-C6-алкілкарбамат, C1-C6-алкіламіно-, C1-C6-алкілалкоксигрупа, C1-C6-алкілсульфаніл, C1-C6-алкілсульфініл, C1-C6-алкілсульфоніл, C1-C6-алкілсульфоніламіноарил, арил, C3-C8-циклоалкіл або гетероциклоалкіл, C1-C6-алкіларил, C2-C6-алкеніларил, C2-C6-алкініларил, карбоксил, ціаногрупа, гідроксил, C1-C6-алкокси-, нітро-, ациламіно-, уреїдо-, сульфоніламіногрупа, сульфаніл та сульфоніл.
20. Тіазолідинонова похідна конденсованого вінілбензолу формули (II)
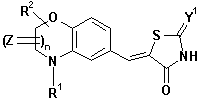 , (II)
, (II)
а також геометричні ізомери, оптично активні форми, наприклад, енантіомери, діастереомери та рацемічні форми, а також фармацевтично прийнятні солі та фармацевтично активні похідні цієї сполуки, де:
Z, Y1, R1, R2 відповідають вищенаведеним визначенням, n – 0 або 1.
21. Тіазолідинонова похідна конденсованого вінілбензолу за п. 20, де Y1
є O.
22. Тіазолідинонова похідна конденсованого вінілбензолу за будь-яким із п. 20 або п. 21, де R1 вибраний з групи, яка складається з C1-C6-алкілу, C1-C6-алкіларилу, арилу, C3-C8-циклоалкілу або гетероциклоалкілу, C1-C6-алкіларилу, C2-C6-алкеніларилу та C2-C6-алкініларилу.
23. Тіазолідинонова похідна конденсованого вінілбензолу за формулою (III)
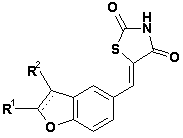 , (III)
, (III)
а також геометричні ізомери, оптично активні форми, наприклад, енантіомери, діастереомери та рацемічні форми, а також фармацевтично прийнятні солі та фармацевтично активні похідні цієї сполуки,
де R1 та R2 відповідають вищенаведеному визначенню.
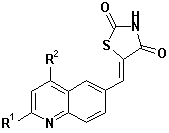
24. Тіазолідинонова похідна конденсованого вінілбензолу за будь-якою з формул (IV), (V) та (VI)
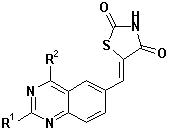 ,
,
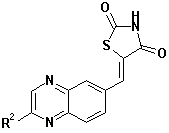 ,
,
 ,
,
(IV)
(V)
(VI)
де R1 вибраний з групи, яка складається з водню, галогену, ціаногрупи, C1-C6-алкілу, C1-C6-алкоксигрупи, ацилу, алкоксикарбонілу, в той час як R2 відповідає вищенаведеному визначенню.
25. Тіазолідинонова похідна конденсованого вінілбензолу за будь-яким із пп. 19-24, вибрана з групи, яка складається з:
5-(1,3-бензодіоксол-5-ілметилен)-1,3-тіазолідин-2,4-діону;
5-(1,3-бензодіоксол-5-ілметилен)-2-тіоксо-1,3-тіазолідин-4-ону;
5-(2,3-дигідро-1,4-бензодіоксин-6-ілметилен)-1,3-тіазолідин-2,4-діону;
5-(2,3-дигідро-1-бензофуран-5-ілметилен)-1,3-тіазолідин-2,4-діону;
5-[(7-метокси-1,3-бензодіоксол-5-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-[(9,10-діоксо-9,10-дигідроантрацен-2-іл)метилен]-1,3-тіазолідин-2,4-діону;
(5-[(2,2-дифтор-1,3-бензодіоксол-5-іл)метилен]-1,3-тіазолідин-2,4-діону;
(5Z)-5-(1,3-дигідро-2-бензофуран-5-ілметилен)-1,3-тіазолідин-2,4-діону;
5-(1-бензофуран-5-ілметилен)-1,3-тіазолідин-2,4-діону;
5-[(4-метил-3-оксо-3,4-дигідро-2H-1,4-бензоксазин-6-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-(1,3-бензодіоксол-5-ілметилен)-2-іміно-1,3-тіазолідин-4-ону;
5-хінолін-6-ілметилентіазолідин-2,4-діону;
5-хінолін-6-ілметилен-2-тіоксотіазолідин-4-ону;
2-іміно-5-хінолін-6-ілметилентіазолідин-4-ону;
5-(3-метилбензо[d]ізоксазол-5-ілметилен)тіазолідин-2,4-діону;
5-(4-фенілхіназолін-6-ілметилен)тіазолідин-2,4-діону;
5-(4-диметиламінохіназолін-6-ілметилен)тіазолідин-2,4-діону;
5-[(4-амінохіназолін-6-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-[(4-піперидин-1-ілхіназолін-6-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-[(4-морфолін-4-ілхіназолін-6-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-{[4-(бензиламіно)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-{[4-(діетиламіно)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-({4-[(піридин-2-ілметил)аміно]хіназолін-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({4-[(піридин-3-ілметил)аміно]хіназолін-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
етил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]хіназолін-4-іл}піперидин-3-карбоксилату;
етил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]хіназолін-4-іл}піперидин-4-карбоксилату;
трет-бутил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]хіназолін-4-іл}-L-пролінату;
5-{[4-(4-метилпіперазин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-{[4-(4-піримідин-2-ілпіперазин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-({4-[4-(4-фторфеніл)піперидин-1-іл]хіназолін-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-{[4-(4-бензилпіперидин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-({4-[4-(2-фенілетил)піперидин-1-іл]хіназолін-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-{[4-(4-метилпіперидин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-{[4-(4-гідроксипіперидин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
1-[6-(2,4-діоксотіазолідин-5-іліденметил)хіназолін-4-іл]піперидин-4-карбонової кислоти;
1-[6-(2,4-діоксотіазолідин-5-іліденметил)хіназолін-4-іл]піперидин-3-карбонової кислоти;
1-[6-(2,4-діоксотіазолідин-5-іліденметил)хіназолін-4-іл]піролідин-2-карбонової кислоти;
5-(4-метиламінохіназолін-6-ілметилен)тіазолідин-2,4-діону;
5-(4-метоксихіназолін-6-ілметилен)тіазолідин-2,4-діону;
2-іміно-5-(4-метиламінохіназолін-6-ілметилен)тіазолідин-4-ону;
2-іміно-5-(4-піперидинхіназолін-6-ілметилен)тіазолідин-4-ону;
2-іміно-5-(4-диметиламінохіназолін-6-ілметилен)тіазолідин-4-ону;
5-(2-метил-2H-бензотриазол-5-ілметилен)тіазолідин-2,4-діону;
5-(3-метил-3H-бензотриазол-5-ілметилен)тіазолідин-2,4-діону;
5-(3-етил-3H-бензимідазол-5-ілметилен)тіазолідин-2,4-діону;
5-{[1-(4-фенілбутил)-1H-бензимідазол-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-[(1-проп-2-ін-1-іл-1H-бензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-[(1-{2-[4-(трифторметил)феніл]етил}-1H-бензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-({1-[2-(4-гідроксифеніл)етил]-1H-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
метил-4-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1H-бензимідазол-1-іл}циклогексанкарбоксилату;
5-({1-[2-(5-метокси-1H-індол-3-іл)етил]-1H-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({1-[(1-метил-1H-піразол-4-іл)метил]-1H-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({1-[2-(3,4-диметоксифеніл)етил]-1H-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({1-[2-(4-феноксифеніл)етил]-1H-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({1-[4-(трифторметил)бензил]-1H-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
4-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1H-бензимідазол-1-іл}циклогексанкарбонової кислоти;
5-[(1-ізобутил-1H-бензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-({1-[2-(1,3-бензодіоксол-4-іл)етил]-1H-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({1-[2-(2-феноксифеніл)етил]-1H-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-{[1-(3,3-дифенілпропіл)-1H-бензимідазол-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-{[1-(2-метоксибензил)-1H-бензимідазол-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-{[1-(3-фурилметил)-1H-бензимідазол-6-іл]метилен}-1,3-тіазолідин-2,4-діону;
5-[(1-пропіл-1H-бензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4-діону;
5-хіноксалін-6-ілметилентіазолідин-2,4-діону;
5-хіноксалін-6-ілметилен-2-тіоксотіазолідин-4-ону;
2-іміно-5-хіноксалін-6-ілметилентіазолідин-4-ону;
5-бензотіазол-6-ілметилентіазолідин-2,4-діону;
5-(3-метилбензофуран-5-ілметилен)тіазолідин-2,4-діону;
5-(2-бром-3-метилбензофуран-5-ілметилен)тіазолідин-2,4-діону;
5-(3-бромбензофуран-5-ілметилен)тіазолідин-2,4-діону;
етилового складного ефіру 3-[5-(2,4-діоксотіазолідин-5-іліденметил)бензофуран-3-іл]акрилової кислоти;
3-[5-(2,4-діоксотіазолідин-5-іліденметил)бензофуран-3-іл]акрилової кислоти;
5-[3-(3-оксо-3-піперидин-1-ілпропеніл)бензофуран-5-ілметилен]тіазолідин-2,4-діону;
метил-1-(3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)пролінату;
метил-1-(3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)-D-пролінату;
5-({3-[3-оксо-3-піролідин-1-ілпроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({3-[3-морфолін-4-іл-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону;
метил-1-(3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)-L-пролінату;
N-циклогексил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}-N-метилакриламіду;
3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}-N-етил-N-(2-гідроксіетил)акриламіду;
N-циклобутил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}акриламіду;
5-({3-[3-азетидин-1-іл-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({3-[3-(1,3-дигідро-2H-ізоіндол-2-іл)-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону;
5-({3-[3-азепан-1-іл-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону;
3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}-N-піперидин-1-ілакриламіду;
3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}-N-(піридин-3-ілметил)акриламіду;
N-циклогексил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}акриламіду;
5-({3-[3-(4-метилпіперазин-1-іл)-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону;
N-циклогептил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}акриламіду;
5-({3-[3-(2,5-дигідро-1H-пірол-1-іл)-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону;
N-циклопентил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}акриламіду;
етилового складного ефіру 3-[5-(2,4-діоксотіазолідин-5-іліденметил)бензофуран-3-іл]пропіонової кислоти;
3-[5-(2,4-діоксотіазолідин-5-іліденметил)бензофуран-3-іл]пропіонової кислоти;
5-[3-(3-оксо-3-піперидин-1-ілпропіл)бензофуран-5-ілметилен]тіазолідин-2,4-діону;
трет-бутилового складного ефіру 6-(2,4-діоксотіазолідин-5-іліденметил)-2,3-дигідробензо[1,4]оксазин-4-карбонової кислоти;
5-(3,4-дигідро-2H-бензо[1,4]оксазин-6-ілметилен)тіазолідин-2,4-діону;
5-(4-бензоїл-3,4-дигідро-2H-бензо[1,4]оксазин-6-ілметилен)тіазолідин-2,4-діону;
5-(4-ацетил-3,4-дигідро-2H-бензо[1,4]оксазин-6-ілметилен)тіазолідин-2,4-діону;
трет-бутилового складного ефіру 6-(2,4-діоксотіазолідин-5-іліденметил)бензо[1,4]оксазин-4-карбонової кислоти;
метилового складного ефіру [6-(2,4-діоксотіазолідин-5-іліденметил)-3-оксо-2,3-дигідробензо[1,4]-оксазин-4-іл]оцтової кислоти;
N-бензил-2-[6-(2,4-діоксотіазолідин-5-іліденметил)-3-оксо-2,3-дигідробензо[1,4]оксазин-4-іл]ацетаміду;
5-(4-бутил-3-оксо-3,4-дигідро-2H-бензо[1,4]оксазин-6-ілметилен)тіазолідин-2,4-діону;
5-(4-бензил-3-оксо-3,4-дигідро-2H-бензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4-діону;
5-(2-хлорбензофуран-5-ілметилен)тіазолідин-2,4-діону;
5-(3-амінобензо[d]ізоксазол-5-ілметилен)тіазолідин-2,4-діону;
5-(3-фенілетинілбензофуран-5-ілметилен)тіазолідин-2,4-діону;
5-бензо[1,2,5]тіадіазол-5-ілметилентіазолідин-2,4-діону;
5-бензо[1,2,5]оксадіазол-5-ілметилентіазолідин-2,4-діону;
5-(2-метилбензофуран-6-ілметилен)тіазолідин-2,4-діону;
5-(2-карбоксиметилбензофуран-6-ілметилен)тіазолідин-2,4-діону;
5-(3-бром-2-фтор-2,3-дигідробензофуран-6-ілметилен)тіазолідин-2,4-діону;
5-(2-фтор-бензофуран-6-ілметилен)тіазолідин-2,4-діону.
26. Тіазолідинонова похідна конденсованого вінілбензолу за будь-яким із пп. 19-25 для застосування як лікарського засобу.
27. Фармацевтична композиція, що містить принаймні одну тіазолідинонову похідну конденсованого вінілбензолу за будь-яким із пп. 19-25 та фармацевтично прийнятні носій, розріджувач або допоміжну речовину.
28. Застосування тіазолідинонової похідної конденсованого вінілбензолу за будь-яким із пп. 19-25 для виготовлення лікарського засобу для профілактики та/або лікування автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, агрегації тромбоцитів, раку, відторгнення трансплантата або травм легенів.
29. Застосування тіазолідинонової похідної конденсованого вінілбензолу за п. 28, причому згадане захворювання вибране з групи, до якої входять розсіяний склероз, псоріаз, ревматоїдний артрит, системний червоний вовчак, запальне захворювання кишок, запалення легенів, тромбоз та інфекційне захворювання чи запалення мозку, наприклад, менінгіт або енцефаліт.
30. Застосування тіазолідинонової похідної конденсованого вінілбензолу за п. 28, де згадане захворювання вибране з групи, до якої входять хвороба Альцгеймера, хорея Гентінгтона, травма центральної нервової системи, інсульт та ішемічні стани.
31. Застосування тіазолідинонової похідної конденсованого вінілбензолу за п. 28, причому згадане захворювання вибране з групи, до якої входять атеросклероз, гіпертрофія серця, дисфункція серцевого міоцита, підвищений кров’яний тиск та судинозвуження.
32. Застосування тіазолідинонової похідної конденсованого вінілбензолу за п. 28, причому згадане захворювання вибрано з групи, до якої входять хронічне обструктивне легеневе захворювання, фіброзний анафілактичний шок, псоріаз, алергічні захворювання, астма, інсульт або ішемічні стани, ішемія-реперфузія, агрегація/активація тромбоцитів, атрофія/гіпертрофія скелетного м’яза, рекрутмент лейкоцитів у раковій тканині, ангіогенез, метастазування пухлин, зокрема, меланоми, саркоми Капоші, гострі та хронічні бактеріальні та вірусні інфекції, сепсис, відторгнення трансплантата, панкреатит, множинна недостатність органів, гломерулосклероз, гломерулонефрит, прогресивний нирковий фіброз, ендотеліальні та епітеліальні травми легенів і генералізоване запалення легеневих дихальних шляхів.
33. Застосування за будь-яким із пп. 28-32 для модулювання, особливо пригнічення, активності PI3-кінази.
34. Застосування за п. 33, де згаданою PI3-кіназою є ![]() -кіназа.
-кіназа.
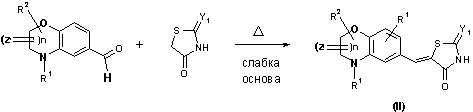
35. Спосіб одержання тіазолідинонових похідних конденсованих вінілбензолів формули (I) за п. 20, який включає такі стадії:
 ,
,
де R1, R2, Y1, Z та n відповідають вищенаведеним визначенням.
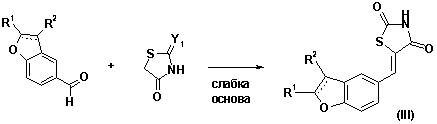
36. Спосіб одержання тіазолідинонових похідних конденсованих вінілбензолів формули (III) за п. 23, який включає такі стадії:
 ,
,
де R1, R2 та Y1 відповідають вищенаведеним визначенням.
Текст
1. Застосування сполуки формули (I) 2 (19) 1 3 79793 алкіламіно-, C1-C6-алкілалкоксигрупа, C1-C6алкілсульфаніл, C1-C6-алкілсульфініл, C1-C6алкілсульфоніл, C1-C6-алкілсульфоніламіноарил, арил, C3-C8-циклоалкіл або гетероциклоалкіл, C1-C6-алкіларил, C2-C6-алкеніларил, C2-C6алкініларил, карбокси-, ціаногрупа, гідроксил, C1C6-алкокси-, нітро-, ациламіно-, уреїдогрупа, C1-C6алкілкарбамат, сульфоніламіногрупа, сульфаніл та сульфоніл; n – 0, 1 або 2; за винятком вказаних нижче сполук: R N 8. Застосування сполук за будь-яким із попередніх пунктів, причому X є S, кожен з Y1 та Y2 є O, R1 та R2 відповідають вищенаведеним визначенням та n є 0. 9. Застосування за будь-яким із попередніх пунктів, причому згадана тіазолідинонова похідна конденсованого вінілбензолу має формулу (Ia) 2 R O S O S , 1 R Y S NH , (TE) (JA) де R1 є нижчий алкіл або аралкіл і R 2 є H або галоген, для виготовлення лікарського засобу для профілактики та/або лікування автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, агрегації тромбоцитів, раку, відторгнення трансплантата або травм легенів. 2. Застосування сполуки за п.1, причому згадане захворювання вибране з групи, до якої входять розсіяний склероз, псоріаз, ревматоїдний артрит, системний червоний вовчак, запальне захворювання кишок, запалення легенів, тромбоз або інфекційне захворювання чи запалення мозку, наприклад, менінгіт або енцефаліт. 3. Застосування сполуки за п.1, причому згадане захворювання вибране з групи, до якої входять хвороба Альцгеймера, хорея Гентінгтона, травма центральної нервової системи, інсульт та ішемічні стани. 4. Застосування сполуки за п.1, причому згадане захворювання вибране з групи, до якої входять атеросклероз, гіпертрофія серця, дисфункція серцевого міоцита, підвищений кров’яний тиск та судинозвуження. 5. Застосування сполуки за п.1, причому згадане захворювання вибране з групи, до якої входять хронічне обструктивне легеневе захворювання, фіброзний анафілактичний шок, псоріаз, алергічні захворювання, астма, інсульт або ішемічні стани, ішемія-реперфузія, агрегація/активація тромбоцитів, атро фія/гіпертрофія скелетного м’яза, рекрутмент лейкоцитів у раковій тканині, панкреатит, множинна недостатність органів, ангіогенез, метастазування пухлин, зокрема, меланоми, саркоми Капоші, гострі та хронічні бактеріальні та вірусні інфекції, сепсис, відторгнення трансплантата, гломерулосклероз, гломерулонефрит, прогресивний нирковий фіброз, ендотеліальні та епітеліальні травми легенів і генералізоване запалення легеневих дихальних шляхів. 6. Застосування за будь-яким із попередніх пунктів, причому кожен з Y1 та Y2 є кисень. 7. Застосування за будь-яким із попередніх пунктів, причому n є 1 або 2 і кожен із R1 та R2 є H. 1 S NH (W)m (CH2)q NH H N 2 (V)o G )n (Z O 1 R O 4 O , (Ia) де Y1 , R1 , R2, Z та n відповідають вищенаведеним визначенням; кожний з V та W незалежно від іншого є O, S або NR3, де R3 є H або C1-C6-алкіл; G є C1-C5-алкіленова або C1-C5-алкеніленова група; кожний з o та m незалежно від іншого є 0 або 1; q – ціле число від 0 до 4. 10. Застосування за п.9, причому згадана тіазолідинонова похідна конденсованого вінілбензолу має формулу (Ib) 2 R (CH2) p (Z (V)o 1 R Y 1 S )n NH (W)m (CH2)q O , (Ib) де Y1, R1 , R2, V, Z, W, m, n, o, q відповідають вищенаведеним визначенням і p – ціле число від 1 до 4. 11. Застосування за будь-яким із п.9 або п.10, причому згадана тіазолідинонова похідна конденсованого вінілбензолу має формулу (Ic) R Y1 N 1 S W NH O , (Ic) де W, а також R1 та Y1 відповідають вищенаведеним визначенням. 12. Застосування за будь-яким із п.9 або п.10, причому тіазолідинонова похідна конденсованого вінілбензолу має формулу (Id): R 2 (O)o (CH 2 )p O 1 O S )n (Z R (CH 2) q NH O , (Id) де R1, R2, Z та n відповідають вищенаведеним визначенням; o – 0 або 1; p – ціле число від 1 до 4 і q – ціле число від 0 до 4. 13. Застосування сполук за будь-яким із п.9, п.10 або п.12, де Z – O, m – 0, n – 1, p – 1 або 2, q – 1, кожний з R1 та R2 відповідає вищенаведеним визначенням. 14. Застосування сполук за будь-яким із п.9, п.10 або п.12, де m – 1, n – 0, p – 1 або 2, q – 0, кожний 5 79793 з R1 та R2 відповідає вищенаведеним визначенням. 15. Застосування за будь-яким із п.9, п.10 та пп.1214, де m – 0, n – 1, p – 1 або 2, q – 0, кожний з R 1 та R2 відповідає визначенню за п.1. 16. Застосування за будь-яким із п.9, п.10 та пп.1214, причому R1 є галоген або водень. 17. Застосування за будь-яким із пп.1-16 для модулювання, зокрема, для пригнічення, активності PI3-кінази. 18. Застосування за п.17, причому згадана PI3кіназа є PI3γ -кіназою. 19. Тіазолідинонова похідна конденсованого вінілбензолу формули (II-a) R 2 O S A 6 23. Тіазолідинонова похідна конденсованого вінілбензолу за формулою (III) O S R 1 O , (III) а також геометричні ізомери, оптично активні форми, наприклад, енантіомери, діастереомери та рацемічні форми, а також фармацевтично прийнятні солі та фармацевтично активні похідні цієї сполуки, де R1 та R2 відповідають вищенаведеному визначенню. 24. Тіазолідинонова похідна конденсованого вінілбензолу за будь-якою з формул (IV), (V) та (VI) O O O , (II-a) де A вибраний з групи, яка складається з діоксолу, діоксину, дигідрофурану, (дигідро)фуранілу, (дигідро)оксазинілу, піридинілу, ізооксазолілу, оксазоліл(дигідро)нафталінілу, піримідинілу, триазолілу, імідазолілу, піразинілу, тіазолідинілу, тіадіазолілу, оксадіазолілу; R2 вибраний з групи, яка складається або до якої входять H, галоген, ацил, аміногрупа, C1-C6-алкіл, C2-C6-алкеніл, C2-C6-алкініл, C1-C6-алкілкарбоксил, C1-C6-алкілацил, C1-C6-алкілалкоксикарбоніл, C1C6-алкіламінокарбоніл, C1-C6-алкілацилокси-, C1C6-алкілациламіно-, C1-C6-алкілуреїдогрупа, C1-C6алкілкарбамат, C1-C6-алкіламіно-, C1-C6алкілалкоксигрупа, C1-C6-алкілсульфаніл, C1-C6алкілсульфініл, C1-C6-алкілсульфоніл, C1-C6алкілсульфоніламіноарил, арил, C3-C8-циклоалкіл або гетероциклоалкіл, C1-C6-алкіларил, C2-C6алкеніларил, C2-C6-алкініларил, карбоксил, ціаногрупа, гідроксил, C1-C6-алкокси-, нітро-, ациламіно-, уреїдо-, сульфоніламіногрупа, сульфаніл та сульфоніл. 20. Тіазолідинонова похідна конденсованого вінілбензолу формули (II) (Z 2 O Y 1 S )n NH N 1 O R2 NH R H N O R , (II) а також геометричні ізомери, оптично активні форми, наприклад, енантіомери, діастереомери та рацемічні форми, а також фармацевтично прийнятні солі та фармацевтично активні похідні цієї сполуки, де: Z, Y1 , R1, R2 відповідають вищенаведеним визначенням, n – 0 або 1. 21. Тіазолідинонова похідна конденсованого вінілбензолу за п.20, де Y1 є O. 22. Тіазолідинонова похідна конденсованого вінілбензолу за будь-яким із п.20 або п.21, де R1 вибраний з групи, яка складається з C1-C6-алкілу, C1C6-алкіларилу, арилу, C3-C8-циклоалкілу або гетероциклоалкілу, C1-C6-алкіларилу, C2-C6алкеніларилу та C2-C6-алкініларилу. 2 R H N S S O 1 2 R N , N , (V) (IV) O R R 1 O N N R H N S 2 , H N O N (VI) де R1 вибраний з групи, яка складається з водню, галогену, ціаногрупи, C1-C6-алкілу, C1-C6алкоксигрупи, ацилу, алкоксикарбонілу, в той час як R2 відповідає вищенаведеному визначенню. 25. Тіазолідинонова похідна конденсованого вінілбензолу за будь-яким із пп.19-24, вибрана з групи, яка складається з: 5-(1,3-бензодіоксол-5-ілметилен)-1,3-тіазолідин2,4-діону; 5-(1,3-бензодіоксол-5-ілметилен)-2-тіоксо-1,3тіазолідин-4-ону; 5-(2,3-дигідро-1,4-бензодіоксин-6-ілметилен)-1,3тіазолідин-2,4-діону; 5-(2,3-дигідро-1-бензофуран-5-ілметилен)-1,3тіазолідин-2,4-діону; 5-[(7-метокси-1,3-бензодіоксол-5-іл)метилен]-1,3тіазолідин-2,4-діону; 5-[(9,10-діоксо-9,10-дигідроантрацен-2іл)метилен]-1,3-тіазолідин-2,4-діону; (5-[(2,2-дифтор-1,3-бензодіоксол-5-іл)метилен]-1,3тіазолідин-2,4-діону; (5Z)-5-(1,3-дигідро-2-бензофуран-5-ілметилен)-1,3тіазолідин-2,4-діону; 5-(1-бензофуран-5-ілметилен)-1,3-тіазолідин-2,4діону; 5-[(4-метил-3-оксо-3,4-дигідро-2H-1,4-бензоксазин6-іл)метилен]-1,3-тіазолідин-2,4-діону; 5-(1,3-бензодіоксол-5-ілметилен)-2-іміно-1,3тіазолідин-4-ону; 5-хінолін-6-ілметилентіазолідин-2,4-діону; 5-хінолін-6-ілметилен-2-тіоксотіазолідин-4-ону; 7 2-іміно-5-хінолін-6-ілметилентіазолідин-4-ону; 5-(3-метилбензо[d]ізоксазол-5ілметилен)тіазолідин-2,4-діону; 5-(4-фенілхіназолін-6-ілметилен)тіазолідин-2,4діону; 5-(4-диметиламінохіназолін-6ілметилен)тіазолідин-2,4-діону; 5-[(4-амінохіназолін-6-іл)метилен]-1,3-тіазолідин2,4-діону; 5-[(4-піперидин-1-ілхіназолін-6-іл)метилен]-1,3тіазолідин-2,4-діону; 5-[(4-морфолін-4-ілхіназолін-6-іл)метилен]-1,3тіазолідин-2,4-діону; 5-{[4-(бензиламіно)хіназолін-6-іл]метилен}-1,3тіазолідин-2,4-діону; 5-{[4-(діетиламіно)хіназолін-6-іл]метилен}-1,3тіазолідин-2,4-діону; 5-({4-[(піридин-2-ілметил)аміно]хіназолін-6іл}метилен)-1,3-тіазолідин-2,4-діону; 5-({4-[(піридин-3-ілметил)аміно]хіназолін-6іл}метилен)-1,3-тіазолідин-2,4-діону; етил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]хіназолін-4-іл}піперидин-3карбоксилату; етил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]хіназолін-4-іл}піперидин-4карбоксилату; трет-бутил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]хіназолін-4-іл}-L-пролінату; 5-{[4-(4-метилпіперазин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону; 5-{[4-(4-піримідин-2-ілпіперазин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону; 5-({4-[4-(4-фторфеніл)піперидин-1-іл]хіназолін-6іл}метилен)-1,3-тіазолідин-2,4-діону; 5-{[4-(4-бензилпіперидин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону; 5-({4-[4-(2-фенілетил)піперидин-1-іл]хіназолін-6іл}метилен)-1,3-тіазолідин-2,4-діону; 5-{[4-(4-метилпіперидин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону; 5-{[4-(4-гідроксипіперидин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону; 1-[6-(2,4-діоксотіазолідин-5-іліденметил)хіназолін4-іл]піперидин-4-карбонової кислоти; 1-[6-(2,4-діоксотіазолідин-5-іліденметил)хіназолін4-іл]піперидин-3-карбонової кислоти; 1-[6-(2,4-діоксотіазолідин-5-іліденметил)хіназолін4-іл]піролідин-2-карбонової кислоти; 5-(4-метиламінохіназолін-6-ілметилен)тіазолідин2,4-діону; 5-(4-метоксихіназолін-6-ілметилен)тіазолідин-2,4діону; 2-іміно-5-(4-метиламінохіназолін-6ілметилен)тіазолідин-4-ону; 2-іміно-5-(4-піперидинхіназолін-6ілметилен)тіазолідин-4-ону; 2-іміно-5-(4-диметиламінохіназолін-6ілметилен)тіазолідин-4-ону; 5-(2-метил-2H-бензотриазол-5ілметилен)тіазолідин-2,4-діону; 5-(3-метил-3H-бензотриазол-5ілметилен)тіазолідин-2,4-діону; 5-(3-етил-3H-бензимідазол-5ілметилен)тіазолідин-2,4-діону; 79793 8 5-{[1-(4-фенілбутил)-1H-бензимідазол-6іл]метилен}-1,3-тіазолідин-2,4-діону; 5-[(1-проп-2-ін-1-іл-1H-бензимідазол-6-іл)метилен]1,3-тіазолідин-2,4-діону; 5-[(1-{2-[4-(трифторметил)феніл]етил}-1Hбензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4діону; 5-({1-[2-(4-гідроксифеніл)етил]-1H-бензимідазол-6іл}метилен)-1,3-тіазолідин-2,4-діону; метил-4-{6-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1H-бензимідазол-1іл}циклогексанкарбоксилату; 5-({1-[2-(5-метокси-1H-індол-3-іл)етил]-1Hбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону; 5-({1-[(1-метил-1H-піразол-4-іл)метил]-1Hбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону; 5-({1-[2-(3,4-диметоксифеніл)етил]-1Hбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону; 5-({1-[2-(4-феноксифеніл)етил]-1H-бензимідазол-6іл}метилен)-1,3-тіазолідин-2,4-діону; 5-({1-[4-(трифторметил)бензил]-1H-бензимідазол6-іл}метилен)-1,3-тіазолідин-2,4-діону; 4-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1Hбензимідазол-1-іл}циклогексанкарбонової кислоти; 5-[(1-ізобутил-1H-бензимідазол-6-іл)метилен]-1,3тіазолідин-2,4-діону; 5-({1-[2-(1,3-бензодіоксол-4-іл)етил]-1Hбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону; 5-({1-[2-(2-феноксифеніл)етил]-1H-бензимідазол-6іл}метилен)-1,3-тіазолідин-2,4-діону; 5-{[1-(3,3-дифенілпропіл)-1H-бензимідазол-6іл]метилен}-1,3-тіазолідин-2,4-діону; 5-{[1-(2-метоксибензил)-1H-бензимідазол-6іл]метилен}-1,3-тіазолідин-2,4-діону; 5-{[1-(3-фурилметил)-1H-бензимідазол-6іл]метилен}-1,3-тіазолідин-2,4-діону; 5-[(1-пропіл-1H-бензимідазол-6-іл)метилен]-1,3тіазолідин-2,4-діону; 5-хіноксалін-6-ілметилентіазолідин-2,4-діону; 5-хіноксалін-6-ілметилен-2-тіоксотіазолідин-4-ону; 2-іміно-5-хіноксалін-6-ілметилентіазолідин-4-ону; 5-бензотіазол-6-ілметилентіазолідин-2,4-діону; 5-(3-метилбензофуран-5-ілметилен)тіазолідин-2,4діону; 5-(2-бром-3-метилбензофуран-5ілметилен)тіазолідин-2,4-діону; 5-(3-бромбензофуран-5-ілметилен)тіазолідин-2,4діону; етилового складного ефіру 3-[5-(2,4діоксотіазолідин-5-іліденметил)бензофуран-3іл]акрилової кислоти; 3-[5-(2,4-діоксотіазолідин-5іліденметил)бензофуран-3-іл]акрилової кислоти; 5-[3-(3-оксо-3-піперидин-1-ілпропеніл)бензофуран5-ілметилен]тіазолідин-2,4-діону; метил-1-(3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}проп-2еноїл)пролінату; метил-1-(3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)-Dпролінату; 9 79793 5-({3-[3-оксо-3-піролідин-1-ілпроп-1-ен-1-іл]-1бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону; 5-({3-[3-морфолін-4-іл-3-оксопроп-1-ен-1-іл]-1бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону; метил-1-(3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)-Lпролінату; N-циклогексил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}-Nметилакриламіду; 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1бензофуран-3-іл}-N-етил-N-(2гідроксіетил)акриламіду; N-циклобутил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}акриламіду; 5-({3-[3-азетидин-1-іл-3-оксопроп-1-ен-1-іл]-1бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону; 5-({3-[3-(1,3-дигідро-2H-ізоіндол-2-іл)-3-оксопроп-1ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3тіазолідин-2,4-діону; 5-({3-[3-азепан-1-іл-3-оксопроп-1-ен-1-іл]-1бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону; 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1бензофуран-3-іл}-N-піперидин-1-ілакриламіду; 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1бензофуран-3-іл}-N-(піридин-3ілметил)акриламіду; N-циклогексил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}акриламіду; 5-({3-[3-(4-метилпіперазин-1-іл)-3-оксопроп-1-ен-1іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4діону; N-циклогептил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}акриламіду; 5-({3-[3-(2,5-дигідро-1H-пірол-1-іл)-3-оксопроп-1ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3тіазолідин-2,4-діону; N-циклопентил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}акриламіду; етилового складного ефіру 3-[5-(2,4діоксотіазолідин-5-іліденметил)бензофуран-3іл]пропіонової кислоти; 3-[5-(2,4-діоксотіазолідин-5іліденметил)бензофуран-3-іл]пропіонової кислоти; 5-[3-(3-оксо-3-піперидин-1-ілпропіл)бензофуран-5ілметилен]тіазолідин-2,4-діону; трет-бутилового складного ефіру 6-(2,4діоксотіазолідин-5-іліденметил)-2,3дигідробензо[1,4]оксазин-4-карбонової кислоти; 5-(3,4-дигідро-2H-бензо[1,4]оксазин-6ілметилен)тіазолідин-2,4-діону; 5-(4-бензоїл-3,4-дигідро-2H-бензо[1,4]оксазин-6ілметилен)тіазолідин-2,4-діону; 5-(4-ацетил-3,4-дигідро-2H-бензо[1,4]оксазин-6ілметилен)тіазолідин-2,4-діону; трет-бутилового складного ефіру 6-(2,4діоксотіазолідин-5-іліденметил)бензо[1,4]оксазин4-карбонової кислоти; метилового складного ефіру [6-(2,4діоксотіазолідин-5-іліденметил)-3-оксо-2,3дигідробензо[1,4]-оксазин-4-іл]оцтової кислоти; N-бензил-2-[6-(2,4-діоксотіазолідин-5-іліденметил)3-оксо-2,3-дигідробензо[1,4]оксазин-4іл]ацетаміду; 10 5-(4-бутил-3-оксо-3,4-дигідро-2Hбензо[1,4]оксазин-6-ілметилен)тіазолідин-2,4діону; 5-(4-бензил-3-оксо-3,4-дигідро-2Hбензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4діону; 5-(2-хлорбензофуран-5-ілметилен)тіазолідин-2,4діону; 5-(3-амінобензо[d]ізоксазол-5ілметилен)тіазолідин-2,4-діону; 5-(3-фенілетинілбензофуран-5ілметилен)тіазолідин-2,4-діону; 5-бензо[1,2,5]тіадіазол-5-ілметилентіазолідин-2,4діону; 5-бензо[1,2,5]оксадіазол-5-ілметилентіазолідин2,4-діону; 5-(2-метилбензофуран-6-ілметилен)тіазолідин-2,4діону; 5-(2-карбоксиметилбензофуран-6ілметилен)тіазолідин-2,4-діону; 5-(3-бром-2-фтор-2,3-дигідробензофуран-6ілметилен)тіазолідин-2,4-діону; 5-(2-фтор-бензофуран-6-ілметилен)тіазолідин-2,4діону. 26. Тіазолідинонова похідна конденсованого вінілбензолу за будь-яким із пп.19-25 для застосування як лікарського засобу. 27. Фармацевтична композиція, що містить принаймні одну тіазолідинонову похідну конденсованого вінілбензолу за будь-яким із пп.19-25 та фармацевтично прийнятні носій, розріджувач або допоміжну речовину. 28. Застосування тіазолідинонової похідної конденсованого вінілбензолу за будь-яким із пп.19-25 для виготовлення лікарського засобу для профілактики та/або лікування автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, агрегації тромбоцитів, раку, відторгнення трансплантата або травм легенів. 29. Застосування тіазолідинонової похідної конденсованого вінілбензолу за п.28, причому згадане захворювання вибране з групи, до якої входять розсіяний склероз, псоріаз, ревматоїдний артрит, системний червоний вовчак, запальне захворювання кишок, запалення легенів, тромбоз та інфекційне захворювання чи запалення мозку, наприклад, менінгіт або енцефаліт. 30. Застосування тіазолідинонової похідної конденсованого вінілбензолу за п.28, де згадане захворювання вибране з групи, до якої входять хвороба Альцгеймера, хорея Гентінгтона, травма центральної нервової системи, інсульт та ішемічні стани. 31. Застосування тіазолідинонової похідної конденсованого вінілбензолу за п.28, причому згадане захворювання вибране з групи, до якої входять атеросклероз, гіпертрофія серця, дисфункція серцевого міоцита, підвищений кров’яний тиск та судинозвуження. 32. Застосування тіазолідинонової похідної конденсованого вінілбензолу за п.28, причому згадане захворювання вибрано з групи, до якої входять хронічне обструктивне легеневе захворювання, 11 79793 фіброзний анафілактичний шок, псоріаз, алергічні захворювання, астма, інсульт або ішемічні стани, ішемія-реперфузія, агрегація/активація тромбоцитів, атро фія/гіпертрофія скелетного м’яза, рекрутмент лейкоцитів у раковій тканині, ангіогенез, метастазування пухлин, зокрема, меланоми, саркоми Капоші, гострі та хронічні бактеріальні та вірусні інфекції, сепсис, відторгнення трансплантата, панкреатит, множинна недостатність органів, гломерулосклероз, гломерулонефрит, прогресивний нирковий фіброз, ендотеліальні та епітеліальні травми легенів і генералізоване запалення легеневих дихальних шляхів. 33. Застосування за будь-яким із пп.28-32 для модулювання, особливо пригнічення, активності PI3кінази. 34. Застосування за п.33, де згаданою PI3-кіназою є PI3γ -кіназа. 12 35. Спосіб одержання тіазолідинонових похідних конденсованих вінілбензолів формули (I) за п.20, який включає такі стадії: 2 R O (z z z R1 + R O (z NH O H R 1 Y1 S )n N z слабка основа NH R1 O , де R1, R2, Y1, Z та n відповідають вищенаведеним визначенням. 36. Спосіб одержання тіазолідинонових похідних конденсованих вінілбензолів формули (III) за п.23, який включає такі стадії: (II) 1 R O 2 R O O Y1 S + S 2 NH O H R сла бка осно ва H N O 1 R O (III ) , де R , R та Y відповідають вищенаведеним визначенням. 1 Цей винахід стосується застосування азолідинонових похідних конденсованих вінілбензолів формули (І) для лікування та/або профілактики автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, aгрeгaцiї тромбоцитів, раку, відторгнення трансплантатів або травм легенів. Зокрема, цей винахід стосується заміщених азолідинонових похідних конденсованих вінілбензолів для модулювання, особливо пригнічення, активності або функції сімейства фосфоінозитид-3'ОН-кіназ, РІ3К, особливо РІ3Kg. Передумови створення винаходу Клітинні плазмові мембрани можна розглядати як великий запас вторинних месенджерів, які можуть бути включені в різноманітні шляхи передачі сигналів. Що стосується функції та регулювання ефекторних ферментів у фосфоліпідних шля хах передачі сигналів, то ці ферменти, які генерують вторинні месенджери з депо мембранних фосфоліпідів (РІ3-кінази класу І (наприклад, РІ3Kg)), є ферментами подвійної специфічності, тобто вони діють одночасно як ліпідкінази (фосфорилування фосфоінозитидів), а також як протеїнкінази; показано, що вони здатні також фосфорилувати інші протеїнові субстрати, в тому числі спричиняти авто-фосфорилування як внутрішньомолекулярний регуляторний механізм. Ці ферменти фосфоліпідних сигнальних шляхів активуються у відповідь на різноманітні позаклітинні сигнали, наприклад, фактори росту, мітогени, інтегринові гормони (гормони міжклітинної взаємодії), цитокіни, віруси та нейротрансмітери, як показано, наприклад, нижче на Схемі 1, а також під впливом внутрішньоклітинного перехресного регулювання, спричиненого іншими сигнальними сполуками (перехресна взаємодія, при якій вихідний сигнал може активувати певні паралельні шляхи передачі, які на другій стадії передають сигнали на ферменти РІ3K внаслідок внутрішньоклітинних сигнальних подій), напри O N 2 Y1 S )n 2 1 клад, низькомолекулярними GTP-азами, кіназами або фосфатазами. Внутрішньоклітинний шлях передачі сигналу за участю інозитових фосфоліпідів (фосфоінозитидів) починається зі зв'язування сигнальних молекул (позаклітинних лігандів, подразників, димеризації рецепторів, трансактивації під впливом гетерологічних рецепторів (наприклад, рецептора тирозинкінази)) з інтегрованим у плазмову мембрану трансмембранним рецептором, що має Gпротеїн як місточковий елемент. РІ3K перетворює мембранний фосфоліпід РІР(4,5)2 у РІР(3,4,5)3, який, у свою чергу, може зазнавати подальшого перетворення в іншу 3'-фосфориловану форму фосфоінозитидів під впливом 5'-специфічних фосфоінозитид-фосфатаз; таким чином, ферментна активність РІ3K безпосередньо або непрямим шляхом викликає утворення двох підтипів 3'фосфоінозитидів, котрі діють як вторинні месенджери при внутрішньоклітинній передачі сигналу [Trends Biochem Sci. 22(7) p.267-272 (1997) by Vanhaesebroeck B. et al.; Chem. Rev. 101(8) p.23652380 (2001) by Leslie N.R. et al. (2001); Annu. Rev. Cell. Dev. Biol. 17 p.615-675 (2001) by Katso R. et al.; and Cell. Моl. Life Sci. 59(5) p.761-779 (2002) by Toker A. et al.]. У цій ферментній реакції беруть участь численні ізоформи РІ3K, які класифікуються за відповідними каталітичними субодиницями, за регулюванням під впливом відповідних регуляторних субодиниць, за схемами експресії та за специфічними сигнальними функціями (p110α, β, d та g) [Exp. Cell. Res. 25(1) p.239-254 (1999) by Vanhaesebroeck В.; Annu. Rev. Cell. Dev. Biol. 17 p.615675 (2001) by Katso R. et al.]. Еволюційно стабільні ізоформи pi 10 α та β експресуються майже всіма тканинами; навпаки, ізоформи d та g експресуються більш специфічно в клітинах гематопоетинової системи, клітинах гладких м'язів, міоцитах та в клітинах ендотелію [Trends Biochem. Sci. 22(7) p.267-272 (1997) by Vanhaesebroeck B. et al.]. Можливо, що їхня екс 13 79793 пресія може регулюватися також шляхом індукування, залежно від типу клітин, тканини та подразників, а також від загальної картини захворювання. На даний час у ссавців ідентифіковано вісім кіназ РІ3K, які розділяються на три основних класи (І, II та III) на основі гомологічної послідовності, структури, партнерів зв'язування, способу активації та переважного субстрату in vitro. РІ3K класу І можуть фосфорилувати фосфатидилінозит (РІ), фосфа тидилінозит-4-фосфат та фосфатидилінозит-4,5-дифосфат (РІР2) з утворенням відповідно фосфа тидилінозит-3-фосфату (PIP), фосфатидилінозит-3,4-дифосфату та фосфатидилінозит3,4,5-трифосфату. РІ3K класу II фосфорилують РІ та фосфатидилінозит-4-фосфат. PI3Ks класу III можуть фосфорилувати тільки PI [Trends Biochem. Sci. 22(7) p.267-272 (1997) by Vanhaesebroeck B. et al., Exp . Cell. Res. 25(1) p.239-254 (1999) by Vanhaesebroeck В. та Chem. Rev. 101(8) p.2365-2380 (2001) by Leslie N.R et al. (2001)]. Рецептори, сполучені з G-протеїном, опосередковують активацію фосфоінозитид-3'ОН-кінази через посередництво GTP-аз, наприклад, Gβg та Ras, і, отже, сигнальний шлях за участю РІ3K відкрає центральну роль у встановленні та координуванні полярності клітин та динамічній організації цитоскелету, тобто чинників, які спільно забезпечують рушійну силу руху клітин. Як показано вище на Схемі 1, фосфоінозитид3-кіназа (РІ3K) бере участь у фосфорилуванні фосфатидилінозиту (Ptdlns) по третьому атому вуглецю інозитового циклу. Продукти фосфорилування Ptdlns до 3,4,5-трифосфату (PtdIns(3,4,5)P3), PtdIns(3,4)P2 та PtdIns(3)P діють як вторинні месенджери для різноманітних шляхів передачі сигналів, в тому числі для таких, що мають істотне значення для проліферації клітин, диференціації клітин, росту клітин, розміру клітин, виживання, апоптозу та адгезії клітин, скорочувальної здатності клітин, міграції клітин, хемотаксису, інвазії, перебудови цитоскелету, змін форми клітин, руху 14 везикул та метаболічних шляхів [Annu. Rev. Cell. Dev. Вiol. 17 p.615-675 (2001) by Katso et al. and Мої. Med. Today 6(9) p. 347-357 (2000) by Stein R.C]. Хемотаксис, тобто впорядкований рух клітин у напрямі грaдiєнтa концентрації хімічних атрактантів, що звуться також хемокінами, є складовим елементом у багатьох важливих захворюваннях, наприклад, у запальних та автоімунних розладах, нейродегенерації, ангіогенезі, інвазії пухлин та утворенні метастазів, а також у загоєнні ран [Immunol. Today 21(6) p.260-264 (2000) by Wyman N.P. et al.; Science 287(5455) p.1049-1053 (2000) by Hirsch et al.; FASEB J. 15(11) p.2019-2021 (2001) by Hirsch et al. and Nat. Immunol. 2(2) p.108-115 (2001) by Gerard C. et al.]. Сучасні дослідження з використанням генетичних підходів та фармакологічних засобів забезпечили розуміння сигнальних та молекулярних шляхів, які опосередковують хемотаксис як реакцію на хемоатрактанти активованих рецепторів, приєднаних до G-протеїну. Дія РІ3-кінази, котра відповідає за продукування цих фосфорилованих продуктів, що передають сигнали, спочатку була охарактеризована як активність, пов'язана з вірусними онкопротеїнами та тирозинкіназами рецепторів фактору росту, яка фосфорилює фосфатидилінозит (РІ) та його похідні, фосфориловані по гідроксилу в положенні 3' інозитового циклу [Panayotou et al., Trends Cell. Biol. 2 p.358-360 (1992)]. Проте при пізніших біохімічних дослідженнях було з'ясовано, що РІ3кінази класу І (наприклад, ізоформа РІ3Kg класу IB) є кіназами подвійної специфічності, тобто вони діють одночасно як ліпідкінази (фосфорилування фосфоінозитидів), а також як протеїн-кінази, які виявилися здатними до фосфорилування інших протеїнів як субстратів, в тому числі до авто фосфорилування як до внутрішньомолекулярного регуляторного механізму. Тому вважається, що активація РІ3-кіназ бере участь у різноманітних клітинних реакціях, в тому числі у рості, ди ференціації та апоптозі клітин [Parker et al., Current Biology, 5 p.577-599 (1995), Yao et al., Science, 267 p.2003-2005 (1995)]. Можливо, РІ3-кіназа бере участь у численних аспектах активації лейкоцитів. Показано, що діяльність пов'язаної з р85 РІ3-кінази фізично пов'язана з цитоплазмовою ділянкою CD28, яка є важливим додатковим стимулятором активації Тклітин як реакції на антиген [Pages et al., Nature, 369 p. 327-329 (1994); Rudd, Immunity 4 p.527-534 (1996)]. Активація Т-клітин під впливом CD28 знижує поріг активації антигеном та підвищує інтенсивність та тривалість проліферативної реакції. Ці ефекти пов'язані з транскрипцією численних генів, в тому числі інтерлейкіну-2 (IL2), який є важливим фактором росту Т-клітин [Fraser et al., Science, 251 p.313-316 (1991)]. Мутація CD28, внаслідок якої він може довше взаємодіяти з РІ3-кіназою, викликає втрату здатності ініціювати продукування IL2, що свідчить про вирішальну роль РІ3-кінази в активації Т-клітин. РІ3Kg ідентифіковано як посередник залежного від G-β-g регулювання активності JNK, при цьому G-β та -g є субодиниці гетеротримерних G-протеїнів [J. Biol. Chem. 273(5) p.2505-2508 (1998)]. До клітинних процесів, у яких РІ3-кінази 15 79793 відпрають важливу роль, належать пригнічення апоптозу, реорганізація актинового скелету, ріст кардіоміоцитів, стимуляція глікогенсинтази інсуліном, опосередкований TNFα праймінг та продукування пероксидів, а також міграція лейкоцитів та їхня адгезія до ендотеліальних клітин. Нещодавно [Immunity 16(3) p.441-451 (2002)] описано, що РІ3Kg переключає запальні сигнали через посередництво різноманітних рецепторів, сполучених із G(i), і відкрає ключову роль у функціюванні мастоцитів, стимуляції лейкоцитів, в імунологічних процесах, в яких беруть участь, наприклад, цитокіни, хемокіни, аденозини, антитіла, iнтeгрини, фактори агрeгацiї, фактори росту, віруси або гормони [J. Cell. Sci. 114(Pt 16) p.2903-2910 (2001) by Lawlor M.A. et al., Immunity 16(3) p.441451 (2002) by Laffargue M. et al. and Сurr. Opinion Cell. Biol. 14(2) p.203-213 (2002) by Stephens L. et al.]. Специфічні інгібітори дії окремих членів сімейства ферментів є неоціненними засобами для точного визначення функцій кожного ферменту. Дві сполуки, а саме LY294002 та вортманін (формули яких подано нижче) широко застосовуються як інгібітори РІ3-кіназ. Ці сполуки є неспецифічними інгібіторами РІ3K, оскільки вони не виявляють селективної спорідненості до жодного з чотирьох членів групи РІ3-кіназ класу І. Наприклад, значення ІС 50 для вортманіну відносно кожної з різних РІ3-кіназ класу І лежать у межах від 1нМ до 10нМ. Аналогічно, значення ІС 50 для LY294002 відносно кожної з цих РІ3-кіназ лежать у межах 15-20мкМ [Fruman et al., An. Rev. Biochem., 67 p.481-507 (1998)]. Ці сполуки також виявляють значення ІС 50 5-10мкМ відносно протеїнкінази СK2 та певну інгібувальну дію на фосфоліпази. Вортманін є продуктом метаболізму грибків, який необоротно інгібує активність РІ3K внаслідок ковалентного зв'язування з каталітичним доменом цього ферменту. Інгібування активності РІ3K вортманіном усуває подальшу реакцію клітини на позаклітинний фактор. Наприклад, нейтрофіли реагують на хемокін fMetLeu-Phe (fMLP) шляхом стимулювання РІ3K та синтезу PtdIns(3,4,5)P3. Цей синтез корелює з активацією викиду респіраторів, який бере участь у деструкції сторонніх мікроорганізмів у нейтрофілах. Оброблення нейтрофілів вортманіном запобігає індукованому fMLP реакції респіраторного викиду [Thelen et al. PNAS 91 p.4960-4964 (1994)]. Очевидно, ці експерименти з вортманіном, як і інші експериментальні свідоцтва, показують, що діяльність РІ3K у клітинах гематопоетинової системи, зокрема, у нейтрофілах, моноцитах та інших типах лейкоцитів, є елементом багатьох несенсибілізованих імунних реакцій, пов'язаних із гострими та хронічними запаленнями. Дослідження із застосуванням вортманіну сві 16 дчать, що функціювання РІ3-кіназ потрібне також у деяких аспектах передачі сигнала лейкоцитам через сполучені з G-протеїном рецептори [Thelen et al., Proc. Nail. Acad. Sci. USA, 91 p.4960-4964 (1994)]. Крім того, показано, що вортманін та LY294002 блокують мпрацію нейтрофілів та вивільнення пероксиду. Проте, оскільки ці сполуки не виявляють селективності до конкретних ізоформ РІ3K, залишається неясним, яка саме ізоформа або ізоформи РІ3K беруть участь у ци х явища х. Азолідинонові похідні вінілбензолу, які, проте, обов'язково включають бензимідазольний фрагмент, [описані у WO 02/051409]. Сповіщається, що ці сполуки інгібують теломеразу і є цілеспрямовано корисними при лікуванні раку. Короткий опис винаходу Цей винахід стосується застосування азолідинонових похідних конденсованих вінілбензолів формули (І) (I) де А, X, Υ, Ζ, n, R1 і R2 детально описані у нижченаведеному описі, а також фармацевтично прийнятних солей цих сполук, для виготовлення фармацевтичних композицій для лікування та/або профілактики автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, агрегації тромбоцитів, раку, ускладнень трансплантації, відторгнення трансплантату або травм легенів. Сполуки за цим винаходом є інгібіторами 3-кіназ фосфа то-інозитидів (PI3Ks), особливо гамма-3кінази фосфатоінозитидів (РІ3Kg). На цей час встановлено, що сполуки за цим винаходом є модуляторами 3-кіназ фосфатоінозитидів (PDKs), особливо 3-кінази фосфатоінозитидів (РІ3Kg). Якщо фермент - 3-кіназа фосфатоінозитидів (РІ3K) - пригнічений сполуками за цим винаходом, РІ3K не здатна виявляти свої ферментні, біологічні та/або фармакологічні ефекти. Сполуки за цим винаходом, таким чином, придатні для лікування та запобігання автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, aгрeгaцiї тромбоцитів, раку, ускладнень трансплантації, відторгнення трансплантата та травм легенів. Нижче подано визначення термінів, що означають різноманітні хімічні фрагменти та групи, з яких складаються сполуки за цим винаходом; ці терміни призначені для однозначного застосування в тексті опису та у пунктах формули винаходу, якщо інше подане в явному вигляді визначення не передбачає більш широкого значення. Термін "C1-С6-алкіл" означає одновалентну алкільну гр упу, що містить від 1 атому до 6 атомів вуглецю. Прикладами значень цього терміну є такі групи, як метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, н-гексил тощо. 17 79793 Термін "арил" означає ненасичену ароматичну карбоциклічну грyпy, що містить від 6 атомів до 14 атомів вуглецю і включає один цикл (наприклад, феніл) або кілька конденсованих циклів (наприклад, нафтил). До арилів, яким віддають перевагу, належать феніл, нафтил, фенантрил тощо. Термін "С1-С6-алкіларил" означає С1-С6алкіл, який має арильний замісник, в тому числі бензил, фенетил то що. Термін "гетероарил" означає моноциклічну гетероароматичнугр упу або біциклічну чи трициклічну гетероароматичну гр yпy, що містить конденсовані цикли. До конкретних прикладів гетероароматичних фуп належать факультативно заміщені піридил, піроліл, фурил, тієніл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, піразоліл, 1,2,3-триазоліл, 1,2,4-триазоліл, 1,2,3оксадіазоліл, 1,2,4-оксадіазоліл, 1,2,5оксадіазоліл, 1,3,4-оксадіазоліл, 1,3,4-триазиніл, 1,2,3-триазиніл, бензофурил, [2,3дигідро]бензофурил, ізобензофурил, бензотієніл, бензотриазоліл, ізобензотієніл, індоліл, ізоіндоліл, 3Н-індоліл, бензимідазоліл, імідазо[1,2-а]піридил, бензотіазоліл, бензоксазоліл, хінолізиніл, хіназолініл, фталазиніл, хіноксалініл, цинолініл, нафтиридиніл, піридо[3,4-b]піридил, піридо[3,2-b]піридил, піридо[4,3-b]піридил, хіноліл, ізохіноліл, тетразоліл, 5,6,7,8-тетрагідрохіноліл, 5,6,7,8тетрагідроізохіноліл, пуриніл, птеридиніл, карбазоліл, ксантеніл та бензохіноліл. Термін "С1-С6-алкілгетероарил" означає С1-С6алкільні групи, які мають гетероарильний замісник, в тому числі 2-фурилметил, 2-тієнілметил, 2-(1Ніндол-3-іл)етил тощо. Термін "С1-С6-алкеніл" означає алкенільні групи, які переважно містять від 2 атомів до 6 атомів вуглецю і включають щонайменше 1 ділянку або 2 ділянки алкенільної ненасиченості. До алкенільних груп, яким віддають перевагу, належать етеніл (СН= СН2), н-2-пропеніл (аліл, -СН2СН=СН2) тощо. Термін "С1-С6-алкеніларил" означає С2-С6алкенільні групи, які мають арильний замісник, в тому числі 2-фенілвініл тощо. Термін "С1-С6-алкенілгетероарил" означає С2С6-алкенільні групи, які мають гетероарильний замісник, в тому числі 2-(3-піридиніл)вініл тощо. Термін "С1-С6-алкініл" означає алкінільні групи, які переважно містять від 2 атомів до 6 атомів вуглецю і включають щонайменше 1-2 ділянки алкінільної ненасиченості. До алкінільних грyп, яким віддають перевагу, належать етиніл (-СºСН), пропаргіл (-СH2СºСН) тощо. Термін "С1-С6-алкініларил" означає С2-С6алкінільні грyпи, які мають арильний замісник, в тому числі фенілетиніл тощо. Термін "С1-С6-алкінілгетероарил" означає С2С6-алкінільні групи, які мають гетероарильний замісник, в тому числі 2-тієнілетиніл тощо. Термін "С3-С8-циклоалкіл" означає насичену карбоциклічну фулу, яка містить від 3 атомів до 8 атомів вуглецю і включає один цикл (наприклад, циклогексил) або кілька конденсованих циклів (наприклад, норборніл). До циклоалкілів, яким віддають перевагу, належать циклопентил, циклогексил, норборніл тощо. 18 Термін "гетероциклоалкіл" означає С3-С8циклоалкільну грyп y згідно з поданим вище визначенням, в якій вуглецеві атоми в кількості до 3 замінені гетероатомами, вибраними з грyпи, до якої входять О, S, NR, причому R є водень або метил. До гетероциклоалкілів, яким віддають перевагу, належать піролідин, піперидин, піперазин, 1метилпіперазин, морфолін тощо. Термін "С1-С6-алкілциклоалкіл" означає С1-С6алкільні групи, які мають циклоалкільний замісник, в тому числі циклогексилметил, циклопентилпропіл тощо. Термін "C1-C6-алкілгетероциклоалкіл" означає С1-С6-алкільні грyпи, які мають гетероциклоалкільний замісник, в тому числі 2-(1-піролідиніл)етил, 4морфолінілметил, (1-метил-4-піперидиніл)метил тощо. Термін "карбокси(л)" означає грyпy -С(О)ОН. Термін "С1-С6-алкілкарбокси(л)" означає С1-С6алкільні групи, які мають карбоксильний замісник, в тому числі 2-карбоксіетил тощо. Термін "ацил" означає групу -C(O)R, де R є "С1-С6-алкіл", "арил", "гетероарил", "С1-С6алкіларил" або "С1-С6-алкілгетероарил". Термін "С1-С6-алкілацил" означає С1-С6алкільні грyпи, які мають ацильний замісник, в тому числі 2-ацетилетил тощо. Термін "арилацил" означає арильні грyпи, які мають ацильний замісник, в тому числі 2ацетилфеніл тощо. Термін "гетероарилацил" означає гетероарильні грyпи, які мають ацильний замісник, в тому числі 2-ацетилпіридил тощо. Термін "С3-С8-(гетеро)циклоалкілацил" означає 3-8-членні циклоалкільні або гетероциклоалкільні групи, які мають ацильний замісник. Термін "ацилокси(група)" означає грyпy OC(O)R, де R є Η, "С1-С6-алкіл", "С2-С6-алкеніл", "С2-С6-алкініл", "С3-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6-алкілгетероарил", "С2-С6-алкеніларил", "С2С6-алкенілгетероарил", "С2-С6-алкініларил", "С2-С6алкінілгетероарил", "С1-С6-алкілциклоалкіл", "С1С6-алкілгетероцикл оалкіл ". Термін "С1-С6-алкілацилокси(група)" означає С1-С6-алкільні групи, які мають aцилoкcигрyпy як замісник, в тому числі 2-(ацетилокси)етил тощо. Термін "алкокси(група)" означає грyпy -O-R, де R є "С1-С6-алкіл", "арил", "гетероарил", "С1-С6алкіларил" або "С1-С6-алкілгетероарил". До aлкoкcигрyп, яким віддають перевагу, належать, наприклад, метокси-, етокси-, фeнoкcигрyпa тощо. Термін "С1-С6-алкілалкокси^упа)" означає С1С6-алкільні грyпи, які мають aлкoкcигрyпy як замісник, в тому числі 2-етоксіетил тощо. Термін "алкоксикарбоніл" означає грyпy C(O)OR, де R є Η, "С1-С6-алкіл", "арил", "гетероарил", "С1-С6-алкiлapил" або "С1-С6алкілгетероарил". Термін "С1-С6-алкілалкоксикарбоніл" означає С1-С6-алкільні грyпи, які мають алкоксикарбонільний замісник, в тому числі 2(бензилоксикарбоніл)етил тощо. Термін "амінокарбоніл" означає грyпy C(O)NRR', де кожний з R, R' незалежно від іншого 19 79793 є водень або С 1-С6-алкіл, арил, гетероарил, "С1С6-алкіларил" або "С1-С6-алкілгетероарил". Термін "С1-С6-алкіл амінокарбоніл" означає С1С6-алкільні грyпи, які мають амінокарбоніл замісник, в тому числі 2-(диметиламінокарбоніл)етил тощо. Термін "ациламіно(група)" означає грyпy NRC(O)R', де кожний з R, R' незалежно від іншого є водень, "С1-С6-алкіл", "С2-С6-алкеніл", "С2-С6алкініл", "С3-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6алкілгетероарил", "С2-С6-алкеніларил", "С2-С6алкенілгетероарил", "С2-С6-алкініларил", "С2-С6алкінілгетероарил", "С1-С6-алкілциклоалкіл", "С1С6-алкілгетероциклоалкіл". Термін "С1-С6-алкілациламіногрупа)" означає С1-С6-алкільні групи, які мають aцилaмiнoгрyпy як замісник, в тому числі 2-(пропіоніламіно)етил тощо. Термін "ypeїдo(грyпa)" означає групу NRC(O)NR'R", де кожний з R, R', R" незалежно від іншого є водень, "С1-С6-алкіл", "С2-С6-алкеніл", "С2С6-алкініл", "С3-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6алкілгетероарил", "С2-С6-алкеніларил", "С2-С6алкенілгетероарил", "С2-С6-алкініларил", "С2-С6-алкінілгетероарил", "С1-С6-алкілциклоалкіл", "С1С6-алкілгетероциклоалкіл", і де R' та R", спільно з атомом азоту, до якого вони приєднані, можуть факультативно утворювати 3-8-членний гетероциклоалкіл. Термін "С1-С6-алкілуреїдо(група)" означає С1С6-алкільні групи, які мають уреїдогрупу як замісник, в тому числі 2-(N'-метилуреїдо)етил тощо. Термін "карбамат" означає групу -NRC(O)OR', де кожний з R, R' незалежно від іншого є водень, "С1-С6-алкіл", "С2-С6-алкеніл", "С2-С6-алкініл", "С3С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6алкілгетероарил", "С2-С6-алкеніларил", "С2-С6алкенілгетероарил", "С2-С6-алкініларил", "С2-С6алкінілгетероарил", "С1-С6-алкілциклоалкіл", "С1С6-алкілгетероциклоалкіл". Термін "aмiнo(грyпa)" означає грyпy -NRR', де кожний з R,R' незалежно від іншого є водень, "С1С6-алкіл", "арил", "гетероарил", "С1-С6-алкіларил", "С1-С6-алкілгетероарил", "циклоалкіл" або "гетероциклоалкіл" і де R та R', спільно з атомом азоту, до якого вони приєднані, можуть факультативно утворювати 3-8-членний гетероциклоалкіл. Термін "С1-С6-алкіламіно(група)" означає С1С6-алкільні групи, які мають aмiнoгрyпy як замісник, в тому числі 2-(1-піролідиніл)етил тощо. Термін "амоній" означає позитивно заряджену груп у -N+RR'R" де кожний з R,R',R" незалежно від інших є "С1-С6-алкіл", "С1-С6-алкіларил", "С1-С6алкілгетероарил", "циклоалкіл" або "гетероциклоалкіл" і де R та R', спільно з атомом азоту, до якого вони приєднані, можуть факультативно утворювати 3-8-членний гетероциклоалкіл. Термін "С1-С6-алкіламоній" означає "С1-С6алкільні групи, які мають амоній як замісник, в тому числі 2-(1-піролідиніл)етил тощо. Термін "галоген" означає атоми фтору, хлору, брому або йоду. 20 Термін "сульфонілокси(група)" означає грyпy OSO2-R, де R вибраний з групи, до якої входять Н, "С1-С6-алкіл", "С1-С6-алкіл", заміщений галогенами, наприклад, грyпa -OSO2-CF3, "C2-C6-алкеніл", "С2С6-алкініл", "С3-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6алкілгетероарил", "С2-С6-алкеніларил", "С2-С6алкенілгетероарил", "С2-С6-алкініларил", "С2-С6алкінілгетероарил", "С1-С6-алкілциклоалкіл ", "С1С6-алкілгетероциклоалкіл". Термін "С1-С6-aлкiлcyльфoнiлoкcи(грyпa)" означає С1-С6-алкільні групи, які мають cyльфoнiлoкcигрyпy як замісник, в тому числі 2(метилсульфонілокси)етил тощо. Термін "сульфоніл" означає групу "-SO2-R", де R вибраний з грyпи, до якої входять Н, "арил", "гетероарил", "С1-С6-алкіл", "С1-С6-алкіл", заміщений галогенами, наприклад, грyпy -SO2-CF 3, "С2-С6алкеніл", "С2-С6-алкініл", "С3-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6алкіларил" або "С1-С6-алкілгетероарил", "С2-С6алкеніларил", "С2-С6-алкенілгетероарил", "С2-С6алкініларил", "С2-С6-алкінілгетероарил", "С1-С6алкілциклоалкіл", "С1-С6-алкілгетероциклоалкіл". Термін "С1-С6-алкілсульфоніл" означає "С1-С6алкільні грyпи, які мають сульфонільний замісник, в тому числі 2-(метилсульфоніл)етил тощо. Термін "сульфініл" означає грyпy "-S(O)-R", де R вибраний з групи, до якої входять Н, "С1-С6алкіл", "С1-С6-алкіл", заміщений галогенами, наприклад, грyпy -SO-CF3, "С2-С6-алкеніл", "С2-С6алкініл", "С3-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6алкілгетероарил", "С2-С6-алкеніларил", "С2-С6алкенілгетероарил", "С2-С6-алкініларил", "С2-С6алкінілгетероарил", "С1-С6-алкілциклоалкіл", "С1С6-алкілгетероциклоалкіл". Термін "С1-С6-алкілсульфініл" означає "С1-С6алкільні грyпи, які мають сульфінільний замісник, в тому числі 2-(метилсульфініл)етил тощо. Термін "сульфаніл" означає грyпи -S-R, де R є Н, "С1-С6-алкіл", "С1-С6-алкіл", заміщений галогенами, наприклад, грyпy -SO-CF3 , "С2-С6-алкеніл", "С2-С6-алкініл", "С3-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6-алкілгетероарил", "С2-С6-алкеніларил", "С2С6-алкенілгетероарил", "С2-С6-алкініларил", "С2-С6алкінілгетероарил", "С1-С6-алкілциклоалкіл", "С1С6-алкілгетероциклоалкіл". До сульфанільних грyп, яким віддають перевагу, належать метилсульфаніл, етил сульфаніл то що. Термін "С1-С6-алкілсульфаніл" означає "С1-С6алкільні грyпи, які мають сульфанільний замісник, в тому числі 2-(етилсульфаніл)етил тощо. Термін "сульфоніламіно(група)" означає грyпy -NRSO2-R', де кожний з R, R' незалежно від іншого є водень, "С1-С6-алкіл", "С2-С6-алкеніл", "С2-С6алкініл", "С3-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6алкілгетероарил", "С2-С6-алкеніларил", "С2-С6алкенілгетероарил", "С2-С6-алкініларил", "С2-С6алкінілгетероарил", "С1-С6-алкілциклоалкіл", "С1С6-алкілгетероциклоалкіл". Термін "С1-С6-алкілсульфоніламіно(група)" означає "С1-С6-алкільні грyпи, які мають 21 79793 cyльфoнiлaмiнoгрyпy як замісник, в тому числі 2(етилсульфоніламіно)етил тощо. Термін "аміносульфоніл" означає грyпy -SO 2NRR', де кожний з R, R' незалежно від іншого є водень, "С1-С6-алкіл", "С2-С6-алкеніл", "С2-С6алкініл", "Сз-С8-циклоалкіл", "гетероциклоалкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6алкілгетероарил", "С2-С6-алкеніларил", "С2-С6алкенілгетероарил", "С2-С6-алкініларил", "С2-С6алкінілгетероарил", "С1-С6-алкілциклоалкіл", "С1С6-алкілгетероциклоалкіл ". Термін "С1-С6-алкіламіносульфоніл" означає С1-С6-алкільні грyпи, які мають аміносульфонільний замісник, в тому числі 2(циклогексиламіносульфоніл)етил тощо. Термін "заміщений або незаміщений": якщо визначення індивідуального замісника не обмежене іншим чином, то вищезазначені грyпи, наприклад, "алкіл", "алкеніл", "алкініл", "арил" та "гетероарил" тощо можуть бути факультативно заміщені замісниками в кількості від 1 до 5, вибраними з групи, до якої входять "С1-С6-алкіл", "С2-С6алкеніл", "С2-С6-алкініл", "циклоалкіл", "гетероциклоалкіл", "С1-С6-алкіларил", "С1-С6алкілгетероарил", "С1-С6-алкілциклоалкіл", "С1-С6алкілгетероциклоалкіл", "аміно(група)", "амоній", "ацил", "ацилокси(група)", "ациламіно(група)", "амінокарбоніл", "алкоксикарбоніл", "уреїдо(група)", "арил", "карбамат", "гетероарил", "сульфініл", "сульфоніл", "алкокси(група)", "сульфаніл", "галоген", "карбокси(л)", тригалогенметил, ціано-, гідрокси-, меркапто-, нiтpoгрyпa тощо. В альтернативних варіантах таке заміщення може охоплювати також випадки, коли сусідні замісники можуть бути піддані замиканню циклу, особливо коли сусідні функціональні замісники введені в реакцію з утворенням, наприклад, лактамів, лактонів, циклічних ангідридів, але також і ацеталів, тіоацеталів, аміналів, що утворюються шляхом замикання циклу, наприклад, із метою утворення захисної грyпи. Термін "фармацевтично прийнятні катіонні солі або комплекси" призначений для визначення таких солей, як солі лужних металів, (наприклад, натрію та калію), солі лужноземельних металів (наприклад, кальцію або магнію), солі алюмінію, солі амонію та солі з органічними амінами, наприклад, із метиламіном, диметиламіном, триметиламіном, етиламіном, триетиламіном, морфоліном, N-Me-D-глюкаміном, N,N'-біс(фенілметил)-1,2етандіаміном, етаноламіном, діетаноламіном, етилендіаміном, N-метилморфоліном, піперидином, бензатином (Ν,Ν'-дибензилетилендіаміном), холіном, етилендіаміном, меглуміном (Nметилглюкаміном), бенетаміном (Nбензилфенетиламіном), діетиламіном, піперазином, трометаміном (2-аміно-2-гідроксиметил-1,3пропандіолом), прокатом, а також амінами формули -NR,R',R", де R, R', R" незалежно від іншого є водень, алкіл або бензил. Солями, яким віддається особлива перевага, є солі натрію та калію. Термін "фармацевтично прийнятні солі або комплекси" означає солі або комплекси визначених нижче сполук за цим винаходом, які зберігають бажану біологічну активність. До прикладів 22 таких солей належать, але без обмеження, солі кислот, утворені з неорганічними кислотами (наприклад, із хлористоводневою, бромистоводневою, сірчаною, фосфорною, азотною кислотами тощо), та солі, утворені з органічними кислотами, наприклад, з оцтовою, щавлевою, винною, бурштиновою, яблучною, фумаровою, малеїновою, аскорбіновою, бензойною, дубильною, памовою, альгіновою, поліглутаміновою, нафталінсульфоновою, нафталіндисульфоновою та полігалактуроновою кислотами. Вищезгадані сполуки можна застосовувати також у формі фармацевтично прийнятних четвертинних солей, відомих фахівцям, до яких, зокрема, належать четвертинні амонієві солі формули -NR,R',R"+Z-, де R, R', R" незалежно від інших є водень, алкіл або бензил, С1-С6-алкіл, С2-С6-алкеніл, С2-С6-алкініл, С1-С6-алкіларил, С1С6-алкілгетероарил, циклоалкіл, гетероциклоалкіл та Ζ є протиіон, в тому числі хлорид, бромід, йодид, -О-алкіл, толуолсульфонат, метилсуль фонат, сульфонат, фосфат або карбоксилат (наприклад, бензоат, сукцинат, ацетат, гліколят, малеат, мадат, фумарат, цитрат, тартрат, аскорбат, цінамоат, манделоат та дифеніл ацетат). Термін "фармацевтично активна похідна" означає будь-яку сполуку, яка при введенні в організм здатна забезпечити прямим або непрямим шляхом дію, описану в цьому документі. Термін "енантіомерний надлишок (ее)" стосується продуктів, одержаних шляхом асиметричного синтезу, тобто синтезу із застосуванням нерацемічних ви хідних матеріалів та/або реагентів або синтезу, який включає щонайменше одну енантіоселективну стадію, причому одержують надлишок одного енантіомеру порядку щонайменше 52% ее. Загальна формула (І) за даним винаходом охоплює також таутомери, геометричні ізомери, оптично активні форми, наприклад, енантіомери, діастереомери та рацемічні форми, а також фармацевтично прийнятні солі згаданої сполуки. Серед фармацевтично прийнятних солей формули за цим винаходом перевага віддається солям із фармацевтично прийнятними кислотами, наприклад, гідрохлориду, гідроброміду, сульфату або бісульфату, фосфату або гідрофосфату, ацетату, бензоату, сукцинату, фумарату, малеату, лактату, цитрату, тартрату, глюконату, метансульфонату, бензолсульфонату та пара-толуолсульфонату. Сполуки за цим винаходом можуть бути одержані у вигляді суміші ізомерів E/Z або як практично чисті Ε-ізомери або Z-ізомери. Згадана E/Zізомерія за варіантом, якому віддається перевага, стосується вінілового містка між фенілом та азолідиноновою грyпoю. За одним конкретним варіантом здійснення, сполуки формули (І) є Z-ізомери. Перший аспект цього винаходу полягає у застосуванні сполук формули (І) (I) а також геометричних ізомерів, оптично активних форм, наприклад, енантіомерів, діастереоме 23 79793 рів та рацемічних форм, а також фармацевтично прийнятних солей та фармацевтично активних похідних цих сполук для виготовлення лікарського засобу для профілактики та/або лікування автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, aгрeгaцiї тромбоцитів, раку, ускладнень трансплантації, обумовлених реакціями відторгнення, відторгнення трансплантата або травм легенів. За варіантом здійснення, якому віддається перевага, ці сполуки застосовуються для лікування та/або профілактики автоімунних розладів або запальних захворювань, наприклад, розсіяного склерозу, псоріазу, ревматоїдного артриту, системного червоного вовчака, запального захворювання кишок, запалення легенів, тромбозу або інфекційного захворювання чи запалення мозку, наприклад, менінгіту або енцефаліту. За іншим варіантом здійснення цього винаходу, якому віддається перевага, ці сполуки застосовуються для лікування та/або профілактики нейродегенеративних захворювань, в тому числі розсіяного склерозу, хвороби Альцгеймера, хореї Гентінгтона, травми центральної нервової системи, інсульту або ішемічних станів. За варіантом здійснення цього винаходу, якому віддається особлива перевага, ці сполуки застосовуються для лікування та/або профілактики серцево-судинних захворювань, наприклад, атеросклерозу, гіпертрофії серця, дисфункції серцевого міоцита, підвищеного кров'яного тиску або судинозвуження. За іншим варіантом здійснення цього винаходу, якому віддається особлива перевага, ці сполуки застосовуються для лікування та/або профілактики хронічного обструктивного захворювання легенів, фіброзного анафілактичного шоку, псоріазу, алергічних захворювань, астми, інсульту або ішемічних станів, і шемії-реперфузії, а фегації/активації тромбоцитів, атрофії/гіпертофії скелетного м'яза, рекрутмента лейкоцитів у раковій тканині, ангіогенезу, метастазування пухлин, зокрема, меланоми, саркоми Капоші, гострих та хронічних бактеріальних та вірусни х інфекцій, сепсису, обумовлених реакціями відторгнення ускладнень трансплантації, відторгнення трансплантата, гломерулосклерозу, гломерулонефриту, прогресивного ниркового фіброзу, ендотеліальних та епітеліальних травм легенів і взагалі запалень легеневих дихальних шляхі в. Замісники у формулі (І) відповідають нижченаведеним визначенням: А - незаміщена або заміщена 5-8-членна гетероциклічна група або незаміщена або заміщена карбоциклічна група. Згадана карбоциклічна група може бути конденсована з незаміщеним або заміщеним арилом, незаміщеним або заміщеним гетероарилом, незаміщеним або заміщеним циклоалкілом чи незаміщеним або заміщеним гeтepoциклoалкiлoм. До цих гетероциклічних або карбоциклічних груп належать арил, гетероарил, циклоалкіл та гетероциклоалкіл, в тому числі феніл, фенантре 24 ніл, циклопентан, циклогексил, норборніл, піролідин, піперидин, піперазин, 1-метилпіперазин, морфолін, піроліл, фураніл, тієніл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, піразоліл, 1,2,3-триазоліл, 1,2,4-триазоліл, 1,2,3оксадіазоліл, 1,2,4-оксадіазоліл, 1,2,5оксадіазоліл, 1,3,4-оксадіазоліл, 1,3,4-триазиніл, 1,2,3-триазиніл, бензофурил, [2,3дигідро]бензофурил, ізобензофурил, бензотієніл, бензотриазоліл, ізобензотієніл, індоліл, ізоіндоліл, 3Н-індоліл, бензимідазоліл, імідазо[1,2-а]піридил, бензотіазоліл, бензоксазоліл, хінолізиніл, хіназолініл, фталазиніл, хіноксалініл, цинолініл, нафтиридиніл, піридо[3,4-b]піридил, піридо[3,2-b]тридил, піридо[4,3-b]піридил, хіноліл, ізохіноліл, тетразоліл, 5,6,7,8-тетрагідрохіноліл, 5,6,7,8тетрагідроізохіноліл, пуриніл, птеридиніл, карбазоліл, ксантеніл та бензохіноліл. До додаткових прикладів гетероциклічних або карбоциклічних грyп А належать незаміщений або заміщений діоксол, незаміщений або заміщений діоксин, незаміщений або заміщений дигідрофуран, незаміщений або заміщений (дигідро)фураніл, незаміщений або заміщений (дигідро)оксазиніл, незаміщений або заміщений оксазиноїл, незаміщений або заміщений піридиніл, незаміщений або заміщений ізоксазоліл, незаміщений або заміщений оксазоліл, незаміщений або заміщений (дигідро)нафталініл, незаміщений або заміщений піримідиніл, незаміщений або заміщений триазоліл, незаміщений або заміщений імідазоліл, незаміщений або заміщений піразиніл, незаміщений або заміщений тіазоліл, незаміщений або заміщений тіадіазоліл, незаміщений або заміщений оксадіазоліл. X - S, О або ΝΗ, за варіантом, якому віддається перевага, S. Кожний з Υ1 і Υ2 незалежно один від одного вибрані з грyпи, до якої входять S, О та -ΝΗ, за варіантом, якому віддається перевага, О. Ζ - S або О, за варіантом, якому віддається перевага, О. R1 вибраний з грyпи, яка складається або до якої входять Н, CN, карбоксил, ацил, С1-С6алкоксигрупа, галоген, гідрокси-, ацилоксгарупа, незаміщена або заміщена C1-C6aлкiлкapбoкcигрyпa, незаміщена або заміщена С 1С6-алкілацилоксигрупа, незаміщена або заміщена С1-С6-алкілалкоксигрупа, алкоксикарбоніл, незаміщений або заміщений С 1-С6алкілалкоксикарбоніл, амінокарбоніл, незаміщений або заміщений С 1-С6-алкіламінокарбоніл, ациламіногрупа, незаміщена або заміщена C1-C6aлкiлaцилaмiнoгрyпa, ypeїдoгрyпa, незаміщена або заміщена С1-С6-алкілуреїдогрупа, aмiнoгрyпa, незаміщена або заміщена С 1-С6-aлкiлaмiнoгрyпa, амоній, сульфонілоксигрупа, незаміщена або заміщена С1-С6-алкілсульфонілоксгарупа, сульфоніл, незаміщений або заміщений С 1-С6алкілсульфоніл, сульфініл, незаміщений або заміщений С1-С6-алкілсульфініл, сульфаніл, незаміщений або заміщений С 1-С6-алкілсульфаніл, сульфоніламіногрупа, незаміщена або заміщена С 1С6-aлкiлcyльфoнiлaмінoгрyпa та карбамат. За конкретним варіантом здійснення R1 є Н. 25 79793 R2 вибраний з групи, яка складається або до якої входять Н, галоген, ацил, аміногрупа, незаміщений або заміщений С 1-С6-алкіл, незаміщений або заміщений С 2-С6-алкеніл, незаміщений або заміщений С2-С6-алкініл, незаміщена або заміщена С1-С6-алкілкарбоксигрупа, незаміщений або заміщений С1-С6-алкілацил, незаміщений або заміщений С1-С6-алкілалкоксикарбоніл, незаміщений або заміщений С 1-С6-алкіламінокарбоніл, незаміщена або заміщена С 1-С6-алкілациклоксигрупа, незаміщена або заміщена С 1-С6алкіоациламіногрупа, незаміщена або заміщена С1-С6-алкілуреїдогрупа, незаміщений або заміщений С1-С6-алкілкарбамат, незаміщена або заміщена С1-С6-aлкiлaмiнoгрyпa, незаміщена або заміщена С1-С6-алкілалкоксигрупа, незаміщений або заміщений C1-C6-алкiлcyльфaнiл, незаміщений або заміщений С1-С6-алкілсульфініл, незаміщений або заміщений С1-С6-алкілсульфоніл, незаміщений або заміщений С 1-С6-алкілсульфоніламіноарил, незаміщений або заміщений арил, незаміщений або заміщений С3-С8-циклоалкіл або гетероциклоалкіл, незаміщений або заміщений С1-С6-алкіларил, незаміщений або заміщений С 2-С6-алкеніларил, незаміщений або заміщений С 2-С6-алкініларил, карбоксил, ціаногрупа, гідроксил, С1-С6-алкокси-, нітро-, ациламіно-, уреїдо-, сульфоніламіногрупа, сульфаніл та сульфоніл. n - ціле число 0, 1 або 2, за варіантом, якому віддається перевага, n - 0 або 1. За варіантом, якому віддається найбільша перевага, n=0. За конкретним варіантом здійснення цього винаходу, кожен з R1 і R2 є Н. За подальшим конкретним варіантом здійснення цього винаходу, X є S, кожен з Υ1 і Υ2 є О, R1 і R2 відповідають вищенаведеним визначенням та n - 0. Подальший конкретний аспект цього винаходу, якому віддається перевага, стосується застосування тіазолідиндіонових похідних конденсованих вінілбензолів формул (Іа), (Іb), (Іс) та (Id) для виготовлення лікарського засобу для профілактики та/або лікування автоімунних розладів та/або запальних захворювань, серцево-судинних захворювань, нейродегенеративних захворювань, бактеріальних або вірусних інфекцій, захворювань нирок, aгрeгaції тромбоцитів, раку, обумовлених реакціями відторгнення ускладнень трансплантації, відторгнення трансплантата або травм легенів: (Ia) R1, R2, Υ1, Ζ та η у формулі (Іа) відповідають вищенаведеним визначенням. G у формулі (Іа) є незаміщений або заміщений С1-С5-алкілен (наприклад, метилен, етилен, пропілен тощо) або незаміщена або заміщена С 1-С5алкеніленова грyпa (наприклад метин (-СН=), група -СН=СН-, пропеніленова група тощо). Кожний з W та V у формулі (Іа) незалежно від іншого вибраний з групи, яка складається з О, S, NR3, де R3 є Η або незаміщена або заміщена С 1С6-алкільна грyпa, кожний з m та о незалежно від 26 іншого є 0 або 1; о - ціле число від 1 до 4 та q ціле число від 0 до 4. Ще більша перевага віддається сполукам формули (Іа), де G є С1-С4-алкілен, які відповідно утворюють сполуки формули (Іb) (тобто р=1, 2, 3 або 4, за варіантом, якому віддається перевага, 1 або 2). (Ib) Конкретною підгрупою формули (Іb) є сполуки, що мають формулу (Іс), причому W, R1, Y1 відповідають вищенаведеним визначенням; зокрема, R1 може бути вибраний з грyпи, яка складається з незаміщеної або заміщеної С 1-С4-алкільної групи чи незаміщеної або заміщеної С 1-С5-алкенільної групи, карбоксилу, ціано-, С1-С4-алкокси-, нітро-, ациламіно-, ypeїдогрупи. (Ic) Іншою конкретною пiдгрyпoю формули (Іа) є сполуки, де кожний з V, W та Y1 є О, тобто сполуки формули (Id). (Id) За варіантом здійснення, якому віддається перевага, у формула х (Іа), (Іb) і (Id), n - 0, m - 1, p - 1 або 2, о - 0, q - 1, та R1 і R2 відповідають вищенаведеним визначенням. За подальшим конкретним варіантом здійснення, у формулах (Іа), (Іb) і (Id), m - 1, n - 0, p - 1 або 2, q - 0, о - 1, в той час як R1 та R2 відповідають вищенаведеним визначенням, більш конкретно R1 є атом галогену або водню. За подальшим конкретним варіантом здійснення, у формула х (Іа), (Іb) і (Id), p - 1 або 2, q - 0, m - 0, n - 1 та R1 і R2 відповідають вищенаведеним визначенням. Сполуки за цим винаходом придатні для модулювання, особливо пригнічення, активності 3кіназ фосфатоінозитидів (РІ3K), особливо g-3кінази фосфатоінозитидів (РІ3Kg). Таким чином, мається на увазі, що сполуки за цим винаходом також особливо придатні для лікування та/або запобігання розладів, опосередкованих РІ3K, особливо РІ3Kg. Згадане лікування охоплює модулювання - особливо пригнічення або регуляцію за типом негативного (зворотного) зв'язку - 3-кіназ фосфа тоінозитидів. Нижченаведені сполуки не охоплюються формулою (І): 27 79793 R1 є нижчий алкіл або аралкіл та R2 є Η або галоген. Сполуки ТЕ розкриті [у JP 55 045648] як проміжні сполуки без будь-якої біологічної активності, в той час [як JA згадується у Journal of Medicinal Chemistry (1998), 41(18), 3515-3529] як неактивна при пробі на набрякання кінцівки. До сполук за цим винаходом, зокрема, належать сполуки, які входять до нижченаведеної грyпи, яка складається з: 5-(1,3-бензодіоксол-5-ілметилен)-1,3тіазолідин-2,4-діону 5-(1,3-бензодіоксол-5-ілметилен)-2-тіоксо-1,3тіазолідин-4-ону 5-(2,3-дигідро-1,4-бензодіоксин-6-ілметилен)1,3-тіазолідин-2,4-діону 5-(2,3-дигідро-1-бензофуран-5-ілметилен)-1,3тіазолідин-2,4-діону 5-[(7-метокси-1,3-бензодіоксол-5-іл)метилен]1,3-тіазолідин-2,4-діону 5-[(9,10-діоксо-9,10-дигідроантрацен-2іл)метилен]-1,3-тіазолідин-2,4-діону (5-[(2,2-дифтор-1,3-бензодіоксол-5іл)метилен]-1,3-тіазолідин-2,4-діону (5Z)-5-(1,3-дигідро-2-бензофуран-5ілметилен)-1,3-тіазолідин-2,4-діону 5-(1-бензофуран-5-ілметилен)-1,3-тіазолідин2,4-діону 5-[(4-метил-3-оксо-3,4-дигідро-2Н-1,4бензоксазин-6-іл)метилен]-1,3-тіазолідин-2,4-діону 5-(1,3-бензодіоксол-5-ілметилен)-2-іміно-1,3тіазолідин-4-ону 5-хінолін-6-ілметилен-тіазолідин-2,4-діону 5-хінолін-6-ілметилен-2-тіоксо-тіазолідин-4-ону 2-іміно-5-хінолін-6-ілметилен-тіазолідин-4-ону 5-(3-метил-бензо[d]ізоксазол-5-ілметилен)тіазолідин-2,4-діону 5-(4-феніл-хіназолін-6-ілметилен)-тіазолідин2,4-діону 5-(4-диметиламіно-хіназолін-6-ілметилен)тіазолідин-2,4-діону 5-[(4-амінохіназолін-6-іл)метилен]-1,3тіазолідин-2,4-діону 5-[(4-піперидин-1-ілхіназолін-6-іл)метилен]-1,3тіазолідин-2,4-діону 5-[(4-морфолін-4-ілхіназолін-6-іл)метилен]-1,3тіазолідин-2,4-діону 5-{[4-(бензиламіно)хіназолін-6-іл]метилен}-1,3тіазолідин-2,4-діону 5-{[4-(діетиламіно)хіназолін-6-іл]метилен}-1,3тіазолідин-2,4-діону 5-({4-[(пірвдин-2-ілметил)аміно]хіназолін-6іл}метилен)-1,3-тіазолідин-2,4-діону 5-({4-[(піридин-3-ілметил)аміно]хіназолін-6іл}метилен)-1,3-тіазолідин-2,4-діону етил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]хіназолін-4-іл}піперидин-3карбоксилату етил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5 28 іліден)метил]хіназолін-4-іл}піперидин-4карбоксилату трет-бутил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]хіназолін-4-іл}-L-пролінату 5-{[4-(4-метилпіперазин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону 5-{[4-(4-піримідин-2-ілпіперазин-1-іл)хіназолін6-іл]метилен}-1,3-тіазолідин-2,4-діону 5-({4-[4-(4-фторфеніл)тперидин-1-іл]хіназолін6-іл}метилен)-1,3-тіазолідин-2,4-діону 5-{[4-(4-бензилпіперидин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону 5-({4-[4-(2-фенілетил)піперидин-1-іл]хіназолін6-іл}метилен)-1,3-тіазолідин-2,4-діону 5-{[4-(4-метилпіперидин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону 5-{[4-(4-гідроксипіперидин-1-іл)хіназолін-6іл]метилен}-1,3-тіазолідин-2,4-діону 1-[6-(2,4-діоксо-тіазолідин-5-іліденметил)хіназолін-4-іл]-піперидин-4-карбонової кислоти 1-[6-(2,4-діоксо-тіазолідин-5-іліденметил)хіназолін-4-іл]-піперидин-3-карбонової кислоти 1-[6-(2,4-діоксо-тіазолідин-5-іліденметил)хіназолін-4-іл]-піролідин-2-карбонової кислоти 5-(4-метиламіно-хіназолін-6-ілметилен)тіазолідин-2,4-діону 5-(4-метокси-хіназолін-6-ілметилен)тіазолідин-2,4-діону 2-іміно-5-(4-метиламіно-хіназолін-6ілметилен)-тіазолідин-4-ону 2-іміно-5-(4-піперидин-хіназолін-6-ілметилен)тіазолідин-4-ону 2-іміно-5-(4-диметиламіно-хіназолін-6ілметилен)-тіазолідин-4-ону 5-(2-метил-2Н-бензотриазол-5-ілметилен)тіазолідин-2,4-діону 5-(3-метил-3Н-бензотриазол-5-ілметилен)тіазолідин-2,4-діону 5-(3-етил-3Н-бензимідазол-5-ілметилен)тіазолідин-2,4-діону 5-{[1-(4-фенілбутил)-1Н-бензимідазол-6іл]метилен}-1,3-тіазолідин-2,4-діону 5-[(1-проп-2-ін-1-іл-1Н-бензимідазол-6іл)метилен]-1,3-тіазолідин-2,4-діону 5-[(1-{2-[4-(трифторметил)феніл]етил}-1Нбензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4діону 5-({1-[2-(4-гідроксифеніл)етил]-1Нбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону метил-4-{6-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1Н-бензимідазол-1іл}циклогексанкарбоксилату 5-({1-[2-(5-метокси-1Н-індол-3-іл)етил]-1Нбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону 5-({1-[(1-метил-1Н-піразол-4-іл)метил]-1Нбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону 5-({1-[2-(3,4-диметоксифеніл)етил]-1Нбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону 5-({1-[2-(4-феноксифеніл)етил]-1Нбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону 29 79793 5-({1-[4-(трифторметил)бензил]-1Нбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону 4-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]1Н-бензимідазол-1-іл}циклогексанкарбонової кислоти 5-[(1-ізобутил-1Н-бензимідазол-6-іл)метилен]1,3-тіазолідин-2,4-діону 5-({1-[2-(1,3-бензодіоксол-4-іл)етил]-1Нбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону 5-({1-[2-(2-феноксифеніл)етил]-1Нбензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4діону 5-{[1-(3,3-дифенілпропіл)-1Н-бензимідазол-6іл]метилен}-1,3-тіазолідин-2,4-діону 5-{[1-(2-метоксибензил)-1Н-бензимідазол-6іл]метилен}-1,3-тіазолідин-2,4-діону 5-{[1-(3-фурилметил)-1Н-бензимідазол-6іл]метилен}-1,3-тіазолідин-2,4-діону 5-[(1-пропіл-1Н-бензимідазол-6-іл)метилен]1,3-тіазолідин-2,4-діону 5-хіноксалін-6-ілметилен-тіазолідин-2,4-діону 5-хіноксалін-6-ілметилен-2-тіоксо-тіазолідин-4ону 2-іміно-5-хіноксалін-6-ілметилен-тіазолідин-4ону 5-бензотіазол-6-ілметилен-тіазолідин-2,4-діону 5-(3-метил-бензофуран-5-ілметилен)тіазолідин-2,4-діону 5-(2-бром-3-метил-бензофуран-5-ілметилен)тіазолідин-2,4-діону 5-(3-бром-бензофуран-5-ілметилен)тіазолідин-2,4-діону етилового складного ефіру 3-[5-(2,4-діоксотіазолідин-5-іліденметил)-бензофуран-3-іл]акрилової кислоти 3-[5-(2,4-діоксо-тіазолідин-5-іліденметил)бензофуран-3-іл]-акрилова кислота 5-[3-(3-оксо-3-піперидин-1-іл-пропеніл)бензофуран-5-ілметилен]-тіазолідин-2,4-діону метил-1-((3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}проп-2еноїл)пролінату метил-1-((3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)-Dпролінату (5-({3-[(3-оксо-3-піролідин-1-ілпроп-1-ен-1-іл]-1бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону 5-({3-[3-морфолін-4-іл-3-оксопроп-1-ен-1-іл]-1бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону метил-1-(3-{5-[(2,4-діоксо-1,3-тіазолідин-5іліден)метил]-1-бензофуран-3-іл}проп-2-еноііл)-Lпролінату N-циклогексил-3-{5-[(2,4-діоксо-1,3-тіазолідин5-іліден)метил]-1-бензофуран-3-iл}-Nмeтилaкpилaмiдy 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]1-бензофуран-3-іл}-N-етил-N-(2-гідроксіетил)акрил аміду N-циклобутил-3-{5-[(2,4-діоксо-1,3-тіазолідин5-іліден)метил]-1-бензофуран-3-іл}акриламіду 5-({3-[3-азетидин-1-іл-3-оксопроп-1-ен-1-іл]-1бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону 5-({3-[3-(1,3-дигідро-2Н-ізоіндол-2-іл)-3 30 оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)1,3-тіазолідин-2,4-діону 5-({3-[3-азепан-1-іл-3-оксопроп-1-ен-1-іл]-1бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діону 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]1-бензофуран-3-іл}-N-піперидин-1-ілакриламіду 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]1-бензофуран-3-іл}-N-(піридин-3ілметил)акриламіду N-циклогексил-3-{5-[(2,4-діоксо-1,3-тіазолідин5-іліден)метил]-1-бензофуран-3-іл}акриламіду 5-({3-[3-(4-метилпіперазин-1-іл)-3-оксопроп-1ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3тіазолідин-2,4-діону N-циклогептил-3-{5-[(2,4-діоксо-1,3-тіазолідин5-іліден)метил]-1-бензофуран-3-іл}акриламіду 5-({3-[3-(2,5-дигідро-1Н-пірол-1-іл)-3-оксопроп1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3тіазолідин-2,4-діону N-циклопентил-3-{5-[(2,4-діоксо-1,3-тіазолідин5-іліден)метил]-1-бензофуран-3-іл}акриламіду етилового складного ефіру 3-[5-(2,4-діоксотіазолідин-5-іліденметил)-бензофуран-3-іл]пропіонової кислоти 3-[5-(2,4-діоксо-тіазолідин-5-іліденметил)бензофуран-3-іл]-пропіонової кислоти 5-[3-(3-оксо-3-піперидин-1-іл-пропіл)бензофуран-5-ілметилен]-тіазолідин-2,4-діону трет-бутилового складного ефіру 6-(2,4-діоксотіазолідин-5-іліденметил)-2,3-дигідробензо[1,4]оксазин-4-карбонової кислоти 5-(3,4-дигідро-2Н-бензо[1,4]оксазин-6ілметилен)-тіазолідин-2,4-діону 5-(4-бензоїл-3,4-дигідро-2Н-бензо[1,4]оксазин6-ілметилен)-тіазолідин-2,4-діону 5-(4-ацетил-3,4-дигідро-2Н-бензо[1,4]оксазин6-ілметилен)-тіазолідин-2,4-діону трет-бутилового складного ефіру 6-(2,4-діоксотіазолідин-5-іліденметил)-бензо[1,4]оксазин-4карбонової кислоти метилового складного ефіру [6-(2,4-діоксотіазолідин-5-іліденметил)-3-оксо-2,3-дигідробензо[1,4]-оксазин-4-іл]-оцтової кислоти N-бензил-2-[6-(2,4-діоксо-тіазолідин-5іліденметил)-3-оксо-2,3-дигідро-бензо[1,4]оксазин4-іл]-ацетаміду 5-(4-бутил-3-оксо-3,4-дигідро-2Нбензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4діону 5-(4-бензил-3-оксо-3,4-дигідро-2Нбензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4діону 5-(2-хлор-бензофуран-5-ілметилен)тіазолідин-2,4-діону 5-(3-аміно-бензо[d]ізоксазол-5-ілметилен)тіазолідин-2,4-діону 5-(3-фенілетиніл-бензофуран-5-ілметилен)тіазолідин-2,4-діону 5-бензо[1,2,5]тіадіазол-5-ілметилен-тіазолідин2,4-діону 5-бензо[1,2,5]оксадіазол-5-ілметилентіазолідин-2,4-діону 5-(2-метил-бензофуран-6-ілметилен)тіазолідин-2,4-діону 5-(2-карбоксиметил-бензофуран-6-ілметилен) 31 79793 тіазолідин-2,4-діону 5-(3-бром-2-фтор-2,3-дигідро-бензофуран-6ілметилен)-тіазолідин-2,4-діону 5-(2-фтор-бензофуран-6-ілметилен)тіазолідин-2,4-діону Подальший аспект цього винаходу полягає в нових тіазолідиндіонових похідних конденсованих вінілбензолів формули (II-а) (II-a) Група А вибрана з групи, яка складається з незаміщеного або заміщеного діоксолу, незаміщеного або заміщеного діоксину, незаміщеного або заміщеного дигідрофурану, незаміщеного або заміщеного (дигідро)фуранілу, незаміщеного або заміщеного (дигідро)оксазинілу, незаміщеного або заміщеного оксазиноїлу, незаміщеного або заміщеного піридинілу, незаміщеного або заміщеного ізооксазолілу, незаміщеного або заміщеного оксазолілу, незаміщеного або заміщеного (дигідро)нафталінілу, незаміщеного або заміщеного піримідинілу, незаміщеного або заміщеного триазолілу, незаміщеного або заміщеного імідазолілу, незаміщеного або заміщеного піразинілу, незаміщеного або заміщеного тіазолілу, незаміщеного або заміщеного тіадіазолілу, незаміщеного або заміщеного оксадіазолілу. R2 вибраний з грyпи, яка складається або до якої входять Н, галоген, ацил, аміно, незаміщений або заміщений С 1-С6-алкіл, незаміщений або заміщений С2-С6-алкеніл, незаміщений або заміщений С2-С6-алкініл, незаміщена або заміщена С 1-С6алкілкарбоксигрупа, незаміщений або заміщений С1-С6-алкілацил, незаміщений або заміщений С 1С6-алкілалкоксикарбоніл, незаміщений або заміщений С1-С6-алкіламінокарбоніл, незаміщена або заміщена С 1-С6-алкілацилоксигрупа, незаміщена або заміщена С 1-С6-aлкiлaцилaмiнoгрyпa, незаміщена або заміщена С 1-С6-алкілуреїдогрупа, незаміщений або заміщений С 1-С6-алкілкарбамат, незаміщена або заміщена С 1-С6-алкіламіногрупа, незаміщена або заміщена С 1-С6алкілалкоксигрупа, незаміщений або заміщений С1-С6-алкілсульфаніл, незаміщений або заміщений С1-С6-алкілсульфініл, незаміщений або заміщений С1-С6-алкілсульфоніл, незаміщений або заміщений С1-С6-алкілсульфоніламіноарил, незаміщений або заміщений арил, незаміщений або заміщений С 3C8-циклоалкіл або гетероциклоалкіл, незаміщений або заміщений С 1-С6-алкіларил, незаміщений або заміщений С2-С6-алкеніларил, незаміщений або заміщений С 2-С6-алкініларил, карбоксил, цiaнoгрyпa, гідроксил, С1-С6-алкокси-, нітро-, ациламіно-, уреїдо-, cyльфoнiлaмiнoгрyпa, сульфаніл або сульфоніл. Більш конкретно, нові тіазолідинонові похідні конденсованих вінілбензолів формули (II) (II) 32 а також геометричні ізомери, оптично активні форми, наприклад, енантіомери, діастереомери та рацемічні форми, а також фармацевтично прийнятні солі та фармацевтично активні похідні цих сполук, де Υ1, Ζ, R1 , R2 відповідають вищенаведеним визначенням та n - 0 або 1. За конкретним варіантом здійснення, R1 є незаміщений або заміщений С 1-С6-алкіл, незаміщений або заміщений С 1-С6-алкіларил, незаміщений або заміщений арил, незаміщений або заміщений С3-С8-циклоалкіл або -гетероциклоалкіл, незаміщений або заміщений С 1-С6-алкіларил, незаміщений або заміщений С 2-С6-алкеніларил, незаміщений або заміщений С 2-С6-алкініларил. За іншим варіантом здійснення цього винаходу, якому віддається перевага, Y1 є О. Подальший аспект цього винаходу полягає в нових тіазолідиндіонових похідних конденсованих вінілбензолів формули (III) (III) а також геометричних ізомерах, оптично активних формах, наприклад, енантіомерах, діастереомерах та рацемічних формах, а також фармацевтично прийнятних солях та фармацевтично активних похідних цих сполук, де R1 та R2 відповідають вищенаведеним визначенням (пунктирна лінія означає факультативну наявність подвійного зв'язку). Подальший варіант здійснення охоплює сполуки формул (IV), (V) та (VI): R1 вибраний з грyпи, яка складається з водню, галогену, цiaнoгрyпи, С1-С6-алкілу, С1-С6алкокигрупи, ацилу, алкоксикарбонілу, в той час як R2 відповідає вищенаведеному визначенню. За конкретним варіантом здійснення R2 є aмінoгрyпa. Подальшим аспектом цього винаходу є застосування нових сполук формул (II), (ІІ-а), (III), (IV), (V) або (VI) як лікарські засоби. Іншим додатковим аспектом цього винаходу є фармацевтична композиція, що містить принаймні одну тіазолідинонову похідну конденсованого вінілбензолу за формулами (II), (III), (IV), (V) або (VI) та фармацевтично прийнятні носій, розріджувач або допоміжну речовину. Іншим додатковим аспектом цього винаходу є застосування сполук за формулами (II), (III), (IV), (V) або (VI) для виготовлення лікарського засобу для профілактики та/або лікування хвороб, опосередкованих РІ3 кіназою, особливо g-РІ3 кіназою. Конкретними хворобами є хвороби, вибрані з грyпи, до якої входять автоімунні розлади та/або запальні захворювання, серцево-судинні захворювання, нейродегенеративні захворювання, бакте 33 79793 34 ріальні або вірусні інфекції, захворювання нирок, aгрeгaцiя тромбоцитів, рак, обумовлені реакціями відторгнення ускладнення трансплантації, відторгнення трансплантата або травми легенів. За варіантом здійснення, якому віддається перевага, згадані сполуки застосовують для лікування та/або профілактики автоімунних розладів або запальних захворювань наприклад, розсіяного склерозу, псоріазу, ревматоїдного артриту, системного червоного вовчака, запального захворювання кишок, запалення легенів, тромбозу або інфекційного захворювання чи запалення мозку наприклад, менінгіту або енцефаліту. За іншим варіантом здійснення цього винаходу, якому віддається перевага, ці сполуки застосовуються для лікування та/або профілактики нейродегенеративних захворювань, в тому числі розсіяного склерозу, хвороби Альцгеймера, хореї Гантінгтона, травми центральної нервової системи, інсульту або ішемічних станів. За варіантом здійснення цього винаходу, якому віддається особлива перевага, ці сполуки застосовуються для лікування та/або профілактики серцево-судинних захворювань, наприклад, атеросклерозу, гіпертрофії серця, дисфункції серцевих міоцитів, підвищеного кров'яного тиску або судинозвуження. За іншим варіантом здійснення цього винаходу, якому віддається особлива перевага, ці сполуки застосовуються для лікування та/або профілактики хронічного обструктивного захворювання легенів, фіброзного анафілактичного шоку, псоріазу, алергічних захворювань, астми, інсульту або ішемічних станів, ішемії-реперфузії, агрегації/активації тромбоцитів, атрофії/гіпертофії скелетного м'яза, рекрутмента лейкоцитів у раковій тканині, ангіогенезу, метастазування пухлин, зокрема, меланоми, саркоми Капоші, гострих та хронічних бактеріальних та вірусни х інфекцій, сепсису, обумовлених реакціями відторгнення ускладнень трансплантації, відторгнення трансплантата, гломерулосклерозу, гломерулонефриту, пpoгрecивнoгo ниркового фіброзу, ендотеліальних та епітеліальних травм легенів і взагалі запалень легеневих дихальних шля хів. За даним винаходом, сполуки формул (II), (ІІа), (III) (IV), (V) або (VI) придатні для модулювання, особливо пригнічення, активності РІ3 кінази та більш конкретно активності РІ3Kg. Подальшим об'єктом цього винаходу є спосіб одержання тіазолідинонових похідних конденсованих вінілбензолів за формулами (І), (Іа), (Іb), (Іс) або (Id), а також тіазолідиндіонових похідних конденсованих вінілбензолів формул (II), (ІІ-а), (III), (IV), (V) або (VI). Тіазолідинонові похідні конденсованих вінілбензолів, наведені як приклади у цьому описі, можна одержати з легко доступних вихідних матеріалів, використовуючи подані нижче загальні способи та методики. Слід мати на увазі, що у випадках, де вказано типові або такі, яким віддається перевага, експериментальні умови (тобто температури та тривалості реакцій, молярні співвідношення реагентів, розчинники тощо), можна застосовува ти також інші умови експериментів, якщо не обумовлено інше. Оптимальні умови проведення реакцій можуть варіювати залежно від конкретних використовуваних реагентів або розчинників, але такі умови може легко визначити фа хівець, використовуючи звичайні процедури оптимізації. У способі, ілюстрованому нижченаведеними схемами, кожний з R1, R2, G, V, W, Υ1, Υ2, Ζ, m, n, ο, p та q відповідає визначенням, поданим вище у цьому описі. Як правило, азолідинонові похідні конденсованих вінілбензолів загальної формули (І) можна одержати за кількома способами синтезу, використовуючи методики як рідкофазового, так і твердофазового хімічного синтезу [Brummond et. al., J.O.C., 64, 1723-1726 (1999)], або звичайними способами, або з застосуванням мікрохвильової техніки. На першій стадії приблизно еквімолярні кількості альдегідного реагента PI (Pla) та сполуки 2 (конкретно, тіазолідиндіону або роданіну, Р3) нагрівають у присутності основи (перевага віддається слабким основам) і одержують відповідний олефін формули (Іа). На першій стадії Ρ1а може бути замінений вихідними сполуками P1b та Р1с з метою одержання кінцевих сполук відповідно (Іb) та (Іс), описаних ви ще. 35 79793 36 Способи, яким за цим винаходом віддається особлива перевага, ілюстровано поданими нижче схемами 3 та 4, за якими можна одержати відповідно сполуки формул (II) та (III), використовуючи вищезгадану реакцію. Хоча ця стадія може бути проведена у відсутності розчинника при температурі, достатньо високій для щонайменше часткового розплавлення реакційної суміші, за варіантом, якому віддається перевага, її виконують у присутності інертного розчинника. Перевага віддається температурам в межах від приблизно 100°С до 250°С, а особлива перевага - температурам від приблизно 120°С до 200°С. До прикладів розчинників, придатних для вищезгаданої реакції, належать такі розчинники, як диметоксиметан, ксилол, толуол, о-дихлорбензол тощо. Прикладами слабких основ, придатних для проведення вищезгаданої реакції, є лужні та лужноземельні солі слабких кислот, наприклад, (С1С12)-алкілкарбонових кислот та бензойної кислоти, карбонати та бікарбонати лужних та лужноземельних металів, наприклад, карбонат кальцію, карбонат магнію, бікарбонат калію, та вторинні аміни, наприклад, піперидин, морфолін, а також третинні аміни, наприклад, піридин, триетиламін, діізопропілетиламін, N-метилморфолін, N-етилпіперидин, N-метилпіперидин тощо. Особлива перевага серед слабких основ віддається ацетату натрію або піперидину з міркувань економічності та ефективності. Як правило, при проведенні реакції цього типу [Tietze et. al., in "The Knoevenagel Reaction", p.341 ff., Pergamon Press, Oxford 1991, Eds.: Trost B.M., Fleming І.] альдегідний вихідний матеріал P1a та інший вихідний матеріал (наприклад, тіазолідиндіон) Р3 у приблизно еквімолярних кількостях змішують з 0,5-1 еквівалентом піперидину в диметоксиметані або аналогічному розчиннику і нагрівають при температурі від 120°С до 200°С, при якій реакція практично завершується за час від приблизно 15хв. до 3год. Потім цільовий олефін формули (Іа) відділяють фільтруванням, якщо він випадає в осад із реакційної суміші при охолодженні, або, наприклад, шляхом змішування з водою з подальшим фільтруванням, і одержують неочищений продукт, який в разі потреби очищають, напри клад, кристалізацією або стандартними xpoмaтoгрaфiчними методами. За альтернативним варіантом, сполуку формули (Іа) можна одержати в типовому випадку шляхом змішування еквімолярних кількостей тіазолідиндіону Р3 з альдегідом P1a та молярним надлишком (у варіанті, якому віддається перевага, 2-4-кратним надлишком) безводного ацетату натрію і нагрівання одержаної суміші при температурі, достатньо високій для плавлення; при такій температурі реакція практично завершується за час від 5хв. до 60 хв. За варіантом, якому віддається перевага, вищезгадану реакцію проводять у кислотному середовищі, наприклад, в оцтовій кислоті, у присутності ацетату натрію або β-аланіну. Альтернативно, вищезгадані реакції можна виконувати при застосуванні мікрохвильової енергії як джерела тепла. Як правило, альдегідний вихідний матеріал Ρ1а та тіазолідиндіон Р3 у приблизно еквімолярних кількостях змішують з 0,5-1 еквівалентом піперидину в диметоксиметані або аналогічному розчиннику та нагрівають при температурі від 140°С до 240°С, при якій реакція практично завершується за час від 3хв. до 10 хв. Фармацевтично прийнятні катіонні солі сполук за цим винаходом легко одержати шляхом проведення реакції їхніх кислотних форм із придатною основою, як правило, в кількості 1екв., у спільному розчиннику. До типових основ належить гідроксид натрію, метилат натрію, етилат натрію, гідрид натрію, гідроксид калію, метилат калію, гідроксид магнію, гідроксид кальцію, бензатин, холін, діетаноламін, етилендіамін, меглумін, бенетамін, діетиламін, піперазин та трометамін. Одержану сіль виділяють шляхом концентрування досуха або додавання осаджувача (рідини, в якій сіль не розчиняється). У деяких випадках солі можна одержувати шляхом змішування розчину кислоти з розчином солі, яка містить відповідний катіон (етилгексаноату натрію, олеату магнію), застосо 37 79793 вуючи розчинник, з якого бажана сіль випадає, або виділяючи її шляхом концентрування та додання осаджувача. Похідні 2,4-азолідинону Р3 можна придбати на ринку у різних постачальників. Альдегіди формули Р1а одержують різноманітними відомими способами, наприклад, шляхом окиснення та відновлення з використанням як вихідної сполуки аліфатичного складного ефіру відповідної карбонової кислоти або карбонової кислоти, використовуючи стандартні способи для відновлення складного ефіру карбонової кислоти або карбонової кислоти до бензилового спирту літій-алюмінійгідридом, діізопропілалюмінієм тощо та подальшим окисненням відповідного бензилового спирту у відповідний альдегід шляхом окиснення у м'яких умовах із застосуванням, наприклад, діоксиду марганцю, хромової кислоти, реагенту Десса-Мартіна або окиснення за Сверном, або у відомих умовах одержання альдегідів із первинних спиртів. Альтернативним способом може бути безпосереднє відновлення відповідного складного ефіру карбонової кислоти або карбонової кислоти до відповідного альдегіду з використанням DIBAL при низькій температурі або будьякого іншого способу, відомого в галузі. Альтернативним способом одержання придатних альдегідів є селективне відновлення нітрильної групи до відповідного альдегіду із застосуванням відомих способів, наприклад, DIBAL тощо. Іншим способом одержання альдегідів формули Ρ1а є селективне відновлення відповідних ацилхлоридів із застосуванням, наприклад, три-третбутоксигідриду літію-алюмінію [ChaJ.S., Brown Η.С, J.O.C 1993, 58, p.4732-4734]. Ще одним альтернативним способом одержання придатних альдегідів є проведення реакції типу Фріделя-Крафтса з відповідною похідною бензолу, при якій сполуку Р4, як показано вище на Схемі 5, вводять в реакцію з 1,1-дихлорметилметиловим простим ефіром у присутності кислоти Льюїса, наприклад, тетрахло 38 риду титану або трихлориду алюмінію, або будьякої відповідної кислоти Льюїса, придатної для реакції такого типу. Згідно зі способом за цим винаходом, якому віддається більша перевага, описаним у літературі [Petrov O.I., Kalcheva V.B., Antonova A.T., Collect. Czech. Chem. Commun, 62, p.494-497 (1997)] та ілюстрованим нижченаведеною Схемою 6, реагент Р2 можна одержати, використовуючи як вихідний матеріал сполуку Р5, шля хом проведення її реакції з 1,1-дихлорметилметиловим простим ефіром, як описано вище. Згідно з іншим способом за цим винаходом, якому віддається більша перевага, ілюстрованим поданою нижче Схемою 7, реагент Р6 можна одержати, використовуючи як вихідний матеріал сполуку Р7, шляхом проведення її реакції з DMF у присутності магнію або н-бутиллітію, або будь-яким іншим способом, відомим фахівцям. Згідно зі ще одним способом за цим винаходом, якому віддається більша перевага, ілюстрованим поданою нижче Схемою 8, реагент Р6 можна одержати, використовуючи як вихідний матеріал сполуку Р9, шля хом проведення її реакції з н-бутиллітієм або LDA у присутності відповідної електрофільної сполуки R1-X, або будь-яким іншим способом, відомим фахівцям. Цей самий спосіб можна повторно застосувати до Р8 з метою одержання Р6. 39 79793 Аналогічно, насичені вихідні сполуки Р6 можна одержати без виділення проміжних продуктів, використовуючи Р9 та відповідні електрофільні сполуки R1-Х та R2-X, як показано на Схемі 9. Якщо вищезазначені загальні способи синтезу не є придатними для одержання сполук формули (І) та/або необхідних проміжних сполук для синтезу сполук формули (І), слід застосовувати відповідні придатні способи одержання, відомі фахівцям. Як правило, схема синтезу кожної індивідуальної сполуки формули (І) залежить від конкретних замісників, які містить кожна молекула, та від доступності необхідних проміжних продуктів; ці фактори також може врахувати пересічний фахівець. Щодо всіх способів введення та відщеплення грyп захисту, [дивись Philip J. Kocienski, у мoнoгрaфiї "Protecting Groups", Georg Thieme Verlag Stuttgart, New York, 1994, and Theodora W. Greene, Peter G.M. Wuts "Protective Groups in Organic Synthesis", Wiley Interscience, 3rd Edition, 1999]. Сполуки за цим винаходом можна виділяти у поєднанні з молекулами розчинника шляхом кристалізації після випарювання розчину у придатному розчиннику. Фармацевтично прийнятні солі кислот зі сполуками за цим винаходом, які містять основні центри, можна одержати звичайним способом. Наприклад, до розчину вільної основи можна додавати придатну кислоту, у чистому вигляді або у придатному розчині, і сіль, що утворюється, відділяти фільтруванням або шляхом випарювання у вакуумі розчинника, який міститься в реакційній суміші. Фармацевтично прийнятні солі основ можна одержати аналогічним способом, поєднуючи розчин сполуки за цим винаходом із придатною основою. Обидва типи солей можна одержувати або взаємно перетворювати, використовуючи іонообмінні смоли. Якщо азолідиндіонові похідні конденсованих вінілбензолів за цим винаходом застосовуються як лікарські засоби, їх вводять в організм, як правило, у формі фармацевтичних композицій. Таким чином, фармацевтичні композиції, які містять сполуку (сполуки) за цим винаходом у фармацевтично прийнятному носіі, розріджувачі або наповнювачі, також охоплюються цим винаходом. Фахівцям відоме все різноманіття таких носіїв, розріджувачів або наповнювачів, придатних для виготовлення фармацевтичних композицій. Сполуки за цим винаходом спільно зі звичайно застосовуваними допоміжними речовинами, носіями, розріджувачами або наповнювачами можна випускати у формах фармацевтичних композицій та їхні х дозованих одиниць, і такі форми можуть мати вигляд твердих продуктів, наприклад, таблеток або заповнених капсул, або рідин, наприклад, 40 розчинів, суспензій, емульсій, еліксирів, або капсул, заповнених такими рідинами, причому всі згадані форми призначені для перорального застосування, або вигляд стерильних ін'єкційних розчинів для парентерального (в тому числі підшкірного) застосування. Такі фармацевтичні композиції та їхні дозовані одиниці можуть містити інгредієнти у звичайних співвідношеннях, у присутності або у відсутності додаткових активних сполук або діючих речовин, причому такі дозовані одиниці можуть містити будь-яку придатну ефективну кількість активного інгредієнта, співмірну з передбаченим для застосування діапазоном добових доз. Фармацевтичні композиції, які містять азолідиндіонові похідні конденсованих вінілбензолів за цим винаходом, можуть бути виготовлені способами, добре відомими у фармацевтичній практиці, і містити щонайменше одну активну сполук у. Як правило, сполуки за цим винаходом застосовуються у фармацевтично ефективній кількості. Реальну застосовувану кількість сполуки, як правило, визначає лікар-куратор хворого з урахуванням релевантних обставин, в тому числі захворювання, яке підлягає лікуванню, обраного способу введення, конкретної застосовуваної сполуки, віку, маси тіла та індивідуальної реакції пацієнта, тяжкості симптомів захворювання у пацієнта тощо. Фармацевтичні композиції за цим винаходом можна вводити в організм різноманітними шляхами, в тому числі пероральним, ректальним, черезшкірним, підшкірним, внутрішньовенним, внутрішньом'язовим та назальним. Композиції для перорального застосування можуть мати форму нефасованих рідких розчинів або суспензій, або нефасованих порошків. Більш розповсюдженим, однак, є виготовлення композицій у формі дозованих одиниць із метою спрощення точного дозування. Термін "дозовані одиниці" означає фізично дискретні одиниці, придатні як одиничні дози для людей та інших ссавців, причому кожна з одиниць містить заздалегідь визначену кількість активного матеріалу, розраховану на досягнення бажаного терапевтичного ефекту, у поєднанні з придатними фармацевтичними допоміжними речовинами. До типових дозованих одиниць належать попередньо наповнені відміряною кількістю композиції ампули або шприци з рідкими композиціями або пілюлі, таблетки, капсули тощо у випадку твердих композицій. В таких композиціях тіазолідиндіонова похідна конденсованого вінілбензолу є звичайно неосновним компонентом (від приблизно 0,1% (мас.) до приблизно 50% (мас.) або за варіантом, якому віддається перевага, від приблизно 1% (мас.) до приблизно 40% (мас.)), при цьому решту складають різноманітні середовища або носії та технологічні домішки, які сприяють виготовленню бажаної дозованої лікарської форми. Рідкі форми, придатні для перорального застосування, можуть містити придатні водні або неводні носії з буферними сполуками, суспензаторами та диспергаторами, барвниками, ароматизаторами тощо. Тверді форми можуть містити, наприклад, будь-які з перелічених нижче інгредієнтів або сполуки * аналогічної природи: в'яжучі, наприклад, мікрокристалічну целюлозу, трагант або же 41 79793 латин; наповнювачі, наприклад, крохмаль або лактозу; дезінтегратори, наприклад, альгінову кислоту, Primogel або кукурудзяний крохмаль; змащувальні агенти, наприклад, стеарат магнію; ковзні агенти, наприклад, колоїдний діоксид кремнію; підсолоджувачі, наприклад, сахарозу або сахарин; або смакоароматичні домішки, наприклад, м'яту, метилсаліцилат або цитрусовий ароматизатор. Розчини для ін'єкцій виготовляють, як правило, на основі стерильного ін'єкційного сольового розчину або сольового розчину з фосфатним буфером, або інших носіїв для ін'єкцій, відомих у галузі. Як вказано вище, тіазолідиндіонова похідна конденсованого вінілбензолу формули (І) в таких композиціях є звичайно неосновним компонентом, вміст якого часто становить від 0,05% (мас.) до 10% (мас), а решту становить носій для ін'єкцій тощо. Описані вище компоненти композицій для перорального застосування та для ін'єкцій є лише типовими прикладами. Подальші відомості про матеріали, а також способи оброблення тощо можна знайти [в Розділі 5 мoнoгрaфiї Remington's Pharmaceutical Sciences, 20th Edition, 2000, Marck Publishing Company, Easton, Pennsylvania], яку включено до цього опису шля хом посилання. Сполуки за цим винаходом можуть бути застосовані також у лікарських формах із модифікованим вивільненням або в терапевтичних системах із модифікованим вивільненням. Опис типових форм із модифікованим вивільненням також можна знайти в мoнoгрaфїї Remington's Pharmaceutical Sciences. Цей винахід нижче ілюстровано деякими приПриклад 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 42 кладами, які не слід розглядати як такі, що обмежують обсяг винаходу. У поданих нижче прикладах застосовано такі абревіатури: хв (хвилини), год (години), г (грами), ммоль (мілімолі), т.пл. (температура плавлення), екв. (еквіваленти), мл (мілілітри), мкл (мікролітри), ACN (ацетонітрил), Вос (бутоксикарбоніл), Cbz (карбоксибензил), CDCI3 (дейтерований хлороформ), сНех (циклогексан), dba (дибензиліденацетон), DCM (дихлорметан), DEAD (діетилазодікарбоксилат), DIC (діізопропілкарбодіімід), DIEA (діізопропілетиламін), DMAP (4диметиламінопіридин), DME (диметоксіетан), DMF (диметилформамід), DMSO (диметилсульфоксид), DMSO-d6 (дейтерований диметилсульфоксид), EDC (гідрохлорид 1-(3-диметиламінопропіл)-3етилкарбодііміду), EtOAc (етилацетат), Et2O (діетиловий простий ефір, Fmoc (9-флуоренілметоксикарбоніл), HOBt (1-гідроксибензотриазол), K2СО3 (карбонат калію), MgSO4 (сульфат магнію), MsCl (метилсульфонілхлорид), МТВЕ (третбутилметиловий простий ефір), NaH (гідрид натрію), NaHCO3 (бікарбонат натрію), nBuLi (nбутиллітій), РСС (хлорхромат піридинію), РЕ (петролейний ефір), QCl (тетрабутиламонійхлорид), к.т. (кімнатна температура), TBTU (Обензотриазоліл-N,N,N',N'-тетраметилуронійтетрафторборат), TEA (триетиламін), TFA (трифтороцтова кислота), THF (тетрагідрофуран), TMOF (триметилортоформіат), TMAD (N,N,N',N'тетраметилазодікарбоксамід), TosCl (толуолсульфонілхлорид). Приклади: Нижче подано перелік сполук, які були синтезовані відповідно до описаних нижче методик: Назв а 5-(1,3-бензодіоксол-5-ілметилен)-1,3-тіазолідин-2,4-діон 5-(1,3-бензодіоксол-5-ілметилен)-2-тіоксо-1,3-тіазолідин-4-он 5-(2,3-дигідро-1,4-бензодіоксин-6-ілметилен)-1,3-тіазолідин-2,4-діон 5-(2,3-дигідро-1-бензофуран-5-ілметилен)-1,3-тіазолідин-2,4-діон 5-[(7-метокси-1,3-бензодіоксол-5-іл)метилен]-1,3-тіазолідин-2,4-діон 5-[(9,10-діоксо-9,10-дигідроантрацен-2-іл)метилен]-1,3-тіазолідин-2,4-діон (5-[(2,2-дифтор-1,3-бензодіоксол-5-іл)метилен]-1,3-тіазолідин-2,4-діон (5г)-5-(1,3-дигідро-2-бензофуран-5-ілметилен)-1,3-тіазолідин-2,4-діон 5-(1-бензофуран-5-ілметилен)-1,3-тіазолідин-2,4-діон 5-[(4-метил-3-оксо-3,4-дигідро-2Н-1,4-бензоксазин-6-іл)метилен]-1,3-тіазолідин-2,4-діон 5-(1,3-бензодіоксол-5-ілметилен)-2-іміно-1,3-тіазолідин-4-он 5-хінолін-6-ілметилен-тіазолідин-2,4-діон 5-хінолін-6-ілметилен-2-тіоксо-тіазолідин-4-он 2-іміно-5-хінолін-6-ілметилен-тіазолідин-4-он 5-(3-метріл-бензо[(і]ізоксазол-5-ілметилен)-тіазолідин-2,4-діон 5-(4-феніл-хіназолін-6-ілметилен)-тіазолідин-2,4-діон 5-(4-диметиламіно-хіназолін-6-ілметилен)-тіазолідин-2,4-діон 5-[(4-амінохіназолін-6-іл)метилен]-1,3-тіазолідин-2,4-діон 5-[(4-піперв дин-1-ілхіназолін-6-іл)метилен]-1,3-тіазолідин-2,4-діон 5-[(4-морфолін-4-ілхіназолін-6-іл)метилен]-1,3-тіазолідин-2,4-діон 5-{[4-(бензиламіно)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-{[4-(діетиламіно)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-({4-[(піридин-2-ілметил)аміно]хіназолін-6-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({4-[(піридин-3-ілметил)аміно]хіназолін-6-іл}метилен)-1,3-тіазолідин-2,4-діон етил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]хіназолін-4-іл}піперидин-3-карбоксилат етил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]хіназолін-4-іл}піперидин-4-карбоксилат трет-бутил-1-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-хіназолін-4-іл}-L-пролінат 5-{[4-(4-метилпіперазин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-{[4-(4-піримідин-2-ілпіперазин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-({4-[4-(4-фторфеніл)піперидин-1-іл]хіназолін-6-іл}метилен)-1,3-тіазолідин-2,4-діон 43 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 79793 44 5-{[4-(4-бензилпіперидин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-({4-[4-(2-фенілетил)піперидин-1-іл]хіназолін-6-іл}метилен)-1,3-тіазолідин-2,4-діон 5-{[4-(4-метилпіперидин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-{[4-(4-гідроксипіперв дин-1-іл)хіназолін-6-іл]метилен}-1,3-тіазолідин-2,4-діон 1-[6-(2,4-діоксо-тіазолідин-5-іліденметил)-хіназолін-4-іл]-піперидин-4-карбонов а кислота 1-[6-(2,4-діоксо-тіазолідин-5-іліденметил)-хіназолін-4-іл]-піперв дин-3-карбонов а кислота 1-[6-(2,4-діоксо-тіазолідин-5-іліденметил)-хіназолін-4-іл]-піролідин-2-карбонов а кислота 5-(4-метиламіно-хіназолін-6-ілметилен)-тіазолідин-2,4-діон 5-(4-метокси-хіназолін-6-ілметилен)-тіазолідин-2,4-діон 2-іміно-5-(4-метиламіно-хіназолін-6-ілметилен)-тіазолідин-4-он 2-іміно-5-(4-піперидин-хіназолін-6-ілметилен)-тіазолідин-4-он 2-іміно-5-(4-диметиламіно-хіназолін-6-ілметилен)-тіазолідин-4-он 5-(2-метил-2Н-бензотриазол-5-ілметилен)-тіазолідин-2,4-діон 5-(3-метил-3Н-бензотриазол-5-ілметилен)-тіазолідин-2,4-діон 5-(3-етил-3Н-бензимідазол-5-ілметилен)-тіазолідин-2,4-діон 5-{[1-(4-фенілбутил)-1Н-бензимідазол-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-[(1-проп-2-ін-1-іл-1Н-бензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4-діон 5-[(1-{2-[4-(трифторметил)феніл]етил}-1Н-бензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4-діон 5-({1-[2-(4-гідроксифеніл)етил]-1Н-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діон метил-4-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1Н-бензимідазол-1-іл}циклогексанкарбоксилат 5-({1-[2-(5-метокси-1Н-індол-3-іл)етил]-1Н-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({1-[(1-метил-1Н-піразол-4-іл)метил]-1Н-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({1-[2-(3,4-диметоксифеніл)етил]-1Н-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({1-[2-(4-феноксифеніл)етил]-1Н-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({1-[4-(трифторметил)бензил]-1Н-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діон 4-{6-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1Н-бензимідазол-1-іл}циклогексанкарбонов а кислота 5-[(1-ізобутил-1Н-бензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4-діон 5-({1-[2-(1,3-бензодюксол-4-іл)етил]-1Н-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({1-[2-(2-феноксифеніл)етил]-1Н-бензимідазол-6-іл}метилен)-1,3-тіазолідин-2,4-діон 5-{[1-(3,3-дифенілпропіл)-1Н-бензимідазол-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-{[1-(2-метоксибензил)-1Н-бензимідазол-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-{[1-(3-фурилметил)-1Н-бензимідазол-6-іл]метилен}-1,3-тіазолідин-2,4-діон 5-[(1-пропіл-1Н-бензимідазол-6-іл)метилен]-1,3-тіазолідин-2,4-діон 5-хіноксалін-6-ілметилен-тіазолідин-2,4-діон 5-хіноксалін-6-ілметилен-2-тіоксо-тіазолідин-4-он 2-іміно-5-хіноксалін-6-ілметилен-тіазолідин-4-он 5-бензотіазол-6-ілметилен-тіазолідин-2,4-діон 5-(3-метил-бензофуран-5-ілметилен)-тіазолідин-2,4-діон 5-(2-бром-3-метил-бензофуран-5-ілметилен)-тіазолідин-2,4-діон 5-(3-бром-бензофуран-5-ілметилен)-тіазолідин-2,4-діон етилов ий складний ефір 3-[5-(2,4-діоксо-тіазолідин-5-іліденметил)-бензофуран-3-іл]-акрилов ої кислоти 3-[5-(2,4-діоксо-тіазолідин-5-іліденметил)-бензофуран-3-іл]-акрилов а кислота 5-[3-(3-оксо-3-піперидин-1-іл-пропеніл)-бензофуран-5-ілметилен]-тіазолідин-2,4-діон метил-1-((3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)пролінат метил-1-((3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)-В-пролінат (5-({3-[(3-оксо-3-піролідин-1-ілпроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({3-[3-морфолін-4-іл-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діон метил-1-(3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}проп-2-еноїл)-L-пролінат N-циклогексил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}-N-метилакриламід 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}-N-етил-N-(2-гідроксіетил)акриламід N-циклобутил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}акриламід 5-({3-[3-азетидин-1-іл-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({3-[3-(1,3-дигідро-2Н-ізоіндол-2-іл)-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діон 5-({3-[3-азепан-1-іл-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діон 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}-N-піперв дин-1-ілакриламід 3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}-N-(піридин-3-ілметил)акриламід N-циклогексил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}акриламід 5-({3-[3-(4-метилпіперазин-1-іл)-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діон N-циклогептил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}акриламід 5-({3-[3-(2,5-дигідро-1H-пірол-1-іл)-3-оксопроп-1-ен-1-іл]-1-бензофуран-5-іл}метилен)-1,3-тіазолідин-2,4-діон N-циклопентил-3-{5-[(2,4-діоксо-1,3-тіазолідин-5-іліден)метил]-1-бензофуран-3-іл}акриламід етилов ий складний ефір 3-[5-(2,4-діоксо-тіазолідин-5-іліденметил)-бензофуран-3-іл]-пропіонов ої кислоти 3-[5-(2,4-діоксо-тіазолідин-5-іліденметил)-бензофуран-3-іл]-пропіонов а кислота 5-[3-(3-оксо-3-піперидин-1-іл-пропіл)-бензофуран-5-ілметилен]-тіазолідин-2,4-діон трет-бутилов ий складний ефір 6-(2,4-діоксо-тіазолідин-5-іліденметил)-2,3-дигідро-бензо[1,4]оксазин-4-карбонова кислота 5-(3,4-дигідро-2Н-бензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4-діон 5-(4-бензоїд-3,4-дигідро-2Н-бензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4-діон 5-(4-ацетил-3,4-дигідро-2Н-бензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4-діон 45 99 100 101 102 103 104 105 106 107 108 109 110 111 112 79793 46 трет-бутилов ий складний ефір 6-(2,4-діоксо-тіазолідин-5-іліденметил)-бензо[1,4]оксазин-4-карбонов ої кислоти метилов ий складний ефір [6-(2,4-дюксо-тіазолідин-5-іліденметил)-3-оксо-2,3-дигідро-бензо[ 1,4]-оксазин-4іл]-оцтов ої кислоти N-бензил-2-[6-(2,4-діоксо-тіазолідин-5-іліденметил)-3-оксо-2,3-дигідро-бензо[1,4]оксазин-4-іл]-ацетамід 5-(4-бутил-3-оксо-3,4-дигідро-2Н-бензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4-діон 5-(4-бензил-3-оксо-3,4-дигідро-2Н-бензо[1,4]оксазин-6-ілметилен)-тіазолідин-2,4-діон 5-(2-хлор-бензофуран-5-ілметилен)-тіазолідин-2,4-діон 5-(3-аміно-бензо[d]ізоксазол-5-ілметилен)-тіазолідин-2,4-діон 5-(3-фенілетиніл-бензофуран-5-ілметилен)-тіазолідин-2,4-діон 5-бензо[1,2,5]тіадіазол-5-ілметилен-тіазолідин-2,4-діон 5-бензо[1,2,5]оксадіазол-5-ілметилен-тіазолідин-2,4-діон 5-(2-метил-бензофуран-6-ілметилен)-тіазолідин-2,4-діон 5-(2-карбоксиметил-бензофуран-6-ілметилен)-тіазолідин-2,4-діон 5-(3-бром-2-фтор-2,3-дигідро-бензофуран-6-ілметилен)-тіазолідин-2,4-діон 5-(2-фтор-бензофуран-6-ілметилен)-тіазолідин-2,4-діон На ринку наявні перелічені нижче проміжні альдегіди: 2,2-дифтор-1,3-бензодіоксол-5карбоксальдегід, 1,3-бензодіоксол-5карбоксальдегід, 1,4-бензодіоксан-6карбоксальдегід, 9,10-діоксо-9,10-дигідроантрацен-2-карбальдегід, 2,3-дигідробензо[b]фуран-5-карбоксальдегід, 3-метокси-4,5метилендіоксибензальдегід. Тіазолідиндіон та роданін наявні на ринку. Проміжні альдегіди синтезували за методикою, описаною нижче. Характеристики HPLC, ЯМР та МС, вказані у поданих нижче прикладах, одержано в таких умовах: HPLC: колонка Waters Symmetry C8 50x4,6мм, елюент: MeCN/H2O, 5®100% (8хв.), детектування на довжині хвилі 230-400нм; мас-спектри: PESCIEX АРІ 150 ЕХ (АРСІ та ESI), LC/MS спектри: Waters ZMD (ES); 1H-ЯМР: Bruker DPX-300МГц. Для очищення застосовували такі умови: препаративний xpoмaтoгрaф HPLC Waters Prep LC 4000 System, обладнаний колонками Prep NovaPak®HR C186мкм 60Å, 40´30мм (до 100мг) або 40´300мм (до 1г). При очищенні у всіх випадках застосовували грaдiєнтнe елюювання MeCN/Н2O з домішкою 0,09% TFA. Проміжна сполука 1: одержання 5-форміл-1бензофурану Стадія І: етил-2-форміл-4-бромфеноксіацетат: Суміш 5-бромсаліцилальдегіду (50г, 0,248моль), етилбромацетату (42г, 0,248моль) та K2СО3 (68г, 0,49моль) у безводному DMF (200мл) перемішували при кімнатній температурі протягом 12год. Реакційну суміш фільтрували, і фільтрат розводили водою. Одержану суміш екстрагували діетиловим простим ефіром (4´200мл), промивали розсолом та концентрували, одержуючи неочищений етил-2-форміл-4-бромфеноксіацетат (64г, 90%) у вигляді твердої речовини. Стадія II: 4-бром-2-формілфеноксіоцтова кислота: Суміш етил-2-форміл-4-бромфеноксіацетату (60г, 0,209моль), LiOH (7,5г, 0,31моль), THF (250мл) та води (100мл) перемішували при кімнатній температурі протягом 24год. Реакційну суміш концентрували під зниженим тиском, і залишок підкислювали 1,5-н. НСl до рН=2. Одержаний твердий осад фільтрували та сушили, одержуючи 4бром-2-формілфеноксіоцтову кислоту (50г, 94%). Стадія III: 5-бром-1-бензофуран: До суміші 2-форміл-4-бромфеноксіоцтової кислоти (50г, 0,192моль), ацетату натрію (100г, 1,21моль) в оцтовій кислоті (250мл) при 100°С додавали частинами оцтовий ангідрид (100мл) протягом 3год. Реакційну суміш потім нагрівали зі зворотним холодильником протягом 20год. Розчинник видаляли дистилюванням, і залишок розводили 3-н. НСl (500мл) та нагрівали зі зворотним холодильником протягом 2год. Реакційну суміш потім концентрували у вакуумі, і продукт екстрагували петролейним простим ефіром (3´200мл). Органічний шар промивали 10% розчином NaHCO3 та випарювали, одержуючи 5-бром-1бензофуран (15г, 40%) у вигляді блідо-жовтої рідини. Стадія IV: 5-форміл-1-бензофуран (Р1а на схемі 2 для прикладу 9): Суміш 5-бром-1-бензофуран (0,5г), мг (0,92г, 0,038моль), І2 (1 кристал) у безводному THF (2,5мл) у атмосфері азоту назвали зі зворотним холодильником протягом 30хв. До неї додавали розчин 5-бром-1-бензофурану (4,5г) у 25мл безводного THF) як тільки зникало забарвлення І2 та назвали зі зворотним холодильником протягом додаткових 2год. Реакційну суміш потім охолоджували до -40°С, додавали краплями безводний DMF (3,6г) та повільно нагрівали до кімнатної температури протягом 12год. Реакційну суміш потім охолоджували до 0°С, підкислювали 3-н. НСl до рН=2 та перемішували протягом 30хв. Потім реакційну суміш розводили водою (500мл), екстрагували етилацетатом (2´200мл), промивали розсолом та сушили. Розчинник видаляли у вакуумі та очищали хроматографією на колонці із силікагелем (елюент суміш петролейного простого ефіру з СН2СІ2), одержуючи 5-форміл-1-бензофуран (2г, 54%) у вигляді рідини. LC-MS: M/Z ESI: 1,47хв., 147,34 (М+1). Проміжна сполука 2: одержання 4-метил-3оксо-3,4-дигідро-2Н-бензо[1,4]оксазин-6карбальдегіду 47 79793 Стадія І: 2-(N-метиламіно)-фенол: 1г бензоксазолу розчиняли у 20мл THF. Додавали 0,9г NаВH4 у атмосфері азоту та перемішували. Одержану супензію охолоджували до 0°С, і повільно додавали 0,86мл оцтової кислоти, розчиненої в 5мл THF, підтримуючи температур у реакції нижче 5°С. Реакційну суміш перемішували при 0°С протягом 30хв. і протягом додаткових 12год. при кімнатній температурі. Реакційну суміш знову охолоджували до 0°С, і обережно додавали 50мл насиченого розчину NH4CI. Одержані фази розділяли, і водний шар двічі екстрагували EtOAc. Об'єднані органічні шари промивали розсолом, сушили над MgSO4 та фільтрували. Видаляли розчинник, і одержували 0,97г чистого 2-(Nметиламіно)-фенолу. Стадія II: 4-метил-4Н-бензо[1,4]оксазин-3-он 1г 2-(N-метиламіно)-фенолу розчиняли у хлороформі, після чого додавали 10мл насиченого розчину NaHCO3 у воді. До цієї суспензії повільно додавали при інтенсивному перемішуванні розчин 1г 2-хлорацетилхлориду у ацетоні. Реакційну суміш перемішували протягом 2год. при кімнатній температурі. Шари розділяли. Органічний шар промивали водою та сушили над Na2SO4. Після випарювання розчинника одержане червоне масло розчиняли у 30мл DMF і додавали 1г K2СО3, одержану суспензію назвали при 70°С протягом додаткових 2год. Процес замикання циклу контролювали методом ТІПХ. Додавали 200мл EtOAc, і органічний шар промивали 3´0,1-н. НСl та 5´ розсолом. Органічний залишок сушили над MgSO 4 та фільтрували. EtOAc видаляли під зниженим тиском, одержуючи 1,45г чистого 4-метил-4Нбензо[1,4]оксазин-3-ону. Стадія III: 4-метил-3-оксо-3,4-дигідро-2Нбензо[1,4]оксазин-6-карбальдегід 1г АІСІ 3 суспендували у 10мл DCM, додавали 0,5мл нітрометану для розчинення АІСІ3, і одержаний розчин охолоджували до 0°С. До згаданого розчину додавали 4-метил-4Н-бензо[1,4]оксазин-3он (0,5г, 3,06ммоль), розчинений у DCM, і перемішували протягом 15хв. при 0°С. До цього розчину додатково додавали 0,36мл біс-хлорметилметилового простого ефіру в DCM. Реакційну суміш перемішували при 0°С протягом 15хв. та при кімнатній температурі протягом 3год. Цю неочищену реакційну суміш потім виливали на лід, шари розділяли, і органічну фазу промивали NaHCO3 та розсолом. Сушили над MgSO4 і фільтрували, після чого розчинник випарювали, одержуючи 0,43г неочищеного продукту. Темне масло очищали флеш-xpoмaтoгрaфiєю із застосуванням EtOAc та циклогексану як елюентів, одержуючи 0,2г (37%) 4метил-3-оксо-3,4-дигідро-2Н-бензо[1,4]оксазин-6карбальдегіду у вигляді безбарвної твердої речовини. HPLC: 2,07хв. LC-MS: M/Z ESI: 1,31хв., 192,28 (М+1). Проміжна сполука 3: одержання 4-метил-3,4дигідро-2Н-бензо[1,4] оксазин-7-карбальдегіду 48 Стадія І: 4-метил-3,4-дигідро-2Нбензо[1,4]оксазин Розчиняли 0,97г 2-(N-метиламіно)-фенолу у 50мл ацетону, після чого додавали 2г K2СО 3, розчиненого у воді. До цієї суспензії повільно додавали розчин 2,66г диброметану у ацетоні. Реакційну суміш перемішували протягом 22год. при нагріванні зі зворотним холодильником. Ацетон випарювали, додавали 200мл EtOAc, і органічний шар промивали 3´0,1-н. НСl та 3´ розсолом. Органічний залишок сушили над MgSO4 і фільтрували. EtOAc видаляли під зниженим тиском, одержуючи 1г чистого 4-метил-3,4-дигідро-2Н-бензо [1,4] оксазину. Стадія II: 4-метил-3,4-дигідро-2Нбензо[1,4]оксазин-7-карбальдегід 4-метил-3,4-дигідро-2Н-бензо[1,4]оксазин розчиняли у 200мкл DMF у атмосфері аргону. Додавали РОСІ3 у атмосфері аргону. Реакційну суміш нaгрiвaли у закритій пробірці при 90° С протягом 75хв. Додавали 1мл NaAc у воді та перемішували, доки не утворилося коричневе масло. Це масло екстрагували DCM. Органічний шар промивали розсолом, сушили та випарювали до сухості, одержуючи 0,18г (76%) 4-метил-3,4-дигідро-2Нбензо[1,4]оксазин-7-карбальдегіду у вигляді безбарвної твердої речовини. LC-MS: M/Z ESI: 1,37хв, 178,35 (М+1). Проміжна сполука 4: одержання 1,3дигідроізобензофуран-5-карбальдегід Стадія І (1.3-дигідро-ізобензофуран-5-іл)метанол У круглодонну колбу із зрошувальним конденсором завантажували 1,0г 3-проп-2-інілоксипропіну та 2,08г пропаргілового спирту у 10мл етанолу, після чого додавали 9,8мг хлориду трис(трифенілфосфін)родію (каталізатор Вілкінсона (Wilkinson)) при кімнатній температурі. Реакційну суміш назвали до 70°С, в той час як колір реакційної суміші швидко ставав жовтим. Після 1 доби перемішування при кімнатній температурі, ТШХ аналіз посвідчив завершення перетворення вихідних матеріалів. Розчинник випарювали, розводили DCM та екстрагували Н 2О, сушили над MgSO4 Коричневу суміш очищали флeш-xpoмaтoгрaфiєю, використовуючи як рухому фазу суміш 8/2 циклогексан/AcOEt, і одержували (1,3-дигідроізобензофуран-5-іл)-метанол у вигляді безбарвної чистої твердої речовини (0,92г, 60%). Стадія II: 1.3-дигідроізобензофуран-5карбальдегід (1,3-дигідро-ізобензофуран-5-іл)-метанол (440мг, 2,9ммоль) розчиняли у 20мл DCM. Додавали 1,1,1-триацетокси-1,1-дигідро-1,2бензйодоксол-3(1Н)-он (реагент Десса-Мартіна (Dess-Martin)) (1,3г, 3,2ммоль), і реакційну суміш 49 79793 перемішували при кімнатній температурі протягом 4год. Реакційну суміш розводили простим ефіром, екстрагували 2´1-н. NaOH, 2´Η2Ο і сушили над MgSO4 . Неочищений продукт, що мав достатній ступінь чистоти, використовували без будь-якого додаткового очищення. HPLC: 2,00хв. LC-MS: M/Z ESI: 1,50хв., 149,18 (М+1). Проміжна сполука 5: одержання хінолін-6карбальдегіду Стадія І: хінолін-6-іл-метанол Розчиняли 5г метилхінолін-6-карбоксилату у безводному THF. У атмосфері аргону додавали 1М LiАІH4 у THF (2екв.) при -20°С. Одержаний розчин перемішували при цій температурі протягом 1год. Повільно додавали ізопропанол, неочищений продукт фільтрували через целіт та промивали DCM. Концентрували і одержувми 3,6г (85%) чистого спирту. HPLC: 1,10хв. LC-MS: M/Z ESI: 0,91хв, 160,43 (М+1). Стадія II: хінолін-6-карбальдегід Розчиняли 2г хінолін-6-іл-метанолу в DCM. Додавали 15г МnО2, і реакційну суміш перемішували протягом 5год. Неочищений продукт фільтрували через целіт та екстенсивно промивали DCM. Концентрували і одержували 1,85г (93%) чистого альдегіду. HPLC: 0,8хв. LC-MS: M/Z ESI: 1,07хв., 158,37 (M+1). 1 H ЯМР (DMSO-d6) δ 10,19 (s, 1Н), 9,06 (t, J=3Гц, 1H), 8,6-8,66 (m, 2H), 8,15 (s, 2H), 7,68 (dd, J=3Гц, 9Гц, 1H). Нижченаведені проміжні сполуки синтезували відповідним чином із використанням придатних вихідних матеріалів. Проміжна сполука 6: одержання 3-метилбензо[d]ізоксазол-5-карбальдегіду HPLC: 2,06хв. LC-MS: M/Z ESI: 1,26хв, 162,31 (М+1). 1Н Я МР (DMSO-d 6) δ 10,10 (s, 1Н), 8,52 (s, 1H), 8,16 (d, J=12Гц, 1H), 8,15 (s, 2H), 7,90 (d, J=9Гц, 1H), 2,63 (s, 3H). Проміжна сполука 7: одержання метилового складного ефіру 4-хлор-хіназолін-6-карбонової кислоти Стадія І: 4-нітроізофталева кислота Суміш 3-метил-4-нітробензойної кислоти (150г, 0,825моль), піридину (1,5л) та води (1,5л) нагрівали до кипіння. До цієї гарячої реакційної суміші частинами додавали КМпО4 (10моль) та нагрівали зі зворотним холодильником протягом 72год. Цю гарячу реакційну суміш фільтр ували через целіт та промивали гарячою водою. Фільтрат концентрува 50 ли у вакуумі, залишок розводили водою (750мл) та підкислювали концентрованою НСl при 0°С. Одержану тверду речовину фільтрували, промивали водою та сушили у вакуумі, одержуючи 4нітроізофталеву кислоту (98г, 56%). ТШХ, хлороформ/метанол, 7:3, Rf=0,2. Стадія II: 4-аміноізофталева кислота До розчину 4-нітроізофталевої кислоти (98г, 0,457моль) у метанолі (5л) додавали Pd/C (20%) та гідрогенізували при кімнатній температурі протягом 4год. Реакційну суміш фільтрували через целіт, і фільтрат концентрували у вакуумі, одержуючи 4-аміноізофталеву кислоту (72г, 87%) у вигляді твердої речовини. ТШХ, хлороформ/метанол, 7:3, Rf=0,4. Стадія IIІ: 4-оксо-3.4-дигідрохіназолін-6карбонова кислота Суміш 4-аміноізофталевої кислоти (17г, 0,093моль) та формаміду (85мл) нагрівали при 180°С протягом 5год. Реакційну суміш охолоджували до кімнатної температури та додавали ацетон. Одержаний таким чином твердий осад перемішували протягом 2год, фільтрували та сушили, одержуючи 4-оксо-3,4-дигідрохіназолін-6карбонову кислоту (11г, 61%). ТШХ, хлороформ/метанол, 8:2, Rf=0,25. Стадія IV: 4-оксо-3.4-дигідрохіназолін-6метилкарбоксилат До розчину 4-оксо-3,4-дигідрохіназолін-6карбонової кислоти (24г, 0,126моль) у безводному метанолі (800мл) додавали тіонілхлорид (37г) при 5°С, і потім нагрівали зі зворотним холодильником при 80°С протягом 5год. Реакційну суміш концентрували у вакуумі і неочищеною розчиняли у етилацетаті (250мл). Органічний шар промивали 10% водним розчином NaHCO3, водою, розсолом та сушили. Розчинник видаляли у вакуумі, одержуючи 4-оксо-3,4-дигідрохіназолін-6-метилкарбоксилат (24г, 92%) у ви гляді твердої речовини. ТШХ, хлороформ/метанол, 8:2, Rf=0,6. Стадія V: метил-4-хлорхіназолін-6-карбоксилат Суміш 4-оксо-3,4-дигідрохінолін-6метилкарбоксилату (12г, 0,058моль) та фосфорилхлориду (180мл) нафівали зі зворотним холодильником протягом 7год. Надлишок фосфорилхлориду відганяли, і неочищений продукт розчиняли у етилацетаті (250мл). Органічний шар промивали 10% водним розчином NаНСО3, водою, розсолом та сушили. Розчинник видаляли у вакуумі, і неочищений продукт очищали хроматографією на колонці із силікагелем (елюент 30% етилацетату в петролейному простому ефірі), одержуючи метил4-хлорхіназолін-б-карбоксилат (4,5г, 34%) у вигляді твердої речовини. ТШХ, петролейний ефір/EtOAc, 1:1, R f=0,65. LC-MS: M/Z ESI: 1,50хв., 223,19 (М+1). 1H ЯМР (DMSO-d6) δ 8,66 (d, J=1,9Гц, 1H), 8,39 (s, 1H), 8,30 (dd, J=0,6Гц, 8,5Гц, 1H), 7,79 (d, J=8,5Гц, 1H), 3,90 (s, 3H). Проміжна сполука 8: одержання метилового складного ефіру 4-метокси-хіназолін-б-каобонової кислоти 51 79793 Розмішували 200мг метил-4-хлорхінолін-6карбоксилату в 5мл МеОН у присутності 1екв. DIEA при 60°С протягом 24год. МеОН випарювали, і одержаний неочищений залишок розчиняли у EtOAc та промивали NH4Cl, одержуючи білу тверду речовину в достатній мірі чисту для наступної стадії. HPLC: 2,3хв. LC-MS: M/Z ESI: 1,19хв., 219,17 (М+1). Нижченаведені проміжні сполуки синтезували за методикою синтезу проміжної сполуки 8: Проміжна сполука 9: одержання метилового складного ефіру 4-метиламіно-хіназолін-6карбонової кислоти HPLC: 1,12хв. LC-MS: M/Z ESI: 1,06хв., 218,31 (М+1). Проміжна сполука 10: одержання 4-метоксихіназолін-6-карбальдегіду Цю проміжну сполуку одержали за методикою синтезу проміжної сполуки 5 із використанням метилового складного ефіру 4-метокси-хіназолін-6карбонової кислоти як вихідної сполуки. HPLC: 1,41хв. LC-MS: M/Z ESI: 1,24хв., 189,31 (М+1). Проміжна сполука 11: одержання 4метиламіно-хіназолін-6-карбальдегіду Цю проміжну сполуку одержали за методикою синтезу проміжної сполуки 5 із використанням метилового складного ефіру 4-метиламіно-хіназолін6-карбонової кислоти як вихідної сполуки. HPLC: 1,3хв. LC-MS: M/Z ESI: 0,90хв., 188,34 (М+1). Проміжна сполука 12: одержання 4-хлорхіназолін-6-карбальдегіду Стадія І: 4-хлорхіназолін-6-ілметанол До розчину метил-4-хлорхіназолін-6карбоксилату (3,5г, 0,015моль) у безводному THF (35мл) при -25°С додавали DIBAL-H (4,4г, 0,031моль) та перемішували при кімнатній температурі протягом 2год. Реакційну суміш охолоджували до -10°С, і гасили реакцію 10% водним роз 52 чином NaНСО3 (9мл). Реакційну суміш екстрагували етилацетатом (100мл), промивали водою, розсолом та сушили. Розчинник видаляли у вакуумі, одержуючи 4-хлорхінолін-6-іл метанол (2г, 66%). ТШХ, хлороформ/метанол, 8:2, Rf=0,35. Стадія II : 4-xлopxiнaзoлiн-6-кapбoкcальдeгiд До розчину 4-хлорхіназолін-6-іл-метанолу (3,5г, 0,018моль) у безводному СН 2Сl2 (100мл) додавали перйодатний реактив Десса-Мартіна (8,4г, 0,019моль) і перемішували при кімнатній температурі протягом 30хв. Реакційну суміш промивали 10% водним розчином NaНСО3 (75мл), водою, розсолом і сушили. Розчинник видаляли у вакуумі, одержуючи 4-хлорхіназолін-6карбоксальдегід (3г, 88%) у вигляді блідо-жовтої твердої речовини. ТШХ, хлороформ/метанол, 9:1, Rf=0,6. Проміжна сполука 13: одержання 4-фенілхіназолін-6-карбальдегіду 4-хлор-хіназолін-6-карбальдегід (50мг, 0,26ммоль), Рd(РРh3)4 (13мг, 0,01ммоль), фенілборну кислоту (63мг, 0,52ммоль) та карбонат натрію (насичений розчин: 50мкл) назвали в толуолі при 100°С протягом 12год. Після випарювання розчинників, одержаний залишок розчиняли у етилацетаті і промивали розсолом двічі. Потім органічні фази концентрували, і первісний матеріал очищали на силікагелі, використовуючи суміш DCM/EtOH 95:5 як елюент, одержуючи 50мг (82%) бажаної сполуки з 85% чистотою. HPLC: 2,68хв. LC-MS: M/Z ESI: 1,25хв., 235,30 (М+1). Проміжна сполука 14: одержання 4диметиламіно-хіназолін-6-карбальдегіду 4-хлор-хіназолін-6-карбальдегід (200мг, 1ммоль) розчиняли у 10мл діоксану. До цього розчину додавали розчин диметиламіну у воді (5екв.). Одержану суміш перемішували протягом 2год. при кімнатній температурі. Випарювали розчинники, видаляли амін у високому вакуумі, і одержували чистий 4-диметиламіно-хіназолін-6-карбальдегід у вигляді жовтої твердої речовини, яку використовували на наступній стадії без додаткового очищення (190мг, вихід 91%). HPLC: 0,91хв. LC-MS: M/Z ESI: 1,23хв., 202,33 (М+1). 1H ЯМР (CDCI3): δ 10,19 (s, 1Н), 8,70 (s, 1H), 8,50 (d, J=3Гц, 1H), 8,15 (dd, J=3Гц, 9Гц, 1Н), 7,88 (d, J=9Гц, 1Н). Нижченаведені проміжні сполуки синтезували аналогічним чином, використовуючи відповідні аміни як нуклеофіли. 53 № 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 79793 54 Проміжна сполука 4-піперидин-1-іл-хіназолін-6-карбальдегід 4-аміно-хіназолін-б-карбальдегід 4-бензиламіно-хіназолін-6-карбальдегід 4-[(піридин-2-ілметил)-аміно]-хіназолін-6-карбальдегід 4-[(піридин-3-ілметил)-аміно]-хіназолін-6-карбальдегід 4-(4-метил-піперазин-1-іл)-хіназолін-6-карбальдегід 4-діетиламіно-хіназолін-6-карбальдегід 4-морфолін-4-іл-хіназолін-6-карбальдегід етилов ий складний ефір 1-(6-форміл-хіназолін-4-іл)-піперидин-3-карбонов ої кислоти трет-бутилов ий складний ефір 1-(6-форміл-хіназолін-4-іл)-піролідин-2-карбонової кислоти етилов ий складний ефір 1-(6-форміл-хіназолін-4-іл)-піперидин-4-карбонов ої кислоти 4-(4-гідрокси-піперидин-1-іл)-хіназолін-6-карбальдегід 4-(4-метил-піперидин-1-іл)-хіназолін-6-карбальдегід 4-(4-фенетил-піперидин-1-іл)-хіназолін-6-карбальдегід 4-(4-бензил-піперидин-1-іл)-хіназолін-6-карбальдегід 4-[4-(4-фтор-феніл)-піперидин-1-іл]-хіназолін-6-карбальдегід 4-(4-піримідин-2-іл-піперазин-1-іл)-хіназолін-6-карбальдегід Проміжні сполуки 32: Одержання метилового складного ефіру метил-бензотриазол-5-карбонової кислоти Розчиняли 1г метилового складного ефіру бензотриазол-5-карбонової кислоти (5,64ммоль) у 20мл DMF при 0°С. До цього розчину додавали 1екв. NaH (60%) при 0°С. Одержану суміш перемішували протягом 30хв. при 0°С, повільно додавали 801 мг (1екв.) метилйодиду, і одержану реакційну суміш перемішували протягом 2 год при кімнатній температурі. Додавали EtOAc, органічний шар промивали великими кількостями розсолу та води, сушили над MgSO4 та фільтрували, одержуючи 1г неочищеного метилового складного ефіру метил-бензотриазол-5-карбонової кислоти у вигляді трьох різних регіо-ізомерів. Розділення виконували на силікагелі, використовуючи суміш EtOAc/CH 3:7 як елюент. Проміжна сполука 32а: метиловий складний ефір 2-метил-2Н-бензотриазол-5-карбонової кислоти Метиловий складний ефір 2-метил-2Нбензотриазол-5-карбонової кислоти елюювали як першу фракцію (250мг, 22%). HPLC: 2,32хв. 1Н ЯМР (D MSO-d6) δ 8 ,56 (s, 1Н), 8,02 (d, J=9Гц, 1Н), 7,93 (d, J=9Гц, 1Н), 4,55 (s, 3H), 3,90 (s, 1H). Проміжна сполука 32b: метиловий складний ефір 3-метил-3Н-бензотриазол-5-карбонової кислоти Метиловий складний ефір З-метил-3Нбензотриазол-5-карбонової кислоти елюювали як другу фракцію (130мг, 12%). HPLC: 2,03хв. 1Н ЯМР (DMSO-d6) δ 8,56 (s, 1Н), 8,13 (d, J=6Гц, 1Н), 7,93 (d, J=9Гц, 1Н), 4,39 (s, 3H), 3,92 (s, 3H). Проміжна сполука 32с: метиловий складний ефір 1-метил-1Н-бензотриазол-5-карбонової кислоти M/Z ESI:(M+1) 242,27 174,18 264,30 265,33 265,33 257,31 230,28 244,26 314,36 328,39 314,36 258,30 256,32 346,42 332,40 336,38 321,36 Метиловий складний ефір 1-метил-1Нбензотриазол-5-карбонової кислоти елюювали як третю фракцію (135мг, 12%). HPLC: 2,03хв. 1Н ЯМР (D MSO-d6) δ 8 ,62 (s, 1Н), 8,11 (d, J=9Гц, 1H), 7,97(d, 9Гц, 1H), 4,35 (s, 3H), 3,90 (s, 3H). Проміжна сполука 33: 2-метил-2Нбензотриазол-5-карбальдегід Цю проміжну сполуку синтезували за методикою синтезу проміжної сполуки 5, використовуючи метиловий складний ефір 2-метил-2Нбензотриазол-5-карбонової кислоти (проміжна сполука 32а) як вихідну сполуку. HPLC: 1,88хв. 1Н ЯМР (DMSO-d6) δ 10,12 (s, 1Н), 8,65 (s, 1H), 8,06 (d, J=9Гц, 1H), 7,85 (d, J=9Гц, 1H), 4,57 (s, 3H). Проміжна сполука 34: 3-метил-3Нбензотриазол-5-карбальдегід Цю проміжну сполуку синтезували за методикою синтезу проміжної сполуки 5, використовуючи метиловий складний ефір 3-метил-3Нбензотриазол-5-карбонової кислоти (проміжна сполука 32b) як вихідну сполуку. HPLC: 1,49хв. 1Н ЯМР (DMSO-d6) δ 10,18 (s, 1Н), 8,54 (s, 1H), 8,20 (d, J=9Гц, 1H), 7,88(d, J=9Гц, 1H), 4,41 (s, 3H). Проміжна сполука 35: 1-метил-1Нбензотриазол-5-карбальдегід 55 79793 Цю проміжну сполуку синтезували за методикою синтезу проміжної сполуки 5, використовуючи метиловий складний ефір 1-метил-1Нбензотриазол-5-карбонової кислоти як вихідну сполуку (проміжна сполука 32с). HPLC: 1,49хв. LC-MS: M/Z ESI: 1,07хв., 162,32 (М+1). 1Н Я МР (DMSO-d 6) δ 10,13 (s, 1Н), 8,70 (s, 1H), 8,05 (s, 2H), 4,36 (s, 3H). Проміжна сполука 36: 5-(4-аміно-3-етиламінобензиліден)-тіазолідин-2,4-діон Стадія 1: 3-фтор 4-нітробензиловий спирт [Bioorg. Med. Chem. 7. 1999, 2647] До охолодженої на льодяній бані суспензії NaBH4 (204мг, 5,4ммоль, 2екв.) у THF (10мл) додавали краплями З-фтор-4-нітробензойну кислоту (500мг, 2,7ммоль, 1екв.) у THF (10мл) протягом 30хв. Потім додавали краплями BF3-Et2O(7,3ммоль, 2,7екв.) протягом 30хв. Одержаний розчин перемішували при кімнатній температурі протягом ночі. Додавали краплями 1-н. НСI для нейтралізації надлишку NaBH4. Розчинник видаляли у вакуумі, одержаний залишок розчиняли у DCM, промивали водою, розсолом. Потім органічний шар сушили над MgSO4, розчинник видаляли у вакуумі, одержуючи 425мг 3-фтор-4нітробензилового спирту (92% ви хід). Цю сполуку використовували на наступній стадії без додаткового очищення. 1 Н ЯМР: δ=(400МГц, CDCI3): 7,97 (m, 1H), 7,28 (m, 1H), 7,18 (m, 1H), 4,75 (m, 2H). Стадія II: 3-фтор-4-нітробензилальдегід 3-фтор-4-нітробензиловий спирт (116мг, 0,68ммоль, 1екв.) розчиняли в DCM (10мл) і додавали МnО2 (580мг, 6,73ммоль, 10екв.), одержану суспензію перемішували при кімнатній температурі протягом ночі. Відфільтровували МnО2 із суспензії, використовуючи целіт, розчинник випарювали, одержуючи відповідний альдегід у вигляді білої твердої речовини (66% вихід). 1 Н ЯМР: δ=(400МГц, CDCI3): 9,98 (s, 1H, CHO), 8,08 (m, 1H, ArH), 7,78 (m, 2H, ArH). Стадія ІІІ: 5-(3-фтор-4-нітро-бензиліден)№ 37 38 39 40 41 42 43 № 44 45 46 47 48 49 50 56 тіазолідин-2.4-діон [J. Med. Chem. 37. 2. 1994. 322] Суміш 3-фтор-4-нітробензилальдегіду (280мг, 1,65ммоль, 1екв.), тіазолідин-діону (193мг, 1,65ммоль, 1екв.) та β-аланіну (95мг, 1,1ммоль, 0,65екв.) в оцтовій кислоті (5мл) перемішували протягом ночі при 100°С. Охолоджену реакційну суміш додавали до води та перемішували протягом 1год. Осаджений продукт відфільтровували, промивали водою та сушили, одержуючи кінцевий продукт у вигляді жовто-оранжевої твердої речовини (77% вихід). 1 Н ЯМР: δ=(400МГц, (CD3)2CO): 8,0 (m, 1H, ArH), 7,68 (m, 2H, ArH), 7,53 (s, 1H, CН=C). Стадія IV: 5-(3-етиламіно-4-нітро-бензиліден)тіазолідин-2.4-діон 5-(3-фтор-4-нітро-бензиліден)-тіазолідин-2,4діон (200мг, 0,75ммоль, 1екв.), розчиняли в DME (6мл) та TEA (208мл, 1,5ммоль, 2екв.) і додавали розчин етиламіну (2екв.). Реакційну суміш стр ушували при 60°С протягом ночі. Розчинник видаляли у вакуумі, залишок розчиняли у етилацетаті та промивали 10% водним розчином хлориду амонію. Органічний шар сушили над Na2SO4, а розчинник випарювали, одержуючи відповідну анілінову похідну у вигляді червоного масла, яку використовували на наступній стадії без додаткового очищення. Стадія V: 5-(3-етиламіно-4-аміно-бензиліден)тіазолідин-2.4-діон До перемішуваного розчину 5-(3-етиламіно-4нітро-бензиліден)-тіазолідин-2,4-діону у THF, повільно додавали розчин гідросульфіту натрію (3екв.) у воді, а потім водний розчин K2СО3. Реакційну суміш назвали зі зворотним холодильником протягом ночі. THF видаляли у вакуумі, і задишок екстрагували етилацетатом. Органічний шар сушили над Na2SO4, і розчинник випарювали, одержуючи відповідну анілінову похідну, яку використовували без будь-якого додаткового очищення. Нижченаведені проміжні сполуки синтезували подібним чином, використовуючи придатні аміни як нуклеофіли, за методикою стадії IV проміжної сполуки 36. Спільно одержані 3-алкіламіно-4-нітробензиліден)-тіазолідин-2,4-діони відновлювали за методикою стадії V проміжної сполуки 36, одержуючи 3-алкіламіно-4-аміно-бензиліден)-тіазолідин2,4-діони. Проміжна сполука 5-[4-аміно-3-(4-феніл-бутиламіно)-бензиліден]-тіазолідин-2,4-діон 5-{4-аміно-3-[2-(4-трифторметил-феніл)-етиламіно]-бензиліден}-тіазолідин-2,4-діон 5-{4-аміно-3-[2-(4-гідрокси-феніл)-етиламіно]-бензиліден}-тіазолідин-2,4-діон метилов ий складний ефір 4-[2-аміно-5-(2,4-діоксо-тіазолідин-5-іліденметил)-феніламіно]циклогексанкарбонов ої кислоти 5-{4-аміно-3-[2-(1Н-індол-3-іл)-етиламіно]-бензиліден}-тіазолідин-2,4-діон 5-{4-аміно-3-[(1-метил-1Н-піразол-4-ілметил)-аміно]-бензиліден}-тіазолідин-2,4-діон 5-{4-аміно-3-[2-(3,4-диметокси-феніл)-етиламіно]-бензиліден}-тіазолідин-2,4-діон Проміжна сполука 5-[4-аміно-3-(4-трифторметил-бензиламіно)-бензиліден]-тіазолідин-2,4-діон 4-[2-аміно-5-(2,4-дюксо-тіазолідин-5-іліденметил)-феніламіно]-циклогексанкарбонова кислота 5-(4-аміно-3-ізобутиламіно-бегоиліден)-тіазолідин-2,4-діон 5-[4-аміно-3-(2-бензо[1,3]діоксол-4-іл-етиламіно)-бензиліден] -тіазолідин-2,4-діон 5-{4-аміно-3-[2-(2-фенокси-феніл)-етиламіно]-бензиліден}-тіазолідин-2,4-діон 5-[4-аміно-3-(3,3-дифеніл-пропіламіно)-бензиліден]-тіазолідин-2,4-діон 5-(4-аміно-3-проп-2-ініламіно-бензиліден)-тіазолідин-2,4-діон M/Z ESI:(M+1) 368,2 408,12 356,13 376,35 409,21 331,1 400,21 M/Z ESI:(M+1) 394,15 362,17 292,22 384,26 432,28 430,27 274,21 57 51 52 53 54 79793 5-[4-аміно-3-(2-метокси-бензиламіно)-бензиліден]-тіазолідин-2,4-діон 5-{4-аміно-3-[(фуран-3-ілметил)-аміно]-бензиліден}-тіазолідин-2,4-діон 5-(4-аміно-3-пропіламіно-бензиліден)-тіазолідин-2,4-діон 5-{4-аміно-3-[2-(4-фенокси-феніл)-етиламіно]-бензиліден}-тіазолідин-2,4-діон Проміжна карбальдегід сполука 55: хіноксалін-6 Стадія І: хіноксалін-6-карбонілхлорид У 3-горлу колбу місткістю 1 л завантажували хіноксалін-6-карбонову кислоту (20,2г) у 500мл THF. До цього розчину повільно додавали тіонілхлорид (42мл, 5екв.). Перемішуван у за допомогою механічної мішалки реакційну суміш нaгрiвaли при кипінні зі зворотним холодильником, і контролювали хід реакції за допомогою HPLC, нейтралізуючи проби NH4OH. Після 3год. названия зі зворотним холодильником аналіз посвідчив відсутність ви хідного матеріалу. Розчинник видаляли під зниженим тиском, а SOCІ2 видаляли шляхом триразового промивання толуолом. Одержану тверду речовину суспендували в 100мл EtOAc і фільтрували, одержуючи 23,47г бежевої твердої речовини. HPLC: 1,114хв. 1Н ЯМР (DMSO-d6) δ 9,01-7,40 (m, 5H). Стадія II: хіноксалін-6-карбальдегід У 3-горлу колбу місткістю 1л у атмосфері аргону завантажували хіноксалін-6-карбонілхлорид у 600мл DME. До цього розчину додавали три-третбутоксіалюмогідрид літію (1екв.) при -78°С протягом 1,5год. Реакційну суміш витримували при цій температурі протягом 5 год. Потім додавали лід, і реакційну суміш розводили AcOEt і фільтрували через целіт. Одержані два шари розділяли, і органічну фазу промивали насиченим розчином NaНСО3-Хіноксалін-6-карбальдегід одержали після випарювання розчинника (73% вихід) у вигляді жовтуватої твердої речовини. HPLC: 1,49хв. LC-MS: M/Z ESI: 0,81 хв., 159,37(М+1). 1Н ЯМР (CDCI3) δ 10,28 (s, 1Н), 8,97 (s, 2H), 8,61 (s, 1H), 8,27 (q, 6Гц, 9Гц, 2Н). Проміжна сполука 56: бензотіазол-6-карбальдегід Цю проміжну сполуку синтезували за методикою синтезу проміжної сполуки 55 із використанням бензотіазол-6-карбонової кислоти як вихідної сполуки. Загальний вихід становив 38%. HPLC: 1,92хв. LC-MS: M/Z ESI: 0,97хв., 164,27 (М+1). 1Н ЯМР (DMSO-d6) δ 10,1 (s, 1Н), 9,60 (s, 1H), 8,60 (s, 1H), 8,20 (m, 1H), 8,10 (d, 1H). Проміжна сполука 57: 3-метил-бензофуран-5карбальдегід Цю проміжну сполуку одержали за методикою 58 356,23 316,21 278,16 432,23 синтезу проміжної сполуки 1, використовуючи етил-2-ацетил-4-бромфеноксіацетат як вихідний матеріал. Загальний вихід 50%. LC-MS: M/Z ESI: 1,55хв., 161,34 (M+1). 1Н ЯМР (DMSO-d6) δ 10,1 (s, 1Н), 8,21 (d, J=1,5 Гц 1Н), 7,92 (d, J=1,3Гц, 1Н), 7,88-7,84 (dd, J=1,6Гц, 1Н), 7,737,71 (d, J=8,5Гц, 1H), 2,25 (s, 3H). Проміжна сполука 58: 3-бром-бензофуран-5карбальдегід Стадія І: 2.3-дибром-2.3-дигідро-бензофуран5-карбальдегід Проміжну сполуку 1 (2г, 13,7ммоль) розчиняли у 10мл СНСІ3 та охолоджували до -10°С. До неї додавали розчин Вr2 у СНСI3 (1,55екв., с=4,162моль/л). Реакційна суміш темніла, і її витримували для названия до кімнатної температури протягом 1 год. HPLC посвідчила завершення додавання брому. Розчинник і залишок брому випарювали під зниженим тиском, одержуючи червонувате масло (4,1г, вихід 90%), яке використовували на наступній стадії без додаткового очищення. HPLC: 3,43хв. Стадія II: 3-бром-1-бензосфуран-5карбальдегід До розчину 2,3-дибром-2,3-дигідро-1бензофуран-5-карбальдегіду (4,1г) у безводному етанолі (15мл) додавали розчин КОН (2,2екв.) у безводному етанолі (14мл) та нaгрiвaли зі зворотним холодильником при 70°С протягом 1год. Реакційну суміш охолоджували, розводили водою та екстрагували EtOAc (3´50мл). Органічний шар промивали водою, розсолом і сушили. Розчинник видаляли у вакуумі, і одержаний залишок очищали флeш-xpoмaтoгрaфiєю (елюент петролейний ефір/EtOAc 99,5:0,5), одержуючи вказану в заголовку сполуку у вигляді блідо-жовтої твердої речовини (2,91г (80% чистота), вихід 78%). HPLC: 3,35хв. 1Н ЯМР (D MSO-d 6, 300МГц) δ 10,12 (s, 1H), 8,47 (s, 1H), 8,14 (d, J=1,5Гц, 1Н), 7,97 (dd, J=8,6, 1,5Гц, 1Н), 7,87 (d, J=8,6Гц, 1Н). Проміжна сполука 59: 3-фенілетинілбензофуран-5-карбальдегід У сухій колбі розчиняли 3-бром-1-бензофуран5-карбальдегід (1г, 4,4ммоль) у безводному THF (50мл). До цього розчину додавали у а тмосфері аргону хлорид біс(трифенілфосфін)паладію (II) (160мг, 0,2ммоль), TEA (2,81мл, 5екв.), Cul (40мг, 0,2ммоль) та фенілацетилен (897мг, 8,8ммоль). Реакційну суміш нагрівали при 55°С протягом 2 днів. Неочищений продукт фільтрували через це 59 79793 літ та очищали на силікагелі, використовуючи як елюент суміш циклогексан-етилацетат (7-3), одержуючи 680 мг (вихід: 56%). HPLC: 4,71хв. 1Н ЯМР (DMSO-d6) δ 10,14 (s, 1Н), 8,64 (s, 1H), 8,38 (s, 1H), 7,97 (dd, J=1,5Гц, 8,3Гц, 1Н), 7,90 (d, J=8,6Гц, 1H), 7,65 (m, 2H), 7,46 (m, 3H). Проміжна сполука 60: етиловий складний ефір 3-(5-форміл-бензофуран-3-іл)-акрилової кислоти У запаяній трубці розчиняли 3-бром-1бензофуран-5-карбальдегід (500мг, 2,22ммоль) у 7мл ACN. До цього розчину додавали РРh3 (1,16г, 4,44ммоль), Pd(II)aцетат (500мг, 2,2ммоль), Et3N (073мл, 5,55ммоль) і нарешті етиловий складний ефір акрилової кислоти (2,41мл, 22ммоль). Трубку запаювали, і реакційну суміш нaгрiвaли при 120°С протягом 1год. Неочищений продукт фільтрували через целіт для видалення неорганічних забруднювачів. Розчинники випарювали, а одержаний неочищений продукт очищали хроматографією на силікагелі, використовуючи суміш циклогексанAcOEt (градієнт від 95:5 до 50:50). Одержали блідо-жовту тверду речовину (400мг, вихід: 42%). HPLC: 3,69хв. 1Н ЯМР (DMSO-d6) δ 10,15 (s, 1Н), 8,70 (s, 2H), 7,97 (d, J=9 Гц 1H), 7,88 (s, 1H), 7,82 (s, 1H), 6,76 (d, J=15Гц, 1Н), 4,23 (q, J=6Гц, 12Гц, 2H), 1,28 (t, J=9Гц, ЗН). Проміжна сполука 61: 6-метиловий складний ефір 4-трет-бутилового складного ефіру 2,3дигідро-бензо[1,4]оксазин-4,6-дикарбонової кислоти Стадія І: метиловий складний ефір 3-аміно-4гідрокси-бензойної кислоти У тригорлу колбу місткістю 2000мл, яка містила метиловий складний ефір 3-нітро-4-гідроксибензойної кислоти (43г, 218ммоль) у МеОН (860мл; 20 об'ємів) додавали паладій на вугіллі у воді (2г у 10мл води). Додавали однією порцією при перемішуванні амонійформіат (68,76г, 5екв.). Через 2-3хв. утворювалася суспензія, і температура піднімалася від 20°С до 30°С. Застосовували льодяну баню для охолодження реакційної суміші до 20°С, і реакційну суміш пepeмiшyвали при 20°С протягом 40хв. до завершення реакції (зникнення жовтого кольору). Реакційну суміш фільтр ували через шар силікагелю, промивали МеОН, а фільтрат концентрували у вакуумі, одержуючи зелене масло, яке розчиняли у етилацетаті (400мл). Органічну фаз у промивали двічі водою, сушили над MgSO4 , фільтрували та концентрували, одержуючи кремову тверду речовину m=31,35г (86%). LC-MS: M/Z ESI: 0,81хв, 168,37 (M+1). 60 Стадія II: гідрохлорид метилового складного ефіру 3,4-дигідро-2Н-бензо[1,4]оксазин-6карбонової кислоти У тригорлу колбу місткістю 2000мл, яка містила метиловий складний ефір 3-аміно-4-гідроксибензойної кислоти (31,35г, 187ммоль) у безводному DMF (630мл; 20 об'ємів) при кімнатній температурі у атмосфері азоту додавали однією порцією K2СО3 (103г, 4екв.), а потім однією порцією 1,2диброметан (65мл, 4екв.). Реакційну суміш перемішували при 70°С протягом 12год. Давали суміші охолодитися до кімнатної температури, додавали 1-н. НСI до досягнення рН=8, та екстрагували, використовуючи діетиловий простий ефір (3´200мл). Органічну фазу промивали водою (2´200мл), сушили над MgSO 4 і концентрували, одержуючи коричнево-червоне масло з твердою речовиною, яке знову розчиняли в діетиловому простому ефірі (450мл) та THF (50мл) і фільтрували для видалення білої твердої речовини. До фільтрату додавали 1-н. НСI, після чого додавали діетиловий простий ефір (130мл), суспензію перемішували при кімнатній температурі протягом 5хв. та фільтрували, одержуючи 27,6г неочищеного продукту. Водні фази знову екстрагували етилацетатом, одержуючи додаткові 6,23г продукту. Об'єднані фракції (32г) перекристалізовували з EtOH (420мл; 13 об'ємів), фільтрували, сушили і одержували білий порошок (19,47г (16,37г вільна основа)), ви хід 40%. HPLC: 1,954хв. LC-MS: M/Z ESI: 1,27хв., 194,45 (М+1). Стадія IIІ: 4-трет-бутиловий складний ефір 6метилового складного ефіру 2,3-дигідробензо[1,4]оксазин-4,6-дикарбонової кислоти У тригорлу колбу місткістю 500мл, що містила гідрохлорид метилового складного ефіру 3,4дигідро-2Н-бензо[1,4]оксазин-6-карбонової кислоти, суспендованого у THF (145мл; 10 об'ємів), додавали однією порцією DIEA (27мл, 2,5екв.) при кімнатній температурі у атмосфері азоту і спостерігали часткове розчинення. Додавали однією порцією ангідрид бутоксикарбонілу (16,4г, 1,2екв.), і реакційну суміш перемішували при 65°С протягом 5 діб. Протягом цього часу додавали кількома невеликими порціями 0,2екв. Вос2О та DIEA. THF видаляли у вакуумі, і одержаний залишок розчиняли у DCM (150мл). Органічну фазу промивали насиченим розчином NaHCO3 і потім розсолом. Сушили над MgSO4 та фільтр ували, після чого леткі фракції видаляли у вакуумі; одержаний залишок перекристалізовували з EtOH (80мл), одержуючи кремові кристали (14,8г, 76%). HPLC: 4,038хв. 1Н ЯМР (CDCI3) δ 8,49 (s, 1Н), 7,68 (dd, J=3Гц, 9Гц, 1H), 6,89 (d, J=9Гц, 1H), 4,30 (q, J=3Гц, 9Гц, 2H), 3,89 (m, 5H), 1,62 (s, 9H). Проміжна сполука 62: трет-бутиловий складний ефір 6-форміл-2,3-дигідро-бензо [1,4] оксазин4-карбонової кислоти
ДивитисяДодаткова інформація
Назва патенту англійськоюAzolidinone-vinyl fused-benzene derivatives
Автори англійськоюRueckle Thomas, Jiang Xuliang, Gaillard Pascale
Назва патенту російськоюАзолидиноновые производные конденсированных винилбензолов
Автори російськоюРюкле Томас, Дзянь Сюлянь, Гейяр Паскаль
МПК / Мітки
МПК: A61K 31/4709, A61P 43/00, A61K 31/5377, A61P 37/02, C07D 417/14, A61P 37/08, A61P 31/12, A61K 31/517, A61P 9/00, A61P 35/00, A61P 9/12, A61P 35/04, A61P 11/06, A61K 31/454, A61P 25/14, A61P 37/06, A61P 9/10, A61K 31/426, A61P 25/28, A61P 19/02, A61P 25/00, A61P 29/00, A61P 13/12, C07D 277/34, C07D 277/20, A61P 21/00, A61P 31/00, A61K 31/427, C07D 417/06, A61P 7/02, A61P 1/04, A61P 17/06, A61P 11/00
Мітки: похідні, вінілбензолів, азолідинонові, конденсованих
Код посилання
<a href="https://ua.patents.su/45-79793-azolidinonovi-pokhidni-kondensovanikh-vinilbenzoliv.html" target="_blank" rel="follow" title="База патентів України">Азолідинонові похідні конденсованих вінілбензолів</a>
Попередній патент: Універсальна відцентрова ливарна машина
Наступний патент: Картоплевисаджувальний апарат з наколювальним пристроєм
Випадковий патент: Спосіб керування автономним асинхронним генератором з короткозамкненим ротором

















































