Спосіб отримання нітрозилгемоглобіну
Номер патенту: 115628
Опубліковано: 25.04.2017
Автори: Бурда Володимира Адамівна, Федорович Андрій Миколайович, Сибірна Наталія Олександрівна
Формула / Реферат
Спосіб отримання нітрозилгемоглобіну, за яким дезоксигенують гемоглобін, після чого проводять нітритредуктазну реакцію з додаванням NaNO2, який відрізняється тим, що дезоксигенацію проводять додаванням кількох кристалів дитіоніту Na і за спектром поглинання фіксують утворення дезоксигемоглобіну, до якого додають розчин 20 мМ NaNO2, знову знімають спектр поглинання і відмічають максимуми, характерні для нітрозилгемоглобіну, причому увесь процес проводять у вимірювальній кюветі.
Текст
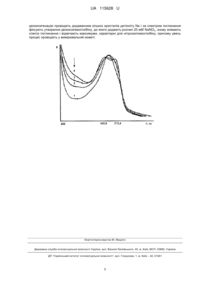
Реферат: Спосіб отримання нітрозилгемоглобіну, за яким дезоксигенують гемоглобін, після чого проводять нітритредуктазну реакцію з додаванням NaNO2. Дезоксигенацію проводять додаванням кількох кристалів дитіоніту Na і за спектром поглинання фіксують утворення дезоксигемоглобіну, до якого додають розчин 20 мМ NaNO2, знову знімають спектр поглинання і відмічають максимуми, характерні для нітрозилгемоглобіну, причому увесь процес проводять у вимірювальній кюветі. UA 115628 U (54) СПОСІБ ОТРИМАННЯ НІТРОЗИЛГЕМОГЛОБІНУ UA 115628 U UA 115628 U 5 10 15 20 25 30 35 40 45 50 55 60 Корисна модель належить до галузі біології та медицини і може бути використана для дослідження параметрів NO-зв'язуючих властивостей гемоглобіну in vitro. Відомий спосіб отримання нітрозилгемоглобіну [М. Salgado, Red Blood Cell Membranefacilitated of nitrite-Derived Nitric oxide bioactivity /M. Salgado, Z. Cao, E. Nagababu, J. Mohanty //Biochemistry.- 2015. - P. 395-411], за яким спочатку отриманий гемоглобін дезоксигенують у спеціальній анаеробічній колбі і отримують дезоксигемоглобін, через який пропускають газ Нітроген, використовуючи паладій як каталізатор, отримують NO, який взаємодіє із дезоксигемоглобіном, утворюючи нітрозилгемоглобін. Недоліком способу є як складність отримання дезоксигемоглобіну, так і використання газу нітрогену для одержання нітрозилгемоглобіну. Найближчим за технічною суттю - прототипом - є спосіб отримання нітрозилгемоглобіну за допомогою пристрою для отримання і дозованої подачі оксиду азоту і побудови кривих дисоціації оксигемоглобіну у присутності NО [Патент UA 45158 А. Пристрій для отримання і дозованої подачі оксиду азоту NO і побудови кривих дисоціації оксигемоглобіну в присутності NO. Бюл. № 3 від 15.03.2002]. Прилад складається з чотирьох частин: NO - синтезуючого вузла, дозуючого вузла, вузла для оксигенації і виміру оптичної густини, вузла контролю вакууму і дозованої подачі атмосферного повітря. Усі ці вузли з'єднані між собою скляними шліфами і вакуумними шлангами. Вузли приєднують до вакуумного насоса. За допомогою модифікованого шприца гемоглобін вносять у вузол для оксигенації і виміру оптичної густини. Включають насос і проводять дезоксигенацію упродовж 10-15 хв. Далі до синтезуючого вузла вносять кристали NaNO2 і, відкриваючи кран, уводять NO до дезоксигемоглобіну, утворюють нітрозилгемоглобін. Недоліком є те, що отримання нітрозилгемоглобіну є незручним, складним і недосконалим. В основу корисної моделі поставлено задачу удосконалити спосіб отримання нітрозилгемоглобіну шляхом використання дезоксигенації, додаванням кристалів дитіоніту Na до гемоглобіну з наступним додаванням отриманого NO і його приєднання до дезоксигемоглобіну, що дасть змогу спростити процес утворення нітрозилгемоглобіну. Поставлена задача вирішується тим, що весь процес відбувається у вимірювальній кюветі, причому дезоксигенацію проводять з додаванням кількох кристалів дитіоніту Na і за спектром поглинання фіксують утворення дезоксигемоглобіну, до якого додають розчин 20 мМ NaNO2, знову знімають спектр поглинання і відмічають максимуми, характерні для нітрозилгемоглобіну. Відомо про наявність двох шляхів природного синтезу NO у живому організмі, а саме в еритроцитах: NO-синтазний і нітритгемоглобіновий, який забезпечується нітритредуктазною активністю дезоксигемоглобіну. За науковою літературою, еритроцитам відводиться роль клітин, що можуть формувати депо оксиду азоту для подальшого використання організмом згідно з його фізіологічними потребами (A. Dejam, 2005). Окислювальний процес перетворення гемоглобіну (Hb) в Met-Hb під дією нітрит-іонів може бути спряженим із утворенням N0. Реутовим В.П. (2006) запропонована концепція циклу азоту, згідно з якою в утворенні NO має значення не лише L-аргінін/NO-синтазна система, але і нітритредуктазна система. Існує наявність двох власних механізмів синтезу NO в еритроцитах: NO-синтазного і нітритгемоглобінового, останній забезпечується нітритредуктазною активністю дезоксигемоглобіну. За аналізом взаємодії NO з Hb in vivo є така послідовність і співвідношення 3між реакціями утворення NO-похідних: Met-Hb і NO >> NO-Hb> SNO-Hb. Регуляторна роль NO можлива лише при екзогенному утворенні його у кількості менше одного проценту від загального гемоглобіну. Надмірне утворення NО небезпечне і негативно впливає на газотранспортну функцію крові, оскільки приєднання його до β-ланцюгів значно збільшує спорідненість гемоглобіну до кисню, одночасно накопичується метгемоглобін, що обмежує постачання кисню до тканин, що призводить до розвитку гіпоксичних станів і загибелі клітин. При гіпоксії клітини переходять з кисневого на нітратно-нітритне дихання. Гемоглобін і міоглобін мають властивість відновлювати нітрит іони до оксиду азоту, вони замикають ланцюжок: L-аргінін - NO –NO2 /NO3-NO в один цикл. Властивість гемопротеїдів відновлювати нітрит-іони до NO проявляється лише у відновленому стані. NO у реакціях з гемоглобіном (Hb) утворює метгемоглобін (Met-Hb), нітрозилгемоглобін (NO2+ Hb - нітрозування по Fe у гемовій групі) та S-нітрозогемоглобін (SNO-Hb - нітрозилювання по β-93-цистеїну). Біологічна функція NO-похідних Нb досить широка: транспорт NO, його депонування, елімінація і інше. Вони також приймають участь у генезі багатьох патологічних станів. SNO-Hb діє як "алостерично контрольований буфер", який обмінює свою NO-групу з тіолами середовища, у тому числі з глутатіоном, і тим самим змінює кровоплин, як вазодилататор, виконуючи роль критичного фактора постачання О 2. Метаболічний цикл NO може активуватися при різноманітних гіпоксичних станах, так як за умов дефіциту О2 відновлені і гемумісні білки переносять електрони на іони NO2, відновлюючи 1 UA 115628 U 5 10 15 20 25 30 35 40 45 50 55 їх до NO. Час життя вільного NO становить кілька секунд. Не дивлячись на це, синтезований NO може діяти як аукринно, так і паракринно. Однак, для здійснення своєї паракринної дії NO повинен бути включений у більш стабільні сполуки. Частина синтезованого NO може стабілізуватися для запасання і транспортування у вигляді комплексів, які утворюють так зване депо NO. Ці депо є фізіологічно активними, так як вони не лише зв'язують, але і поступово вивільняють NO. Основними біологічними формами депо NO є S-нітрозотіоли і динітрозильні комплекси заліза, які здатні до взаємоперетворень. NO може депонуватися у судинних стінках, вісцеральних гладких м'язах, макрофагах та еритроцитах. Депонування NO відбувається за умов будь-якого підвищення його рівня в організмі, незалежно від причини. Це підвищення може бути як результатом посилення синтезу ендогенного оксиду азоту, так і уведення екзогенного NO у вигляді донора. Посилення синтезу NO практично завжди присутнє в організмі, який адаптується до зміни умов зовнішнього та внутрішнього середовища - гіпоксії, фізичному навантаженні, стресі, тепловому шоку. NO може зв'язуватись із гемовою частиною гемоглобіну, утворюючи нітрозилгемоглобін, або з цистеїном глобіну, утворюючи нітрозогемоглобін. Оксидативно-нітративний стрес, який супроводжується нітруванням білків, перекисним окисненням ліпідів, розривами ДНК, змінами у клітинному сигналюванні, активацією PARP-1, призводить до порушення метаболізму і шляхів сигналювання у клітинах, є характерним для багатьох захворювань, зокрема цукрового діабету. Характер рівноваги між інтенсивністю вільнорадикальних процесів та функціонуванням системи антиоксидантного захисту значною мірою залежить від рівня продукування NO. Авторами вперше у дослідах in vitro показано, що при взаємодії іонів NO2 з дезоксигемоглобіном здійснюється окисно-відновна реакція, в ході якої дезокси-Hb окислюється в мет-Hb, а іони NO2 відновлюються до NO. Взаємодіючи з відновленим гемоглобіном, NO утворює стійкі Hb-NO-комплекси, а комплекси мет-Hb з NO нестабільні і тому легко розпадаються. Підтвердженням того є отримані нами електронні абсорбційні спектри переходу дезокси-Hb в нітрозо-Hb (Креслення). Креслення: Електронні спектри при переході дезоксигемоглобіну у нітрозилгемоглобін: де 1 перша реєстрація дезоксигемоглобіну; 2, 3 - перехідні форми; 4 - остання реєстрація нітрозилгемоглобіну. Приклад отримання нітрозилгемоглобіну: У вимірювальну кварцову кювету (1 см) вносять гемоглобін, який отримують з попередньо відмитих еритроцитів і прогемолізованих 1/30 Μ Na/K фосфатним буфером, рН 7,36. Використовують гемоглобін з концентрацією - 20 мМ, яку визначають при 540 нм, -1 -1 використовуючи мілімолярний коефіцієнт поглинання ціаноферигену (11 мМ /см ). До гемоглобіну об'ємом 1 мл додають кілька кристаликів дитіоніту Na для дезоксигенації гемоглобіну і фіксують утворення дезоксигемоглобіну, реєструючи спектр з максимумом 554,9 нм характерний для дезоксигемоглобіну. Нітритредуктазну реакцію запускають додаванням 1 мл 20 мМ NaNO2 Перемішують і закривають кювету кришечкою для обмеження доступу кисню і витримують 3 хв. Поступове перетворення дезокси-Hb в HbNO спостерігають за характерними змінами поглинання у видимій області спектра (Креслення). Широка асиметрична смуга з максимумом при 555-560 нм замінюється двома смугами із максимумами поглинання 545,8 нм і 572,4 нм, які є характерними для нітрозилгемоглобіну. Вимірювання проводять за допомогою спектрофотометра UV-VIS "Specord Μ-40" (Німеччина). Дослідження НвNO має подвійне значення як для використання в клінічних умовах, так і в різних екстремальних польових умовах, а результати можуть бути використанні у медицині критичних станів при визначенні ступеня отруєння монооксидом Карбону, нітратами і нітритами та іншими екзогенними сполуками, що можуть провокувати інтоксикацію організму. Зростання вмісту метгемоглобіну та нітрозилгемоглобіну часто пов'язане із передозуванням таких ліків як лідокаїн, новокаїн, нітрогліцерин та ін., а також внаслідок інтоксикації екзогенними сполуками: анілінові барвники, хлорбензол, тринітротолуол, нафтален, нітрити та нітрати. Дослідження швидкості приєднання NO та інших лігандів до гемоглобіну поряд зі спектральними характеристиками утворених лігандних форм є основою розуміння механізмів взаємодії цих молекул за різних патологічних станів. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 60 Спосіб отримання нітрозилгемоглобіну, за яким дезоксигенують гемоглобін, після чого проводять нітритредуктазну реакцію з додаванням NaNO2, який відрізняється тим, що 2 UA 115628 U дезоксигенацію проводять додаванням кількох кристалів дитіоніту Na і за спектром поглинання фіксують утворення дезоксигемоглобіну, до якого додають розчин 20 мМ NaNO2, знову знімають спектр поглинання і відмічають максимуми, характерні для нітрозилгемоглобіну, причому увесь процес проводять у вимірювальній кюветі. Комп’ютерна верстка М. Мацело Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 3
ДивитисяДодаткова інформація
Автори англійськоюBurda Volodymyra Adamivna
Автори російськоюБурда Владимира Адамовна
МПК / Мітки
МПК: C01B 21/24, G01N 33/50
Мітки: спосіб, отримання, нітрозилгемоглобіну
Код посилання
<a href="https://ua.patents.su/5-115628-sposib-otrimannya-nitrozilgemoglobinu.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання нітрозилгемоглобіну</a>
Попередній патент: Спосіб одержання 2-аміно-7-r-5-оксо-4-(5-арил-2-фуран)-5,6,7,8-тетрагідро-4н-хромен-3-карбонітрилів
Наступний патент: Спосіб криптографічного перетворення інформації
Випадковий патент: Спосіб хірургічного лікування нейроендокринної пухлини підшлункової залози