Похідні 4-(бромометил)-2-r-1,3-тіазол-3-іум бромідів та 4-бромометил-2-r-1,3-тіазолів
Номер патенту: 41094
Опубліковано: 12.05.2009
Автори: Воловенко Юліан Михайлович, Коваленко Наталія Володимирівна
Формула / Реферат
Похідні 4-(бромометил)-2-R-1,3-тіазол-3-іум бромідів та 4-бромометил-2-R-1,3-тіазолів загальної формули Ic-f і ІІс-е як проміжні сполуки
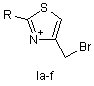
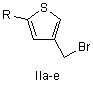 R=a: CH3; b: Ph; c: CH2CN; d:
R=a: CH3; b: Ph; c: CH2CN; d: 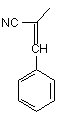 , e:
, e: 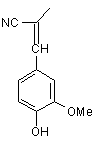 , f:
, f: 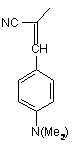
для одержання фармацевтичних сполук.
Текст
Похідні 4-(бромометил)-2-R-1,3-тіазол-3-іум бромідів та 4-бромометил-2-R-1,3-тіазолів загальної формули Ic-f і ІІс-е як проміжні сполуки S R 2 S R Br IIa-e R=a: CH3; b: Ph; c: CH2CN; d: NC CH CH CH + N NC NC Br OMe Ia-f + Br- N Br S I S R N H2 N Br II Br H3C Br a + O IIIa схема 1 IV H3 C S N+ BrIa (11) UA S R Відомий метод отримання 4-(бромометил)-2метил-1,3-тіазол-3-іум броміду (Іа), за яким процес відбувається за схемою 1 [1], сполуки ІІа за схемою 2 [2], сполуки IIб за схемою 3 [3]: 4-(Бромометил)-2-метил-1,3-тіазол-3-іум бромід (Іа) отримано взаємодією тіоацетаміду (IIIа) з 1,3-дибромо-пропан-2-оном (IV) у диоксані при нагріванні впродовж 30 хвилин (схема 1). (19) Корисна модель відноситься до похідних 4(бромометил)-2-R-1,3-тіазол-3-іум бромідів (І) та 4бромометил-2-R-1,3-тіазолів (II) які можуть бути застосовані як проміжні сполуки для отримання фізіологічно активних речовин в медицині та способу їх одержання. 41094 (13) U N(Me2) OH , e: , f: для одержання фармацевтичних сполук. Br 3 41094 Недоліком цього способу є: недостатній вихід цільового продукту реакції. Відомий метод отримання 4-бромометил-2метил-1,3-тіазолу (IIа), за яким процес відбувається у три стадії за схемою 2 [2]: Перша стадія: етил 2-метил1-1,3-тіазол-4карбоксиетил (VI) отримано взаємодією тіоацетоміду з етиловий естером бромпірувату у спирті при H3C S кімнатній температурі впродовж 20 годин (вихід 70%). Друга стадія: Сполуку VI в етері при -78°С за 3 години дією LiАlH4, перетворено в (2-метил-1,3тіазол-4-ил)метанол (VII) (вихід 84%). Третя стадія: Сполуку VII взаємодією з Ph3P, CBr4 в CCl4 за 3 години перетворено в 4бромометил-2-метил-1,3-тіазол (IIа) (вихід 85%). S H3C a b N 4 S H3 C H2N N OH VII VI IIIa c N CO2Et S H3C Br IIa (а) етиловий естер бромпірувату, EtOH, кт 20год, 70%; (b) LiАlН4, етер, -78°С, 3г, 84%; (с) Ph3P, CBr4, CCl4, кт, 3г, 85%. схема 2 Недоліком цього способу є: 1) низький за трьома стадіями вихід цільового продукту реакції, а саме 50%; 2) тривалий час проведення реакціі: перша стадія до 20 годин; друга і третя стадії по 3 години. 3) необхідність застосування вогне- і вибухонебезпечного LiAlH4. Відомий метод отримання 4бромометил-2-феніл-1,3-тіазолу (IIb) (схема 3), за яким 4-метил-2-фенілтіазол (X) який отримано з Ph X Ph S H2N CH3 + a S N+ Br O IIIb VIII IX (а) органічний розчинник; (с) NBS, ВРО і ABN схема 3 Недоліком цього способу є: низький вихід цільового продукту реакції, а саме 28%; В основу корисної моделі поставлено задачу одержати сполуки, які можуть бути застосовані як проміжні сполуки для отримання фізіологічно активних речовин в медицині. Поставлена задача вирішується одержанням похідних 4-(бромометил)-2-R-1,3-тіазол-3-іум бромідів загальної формули (І) та 4-бромометил-2-R1,3-тіазолів загальної формули (II), S R + Br- N Br I S R N Br II бензкарботіоаміду формули IIIb з aгалогенкетоном - формула VIII в органічних розчинниках (вихід 78%) [3], піддається дії Nбромсукциніміду у суміші розчинників С6Н6/С2Н5ОН в присутності ВРО і ABN отримано суміш продуктів, з якої за допомогою хроматографії [ССl4/етилацетат (100:3)] було вилучено IIb з виходом 28%, Т.пл. 76,2-77,1°С (з пентану)[4]. S Ph b c N CH3 S Ph N Br CH3 X=Br,Cl X IIb де R - (С1-С2)алкіл, феніл, 2-ціанометил, 1ціано-2-фенілзтил, 1-ціано-2-(4-гідрокси-3-(С1С2)алкілоксифеніл)етил, 1-ціано-2-[4-(ди(С1С2)алкіламіно)феніл]етил, способом, який включає проведення реакції похідних тіоаміду з 1,3дибромацетоном, згідно з корисною моделлю, що заявляється, реакцію проводять в органічному розчиннику з наступною дегідратацією утвореного осаду і виділенням з солі цільового продукту. При цьому реакцію проводять у стехіометричному співвідношенні реагентів, розчинником може бути етилацетат або ацетонітрил (схема 4): Використання етилацетату як розчинника при проведенні реакції конденсації тіоаміду з 1,3-дибромацетоном забезпечило підвищений вихід солі Іа, а розроблений спосіб переведення солі Іа у основу IIа дозволив виділити цільовий продукт з високим виходом в одну стадію. 5 Br R S H2N S R Br a + N+ Br O IV IIIa-f R 41094 R OH b N c Ic N Br S R c N+ N Br N+ H (B) Br IIa-e Ia-f Ic S N S R=a: CH3; b: Ph; c: CH2CH; S Br (A) b Va-f S N+ 6 Br CH CH CH d: NC NC NC f: e: OMe OH N(Me2) Br IIc схема 4 Одержані продукти мають достатню чистоту для подальшого використання у синтезі інших хімічних сполук, в тому числі й біологічно активних. Корисна модель підтверджується наступними прикладами, які ілюструють, але не обмежують об'єм даного винаходу. Синтез 4-(бромометил)-2-метил-1,3-тіазол-3іум броміду (Іа). Приклад 1 До 0,1моль тіоацетаміду (IIIа) додають 0,1моль 1,3-дибромацетону (IV) у 150мл етилацетату, перемішують до повного розчинення і залишають до повного виділення продукту реакції. Осад фільтрують, промивають спиртом і висушують. В результаті виділяють 28г чистого (бромометил)-4-гідрокси-2-метил-4,5-дигідро-1,3-тіазол-3іум броміду (Va) вихід (98%). т.розк. 155°С. Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц), d, м.д.: 4,88 уш.с (1Н, ОН), [3,87 д (1Н), и 3,52 д (1Н), J 12.7, СН2], 3,89 с (2Н, СН2), 2,63 с (3Н, СН3). Знайдено, %: С 22,37; Вr 52.70; N 4,51. C5H9Br2NOS. Вираховано, %: С 20,64; Вr 54,92; N 4,81. Сіль Va кип'ятять у 50мл льодяної оцтової кислоти впродовж 30 хвилин, реакційну суміш охолоджують, кристали солі Іа фільтрують, промивають 7мл льодяної оцтової кислоти, естером і висушують. В результаті виділяють 25г чистого 4(бромометил)-2-метил-1,3-тіазол-3-іум броміду (Іа). Вихід 25г (92%), т.розкл. 137°С. Спектр ЯМР 1 Н (ДМСО-d6); Varian Mercury 400; (400МГц), d, м.д.: 7,48 с (1Н, CH-S), 4,59 с (2H, СН2), 2,66 с (3Н, СН3). Знайдено, %: С 21,04; Вr 59,02; N 5,34. C5H7Br2NS. Вираховано, %: С 22,00; Вr 58,54; N 5,13. Синтез 4-бромометил-2-метил-1,3-тіазолу (IIа) Водний розчин солі Іа обробляють розчином амоніаку і одержують 4-бромометил-2-метил-1,3тіазол (IIа). Отриману основу IIа экстрагують (3´25мл) бензолу або (3´40мл) хлороформу. Органічну фазу відділяють, струшують з СаСl2 і пропускають через тонкий шар силікагелю, розчинник випарюють. В результаті виділяють 15г чистого 4(бромометил)-2-метил-1,3-тіазолу (IIа). Вихід 15г (78%), (жидк.) Спектр ЯМР 1Н (ДМСО-d6); d, м.д.: 7.58 с (1H, CH-S), 4.62 с (2Н, СН2), 2.69 с (3Н, СН3). Знайдено, %: С 31,37; Вr 41,70; N 7,51. C5H6BrNS. Вираховано, %: С 31,27; Вr 41,60; N 7,29. Приклад 2 До 0,1моль тіоацетаміду (IIIа) додають 0,1моль 1,3-дибромацетону (IV) у 100мл ацетонітрилу, перемішують до повного розчинення і залишають до повного виділення продукту реакції. Осад фільтрують, промивають спиртом і висушують. В результаті виділяють 25г чистого (бромометил)-4-гідрокси-2-метил-4,5-дигідро-1,3-тіазол-3іум броміду (Va) вихід (90%). Сіль Va кип’ятять у 50мл льодяної оцтової кислоти впродовж 30 хвилин, реакційну суміш охолоджують, кристали солі Іа фільтрують, промивають 7мл льодяної оцтової кислоти, естером і висушують. В результаті виділяють 20г чистого 4(бромометил)-2-метил-1,3-тіазол-3-іум броміду (Іа). Вихід 20г (73%). Синтез 4-бромометил-2-метил-1,3-тіазолу (IIа) Водний розчин солі Іа обробляють розчином К2СО3 і одержують 4-бромометил-2-метил-1,3тіазол (IIа). Основу IIа экстрагують (3´25мл) бензолу або (3´40мл) хлороформу. Органічну фазу відділяють, струшують з СаСl2 і пропускають через тонкий шар силікагелю, розчинник випарюють. В результаті виділяють 12г чистого 4-(бромометил)2-метил-1,3-тіазолу (IIа). Вихід 13г (67%). Синтез 4-(бромометил)-2-феніл-1,3-тіазол-3іум броміду (Іb) Приклад 1 До розчину 0,1 моль бензкарботіоаміду (4)додають 0,1 моль 1,3-дибромацетону 5 в 150мл етилацетату перемішують до повного розчинення і залишають до повного виділення продукту реакції. Осад відфільтровують промивають етилацетатом, спиртом і висушують. В результаті виділяють 31г 4-(бромометил)-4-гідрокси-2-феніл-4,5-дигідро-1,3тіазол-3-іум броміду (Vb). Вихід 31г (87%), т.пл. 142°С. Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц), d, м.д.: 7.85 д (2Н, J 7,6 Гц, H2,6Ph), 7.48 м (3Н, H3,4,5Ph), 6.45 уш.с (1Н, ОН), 4,71 с (2Н, 7 СН2), [3,73 д (1Н) и 3,41 д (1Н, J 12,4Гц) СН2], 3,74 с (2Н, СН2), 2,92 с (3Н, СН3). Знайдено, %: С 34,31; Вr 45,51; N 4,11. C10H11Br2NOS. Вираховано, %: С 34,02; Вr 45,36; N 3,97. Сіль Vb кипятять у 50мл льодяної оцтової кислоти впродовж 30 хвилин, реакційну суміш охолоджують, кристали солі фільтрують, промивають 7мл льодяної оцтової кислоти, естером і висушують. В результаті виділяють 28г чистого 4(бромометил)-2-метил-1,3-тіазол-3-іум броміду (Іb). Вихід 28г (84%), т.пл. 152°С. Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц), d, м.д.: 7,93 д (2Н, J 7,6Гц, H2,6Ph), 7,46 м (3Н, H3,4,5Ph), 7,70 с (1Н, CH-S), 4,71 с (2Н, СН2). Знайдено, %: С 36,04; Вr 48,02; N 5,04. C10H9Br2NS. Вираховано, %: С 35,85; Вr 47,70; N 4,80. Синтез 4-(бромометил)-2-феніл-1,3-тіазолу (IIb). Водний розчин солі Іb обробляють розчином амоніаку. Осад экстрагують (3´25мл) бензолу або (3´40мл) хлороформу. Органічну фазу відділяють, струшують з СаСl2 і пропускають через тонкий слой силікагелю, розчинник випарюють. В результаті виділяють 23г 4-(бромометил)-2-феніл-1,3тіазолу (IIb). Вихід 23г (90%), т.пл. 75°С. Спектр ЯМР 1Н (ДМСО-d6), Varian Mercury 400; (400МГц), d, м.д.: 7,93 д (2Н, J 7,6Гц, H2,6Ph), 7,70 с (1Н, CHS); 7,47 м (3Н, H3,4,5Ph), 4,73 с (2Н, СН2). Знайдено, %: С 47.37; Вr 31.70; N 5,71. C10H8BrNS. Вираховано, %: С 47,26; Вr 31,44; N 5,51. Приклад 2 До розчину 0,1моль бензкарботіоаміду додають 0,2моль 1,3-дибромацетону 5 в 100мл ацетонітрилу, перемішують до повного розчинення і залишають до повного виділення продукту реакції. Осад відфільтровують промивають спиртом і висушують. В результаті виділяють 31г 4(бромометил)-4-гідрокси-2-феніл-4,5-дигідро-1,3тіазол-3-іум броміду (Vb). Вихід 29г (80%). Сіль V кип’ятять у 50мл льодяної оцтової кислоти впродовж 30 хвилин, реакційну суміш охолоджують, кристали солі фільтрують, промивають 7мл льодяної оцтової кислоти, естером і висушують. В результаті виділяють 27г чистого 4(бромометил)-2-метил-1,3-тіазол-3-іум броміду (Іb). Вихід 25г (80%). Водний розчин солі Іb обробляють розчином основи, наприклад К2СО3 осад экстрагують (3´25мл) бензолу або (3´40мл) хлороформу. Органічну фазу відділяють, струшують з СаСl2 і пропускають через тонкий шар силікагелю, розчинник випарюють. В результаті виділяють 21г 4(бромометил)-2-феніл-1,3-тіазолу (IIb). Вихід 21г (82%). Синтез 4-(бромометил)-2-R-1,3-тиазол-3-іум бромідів (IIc-f). Загальний метод Приклад 1 До розчину a-ціанотіоацетамиду (IIIс) або відповідного похідного a-ціанотіоацетаміду (IIIс) IIId, IIIе, додають 0,1моль 1,3-дибромацетону (IV) в 100-150мл етилацетату перемішують до повного розчинення і залишають до повного виділення продукту реакції. Осад відфільтровують промивають етилацетатом, спиртом і піддають дегідратації 41094 8 (наприклад кип'ятінням в льодяній оцтовій кислоті). За цим методом отримують наступні проміжні четвертинні солі: 24г (84%) 4-(бромометил)-2(ціанометил)-1,3-тіазол-3-іум бромід (Іс), 20г (52%) 4-(бромометил)-2-[(Z)-1-ціано-2-фенілетил]-1,3тіазол-3-іум бромід (Id), 39г (90%), 4-(бромометил)2-[(Z)-1-ціано-2-(4-гідрокси-3-метоксифеніл)-eтил]1,3-тіазол-3-іум бромід (Іе), 28г (64%) 4(бромометил)-2-{[(Z)-1-ціано-2-[4(диметиламіно)феніл]-eтил}-1,3-тіазол-3-іум бромід (If). 4-(бромометил)-2-(ціанометил)-1,3-тіазол-3-іум бромід (Іс). Вихід 24г (84%), т. розк. 138°С. Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц), d, м.д.: 7,95 с, (1Н, CH-S); 7,02 с, (1H, с, СН); 4.70 (2Н, с, СН2-Вr). Знайдено, %: С 24,14; Вr 53,54; N 9,36; S 10,68. C6H6Br2N2S. Вираховано, %: С 24,18; Вr 53,63; N 9,40; S 10,76. 4-(бромометил)-2-[(Z)-1-ціано-2-фенілeтил]1,3-тіазол-3-іум бромід (Id). Вихід 20г (52%), т. розк. 232°С. Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц), d, м.д.: 8,23 с, (1Н, CH-S); 8.01-7.99 м., (2Н, прот. феніл.); 7,87 с, (1Н, с, СН); 7,54-7,53 м., (3Н, прот. феніл.); 4.71 (2Н, с, СН2Br). Знайдено, %: С 40,32; Вr 41,30; N 7,19; S 8,23. C13H10Br2N2S. Вираховано, %: С 40,44; Вr 41,39; N 7,26; S 8.30. 4-(бромометил)-2-[(Z)-1-ціано-2–(4-гідрокси-3метоксифеніл)-eтил]-1,3-тіазол-3-іум бромід (Іе). Вихід 39г (90%), т. розк. 217-218°С. Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц), d, м.д.: 8,07 с, (1Н, CH-S); 7,76 с, (1Н, с, СН); 7,69 м., (1Н, a¢-прот. феніл.); 7.49 д., (1Н, 3JH,H=8,0Гц, a-прот. феніл.); 7.90 д., (1Н, 3JH,H=7,6Гц, b-прот. феніл.); 4.69 (2Н, с, СH2-Br); 3.87 (3Н, с, О-СН3). Знайдено, %: С 38,89; Вr 36,86; N 6,39; S 7,37. C14H12Br2N2O2S. Вираховано, %: С 38,91; Вr 36,98; N 6,48; S 7,42. 4-(бромометил)-2-{[(Z)-1-ціано-2-[4(диметиламіно)феніл]-eтил}-1,3-тіазол-3-іум бромід (If). Вихід 28г (64%), т. розк. 175°С. Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц), d, м.д.: 7,97 с, (1Н, CH-S); 7,89 д., (2Н, 3JH,H=8,8Гц, a, a¢-прот. феніл.); 7,68 с, (1Н, с, СН); 6,80 д., (1Н, 3 JH,H=8,8Гц, b¢, b-прот. феніл.); 4,67 (2Н, с, СН2-Вr); 3.3 (6Н, с, СН3 и СН3). Знайдено, %: С 41.86; Вr 37.13; N 9.68; S 7,39. C15H14Br2N3OS. Вираховано, %: С 41,98; Вr 37,24; N 9,79; S 7,47. Приклад 2 До розчину a-ціанотіоацетамиду (IIIс) або відповідного похідного a-ціанотіоацетаміду (IIIс) IIId, IIIе, НК додають 0,1моль 1,3-дибромацетону (5) в 100-200мл ацетонітрилу перемішують до повного розчинення і залишають до повного виділення продукту реакції. Осад відфільтровують промивають етилацетатом, спиртом і піддають дегідратації (наприклад кип'ятінням в льодяній оцтовій кислоті). За цим методом отримують наступні проміжні четвертинні солі: Вихід 18г (63%), 4-(бромометил)2-(ціанометил)-1,3-тіазол-3-іум бромід (Іс), 29г (49%), 4-(бромометил)-2-[(Z)-1-ціано-2-фенілзтил]1,3-тіазол-3-іум бромід (Id), 32г (73%), 4(бромометил)-2-[(Z)-1-ціано-2-(4-гідрокси-3метоксифеніл)-eтил]-1,3-тіазол-3-іум бромід (Іе), 9 41094 27г (61%), 4-(бромометил)-2-{[(Z)-1-ціано-2-[4(диметиламіно)феніл]-eтил}-1,3-тіазол-3-іум бромід (If). Синтез 4-Бромометил-2-R-1,3-тіазолів (IIс-е). Приклад 1 Загальний метод: Солі Іс-е розчиняють у воді і по каплям додають розчин основи (наприклад насичен. розчин К2СО3) осад экстрагують (3´25мл) бензолу або (3´40мл) хлороформу. Органічну фазу відділяють, струшують з СаСl2 і пропускають через тонкий шар силікагелю, розчинник випарюють. В результаті виділяють 17г (80%), 2-[4-(бромометил)-1,3тіазол]ацетонітрил (IIс), 15г (51%) (Z)-2-[4(бромометил)-1,3-тіазол-2-іл]-3-феніл-2пропененітрил (IId), 30г (86%), (Z)-2-[4(бромометил)-1,3-тіазол-2-іл]-3-(4-гідрокси-3метоксифеніл)-2-пропененітрил (IIе). 2-[4-(бромометил)-1,3-тіазол]ацетонітрил (IIе). Вихід 17г (80%), т. пл. 56-57°С. ІЧ спектр, v, см-1: 2248 (CN). Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц),d, м. д.: 7,69 с, (1Н, CH-S); 4,66 с, (2Н, с, СН2); 4.43 (2Н, с, СН2-Вr). Знайдено, %: С 33,92; Вr 37,08; N 13,12; S 15,09. C6H5BrN2S. Вираховано, %: С 33,20; Вr 36,81; N 12,90; S 14,77. (Z)-2-[4-(бромометил)-1,3-тіазол-2-іл]-3-феніл2-пропененітрил (IId). Вихід 15г (51%), т. пл. 133134°С. ІЧ спектр, n, см-1: 2219 (CN). Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц),d, м. д.: 8,24 с, (1H, CH-S); 8,02-8,01 м., (2Н, прот. феніл.); 7,85 с, (1Н, с, СН); 7,55-7,54 м., (3Н, прот. феніл.); 4.73 (2Н, с, СН2-Вr). Знайдено, %: С 51,67; Вr 66,70; N 9,66; S 10,91. C13H9BrN2S. Вираховано, %: С 51,16; Вr 66,18; N 9,18; S 10,51. (Z)-2-[4-(бромометил)-1,3-тіазол-2-іл]-3-(4гідрокси-3-метоксифе-ніл)-2-пропененітрил (IIе). Вихід 30г (86%), т. пл. 134°С. ІЧ спектр, n, см-1: 2215 (CN). Спектр ЯМР 1Н (ДМСО-d6); Varian Mercury 400; (400МГц),d, м. д.: 8,19 с, (1H, CH-S); 7,77 с, (1H, с, СН); 7,69 с, (1Н, a¢-прот. феніл.); 7,51 д., (1Н, 3JH,H=8,0Гц, a-прот. феніл.); 6.90 д., (1Н, VH,H=8,0Гц, b-прот. феніл.); 4.70 (2Н, с, СН2Вr); 3.89 (3Н, с, О-СН3). Знайдено, %: С 48,07; Вr Комп’ютерна верстка О. Рябко 10 23,02; N 8,01; S 9.26. C14H11BrN2O2S. Вираховано, %: С 47,88; Вr 22,75; N 7,98; S 9,13. Приклад 2 Загальний метод: Солі Іс-е розчиняють у воді і по каплям додають розчин основи (наприклад NH4OH) осад экстрагують (3´25мл) бензолу або (3´40мл) хлороформу. Органічну фазу відділяють, струшують з СаСl2 і пропускають через тонкий шар силікагелю, розчинник випарюють. В результаті виділяють 16г (75%), 2-[4-(бромометил)-1,3-тіазол]ацетонітрил (IIс), 14г (47%) (Z)-2-[4-(бромометил)-1,3-тіазол-2іл]-3-феніл-2-пропененітрил (IId), 26г (74%), (Z)-2[4-(бромометил)-1,3-тіазол-2-іл]-3-(4-гідрокси-3метоксифеніл)-2-пропененітрил (IIе). Таким чином створено більш зручний спосіб синтезу похідних 4-(бромометил)-2-R-1,3-тіазол-3іум бромідів та 4-бромометил-2-R-1,3-тіазолів, застосування яких дозволить розширити асортимент проміжних сполук які можуть бути застосовані для синтезу фізіологічно активних речовин в медицині, який зменшив трудоємкість виділення продукту, час проведення самої реакції, підвищив вихід продукту реакції та безпеку проведення синтезу. Джерела інформації: 1. Storer, R. Ian; Takemoto, Toshiyasu: Jackson, Philip S.; Brown, DeargS.; Baxendale, Ian R.; Ley, Steven V.; //CEUJED; Chem. Europ. J. EN; - 2004, 10;-10, - p.2529-2547. 2. Jae-Chul Jung, Rajashaker Kache, Kimberly K. Vines, Yan-Song Zheng, Panicker Bijoy, Muralikrishna Valluri, and Mitchell A. Avery. // Total Syntheses of Epothilones В and D // J. Org. Chem. 2004, - 69, - p.9269-9284. 3. G. Vervin, J.P. Aune, H.J.M. Dou und J. Metzger. //Réactivite radicalaire en série thiazolique. Synthéses en série thiazolique daryl thiazoles et derives. Etud analytigue. //Bull. Soc. Chim. Fr. - 1967 - p.4523-4533. 4. Benno Krieg und Jtirgen Mittner. // NBromsuccinimid-Bromierung von substituierten Methylthiazolen // Liebigs Ann. Chem. - 1981, - p.623632. Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of 4-(bromomethyl)-2-r-1,3-thiazol-3-ium bromides and 4-bromomethyl-2-r-1,3-thiazoles
Автори англійськоюKovalenko Natalia Volodymyrivna, Volovenko Yulian Mykhailovych
Назва патенту російськоюПроизводные 4-(бромометил)-2-r-1,3-тиазол-3-иум бромидов и 4-бромометил-2-r-1,3-тиазолов
Автори російськоюКоваленко Наталия Владимировна, Воловенко Юлиан Михайлович
МПК / Мітки
МПК: C07D 277/00
Мітки: 4-(бромометил)-2-r-1,3-тіазол-3-іум, бромідів, 4-бромометил-2-r-1,3-тіазолів, похідні
Код посилання
<a href="https://ua.patents.su/5-41094-pokhidni-4-bromometil-2-r-13-tiazol-3-ium-bromidiv-ta-4-bromometil-2-r-13-tiazoliv.html" target="_blank" rel="follow" title="База патентів України">Похідні 4-(бромометил)-2-r-1,3-тіазол-3-іум бромідів та 4-бромометил-2-r-1,3-тіазолів</a>
Попередній патент: Цифровий поляриметр
Наступний патент: Склад для захисту металів від корозії
Випадковий патент: Спосіб діагностики розвитку остеопорозу









