Спосіб визначення амонійного азоту
Номер патенту: 57802
Опубліковано: 15.07.2003
Автори: Демуцька Людмила Миколаївна, Калініченко Іван Омелянович
Формула / Реферат
1. Спосіб визначення амонійного азоту, що включає обробку аналізованої проби сумішшю розчинів тетрайодомеркуріату калію та гідроксиду калію (натрію) з наступним вимірюванням оптичної густини одержаного розчину, який відрізняється тим, що суміш розчинів тетрайодомеркуріату калію та гідроксиду калію (натрію) готують безпосередньо перед введенням в пробу, а об'єми вказаних розчинів визначають із таких співвідношень:
VHg = 0,001Vo/СHg ÷ 0,002Vo/CHg,
VОН = 80VHgCHg/СOH ÷ 100VHgCHg/COH,
де VHg - об'єм розчину тетрайодомеркуріату калію з молярною концентрацією (0,05 - 0,2) М, в перерахунку на ртуть (ІІ), см3;
VOH - об’єм розчину гідроксиду калію (натрію) з молярною концентрацією (2 - 8) М, в перерахунку на гідроксид, см3;
Vо – реакційний об'єм, см3;
СHg - молярна концентрація тетрайодомеркуріату калію в перерахунку на ртуть(ІІ), М;
COH - молярна концентрація гідроксиду калію (натрію) в перерахунку на гідроксид, М,
а оптичну густину вимірюють при двох значеннях довжини хвилі.
2. Спосіб за п.1, який відрізняється тим, що вимірювання здійснюють при значеннях довжини хвилі 440 та 600 нм.
Текст
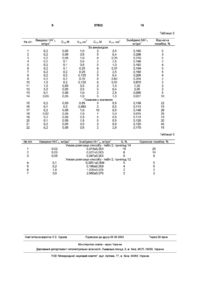
1 Спосіб визначення амонійного азоту, що включає обробку аналізованої проби сумішшю розчинів тетрайодомеркуріату калію та гідроксиду калію (натрію) з наступним вимірюванням оптичної густини одержаного розчину, який відрізняється тим, що суміш розчинів тетрайодомеркуріату калію та гідроксиду калію (натрію) готують безпосередньо перед введенням в пробу, а об'єми вказаних розчинів визначають із таких співвідношень Винахід відноситься до аналітичної хімії, зокрема, до методів визначення аміаку та ІОНІВ амонію в водних розчинах, і може бути використаний в аналізі питних, природних і стічних вод, в контролі процесів водоочистки, в наукових дослідженнях Найбільш чутливими методами визначення амонійного азоту є фотометричні [Волынец В Ф , Волынец М П Аналитическая химия азота Москва Наука, 1977 - С 84-109] [1] Серед них метод з реактивом Несслера та метод з фенолппохлоритним реагентом найбільш широко застосовуються для аналізу водних розчинів [Новиков Ю В , Ласточкина К О , Болдина З Н Методы исследования качества воды водоемов Москва Медицина, 1990 - С 74-80] [2] Спосіб визначення амонійного азоту з фенолппохлоритним реагентом полягає в обробці аналізованої проби розчином солі марганцю (каталізатор), лужними розчинами феноляту натрію та гіпохлориту і фо-тометруванні утвореної забарвленої сполуки Межа визначення становить 0,0iMrNH + 4 /flM 3 [2, C 78-80] Суттєвими недоліками способу є трудоємкість та велика затратність часу на приготування розчинів реагентів, що унеможливлює його застосування для експресного моніторингу стану водних об'єктів, незважаючи на його високу чутливість Найбільш близьким до винаходу за технічною суттю і результатом, що досягається, є спосіб визначення амонійного азоту з реактивом Несслера [2 С 74-77] Цей реактив являє собою суміш розчинів тетрайодомеркуріату(11) калію і гідроксиду калію (натрію) - К2[НдІ4]КОН(ІЧаОН) ВІДОМИЙ спосіб реалізується наступним чином До 50см3 аналізованої проби додають по 1см3 розчину тартрату калію-натрію (для усунення V H g = 0,001 Vo/Снд - 0 , 0 0 2 V 0 / C H 9 , VoH - 80\/ндСнд/СоН ~ 1 00\/ндСнд/СоН, де \/нд - об'єм розчину тетрайодомеркуріату калію з молярною концентрацією (0,05 - 0,2) М, в перерахунку на ртуть (II), см 3 , VOH - об'єм розчину гідроксиду калію (натрію) з молярною концентрацією (2 - 8) М, в перерахунку на гідроксид, см 3 , Vo - реакційний об'єм, см 3 , Снд - молярна концентрація тетрайодомеркуріату калію в перерахунку на ртуть(ІІ), М, Сон - молярна концентрація гідроксиду калію (натрію) в перерахунку на гідроксид, М, а оптичну густину вимірюють при двох значеннях ДОВЖИНИ ХВИЛІ 2 Спосіб за п 1 , який відрізняється тим, що вимірювання здійснюють при значеннях довжини хвилі 440 та 600 нм О о 00 ю 57802 заважаючого впливу домішок металів у пробі) та реактиву Несслера Через 10хв вимірюють оптичну густину розчину забарвленої сполуки, що утворилась, при довжині хвилі 425нм Згідно стандарту [ГОСТ 4Г92-82 Вода питьевая Методы определения минеральных азотсодержащих веществ] [3], даний метод повинен забезпечувати нижню межу визначення амонійного азоту у воді на рівні 0,15мг NHVflM 3 При цьому відносна похибка результатів повинна становитиі 5% в усьому інтервалі концентрацій (до Змг NHVflM 3 ) Як показали наші дослідження, застосування торгових препаратів реактиву Несслера, виготовлених згідно одних і тих же технічних умов [Технические условия 6-09-2089-77 Реактив Несслера (калия тетраиодомеркуриат в щелочном растворе)] [4], при аналізі однієї і тієї ж проби води дає різні результати як по чутливості, так і по точності (експериментальні дані наведені в табл 1), Для з'ясування причин розбіжностей результатів визначення амонійного азоту з різними препаратами реактиву Несслера нами був проведений аналіз двох торгових препаратів А (з етикеткою - УКРХИМЭКСПО Реактив Несслера чда ТУ 6-09-2089-77 Перефасовано ОАО "Киевский завод РИАП") і Б (з етикеткою - 160008 Реактив Несслера Калия тетраиодо-меркуриат(ІІ) в щелочном растворе чда ^[HgUJKOHfNaOH) ТУ 6-09-2089-77 Серия 5 Дата 12-97 Гарантийный срок хранения 1 год) на вміст тетрайодомеркуріату та гідроксиду, оскільки концентрації цих компонентів не вказуються ні на етикетках торгових препаратів, ні в ТУ [4] Встановлено, що препарат А містить 0.0490М К2НдЦ і 1,16М КОН, а препарат Б - 0.0613М К2НдЦ і 2.15М NaOH Таким чином, у препараті А концентрації тетрайодомеркуріату та гідроксиду менші, ніж в препараті Б ВІДПОВІДНО В 1,25 та 1,85 разів Оскільки при визначенні амонійного азоту за відомим способом додається один і той же об'єм реактиву Несслера, при застосуванні різних препаратів цього реактиву в аналізованій пробі встановлюються різні концентрації тетрайодомеркуріату та гідроксиду І, як випливає з даних табл 1, це призводить до розбіжностей в результатах аналізу, високої похибки визначення та низької чутливості Так, нормована стандартом [3] чутливість визначення з препаратами А і Б не досягається ні для природної, ні для дистильованої води Більше того, препарат А взагалі є непридатним для аналітичного застосування, тому що він не забезпечує повноти переведення визначуваного компонента в забарвлений продукт реакції ні при низьких, ні при високих концентраціях амонійного азоту в пробі, а звідси - висока похибка визначення У порівнянні з препаратом А препарат Б дає кращі результати, особливо на дистильованій волі Але при переході до високомшералізованої води, якою, наприклад, є колодязна, результати визначення амонійного азоту з препаратом Б також характеризуються високою похибкою, а отже низькою точністю Таким чином, основними недоліками відомого способу визначення амонійного азоту з реактивом Несслера є низька чутливість, низька точність, велика розбіжність результатів при переході від одного препарату реактиву до іншого В основу винаходу поставлена задача вдосконалити спосіб визначення амонійного азоту з реактивом Несслера шляхом встановлення оптимальних умов проходження хімічної реакції, які-забезпечать найбільш повне переведення визначуваного компонента в забарвлений продукт реакції, а також оптимальних умов вимірювання аналітичного сигналу, і тим самим - досягнення технічного результату підвищення чутливості та точності визначення амонійного азоту Для вирішення поставленої задачі запропоновано спосіб визначення амонійного азоту, що включає обробку аналізованої проби сумішшю розчинів тетрайодомеркуріату калію та гідроксиду калію (натрію) з наступним вимірюванням оптичної густини розчину, в якому, згідно винаходу, готують розчини тетрайодомеркуріату калію з концентрацією (0,050,2)М, в перерахунку на ртуть(ІІ), і ппроксиду калію або натрію з концентрацією (2-8)М, в перерахунку на гідроксид, і визначають об'єми вказаних розчинів із наступних співвідношень VHg=0,001 Vo/Снд •• 0,002 V0/CH9 * V 0 H = 80 VHg Снд/Сон - 100 VHg Сн9/СОн, Де VHQ - об'єм розчину тетрайодомеркуріату калію з молярною концентрацією (0,05-0,2)М, в перерахунку на ртуть(ІІ), см 3 , VOH - об'єм розчину гідроксиду калію або натрію з молярною концентрацією (2-8)М, в перерахунку на гідроксид, см Vo - реакційний об'єм, см , Снд молярна концентрація тетрайодомеркуріату калію, в перерахунку на ртуть(ІІ), М, Сон - молярна концентрація гідроксиду калію або натрію, в перерахунку на гідроксид, М, причому суміш розчинів готують безпосередньо перед введенням в пробу, а оптичну густину вимірюють при двох значеннях ДОВЖИНИ ХВИЛІ Нами експериментальне встановлено, що саме заявлені концентрації та об'єми вказаних розчинів створюють в реакційному об'ємі оптимальні концентрації тетрайодомеркуріату калію (0,001-0,002)М, в перерахунку на ртуть(ІІ), і гідроксиду калію (натрію) (0,08-0,2)М , в перерахунку на гідроксид, що забезпечує високу чутливість і високу точність визначення амонійного азоту При цьому слід ВІДМІТИТИ, що підвищення точності визначення, особливо при низькій концентрації амонійного азоту в пробі, досягається одночасно і оптимізаціею умов вимірювання аналітичного сигналу, тобто вимірюванням оптичної густини одержаного розчину при двох значеннях довжини хвилі - в умовах сильного поглинання світла забарвленою сполукою і в умовах, де вона світло практично не поглинає Це дає змогу врахувати поглинання світла випадково забрудненими стінками кювети та домішками завислих речовин у пробі, що не здійснюється відомим способом 57802 Таким чином, сукупність суттєвих ознак способу, що пропонується, є необхідною і достаньою для досягнення технічного результату, який забезпечується винаходом - збільшення чутливості визначення амонійного азоту до 0,03мг NHVflM 3 1 точності до (10-2)% Спосіб реалізується наступним чином Як фотометричний реагент використовують суміш розчину І - тетрайодомеркуріату калію з концентрацією Снд= (0,05-0,2)М, в перерахунку на ртуть(ІІ), і розчину II - гідроксиду калію або натрію з концентрацією Сон-(2-8)М, в перерахунку на гідроксид Розчин І готують розчиненням у воді наважок препаратів йодиду ртуті (І І) і йодиду калію, взятих у молярному співвідношенні 1 2 Для визначення амонійного азоту у мірну колбу МІСТКІСТЮ 25-50см вносять ВІДПОВІДНІ об'єми розчинів І і II, встановлені із заявлених співвідношень, додають при перемішуванні аналізовану пробу, дистильовану воду до мітки і через Юхв вимірюють оптичну густину розчину при 44нм (А-і) і при бООнм (А2) Розраховують різницю величин оптичної густини (А1-А2) і за градуювальним графіком визначають концентрацію амонійного азоту в пробі При аналізі води, що містить солі кальцію та магнію, в пробу води попередньо вводять розчин тартрату калію-натрію Спосіб дозволяє визначати концентрацію амонійного азоту в розчині від 0,03 до Змг/дм3, в перерахунку на ННд Відносна похибка визначення становить (10-2)% Характеристика реагентів і приладів Ртуті(ІІ) йодид, ТУ 6-09-ОР-374-85, х ч Калію йодид, ГОСТ 4232-74, х ч Натрію ппроксид, ГОСТ 4328-77, х ч Калій-натрій виннокислий 4-водний, ГОСТ 5845-79, ч д а Вода дистильована, ГОСТ 6709-72, очищена від домішок аміаку перегонкою з 0,01 М сірчаною кислотою Спектрофотометр СФ-26, ТУ 25-04 ОПБ 533 319-73 Приклади реалізації способу за винаходом Приклад 1 Визначення амонійного азоту в модельному розчині, що містить 1мг NHVflM 3 Попередньо готують розчин І, у якому Снэ=0,05М (розчиняють у ВОДІ 2,2720г йодиду ртуті (І І) і 1,6600г йодиду калію і доводять об'єм розчину до 100см3) і розчин II, у якому Сон-2М (розчиняють у воді 8,000 г гідроксиду натрію і доводять об'єм розчину до 100см3) Відбирають певні об'єми одержаних розчинів у ВІДПОВІДНОСТІ З заявленими співвідношеннями \/нд=0,001 25/0,05= 0,5см3, VOH-80 0,5 0,05/2=1,0см3 і вносять їх у мірну колбу МІСТКІСТЮ 25см 3 Після ЦЬОГО ВНОСЯТЬ при перемішуванні суміш, що складається з 20см3 розчину хлориду амонію з концентрацією 1,25мкг N H V C M 3 І 0,5СМ 3 50%-ГО розчину тартрату ка-лів натрів, додають воду до мітки і через 10хв вимірюють оптичну густину при 440нм і при бООнм в кюветі з товщиною шару 5см Одержано Аі=0,549, А2=0,026 Знайдено NH + 4 1,02мг/дм3 Відносна похибка визначення становить 2% (табл 2, приклад 11) Приклад 2 Визначення амонійного азоту в модельному розчині, що містить 0,1мг NH 4/дм , Проводять ті ж операції і використовують ті ж розчини, що і в прикдаді 1 Але для приготування суміші реагентів об'єми розчинів І і II визначають із наступних співвідношень \/нд= 0,002 25/0,05=1,0см3, V OH =100 1 0,05/2=2,5см3, а для створення у модельному розчині заданої концентрації амонійного азоту відбирають 2,0см3 розчину хлориду амонію Одержано Аі=0,061, А2=0,010 Знайдено І\ІН+40,095мг/дм3 Відносна похибка визначення становить 5% (табл 2, приклад 13) Аналогічно, описаним прикладам були проведені досліди по визначенню амонійного азоту в широкому діапазоні його концентрацій з використанням розчинів тетрайодомеркуріату калію та гідроксиду натрію в концентраціях та об'ємах, що знаходяться як в заявлених діапазонах, так і за їх межами Встановлено, що заявлені концентрації та об'єми вказаних розчинів вибрані з умов, які забезпечують максимальну чутливість і точність визначення амонійного азоту (табл 2, приклади 114) Застосування менш концентрованих розчинів тетрайодомеркуріату калію, ніж заявлені, призводить до різкого збільшення відносної похибки результату аналізу внаслідок зменшення виходу забарвленого продукту реакції Останнє обумовлене розкладом реактиву в сильно розведених розчинах (табл 2, приклад 15) При використанні більш концентровних розчинів тетрайодомеркуріату калію, ніж заявлені, відносна похибка визначення теж зростає Але тепер вона обумовлена збільшенням похибки вимірювання об'єму реактиву внаслідок зменшення його величини зі збільшенням концентрації, що випливає із заявлених співвідношень (табл 2, приклад 16) При позамежному збільшенні концентрації гідроксиду натрію він спричинює розклад тетрайодомеркуріату з утворенням гідроксиду ртуті в процесі приготування суміші розчинів цих реагентів Вихід забарвленої сполуки стає неповним, і похибка визначення різко збільшується (табл 2, приклад 17) При застосуванні менш концентрованих розчинів гідроксиду натрію, ніж заявлені, зменшується чутливість способу, оскільки постає необхідність збільшення об'єму реактиву (із заявлених співвідношень) за рахунок зменшення об'єму проби Не ілюструють приклади 14 і 18 табл 2 При об'ємі проби 20см3 амонійний азот при концентрації 0,03мг/дм3 визначається з задовільною точністю (приклад 14) При зменшенні об'яму проби до 15см3 концентрація амонійного азоту в розчині (після змішування всіх компонентів реакції") стає нижчою, ніж нижня межа визначення, і відносна похибка визначення різко збільшується (приклад 18) Використання розчинів як тетрайопомеркуріату калію, так і гідроксиду натрію в об'ємах менших, ніж визначені із заявлених співвідношень, призводить до збільшення відносної похибки результатів (табл 2, приклади 19 і 21) В цих випадках концентрації ртуті (І І) або 57802 гідроксиду натрію, які встановлюються в розчині, стають недостатніми для повного переведення амонійного азоту в забарвлену сполуку При позамежному збільшенні об'єму розчину тетрайодомеркуріату калію зростає величина оптичної густини холостої проби, що збільшує відносну похибку визначення, особливо малих концентрацій амонійного азоту (табл 2, приклад 20) Варто ВІДМІТИТИ також, що використання зайвого надлишку сполуки ртуті (І І) недоцільне і з точки зору екології внаслідок її токсичності При збільшенні об'єму гідроксиду натрію до позамежних значень відносна похибка визначення зростає, тому що в цих умовах крім забарвленої розчинної сполуки, в яку переходить амонійний азот, частково утворюється також майже безбарвна нерозчинна сполука (табл 2, приклад 22) Нами встановлено також, що результати, одержані для нижніх заявлених концентрацій тетрайодомеркуріату калію та гідроксиду натрію, але позамежних об'ємів їх розчинів, (табл 2, приклади 19-22) підтверджуються для всього заявленого інтервалу концентрацій цих реагентів Суттєвою ознакою запропонованого способу є вимірювання оптичної густини забарвленого розчину при двох значеннях довжини хвилі, що забезпечує при наявності решти ознак високу точність результатів визначення Дослідження показують, що вимірювання оптичної густини цього розчину лише при одному значенні довжини хвилі, як це робиться у відомому способі, призводить до зниження точності визначення амонійного азоту, особливо при його низьких концентраціях Так, у модельному розчині, що містить 0,1мг NHVflM 3 , знайдено 0,115мг/дм3 (відносна похибка - 15%), у модельному розчині що містить 0,05мг NHVflM знайдено 0,034мг/дм (відносна похибка - 34%) В умовах визначення амонійного азоту за винаходом при тих же 8 концентраціях значення відносної похибки становлять ВІДПОВІДНО 5 % і 6% (табл 3, приклади 3,4) В табл 3 наведені дані, які характеризують чутливість, точність та відтворюваність (відносне стандартне відхилення) результатів визначення амонійного азоту за винаходом Амонійний азот у вигляді хлориду амонію вводили в модельний розчин (джерельна вода, що містила менше, ніж 0,01мг NHVflM 3 ) і визначали його в оптимальних умовах проведення реакції з тетрайодомеркуріатом калію та гідроксидом натрію (п=5, Р=0,95) Як видно з даних табл 3, нижня межа визначення (чутливість) способу становить 0,03мг NHVflM 3 Ця концентрація визначається з задовільною точністю (відносна похибка не перевищує 10%) При подальшому ж зниженні концентрації (наприклад, до 0,02 мг/дм3) відносна похибка визначення різко збільшується (25%) При цьому слід ВІДМІТИТИ, шо в інтервалі концентрацій амонійного азоту від 0,05 до Змг/дм3 запропонований спосіб забезпечує високу точність визначення -відносна похибка не перевищує 6% Таким чином, запропонований спосіб визначення амонійного азоту характеризується високою чутливістю (0,03мг NHVflM 3 ), точністю (відносна похибка становить 10-2%) та надійністю результатів, що не досягається втомим способом з застосуванням торгових препаратів реактиву Несслера, і в цьому полягають незаперечні переваги запропонованого способу над відомим До того ж, у зв'язку з тим, що в запропонованому способі не використовуються торгові препарати реактиву Несслера, він є більш економічно вигідним і екологічно безпечним Це пов'язане з тим, що вказані препарати внаслідок обмеженого терміну їх придатності, як правило, використовуються неповністю, а залишки-відходи забруднюють довкілля Таблиця 1 Вода Дистильована Колодязна Введено NH мг/дм3 за 0,07 0,20 0,20 0.60 Знайдено з Відносна препаратом А, похибка, % 3 мг/дм Невизначавється ЗО 0,,14 0,02 Не визначається 0..08 0.02 87 Знайдено з Відносна препаратом Б, похибка, % 3 мг/дм Не визначається 0,19 0,02 5 0,11 0,02 45 0,45 0,05 25 57802 10 Таблиця 2 № п/п Введено NH+4, мг/дм3 Сн 9 М 1 2 3 4 5 6 7 8 9 10 11 12 13 14 0,2 0,2 0,2 0,2 0,2 0,2 0,2 0,2 0,2 1,0 1,0 3,0 0,1 0,03 0,05 0,05 0,05 0,1 0,1 0,1 0,2 0,2 0,2 0,2 0,05 0,05 0,05 0,05 15 16 17 18 19 20 21 22 0,2 0,1 0,2 0,02 0,2 0,1 0,2 0,2 0,03 0,3 0,05 0,05 0,05 0,05 0,05 0,05 VHg см 3 СонМ V он, см Знайдено NH+4 мг/дм3 Відносна похибка, % 0,190 0,206 0,210 0,196 0,192 0,194 0,190 0,208 0,204 0,970 1,02 2,95 0,095 0,027 5 3 5 2 4 3 5 4 2 3 2 2 5 10 0,156 0,113 0,148 0,015 0,174 0,120 0,120 0,170 22 13 26 25 13 20 40 15 За винаходом 1,0 2 2,5 0,5 5 0,4 1,0 8 0,25 0,5 2 2,5 0,5 5 1,0 0,25 8 0,31 0,25 2 2,5 0,125 5 0,4 0,25 8 0,62 0,125 8 0,31 0,5 2 1,0 0,5 5 0,4 1,0 2 2,5 1,0 5 1,0 Позамежні значення 0,85 5 0,5 0,083 5 0,5 1,0 10 0,5 1,0 1 5,0 0,3 5 0,5 5 0,5 1,5 0,5 2 0,6 0,5 2 2,8 Таблиця 3 № п/п С Введено NH+4., мг/дм'5 Знайдено NH+4, МГ/ДМ"' :r % Умови реалізації способу -табл 2, приклад 14 0,02 0,015±0,003 16 0,03 0,027±0,003 8 0,05 0,047±0,003 5 Умови реалізації способу-табл 2, приклад 12 0,1 0,0951±0,006 5 0,2 0,190±0,009 4 1,0 1,020±0,025 2 3,0 2,950±0,075 2 Комп'ютерна верстка О В Кураєв Відносна похибка, % Підписано до друку 05 08 2003 25 10 6 5 5 2 2 Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ТОВ "Міжнародний науковий комітет", вул Артема, 77, м Київ, 04050, Україна
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for determining content of ammonia nitrogen
Автори англійськоюDemutska Liudmyla Mykolaivna, Kalinichenko Ivan Omelianovych
Назва патенту російськоюСпособ определения содержания аммонийного азота
Автори російськоюДемуцкая Людмила Николаевна, Калиниченко Иван Емельянович
МПК / Мітки
МПК: G01N 21/00, G01N 21/27
Мітки: азоту, амонійного, визначення, спосіб
Код посилання
<a href="https://ua.patents.su/5-57802-sposib-viznachennya-amonijjnogo-azotu.html" target="_blank" rel="follow" title="База патентів України">Спосіб визначення амонійного азоту</a>
Попередній патент: Спосіб виготовлення фундаментів та пристрій для його здійснення
Наступний патент: Спосіб збудження сейсмічних коливань
Випадковий патент: Спосіб стимуляції функціонального дозрівання дендритних клітин, отриманих з моноцитів периферичної крові людини