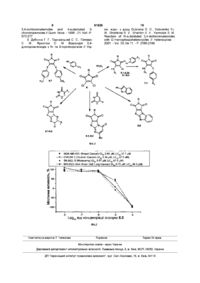
Структури активних сполук, що мають протипухлинну активність, в ряду похідних 1-бензил-3-хлоро-4-аніліно-2,5-дигідро-1н-2,5-піролдіону
Номер патенту: 61626
Опубліковано: 17.11.2003
Автори: Дубініна Галина Григорівна, Тарнавський Сергій Степанович, Ярмолюк Сергій Миколайович, Головач Сергій Михайлович
Формула / Реферат
Структури активних сполук, що мають протипухлинну активність, в ряду похідних 1-бензил-3-хлоро-4-аніліно-2,5-дигідро-1H-2,5-піролдіону, а саме, 1-бензил-3-хлоро-4-(3-гідроксианіліно)-2,5-дигідро-1Н-2,5-піролдіону (а) та 1-бензил-3-хлоро-4-(2-метокси-5-хлораніліно)-2,5-дигідро-1Н-2,5-піролдіону (б), структурних формул:
.
Текст
Структури активних сполук, що мають протипухлинну активність, в ряду похідних 1-бензил-Зхлоро-4-аніліно-2,5-дипдро-1Н-2,5-піролдюну, а саме, 1-бензил-3-хлоро-4-(3-пдроксианілшо)-2,5дипдро-1Н-2,5-піролдюну (а) та 1-бензил-3-хлоро4-(2-метокси-5-хлоранілшо)-2,5-дипдро-1Н-2,5піролдюну (б), структурних формул Пропонований винахід стосується гетероциклічних сполук, а більш конкретно, активних сполук, що мають протипухлинну активність в ряду похідних 1-бензил-3-хлоро-4-анілшо-2,5-дипдро1Н-2,5-піролдюну У 1977р із стрептоміцетів (Streptomyces staurosporeus) був виділений стауроспорин, структура якого була пізніше доведена за допомогою рентгеноструктурного аналізу Дослідження стауроспорину показали, що він інгібує більшість відомих протеш-кіназ, як серин-треонінових, так і тирозинових в низьких концентраціях та виявляє протиракову активність (in vivo) Саме це зумовило підвищений інтерес ХІМІКІВ-СИНТЄТИКІВ до син тезу аналогів стауроспорину Переважна більшість робіт з хімії малеімідів за останні десятиріччя була присвячена синтезу стауроспорину та його аналогів - 3,4-бісіндолілмалеімідних похідних, що в багатьох випадках виявили вищу за стауроспорин специфічність інгібування та протипухлинну активність Важливим фармакофорним фрагментом цих сполук є N-H група малеімідного циклу Синтетично одержані 7-пдроксистауроспорин та сполука NB-506 використовуються в КЛІНІЧНІЙ практиці як антиракові препарати, що діють як інгібітори ВІДПОВІДНО циклінзалежних кіназ (CDKs) татопоізомерази І Відомо, ЩО деякі 3-заміщені N-арил- та Nалкіл-3-хлор-2,5-дипдро-1 Н-2,5-піролдюни мають антибактеріальну активність (Staphylococcus, Eschenchia Coh) [7], але на протипухлинну активність вони перевірені не були В основу пропонованого винаходу поставлена задача виявлення активних структур в ряду похідних 1-бензил-3-хлоро-4-анілшо-2,5-дипдро1Н-2,5-піролдюну, шляхом синтезу похідних 2,5дипдропірол-2,5-дюну з вар'юванням замісників в першому, третьому та четвертому положеннях пірольного циклу та визначення їх протипухлинної активності Поставлена задача вирішується пропонованими активними структурами в ряду похідних 1бензил-3-хлоро-4-анілшо-2,5-дипдро-1Н-2,5піролдюну, а саме, 1-бензил-3-хлоро-4-(3пдроксианіліно)-2,5-дипдро-1Н-2,5-піролдюну (а) та 1-бензил-3-хлоро-4-(2-метокси-5-хлоранілшо)2,5-дипдро-1Н-2,5-піролдюну (б), структурних формул (а) та (б), що мають протипухлинну активність (О (О (О 61626 52 Синтезовані сполуки були тестовані на протипухлинну активність Суть винаходу пояснюється за допомогою графічних матеріалів На фіг 1 - показана схема синтезу На фіг 2 - Графік залежності мітотичної активності від концентрації сполуки 5 2 (активна сполука а) для різних клітинних ЛІНІЙ пухлин Матеріали і методи Контроль за проходженням реакції та чистотою синтезованих сполук здійснювався хроматографічне на пластинах "Silufol UV-254", елюент хлороформ - метанол (9 1) Структуру одержаних сполук доведено за допомогою ПМР-, ІЧ-спектрів та елементного аналізу ІЧ спектри записані на приладах UR-20, Specord 75-IR та Pye Umcam в області 4000-400 см 1 в таблетках КВг Спектри ПМР записані в ДМСО-Оє на приладі "Vanan" з робочою частотою 300МГц і внутрішнім стандартом - тетраметилсиланом Величини ХІМІЧНИХ зсувів визначались з точністю до 0 001 м ч Загальна методика синтезу 1-R-3-xnopo-4г\ІНРі-2,5-дипдро-1Н-2,5-піролдіонів 5 1-5 24 До розчину 0 01 Моль ВІДПОВІДНОГО дихлормалеіміду 4 у 50мл ізопропилового спирту додають 0 021 Моль ВІДПОВІДНОГО аміну і кип'ятять 2 години, охолоджують, відфільтровують, промивають невеликою КІЛЬКІСТЮ ізопропилового спирту та водою Одержані продукти хроматографічно чисті, при необхідності можуть бути перекристалізовані із ізопропілового або етилового спирту Виходи сполук 5 1-5 24-70-95% Біологічне тестування Біологічне тестування синтезованих речовин проводилось на 56 ЛІНІЯХ ракових клітин людини при 5-ти різних концентраціях речовини (10 8 -10 4 М) для з'ясування найбільш ефективної концентрації На першому етапі здійснювався прескринінг сполук на трьох ЛІНІЯХ ракових клітин (Breast, Non-Small Cell Lung, CNS) при одній стандартній концентрації речовини - 10 4 М (Таблиця 1) Ефективність дії речовини на клітинну ЛІНІЮ розраховувалась ВІДПОВІДНО ДО ОДНОГО З наведе них виразів 1)При ({OD t e s t }-{OD 0 })>0 PG = 100x({OD test } - {OD0})/({ODctr,} - {OD0}) 2) При ({OD t e s t } - {OD0}) < 0 .тоді PG = 100x({OD test } - {OD0})/{OD0} , де {OD 0 } - середнє значення вимірів оптичної густини одразу після додавання речовини, {OD t e s t } - середнє значення вимірів оптичної густини після 48 годинної інкубації клітин оброблених речовиною, що тестується, {ODctr|} - середнє значення вимірів оптичної густини після 48 годинної інкубації клітин без додавання речовини (контроль), PG - Percentage Growth - рівень мітотичної активності клітинної лінії після обробки речовиною порівняно з контролем На першому етапі здійснювався прескринінг сполук на трьох ЛІНІЯХ ракових клітин (Breast (рак грудей), Non-Small Cell Lung (карцинома легенів), CNS (рак центральної нервової системи)) при одній стандартній концентрації речовини - 10 М (Таблиця 1) Результати Авторами синтезовано і тестовано на протипухлинну активність 39 похідних 2,5-дипдропірол-2,5-дюну (малеіміду) 5 1-92 (Схема синтезу) Результати прескринінгу, ХІМІЧНІ структури (або назви) замісників R, Ri, R2, R3, R4 сполук 5 1-92 наведені в Таблиці 1 Сполука 5 2 (активна сполука 1-бензил-Зхлоро-4-(3-пдроксианілшо)-2,5-дипдро-1Н-2,5піролдюн (а)) успішно пройшла етап прескринінгу, для неї тотальна мітотична активність для всіх трьох культур клітин склала менше ніж 32% порівняно з контролем Дана сполука була відібрана для подальшого тестування на 56 ЛІНІЯХ пухлинних клітин людини (Таблиці 2, 3) Сполука 5 6 1бензил-3-хлоро-4-(2-метокси-5-хлоранілшо)-2,5дипдро-1Н-2,5-піролдюн (6) виявила меншу активність порівняно зі сполукою а Вона пригнічує проліферативну (мітотичну) активність ракових клітин ВІДПОВІДНО на 51% (рак грудей), 6 1 % (карцинома легенів) та 37% (ЦНС) при концентрації 100DM Результати тестування сполуки 5 2 (активна сполука а) на 56 ЛІНІЯХ пухлинних клітин представлені в Таблиці 3 та на фіг 2 Для тестованого ряду 39 похідних 2,5дипдропірол-2,5-дюну (малеіміду) можна зробити деякі висновки стосовно залежності протипухлинної активності від структури сполуки Якщо в третьому положенні малеімідного циклу сполуки 5 2 (Рис 3 ) замість м-пдрокси-анілінового фрагменту знаходиться залишок первинного або вторинного аліфатичного аміну (сполуки 5 1, 5 105 14, 5 18), то активність -відсутня Заміна -ОН (гідроксильної) групи в структурі 5 2 на -ОСНз (метокси групу) (сполука 5 4) приводить до втрати активності Наявність -ОСНз в положенні 4' (сполука 5 5) або в положенні 2' (сполука 5 3) також веде до втрати активності 2',4'-Диметокси (сполука 5 7) та 2',5'-диметокси похідне (сполука 5 8) - теж не активні Для сполуки 5 6 (N-CH2Ph, 2'-ОСНз-5'-СІ) мітотична активність на клітинах раку легенів - 39%, тобто мітотична активність порівняно з контролем пригнічується на 6 1 % Сполука 6 1, в якій відсутній бензильний замісник в положенні 1 малеімідного циклу, а в положенні З, як і в структурі 5 2, знаходиться залишок мпдроксианілшу, виявляє лише невелике пригнічення мітотичної активності, тому є підстави вважати, що N-бензильний замісник малеімідного циклу - критичний 61626 Продукти анелювання гетероциклічних систем по грані [с] малеімідного циклу (сполуки 8 18 6, 9 1, 9 2) не мають протипухлинного ефекту Отже, біологічне тестування на протипухлинну активність 39 похідних 2,5-дипдропірол-2,5дюну (малеіміду) показало, що 1-бензил-З-хлоро4-(3-пдроксианіліно)-2,5-дипдро-1Н-2,5-піролдюн 5 2 виявляє протипухлинну активність у низько мікромолярній концентрації Для сполуки 5 2 (активна сполука а) знайдено Glso 2 68ПМ, LC50 31 7ПМ (клітинна ЛІНІЯ MDA-MB-435 (Breast Cancer)), GI50 З 35ПМ, LC50 37 6ПМ (клітинна ЛІНІЯ OVCAR-3 (Ovarian Cancer)), GI50 6 75ПМ, 44 5ПМ (клітинна ЛІНІЯ NCI-H23 (Non-small Cell Lung Cancer)) Таким чином, в ряду 3-хлоро-4-анілшо-2,5дипдропірол-2,5-дюну знайдено протипухлинну активність Протипухлинна активність виявлена у 1-бензил-3-хлоро-4-(3-пдроксианіліно)-2,5дипдро-1Н-2,5-піролдюну (1) та у 1-бензил-Зхлоро-4-(2-метокси-5-хлоранілшо)-2,5-дипдро-1Н2,5-піролдюну (2), що може бути використано для подальшої оптимізацм активних структур і створенню на їх основі протипухлинних ЛІКІВ Таблиця 1 Результати прескринінгу сполук 5 1-9 2 на протиракову активність Номер структури 51 5 2 (а) 53 54 55 5 6(6) 57 58 59 510 511 512 513 514 5,15 516 517 518 519 5 20 5 21 5 22 5 23 5 24 61 62 63 64 65 71 81 82 83 84 85 86 87 91 92 Мітотична активність порівняно з контролем, % Замісники R=CH2Ph, Ріциклогексил R=CH2Ph, Ri=(3'-OH3)Ph R=CH2Ph, Ri=(2'-OCH3)Ph R=CH2Ph, Ri=(3'-OCH3)Ph R=CH2Ph, Ri=(4'-OCH3)Ph R=CH2Ph, Ri=(2'-OCH3-5'-CI)Ph R=CH2Ph, Ri=(2',4'-OCH3)2)Ph R=CH2Ph, Ri=(2',5'-(OCH3)2)Ph R=CH2Ph, NHRi=N-(CH3)Ph R=CH2Ph, R1=тeтpaгlдpoфypфypил R=CH2Ph, NHRi=mnepHflHH R=CH2Ph, NHRi=(4'-N-CH3)-nmepa3HH R=CH2Ph, Ri=CH2CH2N(CH3)2 R=CH2Ph, Ri=CH2CH2(3',4'-(OCH3)2)Ph R=CH2Ph, Ri=(2'-COOH)Ph R=CH2Ph, Ri=(3'-COOEt)Ph R=CH2Ph, R1=lll5l-(CH3)2-31-OKCO-21-Ph-21131дипдро-1 Н-4'-піразоліл R=CH2Ph, NHRi=(4'-N-CH2Ph)-ninepa3HH R=CH2CH2Ph, Ri=(2'-OH)Ph R=CH2CH2Ph, Ri=(3'-C1-4'-CH3)Ph R=CH2CH2Ph, R^S'-морфолінопропил R=CH2CH2Ph, R1=тeтpaгlдpoфypфypил R=CH2CH2Ph, Ri=nipHflnnMeTHn R=Ph, Ri=4'-(N-(4"-OCH3Ph))6eH3aMifl R=H, Ri=(3'-OH)Ph R=H, Ri=(4'-OPh)Ph R=H, NHRi=TeTpariflpoi3oxiHoniH R=H, R1=4'-бeнзeнcyльфoнaмlд R=H, NHRi=(4'-N-CH2Ph)-ninepa3HH R=H, Ri=(3',4'-(CH3)2)Ph, R2=CH3 R=CH2Ph, R3=21-тloфeн R=Ph, R3=H R=(3'-C1-4l-CH3)Phl R3=CH3 R=Ph, R3=PH R=Ph, R3=21-тloфeн R=4'-OCH3Ph R=H R=CH2Ph, R4=H R=CH2Ph, R4=CH3 CNS (рак Non-Small Cell центральної Breast (рак Lung (карцинервової сисгрудей) нома легенів) теми) 119 113 125 4 18 1 119 115 114 114 118 130 114 126 137 39 63 49 118 120 117 109 105 94 119 122 131 111 114 116 97 106 94 101 102 93 101 102 99 91 120 96 114 114 131 111 117 126 Висновок Не активна Активна(а) Не активна Не активна Не активна Активна(б) Не активна Не активна Не активна Не активна Не активна Не активна Не активна Не активна Не активна Не активна 125 115 120 Не активна 115 85 94 105 107 103 123 63 64 127 109 123 117 77 89 111 118 106 121 62 100 124 109 111 109 110 104 98 117 61 67 100 103 100 93 99 105 99 107 109 111 88 105 117 132 140 140 140 126 113 115 73 76 129 138 144 128 92 103 131 118 138 142 44 106 115 Не Не Не Не Не Не Не Не Не Не Не Не Не Не Не Не Не Не Не Не Не Не активна активна активна активна активна активна активна активна активна активна активна активна активна активна активна активна активна активна активна активна активна активна 8 61626 Таблиця 2 Перелік ракових клітин, що були використані в біологічних тестах для сполуки 6 2 (активна сполука а) Leukemia CCRF-CEM 1-1І_-60(ТВ) К-562 MOLT-4 RPMI-8226 SR Non-Small Colon CNS Cell Lung Cancer Cancer А549/АТСС COLO205 SF-268 EKVX HCT-15 SF-295 HOP-62 HCT-116 SF-539 HOP-92 НТ29 NCI-H226 KM 12 NCI-H23 SW-620 NCI-H322M NCI-H460 NCI-H522 SNB-19 SNB-75 U251 Renal Prostate Breast Cancer Cancer Cancer 786-0 PC-3 MCF7 ACHN DU-145 NCI/ADR-RES CAKJ-1 MDA-MB231/ATCC HS 578T SK-MEL-28 OVCAR-5 RXr 393 MDA-MB-435 SK-MEL-5 SK-OV-3 SN12C T-47D UACC-257 OVCAR-8 TK-10 UO-31 LOX IMVI UACC-62 Ovarian Cancer MALME-3M IGROV1 OVCAR-3 M14 SK-MEL-2 OVCAR-4 Melanoma Таблиця З Результати тестування сполуки 5 2 (активна сполука а) на 56 ЛІНІЯХ пухлинних клітин людини 50 < (наведені результати досліджень з Клітинна ЛІНІЯ пухлини GI *(|-LM) KM 12 (Colon Cancer) 108 LOX IMVI (Melanoma) 11 2 OVCAR-5 (Ovarian Cancer) 174 SNB-19 (CNS Cancer) 11 8 SN12C (Renal Cancer) 132 MALME-3M (Melanoma) 183 HCT-116 (Colon Cancer) 6 54 DU-145 (Prostate Cancer) 149 UACC-62 (Melanoma) 11 3 HOP-62 (Non-Small Cell Lung Cancer) 126 SF-539 (CNS Cancer) 12,6 SK-MEL-5 (Melanoma) 8 67 NCI-H23 (Non-Small Cell Lung Cancer) 6 75 OVCAR-3 (Ovarian Cancer) 3 35 MDA-MB-435 (Breast Cancer) 2 68 50 ^ TGI (цМ) 25 3 25 7 32 0 26 3 27 5 32 6 21 8 28 1 24 3 25 7 25 4 21 4 19,8 121 8 37 LC 5 0 (цМ) 59 3 59 0 58 9 58 6 57 2 58 1 55 6 53 0 52 4 52 1 51 3 47 5 44 5 37 6 31 7 *Gl5Q концентрація досліджуваної речовини (цМ), при якій ріст ракових клітин зменшується ВДВІЧІ порівняно з контролем, TGI - концентрація, при якій ріст ракових клітин не спостерігається, LC50 ' концентрація, при якій половина ракових клітин гине Перелік літератури 1 Omura S , Iwai Y , Hirano A , Nakayawa A , Awaya J , Tsuchiya T , Takahashi Y , Masuma R A new Alkaloid AM-2282 of streptomyces origin taxonomy, fermentation, isolation and preliminary characterization//J Antibiot -1977 -30 -P 275282 2 Furusaki A , Hashiba N , Matsumoto T X-Ray Crystal Structure of Staurosporme a New Alkaloid from a Streptomyces Strain / J Chem Soc , Chem Commun -1978 -P 800-801 3 Furusaki A, Hashiba N , Matsumoto T, Hirano A, Iwai Y , Omura S The Crystal and Molecular Structure of Staurosporme, a New Alcaloid from a Streptomyces Strain / Bull Chem Soc Jpn -1982 -55 -P 3681-3685 4 Fisher P M , Lane D P Inhibitors of CyclmDependent Kmases as Anti-Cancer Therapeutics // Cur Med Chem -2000 -7 -P 1213-1245 5 Senderowicz A M The Cell Cycle as a Target for Cancer Therapy Basic and Clinical Findings with the Small Molecule Inhibitors Flavopindol and UCN-01 // Oncologist - 2002 -12 P 12-19 6 Bailly С , Qu X , Chaires J В , Co/son P , Houssier С , Ohkubo M , Nishimura S , Yoshman T Substitution at the F-Rmg N-lmide of the Indolocarbazole Antitumor Drug NB-506 Increases the Cytotoxyty, DNA Binding, and Topoisomerase I Inhibition Activities//J Med Chem -1999 -42 -P 2927-2935 7 Andncopulo A D , Yunes R A , Nunes R J , Savi A 0 S , Correa R , Cruz А В , Filho V С Synthesis and antibacterial activity of cyclic imides 61626 3,4-dichloromaleimides and 4-substituted 3 chloromaleimides//Quim Nova -1998 -21, №5-P 573-577 8 Дубинина Г Г, Тарнавський С С, Головач С М , Ярмопюк С М Взаємодія 3,4дихлормалеімідів з N- та S-нуклеофілами // Укр 10 хім журн у друці Dubmma G G , Volovenko Yu М , Shishkina S V , Shishkin 0 V , Yarmoluk S M Reaction of N-substituted 3,4-dichloromaleimides with D-m erca ptoaza h ete rocyc I es // Heterocycles 2001 -Vol 55, №11 -P 2189-2198 Фіг. Комп'ютерна верстка Т Чепелєва Підписне Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійськоюStructures of active compounds having an antitumor activity in the series of derivatives of 1-benzyl-3-chloro-4-aniline-2,5-dihydro-1н-2,5-pyroldion
Назва патенту російськоюСтруктуры активных соединений, обладающих противоопухолевой активностью, в ряду производных 1-бензил-3-хлоро-4-анилино-2,5-дигидро-1н-2,5-пиролдиона
МПК / Мітки
МПК: A61P 35/00, A61K 31/4015, C07D 207/456
Мітки: ряду, похідних, активність, 1-бензил-3-хлоро-4-аніліно-2,5-дигідро-1н-2,5-піролдіону, активних, структури, сполук, мають, протипухлинну
Код посилання
<a href="https://ua.patents.su/5-61626-strukturi-aktivnikh-spoluk-shho-mayut-protipukhlinnu-aktivnist-v-ryadu-pokhidnikh-1-benzil-3-khloro-4-anilino-25-digidro-1n-25-piroldionu.html" target="_blank" rel="follow" title="База патентів України">Структури активних сполук, що мають протипухлинну активність, в ряду похідних 1-бензил-3-хлоро-4-аніліно-2,5-дигідро-1н-2,5-піролдіону</a>