Спосіб одержання імідазолових сполук
Номер патенту: 74871
Опубліковано: 15.02.2006
Автори: Броекс Руді Лоран Марія, Філлерс Вальтер Фердінанд Марія, Леюрс Стефан Марсель Герман
Формула / Реферат
1. Спосіб одержання 4-(3-хлорофеніл)-6-[(4-хлорофеніл)гідрокси(1-метил-1Н-імідазол-5-іл)метил]-1-метил-2(1Н)-хінолінону (ІІІ) та його фармацевтично прийнятних солей:
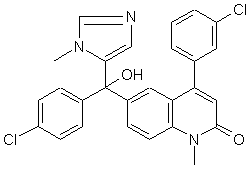 , (ІІІ)
, (ІІІ)
який включає реакцію 6-(4-хлоробензоїл)-4-(3-хлорофеніл)-1-метил-2(1Н)-хінолінону (II):
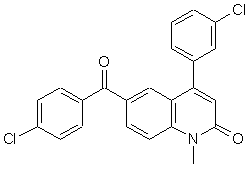 (ІІ)
(ІІ)
зі сполукою С6-8алкіллітію, 1-метилімідазолом та три(С4-6алкіл)силілгалідом.
2. Спосіб за п. 1, який відрізняється тим, що сполукою С6-8алкіллітію є сполука гексиллітію.
3. Спосіб за п. 2, який відрізняється тим, що сполукою гексиллітію є n-гексиллітій.
4. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що три(С4-6алкіл)силілгалід є трибутилсилілгалідом.
5. Спосіб за п. 4, який відрізняється тим, що трибутилсилілгалідом є триізобутилсилілгалідом.
6. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що три(С4-6алкіл)силілгалідом є три(С4-6алкіл)силілхлорид.
7. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що реакцію проводять при температурі принаймні -40°С.
8. Спосіб за п. 7, який відрізняється тим, що реакцію проводять при температурі принаймні -20°С.
9. Спосіб за п. 8, який відрізняється тим, що реакцію проводять при температурі від -5 до +5°С.
10. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що одержану сполуку (III) використовують як проміжну сполуку для одержання (R)-(+)-6-[аміно(4-хлорофеніл)(1-метил-1Н-імідазол-5-іл)метил]-4-(3-хлорофеніл)-1-метил-2(1Н)-хінолінону.
Текст
1. Спосіб одержання 4-(3-хлорофеніл)-6-[(4хлорофеніл)гідрокси(1-метил-1Н-імідазол-5іл)метил]-1-метил-2(1Н)-хінолінону (ІІІ) та його фармацевтично прийнятних солей: 2 74871 1 3 74871 4 ідентифікована у ссавців, птахів, комах, молюсків, рослин, грибів та дріжджів. Сімейство гал онкогенів, що відносяться до ссавців, складається з трьох головних членів ("ізоформів"): Н-ras, K-ras та N-ras онкогенів. Ці ras онкогени кодують високо ras зв'язані білки ,загалом відомі як р21 . Після приєднання до плазматичних мембран, мутант або онкогенна форма р21ras забезпечує сигнал для Як описано у Прикладі В1 вищенаведеного патрансформації та неконтрольованого зростання тентного опису, 1-метил імідазол у тетрагідрофузлоякісних пухлинних клітин. Для досягнення цього рані перемішують з розчином n-бутиллітію у гексапотенціалу, що трансформує, попередник р21ras новому розчиннику до якого доданий онкогенного білку повинен піддатися ензиматично хлоротриетилсилан (триетилсиліл хлорид), з накаталізованому фарнезілуванню цистеїнового заступним додатковим додаванням n-бутиллітію у лишку розміщеного на карбокси-кінцевому тетрагексані, отриману суміш охолоджували до -78°С до пептиді. Таким чином, інгібітори ензимів, що катадодавання розчину сполуки (ll) у тетрагідрофурані. лізують цю модифікацію, тобто фарнезіл Надалі реакційну суміш доводять до кімнатної тетрансферазу, запобігають мембранному приєдмператури, та потім гідролізують, екстрагують ras нанню р21 та блокують аберантне зростання етил ацетатом та органічний шар підготовлюють ras-трансформованих пухлин. Таким чином, загадля отримання бажаного продукту, який отримульноприйнятим є те, що інгібітори фарнезіл транють при 52% виході сполуки (Е). Остання сполука сферази можуть бути дуже корисними як протираможе потім бути перетворена у R115777 як описакові речовини для пухлин у яких гад сприяє но [у міжнародній публікації WO 97/21701]. трансформації. Для того, щоб забезпечити економічну вигідну [У міжнародних публікаціях WO 97/16443, WO пропозицію R115777 з метою розвитку та продажу, 97/2ί701, WO 98/40383 та WO 98/49157], описано необхідний ефективний штучний спосіб одержання похідні 2-хінолону, які виявляють інгібувальну акR115777. Проте, спосіб, описаний у вищезазначетивність до фарнезіл трансферази. [Міжнародна ній [міжнародній публікації WO 97/21701] для пепублікація WO 00/39082] описує клас нових 1,2ретворення сполуки (ll) у сполуку (lll). має деяку анельованих хінолінових сполук, які несуть азотокількість недоліків. Наприклад, спосіб призводить або вуглецево - зв'язаний імідазол, які демонструдо небажаного утворення відповідної сполуки де ють інгібувальну активність до фарнезіл протеїн імідазольне кільце приєднане до залишку молекутрансферази та гераніл трансферази. Інші хінололи у 2-положенні кільця замість бажаного 5нові сполуки, які мають інгібувальну активність до положення у R115777. Для того, щоб отримати фарнезіл трансферази описані [у міжнародних економічно вигідне одержання бажаного 5-ізомеру, публікаціях WO 00/12498,WO 00/12499 та WO важливо зменшити утворення небажаного 200/47574]. У окремої сполуки, яка описана у вищеізомеру, та при комерційних об'ємах, навіть таке зазначеній [міжнародній публікації WO 97/21701], а зменшення за допомогою однієї або двох проценсаме (R)-(+)-6-[аміно(4-хлорофеніл)(1-метил-1Нтних одиниць є дуже бажаним. Також при цьому імідазол-5-іл)метил]-4-(3-хлорофеніл)-1-метиліснує значне утворення інших домішок у одержа2(1Н)-хінолінону. було виявлено дуже сильну акному продукті, наприклад, відповідної бістивність проти пухлинних захворювань та, в даний імідазольної сполуки. Використання n-бутиллітію є час, є об'єктом клінічних досліджень для визнатакож небажаним у комерційному способі у з погчення об'єму терапевтичного ефекту проти різноляду його пірофорного походження та утворення манітних ракових пухлин. Абсолютна стереохімічбутану, пального газу, як побічного продукту. Зрена конфігурація сполуки не була визначена у штою, виконання способу при температурі такій експериментах, які описані у вищезгаданому описі низькій як -78°С є неприйнятним та дорогим у кодо патентної заявки, але сполука ототожнюється мерційних масштабах з погляду спеціального обза допомогою префікса "(В)" для визначення того, ладнання необхідного для виконання великомасщо вона була другою сполукою виділеною за доштабного способу при такій низькій температурі. помогою колонкової хроматографії. У отриманої Таким чином існує необхідність поліпшення вищетаким чином сполуки було виявлено (R)-(+)згаданої стадії реакції завдяки чому вона може конфігурацію. Ця сполука, посилання на яку надалі бути проведена ефективним та економічно вигідбуде наведено за допомогою номеру її довідкового ним способом у комерційному масштабі. коду R115777, має наступну формулу (І): Об'єктом даного винаходу є забезпечення нового та поліпшеного способу одержання сполуки (lll) з сполуки (ll) при покрашеному виході останньої сполуки при мінімізації утворення небажаних (I) ізомерів та при умовах, які б забезпечували економічні переваги для експлуатації у комерційному масштабі. Одержання у R115777 описано [у міжнародній Ми знайшли, що подібні покращення виходу публікації WO 97/21701] за допомогою штучного продукту, домішкового профілю та комерційної шляху, який включає ключову стадію введення 1придатності процесу можуть бути досягнуті за дометил імідазолільної групи у відповідну оксо спопомогою використання n-гексиллітію замість nлуку як показано нижче: бутиллітію та використання триізобутилсиліл хлориду замість триетилсиліл хлориду, з дуже корис 5 74871 6 ними результатами отриманими за допомогою нтрування реакційної суміші, до залишку та осаду використання температури принаймні -40°С. результатів продукту, додають прийнятний розВідповідно до визначеної ознаки даного виначинник, переважно ізопропілацетат. Для утворення ходу ми забезпечуємо спосіб отримання сполуки солі додають газ соляної кислоти, або розчин со(lll), тобто 4-(3-хлорофеніл)-6-[(4ляної кислоти у переважно 2-пропанолі, безпосехлорофеніл)гідрокси(1-метил-1Н-імідазол-5редньо до реакційної суміші у тетрагідрофурані, іл)метил]-1-метил-2(1Н)-хінолінону, та його фарщо приводить до осадження солі. Альтернативно, мацевтично прийнятних солей: соляну кислоту додають до розчину реакційного залишку у прийнятному розчиннику, переважно ацетоні, що приводить до осадження солі. Вихідна сполука формули (llІ) може бути пізніше перетво(III) рена у R115777 наприклад як описано [у міжнародній публікації WO 97/21701], або більш конкретно як описано нижче. Таким чином, наприклад, сполука формули (III) який включає реакцію сполуки формули (ll), тобто може бути хлорована для утворення наступної 6-(4-хлоробензоіл)-4-(3-хлорофеніл)-1-метилсполуки формули (IV), тобто 4-(3-хлорофеніл)-62(1Н)-хіноліноном: [хлоро-(4-хлорофеніл)(1-метил-1Н-імідазол-5іл)метил]-1-метил-2(1Н)-хінолінону: (II) (IV) з сполукою С6-8алкіллітію, 1-метилімідазолу та три(С4-6алкіл)силіл галід. Сполука С6-8алкіллітію бажано є сполукою гексиллітієм особливо n-гексиллітієм. Три(С46алкіл)силіл галід є бажано трибутилсиліл галідом особливо три-ізо-бутилсиліл галідом. Силіл галід є бажанно силіл хлоридом. Вищенаведену реакцію загалом виконують при температурі принаймні -40°С, бажано при температурі принаймні -20°С, та переважно від -5 до +3°С, найкраще приблизно 0°С, вища температура забезпечує підвищене відношення С5-/С2-ізомер, тобто співвідношення сполуки у якій імідазолільна група приєднана до залишку молекули у С5положенні та відповідна сполука приєднана у С2положенні. Ця вибірковість при такій відносно високій температурі є видатною з погляду пропозиції у літературі того, що група силілу є непридатною як блокувальна група, завдяки переміщенню з 2до 5- положення 2-(триалкілсиліл)-заміщених 5літіо-1-метилімідазолів [G.Shapiro та Μ.Marzi, Tetrahedron Letters, Vol.34, No.21, pp.34013404,1993: G. Shapiro and B.Gomez-Lor, J.Organic Chemistry, Vol.59, pp.5524-5526.1994]. Реакцію прийнятно виконують у ефірному органічному розчиннику, наприклад діетиловому ефірі, терт-бутил метиловому ефірі або більш бажано тетрагідрофурані. Більш детально, реакція може бути прийнятно проведена за допомогою початкового приготування розчину 1-метилімідазолу у розчиннику такому як тетрагідрофуран, до якого додають порцію гексиллітію у розчиннику такому як n-гексан. Потім додають силіл галід до отриманої реакційної суміші, та також додають додаткову порцію гексиллітію у розчиннику такому як n-гексан. Потім додають сполука формули (II) у розчиннику такому як тетрагідрофуран до реакційної суміші, витримують температуру між -5°С та 0°С. Вихідний продукт формули (llІ) може бути легко виділений за допомогою кристалізації як основа, або за допомогою утворення солі. Після конце Вищезазначена реакція хлорування може бути проведена, наприклад, за допомогою обробки сполуки формули (III) тіоніл хлоридом або трихлоридом фосфору, у інертному розчиннику, наприклад толуолі, N,N-диметилацетаміді або, більш бажано, N,N-диметилімідазолідиноні, наприклад при температурі від 0°С температури флегми реакційної суміші, бажано при кімнатній температурі. Хлоро сполука формули (IV) може потім бути одразу легко оброблена без необхідності виділення сполуки, за допомогою амінувального агента для утворення наступної аміно сполуки формули (V), тобто 6-[аміно(4-хлорофеніл)(1-метил-1Η-імідазол5-іл)метил]-4-(3-хлорофеніл)-1-метил-2(1H)хінолінону: (V) Реакція амінування може бути легко проведена за допомогою обробки сполуки формули (IV) газоподібним аміаком або розчином аміаку у прийнятному розчиннику, переважно метанолі, реакцію зазвичай проводять у інертному розчиннику наприклад толуолі, або за допомогою додавання аміаку до розчину сполуки (IV) у Ν,Νдиметилацетаміді або бажано Ν,Νдиметилімідазолідиноні. Реакцію проводять, наприклад, при температурі від 0° до 40°С, переважно при кімнатній температурі. Якщо розчинником є Ν,N-диметилімідазолідинон, отриману сполуку виділяють шляхом додавання води, що приводить до осадження сполуки (V) яка може потім бути відфільтрована, промита водою та висушена. Сполуку формули (V) отримують у нерозчиненій формі та вона може бути розкладена прийнятним способом у її складові енантіомери, наприклад, за 7 74871 8 допомогою обробки хіральною кислотою для утвопроаналізували за допомогою рідинної хроматогрення відповідних діастереомерних солей, які порафії високого тиску використовуючи наступні тім виділяють та сіль, яка має бажану Rумови: конфігурації, перетворюють у відповідну вихідну Колонка: сполуку R115777. Таким чином, наприклад, сполуХайперсил C18-BD 3мкм, ка може бути введена у реакцію з L-(-)100мм 4мм (і.d.) дибензоілом винної кислоти (ДБВК) для утворення Рухлива фаза: діастереомерної виннокислої солі, яку оброблюРозчинник А: 0,5% NH4OAc ють основою, переважно водним гидроксидом Розчинник В: CH3CN амонію, для утворення неочищеної (R)-(+)R115777 Градієнт: яку потім очищають за допомогою рекристалізація з етанолу. Вищезазначена проміжна сполука винTime %А %B нокислої солі, тобто R-(-)-6-[аміно(40 100 0 хлорофеніл)(1-метил-1Н-імідазол-5-іл)метил]-4-(315 0 100 хлорофеніл)-1-метил-2(1Н)-хінолінон[R-(R*,R*)]2,318 0 100 бic (бензоілокси) бутандіоат (2:3), є новою сполу19 100 0 кою та представляє собою додаткову ознаку вина23 100 0 ходу. Отримана сполука (R)-(+)R115777 може бути використана для терапевтичного лікування ракоІндикатор: УФ 254нм вих пухлин як описано [у міжнародній публікації Розчинник: ДМФ WO 97/21701]. Вихідна сполука формули (II), яка У продукті було знайдено відношення С5:С2 застосовується у способі за даним винаходом, рівне 99,8:0,2, у відмінності від випадку викорисможе бути одержана як описано [у міжнародній тання n-бутиллітію замість n-гексиллітію, триетилпублікації WO 97/ 21701]. силіл хлорид замість три-ізобутилсиліл хлориду та Наступні приклади ілюструють даний винахід. проведення процесу при -70°С, тобто загалом у Одержання сполуки (lll): відповідності з процедурою відомою з рівня техні110мл сухого тетрагідрофурану додали до ки, яку розглядали вище, вихідний продукт мав 7,6мл 1-метилімідазолу (0,0946молля) та одержавідношення С5:С2 - 95:5, значну різницю у комерний розчин охолодили до -15°С. Додали 37,8мл nційних строках. гексиллітію 2,5Μ у n-гексані (0,0946молля), під час Одержання сполуки (IV) додавання температуру витримували між 5°С та Реакційна судина ємністю 1 літр була запов0°С. Після додавання, реакційну суміш перемішунена 105,4г 4-(3-хлорофеніл)-6-[(4вали протягом 15 хвилин, з одночасним охолохлорофеніл)гідрокси(1-метил-1Н-імідазол-5дженням до -12°С. Додали 26,2мл три-ізоіл)метил]-1-метил-2(1Н)-хіноліноновою сіллю собутилсиліл хлорид (0,0964молля), підчас додаванляної кислоти (сполука (lll) та 400мл Ν,Νня температуру витримували між -5° та 0°С. Після диметилімідазолідинон додавали при температурі додавання, реакційну суміш перемішували протя22°С. Суміш енергійно перемішували протягом 15 гом 15 хвилин, з одночасним охолодженням до хвилин при 22°С до однорідності. До реакційної 13°С. Додали 37,2мл n-гексиллітію 2,5Μ у n-гексані суміші додавали 32,1мл тіоніл хлориду протягом (0.0930молля), підчас додавання температуру вибільше ніж 10 хвилин, реакційну температуру підтримували між -5°С та 0°С (мало місце деяке вивищили з 22°С до 40°С. Після додавання тіоніл падання осаду). Після додавання, реакційну суміш хлориду, реакційну суміш охолодили з 40°С до перемішували протягом 15 хвилин, з одночасним 22°С та перемішували протягом трьох годин при охолодженням до -14°С. 128мл сухого тетрагідроостанній температурі для забезпечення розчину 4фурану додали до 26,22г 6-(4-хлоробензоіл)-4-(3(3-хлорофеніл)-6-[хлоро-(4-хлорофеніл)(1-метилхлорофеніл)-1-метил-2(1Н)-хінолінон (сполука (ll)) 1Н-імідазол-5-іл)метил]-1-метил-2(1Н)-хінолінону (0,0642молля) та перемішували до розкладання. (сполука (IV)). Цей розчин додали до реакційної суміші, темпераОдержання нерозчиненої сполуки (l) туру підчас додавання витримували між -5°С та 429мламіаку у метанолі 7N охолоджували до 0°С. Після додавання, реакційну суміш перемішу5°С у 3 літровій реакційній судині та розчин сполували протягом 15 хвилин між -5°С та 0°С. Додали ки (IV), одержаний отриманий у попередній стадій, 128мл води до реакційної суміші, з наступним дододавали, з одночасним перемішуванням, протядаванням 10,6мл оцтової кислоти. Суміш потім гом 10 хвилин, з екзотермічною реакцією, темпенагрівали до 40°С та перемішували протягом 2 ратуру підняли з 5°С до 37°С. Після закінчення годин. Шари розділили та органічний шар промили додавання, реакційну суміш охолодили до 22°С та 32мл води. Додали 64мл води та 7,8мл водного перемішували протягом 20 годин. Потім додавали NaOH 50% до органічного шару, який перемішува1000мл води протягом 20 хвилин, додавання було ли протягом 1 години при температурі зовнішнього ледь екзотермічною таким чином реакційна суміш середовища. Шари розділили та органічний шар була охолоджена для витримування температури концентрували під зменшеним тиском, що дало нижче 30°С. Суміш потім перемішували протягом 51,08г коричневого масла (46,6мас.% 4-(322 годин при 22°С, вихідний осад відфільтрували хлорофеніл)-6-[(4-хлорофеніл)гідрокси(1-метилта осад три рази промили 100мл води для забез1Н-імідазол-5-іл)метил]-1-метил-2(1Н)-хінолінону печення виходу 70-75% 6-[аміно(4-хлорофеніл)-](сполука llІ); 75,6% вихід). метил-1Η-імідазол-5-ілметил]-4-(3-хлорофеніл)-1Продукт може бути виділений за допомогою метил-2(1Н)-хінолінону. процедури згаданої вище. Отриманий продукт 9 74871 10 Розділення сполуки (l) протягом 16 годин при 20°С. Продукт відфільтруa) Реакційна судина ємністю 3 літра була завали, двічі промили 8мл води та висушували при повнена 146,8г 6-[аміно(4-хлорофеніл)(1-метил50°С у вакуумі, що дало 16,87г (R)-(+)-6-[аміно(41H-імідазол-5-іл)метил]-4-(3-хлорофеніл)-1-метилхлорофеніл)(1-метил-1Н-імідазол-5-іл)метил]-4-(32(1Н)-хіноліноном та 301,1г L-(-)-дибензоіл-винної хлорофеніл)-1-метил-2(1Н)-хінолінон(сполука (І)). кислоти моногідратом, додали 1200мл ацетону та Очищення сполуки (І) реакційну суміш енергійно перемішували протягом 265мл етанолу додали до 19,9г сполуки (І), 10 хвилин при 22°С для утворення розчину, який отриманої як описано у попередній стадії, та суміш був зацькований 100мг тартратної солі заключного нагрівали протягом перемішування до температупродукту (отриманого з попередніх експериментів, ри флегми (78°С) та потім перемішували при темщо відсівають) та потім підданий перемішуванню пературі флегми протягом 15 хвилин для охоло22 годин при температурі 22°С. Отриманий осад дження розчину до температури 75°С. Потім відфільтрували та осад промили двічі 75мл ацетододали 1,0г активованого вугілля (Norit A Supra) до ну та продукт висушили при 50°С у вакуумі, що суміші, яку перемішували при температурі флегми дало 114,7г R-(-)-6-[аміно(4-хлорофеніл)(1-метилпротягом 1 години, відфільтрували доки вона була 1Н-імідазол-5-іл)метил]-4-(3-хлорофеніл)-1-метилтеплою та фільтр потім промили 20мл теплого 2(1Н)-хінолінон [R(R*,R*)]-2,3етанолу. Фільтрат та промивний розчинник поєдбіс(бензоілокси)бутандіоату (2:3). нали (продукт самовільно кристалізувався при b) 41.08г продукту стадії а) та 80мл етанолу 48°С), та суміш нагріли температури флегми та перемішували протягом 15 хвилин при 22°С. концентрували шляхом виділення 203мл етанолу. 12,0мл концентрованого водного гідроксиду амоОтриману суспензію охолодили до 22°С. перемінію додавали протягом 2 хвилин, та реакційну сушували протягом 18 годин при 22°С, охолодили до міш перемішували протягом 1 години при 25°С. 2°С та перемішували протягом більше 5 годин при 160мл води додавали протягом 10 хвилин при 2°С. Осад відфільтрували та промили 4мл етанолу 25°С та суміш нагрівали з оберненим холодильнита продукт висушили при 50°С у вакуумі, що дало ком та перемішували при нагріванні з оберненим 17,25г очищеної сполуки (І), яка відповідає інфрахолодильником протягом 1 години. Реакційну сучервоному спектру еталонного матеріалу. міш потім охолодили до 20°С та перемішували Комп’ютерна верстка Т. Чепелева Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA process for the preparation of imidazole compounds
Назва патенту російськоюСпособ получения имидазоловых соединений
МПК / Мітки
МПК: C07D 401/06, A61K 31/4709, A61P 35/00
Мітки: спосіб, одержання, сполук, імідазолових
Код посилання
<a href="https://ua.patents.su/5-74871-sposib-oderzhannya-imidazolovikh-spoluk.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання імідазолових сполук</a>
Попередній патент: Спосіб одержання карбапенему
Наступний патент: Конструкційна ізотропна сталь, спосіб одержання листа цієї сталі й одержуваний листовий прокат
Випадковий патент: Установка для адсорбційного осушування газу









