Спосіб синтезу біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламіну
Формула / Реферат
Спосіб синтезу біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламіну загальної формули C8H13N,
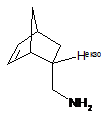 ,
,
який включає відновлення біцикло[2.2.1]гепт-5-ен-ендо-2-карбонітрилу, який відрізняється тим, що використовують як відновник 1.1 мольний надлишок гідриду алюмінію (АlН3, алан), який отримують in situ із еквімольних кількостей алюмогідриду літію та триметилсилілхлориду в тетрагідрофурані, реакцію проводять при кип'ятінні реакційної суміші протягом 8-12 годин.
Текст
Реферат: Некзо NH2 , який включає відновлення біцикло[2.2.1]гепт-5-ен-ендо-2-карбонітрилу. Використовують як відновник 1.1 мольний надлишок гідриду алюмінію (АlН3, алан), який отримують in situ із еквімольних кількостей алюмогідриду літію та триметилсилілхлориду в тетрагідрофурані, реакцію проводять при кип'ятінні реакційної суміші протягом 8-12 годин. UA 82477 U Спосіб синтезу біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламіну загальної формули C8H13N, UA 82477 U UA 82477 U 5 10 Корисна модель стосується нового способу синтезу біцикло[2.2.1]гепт-5-ен-eндo-2ілметиламіну - біциклічного аміну, що містить фармакофорний норборненовий фрагмент і використовується в синтезі біологічно-активних речовин. Ендо-2-амінометилнорборнен (Іа, біцикло[2.2.1]гепт-5-ен-2-ілметиламін) відомий раніше [1] і вивчено його численні реакції [2]. Із літературних джерел [3] та наших досліджень відомо, що відновлення стереохімічно чистого ендо-2-ціанонорборнену (II) алюмогідридом літію в киплячому діетиловому ефірі призводить до суміші стереоізомерних амінів (Іа, б), в якій вміст 1 альтернативного продукту в окремих випадках досягає 30 % (дані ЯМР Н). З метою синтезу ендо- і екзо-2-амінометилнорборненів (Іа, б) відновлюють (LiAlH4) також стереохімічно чисті аміди норборнен-2-карбонової кислоти (виходи до 70 %) [4] та оксими норборнен-2карбальдегіду (вихід 43 %) [5] або піддають вакуумній ректифікації суміш продуктів реакції Дільса-Альдера дициклопентадієну з алліламіном [6]. В останньому випадку виділити окремі стереоізомери (Іа, б) особливо важко у зв'язку з тим, що реакція в жорстких умовах (170 °C) проходить не стереоспецифічно 15 LiAlH4 (4.16 моль) Et2O, кип' ятіння, 22год + 78.5 % [1] NH2 NH2 II 20 25 30 35 40 Ia N Iб . Найбільш близьким до об'єкта, що заявляється (прототип), є відомий спосіб синтезу біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламіну (Іа) відновленням нітрилу (II) великим надлишком алюмогідриду літію в середовищі киплячого діетилового ефіру протягом 22 годин [1]. Значним недоліком цього способу синтезу є невисока стереохімічна чистота продукту. Частково проблему синтезу стереохімічно чистого аміну (Іа) можливо вирішити використанням надмірної кількості алюмогідриду літію (мольне співвідношення нітрил (II) - LiAlH4=1:4,16), проте навіть в цьому випадку домішка стереоізомерного аміну (16) досягає 6-11 % [1, 3]. В основу корисної моделі поставлена задача розробки умов синтезу стереохімічно однорідного eндo-2-амінометилнорборнену (Іа) із вмістом основного компоненту не менш 95 %. Така чистота є звичайною умовою, що пред'являється до комерційних синтетичних будівельнихблоків (building block). Запропонований спосіб розширяє можливості синтетичних підходів до аналогічних каркасних амінів. Поставлена задача вирішується тим, що розробленим способом синтезу аміну (Іа) з використанням як відновника нітрилу (II) 1.1 мольного надлишку гідриду алюмінію (АlН 3, алан), який отримують in situ із еквімольних кількостей алюмогідриду літію та триметилсилілхлориду в тетрагідрофурані, реакцію проводять при кип'ятінні реакційної суміші протягом 8-12 годин . 1 Структуру синтезованої сполуки (Іа) підтверджено даними спектру ЯМР Н (CDCl3). Найбільш суттєві розбіжності в спектральній поведінці ізомерних амінів (Іа, б) торкаються положення в спектрі (6,11 та 5,91 м.ч. для ендо-ізомеру Іа, 6,07 та 6,04 м.ч. для екзо-ізомеру 16) 5,6 та ступеню нееквівалентності сигналів протонів олефінового фрагменту Н (А8 0,20 м.ч. для eндo-ізомеру Іа, 0,03 м.ч. для екзо-ізомеру 16). Вказані критерії показані на приведеному рисунку і дозволяють чітко контролювати стереохімічну чистоту продукту реакції методом 1 ядерного магнітного резонансу на ядрах Н. Суть корисної моделі пояснює креслення. 1 UA 82477 U 5 10 15 20 25 30 Приклад синтезу. Біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламін (Іа). До 4,18 г (0,11 моль) алюмогідриду літію в 250 мл абсолютного тетрагідрофурану при 0 °C (льодяна баня) та перемішуванні добавляли по краплях 11,95 г (13,99 мл, 0,11 моль) триметилсилілхлориду в токі сухого аргону. Після перемішування реакційної суміші впродовж 30 хвилин повільно добавляли по краплях розчин 11,90 г (0.10 моль) ендо-2-ціанонорборнену (II) в 50 мл тетрагідрофурану. Отриманій суміші дали змогу нагрітися до 25 °C і продовжили реакцію при кип'ятінні та перемішуванні протягом 12 годин (контроль методом тонкошарової хроматографії). Після охолодження надлишок відновника повільно розкладали додаванням води (4,2 мл), 20 %-ного розчину гідроксиду натрію (4,2 мл) та знову води (~10 мл). Осад гідроксидів відфільтровували та ретельно промивали на фільтрі хлористим метиленом (200 мл). Фільтрат висушували сульфатом натрію, концентрували на роторному випарювані та перегоняли маслоподібний залишок в вакуумі водоструменевого насоса. Вихід ендо-аміну (Іа) 8,38 г (68 %), т.кип. 70-72 °C (12 мм рт. ст.), стереохімічна чистота 97,4 % (дані ГРХ). Аналогічний експеримент з синтезу аміну (Іа), проведений при кип'ятінні та перемішуванні реакційної суміші протягом 8 годин, призводить до продукту (Іа) з виходом 60 % та 1 стереохімічною чистотою 96,5 % (дані ГРХ). Дані 14 спектрів та спектрів ЯМР] Н продукту відповідають літературним [1,3]. 1 Спектри ЯМР Н реєстрували на радіоспектрометрі Bruker Avance DRX 500 (робоча частота генератора 500 МГц) для розчинів сполук в дейтерохлороформі з використанням ТМС як внутрішнього стандарту. Проходження реакцій та чистоту синтезованих сполук контролювали методом ТШХ на пластинах Silufol UV-254 в суміші гексан - етилацетат, 3:1, проявник - пари йоду. До переваг запропонованого способу синтезу біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламіну (Іа) можна віднести наступні: зменшення мольного надлишку цінного відновника (алюмогідриду літію, LiАlН4); зменшення тривалості реакції на 10 годин у порівнянні з прототипом завдяки використанню більш висококиплячого розчинника (тетрагідрофуран); використання більш дешевого тетрагідрофурану як альтернативу діетиловому ефіру, обіг якого в Україні обмежено у зв'язку із внесенням його до списку прекурсорів; триметилсилілхлорид (Mе3SіСl), що використовується в запропонованому способі, є багатотонажним доступним промисловим продуктом, який знайшов використання в хімії силіконових високомолекулярних сполук; висока стереохімічна чистота продукту (97.4 %) через високу стереоселективність процесу відновлення. 35 40 45 50 Джерела інформації: 1. Uber den sterischen Verlauf der Addition von Acrylnitril an cyclische Diene / K. Alder, K. Heimbach, R. Reubke // Chem. Ber. -- 1958. - Bd. 91, № 7. - S. 1516-1524. 8 2. Пат. 69138 Україна, МПК A01N 33/00, C07C 211/03. Похідні біциклічних каркасних амінів як регулятори росту рослин / Кас'ян Л.І., Пальчиков В.О., Карабанов Ю.В., Кас'ян А.О. - Заявл. 29.08.2011; Опубл. 25.04.2012; Бюл. № 8.-4 с 3. Equilibrium and Isomerization in Bicyclic Nitriles / P. Wilder, D. B. Knight // J. Org. Chem.-1965. -Vol. 30, № 9. - P. 3078-3081. 4. General Synthetic Route to Cell-Permeable Block Copolymers via ROMP / Kolonko E.M., Pontrello J.K., Mangold S.L., Kiessling L.L. // J. Am. Chem. Soc.-2009. - Vol. 131, № 21. - P. 73277333. 5. Пат. 3072720 США, МПК A61K 31/64, C07C 311/54. Novel n-arylsulfonyl-n'-(2, 5endomethylene-l, 2,5,6-tetrahydrobenzyl)ureas / Wright J.B. - Заявл. 07.04.1960; Опубл. 08.01.1963 //Chem. Abstr.-1963. -Vol. 58, 13843. 6. High-load, oligomeric monoamine hydrochloride: facile generation via ROM polymerization and application as an electrophile scavenger / Stoianova D.S., Yao L., Rolfe A. et al. // Tetrahedron Lett.2008. - Vol. 49, № 29-30. - P. 4553-4555. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 55 Спосіб синтезу біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламіну загальної формули C8H13N, 2 UA 82477 U Некзо NH2 5 , який включає відновлення біцикло[2.2.1]гепт-5-ен-ендо-2-карбонітрилу, який відрізняється тим, що використовують як відновник 1.1 мольний надлишок гідриду алюмінію (АlН3, алан), який отримують in situ із еквімольних кількостей алюмогідриду літію та триметилсилілхлориду в тетрагідрофурані, реакцію проводять при кип'ятінні реакційної суміші протягом 8-12 годин. Комп’ютерна верстка М. Мацело Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 3
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess of synthesis of bicyclo[2.2.1]hept-5-ene-endo-2-ylmethylamine
Автори англійськоюPalchikov Vitalii Oleksandrovych
Назва патенту російськоюСпособ синтеза бицикло[2.2.1]гепт-5-ен-эндо-2-илметиламина
Автори російськоюПальчиков Виталий Александрович
МПК / Мітки
МПК: C07C 209/48
Мітки: біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламіну, спосіб, синтезу
Код посилання
<a href="https://ua.patents.su/5-82477-sposib-sintezu-biciklo221gept-5-en-endo-2-ilmetilaminu.html" target="_blank" rel="follow" title="База патентів України">Спосіб синтезу біцикло[2.2.1]гепт-5-ен-ендо-2-ілметиламіну</a>
Попередній патент: Крокети картопляні “верде” з соєвим борошном та начинкою з сочевиці і спіруліни
Наступний патент: Спосіб сатурації цукрових розчинів
Випадковий патент: Очисник головок коренеплодів









