Спосіб одержання енантіомерно чистого міртазапіну
Номер патенту: 83666
Опубліковано: 11.08.2008
Автори: Вєрінґа Йоганнес Губертус, Кемперман Ґерардус Йоганнес, ван де Вен Адріанус Антоніус Мартінус
Формула / Реферат
1. Спосіб одержання міртазапіну, що має енантіомерний надлишок близько 90 %, що включає етап замикання циклу сполуки формули (ІІ)
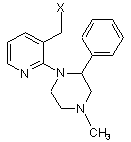 , (ІІ)
, (ІІ)
де X - відщеплювана група, при обробці її кислотою, який відрізняється тим, що міртазапін з енантіомерним надлишком утворюють замиканням циклу R- або S-енантіомеру сполуки формули (II), шляхом обробки кислотою або комбінацією кислота/розчинник, вибраними з переліку, який включає:
а) поліфосфатну кислоту,
б) пентоксид фосфору в присутності розчинника N-метилпіролідинону або диметилформаміду (ДМФ).
2. Спосіб за п. 1, який відрізняється тим, що міртазапін з енантіомерним надлишком утворюють шляхом обробки енантіомера сполуки формули (II) поліфосфатною кислотою в присутності розчинника.
3. Спосіб за п. 2, який відрізняється тим, що розчинником є N-метилпіролідинон або ДМФ.
4. Спосіб за п. 2, який відрізняється тим, що масове співвідношення між поліфосфатною кислотою та сполукою формули II є меншим 5:1.
5. Спосіб за п. 2, який відрізняється тим, що масове співвідношення між поліфосфатною кислотою та сполукою формули II є меншим 2,5:1.
Текст
1. Спосіб одержання міртазапіну, що має енантіомерний надлишок близько 90 %, що включає етап замикання циклу сполуки формули (ІІ) 2 (13) 1 N (11) Сполука є хіральною рацемічною сумішшю, що знаходить широке застосування як медикамент для лікування депресії. Інші медичні застосування міртазапін розкрито також, наприклад, [WO 99/25356 та WO 01/58453] розкривають його застосування у лікуванні розладів сну та апное. Дослідження біологічної дії енантіомерів міртазапіну [наприклад, O'Connor та Leonard, Neuropharmacology, 1986, vol. 25, pp. 267-270; Kooyman et al., 1994, vol. 33, pp. 501-507; De Boer et a/., Neuropharmacology, 1988, vol. 27, pp. 399408; Gower et al., 1988, vol. 291, pp 185-201] сприяють застосуванню сполуки у її чистій енантіомерній формі, що відкриває необхідність ефективного отримання великої кількості енантіомерно чистого UA Заявлений винахід стосується способу отримання енантіомерно чистого міртазапіну, що має етап замикання циклу кислотою. Міртазапін, 1,2,3,4,10,14b-гексагідро-2-метилпіразино[2,1-а]піридо[2,3-с][2]бензазепін є тетрациклічною сполукою, що має формулу І: 83666 , (ІІ) (19) CH3 3 83666 міртазапіну. Заявлений винахід стосується розвитку такого способу отримання. Різні способи відомі у рівні техніки отримання міртазапіну. [US 4062848] описує варіації чотирьох-етапної схеми синтезу, котрою синтез міртазапіну можна досягти, починаючи з 2-заміщеного нікотинітрилу. Наступні модифікації різних етапів цього шляху описано у [WO 00/62782, WO 01/23345 та US 6,376,668]. Отримання енантіомерно чистого міртазапіну описано y [US 4062848, WO 00/62782 та Selditz et al., 1808 (J. Chromatography, 1998, vol 803, pp 169177)]. Способом, розкритим у US 4062848, енантіомерно чистий міртазапін отримують фракційною кристалізацією діас-тереомерних солей, утворених реакцією рацемічного міртазапіну з енантіомерно чистою дибензоїлвинною кислотою в етанолі, а потім регенерацією вільної основи обробкою водним аміаком. Інші способи утворення чистого міртазапіну перекристалізацією сирого міртазапіну розкриті у [WO 00/62782. Selditz et al.] описують хроматографічний спосіб розділення енантіомери. У цих способах розділення відбувається на кінці шляху синтезу, призводячи до створення рацемічної суміші міртазапіну. Це відбувається тому, що загальний вихід кожної отриманої енантіомерно чистої сполуки є відносно низьким та не може ніколи бути більше 50%. Краще було б мати більш економічній спосіб, котрим енантіомерно чистий мі-ртазапін можна було б отримувати з загальним поліпшеним виходом. Способом, описаним у US 4062848 міртазапін можна отримувати замиканням циклу сполуки формули(И),. де X може бути відщеплюваною групою, як-то гідроксил, естерифікований або ете-рифікований гідроксил або галоген, застосуванням різних реагентів замикання циклу. Приклади таких реагентів охоплюють кислоти як-то сульфатна кислота, концентрована гідро-хлоридна кислота, пікринова кислота, трифлуороцтова кислота, фосфатна кислота, полі-фосфатна кислота (ПФК), фосфор оксихлорид, фосфор триоксид, фосфор пентоксид та кислоти Льюїса як-то алюміній хлорид, ферум(ІІІ) хлорид, цинк хлорид, станум хлорид, титан хлорид, бор трифлуорид, стибій пентахлорид та цирконій тетрахлорид. У [US 4062848] отримання міртазапіну досягнуто замиканням циклу застосуванням концентрованої сульфатної кислоти. У [WO 00/62782] показано, що концентрована сульфатна кислота є найкращою. У [US 4062848] зауважено, що чисті енантіомери міртазапіну можна отримувати синтетично застосуванням енантіомерно чистого вихідного матеріалу для останнього етапу замикання циклу. Однак, спосіб, описаний 4 у [WO 00/62782] з концентрованою сульфатною кислотою не достатньо зберігає оптичну чистоту. Ймовірно, ці умови реакції дають надлишкову рацемізацію. Зараз несподівано виявлено, що для синтезу енантіомерно чистого міртазапіну замиканням циклу енантіомерно чистої сполуки формули (II) стереохімічну незайманість у вихідному матеріалі можна, однак, зберігати специфічним вибором вищезазначених реагентів замикання циклу. Заявлений винахід тому стосується способу, що полягає у замиканні циклу сполуки формули (II), де X - відщеплювана група, вказаний етап полягає в обробці з утворенням міртазапіну з енантіомерним надлишком замиканням циклу сполуки формули (II) з енантіомерним надлишком придатною кислотою у відсутності розчиннику або придатною комбінацією кислоти та органічного розчиннику. Спирт формули Il переважно застосовують як кристалічну сіль або сольват, як-то оксалат (S) або (R) 1-{3-гідроксиметил-2-піридил)-4-метил-2фенілпіперазин. Як варіант, дикаліт додають до реакційної суміші для попередження утворення грудок. Термін міртазапін застосовують тут у його загальному значенні, звичайно застосованому для позначення хімічної сполуки як основи та, залежно від контексту, її солі та сольвату та доповнено префіксами (R) або (S) та/або (+) або (-) для енантіомерів сполуки. (S) конфігурація викликає позитивне оптичне обертання у звичайних розчинниках. Термін енантіомерний надлишок у сполуці стосується різниці між кількістю кожного з енантіомерів, присутніх у суміші, відносно загальної кількості сполуки у суміші, вираженій у процентах. Наприклад, у 10г суміші 9г міртазапіну (90%), у котрій 4г (R)-міртазапіну та 5г (S)-міртазапіну, енантіомерний надлишок (S)-енантіомеру складає приблизно 11%. Коротше, термін міртазапін або сполука з енантіомерним надлишком стосується суміші міртазапіну або сполуки з енантіомерним надлишком. Винахід може забезпечити енантіомерно чистий міртазапін якщо застосовують ена-нтіомерно чистий вихідний матеріал, а замикання циклу здійснюють обробкою придатною кислотою у відсутності розчиннику або придатної комбінації кислоти та органічного розчиннику. Енантіомерно чиста сполука є сполукою, що містить менше 20% інших енантіомерів, з енантіомерним надлишком 80%. Залежно від конкретних умов способом винаходу можна також отримувати енантіомерно чисту сполуку, що має менше 10% інших енантіомерів або менше 1% інших енантіомерів. Вихід енантіомерно чистого міртазапіну звичайно не менше 50%, але можна також отримувати ви хід не менше 70%. Відщеплювана група є реакційною функціональною групою на молекулі, котра відщеплюється від молекул при утворенні нового зв'язку, яка є звичайно відомою у рівні техніки. Конкретніше, відщеплювана група може бути гідроксильною, її активованою естерною, як-то карбоксилат, сульфонат або фосфонат або галоген. Групи з цією функціональною групою звичайно відомі у рівні 5 83666 техніки і знайдені у звичайних довідниках з органічного синтезу. Придатною кислотою для способу заявленого винаходу є кислота комбінація кислота/розчинник, як-то вищезгадані, або кислота комбінація кислота/розчинник, як-то не згадані вище, але котрі отримують тестом на перетворення як придатні. Тест проводять стосовно замикання циклу з кислотою-кандидатом, та вихідним матеріалом, котрим є сполука II, визначена вище або її сіль або сольват з попередньо визначеною енантіомерною чистотою, та визначають після реакції енантіомерний надлишок утвореного міртазапіну. Кількісний ступінь втрати енантіомерної чистоти можна визначити простим підрахунком та виразити як різницю між енантіомерним надлишком у вихідному матеріалі перед реакцією та енантіомерним надлишком отриманого міртазапіну після реакції. Якщо втрата менше 40%, кислота або комбінація кислота/розчинник є придатними. Більш жорсткий критерій придатності кислоти або комбінації кислота/розчинник можна застосовувати вибором того, що викликає втрату менше 0% - 40%, як-то 35%, 30%, 25%, 20%, 15%, 10%, 5%, 2%, 1 %, 0,5% та 0,3%. вибору кислоти або комбінації кислота/розчинник, придатних для стереоспецифічного замикання, що дає енантіомерно чистий міртазапін. Спосіб полягає у реакції замикання циклу енантіомерно чистої сполуки формули Il або її солі чи сольвату, при значенні X, визначеному ви ще, з будь-якою кислотою-кандидатом або будь-якою комбінацією-кандидатом кислота/розчинник та визначенні втрати енантіомерного надлишку реакцією та ідентифікації кислоти або комбінації кислота/розчинник, які придатні, якщо призводять до втрати менше 40%. Як варіант, жорсткіший критерій, як вищезгаданий, можна застосовувати для більш придатних кислот або комбінацій кислота/розчинник. Придатною кислотою, застосованою у відсутності розчиннику, може бути протонна кислот або похідне протонної кислоти, як-то ангідрид протонної кислоти. Концентрована сульфатна кислота, краща у способі попереднього рівня техніки отримання рацемічного міртазапіну, або алюміній трихлорид є непридатними. Для замикання циклу застосуванням придатної кислоти у відсутності розчиннику, застосування поліфосфатної кислоти або фосфор пентоксиду у фосфа тній кислоті є особливо кращим, рекомендовано застосування поліфосфатної кислоти або фосфор пентоксиду у фосфатній кислоті у кількості малого надлишку стосовно вихідного спирту, визначеного як сполука Il вище. Реакція дасть вищий вихід та краще збереження енантіомерного надлишку, якщо співвідношення (за масою) поліфосфа тної кислоти стосовно спирту (маси основи сполуки II) є менше 10:1 (за масою), або краще 5:1, ще краще, якщо менше 2,5:1. Коли поліфосфатн у кислоту уводять у кількості пентоксиду та поліфосфатної кислоти (можливо у масспіввідношенні пентоксиду стосовно фосфатної кислоти 1:1-1:9) маси фосфор пентоксиду та фосфатної додають, виражаючи як загальну кількість поліфосфатної кислоти. 6 Придатна комбінація кислоти та органічного розчиннику може бути комбінацією протонної кислоти або похідного протонної кислоти, як-то ангідрид протонної кислоти або мінеральної кислоти та полярного координаційного розчиннику, як-то етанол або вищі спирти, ДМФ, ДМА або Nметилпіролідинон. Кращим є застосування комбінації похідного протонної кислоти та Мметилпіролідинону або ДМФ. Поліфосфа тна кислота та N-метилпіролідинон або ДМФ є особливо кращими. Комбінації кислота/розчинник фосфор пентоксид або поліфосфатна кислот чи сульфатна кислота та ксилол; фосфор пентоксид або поліфосфатна кислота та хлорбензол; фосфор пентоксид або поліфосфатна кислота та толуол, та сульфатна кислота і дихлор-метан є не придатними. Коли реакція замикання циклу може відбувається при кімнатній температурі, реакцію можна також полегшува ти додатковим нагріванням. Згідно з наступним аспектом винаходу запропоновано замикання циклу способами заявленого винаходу, охоплюючи додаткове нагрівання. Сполуку формули (II) можна отримувати шляхом синтезу, показаним у схемі І, котра описана у [US 4062848]. Відтак, сполуку (V) можна отримувати реакцією сполуки (IV) з хлорнікотинітрилом (III) в органічному розчиннику, як-то тетрагідрофуран або диметилформамід, у присутності еквіваленту основи, як-то калій флуорид. Сполуку (Vl) можна тоді отримувати гідролізом сполуки (V) застосуванням водної основи, як-то калій гідроксид, у спирті, як-то етанол, звичайно при кипінні під зворотним холодильником. У [WO 00/62782], описано, що молярне співвідношення застосованої основи для здійснення гідролізу нітрилу можна зменшити від 25 молей основи (як розкрито у способі з US 4062848) до приблизно 12 молей основи. Кінцево сполуку (II) можна отримувати відновленням сполуки (Vl) застосуванням знов гідриду металу, як-то літій алюміній гідрид, в органічному розчиннику, як-то тетрагідрофуран. Перетворення спиртової функціональної групи в інші відщеплювані групи, 7 83666 як-то карбоксилатні та сульфонатні естери та у галогени можна легко досягти способами, котрі добре відомі у рівні техніки. Отримання енантіомерно чистої сполуки (II) можна тоді досягти застосуванням способів, добре відомих у рівні техніки. Наприклад, способи асиметричного синтезу, наприклад, синтез з хіральним уведенням, фракційна кристалізація діастереоізомерних солей, утворених реакцією з хіральною кислотою, або відокремлювальною хроматографією на хіральному носії нормальною чи зворотно-фазовою хроматографією. Так способи, наприклад, описані у ['Chirality in industry' edited AN. Collins, G.N. Sheldrake та J. Crosby, 1992; John Wiley] Винахід також охоплює енантіомерно чистий міртазапін, отриманий способом заявленого винаходу, та фармацевтичні композиції його для застосування у терапії. Такі композиції можуть містити терапевтично ефективну кількість енантіомерно чистого міртазапіну у комбінації з фармацевтично прийнятними носіями та ексципієнтами, котрі добре відомі у рівні те хніки. Винахід ілюстровано наступними прикладами: Приклад 1а Отримання (S)-міртазапіну (S)-I-{3-гідроксиметил-2-піридил)-4-метил-2фенілпіперазин (0,23г, 1,03ммоль) розчиняли у Nметилпіролідиноні (10мл), утворений розчин додавали краплями до_поліфос-фатної кислоти (1,46г) у N-метилпіролідоні (5мл) з перемішуванням при 81°С. Реакційну суміш перемішували при 100°C протягом 72 годин. Це далі розбавляли розчином натрій гідроксиду та діетиловим етером. Органічний шар відокремлювали та промивали двічі водою. Магній сульфат додавали, видаляли фільтруванням та фільтрат випарювали. Заголовну сполуку (0,19г, 88%) отримували як маслянистий продукт. Енантіомерний надлишок (е.н.) продуктів був 99,2%. Приклад 1b До суміші поліфосфатної кислоти (41,8г) та Nметилпіролідину (10,5мл) додавали розчин (S)-1(3-Гідроксиметил-2-піридил)-4-метил-2-фенілпіперазину (7,02г, 24,7ммоль) у N-метилпіролідиноні (10мл). Реакційну суміш нагрівали до 130°C протягом 1 години. У реакційну суміш додавали воду (152мл), дикаліт (8,8г), толуол (76мл), та 33% розчин натрій гідроксиду (128мл). Водний шар відокремлювали та екстрагували двічі толуолом (76мл). Поєднані толуольні шари промивали тричі водою (76мл), сушили магній сульфатом та випарювали. Це дало 4,63г (S)-міртазапіну (70%) з е.н. 99%. Приклад 2 Отримання (S)-міртазапіну (S)-1-(3- Гідроксиметил-2-піридил)-4-метил-2фенілпіперазин (0,30г, 1,0587ммоль) розчиняли у 18,75мл диметилформаміду. До розчину додавали 0,75г дикаліту та 1,5г поліфосфатної кислоти. Реакційну суміш перемішували протягом доби при 100°С. Це далі розбавляли натрій гідроксидом та екстрагували діетиловим етером. Органічний шар промивали двічі водою, сушили магній сульфатом, фільтрували та фільтрат випарювали. Заголовну 8 сполуку (0,19г, 88%) отримували як маслянистий продукт. Е.н. продуктів був 99,2%. Приклад 3 Отримання (S)-міртазапіну (S)-1-(3- Гідроксиметил-2-піридил)-4-метил-2фенілпіперазин (0,50г, 1,78ммоль) розчиняли у Nметилпіролідоні (7,5мл) та нагрівали, до 100°C. До цієї додавали суміші дикаліт (0,62г) та фосфор пентоксид (1,26г). Після 86 годин реакція завершувалася. Воду додавали до реакційної суміші, а тоді фільтрували. рН доводили до 14 додаванням 4 H розчину натрій гідроксиду. Водний розчин екстрагували діетиловим етером. Органічний шар сушили магній сульфатом та випарювали. Це дало заголовну сполук у (0,24г, 5,1%) з е.н. 99,7%. Приклад 4 Отримання (S)-міртазапіну До (S)-1-(3-Гідроксиметил-2-піридил)-4-метил2-фенілпіперазину (0,5г, 1,77ммоль) додавали поліфосфатну кислоту (9,6г). Реакційну суміш нагрівали до 100°C протягом 20 годин. Реакційну суміш розбавляли водою (6,5мл) та рН доводили до 8 додаванням 4 H розчину натрій гідроксиду. Водний шар екстрагували етилацетатом. Органічний шар промивали водою, сушили магній сульфатом та випарювали. Це дало заголовну сполуку (0,29г, 62%) з е.н. 76%. Приклад 5 До (S)-1-(3-Гідроксиметил-2-піридил)-4-метил2-фенілпіперазину (1,0г 3,53ммоль) додавали поліфосфатн у кислоту (2г). Реакційну суміш нагрівали до 130°C протягом 18 годин. Реакційну суміш розбавляли водою (8,5мл) та рН доводили до 8 додаванням 4 H розчину натрій гідроксиду. Водний шар екстрагували етилацетатом. Органічний шар промивали водою, сушили магній сульфатом та випарювали. Це дало заголовну сполуку (0,71г, 78%) з е.н. 98%. Приклад 6 Розчин (S)-1-(3-Гідроксиметил-2-піридил)-4метил-2-фенілпіперазину (10г, 3,53ммоль) у дихлорметані додавали до поліфосфатної кислоти, отриманої з 85% фосфатної кислоти (2,8г) та фосфор пентоксиду (1,3г). Реакційну суміш нагрівали до 130°C протягом 18 годин. Реакційну суміш розбавляли водою (6,5мл) та рН доводили до 8 додаванням 4 H розчин натрій гідроксиду. Водний шар екстрагували етилацетатом. Органічний шар промивали водою, сушили магній сульфатом та випарювали. Це дало заголовну сполуку (0,79г, 84%) з е.н. 83%. Приклад 7 До поліфосфатної кислоти (20г) додавали (S)1-(3-Гідроксиметил-2-піридил)4-метил-2-фенілпіперазин оксалат (13,2г, 35,3ммоль). Реакційну суміш перемішували при 130°C протягом 18 годин. У реакційну суміш додавали воду (220мл), етилацетат (220мл) та 33% розчин натрій гідроксиду (65мл). Водний шар відокремлювали та екстрагували двічі етилацетатом (220мл). Поєднані органічні фракції промивали тричі водою (220мл) та випарювали. Це дало 7,9г (S)-міртазапіну (84%) з е.н. 99,2%. 9 83666 Приклад 8 До поліфосфатної кислоти (4г) додавали (S)-1(3-Гідроксиметил-2-піридил)-4-метил-2-фенілпіперазин оксалат (1,32г, 3,53ммоль). Реакційну суміш перемішували при 130°C протягом 18 годин. У реакційну суміш додавали воду (22мл), етилацетат (22мл), та 33% розчин натрій гідроксиду (6,5мл). Водний шар відокремлювали та екстрагували двічі етилацетатом (22мл). Поєднані органічні фракції промивали тричі водою (22мл), сушили магній сульфатом та випарювали. Це дало 0,79г (S)міртазапіну (84%) з е.н. 83%. Приклад 9 Отримання (S)-міртазапіну До сульфатної кислоти (30,36мл) при температур 48°C додавали розчин (S)-1-(3Гідроксиметил-2-піридил)-4-метил-2-фенілпіперазину (15,18г, 51,05ммоль) в етанолі (30мл). Після 1 ночі додавали додаткову кількість сульфатної кислоти (30мл). Через 4 години реакція завершувалася. Воду (195мл) додавали, а потім розчин натрій гідроксиду (8,3M) до утворення осаду. Водний шар Комп’ютерна в ерстка В. Клюкін 10 екстрагували етилацетатом. Органічний шар промивали послідовно розчином натрій гідроксиду, тоді розчин натрій хлориду, сушили магній сульфатом та випарювали. Це дало заголовну сполуку (7,97г, 59%) з е.н. 62%. Приклад 9 Запропоновано для порівняння з непридатною комбінацією кислота/розчинник Отримання (S)-міртазапіну Концентровану сульфатн у кислоту (2,2мл) додавали до (S)-1-(3-Гідроксиметил-2-піридил)-4метил-2-фенілпіперазину (0,129г, 1,03ммоль). Дихлорметан додавали для утворення прозорого розчину. Дихлорметан випарювали під зменшеним тиском при 40°С. Реакційну суміш перемішували при 48°С. Через 4 години реакція завершувалася. Розчин натрій гідроксиду (4 H) додавали до утворення емульсії. Водний шар екстрагували діетиловим етером. Діетиловий етер промивали водою, сушили магній сульфатом та випарювали. Це дало заголовну сполуку (0,17г, 62%) з е.н. 36%. Підписне Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for the preparation of enantiomerically pure mirtazapine
Автори англійськоюWieringa Johannes Hubertus, van de Ven Adrianus Antonius Martinus, Kemperman Gerardus Johannes
Назва патенту російськоюСпособ получения энантиомерно чистого миртазапина
Автори російськоюВеринга Йоганнес Губертус, ван де Вен Адрианус Антониус Мартинус, Кемперман Герардус Йоганнес
МПК / Мітки
МПК: A61P 25/00, C07D 471/14, C07D 401/04
Мітки: міртазапіну, енантіомерно, одержання, чистого, спосіб
Код посилання
<a href="https://ua.patents.su/5-83666-sposib-oderzhannya-enantiomerno-chistogo-mirtazapinu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання енантіомерно чистого міртазапіну</a>
Попередній патент: Спосіб виробництва ординарного десертного солодкого рожевого вина “мускат кримський”
Наступний патент: Порошок діоксиду кремнію, виготовлений у пірогенних умовах, спосіб його виготовлення, поліефір та силіконовий каучук, які його містять
Випадковий патент: Спосіб лікування компенсованого крупу у дітей









