Тверда дозована форма комбінованого препарату, що містить метамізол натрію і триацетоаміно-4-толуолсульфонат, та спосіб її одержання
Номер патенту: 86164
Опубліковано: 25.03.2009
Автори: Павлова Віолета А., Даскалов Веселін Є., Гроздєва Радка К., Тонєв Влайко П., Борісова Янка І., Тімчев Ангел Р., Китовскі Бісер Х., Вижарова Мая К.
Формула / Реферат
1. Тверда дозована форма комбінованого препарату, що містить від 45 до 85 % мас. метамізолу натрію і від 2 до 4 % мас. триацетоаміно-4-толуолсульфонату і допоміжні речовини: пшеничний крохмаль, мікрокристалічну целюлозу, повідон, стеарат магнію і тальк, яка характеризується тим, що містить від 12,0 до 13,5 % мас. пшеничного крохмалю, від 9,0 до 10,5 % мас. мікрокристалічної целюлози, від 5,0 до 6,5 % мас. повідону, від 0,6 до 1,3 % мас. стеарату магнію і від 1,3 до 2,6 % мас. тальку.
2. Тверда дозована форма комбінованого препарату за п. 1, що являє собою таблетку, покриту плівкою.
3. Тверда дозована форма комбінованого препарату за п. 1, що характеризується наступним профілем розчинення триацетоаміно-4-толуолсульфонату, що міститься в таблетці:
Час (хв)
10
15
20
30
45
Ступінь розчинення (%) триацетоаміно-4-толуолсульфонату, що міститься в твердій дозованій формі, не менше
60,00
80,0
90,0
90,0
90,0
4. Спосіб одержання твердої дозованої форми комбінованого препарату, що містить метамізол натрію, триацетоаміно-4-толуолсульфонат і допоміжні речовини, який характеризується тим, що терапевтичні речовини змішують і просівають із частиною від загальної необхідної кількості мікрокристалічної целюлози і частиною пшеничного крохмалю з подальшою сухою гомогенізацією і зволоженням із використанням гранулюючого розчину повідону або суміші водного крохмального клею і водного розчину повідону, із подальшими сушінням, калібруванням і гомогенізацією (подрібнюванням у порошок) одержаного гранулята з частиною мікрокристалічної целюлози, що залишилася, і пшеничного крохмалю в співвідношенні від 2,5 до 3,0 : 1,0 і тальком, із подальшим додаванням стеарату магнію і додатковою гомогенізацією.
5. Спосіб за п. 4, який характеризується тим, що після додаткової гомогенізації здійснюють таблетування і подальше покриття плівкою одержаних ядер таблеток.
Текст
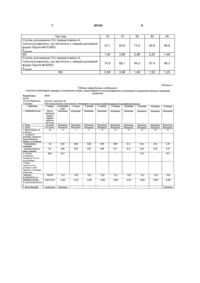
1. Тверда дозована форма комбінованого препарату, що містить від 45 до 85% мас. метамізолу натрію і від 2 до 4% мас. триацетоаміно-4толуолсульфонату і допоміжні речовини: пшеничний крохмаль, мікрокристалічну целюлозу, повідон, стеарат магнію і тальк, яка характеризується тим, що містить від 12,0 до 13,5% мас. пшеничного крохмалю, від 9,0 до 10,5% мас. мікрокристалічної целюлози, від 5,0 до 6,5% мас. повідону, від 0,6 до 1,3% мас. стеарату магнію і від 1,3 до 2,6% мас. тальку. 2. Тверда дозована форма комбінованого препарату за п. 1, що являє собою таблетку, покриту плівкою. 3. Тверда дозована форма комбінованого препарату за п. 1, що характеризується наступним про C2 2 (11) 1 3 86164 стеарату магнію і кукурудзяний крохмаль до 100%. Згідно з описом, препарат одержували змішуванням активних речовин із частиною кукурудзяного крохмалю, мікрокристалічної целюлози і частиною натрійкрохмальгліколяту з подальшими гранулюванням із використанням суміші 1,5% зв'язуючого з розрахунку на кукурудзяний крохмаль і 25% водний розчин полівінілпіролідону, сушінням, подрібнюванням у порошок і таблетуванням. Відома інша тверда дозована форма, що містить від 45 до 85% мас. метамізолу натрію і від 2 до 4% мас. триацетоаміно-4-толуолсульфонату у ролі терапевтичних речовин [патент BG 63147] і допоміжні речовини, такі як пшеничний крохмаль, мікрокристалічна целюлоза, тальк, стеарат магнію і повідон (полівідон) у концентрації від 4,6 до 9% мас, а також від 1 до 15% мас. попередньо желатинованого крохмалю або від 1 до 20% мас. крохмалю. Згідно з описаним винаходом, тверда дозована форма містить наступні кількості (у мг) на таблетку: метамізол натрію - від 300 до 800, триацетоаміно-4-толуолсульфонат (темпідон) - від 10 до 50, мікрокристалічна целюлоза - від 40 до 200, прежелатинований або пшеничний крохмаль - від 20 до 120, стеарат магнію – від 3 до 50, тальк - від 5 до 80 і повідон - від 20 до 80. Цю тверду лікарську форму одержують згідно з описом загальним гранулюванням активних речовин і допоміжних речовин з використанням водно-спиртового розчину повідону. Після гранулювання і регранулюЧас (хвилини) Ступінь розчинення (%) триацетоаміно-4-толуолсульфонату, що міститься у твердій дозованій формі Xсереднє SD Технічною проблемою, яка повинна бути вирішена даним винаходом, є поліпшення профілю розчинення триацетоаміно-4-толуолсульфонату і досягнення швидкого загального терапевтичного ефекту з одночасним збереженням оптимуму швидкості дезінтеграції та механічної міцності таблетки і стабільності активних речовин і твердої дозованої форми. Технічний опис винаходу Розроблена тверда дозована форма комбінованого лікарського препарату, що містить від 45 до 85% метамізолу натрію і від 2 до 4% мас. триацетоаміно-4-толуолсульфонату у ролі терапевтичних Час (хвилини) Ступінь розчинення (%) що міститься у твердій дозованій формі триацетоаміно-4-толуолсульфонату, не менше Спосіб одержання твердої дозованої форми згідно з даним винаходом складається з наступного: - терапевтичні речовини, частину загальної кількості мікрокристалічної целюлози і частину пшеничного крохмалю просівають. Після цього зважені і просіяні терапевтичні речовини і допоміжні речовини піддають сухій гомогенізації і, залежно від обладнання, що використовується, зволожують, 4 вання одержаний гранулят прямо таблетують, використовуючи роторну таблетувальну машину. Задум відомого рішення спрямований на одержання стабільної твердої дозованої форми із високим ступенем розчинення триацетоаміно-4толуолсульфонату. Враховуючи, що метамізол натрію добре розчиняється у воді (у відношенні 1:1) і швидко і повністю поглинається через слизову шлунка, тоді як темпідон розчиняється у воді в пропорції, що знаходиться в інтервалі між 1:10 і 1:3, профіль розчинення темпідону має головне значення в тій мірі, як розглядається терапевтична дія лікарського продукту, оскільки більш швидке вивільнення транквілізатора, що міститься в твердій дозованій формі, буде призводити до швидшого загального аналгетичного ефекту комбінації метамізолу натрію і триацетоаміно-4толуолсульфонату. Ця тверда дозована форма досягає стабільності, але не забезпечує швидкого досягнення високого ступеню розчинення триацетоаміно-4толуолсульфонату, що негативно впливає на фармакологічні властивості комбінованого препарату. Згідно зі специфікацією виробника комбінованого препарату (партія 7С0802), приготованого на основі BG 63147, ступінь розчинення триацетоаміно-4-толуолсульфонату складає принаймні 80% за 45 хвилин. Тест на розчинення того ж препарату показує наступний ступінь розчинення триацетоаміно-4-толуолсульфонату: 10 15 20 30 45 33,1 60,8 74,5 90,8 98,9 1,50 3,68 2,89 2,25 1,46 речовин і допоміжних речовин, що включають від 12,0 до 13,5% мас. пшеничного крохмалю, від 9,0 до 10,5% мас. мікрокристалічної целюлози, від 5,0 до 6,5% мас. повідону, від 0,6 до 1.3% мас. стеарату магнію і від 1,3 до 2,6% мас. тальку. Тверда дозована форма може бути будь-якою дозованою формою для перорального введення, такою як таблетки, капсули або порошок. Перевага віддається таблеткам, особливо таблеткам з плівковим покриттям. Тверда дозована форма відрізняється наступним профілем розчинення триацетоаміно-4толуолсульфонату: 10 15 20 30 45 60,00 80,0 90,0 90,0 90,0 використовуючи гранулюючий розчин повідону або суміш розведеного водою крохмального клею і водного розчину повідону. Гранулят потім сушать і калібрують. Одержаний гранулят гомогенізують (подрібнюють у порошок) із залишком мікрокристалічної целюлози і пшеничного крохмалю у співвідношенні від 2,5-3,0:1,0 і тальком. До нього додають стеарат магнію і всю суміш додатково гомогенізують. Якщо переважною є тверда дозо 5 вана форма, гомогенізовану суміш таблетують і таблетки потім покривають плівкою. Тверда дозована форма згідно з даним винаходом гарантує швидкий загальний терапевтичний ефект завдяки швидкому розчиненню триацетоаміно-4-толуолсульфонату. Несподівано було виявлено, що зменшена кількість лубриканта (стеарату магнію) і точні співвідношення між іншими допоміжними речовинами на стадії подрібнювання в порошок, і між допоміжними речовинами і активними інгредієнтами допомагають досягнути необхідний ступінь розчинення. Одержання таблетованої форми не призводить ні до підвищеної адгезії композиції таблетки до металевих частин таблетувальної машини, ні до пониження швидкості потоку. Нова композиція робить можливою застосування методу вологого гранулювання з подальшою гомогенізацією з використанням придатних лубрикантів і глідантів, і дозволяє уникнути прямого контакту між гідрофобними лубрикантами (тальком і стеаратом магнію) і активними інгредієнтами (зокрема, із триацетоаміно-4Метамізол натрію Триацетоаміно-4-толуолсульфат Повідон Мікрокристалічна целюлоза Пшеничний крохмаль Стеарат магнію Тальк Тверду дозовану форму одержували змішуванням метамізолу натрію і триацетоаміно-4толуолсульфонату із 1/3 загальної кількості мікрокристалічної целюлози і 4/5 пшеничного крохмалю і потім пропускали через сито з розміром комірки 0,7мм. Просіяні і зважені терапевтичні речовини і допоміжні речовини переводили в гранулятор, піддавали сухій гомогенізації і потім зволожували гранулюючим водно-спиртовим розчином повідону. Гранулят сушили і калібрували через сито з розміром комірки 1,2мм. Одержаний гранулят аналізували і гомогенізували (подрібнювали в порошок) із залишком мікрокристалічної целюлози і пшеничного крохмалю у співвідношенні 2,8 до 1,0 і тальком протягом 10 хвилин. Нарешті, до нього додавали стеарат магнію і суміш додатково гомогенізували протягом 5 хвилин. Одержана суміш готова для таблетування. Готову для таблетування суміш таблетували, використовуючи роторну машину, що має розмір пуансона 13мм. Ядра таблеток зі середньою масою 760мг потім покривали плівкою. Приклад 4 Додержуючись тієї же методики, що в прикладах 1, 2 і 3, терапевтичні речовини і допоміжні речовини піддавали сухій гомогенізації в сушарці з псевдозрідженим шаром і потім зволожували, використовуючи суміш водного крохмального клею і водного розчину повідону. Покриті плівкою таблетки, одержані згідно з прикладом 1 (партія №30503) оцінювали на стабі 86164 6 толуолсульфонатом). Це допомагає досягнути швидшого вивільнення триацетоаміно-4толуолсульфонату з твердої дозованої форми і одночасного збереження оптимального рівня дезінтеграції, механічної міцності і стабільності активних інгредієнтів і твердої дозованої форми. Нове рішення дає можливість уникнути дезінтеграції метамізолу натрію і вивільнення монометиламінового антипірину, як відповідає [патенту BG 63147]. Пояснення вкладеної фігури 1 Фігура 1 є наданням результатів порівняльної оцінки ступеня розчинення триацетоаміно-4толуолсульфонату, що міститься в твердій дозованій формі згідно з [патентом BG 63147] (партія 7С0802) і що міститься в комбінованому продукті, одержаному згідно з прикладом 1 даного винаходу (партія 30503). Переважні варіанти здійснення Винахід пояснюється далі, але не обмежується, наступними переважними здійсненнями лікарського препарату в кількостях, даних у мг на ядро таблетки. Приклад 1 500,0 20,0 45,0 80,0 94,0 7,0 14,0 Приклад 2 500,0 20,0 41,0 71,0 98,0 10,0 20,0 Приклад 3 500,0 20,0 50,0 73,0 101,0 8,0 10,0 льність згідно з таблицями 1 і 2. Лікарський препарат залишається стабільним при (25±2)°С протягом періоду в 3 роки і шість місяців і протягом періоду в один рік в умовах прискореного старіння при (40±2)°С (дослідження продовжується). Порівняльний тест був проведений для оцінки ступеня розчинення триацетоаміно-4-толуолсульфонату, що міститься в дозованій формі, одержаній згідно з [патентом BG 63147] (партія №7С0802) і в комбінованому препараті (партія №30503) відповідно до даного винаходу. Випробування розчинення було проведене відповідно до вимог, сформульованих в Європейській Фармакопеї (Ph.Eur. 5, 2.9.3), за наступних умов: Апаратура для тесту на Обладнання розчинність і обертовою лопаттю Параметри середовища: Розріджувач: Дистильована вода Кількість: 1000мл Температура: (37±0,5)°С Кількість таблеток у кошику апарату: 1 Швидкість обертання лопаті: (100±2)об/хв Час: 45хв Кількість зразка: 10мл Були одержані наступні порівняльні результати: 7 86164 Час (хв) Ступінь розчинення (%) триацетоаміно-4толуолсульфонату, що міститься у твердій дозованій формі Партія №7С0802 Xсереднє SD Ступінь розчинення (%) триацетоаміно-4толуолсульфонату, що міститься у твердій дозованій формі Партія №30503 Xсереднє SD 8 10 15 20 30 45 33,1 60,8 74,5 90,8 98,9 1,50 3,68 2,89 2,25 1,46 70,9 88,1 94,3 97,4 98,3 5,58 3,96 1,69 1,52 1,25 9 Комп’ютерна верстка В. Клюкін 86164 Підписне 10 Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSolid dosed form of the combined preparation, containing from metamizole sodium and -4-toluene sulphonate and method for its obtaining
Автори англійськоюTimchev Angel R., Pavlova Violeta A., Grozdeva Radka K., Daskalov Vesselin E., Tonev Vlayko P., Borisova Yanka I, Vajarova Maya K., Katovski Biser H.
Назва патенту російськоюТвердая дозированная форма комбинированного препарата, содержащая метамизол натрия и триацетоамино-4-толуолсульфоната, и способ ее получения
Автори російськоюТимчев Ангел Р., Павлова Виолетта А., Гроздева Радка К., Даскалов Веселин Е., Тонев Влайко П., Борисова Янка И., Вижарова Мая К., Китовски Бисер Х.
МПК / Мітки
МПК: A61K 31/451, A61K 9/20, A61P 29/00, A61K 31/415
Мітки: натрію, дозована, містить, препарату, триацетоаміно-4-толуолсульфонат, спосіб, метамізол, форма, комбінованого, одержання, тверда
Код посилання
<a href="https://ua.patents.su/5-86164-tverda-dozovana-forma-kombinovanogo-preparatu-shho-mistit-metamizol-natriyu-i-triacetoamino-4-toluolsulfonat-ta-sposib-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Тверда дозована форма комбінованого препарату, що містить метамізол натрію і триацетоаміно-4-толуолсульфонат, та спосіб її одержання</a>
Попередній патент: 6-нітро-n-(2′-карбокси-4′-хлорфеніл)антранілова кислота, що проявляє протизапальну, анальгетичну, діуретичну та протигрибкову активність
Наступний патент: Спосіб відбору корів у донори ембріонів для трансплантації
Випадковий патент: Спосіб виготовлення конструкційно-оздоблювального матеріалу та композиція, яка призначена для використання в способі