Спосіб отримання {2-[4-(a-феніл-п-хлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоти n,n-диметиламіду або його енантіомерів
Номер патенту: 92770
Опубліковано: 10.12.2010
Автори: Трінка Петер, Мезей Тібор, Понгьо Ласло, Барта Ференц, Надь Кальман, Рейтер Йожеф, Верецкейне Донат Дйордьі, Катона Золтан
Формула / Реферат
1. Спосіб отримання {2-[4-(a-феніл-п-хлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоти N,N-диметиламіду Формули (І)
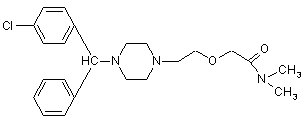 I
I
або його енантіомерів, при якому 1-(a-феніл-п-хлорбензил)-піперазин Формули (II)
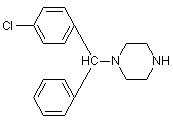 ІІ
ІІ
або його енантіомер взаємодіє з b-хлоретоксіоцтової кислоти N,N-диметиламідом Формули (III)
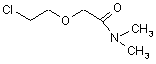 , III
, III
у інертному розчиннику у присутності каталізатора і речовини, що зв'язує кислоту.
2. Спосіб за п. 1, який відрізняється тим, що як розчинник застосовують аліфатичний спирт, що включає 1-4 атоми вуглецю, ацетонітрил, толуол, діоксан або ацетон, або їхню суміш.
3. Спосіб за п. 1, який відрізняється тим, що як речовину, що зв'язує кислоту, застосовують неорганічну або органічну основу.
4. Спосіб за п. 3, який відрізняється тим, що як речовину, що зв'язує кислоту, застосовують неорганічну основу, вибрану з карбонатів лужних металів або карбонатів лужноземельних металів.
5. Спосіб за п. 3, який відрізняється тим, що як речовину, що зв'язує кислоту, застосовують органічну основу, вибрану з триетиламіну або піридину.
6. Спосіб за п. 1, який відрізняється тим, що як каталізатор застосовують йодид лужного металу або бромід лужного металу, переважно йодид калію.
7. Спосіб за п. 1, який відрізняється тим, що реакцію проводять, нагріваючи реакційну суміш при температурі від 50 °С до температури кипіння розчинника, переважно від 80 °С до температури кипіння розчинника, найпереважніше при температурі кипіння розчинника.
8. Спосіб за п. 1, який відрізняється тим, що як початкову речовину застосовують (-)-1-(a-феніл-п-хлорбензил)-піперазин формули (II).
Текст
1. Спосіб отримання {2-[4-( -феніл-пхлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоти N,N-диметиламіду Формули (І) 3 92770 Даний винахід відноситься до отримання {2-[4(феніл-n-хлорбензил)-піперазин-1-іл]-етоксі}оцтової кислоти N,N-диметиламіду Формули (І) (l) його оптичних ізомерів і солей. Сполуки Формули (І) є важливим проміжним сполуками для отримання фармацевтичного активного інгредієнта - {2-[4-(α-феніл-n-хлорбензил)-піперазин-1-іл]етоксі}-оцтової кислоти, яка відома під міжнародною непатентованою назвою цетиризин. Цетиризин є фармацевтичним інгредієнтом неседативного антигістамінного типу. Сполука (-)-{2-[4-(α-феніл-n-хлорбензил)піперазин-1-іл]-етоксі}-оцтової кислоти N,Nдиметиламід Формули (І) є початковою речовиною в способі отримання (-)-{2-[4-(α-феніл-nхлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоти Формули (VI) 4 також відбувається алкілування аміногрупи 2ацетаміду. Побічні продукти, що утворюються у вищезазначеній реакції, не можна відокремити від продукту реакції яким-небудь простим способом. Видалення вказаних побічних продуктів і очищення продукту вимагають дорогого процесу очищення, який призводить також до істотного зниження виходу. У міжнародній заявці на патент, номер публікації WO 01/40211, розкритий спосіб отримання {2[4-(α-феніл-n-хлорбензил)-піперазин-1-іл]-етоксі}оцтової кислоти N,N-диметиламіду Формули (І) із сполуки 2-[4-(α-феніл-n-хлорбензил)-піперазин-1іл]-етанол Формули (IV) (IV) шляхом перетворення вказаного заміщеного похідного етанолу в сіль з лужним металом в інертному розчиннику і взаємодії одержаної таким чином солі з хлороцтової кислоти з N,Nдиметиламідом Формули (V). (VI) (V) яка також є фармацевтично активним інгредієнтом, відомим під міжнародною непатентованою назвою левоцетиризин. Левоцетиризин відноситься до групи фармацевтично активних інгредієнтів неседативного антигістамінного типу. Цетиризин і левоцетиризин відомі з патентів Сполучених Штатів №5 627 083 і 5 698 558. Вперше спосіб отримання цетиризину був розкритий в Європейському патенті №58146. Цетиризин був одержаний шляхом гідролізу {2-[4-(αфеніл-n-хлорбензил)-піперазин-1-іл]-етоксі}ацетаміду Формули (VII). (VII) Вказаний {2-[4-(α-феніл-n-хлорбензил)піперазин-1-іл]-етоксі}-ацетамід Формули (VII) одержували шляхом взаємодії 1-(α-феніл-n-хлорбензил)-піперазину Формули (II) з 2-ацетамідом Формули (VIII) (VIII) в ксилолі в якості розчинника у присутності безводного карбонату натрію. Недолік вищезазначеного способу полягає в тому, що протягом цієї реакції як побічна реакція Продукт {2-[4-(α-феніл-n-хлорбензил)піперазин-1-іл]-етоксі}-оцтової кислоти N,Nдиметиламід Формули (І) - одержують у вигляді дигідрохлориду, солі, яку безпосередньо використовують як початкову речовину в способі отримання цетиризину. Недолік вищезазначеного способу полягає в тому, що О-алкілування сполуки 2-[4-(α-феніл-nхлорбензил)-піперазин-1-іл]-етанолу Формули (IV) може бути виконано тільки в розчині, що не містить води і спиртів, що вимагає використання спеціального устаткування, а також безводних реактивів. Задача дослідницької роботи авторів даного винаходу полягала в розробці способу отримання {2-[4-(α-феніл-n-хлорбензил)-піперазин-1-іл]етоксі}-оцтової кислоти N,N-диметиламіду Формули (І), придатного для виробництва кінцевого продукту -цетиризину - фармакопейної якості без використання дорогих реагентів, складного і дорогого устаткування і без складних операцій (таких як, наприклад, обезводнення і видалення вологи, очищення продукту від побічних продуктів). Вищезазначене завдання розв'язується завдяки способу згідно даному винаходу. Основою даного винаходу є несподіване відкриття, що вищезазначені недоліки можуть бути усунені, коли сполуки {2-[4-(α-феніл-nхлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоти N,N-диметиламід Формули (І) одержують шля 5 хом взаємодії 1-(α-феніл-n-хлорбензил) піперазину Формули (II) 92770 (II) і (2-хлоретоксі)-оцтової диметиламіду Формули (III) кислоти N,N (III) у інертному розчиннику і у присутності речовини, що зв'язує кислоту, і каталізатора. {2-[4-(αфеніл-n-хлорбензил)-піперазин-1-іл]-етоксі}оцтової кислоти Ν,Ν-диметиламід Формули (І), одержаний вказаним способом, придатний для прямого перетворення в цетиризин. Додаткова перевага способу полягає в тому, що шляхом використання єдиного енантіомеру початкової сполуки (-)-1-(α-феніл-n-хлорбензил)-піперазину Формули (II), може бути одержаний левоцетиризин. У вищезазначеному способі за даним винаходом утворюється тільки невелика кількість побічних продуктів, і не потрібно, щоб умови роботи були безводними. Особливо несподіваною особливістюспособу є те, що при лужному гідролізі (-)-{2-[4-(α-феніл-nхлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоти N,N-диметиламіду не відбувається рацемізація, тому вказаний лужний гідроліз дає оптично чисту ()-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1-іл]етоксі}-оцтову кислоту [левоцетиризин], що не містить (+)-ізомера. Згідно даному винаходу, алкілування 1-(αфеніл-n-хлорбензил)-піперазину Формули (II) за допомогою (2-хлоретоксі)-оцтової кислоти N,Nдиметиламіду Формули (III) проводять в протонному або апротонному, полярному або неполярному розчиннику, наприклад, аліфатичних спиртах, що включають 1-4 атоми вуглецю, ацетонітрилі, толуолі, діоксані, ацетоні, переважно в толуолі. Для нейтралізації кислоти, що утворюється в реакції, можна застосовувати слабку органічну або неорганічну основу, наприклад, карбонат або гідрокарбонат лужного металу або лужноземельного металу, переважно карбонат натрію, піридин або третинний аліфатичний амін, де алкільна група включає 2-6 атомів вуглецю, переважно, триетиламін. Як каталізатор можна застосовувати галогенід лужного металу, наприклад, йодид літію, натрію або калію, переважно, йодид калію. Реакцію проводять при температурі від 50°С до температури кипіння розчинника, переважно, від 80°С до температури кипіння розчинника, найпереважніше при температурі кипіння розчинника. Продукт може бути виділений способами, відомими як такі з рівня техніки. Особливо переважний спосіб полягає в отриманні продукту у вигляді його дигідрохлориду. 6 Початкова речовина для способу за даним винаходом, 1-(α-феніл-n-хлорбензил)-піперазин Формули (II), і його оптичні ізомери є відомими сполуками (Yakugaku Zasshi, 74, 1954, 1049; Chem. Abstr., 1955, 11666; патент Великобританії, публікація №2 225 321). Друга початкова речовина для способу за даним винаходом, 2-хлоретоксіоцтової кислоти N,Nдиметиламід, відома з патенту Німеччини №2 150 075. Додаткові деталі даного винаходу представлені в наступних прикладах, проте об'єм охорони не обмежується вказаними прикладами. Приклад 1 (±)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1іл]-етоксі}-оцтової кислоти Ν,Ν-диметиламід 14,4г (0,05моль) (±)-1-(α-феніл-n-хлорбензил)піперазину розчиняють в 120мл толуолу і додають 15г безводного карбонату натрію і 0,7г йодиду калію. Реакційну суміш нагрівають приблизно до 110°С при перемішуванні, і при цій температурі протягом однієї години додають по краплі 8,8г (0,053моль) неочищеного 2-хлоретоксіоцтової кислоти Ν,Ν-диметиламіду. Після додавання реакційну суміш нагрівають і перемішують при вищезгаданій температурі протягом 24 годин. Реакційну суміш охолоджують, до неї додають 20г подрібненого льоду, і значення рН суміші доводять до 6,4 додаванням приблизно 1,5мл концентрованої соляної кислоти. Шари розділяють, до шару толуолу додають 25г подрібненого льоду, і значення рН шару толуолу доводять до 3,8, додаючи приблизно 3мл концентрованої соляної кислоти. Шари розділяють, до водного шару додають 50мл дихлорметану, і значення рН водного шару доводять до 7-8, додаючи приблизно 4,5мл розчину гідроксиду натрію з концентрацією 40мас.%. Шар дихлорметану відокремлюють, висушують над безводним сульфатом натрію, фільтрують і розчинник випаровують у вакуумі. Згідно даному способу одержують 18,4г (88,2%) в'язкого, маслянистого продукту (температура плавлення 183-190°С). Чистота продукту складає більше 98мас.%, як визначено за допомогою високоефективної рідинної хроматографії. Продукт придатний як початкова речовина для виготовлення цетиризину фармакопейної якості, що задовольняє специфікації, приведеній в Європейській Фармакопеї 1997:1084. Згідно вищезазначеним специфікаціям, сумарна кількість домішок не повинна перевищувати 0,5мас.%, і кількість будь-якої окремої домішки повинна бути менше 0,1мас.%. Якщо бажано, вільна основа може бути перетворена в дигідрохлорид з використанням у якості розчинника 2-пропанолу шляхом взаємодії вільної основи з ізопропанольним розчином соляної кислоти з концентрацією 25мас.%. Приклад 2 (±)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1іл]-етоксі}-оцтової кислоти дигідрохлорид 48,9г (0,1моль) (±)-{2-[4-(α-феніл-nхлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоти N,N-диметиламіду дигідрохлориду, одержаного згідно способу з Прикладу 1, розчиняють в 170мл води, і розчин, що виходить, змішують з 100мл 7 92770 8 водного розчину гідроксиду натрію з концентрацічистоту більше 99%, і реакцію проводять в масшєю 40мас.%. Суспензію, що виходить, нагрівають табі 0,02моль. Вихід: 7,3г (79,4%) сполуки, вказапри кипінні протягом трьох годин при безперервної в заголовку, що має оптичне обертання ному барботуванні азоту. Одержаній реакційній [α]36520=+12,2°. Чистота продукту, визначена за суміші дають охолодитися до 40°С, розбавляють допомогою високоефективної рідинної хроматог250мл води і підкислюють з допомогою приблизно рафії, складає більше 98%. Оптична чистота про60мл концентрованої соляної кислоти до значення дукту, визначена за допомогою хіральної високорН3,8. Кислий розчин екстрагують 200мл і 100мл ефективної рідинної хроматографії, складає дихлорметану, відповідно. Шари дихлорметану більше 99%. об'єднують, розчинник випаровують, і залишок Оптичну чистоту продукту визначають за дорозчиняють в 25мл води. Водний розчин змішують помогою ВЕРХ, з використанням колонки Chiracell з 12мл концентрованої соляної кислоти і випароOD-R і рухомої фази, що включає 2-пропанол вують у вакуумі насухо. Густий маслянистий загексан 32:68 (об./об.) і ацетонітрил - 0,5Μ розчин лишок розчиняють в 25мл ацетону, розчин змішуперхлорат натрію. ють з додатковою порцією ацетону об'ємом 300мл Приклад 6 і перемішують протягом однієї години. Кристаліч(+)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1ний продукт, що випав в осад, фільтрують, промиіл]-етоксі}-оцтової кислоти Ν,Ν-диметиламід вають ацетоном та діетиловим ефіром і висушуВідтворюють спосіб з Прикладу 1 з тією відють у вакуумі. Таким чином одержують 39,4г мінністю, що замість (±)-1-(α-феніл-n-хлорбензил)(85,5%) чистої сполуки, вказаної в заголовку, темпіперазину застосовують (+)-1-(α-феніл-nпература плавлення 225,5-228°С. Одержаний тахлорбензил)-піперазин з енантіомерною чистотою ким чином продукт відповідає всім вимогам Євробільше 99%. Вихід: 17,5г (83,8%) в'язкого масляпейської Фармакопеї 3, 1997:1084. нистого продукту, чистота якого складає більше Приклад 3 98%, як визначено за допомогою високоефектив(±)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1ної рідинної хроматографії. Оптична чистота проіл]-етоксі}-оцтової кислоти дигідрохлорид дукту, визначена за допомогою хіральної високоВідтворюють спосіб з Прикладу 2 з тією відефективної рідинної хроматографії, складає мінністю, що замість 48,9г (0,1моль) (±)-{2-[4-(αбільше 99%. Оптичне обертання [α]D20=+6,3° феніл-n-хлорбензил)-піперазин-1-іл]-етоксі}оцтової (с=0,8г/10 см3 етанолу). кислоти N,N-диметиламіду дигідрохлориду застоПриклад 7 совують 41,7г (0,1моль) (±)-{2-[4-(α-феніл-n(-)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1хлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоіл]-етоксі}-оцтової кислоти дигідрохлорид ти N,N-диметиламід. Вихід: 38,1г (82,1%) чистої Сполуку, вказану в заголовку, одержують спосполуки, вказаної в заголовку (температура плавсобом з Прикладу 2 з тією відмінністю, що замість лення 226-228°С), яка відповідає всім вимогам (±)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1-іл]щодо якості, приведеним в Європейській Фармаетоксі}-оцтової кислоти N,N-диметиламіду дигідрокопеї 3, 1997:1084. хлориду як початкову речовину застосовують (+)Приклад 4 {2-[4-(α-феніл-n-хлорбензил)-піперазин-1-іл](-)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1етоксі}-оцтової кислоти N,N-диметиламід, що має іл]-етоксі}-оцтової кислоти Ν,Ν-диметиламід оптичну чистоту більше 99%, і реакцію проводять Відтворюють спосіб з Прикладу 1 з тією відв масштабі 0,02моль. Вихід: 6,9г (75,0%), оптичне 20 мінністю, що замість (±)-1-(α-феніл-n-хлорбензил)обертання [α]365 =-12,4°, чистота, визначена за піперазину застосовують (-)-1-(α-феніл-nдопомогою високоефективної рідинної хроматогхлорбензил)-піперазин, що має енантіомерну чисрафії, складає більше 98%. Оптична чистота, витоту більше 99%. Вихід 18,2г (87,3%) в'язкого масзначена за допомогою хіральної високоефективної лянистого продукту, що має чистоту вище 98%, що рідинної хроматографії, складає більше 99%. визначено за допомогою високоефективної рідинПриклад 8 ної хроматографії. Оптична чистота продукту, ви(±)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1значена за допомогою хіральної високоефективної іл]-етоксі}-оцтової кислоти Ν,Ν-диметиламід рідинної хроматографії, складає більше 99%. ОпСполуку, вказану в заголовку, одержують згідтичне обертання [α]D20=-6,4° (с=0,8г/10см3 етаноно способу з Прикладу 1 з тією відмінністю, що лу). замість 120мл толуолу в якості розчинника застоЧистоту продукту визначають за допомогою совують 100мл ацетонітрилу, і реакцію проводять високоефективної рідинної хроматографії (ВЕРХ), при температурі кипіння ацетонітрилу протягом 24 з використанням колонки Chiralpak AD і рухомої годин. Вихід: 10,2г (48,9%) в'язкого, сиропоподібфази, що включає 2-пропанол - гексан 25:75 ного продукту, з чистотою більше 98%, як визна(об./об.). чено за допомогою високоефективної рідинної Приклад 5 хроматографії, який придатний для прямого пере(+)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1творення в цетиризин, відповідний специфікації, іл]-етоксі}-оцтової кислоти дигідрохлорид приведеній в Європейській Фармакопеї. Проводять спосіб з Прикладу 2 з тією відмінніПриклад 9 стю, що замість (±)-{2-[4-(α-феніл-n-хлорбензил)(±)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1піперазин-1-іл]-етоксі}-оцтової кислоти N,Nіл]-етоксі}-оцтової кислоти Ν,Ν-диметиламід диметиламіду дигідрохлориду застосовують (-)-{2Сполуку, вказану в заголовку, одержують згід[4-(α-феніл-n-хлорбензил)-піперазин-1-іл]-етоксі}но способу з Прикладу 1 з тією відмінністю, що оцтової кислоти Ν,Ν-диметиламід, що має оптичну замість 120мл толуолу в якості розчинника засто 9 92770 10 совують 150мл ацетону, і реакцію проводять шляефективної рідинної хроматографії, більше 98%, хом нагрівання реакційної суміші протягом 48 гоякий придатний для прямого перетворення в цедин при температурі кипіння ацетону. Вихід: 9,4г тиризин фармакопейної якості. (45,1%) сиропоподібного продукту, що має чистоту Приклад 11 більше 95%, як визначено на основі аналізу за (±)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1допомогою високоефективної рідинної хроматогіл]-етоксі}-оцтової кислоти Ν,Ν-диметиламід рафії, який придатний для прямого перетворення Сполуку, вказану в заголовку, одержують згідв цетиризин, відповідний специфікації Європейсьно способу з Прикладу 1 з тією відмінністю, що кої Фармакопеї. замість 120мл толуолу в якості розчинника застоПриклад 10 совують 100мл ацетонітрилу, і замість безводного (±)-{2-[4-(α-феніл-n-хлорбензил)-піперазин-1карбонату натрію в якості речовини, що зв'язує іл]-етоксі}-оцтової кислоти Ν,Ν-диметиламід кислоту, застосовують 10мл триетиламіну, і цю Сполуку, вказану в заголовку, одержують згідреакцію проводять шляхом нагрівання реакційної но способу з Прикладу 1 з тією відмінністю, що суміші при 80°С протягом 72 годин. Вихід 8,2г замість 120мл толуолу в якості розчинника засто(39,3%) сиропоподібного продукту, що має чистосовують 120мл діоксану, і реакцію проводять шляту, визначену за допомогою високоефективної хом нагрівання реакційної суміші до кипіння протярідинної хроматографії, більше 98%, який придатгом 24 годин при температурі кипіння діоксану. ний для перетворення в цетиризин, відповідний Вихід: 10,8г в'язкого, сиропоподібного продукту, вимогам Європейської Фармакопеї. що має чистоту, визначену за допомогою високо Комп’ютерна верстка Т. Чепелева Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of {2-[4-(75ffliph0fflipv0flockaspectratio1picturegray0picturebilevel0frecolorfillaspicture0fuseshapeanchor0ffilled0fhittestfill1fillshape1filluserect0fnofillhittest0fline0fpreferrelativeresize1freallyhidden0fscriptanchor0ffakemaster0fcamefromimgdummy0flayoutincell10100090000039d00000002001c00000000000500000009020000000005000000020101000000050000000102ffffff00050000002e0118000000050000000b0200000000050000000c02400140011200000026060f001a00ffffffff000010000000c0ffffff0100000000010000410100000b00000026060f000c004d61746854797065000030001c000000fb02e0fe0000000000009001000000020002001053796d626f6c007740000000f10b0a85e6c0f477efc0f4770100000000003000040000002d01000008000000320ae00037000100000061790a00000026060f000a00ffffffff0100000000001c000000fb021000070000000000bc02000000cc0102022253797374656d000000000a000000040000000000ffffffff0100000000003000040000002d01010004000000f0010000030000000000-phenyl-p-chlorobenzyl)-piperazin-1-yl]-ethoxy}-acetic acid-n,n-dimethylamide and enantiomers thereof
Автори англійськоюTrinka Peter, Mezei Tibor, Reiter Jozsef, Bartha Ferenc, Katona Zoltan, Vereczkeyne Donath Gyoergyi, Nagy Kalman, Pongo Laszlo
Назва патенту російськоюСпособ получения {2-[4-(а-фенил-п-хлорбензил)-пиперазин-1-ил]-этокси}-уксусной кислоты n,n-диметиламида или его энантиомеров
Автори російськоюТринка Петер, Мезей Тибор, Рейтер Йожеф, Барта Ференц, Катона Зольтан, Верецкейне Донат Дьйорди, Надь Калман, Понго Ласло
МПК / Мітки
МПК: C07D 295/088
Мітки: отримання, спосіб, кислоти, n,n-диметиламіду, 2-[4-(a-феніл-п-хлорбензил)-піперазин-1-іл]-етоксі}-оцтової, енантіомерів
Код посилання
<a href="https://ua.patents.su/5-92770-sposib-otrimannya-2-4-a-fenil-p-khlorbenzil-piperazin-1-il-etoksi-octovo-kisloti-nn-dimetilamidu-abo-jjogo-enantiomeriv.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання {2-[4-(a-феніл-п-хлорбензил)-піперазин-1-іл]-етоксі}-оцтової кислоти n,n-диметиламіду або його енантіомерів</a>
Попередній патент: Система конвеєра, комбінована система, спосіб з’єднання металургійних методів та спосіб експлуатації системи конвеєра
Наступний патент: Композиція інгредієнтів для горілки “сторічна”
Випадковий патент: Спосіб визначення межі вибухобезпечності метаноповітряних сумішей у дегазаційних трубопроводах









