Препарат на основі синтетичних міметиків та спосіб одержання синтетичних міметиків (варіанти)
Номер патенту: 104875
Опубліковано: 25.03.2014
Автори: Тан Хайчжун, Деградо Уілльям Ф., Корчак Божена, Сюй Юнцзян, Лю Дахой, Скотт Річард У.
Формула / Реферат
1. Препарат, який включає сполуку формули I
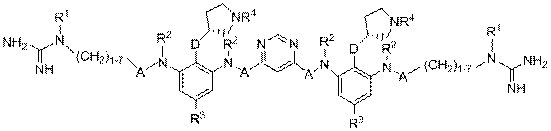 ,
,
де:
кожний A являє собою незалежно -C=O, -C=S або -CH2;
кожний D являє собою незалежно O або S;
кожний R1 являє собою незалежно водень, C1-3алкіл, C1-3алкокси, гало або галоC1-3алкіл;
кожний R2 являє собою незалежно водень, C1-3алкіл, C1-3алкокси, гало або галоC1-3алкіл;
кожний R3 являє собою незалежно водень, C1-4алкіл, C1-4алкокси, гало або галоC1-4алкіл; і
кожний R4 являє собою незалежно водень, C1-3алкіл, C1-3алкокси, гало або галоC1-3алкіл;
або її фармацевтично прийнятну сіль, де препарат включає ексципієнт, вибраний з 20 % маса/об'єм пропіленгліколю у фізіологічному розчині, 30 % маса/об'єм пропіленгліколю у фізіологічному розчині, 40 % маса/об'єм пропіленгліколю у фізіологічному розчині, 50 % маса/об'єм пропіленгліколю у фізіологічному розчині, 15 % маса/об'єм пропіленгліколю в очищеній воді, 30 % маса/об'єм пропіленгліколю в очищеній воді, 50 % маса/об'єм пропіленгліколю в очищеній воді, 30 % маса/об'єм пропіленгліколю і 5 % маса/об'єм етанолу в очищеній воді, 15 % маса/об'єм гліцерину в очищеній воді, 30 % маса/об'єм гліцерину в очищеній воді, 50 % маса/об'єм гліцерину в очищеній воді, 20 % маса/об'єм Клептози в очищеній воді, 40 % маса/об'єм Клептози в очищеній воді і 25 % маса/об'єм Каптизолу в очищеній воді.
2. Препарат за п. 1, де кожний A являє собою -C=O.
3. Препарат за п. 1 або п. 2, де кожний D являє собою O.
4. Препарат за будь-яким з пп. 1-3, де кожний R1 являє собою незалежно водень, метил, етил, метокси, етокси, гало або галоC1-3алкіл.
5. Препарат за будь-яким з пп. 1-3, де кожний R1 являє собою незалежно водень, метил, метокси, гало або галоC1-3алкіл.
6. Препарат за будь-яким з пп. 1-3, де кожний R1 являє собою незалежно водень, метил або метокси.
7. Препарат за будь-яким з пп. 1-3, де кожний R1 являє собою водень.
8. Препарат за будь-яким з пп. 1-7, де кожний R2 являє собою незалежно водень, метил, етил, метокси, етокси, гало або галоC1-3алкіл.
9. Препарат за будь-яким з пп. 1-7, де кожний R2 являє собою незалежно водень, метил, метокси або гало.
10. Препарат за будь-яким з пп. 1-7, де кожний R2 являє собою водень.
11 Препарат за будь-яким з пп. 1-10, де кожний R3 являє собою незалежно водень, метил, етил, метокси, етокси, гало або галоC1-3алкіл.
12. Препарат за будь-яким з пп. 1-10, де кожний R3 являє собою незалежно метил, метокси, гало або галоC1-3алкіл.
13. Препарат за будь-яким з пп. 1-10, де кожний R3 являє собою незалежно гало або галоC1-3алкіл.
14. Препарат за будь-яким з пп. 1-10, де кожний R3 являє собою незалежно галоC1-3алкіл.
15. Препарат за будь-яким з пп. 1-10, де кожний R3 являє собою трифторметил.
16. Препарат за будь-яким з пп. 1-15, де кожний R4 являє собою незалежно водень, метил, етил, метокси, етокси або галоC1-3алкіл.
17. Препарат за будь-яким з пп. 1-15, де кожний R4 являє собою незалежно водень, метил, метокси, гало або галоC1-3алкіл.
18. Препарат за будь-яким з пп. 1-15, де кожний R4 являє собою незалежно водень, метил, метокси або гало.
19. Препарат за будь-яким з пп. 1-15, де кожний R4 являє собою водень.
20. Препарат за п. 1, де:
кожний A являє собою незалежно -C=O або -C=S;
кожний D являє собою незалежно O або S;
кожний R1 являє собою незалежно водень, метил, етил, метокси, етокси, гало, галометил або галоетил;
кожний R2 являє собою незалежно водень, метил, метокси, гало або галометил;
кожний R3 являє собою незалежно C1-3алкіл, C1-3алкокси, гало або галоалкіл; і
кожний R4 являє собою незалежно водень, метил, етил, метокси, етокси, гало, галометил або галоетил.
21. Препарат за п. 1, де:
кожний A являє собою незалежно -C=O або -C=S;
кожний D являє собою незалежно O або S;
кожний R1 являє собою незалежно водень, метил, метокси, гало або галометил;
кожний R2 являє собою незалежно водень, гало або галометил;
кожний R3 являє собою незалежно метил, етил, метокси, етокси, гало, галометил або галоетил; і
кожний R4 являє собою незалежно водень, метил, етил, метокси, етокси, гало, галометил або галоетил.
22. Препарат за п. 1, де:
кожний A являє собою -C=O;
кожний D являє собою O;
кожний R1 являє собою незалежно водень, гало або галометил;
кожний R2 являє собою незалежно водень або гало;
кожний R3 являє собою незалежно метил, метокси, гало або галометил; і
кожний R4 являє собою незалежно водень, метил, метокси, гало або галометил.
23. Препарат за п. 1, де:
кожний A являє собою -C=O;
кожний D являє собою O;
кожний R1 являє собою незалежно водень або гало;
кожний R2 являє собою незалежно водень або гало;
кожний R3 являє собою незалежно метил, гало або галометил; і
кожний R4 являє собою незалежно водень, метил, гало або галометил.
24. Препарат за п. 1, де:
кожний A являє собою -C=O;
кожний D являє собою O;
кожний R1 являє собою незалежно водень або гало;
кожний R2 являє собою незалежно водень або гало;
кожний R3 являє собою незалежно гало або галометил; і
кожний R4 являє собою незалежно водень або гало.
25. Препарат за п. 1, де:
кожний A являє собою -C=O;
кожний D являє собою O;
кожний R1 являє собою незалежно водень або гало;
кожний R2 являє собою незалежно водень або гало;
кожний R3 являє собою незалежно метил, гало або галометил; і
кожний R4 являє собою незалежно водень, метил, гало або галометил.
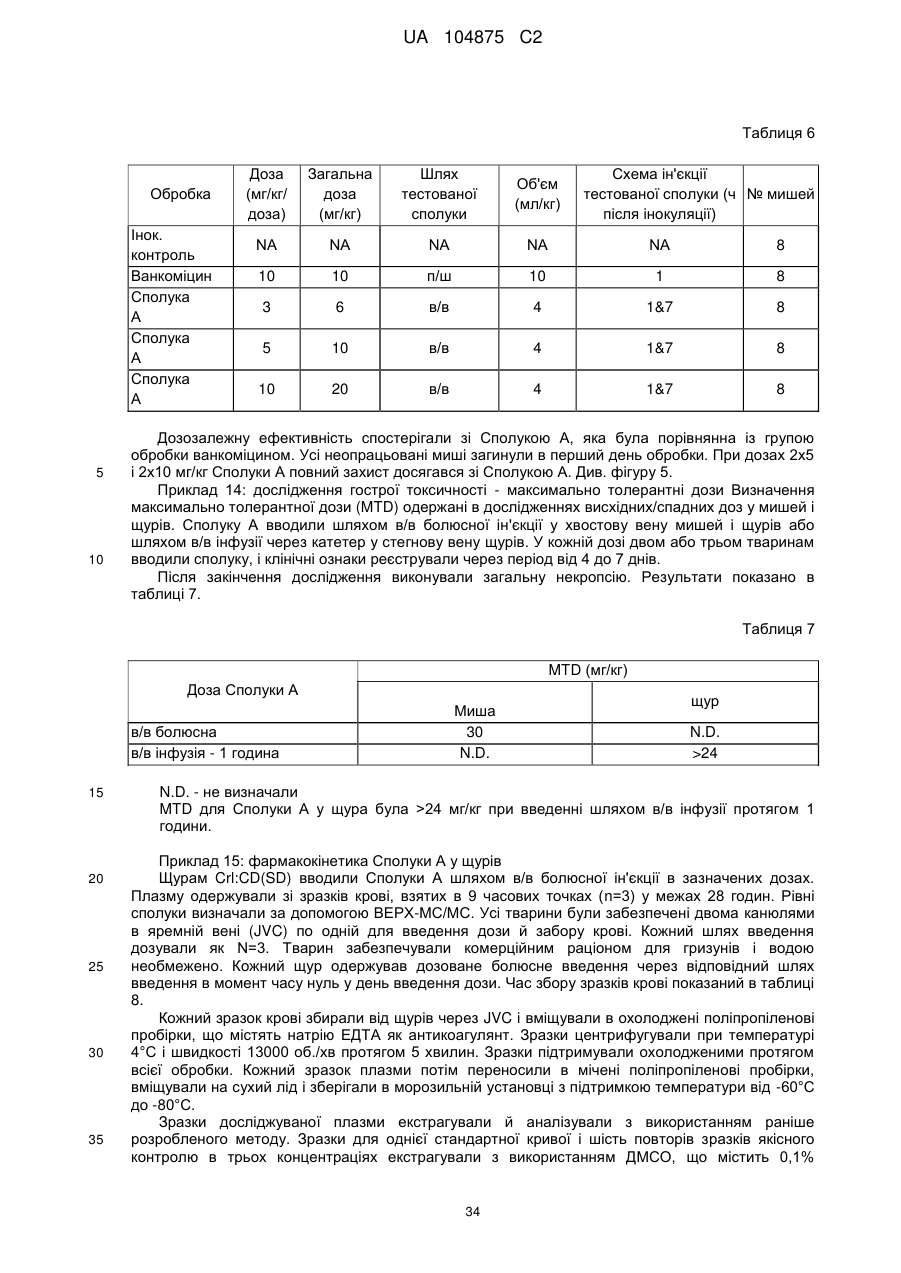
26. Препарат за п. 1, де сполука формули I являє собою сполуку формули
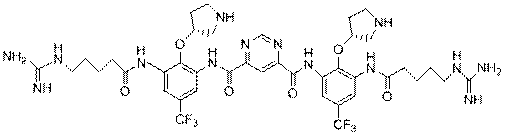
або її фармацевтично прийнятну сіль.
27. Препарат за будь-яким з пп. 1-26, де препарат включає ексципієнт, вибраний з 50 % маса/об'єм пропіленгліколю в очищеній воді, 15 % маса/об'єм гліцерину в очищеній воді, 20 % маса/об'єм Клептози в очищеній воді, 40 % маса/об'єм Клептози в очищеній воді і 25 % маса/об'єм Каптизолу в очищеній воді.
28. Препарат за будь-яким з пп. 1-26, де препарат включає ексципієнт, вибраний з 20 % маса/об'єм Клептози в очищеній воді, 20 % маса/об'єм пропіленгліколю в очищеній воді й 15 % маса/об'єм гліцерину в очищеній воді.
29. Препарат за п. 1, де сполука формули І являє собою

або її фармацевтично прийнятну сіль в 20 % маса/об'єм Клептози в очищеній воді.
30. Препарат за будь-яким з пп. 1-29, де сполука представлена 50 мг/мл.
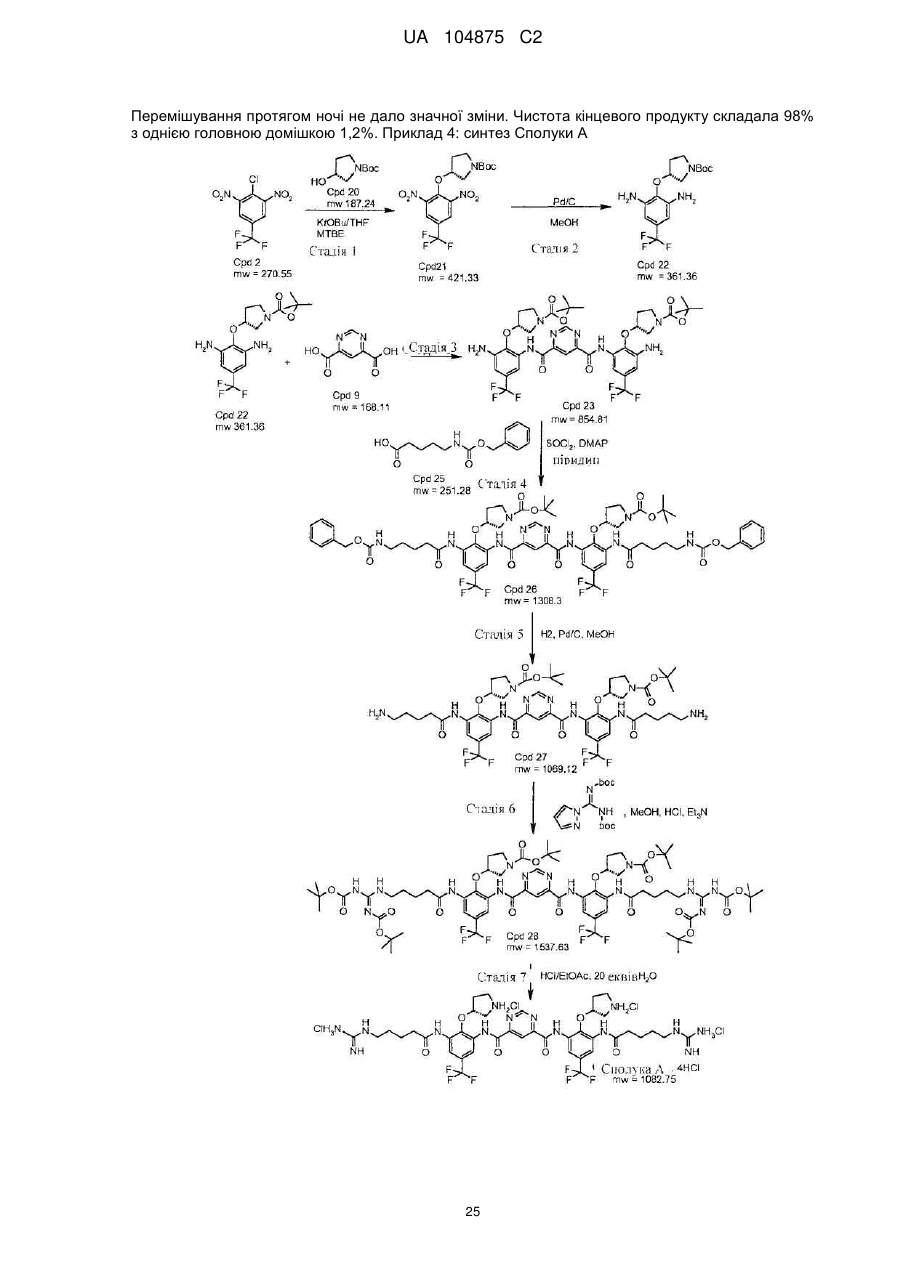
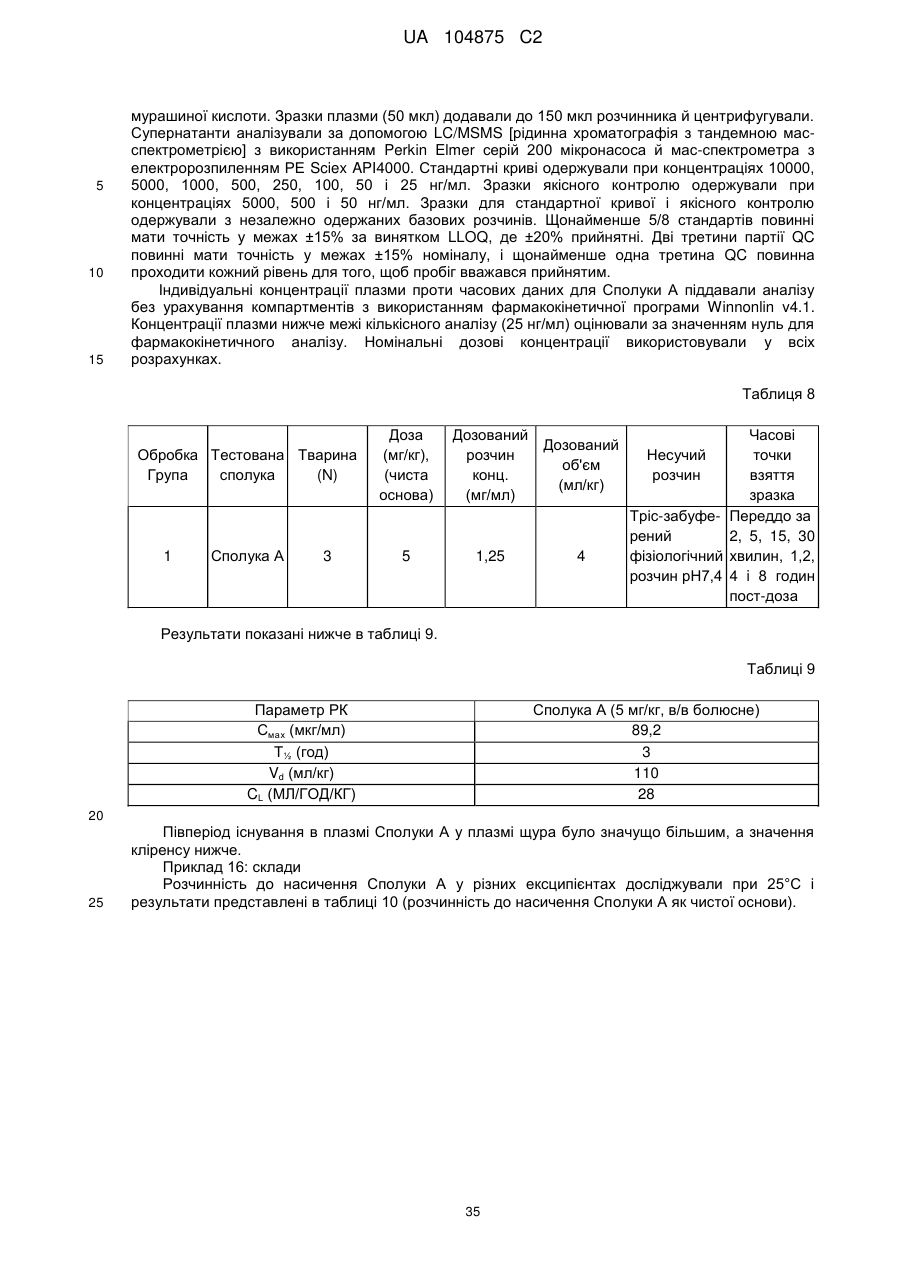
31. Спосіб одержання сполуки формули
 ,
,
який включає:
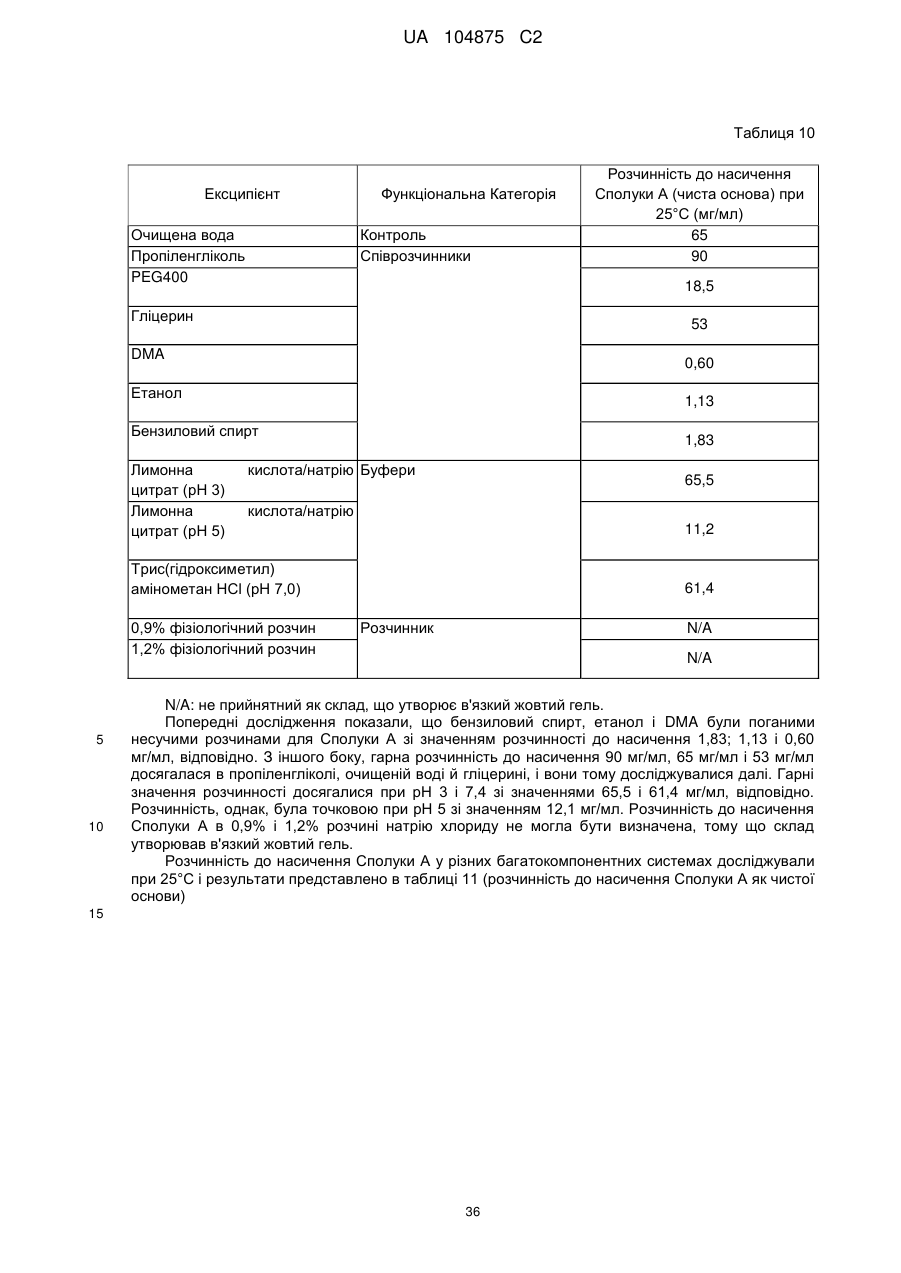
а) взаємодію (R)-(-)-N-Boc-3-піролідинолу із сильною основою з одержанням суміші; і наступну взаємодію суміші із 2-хлор-5-(трифторметил)-1,3-динітробензолом з одержанням сполуки, що має Формулу II
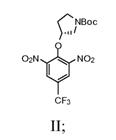
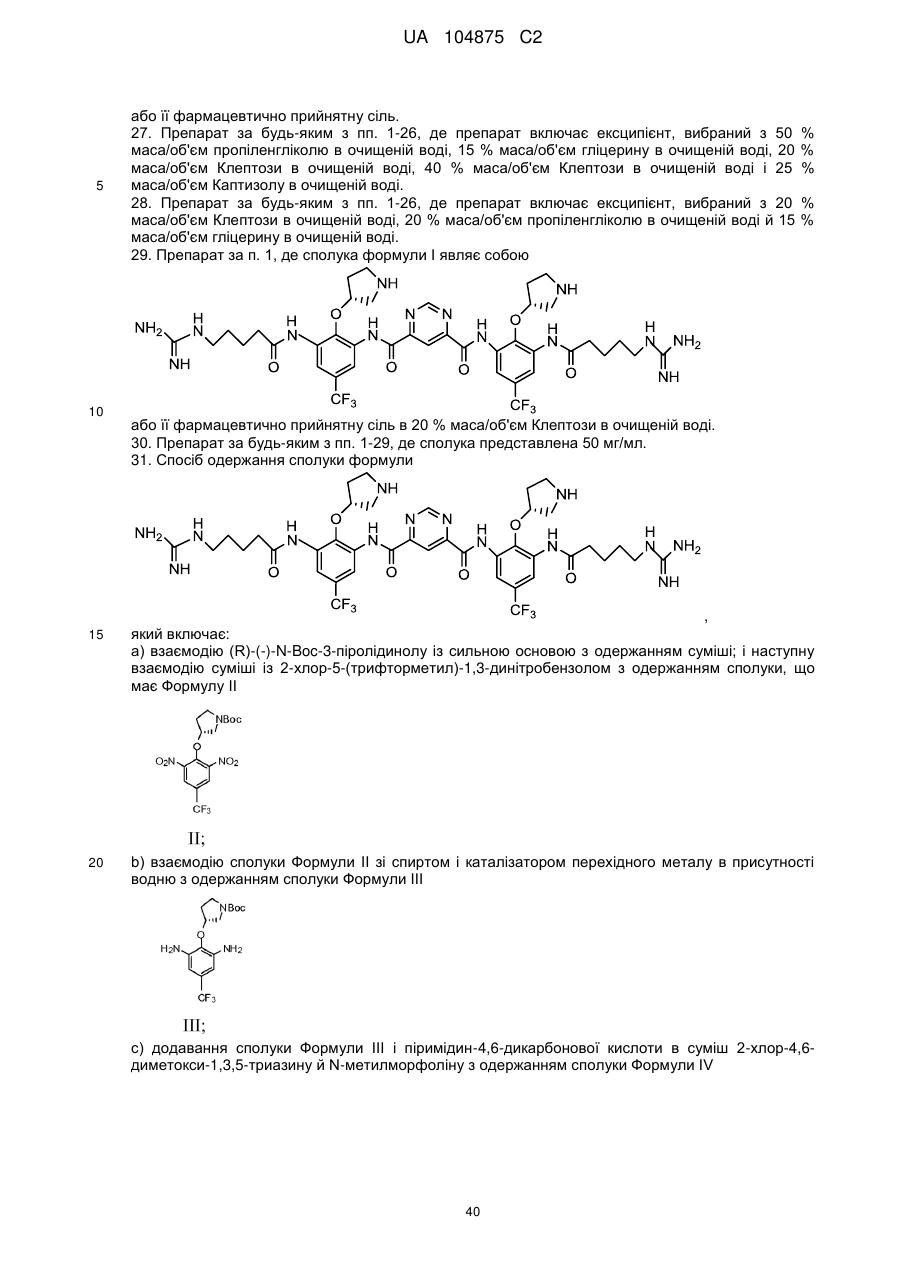
b) взаємодію сполуки Формули II зі спиртом і каталізатором перехідного металу в присутності водню з одержанням сполуки Формули III
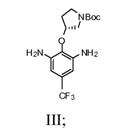
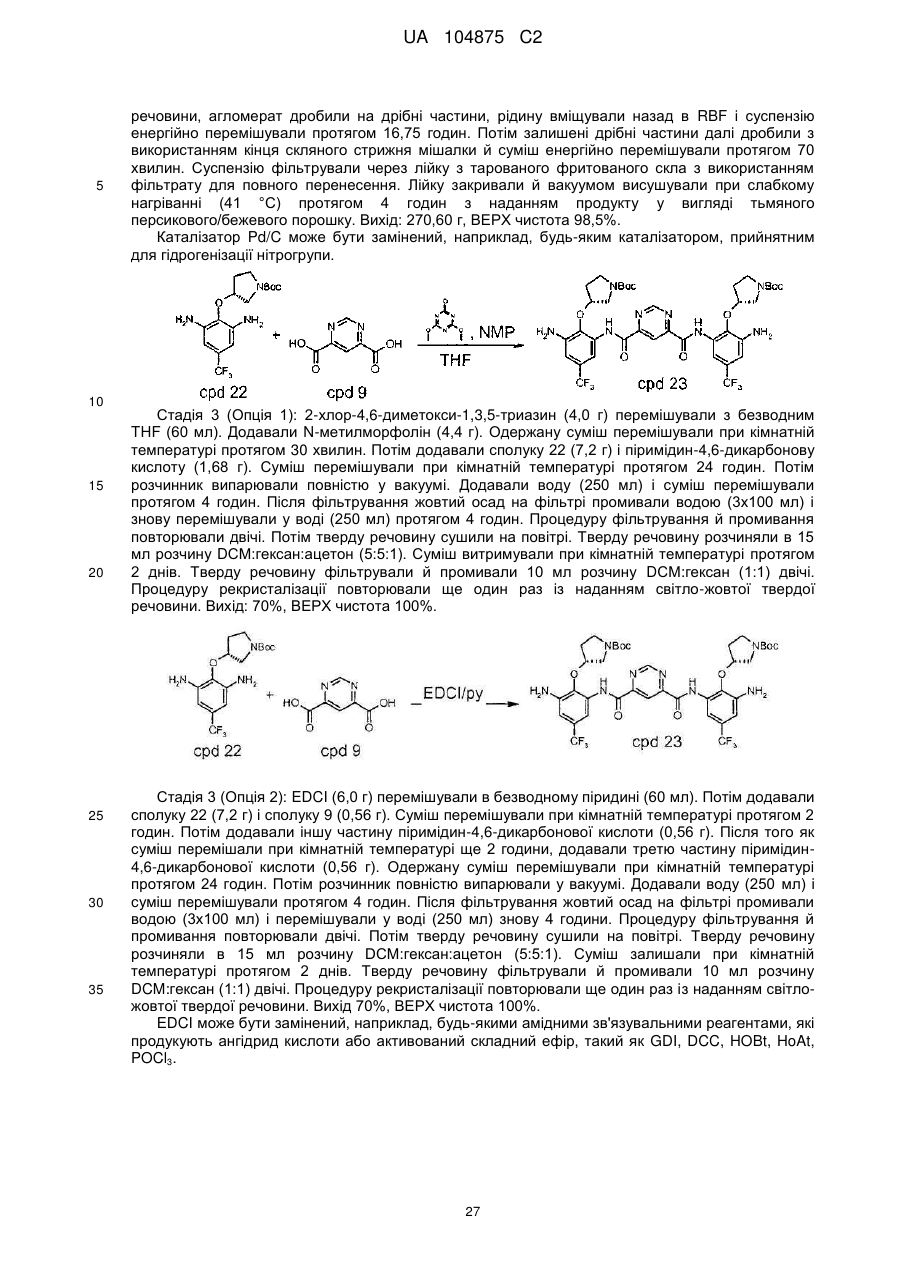
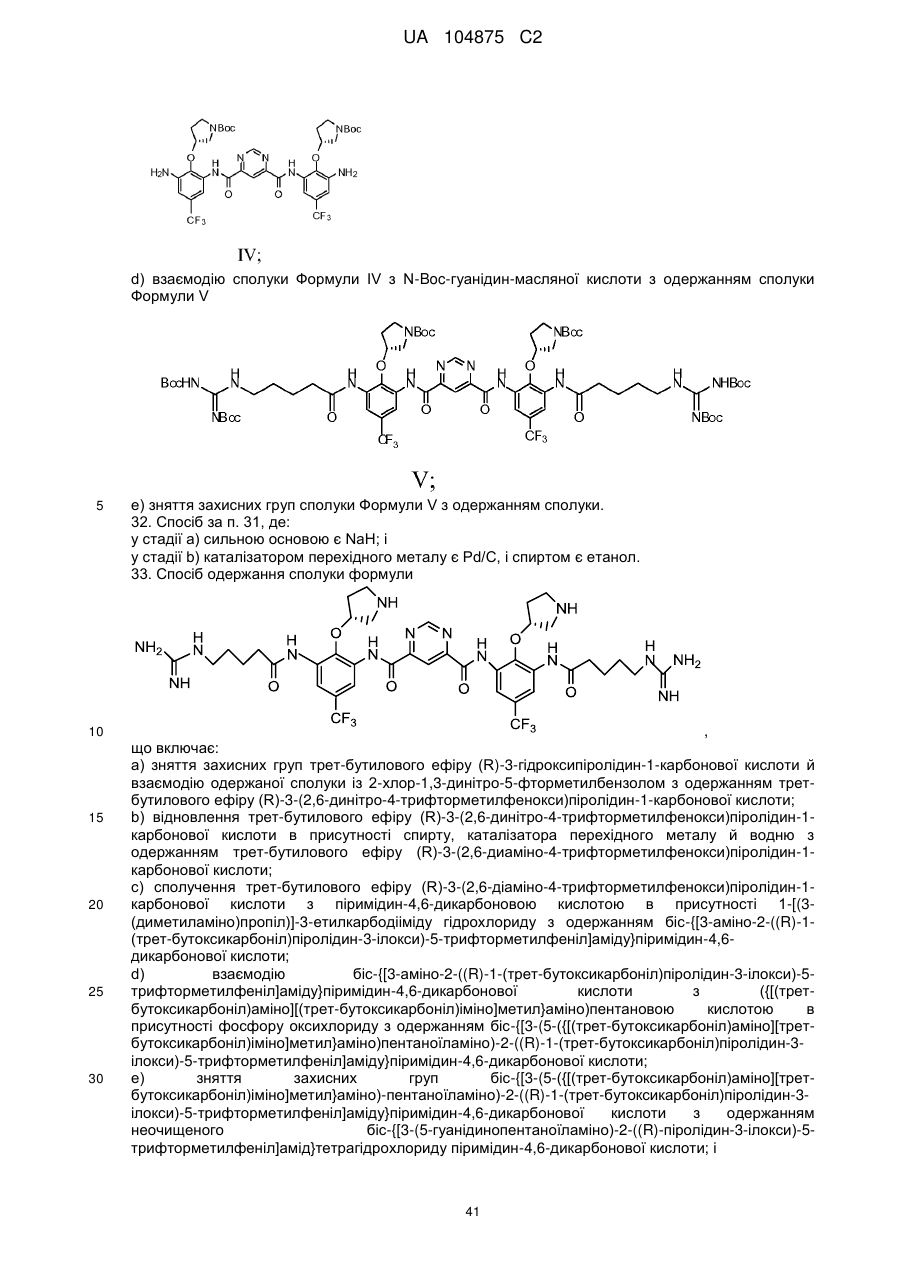
с) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш 2-хлор-4,6-диметокси-1,3,5-триазину й N-метилморфоліну з одержанням сполуки Формули IV
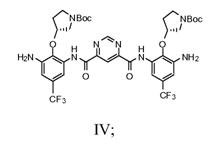
d) взаємодію сполуки Формули IV з N-Boc-гуанідин-масляної кислоти з одержанням сполуки Формули V
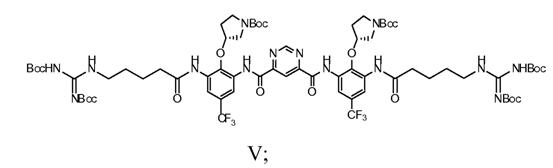
е) зняття захисних груп сполуки Формули V з одержанням сполуки.
32. Спосіб за п. 31, де:
у стадії а) сильною основою є NaН; і
у стадії b) каталізатором перехідного металу є Pd/C, і спиртом є етанол.
33. Спосіб одержання сполуки формули
 ,
,
що включає:
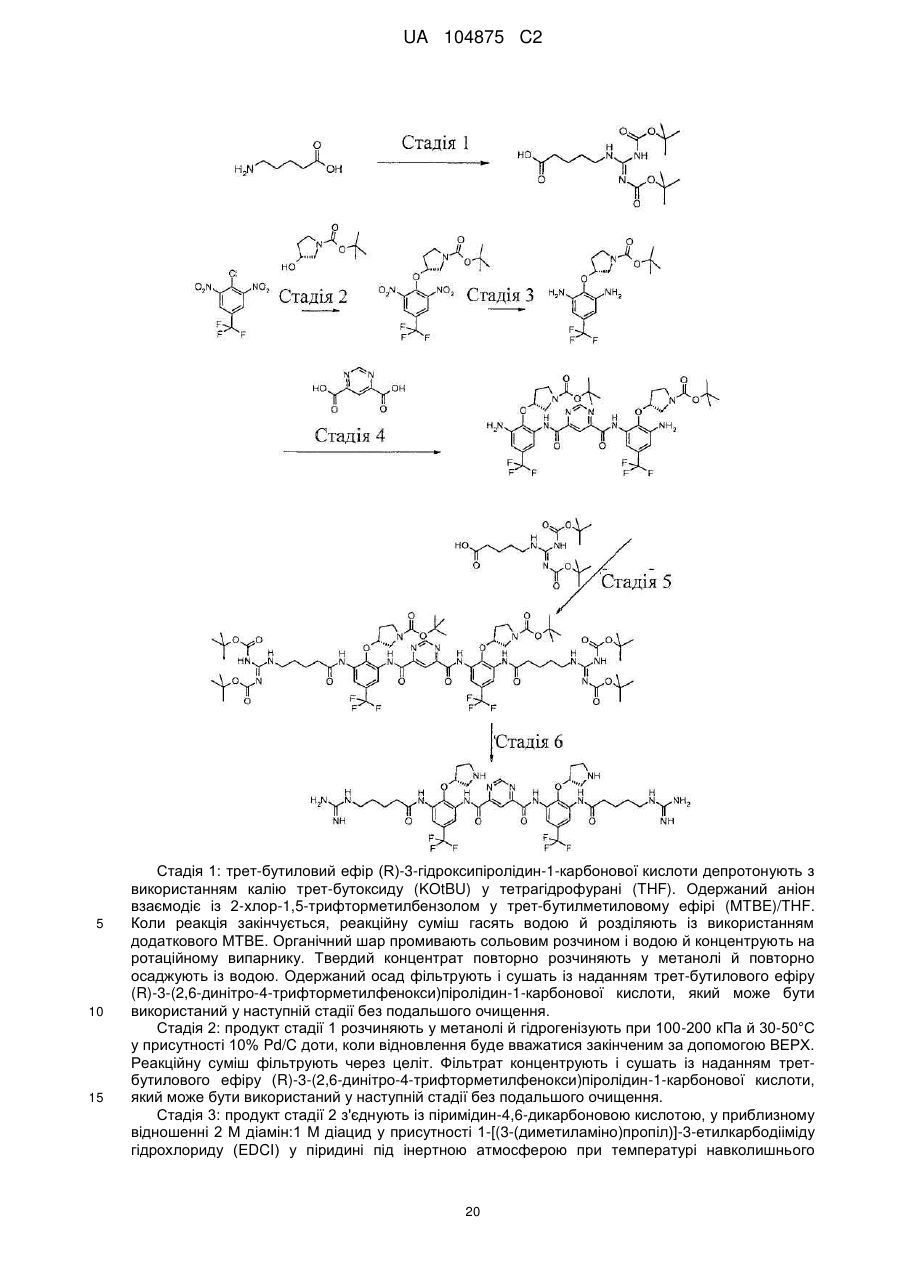
а) зняття захисних груп трет-бутилового ефіру (R)-3-гідроксипіролідин-1-карбонової кислоти й взаємодію одержаної сполуки із 2-хлор-1,3-динітро-5-фторметилбензолом з одержанням трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1-карбонової кислоти;
b) відновлення трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1-карбонової кислоти в присутності спирту, каталізатора перехідного металу й водню з одержанням трет-бутилового ефіру (R)-3-(2,6-диаміно-4-трифторметилфенокси)піролідин-1-карбонової кислоти;
c) сполучення трет-бутилового ефіру (R)-3-(2,6-діаміно-4-трифторметилфенокси)піролідин-1-карбонової кислоти з піримідин-4,6-дикарбоновою кислотою в присутності 1-[(3-(диметиламіно)пропіл)]-3-етилкарбодііміду гідрохлориду з одержанням біс-{[3-аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5-трифторметилфеніл]аміду}піримідин-4,6-дикарбонової кислоти;
d) взаємодію біс-{[3-аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5-трифторметилфеніл]аміду}піримідин-4,6-дикарбонової кислоти з ({[(трет-бутоксикарбоніл)аміно][(трет-бутоксикарбоніл)іміно]метил}аміно)пентановою кислотою в присутності фосфору оксихлориду з одержанням біс-{[3-(5-({[(трет-бутоксикарбоніл)аміно][трет-бутоксикарбоніл)іміно]метил}аміно)пентаноїламіно)-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5-трифторметилфеніл]аміду}піримідин-4,6-дикарбонової кислоти;
e) зняття захисних груп біс-{[3-(5-({[(трет-бутоксикарбоніл)аміно][трет-бутоксикарбоніл)іміно]метил}аміно)-пентаноїламіно)-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5-трифторметилфеніл]аміду}піримідин-4,6-дикарбонової кислоти з одержанням неочищеного біс-{[3-(5-гуанідинопентаноїламіно)-2-((R)-піролідин-3-ілокси)-5-трифторметилфеніл]амід}тетрагідрохлориду піримідин-4,6-дикарбонової кислоти; і
f) очищення неочищеного біс-{[3-(5-гуанідинопентаноїламіно)-2-((R)-піролідин-3-ілокси)-5-трифторметилфеніл]амід}тетрагідрохлориду піримідин-4,6-дикарбонової кислоти за допомогою хроматографії зі зворотною фазою.
34. Спосіб одержання сполуки формули
 ,
,
що включає:
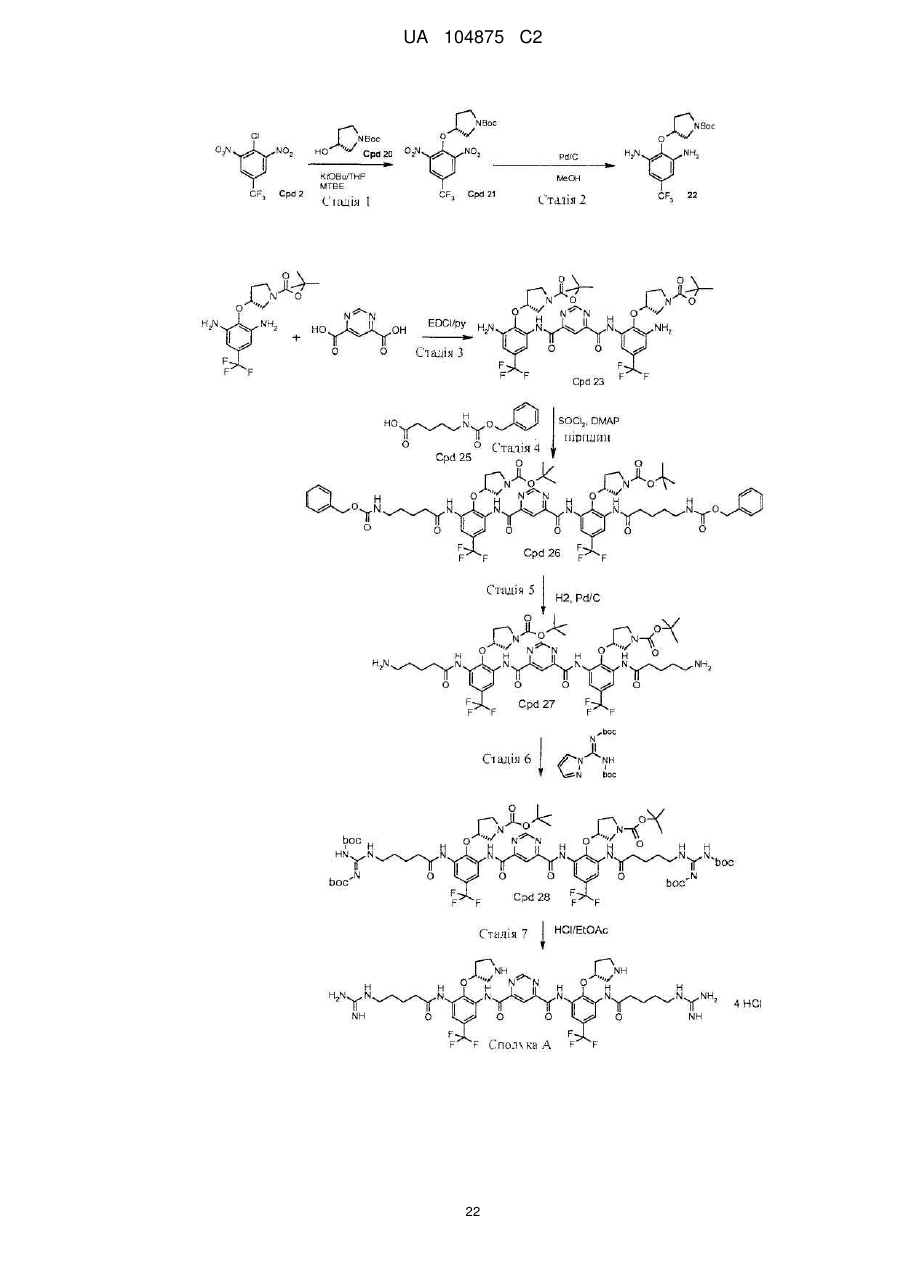
а) зняття захисних груп трет-бутилового ефіру (R)-3-гідроксипіролідин-1-карбонової кислоти й наступну взаємодію одержаної сполуки із 2-хлор-1,3-динітро-5-трифторметилбензолом з одержанням трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1-карбонової кислоти;
b) відновлення трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1-карбонової кислоти в присутності спирту, каталізатора перехідного металу й водню з одержанням трет-бутилового ефіру (R)-3-(2,6-діаміно-4-трифторметилфенокси)піролідин-1-карбонової кислоти;
c) сполучення трет-бутилового ефіру (R)-3-(2,6-діаміно-4-трифторметилфенокси)піролідин-1-карбонової кислоти з піримідин-4,6-дикарбоновою кислотою в присутності 1-[(3-(диметиламіно)пропіл)]-3-етилкарбодііміду гідрохлориду з одержанням біс-{[3-аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5-трифторметилфеніл]аміду}піримідин-4,6-дикарбонової кислоти;
d) взаємодію біс-{[3-аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5-трифторметилфеніл]аміду}піримідин-4,6-дикарбонової кислоти з N-Cbz кислотою в присутності тіонілу хлориду;
e) відновлення одержаної сполуки d) у присутності спирту, каталізатора перехідного металу й водню;
f) взаємодію одержаної сполуки e) з ди-Boc-піразолом;
g) зняття захисних груп одержаної сполуки f) з одержанням сполуки.
35. Спосіб одержання фармацевтично прийнятної солі сполуки
 ,
,
який включає:
а) взаємодію (R)-(-)-N-Boc-3-піролідинолу із сильною основою з одержанням суміші; наступну взаємодію суміші із 2-хлор-5-(трифторметил)-1,3-динітробензолом з одержанням сполуки, що має Формулу II
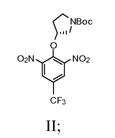
b) взаємодію сполуки Формули II зі спиртом і каталізатором перехідного металу в присутності водню з одержанням сполуки Формули III
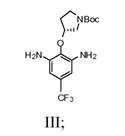
c1) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш 2-хлор-4,6-диметокси-1,3,5-триазину й N-метилморфоліну з одержанням сполуки Формули IV
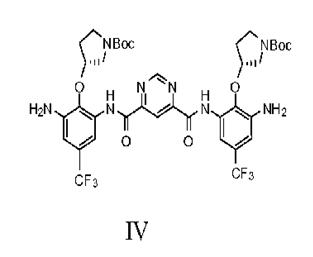 , або
, або
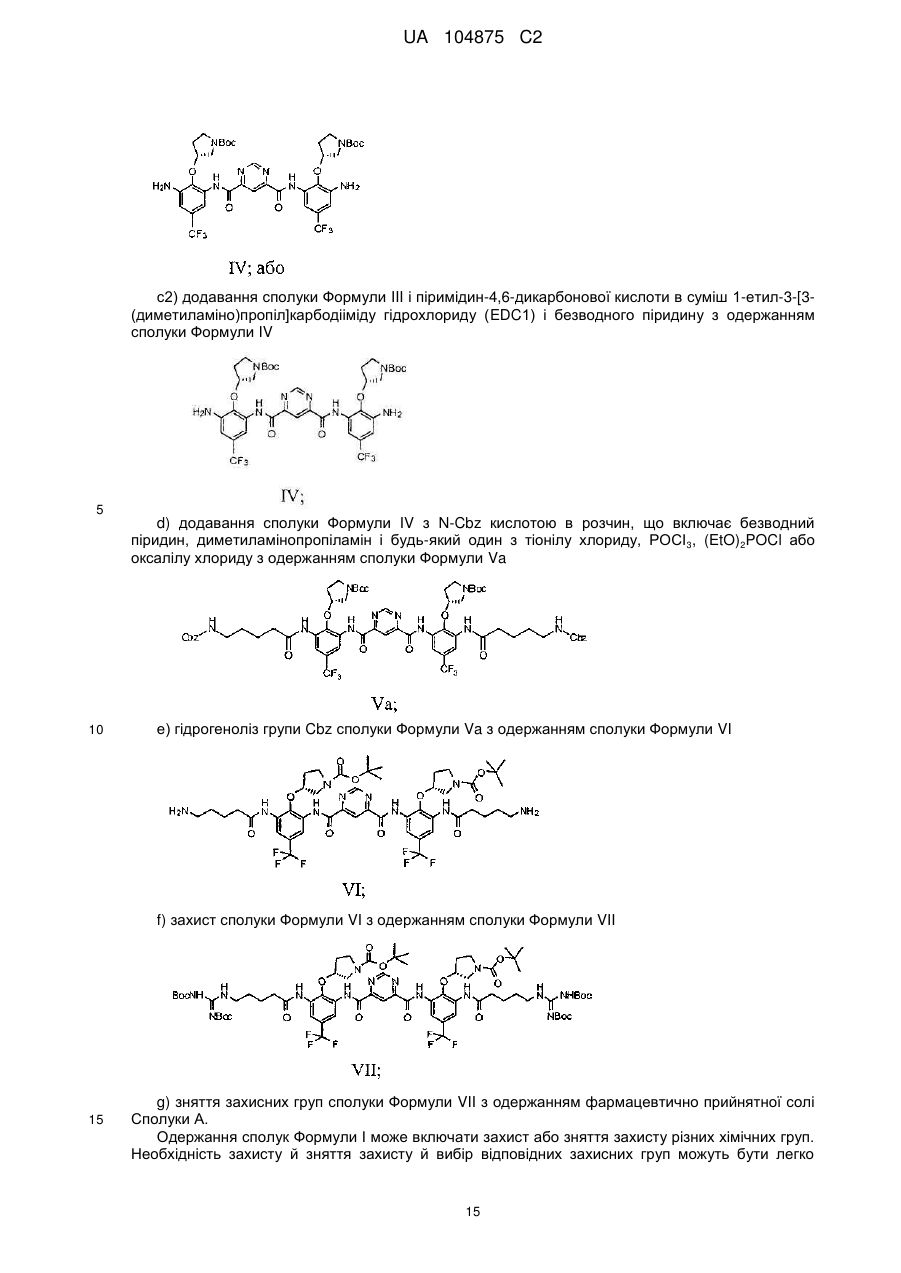
c2) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш 1-етил-3-[3-(диметиламіно)пропіл]карбодііміду гідрохлориду (EDC1) і безводного піридину з одержанням сполуки Формули IV
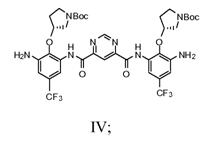
d) додавання сполуки Формули IV з N-Cbz кислотою в розчин, що включає безводний піридин, диметиламінопропіламін і будь-який один з тіонілу хлориду, POCl3, (EtO)2POCl або оксалілу хлориду з одержанням сполуки Формули Va
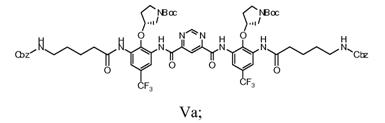
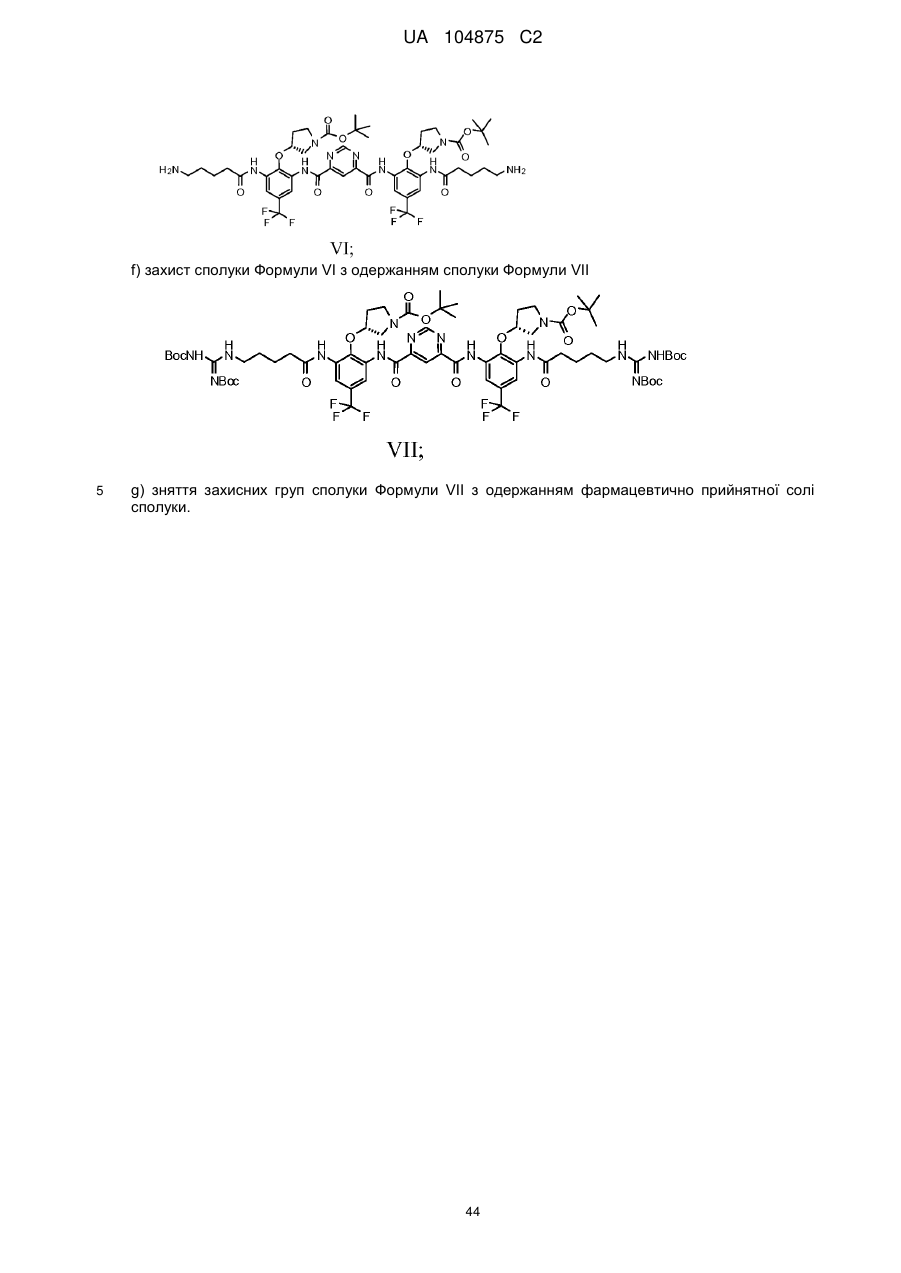
e) гідрогеноліз групи Cbz сполуки Формули Va з одержанням сполуки Формули VI
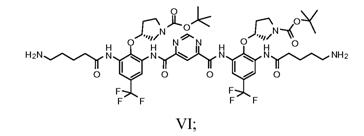
f) захист сполуки Формули VI з одержанням сполуки Формули VII
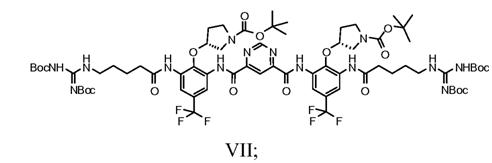
g) зняття захисних груп сполуки Формули VII з одержанням фармацевтично прийнятної солі сполуки.
Текст
Реферат: Даний винахід стосується препарату на основі ариламідних сполук загальної формули І й способів їх одержання. (І) UA 104875 C2 (12) UA 104875 C2 UA 104875 C2 5 10 15 20 25 30 35 40 45 50 Галузь техніки, якої стосується винахід Даний винахід направлений, зокрема, на ариламідні сполуки й способи їх одержання та застосування. Попередній рівень техніки Протимікробні пептиди (AMP) є першою лінією захисту проти мікробів для багатьох видів. AMP зазвичай являють собою маленькі (12-80 амінокислот) катіонні амфіфіли. Існує два типи AMP, що включають рибосомно та нерибосомно синтезовані пептиди. Було ідентифіковано понад 700 AMP і вони мають зазвичай α-спіраль (магаїнін і секропін) або збагачені дисульфідом β-складчасті шари (бактенецин і дефензин). Хоча пептиди складені з множини різних послідовностей, їх фізіологічні властивості найвищою мірою подібні. Вони приймають амфіфільну структуру з позитивно зарядженими групами, ізольованими на одній стороні вторинної структури, і гідрофобними групами на протилежній поверхні. У ссавців пептиди виробляються й секретуються в шкірі, на слизових поверхнях і в нейтрофілах і діють локально у відповідь на інфекцію. Існують загальні фізико-хімічні властивості, які переважно відповідають за біологічну активність цих пептидів. Деякі протимікробні активності білків імунного захисту були пов'язані із прямими цитотоксичними діями й модуляцією уродженої імунної системи. Передбачається, що їх прямі протимікробні активності включають як мембранні, так і немембранні ефекти. Протимікробні пептиди залишаються ефективним засобом захисту від бактеріальної інфекції протягом часу еволюції, вказуючи на те, що їх механізм дії перешкоджає бактеріальним відповідям, які призводять до резистентності до токсичних речовин. Це припущення підтримується прямими експериментальними даними, які показують, що відсутність значущої резистентності до дії протимікробних пептидів спостерігається після багаторазових серійних пасажів бактерій у присутності сублетальних концентрацій пептидів. Існує гостра потреба в розробці нових протимікробних засобів, які атакують нові мішені, вислизаючи від продуктів резистентності, які обмежують застосовність багатьох антибіотиків. Крім того, ці нові засоби повинні проявляти свою протимікробну активність через механізми, які роблять опір бактерій не ефективним. Були розроблені серії непептидних аналогів, які мають множину переваг над пептидами через їх маленький розмір, які збільшують стабільність і поліпшують розподіл у тканинах, і мають можливість тонко регулювати їх фізичні властивості для оптимізації ефективності й безпеки. Було знайдено, що серії ариламідних сполук, які імітують структурні властивості протимікробних пептидів, виявляють ефективні протимікробні активності й широкі індекси вибірковості проти клітин ссавців. Суть винаходу Даний винахід надає сполуки Формули І де: кожний А являє собою незалежно -С=О, -C=S або -СН2; кожний D являє собою 1 незалежно О або S; кожний R являє собою незалежно водень, С1-3алкіл, С1-3алкокси, гало або 2 гало С1-3залкіл; кожний R являє собою незалежно водень, С1-3алкіл, С1-3алкокси, гало або 3 галоС1-3алкіл; кожний R являє собою незалежно водень, С1-4алкіл, С1-4алкокси, гало або галоС14 4алкіл; і кожний R являє собою незалежно водень, С1-3залкіл, С1-3алкокси, гало або галоС 13алкіл; або їх фармацевтично прийнятну сіль. У деяких варіантах здійснення винаходу кожний А являє собою -С=О. У деяких варіантах здійснення винаходу кожний D являє собою О. 1 У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало або галоС1-3алкіл. У деяких варіантах здійснення винаходу кожний 1 R являє собою незалежно водень, метил, метокси, гало або гало С 1-3алкіл. У деяких варіантах 1 здійснення винаходу кожний R являє собою незалежно водень, метил або метокси. У деяких 1 варіантах здійснення винаходу кожний R являє собою водень. 2 У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало або галоС1-3алкіл. У деяких варіантах здійснення винаходу кожний 1 UA 104875 C2 2 5 10 15 20 25 30 35 40 45 R являє собою незалежно водень, метил, метокси або гало. У деяких варіантах здійснення 2 винаходу кожний R являє собою водень. 3 У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало або гало С1-3залкіл. У деяких варіантах здійснення винаходу кожний 3 R являє собою незалежно метил, метокси, гало або гало С 1-3залкіл. У деяких варіантах 3 здійснення винаходу кожний R являє собою незалежно гало або галоС1-3алкіл. У деяких 3 варіантах здійснення винаходу кожний R являє собою незалежно галоС1-3алкіл. У деяких 3 варіантах здійснення винаходу кожний R являє собою трифторметил. 4 У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, 4 етил, метокси, етокси або галoС1-3алкіл. У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, метокси, гало або галоС 1-3алкіл. У деяких варіантах 4 здійснення винаходу кожний R являє собою незалежно водень, метил, метокси або гало. У 4 деяких варіантах здійснення винаходу кожний R являє собою водень. У деяких варіантах здійснення винаходу кожний А являє собою незалежно -С=О, -C=S або 1 СН2; кожний D являє собою незалежно О або S; кожний R являє собою незалежно водень, 2 метил, етил, метокси, етокси, гало, галометил або галоетил; кожний R являє собою незалежно 3 водень, метил, метокси, гало або галометил; кожний R являє собою незалежно С1-3алкіл, С14 3алкокси, гало або галоалкіл; і кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало, галометил або галоетил. У деяких варіантах здійснення винаходу кожний А являє собою незалежно -С=О або -C=S: 1 кожний D являє собою незалежно О або S; кожний R являє собою незалежно водень, метил, 2 метокси, гало або галометил; кожний R являє собою незалежно водень, гало або галометил; 3 кожний R являє собою незалежно метил, етил, метокси, етокси, гало, галометил або галоетил; 4 і кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало, галометил або галоетил. У деяких варіантах здійснення винаходу кожний А являє собою –С=O; кожний D являє 1 2 собою О; кожний R являє собою незалежно водень, гало або галометил; кожний R являє 3 собою незалежно водень або гало; кожний R являє собою незалежно метил, метокси, гало або 4 галометил; і кожний R являє собою незалежно водень, метил, метокси, гало або галометил. У деяких варіантах здійснення винаходу кожний А являє собою -С=О; кожний D являє собою 1 2 О; кожний R являє собою незалежно водень або гало; кожний R являє собою незалежно 3 4 водень або гало; кожний R являє собою незалежно метил, гало або галометил; і кожний R являє собою незалежно водень, метил, гало або галометил. У деяких варіантах здійснення винаходу кожний А являє собою -С=О; кожний D являє собою 1 2 О; кожний R являє собою незалежно водень або гало; кожний R являє собою незалежно 3 4 водень або гало; кожний R являє собою незалежно гало або галометил; і кожний R являє собою незалежно водень або гало. У деяких варіантах здійснення винаходу кожний А являє собою -С=О; кожний D являє собою 1 2 О; кожний R являє собою незалежно водень або гало; кожний R являє собою незалежно 3 4 водень або гало; кожний R являє собою незалежно метил, гало або галометил; і кожний R являє собою незалежно водень, метил, гало або галометил. У деяких варіантах здійснення винаходу сполука являє собою або її фармацевтично прийнятну сіль. Даний винахід також надає фармацевтичні композиції, що включають одну або декілька сполук, описаних вище, або сіль будь-якої зі сполук, описаних вище, і фармацевтично прийнятний носій. Даний винахід також надає препарати, що включають одну або декілька сполук, описаних вище, де препарат включає фізіологічний розчин, воду, розчин циклодекстрину або 2 UA 104875 C2 5 10 15 20 забуферений розчин при рН 3-9. У деяких варіантах здійснення винаходу препарат являє собою пероральний склад, який не абсорбується. У деяких варіантах здійснення винаходу препарат включає ексципієнт, вибраний з очищеної води, пропіленгліколю, поліетиленгліколю 400 (PEG 400), гліцерину, DMA, етанолу, бензилового спирту, лимонної кислоти/натрію цитрату (рН 3), лимонної кислоти/натрію цитрату (рН 5), трис(гідроксиметил)аміно метан НСl (рН 7,0), 0,9% фізіологічного розчину і 1,2% фізіологічного розчину або будь-якої їх комбінації. У деяких варіантах здійснення винаходу склад включає ексципієнт, вибраний із пропіленгліколю, очищеної води й гліцерину. У деяких варіантах здійснення винаходу препарат включає ексципієнт, вибраний з 20% маса/об'єм пропіленгліколю у фізіологічному розчині, 30% маса/об'єм пропіленгліколю у фізіологічному розчині, 40% маса/об'єм пропіленгліколю у фізіологічному розчині, 50% маса/об'єм пропіленгліколю у фізіологічному розчині, 15% маса/об'єм пропіленгліколю в очищеній воді, 30% маса/об'єм пропіленгліколю в очищеній воді, 50% пропіленгліколю в очищеній воді, 30% маса/об'єм пропіленгліколю й 5 маса/об'єм етанолу в очищеній воді, 15% маса/об'єм гліцерину в очищеній воді, 30% маса/об'єм гліцерину в очищеній воді, 50% маса/об'єм гліцерину в очищеній воді, 20% маса/об'єм Клептози в очищеній воді, 40% маса/об'єм Клептози в очищеній воді й 25% маса/об'єм Каптизолу в очищеній воді. Даний винахід також надає способи одержання Сполуки А, що включають: a) взаємодію (R)-(-)-N-Вос-3-піролідинолу із сильною основою з одержанням суміші; далі взаємодію суміші із хлор-5-(трифторметил)-1,3-динітробензолом з одержанням сполуки, що має Формулу II b) взаємодію сполуки Формули II зі спиртом і каталізатором перехідного металу в присутності водню з одержанням сполуки Формули III 25 c) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш 2-хлор-4,6диметокси-1,3,5-триазину й N-метилморфоліну з одержанням сполуки Формули IV d) взаємодію сполуки Формули IV з N-Вос-гуанідин масляною кислотою з одержанням сполуки Формули V 3 UA 104875 C2 5 10 15 20 25 30 35 40 45 50 e) зняття захисних груп сполуки Формули V з одержанням Сполуки А. У деяких варіантах здійснення винаходу в а) сильна основа являє собою NaH; і в b) каталізатор перехідного металу являє собою Pd/C, і спирт являє собою етанол. Даний винахід також надає додаткові способи одержання Сполуки А, що включають: a) зняття захисних груп трет-бутилового ефіру (R)-3-гідроксипіролідин-1-карбонової кислоти й взаємодію одержаної сполуки із 2-хлор-1,3-динітро-5-трифторметилбензолом з одержанням трет-бутилового ефіру R)-3-(2,6-діаміно-4-трифторметилфенокси)піролідин-1-карбонової кислоти; b) відновлення трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин1-карбонової кислоти в присутності спирту, каталізатора перехідного металу й водню з одержанням трет-бутилового ефіру (R)-3-(2,4-трифторметилфенокси)піролідин-1-карбонової кислоти; c) поєднання трет-бутилового ефіру (R)-3-(2,6-діаміно-4-трифторметилфенокси)піролідин-1карбонової кислоти з піримідин-4,6-дикарбоновою кислотою в присутності 1-[(3(диметиламіно)пропіл)]-3-етилкарбодііміду гідрохлориду з одержанням біс-{[3-аміно-2-((R)-1(трет-бутоксикарбоніл)піролідин-3-ілокси)-трифторметил-феніл]аміду}піримідин-4,6дикарбонової кислоти; d) взаємодію біс-{[3-аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-трифторметилфеніл]аміду}піримідин-4,6-дикарбонової кислоти з ({[(трет-бутоксикарбоніл)аміно][(третбутоксикарбоніл)іміно]метил}аміно) пентановою кислотою в присутності фосфору оксихлориду з одержанням біс-{[3-(5-({[(трет-бутоксикарбоніл)аміно][тpeтбутоксикарбоніл)іміно]метил}аміно)пентаноїламіно)-2-((R)-1-(трет-бутоксикарбоніл-піролідин-3ілокси)-трифторметил-феніл]аміду}піримідин-4,6-дикарбонової кислоти; е) зняття захисних груп біс-{[3-(5-({[(трет-бутоксикарбоніл)аміно][третбутоксикарбоніл)іміно]метил}аміно)пентаноїламіно)-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3ілокси)-трифторметил-феніл]аміду} піримідин-4,6-дикарбонової кислоти з одержанням неочищеного біс-{[3-(5-гуанідино-пентаноїламіно)-2-((R)-піролідин-3-ілокси)-5-трифторметилфеніл]амід}тетрагідрохлориду піримідин-4,6-дикарбонової кислоти; і f) очищення неочищеного біс-{[3-(5-гуанідино-пентаноїламіно)-2-((R)-піролідин-3-ілокси)-5трифторметил-феніл]амід}тетрагідрохлориду піримідин-4,6-дикарбонової кислоти за допомогою, наприклад, хроматографії зі зворотною фазою. Даний винахід також надає інші додаткові способи одержання Сполуки А, що включають: а) зняття захисних груп трет-бутипового ефіру (R)-3-гідроксипіролідин-1-карбонової кислоти й далі взаємодію одержаної сполуки із хлор-1,3-динітро-5-трифторметилбензолом з одержанням трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1карбонової кислоти; b) відновлення трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин1-карбонової кислоти в присутності спирту, каталізатора перехідного металу й водню з одержанням трет-бутилового ефіру (R)-3-(2,6-діаміно-4-трифторметилфенокси)піролідин-1карбонової кислоти; c) поєднання трет-бутилового ефіру (R)-3-(2,6-діаміно-4-трифторметилфенокси)-піролідин-1карбонової кислоти з піримідин-4,6-дикарбоновою кислотою в присутності 1-[(3(диметиламіно)пропіл)]-3-етилкарбодііміду гідрохлориду з одержанням біс-{[3-аміно-2-((R)-1(ягрет-бутоксикарбоніл)піролідин-3-ілокси)5-трифторметил-феніл]аміду} піримідин-4,6дикарбонової кислоти; d) взаємодію біс-{[3-аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5трифторметил-феніл]аміду} піримідин-4,6-дикарбонової кислоти з N-Cbz кислотою в присутності тіонілу хлориду; е) відновлення одержаної сполуки d) у присутності спирту, каталізатора перехідного металу й водню; 4 UA 104875 C2 5 10 f) взаємодію одержаної сполуки е) з ди-Вос піразолом; і g) зняття захисних груп одержаної сполуки f) з одержанням Сполуки А. Даний винахід також надає способи одержання фармацевтично прийнятної солі Сполуки А, що включають: a) взаємодію (R)-(-)-N-Вос-3-піролідинолу із сильною основою з одержанням суміші; далі взаємодію суміші із 2-хлор-5-(трифторметил)-1,3-динітробензолом з одержанням сполуки, що має Формулу II b) взаємодію сполуки Формули II зі спиртом і каталізатором перехідного металу в присутності водню з одержанням сполуки Формули III С1) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш 2-хлор-4,6диметокси-1,3,5-триазину і N-метилморфоліну з одержанням сполуки Формули IV 15 20 с2) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш етил-3-[3(диметиламіно)пропіл]карбодііміду гідрохлориду (EDCl) і безводного піридину з одержанням сполуки Формули IV d) додавання сполуки Формули IV з N-Cbz кислотою в розчин, що включає безводний піридин, диметиламінопропіламін і будь-який один з тіонілу хлориду, РОСІз, (EtO)2POCl або оксалілу хлориду з одержанням сполуки Формули Va 5 UA 104875 C2 e) гідрогеноліз групи Cbz сполуки Формули Va з одержанням сполуки Формули VI f) захист сполуки Формули VI з одержанням сполуки Формули VII 5 10 15 20 25 30 35 g) зняття захисних груп сполуки Формули VII з одержанням фармацевтично прийнятної солі Сполуки А. Даний винахід також надає способи інгібування росту мікроба, що включають контактування мікроба з будь-якою зі сполук, описаних вище, або її фармацевтично прийнятними солями. Даний винахід також надає способи лікування ссавця, що страждає мікробною інфекцією, які включають введення ссавцеві, що потребує цього, протимікробної ефективної кількості будьякої зі сполук, описаних вище, або її фармацевтично прийнятних солей. У деяких варіантах здійснення винаходу мікроб або мікробна інфекція являють собою грамнегативний аероб, грампозитивний аероб, грамнегативний анаероб, грампозитивний анаероб, мікобактерію або дріжджі. У деяких варіантах здійснення винаходу грамнегативний аероб являє собою Escherichia coli, Citrobacter freundii, Citrobacter diverus, Citrobacter koseri, Enterobacter cloacae, Enterobacter faecalis, Klebsiella pneumonia, Klebsiella oxytoca, Morganella morganii, Providencia stuartii, Proteus vulgaris, Proteus mirabilis, Serratia marcescens, Acinetobacter haemolyticus, Acinetobacter junii, Acinetobacter lwoffii, Haemophilus influenzae, Stenotrophomonas maltophilia або Pseudomonas aeruginosa. У деяких варіантах здійснення винаходу грампозитивний аероб являє собою Enterococcus faecalis, Enterococcus faecium, Mycobacterium tuberculosis, Staphylococcus aureus, Staphylococcus pneumoniae, Staphylococcus epidermidis, Staphylococcus saprophyticus, Staphylococcus colmii, Staphylococcus sciuri, Staphylococcus warneri, Streptococcus agalactiae, Streptococcus pyogenes, Streptococcus anginosus, Streptococcus mitis або Streptococcus oralis. У деяких варіантах здійснення винаходу-грамнегативний анаероб являє собою Bacteroides fragilis. У деяких варіантах здійснення винаходу грампозитивний анаероб являє собою Clostridium difficile або Clostridium perfringens. У деяких варіантах здійснення винаходу мікобактерія являє собою Mycobacterium tuberculosis, Mycobacterium bovis, Mycobacterium africanum, Mycobacterium canetti або Mycobacterium microti. У деяких варіантах здійснення винаходу дріжджі являють собою Candida albicans або Candida krusei. Даний винахід також надає будь-яку зі сполук, описаних вище, для лікування мікробної інфекції. Даний винахід також надає будь-яку зі сполук, описаних вище, або їх фармацевтично прийнятних солей для використання при виготовленні лікарського засобу для лікування мікробної інфекції. 6 UA 104875 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід також надає використання будь-якої зі сполук, описаних вище, або їх фармацевтично прийнятних солей для інгібування росту мікроба. Даний винахід також надає використання будь-якої зі сполук, описаних вище, або їх фармацевтично прийнятних солей для лікування мікробної інфекції ссавця. Короткий опис креслень На фігурі 1А і фігурі 1В представлені результати дослідження час-ерадикація Сполуки А проти S. aureus ATCC27660 (фігура 1В являє собою розгорнутий вид Фігури 1А). На фігурі 2 показана асоціація пасажу S. aureus з норфлоксацином зі значним підвищенням значень МІС [мінімальна інгібувальна концентрація] при пасажі 3 (4 подвійні розведення) для MSSA і MRSА. На фігурі 3 показана ефективність Сполуки А проти S. aureus на мишачій моделі навантаження на стегнову кістку. На фігурі 4 показана ефективність Сполуки А у порівнянні з ванкоміцином проти S. aureus на щурячій моделі навантаження на стегнову кістку. На фігурі 5 показана ефективність Сполуки А проти S. aureus на мишачій моделі сепсису. Опис варіантів здійснення винаходу Як використано в даному описі, термін «приблизно» означає ±5% описаного значення. Наприклад, приблизно 100 означає від 95 до 105. Як використано в даному описі, терміни «С1-3алкіл», «С1-4алкіл» і «(СН2)1-7» означають насичені, моновалентні нерозгалужені або розгалужені вуглеводневі ланцюги, що містять від 1 до 3 вуглеців, від 1 до 4 вуглеців і від 1 до 7 вуглеців, відповідно. Приклади алкільних груп включають, але не обмежуючись ними, (С1-С7)алкільні групи, такі як метил, етил, пропіл, ізопропіл, 2-метил-1-пропіл, 2-метил-2-пропіл, 2-метил-1-бутил, 3-метил-1-бутил, 2-метил-3бутил, 2-метил-1-пентил, 2,2-диметил-1 -пропіл, З-метил-1-пентил, 4-метил-1-пентил, 2-метил2-пентил, З-метил-2-пентил, 4-метил-2-пентил, 2,2-диметил-1-бутил, 3,3-диметил-1-бутил, 2етил-1-бутил, бутил, ізобутил, трет-бутил, пентил, ізопентил, неопентил, гексил і гептил. Алкільна група може бути незаміщеною або заміщена одним або двома прийнятними замісниками. Як використано в даному описі, терміни «С1-3алкокси» і «С1-4алкокси» означають -О-алкіл з алкілом, визначеним, як вказано вище. Алкокси група може бути незаміщеною або заміщена одним або двома прийнятними замісниками. Алкільний ланцюг алкоксигрупи містить від 1 до 3 або від 1 до 4 атомів вуглецю в довжину. Як використано в даному описі, термін «гало» означає галоген, такий як фтор, хлор, бром або йод. Як використано в даному описі, терміни «галоС1-3алкіл» і «галоСі„4алкіл» означають алкільні групи, як визначено вище, де один або декілька (тобто 1, 2, 3, 4, 5, 6, 7, 8, 9 або 10) воднів заміщуються на гало, як визначено вище. Як використано в даному описі, «ізольований» означає, що сполуки Формули І виділяються з інших компонентів або (а) природного джерела, такого як клітина, такого як бактеріальна культура, або (b) синтетичної органічної хімічної реакційної суміші, такої як використовувана в загальноприйнятих методиках, сполуки Формули І очищуються. Як використано в даному описі, термін «ссавець» означає гризуна (тобто миша, щур або морська свинка), мавпу, кішку, собаку, корову, коня, свиню або людину. У деяких варіантах здійснення винаходу ссавцем є людина. Як використано в даному описі, термін «мікроб» означає бактерії, гриби, найпростіші або вірус. Як використано в даному описі, фраза «фармацевтично прийнятна(і) сіль(і)» включає, але не обмежуючись ними, солі кислих або основних груп. Як використано в даному описі, термін «очищений» означає, що при ізолюванні ізолят містить щонайменше 90%, щонайменше 95%, щонайменше 98% або щонайменше 99% сполуки Формули І за масою ізоляту. Як використано в даному описі, фраза «прийнятний замісник» означає групу, яка не скасовує синтетичну або фармацевтичну цінність сполук Формули І або інтермедіатів, використовуваних для їх одержання. Приклади прийнятних замісників включають, але не обмежуючись ними: (С1-С4)алкіл, (С1-С4)алкеніл, (С1-С4)алкініл, (С1-С4)алкокси, -CN, -ОН, оксо, гало, -NO2, -CO2H, -NH2, -NH((C1-С4)алкіл), -N((С1-С4)алкіл)2, -СНО, -СО((С1-С4)алкіл) і -СО2((С1С4)алкіл). Фахівець у даній галузі може легко вибрати прийнятний замісник на основі стабільності й фармакологічної та синтетичної активності сполуки Формули І. Як використано в даному описі, фраза «протимікробна ефективна кількість» сполуки, що включає Формулу І, оцінюється протимікробною ефективністю сполуки. У деяких варіантах 7 UA 104875 C2 5 10 15 20 25 30 35 40 45 50 здійснення винаходу протимікробна ефективна кількість інгібує ріст певного мікроба на щонайменше 10%, на щонайменше 20%. на щонайменше 30%, на щонайменше 40%, на щонайменше 50%, на щонайменше 60%, на щонайменше 70%, на щонайменше 80%, на щонайменше 90% або на щонайменше 95%. У деяких варіантах здійснення винаходу протимікробна ефективна кількість також означає «терапевтично ефективну кількість», тим самим сполука знижує або усуває щонайменше один несприятливий ефект мікроба на ссавця. Даний винахід надає сполуки Формули І де: кожний А являє собою незалежно -С=О, -C=S або -СН2; кожний D являє собою незалежно О або S; 1 кожний R являє собою незалежно водень, С1-3алкіл, С1-3алкокси, гало або галоС1-3алкіл; 2 кожний R являє собою незалежно водень, С1-3алкіл, С1-3алкокси, гало або галоС1-3алкіл; 3 кожний R являє собою незалежно водень, С1-4алкіл, С1-4алкокси, гало або галоС1-4алкіл; і 4 кожний R являє собою незалежно водень, С1-3алкіл, С1-3алкокси, гало або галоС1-3алкіл; або їх фармацевтично прийнятну сіль. У деяких варіантах здійснення винаходу щонайменше один А являє собою -С=О. У деяких варіантах здійснення винаходу кожний А являє собою –C=О. У деяких варіантах здійснення винаходу щонайменше один D являє собою О. У деяких варіантах здійснення винаходу кожний D являє собою О. 1 У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало або галоС1-3алкіл. У деяких варіантах здійснення винаходу кожний 1 R являє собою незалежно водень, метил, метокси, гало або галоС1-3алкіл. У деяких варіантах 1 здійснення винаходу кожний R являє собою незалежно водень, метил абометокси. У деяких 1 варіантах здійснення винаходу щонайменше один R являє собою водень. У деяких варіантах 1 здійснення винаходу кожний R являє собою водень. 2 У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало або галоС1-3алкіл. У деяких варіантах здійснення винаходу кожний 2 R являє собою незалежно водень, метил, метокси або гало. У деяких варіантах здійснення 2 винаходу щонайменше один R являє собою водень. У деяких варіантах здійснення винаходу 2 кожний R являє собою водень. 3 У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало або галоС1-3алкіл. У деяких варіантах здійснення винаходу кожний 3 R являє собою незалежно метил, метокси, гало або галоС1-3алкіл. У деяких варіантах 3 здійснення винаходу кожний R являє собою незалежно гало або гало С 1-3алкіл. У деяких 3 варіантах здійснення винаходу кожний R являє собою незалежно галоС1-3алкіл. У деяких 3 варіантах здійснення винаходу щонайменше один R являє собою трифторметил. У деяких 3 варіантах здійснення винаходу кожний R являє собою трифторметил. 4 У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, 4 етил, метокси, етокси або галоС1-3алкіл. У деяких варіантах здійснення винаходу кожний R являє собою незалежно водень, метил, метокси, гало або галоС 1-3алкіл. У деяких варіантах 4 здійснення винаходу кожний R являє собою незалежно водень, метил, метокси або гало. У 4 деяких варіантах здійснення винаходу щонайменше один R являє собою водень. У деяких 4 варіантах здійснення винаходу кожний R являє собою водень. У деяких варіантах здійснення винаходу кожний А являє собою незалежно -С=О або -C=S; 1 кожний D являє собою незалежно О або S; кожний R являє собою незалежно водень, метил, 2 етил, метокси, етокси, гало, галометил або галоетил; кожний R являє собою незалежно 3 водень, метил, метокси. гало або галометил; кожний R являє собою незалежно С1-3алкіл, С14 3алкокси, гало або галоалкіл; і кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало, галометил або галоетил. У деяких варіантах здійснення винаходу кожний А являє собою незалежно -С=О або -C=S; 1 кожний D являє собою незалежно О або S; кожний R являє собою незалежно водень, метил, 8 UA 104875 C2 2 5 10 15 20 25 30 35 40 45 50 метокси, гало або галометил; кожний R являє собою незалежно водень, гало або галометил; 3 кожний R являє собою незалежно метил, етил, метокси, етокси, гало, галометил або галоетил; 4 і кожний R являє собою незалежно водень, метил, етил, метокси, етокси, гало, галометил або галоетил. У деяких варіантах здійснення винаходу кожний А являє собою -С=О; кожний D являє собою 1 2 О; кожний R являє собою незалежно водень, гало або галометил; кожний R являє собою 3 незалежно водень або гало; кожний R являє собою незалежно метил, метокси, гало або 4 галометил; і кожний R являє собою незалежно водень, метил, метокси, гало або галометил. У деяких варіантах здійснення винаходу кожний А являє собою -С=О; кожний D являє собою 1 2 О; кожний R являє собою незалежно водень або гало; кожний R являє собою незалежно 3 4 водень або гало; кожний R являє собою незалежно метил, гало або галометил; і кожний R являє собою незалежно водень, метил, гало або галометил. У деяких варіантах здійснення винаходу кожний А являє собою -С=О; кожний D являє собою 1 2 О; кожний R являє собою незалежно водень або гало; кожний R являє собою незалежно 3 4 водень або гало; кожний R являє собою незалежно гало або галометил; і кожний R являє собою незалежно водень або гало. У деяких варіантах здійснення винаходу кожний А являє собою -С=О; кожний D являє собою 1 2 О; кожний R являє собою незалежно водень або гало; кожний R являє собою незалежно 3 4 водень або гало; кожний R являє собою незалежно метил, гало або галометил; і кожний R являє собою незалежно водень, метил, гало або галометил. У деяких варіантах здійснення винаходу кожний А являє собою –С=O; кожний D являє 1 2 собою О; кожний R являє собою незалежно водень або гало; кожний R являє собою 3 4 незалежно водень або гало; кожний R являє собою незшіежно гало або галометил; і кожний R являє собою незалежно водень, метил, гало або галометил. У деяких варіантах здійснення винаходу сполука являє собою Сполуку А або її фармацевтично прийнятну сіль. Прийнятні приклади солей включають, наприклад, соляну кислоту й трифтороцтову кислоту. Сполуки Формули І можуть містити один або декілька хіральних центрів і/або подвійні зв'язки й тому існують як стереоізомери, такі як ізомери з подвійним зв'язком (тобто геометричні ізомери), енантіомери або діастереомери. Відповідно до винаходу хімічні структури представлені в даному описі, і тому Сполуки Формули І охоплюють усі відповідні енантіомери й стереоізомери сполуки, а саме, стереомерно правильну форму (наприклад, геометрично правильна, енантіомерно правильна або діастереомерно правильна) і енантіомерні або стереоізомерні суміші. Енантіомерні або стереоізомерні суміші можуть бути дозволені за своїми компонентними енантіомерами або стереоізомерами за допомогою добре відомих методів, таких як газова хроматографія з хіральною фазою, високоефективна рідинна хроматографія з хіральною фазою, кристалізація сполуки у вигляді комплексу хіральних солей або кристалізація сполуки в хіральному розчиннику. Енантіомери й стереоізомери можуть бути також одержані із стереомерно або енантіомерно чистих інтермедіатів, реагентів і каталізуватися за допомогою добре відомих методів асиметричного синтезу. Сполуки Формули І далі включають гідрати й сольвати. Сполуки, що містять амінну функцію, можуть також утворювати N-оксиди. У даному описі наводиться посилання на сполуку, яка містить амінну функцію, також включаючи N-оксид. У випадку, якщо сполука містить декілька амінних функцій, один або більше ніж один атом азоту може бути окислений з одержанням N-оксиду. Приклади N-оксидів включають N-оксиди третинного аміну або атом азоту гетероциклу, що містить азот. N-оксиди можуть утворюватися шляхом обробки відповідним аміном з окислювальним агентом, таким як водню пероксид або перкислота (наприклад, перкарбонова кислота) (див. Advanced Organic Chemistry, by Jerry th March, 4 Edition, Wiley Interscience). У деяких варіантах здійснення винаходу сполуки Формули І ізолюються і/або очищуються. 9 UA 104875 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід також надає фармацевтичні композиції, що включають одну або декілька сполук, описаних вище, або одну або декілька їх солей, і фармацевтично прийнятний носій. Прийнятні композиції включають, але не обмежуючись ними, пероральні не абсорбовані композиції. Прийнятні композиції також включають, але не обмежуючись ними, фізіологічний розчин, воду, розчини циклодекстрину й забуферені розчини з рН 3-9. Сполуки, описані в даному описі, включаючи Сполуку А або її фармацевтично прийнятні солі, можуть бути одержані з використанням численних ексципієнтів, включаючи, але не обмежуючись ними, очищену воду, пропіленгліколь, PEG 400, гліцерин, DMA, етанол, бензиловий спирт, лимонну кислоту/натрію цитрат (рН 3), лимонну кислоту/натрію цитрат (рН 5), трис(гідроксиметил)аміно метан НСl (рН 7,0), 0,9% фізіологічний розчин і 1,2% фізіологічний розчин і будь-яку їх комбінацію. У деяких варіантах здійснення винаходу ексципієнт вибраний із пропіленгліколю, очищеної води й гліцерину. У деяких варіантах здійснення винаходу ексципієнт являє собою багатокомпонентну систему, вибрану з 20% маса/об'єм пропіленгліколю у фізіологічному розчині, 30% маса/об'єм пропіленгліколю у фізіологічному розчині, 40% маса/об'єм пропіленгліколю у фізіологічному розчині, 50% маса/об'єм пропіленгліколю у фізіологічному розчині, 15% маса/об'єм пропіленгліколю в очищеній воді, 30% маса/об'єм пропіленгліколю в очищеній воді, 50% маса/об'єм пропіленгліколю в очищеній воді, 30% маса/об'єм пропіленгліколю й 5 маса/об'єм етанолу в очищеній воді, 15% маса/об'єм гліцерину в очищеній воді, 30% маса/об'єм гліцерину в очищеній воді, 50% маса/об'єм гліцерину в очищеній воді, 20% маса/об'єм Клептози в очищеній воді, 40% маса/об'єм Клептози в очищеній воді й 25% маса/об'єм Каптизолу в очищеній воді. У деяких варіантах здійснення винаходу ексципієнт вибраний з 50% маса/об'єм пропіленгліколю в очищеній воді, 15% маса/об'єм гліцерину в очищеній воді, 20% маса/об'єм Клептози в очищеній воді, 40% маса/об'єм Клептози в очищеній воді й 25% маса/об'єм Каптизолу в очищеній воді. У деяких варіантах здійснення винаходу ексципієнт вибраний з 20% маса/об'єм Клептози в очищеній воді, 20% маса/об'єм пропіленгліколю в очищеній воді й 15% маса/об'єм гліцерину в очищеній воді. У деяких варіантах здійснення винаходу сполука включає 50 мг/мл Сполуки А в 20% маса/об'єм Клептозі в очищеній воді. У деяких варіантах здійснення винаходу склад може бути ліофілізований у тверду речовину й відновлений, наприклад, водою перед використанням. При введенні ссавцеві (наприклад, тварині для ветеринарного застосування або людині для клінічного застосування) сполуки Формули І можуть бути введені в ізольованій формі. Альтернативно сполуки Формули І можуть бути введені разом з (тобто як комбінований склад або як окремі склади) іншими антибіотиками, такими як, наприклад: 1) інгібітори білкового синтезу, включаючи, але не обмежуючись ними, амікацин, анизоміцин, апраміцин, азитроміцин, бластицидин S, брефелдін А, бутирозин, хлорамфенікол, хлортетрациклін, кліндаміцин, клотримазол, циклогексімід, демеклоциклін, дибекацин, дигідрострептоміцин, доксициклін, дураміцин, еметин, еритроміцин, фузидова кислота, G418, гентаміцин, гельволова кислота, гігроміцин В, джозаміцин, канаміцин, кіроміцин, лінкоміцин, меклоциклін, мепартрицин, мідекаміцин, міноциклін, неоміцин, нетилміцин, нітрофурантоїн, ноурсетрицин, олеандоміцин, окситетрациклін, паромоміцин, пуроміцин, рапаміцин, рибостаміцин, рифампіцин, рифаміцин, розаміцин, сизоміцин, спектиноміцин, спіраміцин, стрептоміцин, тетрациклін, триамфенікол, тіострептон, тобраміцин, тунікаміцин, тилозин, біоміцин і вірджиніаміцин; 2) засоби, що перешкоджають синтезу ДНК, включаючи, але не обмежуючись ними, камптотецин, 10деацетилбакатин III, азацитидин, 7-аміноактиноміцин D, 8-хінолінол, 13-ацетилбакатин III, акларубіцин, актиноміцин D, актиноміцин І, актиноміцин V, бафіломіцин А1, блеоміцин, капреоміцин, хромоміцин, циноксацин, ципрофлоксацин, цистдіамінплатина(ІІ) дихлорид, кумерміцин А1, L(+)-молочну кислоту, цитохалазин В, цитохалазин D, дакарбазин, даунорубіцин, дистаміцин А, доксорубіцин, ехіноміцин, енрофлоксацин, етопозид, флумехін, форміцин, фумагілін, ганцикловір гліотоксин, ломефлоксацин, метронідазол, мітраміцин А, мітоміцин С, налідиксову кислоту, нетропсин, нітрофурантоїн, ногаламіцин, нонактин, новобіоцин, офлоксацин, оксолінову кислоту, паклітаксел, феназин, флеоміцин, піпемідову кислоту, ребескаміцин, синефунгін, стрептонігрин, стрептозоцин, сукцинілсульфатіазол, сульфадіазин, сульфадиметоксин, сульфагуанідин чистий, сульфаметазин, сульфамонометоксин, сульфаніламід, сульфахіноксалін, сульфасалазин, сульфатіазол, триметоприм, туберцидин, 5-азацитидин, кордицепін і форміцин А; 3) засоби, що перешкоджають синтезу клітинної стінки, включаючи але не обмежуючись ними, (+)-6амінопеніциланову кислоту, 7-амінодезацетоксицефалоспоранову кислоту, амоксицилін, ампіцилін, азлоцилін, бацитрацин, карбеніцилін, цефаклор, цефамандол, цефазолін, 10 UA 104875 C2 5 10 15 20 25 30 35 40 45 50 55 60 цефметазол, цефоперазон, цефотаксим, цефсулодін, цефтриаксон, цефалексин, цефалоспорин С, цефалотин, цефрадин, клоксацилін, D-циклосерин, диклоксацилін, Dпеніциламін, еконазол, етамбутол, лізостафін, моксалактам, нафцилін, нікоміцин Z, нітрофурантоїн, оксацилін, пеніцилін, пеніцилін G, фенетицилін, феноксиметилпеніцилинову кислоту, фосфоміцин, піпемідову кислоту, піперацилін, ристоміцин і ванкоміцин; 4) засоби, шо перешкоджають проникності клітинної мембрани (іонофори), включаючи, але не обмежуючись ними, 2-меркаптопіридин, 4-бромкальциміцин А23187, аламетицин, амфотерицин В, кальциміцин А23187, хлоргексидин, клотримазол, колістин, еконазол, гідрокортизон, філіпін, гліотоксин, граміцидін А, граміцидін С, іономіцин, лазалоцид А, лономіцин А, монензин, N-(6аміногексил-5-хлор-1-нафталенсульфонамід, наразин, нігерицин, нізин, нонактин, ністатин, феназин, пімарицин, полімиксин В, DL-пеніциламін, поліміксин В, празиквантел, саліноміцин, сурфактин і валіноміцин; 5) ферментативні інгібітори, включаючи, але не обмежуючись ними, (+)-уснінову кислоту, (±)-міконазол, (S)-(+)-камптотецин, 1-дезоксиманоджириміцин, 2-гептил-4гідроксихінолін N-оксид, кордицептин, 1,10-фенантролін, 6-діазо-5-оксо-1-норлейцин, 8хінолінол, антиміцин, антипаїн, аскоміцин, азасерин, бафіломіцин, церуленін, хлорохін, циноксацин, ципрофлоксацин, мевастатин, конканаміцин А, конканаміцин С, кумерміцин А1, L(+)-молочну кислоту, циклоспорин А, еконазол, енрофлоксацин, етопозид, флумехін, форміцин А, фуразолідон, фузарову кислоту, гелданаміцин, гліотоксин, граміцидін А, граміцидін С, гербіміцин А, індометацин, іргазан, ломефлоксацин, мікофенолову кислоту, міксотіазол, N-[-(6аміногексил)-5-хлор-1-нафталенсульфонамід, налідиксову кислоту, нетропсин, ніклозамід, нікоміцин, N-метил-1-дезоксиноджириміцин, ногаламіцин, нонактин, новобіоцин, офлоксацин, олеандоміцин, олігоміцин, оксолінову кислоту, пірицидин А, піпемідову кислоту, радицикол, рапаміцин, ребескаміцин, синефунгін, стауроспорин, стигмателін, сукцинілсульфатіазол, сульфадіазин, сульфадиметоксин, сульфагуанідин, сульфаметазин, сульфамонометоксин, сульфаніламід, сульфахіноксалін, сульфасалазин, сульфатіазол, триасцин С, триметоприм і вінеоміцин А1; і 6) мембранні модифікатори, включаючи, але не обмежуючись ними, парацельзин. У деяких варіантах здійснення винаходу термін «фармацевтично прийнятний» означає затверджений Агентством з регулювання Федерального або урядового рівня або перерахований у Фармакопеї США, або іншій загальновизнаній фармакопеї, використовуваній для тварин, і конкретніше для людей. Термін «носій» належить до розріджувача, ад'юванту або ексципієнту, з яким вводиться сполука Формули І. Такі фармацевтичні носії можуть являти собою рідини, такі як вода й масла, включаючи масла нафтового, тваринного, рослинного або синтетичного походження, такі як арахісова олія, соєва олія, мінеральне масло, кунжутна олія й таке інше. Фармацевтичні носії можуть також являти собою фізіологічний розчин, аравійську камедь, желатин, крохмальний клейстер, тальк, кератин, колоїдний кремній, сечовину й таке інше. Додатково можуть бути використані допоміжні, стабілізуючі, загущувальні, забарвлюючі і змащувальні агенти. При введенні людині сполуки Формули І і фармацевтично прийнятні носії можуть бути стерильними. Вода є прийнятним носієм, коли сполука Формули І вводиться внутрішньовенно. Фізіологічні розчини й розчини водної декстрози й гліцерину можуть бути також застосовані як рідкі носії, особливо для ін'єктованих розчинів. Прийнятні фармацевтичні носії також включають ексципієнти, такі як крохмаль, глюкоза, лактоза, сахароза, желатин, солод, рис, борошно, крейда, силікатний гель, натрію стеарат, гліцерол моностеарат, тальк, натрію хлорид, сухе знежирене молоко, гліцерин, пропілен, гліколь, вода, етанол і таке інше. Дані композиції, якщо бажано, можуть також містити невелику кількість зволожуючих або емульгуючих агентів або забуферювальних рН агентів. Композиції, описані в даному описі, можуть приймати форму розчину, суспензії, емульсії, таблетки, пігулки, гранули, капсули, капсули, що містить рідину, порошку, склади з уповільненим вивільненням, супозиторію, аерозолю, спрею або будь-яку іншу форму, прийнятну для використання. Приклади прийнятних фармацевтичних носіїв описані в Remington's Pharmaceutical Sciense, A.R. Gennaro (Editor) Mack Publishing Co. В одному з варіантів здійснення винаходу сполуки Формули І одержують відповідно до звичайної процедури як фармацевтичну композицію, адаптовану для введення людям. Зазвичай сполуки Формули І являють собою розчини в стерильному ізотонічному водному буфері. За необхідності сполуки можуть також включати солюбілізуючий агент. Композиції для внутрішньовенного введення можуть за необхідності включати місцевий анестетик, такий як лідокаїн, для полегшення болю в місці ін'єкції. Зазвичай інгредієнти надаються роздільно або змішані в стандартній лікарській формі, наприклад, у вигляді сухого ліофілізованого порошку або безводного концентрату в герметично закритому контейнері, такому як ампула або саше, із вказуванням кількості активного агента. У випадку якщо сполуку винаходу слід вводити шляхом 11 UA 104875 C2 5 10 15 20 25 30 35 інфузії, вона може бути приготовлена, наприклад, з використанням флакона для інфузії, що містить стерильну фармацевтично чисту воду для інфузії або фізіологічний розчин. У випадку якщо сполука Формули І вводиться шляхом ін'єкції, може бути надана ампула стерильної води для ін'єкції або фізіологічного розчину так, щоб інгредієнти могли бути змішані до введення. Сполуки Формули І і композиції, що включають те ж саме, можуть бути введені перорально. Сполуки й композиції для пероральної доставки можуть знаходитися у формі, наприклад, таблеток, пастилок, водних або масляних суспензій, гранул, порошків, емульсій, капсул, сиропів або еліксирів. Перорально введені композиції можуть містити один або декілька необов'язкових агентів, наприклад підсолоджувальні агенти, такі як фруктоза, аспартам або сахарин; ароматизуючі агенти, такі як м'ята перцева, олія гаультерії або вишні; барвні агенти; і консервувальні агенти, з одержанням фармацевтично приємного на смак препарату. Крім того, коли є форма таблетки або пігулки, композиції можуть бути покриті для уповільнення розпадання й абсорбції в шлунково-кишковому тракті, тим самим забезпечуючи безперервну дію протягом тривалого періоду часу. Вибірково проникні мембрани, що оточують сполуку, яка осмотично активно переміщається, також прийнятні для сполук Формули І, що перорально вводяться. Пероральні композиції можуть включати стандартні основи, такі як маніт, лактоза, крохмаль, магнію стеарат, натрію сахарин, целюлоза, магнію карбонат і т.д. Такі основи є відповідно фармацевтично чистими. Фармацевтичні композиції можуть бути в стандартній лікарській формі. У такій формі композиція може бути розділена на одноразові дози, що містять відповідну кількість активного компонента. Стандартна лікарська форма може знаходитися у вигляді упакованого препарату, упаковка містить дискретні кількості препаратів, наприклад, упаковані таблетки, капсули й порошки у флаконах або ампулах. Стандартна лікарська форма може також знаходитися у вигляді капсули, саше або самої таблетки, або вона може являти собою відповідну кількість будь-якої із цих упакованих форм. Даний винахід також надає способи одержання Сполуки А, що включають: 1а) взаємодію (R)-(-)-N-Вос-3-піролідинолу із сильною основою з одержанням суміші; далі взаємодію суміші із 2-хлор-5-(трифторметил)-1,3-динітробензолом з одержанням сполуки, що має Формулу II 1b) взаємодію сполуки Формули II зі спиртом і каталізатором перехідного металу в присутності водню з одержанням сполуки Формули III 1с) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш 2-хлор-4,6диметокси-1,3,5-триазину й N-метилморфоліну з одержанням сполуки Формули IV 12 UA 104875 C2 1d) взаємодію сполуки Формули IV з N-Bос-гуанідином масляної кислоти з одержанням сполуки Формули V 5 10 15 20 25 30 35 40 1e) зняття захисних груп сполуки Формули V з одержанням Сполуки А. У деяких варіантах здійснення винаходу в а) сильна основа являє собою NaH; і в b) каталізатор перехідного металу являє собою Pd/C, а спирт являє собою етанол. Зокрема, цей спосіб описаний нижче більш детально в Прикладі 1. Даний винахід також надає додаткові способи одержання Сполуки А, що включають: a) зняття захисних груп трет-бутилового ефіру (R)-3-гідроксипіролідин-1-карбонової кислоти й взаємодію одержаної сполуки із 2-хлор-1,3-динітро-5-трифторметилбензолом з одержанням трет-бутилового ефіру (N)-3-(2,6-диттро-4-трифторметилфенокси)піролідин-1-карбонової кислоти; b) відновлення трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин1-карбонової кислоти в присутності спирту, каталізатора перехідного металу й водню з одержанням трет-бутилового ефіру (R)-3-(2,6-діаміно-4-трифторметилфенокси)піролідин-1карбонової кислоти; c) поєднання трет-бутилового ефіру (R)-3-(2,6-діаміно-4-трифторметилфенокси)піролідин-1карбонової кислоти з піримідин-4,6-дикарбоновою кислотою в присутності 1-[(3(диметиламіно)пропіл)]-3-етилкарбодііміду гідрохлориду з одержанням біс-{[3-аміно-2-((R)-1(трет-бутоксикарбоніл)піролідин-3-ілокси)-трифторметил-феніл]аміду}піримідин-4,6дикарбонової кислоти; d) взаємодію біс-{[3-аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5трифторметил-феніл]аміду}піримідин-4,6-дикарбонової кислоти з ({[(третбутоксикарбоніл)аміно][(трет-бутоксикарбоніл)іміно]метил}аміно) пентановою кислотою в присутності фосфору оксихлориду з одержанням біс-{[3-(5-({[(трет-бутоксикарбоніл)аміно][третбутоксикарбоніл)іміно]метил}аміно)пентаноїламіно)-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3ілокси)-5-трифторметил-феніл]аміду}піримідин-4,6-дикарбонової кислоти; e) зняття захисних груп біс-{[3-(5-({[(трет-бутоксикарбоніл)аміно][третбутоксикарбоніл)іміно]метил}аміно)-пентаноїламіно)-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3ілокси)-5-трифторметил-феніл]аміду}піримідин-4,6-дикарбонової кислоти з одержанням неочищеного біс-{[3-(5-гуанідино-пентаноїламіно)-2-((R)-піролідин-3-ілокси)-5-трифторметилфеніл]амід}тетрагідрохлориду піримідин-4,6-дикарбонової кислоти; і f) очищення неочищеного біс-{[3-(5-гуанідино-пентаноїламіно)-2-((R)-піролідин-3-ілокси)-5трифторметил-феніл]амід}тетрагідрохлориду піримідин-4,6-дикарбонової кислоти за допомогою хроматографії зі зворотною фазою. У деяких варіантах здійснення винаходу в b) каталізатор перехідного металу являє собою Pd/C, і спирт являє собою етанол. Зокрема, цей спосіб описаний нижче більш детально в Прикладі 2. Даний винахід також надає інші додаткові способи одержання Сполуки А, що включають: 13 UA 104875 C2 5 10 15 20 25 30 a) зняття захисних груп трет-бутилового ефіру (R)-3-гідроксипіролідин-1-карбонової кислоти й далі взаємодію одержаної сполуки із хлор-1,5-трифторметилбензолом з одержанням третбутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1-карбонової кислоти; b) відновлення трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин1-карбонової кислоти в присутності спирту, каталізатора перехідного металу й водню з одержанням трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1карбонової кислоти; c) поєднання трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1карбонової кислоти з піримідин-4,6-дикарбоновою кислотою в присутності 1-[(3(диметиламіно)пропіл)]-3-етилкарбодііміду гідрохлориду з одержанням бic-{[3-aміно-2-((R)-1(трет-бутоксикарбоніл)піролідин-3-ілокси)-трифторметил-феніл]аміду} піримідин-4,6дикарбонової кислоти; d) взаємодію біс-{[3-аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5трифторметил-феніл]аміду}піримідин-4,6-дикарбонової кислоти з N-Cbz кислотою в присутності тіонілу хлориду; e) відновлення одержаної сполуки d) у присутності спирту, каталізатора перехідного металу й водню; f) взаємодію одержаної сполуки e) з ди-Вос піразолом; і g) зняття захисних груп одержаної сполуки f) з одержанням Сполуки А. У деяких варіантах здійснення винаходу в b) і e) каталізатор перехідного металу являє собою Pd/C, і спирт являє собою етанол. Зокрема, цей спосіб описаний нижче більш детально в Прикладі 3. Фахівець у даній галузі зуміє замінити прийнятні реагенти на реагенти, перераховані в способах, описаних у даному описі, з одержанням Сполуки А, а також додаткових сполук Формули І. Даний винахід також надає способи одержання фармацевтично прийнятної солі Сполуки А, що включають: a) взаємодію (R)-(-)-N-Вос-3-піролідинолу із сильною основою з одержанням суміші; далі взаємодію суміші із 2-хлор-5-(трифторметил)-1,3-динітробензолом з одержанням сполуки, що має Формулу II b) взаємодію сполуки Формули II зі спиртом і каталізатором перехідного металу в присутності водню з одержанням сполуки Формули III 35 с1) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш 2-хлор-4,6диметокси-1,3,5-триазину й N-метилморфоліну з одержанням сполуки Формули IV 14 UA 104875 C2 с2) додавання сполуки Формули III і піримідин-4,6-дикарбонової кислоти в суміш 1-етил-3-[3(диметиламіно)пропіл]карбодііміду гідрохлориду (EDC1) і безводного піридину з одержанням сполуки Формули IV 5 10 d) додавання сполуки Формули IV з N-Cbz кислотою в розчин, що включає безводний піридин, диметиламінопропіламін і будь-який один з тіонілу хлориду, РОСІ3, (EtO)2POCl або оксалілу хлориду з одержанням сполуки Формули Va e) гідрогеноліз групи Cbz сполуки Формули Va з одержанням сполуки Формули VI f) захист сполуки Формули VI з одержанням сполуки Формули VII 15 g) зняття захисних груп сполуки Формули VII з одержанням фармацевтично прийнятної солі Сполуки А. Одержання сполук Формули І може включати захист або зняття захисту різних хімічних груп. Необхідність захисту й зняття захисту й вибір відповідних захисних груп можуть бути легко 15 UA 104875 C2 5 10 15 20 25 30 35 40 45 50 55 60 визначені фахівцем у даній галузі. Хімія захисних груп може бути знайдена, наприклад, у роботі rd Т. W. Greene і P. G. М. Wuts, Protective Groups in Organic Synthesis, 3 Ed. Wiley & Sons, Inc. New York (1999), яка включена в даний описі за допомогою посилання у всій своїй повноті. Даний винахід також надає способи інгібування росту мікроба, що включають контактування мікроба з одним або декількома сполуками, описаними вище, або їх фармацевтично прийнятною сіллю. У деяких варіантах здійснення винаходу сполука Формули І може діяти як антисептичний засіб для очищення поверхонь, таких як, наприклад, у кухнях і ванних кімнатах. У цих варіантах здійснення винаходу сполука Формули І може бути одержана для такого використання за допомогою методик, добре відомих фахівцеві в даній галузі. Даний винахід також надає способи лікування ссавця, що страждає мікробною інфекцією, що включають введення ссавцеві, який потребує цього, протимікробної ефективної кількості будь-якої зі сполук, описаних вище, або її фармацевтично прийнятної солі. У деяких варіантах здійснення винаходу ссавець може бути попередньо діагностований на наявність мікробної інфекції до лікування. У деяких варіантах здійснення винаходу офіційний діагноз не може бути зроблений; у таких варіантах здійснення винаходу ссавець може підозрюватися на наявність мікробної інфекції, для якої лікування визнане як бажане. В одному варіанті здійснення винаходу «лікування» або «обробка» належать до послаблення мікробної інфекції або щонайменше її одного помітного симптому; або до послаблення щонайменше одного вимірюваного фізичного параметра, що не обов'язково помічається пацієнтом; або до інгібування прогресування мікробної інфекції; або до затримування початку розвитку мікробної інфекції. У деяких варіантах здійснення винаходу мікроб являє собою або мікробна інфекція викликається грамнегативним аеробом, грампозитивним аеробом, грамнегативним анаеробом, грампозитивним анаеробом або дріжджами. У деяких варіантах здійснення винаходу грамнегативний аероб вибраний з, але не обмежуючись ними, Escherichia coli, Citrobacter freundii, Citrobacter diverus, Citrobacter koseri, Enterobacter cloacae, Enterobacter faecalis, Klebsiella pneumonia, Klebsiella oxytoca, Morganella morganii, Providencia stuartii, Proteus vulgaris, Proteus mirabilis, Serratia marcescens, Acinetobacter haemolyticus, Acinetobacter junii, Acinetobacter lwoffii, Haemophilus influenzae, Stenotrophomonas maltophilia і Pseudomonas aeruginosa. У деяких варіантах здійснення винаходу грампозитивний аероб вибраний з, але не обмежуючись ними, Enterococcus faecalis, Enterococcus faecium, Mycobacterium tuberculosis, Staphylococcus aureus, Staphylococcus pneumoniae, Staphylococcus epidermidis, Staphylococcus saprophyticus, Staphylococcus colmii, Staphylococcus sciuri, Staphylococcus wameri, Streptococcus agalactiae, Streptococcus pyogenes, Streptococcus anginosus, Streptococcus mitis і Streptococcus oralis. У деяких варіантах здійснення винаходу грамнегативний анаероб являє собою Bacteroides fragilis. У деяких варіантах здійснення винаходу грампозитивний анаероб являє собою Clostridiura difficile або Clostridium perfringens. У деяких варіантах здійснення винаходу мікобактерія являє собою Mycobacterium tuberculosis, Mycobacterium bovis, Mycobacterium africanum, Mycobacterium canetti або Mycobacterium microti. У деяких варіантах здійснення винаходу дріжджі вибрані з, але не обмежуючись ними, Candida albicans і Candida krusei. У деяких варіантах здійснення винаходу мікроб являє собою резистентний до антибіотика штам бактерій, такий як штам бактерій, перерахований у Прикладах нижче. Сполуки Формули І або їх фармацевтично прийнятна сіль і композиції , що включають їх, можуть бути введені різними способами, такими як, наприклад, інфузія або болюсна ін'єкція, і можуть бути введені разом з іншим біологічно активним агентом, таким як інший антибіотик. Введення може бути системним або місцевим. Відомі різні системи доставки, наприклад, інкапсульовані в ліпосоми, мікрочастинки, мікрокапсули, капсули, і т.д., і вони можуть бути використані для введення сполуки Формули І. Шляхи введення включають, але не обмежуючись ними, внутрішньодермальний, внутрішньом'язовий, внутрішньочеревинний, внутрішньовенний, підшкірний, інтраназальний, епідуральний, оральний, під'язичний, інтраназальний, інтрацеребральний, інтравагінальний, трансдермальний, ректальний, легеневий, шляхом інгаляції або топічно, особливо у вуха, ніс, очі або на шкіру. У деяких варіантах здійснення винаходу прийнятні шляхи введення включають внутрішньовенний, топічний або підшкірний. Бажаний шлях введення залишається на розсуд практикуючого лікаря й буде залежати, частково, від локалізації мікробної інфекції й стану здоров'я ссавця або людини, яких піддають лікуванню. У більшості випадків введення може призводити до вивільнення сполук Формули І у кров'яне русло. У деяких варіантах здійснення винаходу може бути бажаним застосовувати одну або декілька сполук Формули І або їх фармацевтично прийнятну сіль місцево в ділянку, що потребує лікування. Це може бути досягнуто, наприклад, і без обмеження шляхом місцевої інфузії в 16 UA 104875 C2 5 10 15 20 25 30 35 40 45 50 55 60 процесі хірургічної операції, топічного нанесення, наприклад, разом з рановою пов'язкою після хірургічної операції, шляхом ін'єкції, за допомогою катетера, за допомогою супозиторію або за допомогою імплантату, де імплантат являє собою пористий, не пористий або гелеподібний матеріал, включаючи мембрани, такі як сіаластикові мембрани або волокна. Кількість сполуки Формули І або її фармацевтично прийнятної солі, яка буде ефективна для лікування конкретної мікробної інфекції, буде залежати від природи порушення або патологічного стану й може бути визначена за допомогою стандартної клінічної методики. Додатково за необхідності можуть бути застосовані аналізи in vitro або in vivo, щоб допомогти ідентифікувати оптимальний діапазон доз. Точна доза для застосування в композиціях буде також залежати від шляху введення й тяжкості інфекції, і повинно бути ухвалене рішення відповідно до медичної оцінки практикуючого лікаря й стану кожного пацієнта. Однак прийнятний діапазон доз для введення становить зазвичай від приблизно 0,001 міліграма до приблизно 200 міліграмів на кілограм маси тіла. У деяких варіантах здійснення винаходу доза становить від приблизно 0,01 міліграма до приблизно 70 міліграмів на кілограм маси тіла або від приблизно 0,1 міліграма до приблизно 50 міліграмів на кілограм маси тіла, або від приблизно 0,5 міліграмів до приблизно 20 міліграмів на кілограм маси тіла, або від приблизно 1 міліграма до приблизно 10 міліграмів на кілограм маси тіла. У деяких варіантах здійснення винаходу доза становить приблизно 5 міліграмів на кілограм маси тіла. Кількість доз, описаних у даному описі, належить до загальної введеної кількості; тобто, якщо вводиться більше ніж одна сполука Формули І, дози відповідають загальній кількості введених сполук Формули І. Композиції можуть містити від 10% до 95% активного інгредієнта по масі. Ефективні дози можуть бути екстрапольовані за кривими доза-відповідь, одержаними in vitro або на тваринних модельних тест-системах. Такі тваринні моделі й системи добре відомі в даній галузі. Даний винахід також надає одну або декілька сполук, описаних вище, або їх фармацевтично прийнятну сіль, або фармацевтичну композицію, що включає одну або декілька сполук, описаних вище, для лікування мікробної інфекції. Даний винахід також надає одну або декілька сполук, описаних вище, або їх фармацевтично прийнятну сіль, або фармацевтичну композицію, що включає одну або декілька сполук, описаних вище, для використання при виготовленні лікарського засобу для лікування мікробної інфекції. Даний винахід також надає застосування однієї або декількох сполук, описаних вище, або їх фармацевтично прийнятної солі, або фармацевтичної композиції, що включає одну або декілька сполук, описаних вище, для інгібування росту мікроба. Даний винахід також надає застосування однієї або декількох сполук, описаних вище, або їх фармацевтично прийнятної солі, або фармацевтичної композиції, що включає одну або декілька сполук, описаних вище, для лікування мікробної інфекції ссавця. Для того щоб винахід, розкритий в даному описі, міг бути краще зрозумілий, нижче наводяться приклади. Слід розуміти, що ці приклади служать тільки для ілюстративних цілей і не тлумачаться як обмежуючі винахід будь-яким чином. У цих прикладах виконали реакції молекулярного клонування й інші стандартні методики на основі рекомбінантної ДНК відповідно до методів, описаних в Maniatis із співр., Molecular cloning - A Laboratory Manual, 2nd ed., Cold Spring Harbor Press (1989), з використанням комерційно придатних реагентів, за винятком випадків, коли вказане інше. Приклади Коротко, результати, одержані на підставі прикладів, наведених нижче, вказують, що Сполука А є активною проти Staphylococci spp. і інших грампозитивних і грамнегативних організмів. Наприклад, виконаний скринінг чутливості проти 150 ізолятів S. aureus і негативних за коагулазою стафілококів з визначеною антибактеріальною чутливістю до інших протимікробних агентів. Загалом, були одержані значення МІС90 від 0,5 до 2,0 мкг/мл при скринінгу 150 організмів стафілококів, і була відсутня чутливість фенотипів до інших антибіотиків. Серійний пасаж метицилін-чутливих (MSSA АТСС 29213) і резистентних (MRSА АТСС 33591) штамів S. aureus при концентраціях 0,5х МІС протягом 17 пасажів не викликав будь-якої зміни в значеннях МІС. Загалом, Сполука А була бактерицидною відносно часерадикація в діапазоні від 30 хвилин до 6 годин. Сполука А була ефективною in vivo на мишачій моделі навантаження на стегнову кістку проти MSSA 29213 і MRSA 33591 і на мишачій моделі перитоніту/сепсису проти MSSA 27660. На мишачій моделі навантаження на стегнову кістку з використанням MSSA 27660 Сполука А 10 забезпечувала зниження через 24 години після інфікування аж до 4 КУО/стегнова кістка відносно неопрацьованих інфікованих мишей у дозах, які добре переносилися в повторних дослідженнях токсичності дози. Таким чином, стійку ефективність проти MSSA і MRSA 17 UA 104875 C2 5 10 15 20 25 30 35 40 спостерігали на мишачій моделі навантаження на стегнову кістку й проти MSSA на щурячій моделі навантаження на стегнову кістку й мишачій моделі перитоніту. Сполука А була стабільною у присутності плазми й ізольованих гепатоцитів множини видів. Сполука А була більшою мірою толерантною у дослідженнях гострої токсичності, коли вводилася за допомогою IV [внутрішньовенної] інфузії. MTD [максимальна толерантна доза] (IV болюсне [струминне] введення) для Сполуки А у миші (30 мг/кг) була значущо більш високою, ніж статична ефективна доза на моделі навантаження на стегнову кістку (2-4 мг/кг). Сполука А у даний час знаходиться у Фазі 1 клінічних випробувань на людині для розробки як IV пан-стафілококовий агент. Приклад 1: синтез Сполуки А Стадія 1: Натрію гідрид (1,12 г, 60% у мінеральному маслі, 28 мМ) додавали по частинах у безводний DMF (24 мл) розчин (R)-(-)-N-Boc-3-піролідинолу (5,0 г, 27,6 мМ) при кімнатній температурі. Одержану суміш перемішували додатково 15 хвилин. Цю суміш потім додавали по краплях в DMF (20 мл) розчин 2-хлор-5-(трифторметил)-1,3-динітробензолу (7,45 г, 27,6 мМ) при 0°С. Розчин темно-червоного кольору перемішували при кімнатній температурі протягом 4 годин. Реакцію зупиняли крижаною водою й екстрагували етилацетатом. Органічний шар промивали сольовим розчином і водою й сушили над Na2SO4. Після видалення розчинника залишок очищували за допомогою колони для відгону легких фракцій (етилацетат/гексани = ¼ об'єм/об'єм). Вихід склав 54%. Стадія 2: (R)-трет-бутил-3-(4-трифторметил)-2,6-динітрофенокси)піролідин-1-карбоксилат (4,84 г, 9,8 мм) і Pd/C (0,78 г, 10% на вуглець) і етанол (140 мл) вміщували в колбу Парра. Суміш випарювали під воднем три рази й перемішували при 40 кПа водню при кімнатній температурі протягом ночі. Суміш фільтрували через целіт. Осад на фільтрі промивали двічі етанолом (2x20 мл). Фільтрат випарювали під вакуумом. Одержали сірувато-білу тверду речовину й використовували як таку для наступної реакції. Вихід склав 100%. Стадія 3: 2-Хлор-4,6-диметокси-1,3,5-триазин (5,97 г, 34 мм) перемішували в безводному THF (200 мл). Додавали N-метилморфолін (7,5 мл, 68 мм). Одержану суміш перемішували при кімнатній температурі протягом 30 хвилин. Потім додавали (R)-трет-бутил-3-(2,6-діаміно-4(трифторметил)фенокси)піролідин-1-карбоксилат (10,84 г, 30 мм) і піримідин-4,6-дикарбонову кислоту (2,48 г, 14,8 мм). Суміш перемішували при кімнатній температурі протягом 24 годин. Розчинник випарювали повністю у вакуумі. Додавали воду (250 мл) і суміш перемішували протягом 4 годин. Після фільтрування жовтий осад промивали водою (3х100 мл) і перемішували у воді (250 мл) протягом 4 годин. Процедуру фільтрування й промивання повторювали двічі. Тверду речовину сушили на повітрі й перемішували в дихлорметані (20 мл) протягом 30 хвилин з наступною ультразвуковою обробкою протягом 1 години. Після фільтрування жовтий осад на 18 UA 104875 C2 фільтрі швидко промивали холодним дихлорметаном (2x10 мл). Продукт (10,0 г, вихід: 79,1%) використовували як такий для наступної реакції. Стадія 4: 5 10 15 Вихідний матеріал (6,5 г, 7,6 мМ), N-Вос-гуанідин масляної кислоти (10,9 г, 30,4 мМ) перемішували в безводному піридині (40 мл) при 0°С. РОСl3 (2,78 мл, 30,4 мМ) у піридині (4 мл) додавали по краплях. Одержану суміш перемішували при 0°С протягом 1,5 годин. Реакційну суміш випарювали під вакуумом. Воду (140 мл) додавали до залишку. Суміш екстрагували з використанням етилацетату (260 мл). Органічний шар промивали сольовим розчином (100 мл) і сушили над Na2SO4. Після випарювання залишок очищували з використанням колони (елюент: етилацетат/гексани/дихлорметан = 1/1/1, об'єм/об'єм/об'єм, потім 2%~4% метанол у дихлорметані). Вихід склав 29,1%. Rf був таким самим, як у стандартному зразку, який охарактеризували за допомогою ЯМР. Стадія 5: Вихідний матеріал (3,4 г, 2,3 мм) перемішували в 4н НСl (34 мл) при кімнатній температурі протягом ночі. Розчинник видаляли під вакуумом. Залишок титрували в ефірі. Тверду речовину фільтрували й очищували за допомогою С18 зі зворотною фазою С18 колони. Як продукт одержали світло-жовту тверду речовину із чистотою 98% (ВЕРХ); LC-MC (М+1): 937. Вихід: 51%. Приклад 2: синтез Сполуки А 19 UA 104875 C2 5 10 15 Стадія 1: трет-бутиловий ефір (R)-3-гідроксипіролідин-1-карбонової кислоти депротонують з використанням калію трет-бутоксиду (KOtBU) у тетрагідрофурані (THF). Одержаний аніон взаємодіє із 2-хлор-1,5-трифторметилбензолом у трет-бутилметиловому ефірі (MTBE)/THF. Коли реакція закінчується, реакційну суміш гасять водою й розділяють із використанням додаткового МТВЕ. Органічний шар промивають сольовим розчином і водою й концентрують на ротаційному випарнику. Твердий концентрат повторно розчиняють у метанолі й повторно осаджують із водою. Одержаний осад фільтрують і сушать із наданням трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1-карбонової кислоти, який може бути використаний у наступній стадії без подальшого очищення. Стадія 2: продукт стадії 1 розчиняють у метанолі й гідрогенізують при 100-200 кПа й 30-50°С у присутності 10% Pd/C доти, коли відновлення буде вважатися закінченим за допомогою ВЕРХ. Реакційну суміш фільтрують через целіт. Фільтрат концентрують і сушать із наданням третбутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1-карбонової кислоти, який може бути використаний у наступній стадії без подальшого очищення. Стадія 3: продукт стадії 2 з'єднують із піримідин-4,6-дикарбоновою кислотою, у приблизному відношенні 2 Μ діамін:1 Μ діацид у присутності 1-[(3-(диметиламіно)пропіл)]-3-етилкарбодііміду гідрохлориду (EDCI) у піридині під інертною атмосферою при температурі навколишнього 20 UA 104875 C2 5 10 15 20 25 30 35 40 середовища. Коли реакція закінчується, реакційну суміш розводять у воді. Одержаний осад виділяють і повторно розчиняють в МТВЕ. Розчин МТВЕ промивають водою, 0,2 н НСl і сольовим розчином, сушать над безводним натрію сульфатом, виділяють і розводять у гептані. Одержаний осад ізолюють за допомогою фільтрування й сушать із наданням біс-{[3-аміно-2((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5-трифторметил-феніл]аміду}піримідин-4,6дикарбонової кислоти, який може бути використаний у наступній стадії без подальшого очищення. Стадія 4: продукт стадії 3 взаємодіє з 2,5-3 молярними еквівалентами ({[(третбутоксикарбоніл)аміно][(трет-бутоксикарбоніл)іміно]метил}аміно) пентанової кислоти в піридині в присутності фосфору оксихлориду при температурі приблизно від -5 до -10°С. Реакцію гасять водою при температурі 15°С. Супернатант виділяють із аморфного осаду, який повторно розчиняють в МТВЕ, промивають водою й сольовим розчином, сушать над безводним натрію сульфатом, виділяють і розводять у гептані. Одержаний осад ізолюють за допомогою фільтрування й сушать із наданням бic-{[3-(5-({[(трет-бутоксикарбоніл)аміно] [третбутоксикарбоніл)іміно]метил}аміно)пентаноїламіно)-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3ілокси)-5-трифторметил-феніл]аміду} піримідин-4,6-дикарбонової кислоти, який використовується в наступній стадії без подальшого очищення. Стадія 5: продукт стадії 4 позбавляють захисних груп (видаляючи шість третбутоксикарбонільних груп) з використанням 4М НСl/l, 4-діоксан у мурашиній кислоті при температурі навколишнього середовища. Реакційну суміш розводять в 1,4-діоксані. Одержаний осад фільтрують, промивають в 1,4-діоксані й сушать із наданням неочищеного біс-{[3-(5гуанідино-пентаноїламін)-2-((R)піролідин-3-ілокси)-5-трифторметил-феніл]амід}тетрагідрохлориду піримідин-4,6-дикарбонової кислоти (неочищена Сполука А). Неочищений продукт далі очищують шляхом повторного осадження з розчину метанолу з використанням THF (50°С до температури навколишнього середовища) і/або повторно осаджують із води/розчину метанолу з використанням THF при температурі навколишнього середовища. Стадія 6 (хроматографічне очищення): кінцеве очищення Сполуки А досягається шляхом хроматографії зі зворотною фазою (ЗФ-ВЕРХ) з використанням фази YMC ODS-AQ, 50 мікрон, 120 ангстрем, суспензію упаковували в колонку з динамічним осьовим стисканням Prochrom. Мобільною фазою є градієнт розчинника В у розчиннику А, де розчинник А є водою з 0,05% трифтороцтової кислоти (TFA) і розчинник В є ацетонітрилом з 0,05% TFA. Фракції, що містять очищений продукт, концентрують за допомогою ротаційного випарника з наданням Сполуки А як солі трифторацетату. Кінцеву форму хлористоводневої солі повторно одержують шляхом пропускання водно/метанольного розчину солі трифторацетату через іонообмінну колонку Dowex 1x2-400 (C1-форма), збирають АРІ-вмісний елюат, концентрують і сушать. Речовину нерозфасованої лікарської форми Сполуки А зберігають при 2-8°С, захищаючи від світла й повітря, у жовтих контейнерах HDPE або в сумках з подвійного поліетилену в картонному барабані. Приклад 3: синтез Сполуки А 21 UA 104875 C2 22 UA 104875 C2 5 10 15 20 25 30 Стадія 1: трет-бутиловий ефір (R)-3-гідроксипіролідин-1-карбонової кислоти (сполука 20) депротонують з використанням калію трет-бутоксиду (KOtBU) у тетрагідрофурані (THF). Одержаний аніон реагує із хлор-1,5-трифторметилбензолом (сполука 2) у третбутилметиловому ефірі (MTBE)/THF. Коли реакція закінчується, реакційну суміш гасять водою й розділяють із використанням додаткового МТВЕ. Органічний шар промивають сольовим розчином і водою й концентрують на ротаційному випарнику. Твердий концентрат повторно розчиняють у метанолі й повторно осаджують із водою. Одержаний осад фільтрують і сушать із наданням трет-бутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1карбонової кислоти, який може бути використаний у наступній стадії без подальшого очищення. Ця реакція буде виконуватися в масштабі з використанням 4,2 кг сполуки 2. Стадія 2: сполуку 21 розчиняють у метанолі й гідрогенізують при 100-200 кПа й 30-50°С у присутності 10% Pd/C доти, коли відновлення буде вважатися закінченим за допомогою ВЕРХ. Реакційну суміш фільтрують через целіт. Фільтрат концентрують і сушать із наданням третбутилового ефіру (R)-3-(2,6-динітро-4-трифторметилфенокси)піролідин-1-карбонової кислоти (сполука 22) з ВЕРХ чистотою 92,2%. Реакцію виконують у чотири серії в масштабі 1,64 кг сполуки 21 для кожної серії. Стадія 3: Сполуку 22 з'єднують із піримідин-4,6-дикарбоновою кислотою (сполука 8), у приблизному відношенні 2 Μ діамін:1 Μ діацид у присутності 1-[(3-(диметиламіно)пропіл)]-3етилкарбодііміду гідрохлориду (EDCI) у піридині під інертною атмосферою при температурі навколишнього середовища. Коли реакція закінчується, реакційну суміш розводять водою. Одержаний осад виділяють і повторно розчиняють в МТВЕ. Розчин МТВЕ промивають водою, 0,2 н НСl і сольовим розчином, сушать над безводним натрію сульфатом, виділяють і розводять у гептані. Одержаний осад виділяють за допомогою фільтрування й сушать із наданням біс-{[3аміно-2-((R)-1-(трет-бутоксикарбоніл)піролідин-3-ілокси)-5-трифторметил-феніл]аміду} піримідин-4,6-дикарбонової кислоти (сполука 23), який може бути використаний у наступній стадії без подальшого очищення. Реакцію виконують у масштабі з використанням 3,15 кг сполуки 22. 23 UA 104875 C2 5 10 15 20 25 30 35 40 Стадія 4: розчин 3,66 г DMAP в 60 мл безводного піридину прохолоджували до 0°С у ванні з льодом. Повільно додавали 3,60 г тіонілу хлориду. Одержаний розчин перемішували протягом 10 хвилин. Вихідний матеріал N-Cbz кислота (7,53 г, 30 мМ), сполука (Cpd) 23 (8,54 г, 10 мМ) додавали в розчин, відповідно. Одержану суміш перемішували при кімнатній температурі (RT) протягом 4 годин. Додавали воду (500 мл). Після енергійного перемішування суміші при кімнатній температурі протягом 2 годин тверду речовину фільтрували й промивали 250 мл води. Тверду речовину розчиняли в етилацетаті (300 мл). Органічний шар промивали 10% розчином лимонної кислоти (100 мл) і сольовим розчином (100 мл) і сушили над Na2SO4. Після випарювання залишок розчиняли в 40 мл DCM, потім додавали 250 мл гексану. Осад збирали й сушили під вакуумом. Одержали 13,20 г продукту з 95% чистотою. Вихід: 100%. Стадія 5: сполуку 26 (13,20 г) розчиняли в МеОН з 2 еквів. 1 н НСl і додавали 1,0 г каталізатора Pd/C (10%). Реакційну суміш вводили в гідрогенізатор Парра й струшували протягом 2 годин при 60 кПа водню. Якщо LCMASS показувала відсутність прогресу, додавали ще 1,0 г каталізатора. Реакційну суміш вводили в гідрогенізатор Парра й струшували протягом 3 годин при 60 кПа водню. Суміш фільтрували через целіт для видалення каталізатора. Фільтрат концентрували до сухого стану на ротаційному випарнику при 30°С. Одержали 11,50 г продукту з 95% чистотою. Вихід: 100%. Стадія 6: сполуку 27 (11,50 г, 10 мМ) розчиняли в 60 мл метанолу й DCM (1:1). Потім додавали 4,04 г триетиламіну (40 мМ). Додавали di-Boc піразол 9,3 грамів (30 мМ) і одержану суміш перемішували при кімнатній температурі протягом 1 години. Після видалення 95% розчинника додавали 300 мл води й суміш енергійно перемішували протягом 2 годин. Тверду речовину фільтрували й промивали 300 мл води. Тверду речовину розчиняли в 300 мл етилацетату й сушили над Na2SO4. Після випарювання розчинника тверду речовину розчиняли в 40 мл DCM, потім 500 мл гексану використовували для осадження продукту. Тверду речовину збирали й сушили під вакуумом. Одержали 13,0 грамів продукту з 85% виходом (90% чистота). Стадія 7: сполуку 28 (1,5 г) очищували на колонці з 80 г силікагелю з використанням градієнта 10-88% ЕЮАс в DCM. Фракції із чистотою вище приблизно 95% збирали, випарювали під вакуумом і сушили. Вихід склав 50-60%. Сполуку 28 з 95% чистотою (0,3 г) розчиняли й перемішували в етилацетаті (3 мл) при кімнатній температурі (22°С) під аргоном. Газом НСl барботували розчин протягом 20 хвилин. Колір розчину змінювався на темно-жовтий при проведенні барботування. Тверда речовина починала дробитися протягом 15 хвилин. Розчин перемішували при кімнатній температурі ще 1 годину. Додатково 4 мл етилацетату вводили в реакційну суміш через втрату етилацетату. Суміш барботували газом НСl протягом 10 хвилин. Суміш перемішували протягом 2,5 годин. Одну третину суміші фільтрували й промивали етилацетатом. Дві третини суміші перемішували при кімнатній температурі протягом ночі. Потім у суміш додавали 30 мл етилацетату. Після фільтрування осад на фільтрі промивали етилацетатом двічі (2х140 мл) і сушили. Тверду речовину занурювали в етилацетат (8 мл) і зберігали в морозильній камері. Реакційний процес виконували протягом 4 годин. 24 UA 104875 C2 Перемішування протягом ночі не дало значної зміни. Чистота кінцевого продукту складала 98% з однією головною домішкою 1,2%. Приклад 4: синтез Сполуки А 25 UA 104875 C2 5 10 15 20 25 30 35 40 Стадія 1: у продуту азотом 4-горлу 12 л RBF додавали 305,32 г сполуки 2, 700 мл MTBF з перемішуванням і суміш прохолоджували в льодяній/водній ванні. Сполуку 20 (212,43 г) розчиняли з калію трет-бутоксидом (1,31 л 1 Μ розчину в THF) з одержанням злегка мутної суміші. Цю суміш додавали до розчину сполуки 21 в RBF протягом 86 хвилин з перемішуванням, у той самий час підтримуючи внутрішню температуру
ДивитисяДодаткова інформація
Назва патенту англійськоюSynthetic mimetics of host defense and uses thereof
Автори російськоюDegrado, William, F., Liu, Dahui, Scott, Richard, W., Xu, Yongjiang, Tang, Haizhong, Korczak, Bozena
МПК / Мітки
МПК: A61P 31/04, A61K 31/506
Мітки: одержання, препарат, основі, варіанти, міметиків, синтетичних, спосіб
Код посилання
<a href="https://ua.patents.su/51-104875-preparat-na-osnovi-sintetichnikh-mimetikiv-ta-sposib-oderzhannya-sintetichnikh-mimetikiv-varianti.html" target="_blank" rel="follow" title="База патентів України">Препарат на основі синтетичних міметиків та спосіб одержання синтетичних міметиків (варіанти)</a>
Попередній патент: Зменшення терпкості композиції, яка містить фенольні сполуки
Наступний патент: Модулятори atф-зв’язувальних касетних транспортерів
Випадковий патент: Спосіб збагачення бурштину