Морфоліній 3-(4-піридил)-1,2,4-триазоліл-5-тіоацетат, що виявляє антигіпоксичну, церебропротекторну та кардіопротекторну активність
Номер патенту: 20388
Опубліковано: 15.04.2002
Автори: Зайченко Ганна Володимирівна, Кечін Ігор Леонідович, Головкін Вячеслав Олександрович, Дроговоз Світлана Мефодієвна, Панасенко Олександр Іванович, Візір Анатолій Дмитрович, Філімонов Володимир Іванович, Краснов Євгеній Іванович, Візір Вадим Анатолійович, Мартиновський Олексій Олексійович, Лозюк Любов Василівна, Книш Євгеній Григорович
Формула / Реферат
Морфолиний 3-(4-пиридил)-1,2,4-триазолил-5-тиоацетат формулы
проявляющий антигипоксическую, церебропротекторную и кардиопротекторную активность.
Текст
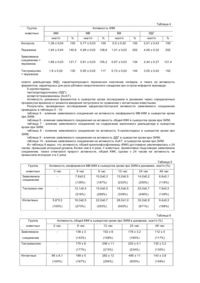
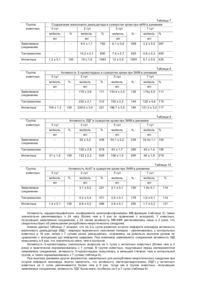
Изобретение относится к медицине, а именно к фармакологии, в частности к новым биологически активным химическим соединениям, на основе которых могут быть созданы лекарственные препараты антигипоксического, церебропротекторного и кардиопротекториого действия. Наиболее близким структурным аналогом заявляемого соединения является морфолиний 3-метия1,2,4-триазолил-5-тиоацетат, проявляющий гепатозащитную, ранозаживляющую и противовирусную активность (см. п. Украины № 1988, приоритет от 22.12.86, опубл. 20.12.94, М.Кл.4 C07D 413/12, А61К 31/41, А61К 31/535). Торговое название морфолиния 3-метил-1,2,4-триазолил-5-тиоацетата-тиотриазолин. Известное соединение обладает слабо выраженными антигипоксической, церебропротекторной и кардиопротекторной активностями. В основу изобретения поставлена задача создания нового биологически активного химического соединения, химическая структура которого обеспечивает антиоксидантные свойства и за счет этого заявляемое соединение проявляет антигипоксическую, церебропротекторную и кардиопротекторную активность при низкой токсичности. Поставленная задача решается тем, что получен морфолиний 3-(4-пиридил)-1,2,4-триазолил-5тиоацетат, проявляющий антигипоксическую, церебропротекторную и кардиопротекторную активность. Заявляемое соединение обладает антиоксидантними свойствами, т.е. препятствует окислению и образованию свободных радикалов в организме, которые возникает при гипоксии, нарушениях мозгового кровообращения и инфаркте миокарда. Заявляемое соединение обладает мембраностабилизирующим действием, что препятствует разрушению клеточных и субклеточных структур. Предотвращение образования свободных радикалов в организме и мюмбраностабилизирующее действие заявляемого соединения и обусловливают его антигипоксическую, церебропротекторную и кардиопротекторную активность. Заявляемое соединение получают следующим образом. Смешивают 0,02 моля 1-изоникотиноил-изотиосемикарбазид- S -уксусной кислоты с 0,02моли морфолина в 20мл этанола и кипятят в течение 6час. Растворитель упаривают, получая заявляемое соединение. Выход: 97%. Желтоватое кристаллическое вещество, легко растворимо в воде, трудно растворимо в спиртах, нерастворимо в эфире и гексане. Тпл – 203 - 205°С Найдено, %: s 9,7 Вычислено, %: s 9,9 ИК-спектр, см-1: волновое число у СОО - 1600 (асс.), 1360(сим.) Врутто-формула: С13 Н17 N5 O3 S Заявляемое соединение обладает антигипоксической, церебропротекторной и кардиопротекторной активностью. ЛД50 заявляемого соединения при внутрибрюшинном введении белым мышам составляет 5000мг/кг, при внутрибрюшинном введении белым крысам - 3500мг/кг, при внутривенном введении кошкам - 850мг/кг. Исследование биологической активности заявляемого соединения показало, что в экспериментах на животных данное соединение проявляет антигипоксическую, церебропротекторную и кардиопротекторную активность. Изучение антигипоксического действия заявляемого соединения проводили на белых мышах-самцах массой 15 - 20г. Антигипоксическое действие изучали по времени выживании животных в условиях гипобарической и токсической гипоксемичеокой гипоксии. Группам животных вводили заявляемое соединение, тиотриаэолин (прототип), а также гутимин и пирацетам - известные антигипоксические препараты. Указанные соединения вводили с помощью желудочного зонда в желудок за 1 час до проведения эксперимента в среднетерапевтических дозах, пересчитанных с учетом коэффициента церебрации. В качестве базы сравнения была выбрана контрольная группа животных, которой не вводили антигипоксические препараты. Результаты исследований антигипоксической активности заявляемого соединения приведены в таблице I. Анализ данных, приведенных в таблице 1, показал, что заявляемое соединение повышает устойчивость животных к гипобарической гипоксии более чем в 2,5 раза, тогда как тиотриазолин (прототип) в ~ 1,5 раза. Заявляемое соединение превосходит по антигипоксической активности и известные антиоксиданты - пирацетам и гутимин. Таблица 1 № Группы животных Вводимое соединение Доза, мг/кг 1 2 3 Гипобарические жизни Цитотоксические жизни минуты % минуты % 4 5 6 7 1 Интактные 2,69 ± 0,18 100 26,7 ± 1,39 100 2 50 6,93 ± 0,31 258 50,4 ± 2,7 189 3 Заявляемое соединение Тиотриазолин 50 3,84 ± 0,21 143 33,2 ± 1,7 124 4 Пирацетам 250 6,50 ± 0,51 242 45,3 ± 2,9 170 5 Гутимин 5 6,43 ± 0,41 239 35,4 ± 1,8 133 Церебропротекторную активность заявляемого соединения исследовали на экспериментальных моделях циркуляторной гипоксии у крыс. Для этого была выбрана модель перевязки внутренних сонных артерий, имитирующая ишемическое повреждение мозга и модель тромботического инсульта, заключавшаяся во введении в общую сонную артерию 1,1ед. тромбина в объеме физиологического раствора 0,1мл на 1 крысу массой 200 - 220г с последующей ее перевязкой, что имитирует картину тяжелого тромботического инсульта, подтвержденную на биохимическом и гистохимическом уровне. Опыты проводили на белых крысах линии Вистар обоего пола, массой 160 - 180г, прошедших карантин и содержащихся на стандартном рационе. Исследования включали изучение ребэнцефалограммы методом вживления электродов, определение напряжения кислорода (РО2) методом игольчатой полярографии. Изучалась микроструктура тканей головного мозга, биохимические показатели углеводно-энергетического обмена в тканях головного мозга, печени, крови, продукты перекисного окисления липидов. Курсовое введение заявляемого соединения в течение 4-х суток после операции в желудок животного в дозе 50мг/кг приводит к нормализации алектрофизиологических показателей и структурных изменений. Увеличивался реографический индекс, форма РЭГ-кривой приближалась к норме у животных с перевязкой и улучшалась по изучаемым показателям у животных с тромботическим повреждением мозга. У всех опытных животных уменьшались различия РЭГ-кривых между полушариями опытных животных. Полная нормализация микроциркуляции наступила у животных с ишемическим повреждением и улучшилась у животных с тромботическим повреждением. Это способствовало улучшению кислородного режима тканей, что проявлялось достоверным повышением PO2 в обеих группах. К улучшению микроциркуляции крови приводило заключительное уменьшение зоны периваскулярного и перицеллюлярного отека. Коэффициент ткань мозга/высушенная ткань уменьшился, что подтверждает уменьшение отека-набухания мозга. При ШИК-реакции наблюдались единичные фрагменты разволокнения эндотелия капилляров. Результаты изучения биохимических показателей углеводно-энергетического обмена в тканях головного мозга крыс при односторонней перевязке и тромботическом повреждении, а также при протективном введении заявляемого соединения и препарата сравнения (тиотриазолина) представлены в таблице 2. Из данных, приведенных в таблице 2, видно, что введение заявляемого соединения белым крысам в остром периоде очагового нарушения мозгового кровообращения (ОНМК), вызванного односторонней перевязкой общей сонной артерии (графа 5 табл.2), приводит к увеличению в тканях головного мозга содержания глюкозы и гликогена, Таблица 2 Группа животных Показатели 1 Интактные Перевязка Тромбоз Заявляемое Заявляемое соединение + соединение + перевязка тромбоз Тиотриазолин Тиотриазолин + перевязка + тромбоз АТФ 7 8 1,080±0,054 1,62±0,078 (26,5) (17,4) (80,5) (73,3) (70,5) (66,1) 3,600±0, 029 2,38±0;13 2,07±0,03 2,98±0,122 2,64±0,093 2,54±0,18 2.380±0,125 (66,1) (57,5) (82,7) (73,3) (70,5) (66,1) 2,705±0,374 5,70±0,493 6,84±0,571 3,20±0,31 4,87±0,241 5,73±0+317 6,72±0,254 (210,7) (252,9) (118,3) (180) (211) (248) 0,17±0,018 0,072±0,008 0,054±0.012 0,107±0,01 0,089±0,09 0,890±0,03 0,72±0,01 о* (42,3) (31,7) (62,9) (52,3) (523) (423) 0,34±0,045 0,28±0,026 0,17±0,03 0,31±0,04 0,239±0,091 0,277±0,026 0,234±0,38 (82,3) (50) (91,1) (69) (81) (68) 0,71±0,105 0,42±0,099 0,42±0,086 0,54±0,104 0,477±0,179 0,486±0,16 0,472±0,18 (100) Изоцитрат 6 1,80±0,043 (100) Малат 5 2,040±0,080 (100)) Пируват 4 0+441±0,612 (100) Лактат 3 0,670±0,78 (1001) Глюкоза 2 2,5-33±0,025 (100) Гликоген (59,1) (59,1) (67,2) (68+4) (66,2) (66,4) 2,000±0,08 1,28±0.09 1,24±0,094 1,83±0,091 1,52±0,094 1,62±0,08 1,38±0,052 (100) (91,5) (76) (81) (69) 0,120±0,006 0,28±0,08 0,29±0,022 0,173±0,04 0,181±0,09 0,17±0,01 0,175±0,021 (218,8) (226,6) (135,1) (141,4) (132) (135) 3,60±0,23 1,60±0,12 1,48±0,146 2,80±0,131 2,550±0,31 1,73±0,54 1,61±0,12 (100) КΦ (62) (100) АМФ (64) (44,4) (41,1) (77,7) (70,8) (48) (44,7) снижению в тканях мозга лактата, увеличению содержания пирувата, увеличивался общий пул электрического заряда. Достоверно увеличилось содержание креатинина. При введении заявляемого соединения на фоне тромботического ОНМК (графа 6 табл.2) также отмечалось изменение почти всех (за исключением изоцитрата, АМФ) показателей энергетического обмена. Так, по сравнению с 3-й группой животных (графа 4 табл.2) увеличилось содержание гликогена, имело тенденцию к повышению содержанке глюкозы, уменьшилось содержание лактата, несколько повысилось содержание пирувата, увеличилось содержание креатинфосфата. Эти данные свидетельствуют о том, что введение заявляемого соединения оказывает протективное действие при ОНМК за счет улучшения энергетических процессов в головном мозге. Защитное метаболическое действие заявляемого соединения выше по сравнению с тиотриазолином (прототипом) по всем изучаемым показателям (см. графы 7, 8 табл.2). Исследование влияния заявляемого соединения на содержание продуктов перекисного окисления липидов проведено на модели ишемического ОНМК (односторонняя перевязка). Препараты сравнения пирацетам и тиотриаэолик (прототип). Результаты исследований представлены в таблице 3. Из данных приведенных в таблице 3, видно, что введение заявляемого соединения перед перевязкой внутренней сонной артерии вызывает нормализацию активности липидов по всем показателям. По ряду показателей (α-ТФ, супероксиддисмутаза, каталаза) действие заявляемого соединения сравнимо с действием пирацетама, по остальным показателям - превосходит его. По сравнению с тиотриазолином (прототипом) заявляемое соединение проявляет более высокие антиоксидантные свойства. Проведено также изучение влияния заявляемого соединения на Таблица 3 Показатели Группа животных Контроль Перевязка Заявленное соединение + перевязка Пирацетам + перевязка Тиотриазолин + перевязка нкат/л % нкат/л % нкат/л % нкат/л % нкат/л % 0,17±0,01 100 0,56±0,04 329 0,24±0,2 141 0,4±0,1 235 0,45±0,1 265 α - ТФ 5,4±0,2 100 3,9±0,4 92,2 4,86±0,31 90 4,6±0,8 85 4,0±0,18 74 COD 189,7±11,4 100 72,5±9,2 38,2 168,3±8,9 89 200,6±4,5 106 150±7,3 79 Каталаза ГПР 11,4±0,2 100 5,8±0,4 50,8 8,7±6,4 76,3 12,0±0,18 105 7,7±0,2 67,5 95,2±7,0 100 68,5±7,0 72,3 91,7±5,8 96 82±6,7 86 80±6,4 84 MDA 0,2±0,03 100 0,57±0,04 285 0,33±0,05 165 0,38±0,02 190 0,44±0,03 220 DK изоферменты креатинфосфатазы (КФК) при экспериментальной ОНМК. Результаты исследований представлены в таблице 4. Как видно из представленных в таблице 4 данных, заявляемое соединение уменьшает уровень гиперферментемии за счет всех фракций. Это свидетельствует о стабилизации мембранных образований клеток мозга под влиянием заявляемого соединения. Сравнение заявляемого соединения с тиотриазолином показывает, что заявляемое соединение обладает более высоким мембраностабилизируюшим действием. Таким образом, проведенные исследования (табл.2, 3, 4) подтверждают, что заявляемое соединение обладает выраженным церебротекторным действием, по силе превосходящим действие тиотриазолина (прототип). Исследование кардиопротекторной активности заявляемого соединения проводили следующим образам. У белых крыс-самцов линии Вистар массой 180 - 220г моделировали по общепринятой методике экспериментальный инфаркт миокарда (ЭИМ), а именно: изадрин-питуитриневую модель инфаркта миокарда, заключающуюся в последовательном внутрибрюшинном введении изадрина в дозе 100мг/кг подкожно и через 1 час - питуитрина в дозе 0,5ЕД на 1кг. За 1 час до эксперимента одной группе животных превентивно вводили заявляемое соединение в дозе 50мг/кг, другой - препарат сравнения - тиотриазолин (прототип) в доза 50мг/кг, третья группа - интактные животные. На модели циркуляторной гипоксии в результате острого инфаркта миокарда исследовали влияние заявляемого соединения на активность кардиоспецифичного изофермента креатинфосфокиназы МВфракции (МВ-КФК), общей креатинфосфокиназы (КФК), на содержание мало Таблица 4 Группа животных Активность КΦК ММ MB ВВ ЛДГ нкат/л % нкат/л % нкат/л % нкат/л % Контроль 1,38 ± 0,04 100 0,77 ± 0,03 100 0,5 ± 0,02 100 2,01 ± 0,43 100 Перевязка 1,94 ± 0,04 140,6 0,99 ± 0,02 128,6 1,01 ± 0,03 202 4,06 ± 0,32 202 1,68 ± 0,03 121,7 0,81 ± 0,03 105,2 0,67 ± 0,03 134 2,44 ± 0,37 121,4 1,8 ± 0,02 130 0,90 ± 0,02 117 0,72 ± 0,02 144 3,05 ± 0,42 152 Заявляемое соединение + перевязка Тиотриазолин + перевязка нового диальдегида (МД), характеризующего перекисное окисление липидов, а также на активность ферментов, характерных для резо-рбтивно-некротического синдрома при остром инфаркте миокарда: 5-нуклеотидазы; лактатдегидрогенаэы (ЛДГ); аспартаттранеаминазы (АсАТ). Активность указанных ферментов в сыворотке крови исследовали в динамике через определенные промежутки времени от момента введения питуитрина по сравнение с интактными животными. Результаты проведенных исследований кардиопротекторной активности заявляемого соединения приведены в таблицах 5 - 10: таблица 5 - влияние заявляемого соединения на активность изофермента МВ-КФК в сыворотке крови при ЭИМ; таблица 6 - влияние заявляемого соединения на активность общей КФК в сыворотке крови ври ЭИМ; таблица 7 - влияние заявляемого соединения на содержание малонового диальдегида в сыворотке крови при ЭИМ; таблица 8 - влияние заявляемого соединения на активность 5-нуклеотидазы в сыворотке крови при ЭИМ; таблица 9 - влияние заявляемого соединения на активность ДДГ в сыворотке крови ври ЭИМ; таблица 10 - влияние заявляемого соединения на активность АсАТ, в сыворотке крови при ЭИМ. Из таблицы 6 видно, что активность обшей креатинфосфокиназы (КФК) достоверно увеличивалась к 24 часам, превышая исходный уровень более чем в 4 раза. У животных, превентивно подучивших заявляемое соединение, также отмечался прирост активности, обшей КФК, однако к 24 часам ее активность не превысила исходную и в 2 раза. Группа животных Таблица 5 Активность иэофермента МВ-КФК в сыворотке крови при ЭИМ в динамике, нкат/л (%) 0 час 6 час 8 час 10 час 24 час 48 час Заявляемое соединение 7,8±0,2 10,5±0,3 13,0±0,5 14,0±0,2 6,6±0,1 (139%) (187%) (232%) (250%) (118%) Тиотриазо-лин 12,1±0,4 15,0±0,5 19,0±0,5 25,0±0,7 7,8±0,3 (216%) (268%) (339%) (446%) (139%) 5,6*0,3 16,3±0,5 22,0±0,7 28,0±1,0 32,0±0,9 9,4±0,3 (100%) (273%) (393%) (500%) (871%) (168%) Интактмые Таблица 6 Группа животных Активность общей КФК в сыворотке крови при ЭИМ в динамике, нкат/л (%) 6 час 12 час 24 час 48 час 136 ± 3 152 ± 6 178 ± 3,2 112 ± 4 (142%) (158%) (185%) (117%) 170 ± 6 206 ± 11 225 ± 4,1 130 ± 3,2 (177%) Заявляемое 0 час (215%) (234%) (135%) 96 ± 6,1 189 ± 5 282 ± 12 485 ± 11 143 ± 3,8 (100%) (197%) (294%) (505%) (149%) соединение Тиотриазолин Интактные Группа животных Таблица 7 Содержание малонового диальдегида в сыворотке крови при аИМ в динамике 0 сут 2 сут 5 сут 7 сут мк/моль % мл мк/моль % мл мк/моль % мл мк/моль % мл Заявляемое соединение 9,5 ± 1,1 792 6,1 ± 0,9 508 3,2 ± 0,4 267 Тиотриазолин 10,2 ± 2,1 850 7,5 ± 0,7 625 4,6 ± 0,3 400 1,2 ± 0,1 100 19 ± 1,6 1583 12 ± 0,9 1000 8,1 ± 0,5 425 Интактные Группа животных Таблица 8 Активность 5-нуклеотидазы в сыворотке крови при ЭИМ в динамике 0 сут 2 сут 5 сут 7 сут мк/моль % мл мк/моль % мл мк/моль % мл мк/моль % мл Заявляемое соединение 178 ± 3,6 171 133,4 ± 2,5 128 115± 4,5 111 Тиотриазолин 220 ± 2,1 212 150 ± 2,2 144 120 ± 4,6 115 104 ± 1,3 100 229,5 ± 3,4 221 186,7 ± 3,5 180 Интактные 121,3 ± 3,2 117 Таблица 9 Группа животных 0 сут мк/моль Активность ЛДГ в сыворотке крови при ЭИМ в динамике 2 сут 5 сут 7 сут % мл мк/моль % мл мк/моль % мл мк/моль % мл Заявляемое соединение 92 ± 3,2 438 50,1 ± 2,2 239 32,4± 1,1 154 Тиотриазолин 130 ± 2,8 619 83 ± 1,7 395 40 ± 1,4 190 21 ± 1,9 100 132 ± 2,2 629 106 ± 1,5 505 46 ± 1,8 219 Интактные Таблица 10 Группа животных 0 сут мк/моль Активность АсАТ в сыворотке крови при ЭИМ в динамике 2 сут 5 сут 7 сут % мл мк/моль % мл мк/моль % мл мк/моль % мл Заявляемое соединение 3,1 ± 0,2 221 2,1 ± 0,1 150 1,6± 0,1 114 Тиотриазолин 5,2 ± 0,4 371 2,5 ± 0,1 179 1,6 ± 0,1 114 1,4 ± 0,1 100 6,8 ± 0,2 486 2,8 ± 0,1 200 1,7 ± 0,2 121 Интактные Активность кардиоспецифичного изофермента креатинфосфокиназы МВ-фракции (таблица 5) также значительно увеличивалась к 24 часу (более чем в 5 раз по сравнению с исходной). У животных, получивших заявляемое соединение, к 24 часам активность МВ-КФК увеличивалась лишь в 2 раза, что свидетельствует об уменьшении резорбтивно-некротического синдрома. Анализ данных таблицы 7 показал, что на 2-е сутки развития острого инфаркта миокарда активность малонового диальдегида (МД) - маркера перекисного окисления липидов - увеличивалась у контрольных животных в 18 раз, затем к 7 суткам резко уменьшалась, сохраняясь на довольно высоком уровне по сравнению с исходными (до инфаркта) цифрами. Под влиянием заявляемого соединения активность МД повысилась в 8 раз, что значительно ниже, чем в контроле. Активность 5-нуклеотидазы значительно возросла на 2 сутки у интактных животных (более чем в 2 раза) и практически нормализовалась к 7 суткам. В группе животных, подучивших перед экспериментом заявляемое соединение, активность 5-нуклеотидазы повысилась в меньшей степени, чем в контрольной группе, и также нормализовалась к 7 суткам (таблица 8). При анализе динамики других ферментов, характерных для резорбтивно-некротического синдрома при остром инфаркте миокарда, можно заключить, что активность лактатдегидрогеназы (ЛДГ) у интактных животных на 2 сутки увеличивается более чем в 6 раз, тогда как в группе животных, получавших заявляемое соединение, активность ЛДГ была ниже, особенно на 5 и 7 сутки (таблица 9). Активность аспартаттрансаминазы (АсАТ) также значительно возросла на 2 сутки у интактных животных (в 5 раз по сравнению с исходными цифрами) и практически нормализовалась к 7 суткам. В группе животных, получавших перед экспериментом заявляемое соединение, активность АсАТ повысилась, однако была в 2 раза ниже, чем в контроле. Нормализация активности АсАТ наступила к 7 суткам (таблица 10). Полученные данные (таблицы 5 - 10) подтверждают, что заявляемое соединение обладает выраженной кардиопротекторной активностью при ЭИМ, более высокой по сравнению с тиотриазолином (прототипом). Положительное влияние заявляемого соединения заключается в значительном уменьшении уровня гиперферментемии, отражающей степень резорбтивно-некротического синдрома. Заявляемое соединение способствует ограничению зоны некроза миокарда, оказывает мощный мембраностабилизирующий эффект, сохраняя целостность как клеточных, так и внутриклеточных мембран миозитов. Кроме того, заявляемое соединение значительно уменьшает процесс перекисного окисления липидов, о чем свидетельствует уменьшение содержания малонового диальдегида. Таким образом, заявляемое соединение проявляет антигипоксическую, церебропротекторную и кардиопротекторную активность, превосходящую по силе как структурный ближайший аналог тиотриазолин, так и известные эталонные препараты аналогичного действия.
ДивитисяДодаткова інформація
Автори англійськоюVizyr Vadym Anatoliiovych, Drohovos Svitlana Mefodiivna, Zaichenko Hanna Volodymyrivna, Loziuk Liubov Vasylivna, Holovkin Viacheslav Oleksandrovych, Filimonov Volodymyr Ivanovych, Knysh Yevhenii Hryhorovych, Panasenko Oleksandr Ivanovych, Panasenko Oleksandr Ivanovych
Автори російськоюВизир Вадим Анатольевич, Дроговоз Светлана Мефодиевна, Зайченко Анна Владимировна, Лозюк Любовь Васильевна, Головкин Вячеслав Александрович, Филимонов Владимир Иванович, Кныш Евгений Григорьевич, Книш Евгений Григорьевич, Панасенко Александр Иванович
МПК / Мітки
МПК: A61P 39/06, C07D 413/02, C07D 249/12
Мітки: виявляє, морфоліній, 3-(4-піридил)-1,2,4-триазоліл-5-тіоацетат, активність, антигіпоксичну, церебропротекторну, кардіопротекторну
Код посилання
<a href="https://ua.patents.su/6-20388-morfolinijj-3-4-piridil-124-triazolil-5-tioacetat-shho-viyavlyaeh-antigipoksichnu-cerebroprotektornu-ta-kardioprotektornu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Морфоліній 3-(4-піридил)-1,2,4-триазоліл-5-тіоацетат, що виявляє антигіпоксичну, церебропротекторну та кардіопротекторну активність</a>
Попередній патент: Система автоматизованого керування насосними агрегатами
Наступний патент: Пневматичний гальмовий привід транспортних засобів
Випадковий патент: Стрічка для кругового пломбування "mehran nano silicon-silver lent"