Кристалічна структура комбінованого лікарського препарату антиагрегативної дії у формі таблеток
Номер патенту: 57179
Опубліковано: 10.02.2011
Автори: ШТЕЙНГАРТ Марк Вольфович, Приходько Роман Миколайович
Формула / Реферат
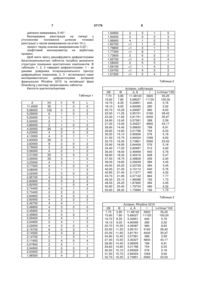
1. Кристалічна структура комбінованого лікарського препарату антиагрегативної дії, яка відрізняється тим, щопри кількості ацетилсаліцилової кислоти 150 мг і магнію гідроксиду 30,4 мг таблетки мають наступну кристалічну структуру:
Аспірин 150 мг і магнію гідроксид 30,4 мг
2Ө
Ө
d, Å
І
І=І/Іmах*100
7,80
3,90
11,33423
3616
51,13
аспірин
9,60
4,80
9,21272
192
2,71
магнію гідроксид
15,60
7,80
5,68027
7072
100,00
аспірин
16,70
8,35
5,30851
224
3,17
аспірин
18,50
9,25
4,79587
2752
38,91
магнію гідроксид
20,80
10,40
4,27046
1184
16,74
аспірин + магнію гідроксид
22,70
11,35
3,91714
3488
49,32
аспірин
23,30
11,65
3,81761
2400
33,94
аспірин
27,00
13,50
3,30227
5024
71,04
аспірин
28,80
14,40
3,09985
224
3,17
аспірин
29,60
14,80
3,01786
96
1,36
аспірин
30,50
15,25
2,93083
96
1,36
аспірин
31,50
15,75
2,84004
384
5,43
аспірин
32,50
16,25
2,75490
832
11,76
аспірин
33,80
16,90
2,65186
128
1,81
аспірин + магнію гідроксид
34,50
17,25
2,59964
192
2,71
аспірин + магнію гідроксид
35,90
17,95
2,50141
352
4,98
аспірин
38,00
19,00
2,36786
2592
36,65
магнію гідроксид
40,50
20,25
2,22728
128
1,81
аспірин
42,00
21,00
2,15114
320
4,52
аспірин + магнію гідроксид
42,90
21,45
2,10808
192
2,71
аспірин + магнію гідроксид
43,70
21,85
2,07132
224
3,17
аспірин
50,80
25,40
1,79724
1088
15,38
аспірин + магнію гідроксид
2. Кристалічна структура за п. 1, яка відрізняється тим, що ацетилсаліцилова кислота має наступну кристалічну структуру:
Аспірин
2Ө
Ө
d, Å
І
І=І/Іmах*100
7,70
3,85
11,48120
3920
35,25
15,60
7,80
5,68027
11120
100,00
16,70
8,35
5,30851
640
5,76
18,10
9,05
4,90095
280
2,52
20,70
10,35
4,29087
960
8,63
22,50
11,25
3,95151
3160
28,42
23,30
11,65
3,81761
4000
35,97
24,90
12,45
3,57581
288
2,59
27,00
13,50
3,30227
4800
43,17
28,90
14,45
3,08935
768
6,91
29,60
14,80
3,01786
704
6,33
30,20
15,10
2,95926
576
5,18
31,50
15,75
2,84004
1056
9,50
32,70
16,35
2,73851
2560
23,02
33,90
16,95
2,64426
576
5,18
34,40
17,20
2,60697
512
4,60
36,00
18,00
2,49469
640
5,76
36,60
18,30
2,45516
608
5,47
37,50
18,75
2,39828
256
2,30
39,30
19,65
2,29248
384
3,45
40,50
20,25
2,22728
384
3,45
42,00
21,00
2,15114
640
5,76
42,80
21,40
2,11277
480
4,32
43,70
21,85
2,07132
864
7,77
46,30
23,15
1,96088
192
1,73
48,50
24,25
1,87695
384
3,45
50,80
25,40
1,79724
480
4,32
52,60
26,30
1,73990
192
1,73
3. Кристалічна структура за п. 1, яка відрізняється тим, що магнію гідроксид має наступну кристалічну структуру:
Магнію гідроксид
2Ө
Ө
d, Å
І
І=І/Іmах*100
9,60
4,80
9,21272
128
1,35
15,40
7,70
5,75358
96
1,01
18,40
9,20
4,82171
4280
45,15
30,80
15,40
2,90297
112
1,18
32,90
16,45
2,72231
448
4,73
38,00
19,00
2,36786
9480
100,00
43,00
21,50
2,10341
768
8,10
51,00
25,50
1,79066
4400
46,41
4. Кристалічна структура за п. 1, яка відрізняється тим, що має характерне значення відносної інтенсивності, яка проявляється при 2Ө=22,6º більше, ніж при 2Ө=23,3º.
5. Кристалічна структура за п. 1, яка відрізняється тим, що значення відносної інтенсивності при 2Ө=27º вище, ніж для субстанції аспірину.
Текст
УКРАЇНА (19) UA (11) 57179 (13) U (51) МПК (2011.01) A61K 31/185 (2011.01) A61K 45/00 МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ОПИС ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ видається під відповідальність власника патенту ДО ПАТЕНТУ НА КОРИСНУ МОДЕЛЬ (54) КРИСТАЛІЧНА СТРУКТУРА КОМБІНОВАНОГО ЛІКАРСЬКОГО ПРЕПАРАТУ АНТИАГРЕГАТИВНОЇ ДІЇ У ФОРМІ ТАБЛЕТОК 1 2 2. Кристалічна структура за п. 1, яка відрізняється тим, що ацетилсаліцилова кислота має наступну кристалічну структуру: Аспірин 2Ө Ө 7,70 3,85 15,60 7,80 16,70 8,35 18,10 9,05 20,70 10,35 d, Å 11,48120 5,68027 5,30851 4,90095 4,29087 І 3920 11120 640 280 960 І=І/Іmах*100 35,25 100,00 5,76 2,52 8,63 22,50 23,30 24,90 27,00 28,90 29,60 30,20 31,50 32,70 33,90 34,40 11,25 11,65 12,45 13,50 14,45 14,80 15,10 15,75 16,35 16,95 17,20 3,95151 3,81761 3,57581 3,30227 3,08935 3,01786 2,95926 2,84004 2,73851 2,64426 2,60697 3160 4000 288 4800 768 704 576 1056 2560 576 512 28,42 35,97 2,59 43,17 6,91 6,33 5,18 9,50 23,02 5,18 4,60 U (13) 57179 аспірин магнію гідроксид аспірин аспірин магнію гідроксид аспірин + магнію гідроксид аспірин аспірин аспірин аспірин аспірин аспірин аспірин аспірин аспірин + магнію гідроксид аспірин + магнію гідроксид аспірин магнію гідроксид аспірин аспірин + магнію гідроксид аспірин + магнію гідроксид аспірин аспірин + магнію гідроксид (11) І=І/Іmах*100 51,13 2,71 100,00 3,17 38,91 16,74 49,32 33,94 71,04 3,17 1,36 1,36 5,43 11,76 1,81 2,71 4,98 36,65 1,81 4,52 2,71 3,17 15,38 UA Аспірин 150 мг і магнію гідроксид 30,4 мг 2Ө Ө d, Å І 7,80 3,90 11,33423 3616 9,60 4,80 9,21272 192 15,60 7,80 5,68027 7072 16,70 8,35 5,30851 224 18,50 9,25 4,79587 2752 20,80 10,40 4,27046 1184 22,70 11,35 3,91714 3488 23,30 11,65 3,81761 2400 27,00 13,50 3,30227 5024 28,80 14,40 3,09985 224 29,60 14,80 3,01786 96 30,50 15,25 2,93083 96 31,50 15,75 2,84004 384 32,50 16,25 2,75490 832 33,80 16,90 2,65186 128 34,50 17,25 2,59964 192 35,90 17,95 2,50141 352 38,00 19,00 2,36786 2592 40,50 20,25 2,22728 128 42,00 21,00 2,15114 320 42,90 21,45 2,10808 192 43,70 21,85 2,07132 224 50,80 25,40 1,79724 1088 (57) 1. Кристалічна структура комбінованого лікарського препарату антиагрегативної дії, яка відрізняється тим, що при кількості ацетилсаліцилової кислоти 150 мг і магнію гідроксиду 30,4 мг таблетки мають наступну кристалічну структуру: (19) (21) u201009978 (22) 12.08.2010 (24) 10.02.2011 (46) 10.02.2011, Бюл.№ 3, 2011 р. (72) ПРИХОДЬКО РОМАН МИКОЛАЙОВИЧ, ШТЕЙНГАРТ МАРК ВОЛЬФОВИЧ (73) ПРИХОДЬКО РОМАН МИКОЛАЙОВИЧ 3 36,00 36,60 37,50 39,30 40,50 42,00 42,80 43,70 46,30 48,50 50,80 52,60 18,00 18,30 18,75 19,65 20,25 21,00 21,40 21,85 23,15 24,25 25,40 26,30 2,49469 2,45516 2,39828 2,29248 2,22728 2,15114 2,11277 2,07132 1,96088 1,87695 1,79724 1,73990 57179 640 608 256 384 384 640 480 864 192 384 480 192 5,76 5,47 2,30 3,45 3,45 5,76 4,32 7,77 1,73 3,45 4,32 1,73 9,60 15,40 18,40 30,80 32,90 38,00 43,00 51,00 3. Кристалічна структура за п. 1, яка відрізняється тим, що магнію гідроксид має наступну кристалічну структуру: Магнію гідроксид 2Ө Ө d, Å І 4,80 7,70 9,20 15,40 16,45 19,00 21,50 25,50 9,21272 5,75358 4,82171 2,90297 2,72231 2,36786 2,10341 1,79066 128 96 4280 112 448 9480 768 4400 1,35 1,01 45,15 1,18 4,73 100,00 8,10 46,41 4. Кристалічна структура за п. 1, яка відрізняється тим, що має характерне значення відносної інтенсивності, яка проявляється при 2Ө=22,6º більше, ніж при 2Ө=23,3º. 5. Кристалічна структура за п. 1, яка відрізняється тим, що значення відносної інтенсивності при 2Ө=27º вище, ніж для субстанції аспірину. І=І/Іmах*1 00 Корисна модель належить до галузі медицини, зокрема, до кардіології, а саме, до препарату твердої лікарської форми, що містить ацетилсаліцилову кислоту. Було встановлено існування двох кристалічних форм ацетилсаліцилової кислоти [РСТ US 2008/0319068А1 А61 К31/216, С07С 69/60]. В німецькому патенті DE 102006045780А1, 2008-04-10, С07С69/86; С07С67/08; С07С67/52 SCICONCEPT GMBH показано можливість і умови створення змішаних кристалів ацетилсаліцилової кислоти, що мають різну стабільність. Досліджень структури такого препарату, який би мав два компоненти ацетилсаліцилову кислоту та магнію гідроксиду, не має. Такі дослідження мають як науковий, так і практичний інтерес, тому що можуть показати вплив змін структур на фізикомеханічні (міцність і стиранність) і біофармацевтичні властивості (розчинення, розпадання, стабільність лікарської форми). Крім того, ці дослідження дозволять встановити, як впливає волога грануляція або пряме пресування, що застосовані при виготовленні лікарської форми. В патенті фірми MERCK UA 57089, 16.06.2003 А61Р25/04, А61К3/5377, А61Р1/08, C07D413/06 вважається необхідним при застосуванні похідних морфоліну або тіоморфоліну як лікарських речовин при лікуванні деяких психічних розладів визначення кристалічної структури діючих речовин. 2Ө 7,80 9,60 15,60 16,70 18,50 4 Визначення кристалічної форми лікарської субстанції вважається необхідним для багатьох препаратів, наприклад, періндоприлу [патенти UA 57187 16.06.2003, А61К45/00, А61К31/404, А61К3/53, C07D209/08C07D209/42] і інших, особливо в тих випадках, коли можливе утворення різних поліморфних структур. Фармакопея США для карбамазепіну дозволяє використовувати лише одну з 5 відомих поліморфних форм. (5 видання, 2005 р, стор. 341) Найближчим до корисної моделі, що заявляється, є патенті UA 28988 25.12.2007, C07D209/42, в якому показана необхідність визначення кристалічної структури лікарської речовини в твердих лікарських формах, де вона застосовується разом з іншими кристалічними допоміжними речовинами. В основу корисної моделі поставлено задачу визначення кристалічної структури таблеток комбінованого лікарського препарату антиагрегативної дії для встановлення, з якої кристалічної субстанції виготовлені таблетки, а також можливу зміну структури під час проведення технологічних операцій. Поставлену задачу, згідно з корисною моделлю, вирішують визначенням кристалічної структури таблеток препарату при кількості ацетилсаліцилової кислоти 150 мг і магнію гідроксиду 30,4 мг Аспірин 150 мг магнію гідроксид 30,4 мг Ө d, Å І І=І/Іmах*100 3,90 11,33423 3616 51,13 4,80 9,21272 192 2,71 7,80 5,68027 7072 100,00 8,35 5,30851 224 3,17 9,25 4,79587 2752 38,91 аспірин магнію гідроксид аспірин аспірин магнію гідроксид аспірин + магнію 5 57179 6 20,80 22,70 23,30 27,00 28,80 29,60 30,50 31,50 32,50 10,40 11,35 11,65 13,50 14,40 14,80 15,25 15,75 16,25 4,27046 3,91714 3,81761 3,30227 3,09985 3,01786 2,93083 2,84004 2,75490 1184 3488 2400 5024 224 96 96 384 832 16,74 49,32 33,94 71,04 3,17 1,36 1,36 5,43 11,76 33,80 16,90 2,65186 128 1,81 34,50 35,90 38,00 40,50 17,25 17,95 19,00 20,25 2,59964 2,50141 2,36786 2,22728 192 352 2592 128 2,71 4,98 36,65 1,81 42,00 21,00 2,15114 320 4,52 42,90 43,70 21,45 21,85 2,10808 2,07132 192 224 2,71 3,17 50,80 25,40 1,79724 1088 15,38 Ацетилсаліцилова кристалічну структуру 2Ө 7,70 15,60 16,70 18,10 20,70 22,50 23,30 24,90 27,00 28,90 29,60 30,20 31,50 32,70 33,90 34,40 36,00 36,60 37,50 39,30 40,50 42,00 42,80 43,70 46,30 48,50 50,80 52,60 кислота має Аспірин d, Å І 11,48120 3920 5,68027 11120 5,30851 640 4,90095 280 4,29087 960 3,95151 3160 3,81761 4000 3,57581 288 3,30227 4800 3,08935 768 3,01786 704 2,95926 576 2,84004 1056 2,73851 2560 2,64426 576 2,60697 512 2,49469 640 2,45516 608 2,39828 256 2,29248 384 2,22728 384 2,15114 640 2,11277 480 2,07132 864 1,96088 192 1,87695 384 1,79724 480 1,73990 192 Ө 3,85 7,80 8,35 9,05 10,35 11,25 11,65 12,45 13,50 14,45 14,80 15,10 15,75 16,35 16,95 17,20 18,00 18,30 18,75 19,65 20,25 21,00 21,40 21,85 23,15 24,25 25,40 26,30 наступну І=І/Іmах*100 35,25 100,00 5,76 2,52 8,63 28,42 35,97 2,59 43,17 6,91 6,33 5,18 9,50 23,02 5,18 4,60 5,76 5,47 2,30 3,45 3,45 5,76 4,32 7,77 1,73 3,45 4,32 1,73 Магнію гідроксид має наступну кристалічну структуру Магнію гідроксид 2Ө Ө d, Å І І=І/Іmах*10 0 9,60 15,40 18,40 30,80 32,90 38,00 43,00 51,00 гідроксид аспірин аспірин аспірин аспірин аспірин аспірин аспірин аспірин аспірин + магнію гідроксид аспірин + магнію гідроксид аспірин магнію гідроксид аспірин аспірин + магнію гідроксид аспірин + магнію гідроксид аспірин аспірин + магнію гідроксид 4,80 7,70 9,20 15,40 16,45 19,00 21,50 25,50 9,21272 5,75358 4,82171 2,90297 2,72231 2,36786 2,10341 1,79066 128 96 4280 112 448 9480 768 4400 1,35 1,01 45,15 1,18 4,73 100,00 8,10 46,41 Кристалічна структура має характерне значення відносної інтенсивності, яка проявляється при 2Ө=22,6° більше, ніж при 2Ө=23,3°. Значення відносної інтенсивності при 2Ө=27° вище, ніж для субстанції аспірину. Визначення кристалічної структури таблеток ацетилсаліцилової кислоти з магнію гідроксидом, що застосовуються в промисловому виробництві, дозволяють знайти показники структури субстанції, які відтворюються в лікарській формі незмінними, і дають змогу встановити, з якої кристалічної субстанції виготовлені таблетки, а також можливу зміну структури під час проведення технологічних операцій. Структурні зміни можуть пояснити природу зміни фізико-механічних властивостей таблеток і можуть бути використані як прогностичний тест в неруйнуючих дослідженнях. Для забезпечення ідентичності структури таблетки визначали ренгеноструктурні показники таблеток Кардіомагнілу 150/30,39 мг і досягай таких же показників в таблетках винаходу. Ці результати одержані при досліджені дифрактограм різних зразків таблеток і субстанції в наступних умовах: дифрактометр ДРОН 3, сцинтиляційний детектор; мідний антикатод λ=1,5405А°, напруга 40 кВ,сила струму 40 мА; розміщення θ-θ; 7 57179 діапазон вимірювань 5-40°; безперервна реєстрація на папері з уточненням положення шляхом точкової реєстрації з часом вимірювання на етапі 10 с; приріст перед кожним вимірюванням 0,02°; графітовий монохроматор на відбитому промені. Щоб мати змогу дешифрувати дифрактограми багатокомпонентних таблеток потрібно визначити структурні показники кристалічних компонентів. В таблицях 1, 2, 3 наведені дифрактограми: 1 - за даними довідника Інтернаціонального Центру дифракційних показників, 2, 3 - встановлені нами експериментально дифрактограми аспіринів франузської Rhodine 3210 та китайської фірм Shandong у вигляді запресованих таблеток Кислота ацетилсаліцилова Таблиця 1 d 11,4000 5,68000 5,29000 5,20000 5,00000 4,89000 4,30000 4,23000 4,13000 3,93000 3,83000 3,79000 3,56000 3,31000 3,29000 3,23000 3,17000 3,08000 3,02000 2,95700 2,84800 2,82000 2,74400 2,73400 2,64800 2,60000 2,49700 2,48800 2,45800 2,39800 2,29400 2,24600 2,22600 2,15700 2,14500 2,12700 2,11600 2,07800 2,04900 2,03000 1,96500 Int 35 100 6 2 2 2 20 4 4 35 8 2 4 20 25 4 2 2 2 4 6 2 6 2 2 4 4 4 6 2 2 2 4 6 4 2 2 2 2 2 2 h 1 0 1 1 1 1 0 2 2 2 2 3 2 3 3 3 1 1 3 3 0 1 3 2 4 2 4 3 4 3 4 4 3 0 4 1 4 5 0 2 4 K 0 0 0 1 1 0 1 0 1 1 0 0 1 0 1 1 2 1 0 1 2 0 1 2 0 2 1 2 1 2 1 1 2 3 2 3 0 1 3 3 2 L 0 2 2 1 1 2 2 2 1 1 2 0 2 2 0 1 0 3 2 2 2 4 2 1 2 2 1 0 2 1 2 3 2 1 1 1 4 1 2 1 2 8 1,94800 1,90000 1,86900 1,83700 1,79800 1,77300 1,73600 1,65700 1,58000 1,56100 1,54700 1,51500 2 2 4 1
ДивитисяДодаткова інформація
Назва патенту англійськоюCrystal structure of combined tableted antiaggregant
Автори англійськоюPrykhodko Roman Mykolaiovych, Shteinhart Mark Volfovych
Назва патенту російськоюКристаллическая структура комбинированного лекарственного препарата антиагрегантного действия b форме таблеток
Автори російськоюПриходько Роман Николаевич, Штейнгарт Марк Вольфович
МПК / Мітки
МПК: A61K 31/185, A61K 45/00
Мітки: лікарського, кристалічна, антиагрегативної, таблеток, препарату, комбінованого, форми, дії, структура
Код посилання
<a href="https://ua.patents.su/6-57179-kristalichna-struktura-kombinovanogo-likarskogo-preparatu-antiagregativno-di-u-formi-tabletok.html" target="_blank" rel="follow" title="База патентів України">Кристалічна структура комбінованого лікарського препарату антиагрегативної дії у формі таблеток</a>
Попередній патент: Комбінований лікарський препарат антиагрегативної дії у формі таблеток
Наступний патент: Кристалічна структура комбінованого лікарського препарату антиагрегативної дії у формі таблеток
Випадковий патент: Спосіб профілактики медикаментозної кропив'янки у дітей з дискінезіями жовчовивідних шляхів