Способи одержання 8-арилхіноліну та його солі бензолсульфонової кислоти
Номер патенту: 74862
Опубліковано: 15.02.2006
Автори: Хо Гуо-Дзіє, Пайпік Бренда, Драю Антуанетт, Лєблонд Карл, Десмонд Річард, Конлон Девід А., Вайлая Анант
Формула / Реферат
1. Спосіб одержання 6-[1-метил-1-(метилсульфоніл)етил]-8-[3-[(E)-2-[3-метил-1,2,4-оксадіазол-5-іл]-2-[4-(метилсульфоніл)феніл]етеніл]феніл]хіноліну формули:
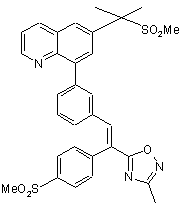 , (I)
, (I)
який включає взаємодію сполуки
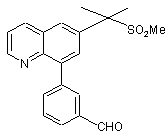
із сполукою
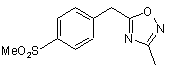
в присутності достатньої кількості основного ініціатора.
2. Спосіб одержання солі бензолсульфонової кислоти 6-[1-метил-1-(метилсульфоніл)етил]-8-[3-[(E)-2-[3-метил-1,2,4-оксадіазол-5-іл]-2-[4-(метилсульфоніл)феніл]етеніл]феніл]хіноліну формули (І), що характеризується піками 10.0, 19.5, 21.4, 22.4 і 30.5 дифракції рентгенівських променів порошку:
 , (I)
, (I)
що полягає в:
доданні достатньої кількості бензолсульфонової кислоти до сполуки (І) в достатній кількості складноефірного розчинника для утворення реакційної суміші;
доданні достатньої кількості спиртового розчинника до вказаної реакційної суміші для утворення реакційного розчину;
проведення кристалізації з утворенням кристалів, які характеризуються піками 10.0, 19.5, 21.4, 22.4 і 30.5 дифракції рентгенівських променів порошку.
3. Спосіб одержання солі бензолсульфонової кислоти 6-[1-метил-1-(метилсульфоніл)етил]-8-[3-[(E)-2-[3-метил-1,2,4-оксадіазол-5-іл]-2-[4-(метилсульфоніл)феніл]етеніл]феніл]хіноліну формули (І), що характеризується піками 14.4, 17.7, 20.0, 20.2, 23.7 і 28.9 дифракції рентгенівських променів порошку:
 , (I)
, (I)
який полягає в:
доданні достатньої кількості бензолсульфонової кислоти до сполуки (І) в достатній кількості з приблизно рівних об'ємів суміші складноефірного і спиртового розчинників для утворення реакційної суміші;
витримування реакційної суміші до розчинення твердих компонентів для утворення реакційного розчину;
проведення кристалізації, яка веде до утворення кристалів, що характеризуються піками 14.4, 17.7, 20.0, 20.2, 23.7 і 28.9 дифракції рентгенівських променів порошку.
Текст
1. Спосіб одержання 6-[1-метил-1(метилсульфоніл)етил]-8-[3-[(E)-2-[3-метил-1,2,4оксадіазол-5-іл]-2-[4(метилсульфоніл)феніл]етеніл]феніл]хіноліну формули: 2 3 74862 4 який полягає в: доданні достатньої кількості бензолсульфонової кислоти до сполуки (І) в достатній кількості з приблизно рівних об'ємів суміші складноефірного і спиртового розчинників для утворення реакційної суміші; витримування реакційної суміші до розчинення твердих компонентів для утворення реакційного розчину; проведення кристалізації, яка веде до утворення кристалів, що характеризуються піками 14.4, 17.7, 20.0, 20.2, 23.7 і 28.9 дифракції рентгенівських променів порошку. SO2Me N O N N MeO2S , (I) Даний винахід відноситься до способу одержання бензолсульфонової солі заміщених 8арилхінолінів. Більш точно, даний винахід відноситься до способу одержання 6-[1-метил-1(метилсульфоніл)етил]-8-[3-[(Е)-2-[3-метил-1,2,4оксадіазол-5-іл]-2-[4(метилсульфоніл)феніл]етеніл]феніл]хінолінію бензолсульфонату, що є інгібітором фосфодіестерази-4. Гормони являють собою сполуки, що різними шляхами впливають на клітинну активність. У багатьох відношеннях, гормони діють як месенджери, що ініціюють певні клітинні реакції і типи активності. Однак, багато які дії, що здійснюються гормонами, не є слідством дії виключно тільки гормону. Навпаки, спочатку гормони зв'язуються з рецептором, таким чином, ініціюючи звільнення вторинної сполуки, яка потім впливає на клітинну активність. У такій схемі, гормон відомий як первинний месенджер, в той час як вторинна речовина називається вторинним месенджером. Циклічний аденозинмонофосфат (аденозин 3',5'цикломонофосфат, "цАМФ" або "циклічний АМФ") відомий як вторинний месенджер гормонів, що включають адреналін, глюкагон, кальцитонін, кортикотропін, ліпотропін, лютеїнізуючий гормон, норепінефрин (норадреналін), паратиреоїдний гормон, тиреотропний гормон, і вазопресин. Таким чином, цАМФ є посередником клітинної відповіді на дію гормонів. Циклічна АМФ також опосередковує клітинну відповідь на різні нейромедіатори. Фосфодіестерази ("ФДЕ") є сімейством ферментів, які в ході обміну перетворюють 3', 5' циклічні нуклеотиди в 5'нуклеозидмонофосфати, таким чином, придушуючи активність цАМФ, як вторинного месенджера. Викликають істотний інтерес такі ФДЕ, як фосфодіестераза-4 ("ФДЕ4", також відома як "ФДЕІV"), що володіє високою спорідненістю, цАМФ специфічна, ФДЕ типу IV, як потенційна мішень для розробки нових антиастматичних і протизапальних сполук. Відомо, щонайменше, існування чотирьох ізоензимів ФДЕ4, кожний з яких кодується окремим геном. Передбачається, що кожний з цих чотирьох відомих продуктів гена ФДЕ4 грає різні ролі в алергічних і/або запальних реакціях. Таким чином, вважається, що інгібування ФДЕ4, і особливо специфічних ізоформ ФДЕ4, що викликають небажані реакції, може благотворно впливати на алергію і запальні симптоми. Було б бажано забезпечити нові речовини і сполуки, які придушують активність ФДЕ4. Речовини, які придушують активність ФДЕ4, є придатними для лікування ссавців, наприклад, у випадках астми, хронічних бронхітів, хронічної обструктивної хвороби легенів (ХОХЛ), еозинофільної гранулеми, псоріазу і інших доброякісних або злоякісних проліферативних шкіряних захворювань, ендотоксичного токсичного шоку (і пов'язаних станів таких як ламініти і коліки у коней), септичного шоку, неспецифічного виразкового коліту, хвороби Крона, реперфузійних пошкоджень міокарда і головного мозку, запальних артритів, остеопорозу, хронічних гломерулонефритів, атонічних дерматитів, кропивниці, респіраторного дистрессиндрому дорослих, респіраторного дистрессиндрому немовлят, хронічної обструктивної хвороби легенів (ХОХЛ) у тварин, нецукрового діабету, алергічного риніту, алергічного кон'юнктивіту, весняного кон'юнктивіту, артеріального рестинозу, атеросклерозу, нейрогенного запалення, болю, кашлю, ревматичного артриту, анкилозуючого спондилоартриту, відторгнення трансплантату і реакцій "трансплантат проти хазяїна", підвищеної секреції шлункового соку, сепсису або септичного шоку, індукованого бактеріями, грибком або вірусом, запалення і цитокін-опосередкованої хронічної дегенерації тканини, остеоартритів, карциноми, кахексії, гіпотрофії м'язів, депресії, порушення пам'яті, монополярної депресії, гострого і хронічного нейродегенеративного розладу із запальним компонентом, хвороби Паркінсона, хвороби Альцгеймера, спинномозкової травми, пошкодження голови, розсіяного склерозу, зростання новоутворень і злоякісної інвазії нормальних тканин. Основну заклопотаність при використанні інгібіторів ФДЕ4 викликає побічний ефект у вигляді блювоти, який спостерігається у деяких речовин-кандидатів, як це описане в С. Burnouf et al, ("Burnouf), Ann. Rep. In Med. Chem., 33:91-109 (1998). B.Hughes et al., Br.J.PharmacoL, 118:1183-1191 (1996); M.J.Perry et al., Cell Biochem.Biophys., 29:113-132 (1998); S.B.Christensen et al., J.Med.Chem.,. 41:821-835 (1998), Burnouf також описав широкий діапазон по тяжкості небажаних побічних дій, що виявляються 5 74862 6 різними сполуками. Як показано в M.D.Houslay et рошку поліморфу Форми А (нижня лінія) і Форми Б al., Adv. In Pharmacol., 44:3 3-89(1998), and D.Spina (верхня лінія) солі БСК і 6-[1-метил-1et al., Adv. In Pharmacol., 44:33-89(1998), існує ве(метилсульфоніл)етил]-8-[3-[(Е)-2-[3-метил-1,2,4ликий інтерес і інтенсивні дослідження відносно оксадіазол-5-іл]-2-[4терапії за допомогою інгібіторів ФДЕ4. (метилсульфоніл)феніл]етеніл]феніл]-хіноліну. Міжнародна патентна заявка W09422852 опиФіг.4 - діаграма характерних піків дифракції Хсує хіноліни як інгібітори ФДЕ4. променів на порошку поліморфу Форми А солі БСК A.H.Cook, et al., J.Chem.Soc, 413-417(1943) і 6-[1-метил-1-(метилсульфоніл)етил]-8-[3-[(Е)-2-[3метил-1,2,4-оксадіазол-5-іл]-2-[4описує -піридилхіноліни. Інші сполуки хінолінів (метилсульфоніл)феніл]етеніл]феніл] хіноліну. описані у Kei Manabe et al., J.Org.Chem., 58(24): Фіг.5 - діаграма характерних піків дифракції Х6692-6700 (1993); Kei Manabe et al., променів на порошку поліморфу Форми Б солі БСК J.Am.Chem.Soc, 115(12):5324-5325(1993); і Kei і 6-[1-метил-1-(метилсульфоніл)етил]-8-[3-[(Е)-2-[3Manabe et al., J.Am.Chem.Soc, 114 (17): 6940-6941 метил-1,2,4-оксадіазол-5-іл]-2-[4(1992). (метилсульфоніл)феніл]етеніл]феніл] хіноліну. Різними дослідниками описані сполуки, що Відповідно до даного винаходу одержують включають кільцеві системи, як ефективні в ряді сполуку ("вільну основу") випадків терапії. Наприклад, Міжнародна патентна заявка W098/25883 описує кетобензаміди як інгібітори калпаїну, Європейська патентна заявка ЕР 811610 і патентні заявки США 5,679,712, 5,693,672 і 5,747,541 описують заміщений бензоїлгуанідин як блокатор натрієвих каналів, патентна заявка США 5,736,297 описує кільцеві системи, що використовуються як фоточутливі склади. Патентні заявки США 5,491,147, 5,608,070, 5,622,977, 5,739,144, 5,776,958, 5,780,477, 5,786,354, 5,798,373, 5,849,770, 5,859,034, 5,866,593, 5,891,896 і Міжнародна патентна заявка W095/35283 описують інгібітори ФДЕ4, що є тризаміщеними арилабо гетероарилфеніл6-[1-метил-1-(метилсульфоніл)етил]-8-[3-[(Е)похідними. Патентна заявка США 5,580,888 описує 2-[3-метил-1,2,4-оксадіазол-5-іл]-2-[4інгібітори ФДЕ4, які є стирил-похідними. Патентна (метилсульфоніл)феніл]етеніл]феніл]хінолін назаявка США 5,550,137 описує інгібітори ФДЕ4, що ступним способом: є феніламінокарбоніл-похідними. Патентна заявка США 5,340,827 описує інгібітори ФДЕ4, що являють собою сполуки фенілкарбоксамідів. Патентна заявка США 5,780,478 описує інгібітори ФДЕ4, що є тетразаміщеними фенілпохідними. Міжнародна патентна заявка W096/00215 описує похідні заміщених оксимів, які використовуються як інгібітори ФДЕ4. Патентна заявка США 5,633,257 описує інгібітори ФДЕ4, які є цикло(алкіл і алкеніл)фенілалкеніл(арил і гетероарил)-сполуками. Однак, зберігається потреба в нових речовинах і сполуках, які з мінімальною побічною дією терапевтично інгібують ФДЕ4. Крім того залишається необхідність в ефективних способах виробництва сполук, що терапевтично інгібують ФДЕ4. Даний винахід відноситься до способу синтезу 6-[1-метил-1-(метилсульфоніл)етил]-8-[3-[(Е)-2-[3метил-1,2,4-оксадіазол-5-іл]-2-[4(метилсульфоніл)феніл]етеніл]феніл]-хіноліну і його бензолсульфонатної солі. Фіг.1 - діаграма залежності кількості відліків від ° при дифракції Х-променів на порошку поліморфу Форми А солі бензолсульфонової кислоти (БСК) і 6-[1-метил-1-(метилсульфоніл)етил]-8-[3Етап 1. Реакція Скраупа. [(Е)-2-[3-метил-1,2,4-оксадіазол-5-іл]-2-[4(метилсульфоніл)феніл]етеніл]феніл]хіноліну. Фіг.2 - діаграма залежності кількості відліків від °θ при дифракції Х-променів на порошку поліморфу Форми Б солі БСК і 6-[1-метил-1(метилсульфоніл)етил]-8-[3-[(Е)-2-[3-метил-1,2,4оксадіазол-5-іл]-2-[4(метилсульфоніл)феніл]етеніл] феніл]-хіноліну. До метансульфонової кислоти (8-10еквів.) при Фіг.3 - порівняння дифракції Х-променів на по20°С був доданий м-нїтробензолсульфонат натрію 7 74862 8 (0,6-0,8еквів.), з подальшим доданням гептагідрату Етап 5. Реакція приєднання Судзуки. сульфату заліза (0,01-0,05еквів.). До одержаної суміші був доданий 2-бром-4-метиланілін (1еквів.). Додали гліцерин (2-3еквів.), одержаний розчин нагрівався до 120-140°С і витримувався до повного завершення реакції. До розчину сульфону з попереднього етапу Суміш була охолоджена до 70-90°С і розбав(1еквів.) був доданий Pd/C (5-10ваг. %, 0,005лена водою. Потім розчин був охолоджений до 0,1еквів.), карбонат калію (2-3еквів.) і 320°С, і нейтралізований водним розчином NaOH і формілфенілборонова кислота (1-2еквів.). Реакбікарбонатом натрію. Був доданий МТВЕ (метилційна суміш, що дегазується, нагрівалася до 60трет-бутиловий ефір), суміш була відфільтрована і 120°С до повного завершення реакції. Суміш відфази розділені (продукт знаходився в шарі МТВЕ). фільтровували, і фільтрат був розведений у воді. Етап 2. Бромування. Продукт кристалізували, відділяли і висушували. Етап 6. Оксадіазол. У розчині з МТВЕ етапу 1 замінили розчинник на хлорбензол. Після фільтрації через силікагель і часткового упарювання, були додані Nбромсукцинімід (NBS, 0,6-0,8еквів.) і 2,2' -азо-бісізобутилнітрил (AIBN, 0,01-0,1еквів.). Суміш, що дегазується, нагрівали при 55-85°С. Одержану суміш розбавили циклогексаном. Додатково були додані NBS (0,3-0,5еквів.) і AIBN (0,01-0,05еквів.). Суміш, що дегазується, нагрівалася при температурі приблизно 55-85°С до повного завершення реакції. Одержану суміш охолодили до 10-40°С, розбавили циклогексаном і витримали. Тверду речовину відділили фільтрацією. Етап 3. Утворення сульфону. До розчину бромметил-бромхіноліну (продукт попереднього етапу, 1еквів.) в DMF був доданий порошкоподібний метансульфінат натрію (1,01,5еквів.) при 10-15°С. Суміш нагрівали до приблизно 50-70°С протягом 30хв. Суміш розбавляли водою при підтримці температури приблизно близько 50-70°С, при інтенсивному перемішуванні, потім суміш охолодили до 10-20°С і витримали. Суміш була відфільтрована і тверда речовина промита послідовно 1:4 DMF/водою і потім водою і висушена. Етап 4. Метилування. Розчин сульфону (продукт попереднього етапу, 1еквів.) в DMF був охолоджений до температури приблизно від -10 до 0°С. Був доданий третбутилат натрію (~1еквів.). Розчин метилйодиду/розчин DMF (~1еквів. МеІ) додавався повільно, і протягом цього часу підтримувалася температура приблизно від -10 до 0°С. Була додана друга частина твердого третбутилату натрію (~1еквів.), потім додавався метилйодид/розчин DMF (~1еквів. МеІ) протягом цього часу підтримували температуру приблизно від -5 до 10°С (якщо реакція не завершиться, додатково можуть бути додані основа і МеІ). Реакцію гасили доданням води, продукт кристалізувався, після чого його відділяли і висушували. До суміші гідрату гідроксибензотриазолу ("HOBt") (1-1,5еквів.), 4метилсульфонілфенілоцтової кислоти (1еквів.) в ацетонітрилі був доданий EDC гідрохлорид (11,5еквів.). Суспензію витримували при температурі приблизно 20-30°С протягом 30хв. Замість HOBt також можуть використовуватися інші N-OH сполуки, наприклад Nгідроксифталімід, 2-гідроксипіридин N-оксид, Nгідроксисукцинімід. Інші карбодііміди, такі як дициклогексилкарбодіімід і діізопропілкарбодіімід можуть бути використані замість EDC гідро хлориду (етилдиметиламінопропілкарбодііміду гідрохлорид). До суспензії був доданий оксим ацетаміду (11,5еквів.). Потім одержана суміш нагрівалася в колбі із зворотним холодильником доти, поки реакція повністю не завершилася. Одержаний розчин був упарений і розбавлений етилацетатом. Одержана суміш була промита водним розчином бікарбонату натрію. Була зроблена заміна розчинника на 2-пропанол, продукт був кристалізований при охолоджуванні, відділений і висушений. Етап 7. Реакція конденсації для одержання вільної основи. До суспензії альдегіду(1еквів.) з етапу 5, описаного вище, в 2-пропанолі був доданий оксадіазол (1-1,5еквів.), з етапу 6, описаного вище, з подальшим доданням піперидину (0,2-1,5еквів.). Замість 2-пропанолу, можуть бути використані інші розчинники, наприклад, DMF, ацетонітрил, 1пропанол, толуол, складні ефіри і інші спирти. Піперидин служить як основний ініціатор. Замість піперидину можуть бути використані інші основні аміни, особливо вторинні аміни. Одержана суміш нагрівалася в колбі із зворотним холодильником над молекулярними ситами до повного завершення реакції. Потім охолоджений продукт був відділений фільтрацією і висушений. 9 74862 10 Сіль вільної основи і бензолсульфонової кис22,4 лоти (БСК) існує в двох кристалічних формах 30,5 ("Форма А" і "Форма Б"). Форми були синтезовані наступними способами: Форма Б Етап 8. Утворення солі. До суспензії вільної основи (1еквів.) з етапу 7, описаного вище, в суміші ізопропілацетату (іРrОАс) і метанолу(1:1) була додана БСК (11,2еквів.). Замість i-PrOAc може бути використані інші складні ефіри, і замість метанолу можуть бути використані інші спирти такі, як етанол або пропанол. Суміш витримували при 20-50°С до повного розчинення твердої речовини. Одержану суміш Форма А фільтрували і переганяли, протягом цього часу До суспензії вільної основи (1еквів.) з етапу 7, підтримувався об'єм шляхом додання 9:1 (об./об.) описаного вище, в етилацетаті була додана бенсуміші і-РrОАс /метанол. Продукт кристалізувався золсульфокислота (1-1,2еквів.). Замість етилацепід час перегонки. тату може бути використані інші складні ефіри. Був Одержану суміш витримували при 20-70°С доданий метанол, і одержану суміш нагрівали до протягом 2-10 годин до забезпечення завершення повного розчинення твердої речовини. Замість утворення Форми Б. Одержана, білувата, тверда метанолу можуть бути використані інші спирти, речовина була виділена шляхом фільтрації і витакі як етанол або пропанол. сушена. Одержаний розчин відфільтрували і упарили. ВЕРХ показала 1:1 молярне співвідношення 6Під час упарювання продукт кристалізувався. [1 -метил-1-(метилсульфоніл)етил]-8-[3-[(Е)-2-[3Одержана суміш була розбавлена етилацетатом і метил-1,2,4-оксадіазол-5-іл]-2-[4витримана. Жовта тверда речовина була зібрана (метилсульфоніл)феніл]етеніл]феніл]хіноліну і шляхом фільтрації. ВЕРХ (високоефективна ріБСК. динна хроматографія) показала молярне співвідТочка плавлення по ДСК:210°С. ношення 1:1 6-[1-метил-1-(метилсульфоніл)етил]Спектрограма дифракції рентгенівських про8-[3-[(Е)-2-[3-метил-1,2,4-оксадіазол-5-іл]-2-[4менів на порошку ("ДРПП") для Форми Б показана (метилсульфоніл)феніл]етеніл]феніл]-хіноліну і на Фіг.2. Ідентифікуючі піки зведені в таблицю нибензолсульфонової кислоти. жче і показані на Фіг.5. На Фіг.3 спектри порівнюТочка плавлення по ДСК (диференціальній ються з ідентифікуючими піками, вказаними стрілскануючій калориметрії): 193°С. ками. Спектрограма дифракції рентгенівських променів на порошку ("ДРПП") для Форми А приведеПіки, що ідентифікують поліморф Форми Б (°2 ) на на Фіг.1. Ідентифікуючі піки зведені в таблицю 14,4 нижче і показані на Фіг.4. 17,7 20,0 Піки, що ідентифікують поліморф Форми Α (°2 ) 20,2 10,0 23,7 19,5 28,9 21,4 11 Комп’ютерна верстка Л. Купенко 74862 Підписне 12 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethods for producing 8-aryl quinoline and its benzenesulfonic acid salts
Назва патенту російськоюСпособы получения 8-арилхинолина и его соли бензолсульфоновой кислоты
МПК / Мітки
МПК: A61P 1/00, A61P 7/00, A61P 27/14, A61P 17/00, A61P 25/16, A61P 11/00, A61P 31/04, A61P 25/28, A61P 19/02, A61P 11/14, A61P 9/10, A61K 31/4709, A61P 39/02, A61P 13/12, A61P 19/10, A61P 37/06, A61P 29/00, A61P 35/00, A61P 11/02, A61P 7/12, A61P 1/04, A61P 11/08, A61P 11/06, A61P 17/06, C07D 413/10, A61P 25/24, A61P 25/00
Мітки: 8-арилхіноліну, одержання, способи, кислоти, бензолсульфонової, солі
Код посилання
<a href="https://ua.patents.su/6-74862-sposobi-oderzhannya-8-arilkhinolinu-ta-jjogo-soli-benzolsulfonovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Способи одержання 8-арилхіноліну та його солі бензолсульфонової кислоти</a>
Попередній патент: Лікарський препарат, що містить вінпоцетин
Наступний патент: Контактний пристрій для рознімного з’єднання рухомого приладового блока з нерухомими контактними тілами
Випадковий патент: Апаратно-програмний комплекс "кондор"










