Спірогетероциклічні сполуки як антагоністи mglu5
Номер патенту: 110343
Опубліковано: 25.12.2015
Автори: Леонарді Амедео, Гуарнері Лучіано, Мотта Джіанні, Ріва Карло, Гразіані Давіде, де Тома Карло, Карамфілова Катя Дімітрова
Формула / Реферат
1. Сполука загальної формули І
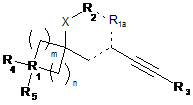 ,
,
I
де
X являє собою атом кисню або сірки;
R1 являє собою атом вуглецю, азоту, кисню або сірки;
R1а являє собою СН-, СН2-, N- або NH-фрагмент;
R2 являє собою валентний зв'язок або СН- або СН2-групу;
R3 являє собою необов'язково заміщену С1-С6алкільну групу, необов'язково заміщену моно-, бі- або трициклічну С1-С13гетероциклічну групу з 1-5 гетероатомами, вибраними з N, О та S, необов'язково заміщену моно-, бі- або трициклічну С6-С14арильну групу, необов'язково заміщену С3-С6циклоалкільну групу або необов'язково заміщену С3-С6циклоалкенільну групу;
якщо R1 являє собою атом вуглецю:
R4 являє собою атом водню, атом галогену, необов'язково заміщену моно- або біциклічну С1-С9гетероциклічну групу з 1-3 гетероатомами, вибраними з N, О та S, або необов'язково заміщену моно-, бі- або трициклічну С6-С14арильну групу;
R5 являє собою атом водню або галогену, ціаногрупу або необов'язково заміщену гідрокси, меркапто, аміно, карбамоїльну, С1-С6алкільну або С1-С6алкоксигрупу, або групу формули -C(=O)-R6, де R6 являє собою необов'язково заміщену С1-С6алкільну або С1-С6алкоксигрупу, необов'язково заміщену моно- або біциклічну С1-С9гетероциклічну групу з 1-3 гетероатомами, вибраними з N, О та S, або необов'язково заміщену моно-, бі- або трициклічну С6-С14арильну групу;
або
R4 та R5 разом представляють оксогрупу або необов'язково заміщену метиленову або гідроксііміногрупу; або
R4 та R5 разом з R1 представляють необов'язково заміщене ненасичене 4-6-членне кільце з 0-3 гетероатомами, вибраними з N, О та S;
якщо R1 являє собою атом кисню:
R4 та R5 відсутні;
якщо R1 являє собою атом азоту:
один з R4 та R5 відсутній та інший такий, як визначено вище;
якщо R1 являє собою атом сірки:
кожний з R4 та R5 незалежно відсутній або являє собою оксогрупу;
m дорівнює 1, 2 або 3;
n дорівнює 1 або 2;
якщо n дорівнює 2 або m дорівнює 2 або 3, кільце, що містить R1, може бути cконденсованим з необов'язково заміщеним бензольним кільцем; та
кожний ---- являє собою простий або подвійний зв'язок, за умови, що один подвійний зв'язок відходить від атома вуглецю, з яким R3-C≡C- зв'язаний, та що жодний кільцевий атом вуглецю не несе два подвійні зв'язки;
необов'язкові замісники, незалежно вибрані з атома галогену та С1-С6алкільної, С1-С6алкокси, гідрокси, меркапто, нітро, ціано, оксо, галоген(С1-С6)алкільної, галоген(С1-С6)алкокси, С1-С6алкілтіо, С1-С6алкілсульфонільної, С1-С6алкілкарбонільної, сульфамоїльної, С1-С6алкілсульфамоїльної, ді(С1-С6)алкілсульфамоїльної, (С1-С6)алкоксикарбонільної та (С1-С6)алкілкарбоніл(С1-С6)алкільної групи, та з групи формул -NR*R*, -C(=O)-NR*R*, -А, -О-А, -С(=О)-А, -(CH2)q-A, -NR**-A, -C(=O)NR**-A, -NR**C(=O)-A та -O-C(=O)-A, де кожний R* незалежно являє собою атом водню або С1-С6алкільну, С1-С6алкілкарбонільну, фенільну або бензильну групу, R** являє собою атом водню або С1-С6алкільну групу, q являє собою ціле число від 1 до 6, та А являє собою фенільну групу або С1-С8гетероциклічну групу з 1-3 гетероатомами, вибраними з N, О та S; кожна група А необов'язково заміщена 1-3 групами, незалежно вибраними з галогену, гідрокси, ціано, нітро та С1-С6алкілу;
або сольват, гідрат, енантіомер, діастереомер, N-оксид або фармацевтично прийнятна сіль такої сполуки.
2. Сполука за п. 1, в якій X являє собою атом кисню, R1a являє собою атом азоту, R2 являє собою зв'язок, та подвійний зв'язок знаходиться між R1a та атомом вуглецю, з яким R3-C≡C- зв'язаний.
3. Сполука за п. 1, в якій X являє собою атом кисню, R1a являє собою СН-групу з подвійним зв'язком, який знаходиться між R1a та атомом вуглецю, з яким R3-C≡C- зв'язаний, або СН2-групу з простим зв'язком, який знаходиться між R1a та атомом вуглецю, з яким R3-C≡C- зв'язаний, та R2 являє собою СН2-групу.
4. Сполука за будь-яким з пп. 1-3, в якій R3 являє собою алкільну групу, необов'язково заміщену С3-С5гетеромоноциклічну групу з 1-3 гетероатомами, вибраними з N, О та S, або необов'язково заміщену фенільну групу; або R3 являє собою групу формули -C(=O)-R3, де R3 є таким, як визначено в цьому пункті.
5. Сполука за будь-яким з пп. 1-3, в якій R3 являє собою метильну, ізопропільну, бутильну, фенільну, 3-(трет-бутил)фенільну, 2-хлорфенільну, 3-хлорфенільну, 3-хлор-5-фторфенільну, 2-ціанофенільну, 3-ціанофенільну, 3-етоксифенільну, 3-етилфенільну, 2-фторфенільну, 3-фторфенільну, 4-фторфенільну, 3-гідроксифенільну, 3-ізопропілфенільну, 3-метоксифенільну, 2-метилфенільну, 3-метилфенільну, 3-(3-метил-[1,2,4]-оксадіазол-5-іл)фенільну, 3-нітрофенільну, 3-трифторметоксифенільну, 3-трифторметилфенільну, 2-піридильну, 4-хлор-2-піридильну, 5-хлор-2-піридильну, 5-фтор-2-піридильну, 6-фтор-2-піридильну, 4-метил-2-піридильну, 6-метокси-3-піридильну, 6-метил-2-піридильну, 4-трифторметил-2-піридильну, 3-піридильну, 6-фтор-3-піридильну, 2-фурильну, 2-тієнільну, 3-тієнільну, 2-піразинільну, 2-метил-1,3-тіазол-4-ільну або 2-фуроїльну групу.
6. Сполука за будь-яким з пп. 1-5, в якій R1 являє собою атом вуглецю, R4 являє собою атом водню, атом галогену, необов'язково заміщену моноциклічну С3-С5гетероциклічну групу з 1-3 гетероатомами, вибраними з N, О та S, або необов'язково заміщену фенільну групу; та R5 являє собою атом водню або галогену, ціаногрупу або необов'язково заміщену гідрокси, меркапто, аміно, карбамоїльну, С1-С6алкільну або С1-С6алкоксигрупу, або групу формули -C(=O)- R6, де R6 являє собою необов'язково заміщену С1-С6алкільну групу, необов'язково заміщену моноциклічну С3-С5гетероциклічну групу з 1-3 гетероатомами, вибраними з N, О та S, або необов'язково заміщену фенільну групу.
7. Сполука за будь-яким з пп. 1-5, в якій R1 являє собою атом вуглецю, R4 являє собою атом водню або фтору або 2-піридильну або 2-піридилметильну групу, та R5 являє собою атом водню або фтору або ціано-, гідрокси- або етоксикарбонільну групу.
8. Сполука за будь-яким з пп. 1-5, в якій R1 являє собою атом вуглецю; та R4 та R5 разом представляють оксо, метиленову, дифторметиленову, 2-піридилметиленову, триметилену, тетраметилену, етилендіокси, пропілендіокси, оксіетилу, оксипропілу, метиленоксиметиленову, гідроксііміно, метоксііміно, 1-карбокси-3-гідроксипропоксііміно або 2-оксотетрагідрофуран-3-ілоксііміногрупу.
9. Сполука за будь-яким з пп. 1-5, в якій R1 являє собою атом вуглецю, та R4 та R5 разом представляють групу формули -(Yp)-, де р являє собою ціле число від 3 до 5, та кожний Y незалежно являє собою атом кисню або необов'язково заміщену метиленову групу, за умови, що жодні два суміжні Y-фрагменти не представляють атоми кисню.
10. Сполука за п. 9, в якій R4 та R5 разом представляють групу формули -О-СН2СН2-О-, -О-СН2СН2СН2-О-, -О-СН2СН2-, -О-СН2СН2СН2, -СН2-О-СН2-, -СН2СН2СН2-, -СН2СН2СН2СН2-, -СН2СН2СН2СН2СН2- або -CH2CH2CF2CH2CH2.
11. Сполука за будь-яким з пп. 1-5, в якій R1 являє собою атом азоту; R4 являє собою необов'язково заміщену С3-С5гетеромоноциклічну групу з 1-3 гетероатомами, вибраними з N, О та S; та R5 відсутній.
12. Сполука за будь-яким з пп. 1-5, в якій R1 являє собою атом азоту; R4 являє собою 3-ціано-2-піразинільну, 3-нітро-2-піридильну або 3-нітро-6-метил-2-піридильну групу; та R5 відсутній.
13. Сполука за будь-яким з пп. 1-5, в якій R1 являє собою атом азоту; R4 відсутній; та R5 являє собою алкоксикарбоніл, необов'язково заміщений арилкарбоніл, необов'язково заміщений гетероциклілкарбоніл, карбамоїл, діалкілкарбамоїл, N-алкоксі-N-алкілкарбамоїл або необов'язково заміщену гетероциклілкарбамоїльну групу.
14. Сполука за будь-яким з пп. 1-5, в якій R1 являє собою атом азоту; R4 відсутній; та R5 являє собою етоксикарбонільну, 3-хлорбензоїльну, 2-фуроїльну, 2-оксо-1-імідазолідинілкарбонільну, 3-метилсульфоніл-2-оксо-1-імідазолідинілкарбонільну, 4-метил-1-піперазинілкарбонільну, піперидинокарбонільну, 1-піролідинілкарбонільну, карбамоїльну, диметилкарбамоїльну, діетилкарбамоїльну, N-метокси-N-метилкарбамоїльну, N-етил-N-ізопропілкарбамоїльну або 4-піридилкарбамоїльну групу.
15. сполука за п. 1, вибрана з групи, що включає:
3-фенілетиніл-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-фенілетиніл-8-(3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-[(6-метил-2-піридил)етиніл]-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(2-тієнілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(2-піридилетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(2-фторфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-фторфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(4-фторфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(2-фурилетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-[(2-метил-1,3-тіазол-4-іл)етиніл]-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(проп-1-ініл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-метилфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-метоксифенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-ціанофенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-тієнілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-піридилетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-{3-(3-метил-[1,2,4]оксадіазол-5-іл)-фенілетиніл}-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-метилбут-1-иніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(гекс-1-иніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(2-ціанофенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-(3-ціано-2-піразиніл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(2-метилфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(2-хлорфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(2-піразинілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-фенілетиніл-8-(6-метил-3-нітро-2-піридил)-1-окса-8-азаспіро[4.5]дец-3-ен,
3-(3-хлорфенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.3]окт-2-ен,
4-фенілетиніл-9-(6-метил-3-нітро-2-піридил)-1-окса-9-азаспіро[5.5]ундец-4-ен,
4-фенілетиніл-9-(6-метил-3-нітро-2-піридил)-1-окса-9-азаспіро[5.5]ундец-3-ен,
3-(3-хлорфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-хлорфенілетиніл)-8-оксо-1-окса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-метилен-1-окса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-метоксііміно-1-окса-2-азаспіро[4.5]дец-2-ен,
3-[(6-метил-2-піридил)-етиніл]-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-фенілетиніл-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-фторфенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-фенілетиніл-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.3]окт-2-ен,
3-(3-гідроксифенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-фторфенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.3]окт-2-ен,
3-(3-хлорфенілетиніл)-8-(2-піридилметилен)-1-окса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-гідрокси-8-(2-піридилметил)-1-окса-2-азаспіро[4.5]дец-2-ен,
3-фенілетиніл-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-фенілетиніл-8-оксо-1-окса-2-азаспіро[4.5]дец-2-ен,
3-фенілетиніл-8-гідроксііміно-1-окса-2-азаспіро[4.5]дец-2-ен,
3-фенілетиніл-8-(2-оксо-3-тетрагідрофуранілоксііміно)-1-окса-2-азаспіро[4.5]дец-2-ен,
3-[(6-метил-2-піридил)-етиніл]-8-ціано-8-(2-піридил)-1-окса-2-азаспіро[4.5]дец-2-ен,
3-[(5-фтор-2-піридил)-етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(6-метил-2-піридил)-етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(6-фтор-2-піридил)-етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(6-фтор-3-піридил)-етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-нітрофенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(2-метил-1,3-тіазол-4-іл)-етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-метоксифенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-хлор-5-фторфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-метилфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-етоксифенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-трифторметоксифенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-трет-бутилфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-ціанофенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-фторфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-етилфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-ізопропілфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(4-хлор-2-піридил)етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(4-метил-2-піридил)етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-трифторметилфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(4-трифторметил-2-піридил)-етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(5-хлор-3-піридил)етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(2-фуроїлетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-фенілетиніл-8-(1-карбокси-3-гідроксипропокііміно)-1-окса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-1,8-діокса-2-азаспіро[4.5]дец-2-ен,
3-[(6-метил-2-піридил)етиніл]-1,8-діокса-2-азаспіро[4.5]дец-2-ен,
3-[(4-хлор-2-піридил)етиніл]-1,8-діокса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-1-окса-8-тіа-2-азаспіро[4.5]дец-2-ену 8,8-діоксид,
3-(3-хлорфенілетиніл)-1,7-діокса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-1,9-діокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-метилфенілетиніл)-1,9-діокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-гідроксифенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.3]окт-2-ен,
3-(3-ціанофенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.3]окт-2-ен,
3'-(3-хлорфенілетиніл)-2,3-дигідро-3-гідрокси-4'Н-спіро[інден-1,5'-ізоксазол],
3'-(3-хлорфенілетиніл)-2,3-дигідро-3-оксо-4'Н-спіро[інден-1,5'-ізоксазол],
3'-(3-хлорфенілетиніл)-2,3-дигідро-3-метоксііміно-4'Н-спіро[інден-1,5'-ізоксазол],
3-(3-хлорфенілетиніл)-1,9-діокса-2-азадиспіро[4.2.3.2]тридец-2-ен,
3-(3-хлорфенілетиніл)-1,9,13-триокса-2-азадиспіро[4.2.5.2]пентадец-2-ен,
3'-[(6-метил-2-піридил)етиніл]-2,3-дигідро-3-гідрокси-4'Н-спіро[інден-1,5'-ізоксазол],
3-(3-хлорфенілетиніл)-1-окса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-(3-хлорфенілетиніл)-8,8-дифтор-1-окса-2-азаспіро[4.5]дец-2-ен,
3-(3-метилфенілетиніл)-1-окса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3-[(6-метокси-3-піридил)етиніл]-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен,
3'-[(6-метил-2-піридил)етиніл]-2,3-дигідро-3-оксо-4'Н-спіро[інден-1,5'-ізоксазол],
3'-[(6-метил-2-піридил)етиніл]-2,3-дигідро-3-метоксііміно-4'Н-спіро[інден-1,5'-ізоксазол],
3-(3-хлорфенілетиніл)-7-диметилкарбамоїл-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-карбамоїл-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-1-окса-2-азадиспіро[4.1.3.1]ундец-2-ен,
3-(3-метилфенілетиніл)-1,9,13-триокса-2-азадиспіро[4.2.5.2]пентадец-2-ен,
3-(3-хлорфенілетиніл)-1-окса-2-азаспіро[4.3]окт-2-ен,
3-(3-хлорфенілетиніл)-1,10-діокса-2-азадиспіро[4.2.3.2]тридец-2-ен,
3-[(4-хлор-2-піридил)етиніл]-8,8-дифтор-1-окса-2-азаспіро[4.5]дец-2-ен,
3-[(4-хлор-2-піридил)етиніл]-8-етоксикарбоніл-1-окса-2-азаспіро[4.5]дец-2-ен,
3'-(3-хлорфенілетиніл)-1Н,4'Н-спіро[ізохроман-4,5'-ізоксазол],
3-(3-хлорфенілетиніл)-7-(4-метил-1-піперазинілкарбоніл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-(2-оксо-1-імідазолідинілкарбоніл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-(1-піролідинілкарбоніл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-піперидинокарбоніл-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-(3-метилсульфоніл-2-оксо-1-імідазолідинілкарбоніл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-(N-етил-N-ізопропілкарбамоїл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-(N-метокси-N-метилкарбамоїл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-(4-піридилкарбамоїл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-7-етоксикарбоніл-1-окса-2,7-діазаспіро[4.4]нон-2-ен,
3-[(6-метил-2-піридил)етиніл]-8,8-дифтор-1-окса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-1,7-діокса-2-азаспіро[4.3]окт-2-ен,
3-(3-хлорфенілетиніл)-1-окса-3-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-дифторметилен-1-окса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-карбамоїл-1-окса-2-азаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-(2-фуроїл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-(N-метокси-N-метилкарбамоїл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-діетилкарбамоїл-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-(3-хлорбензоїл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-етоксикарбоніл-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-(1-піролідинілкарбоніл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-диметилкарбамоїл-1-окса-2,8-діазаспіро[4.5]дец-2-ен,
3-(3-хлорфенілетиніл)-8-(трет-бутоксикарбоніл)-6-метоксі-1-окса-2,8-діазаспіро[4.4]нон-2-ен,
3-(3-хлорфенілетиніл)-8-етоксикарбоніл-6-метоксі-1-окса-2,8-діазаспіро[4.4]нон-2-ен,
або її фармацевтично прийнятна сіль.
16. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-14 або її сольват, гідрат, енантіомер, діастереомер, N-оксид або фармацевтично прийнятну сіль в суміші з фармацевтично прийнятним носієм.
Текст
Реферат: Даний винахід стосується сполуки загальної формули І R 2 X R 4 R1a m R 1 R5 n R3 , де X являє собою О або S; R1 являє собою С, N, О або S; R1a являє собою СН, СН2, N або NH; R2 являє собою зв'язок, СН або СН2; m дорівнює 1, 2 або 3; n дорівнює 1 або 2; якщо n дорівнює 2, або m дорівнює 2 або 3, кільце, яке містить R1 може бути сконденсоване з бензольним кільцем; кожний --- являє собою простий або подвійний зв'язок, за умови, що один подвійний зв'язок відходить від атома вуглецю, з яким R3-С≡С- зв'язаний, та що жодний кільцевий атом вуглецю не несе два подвійні зв'язки; та R3, R4 та R5 являють широкий ряд замісників. Ці сполуки селективні до метаботропного mGlu5-рецептора. Сполуки, їх сольвати, гідрати, UA 110343 C2 (12) UA 110343 C2 енантіомери, діастереомери, N-оксиди та фармацевтично прийнятні солі, та фармацевтичні композиції, які їх містять, можна використовувати для лікування захворювань або розладів нижніх сечовивідних шляхів, особливо нервовом'язових дисфункцій нижніх сечовивідних шляхів, їх можна також застосовувати для лікування мігрені; для лікування гастроезофагеальної рефлюксної хвороби (GERD); для лікування тривожного розладу; для лікування абузусу, розладів, пов'язаних з залежністю від речовини та виведенням речовини; для лікування невропатичного больового розладу та для лікування розладів синдрому ламкої Х-хромосоми. UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 [001] Даний винахід відноситься до нових спірогетероциклічних сполук з селективною афінністю до mGlu5-підтипу метаботропних рецепторів, до фармацевтичних композицій, які містять такі сполуки, та до способів лікування за їх допомогою. Передумови винаходу [002] Розлади нижніх сечових шляхів включають ряд синдромів, які діють на нормальне сечовипускання. Розлади нижніх сечових шляхів можуть виникати через комбінацію патологічних та/або пов'язаних з віком змін сечостатевої системи, або іншої етиології, наприклад, неврологічні розлади. Особи, які страждають від розладів нижніх сечових шляхів, страждають від погіршеної якості життя, включаючи вагання, слабке самосприйняття та загальне зниження в емоційному самопочутті, соціальній функції та загальному стані здоров'я. Розлади нижніх сечових шляхів, більш того, можуть бути зв'язані з іншими фізичними захворюваннями, включаючи целюліт, пролежні, інфекції сечових шляхів, падіння з переломами, депривацію сну, соціальну самоізоляцію, депресію та сексуальні розлади. Старші люди, які страждають від розладів нижніх сечових шляхів, можуть потребувати більшого догляду від медицинськіх працівників, як сім'ї, так і професії, які можуть бути фактором в рішенні для розміщення їх в закладах. [003] Згідно з Національним інститутом охорони здоров'я США (NIH) до 35 мільйонів американців, як оцінено, страждають від розладів нижніх сечових шляхів. Розлади нижніх сечових шляхів більш поширені серед жінок, ніж серед чоловіків (2:1) до 80 років, після цього віку чоловіки та жінки уражені в рівному ступені. Частота розладів нижніх сечових шляхів зростає з віком. До віку 65 років, розлади нижніх сечових шляхів вражають від 15 % до 30 % всіх осіб та приблизно 50 % осіб при довготривалому догляді. [004] Засоби з різними типами дії застосовували для лікування розладів нижніх сечових шляхів. Вони включають засоби, які діють безпосередньо на нижні сечові шляхи, наприклад, антимускаринові засоби та антагоністи альфа-1, та засоби, які діють через центральну нервову систему, наприклад, інгібітори зворотнього заоплення серотоніну та/або норадреналіну. Згідно з NIH, проте, хоча деякий прогрес був зроблений у діагностиці, регулюванні та лікуванні розладів нижніх сечових шляхів, ці розлади часто залишаються неусуненими. Таким чином, існує постійна потреба в покращених засобах, складах та терапіях для лікування розладів нижніх сечових шляхів. [005] Глутамінова кислота, збуджуюча амінокислота, існує в синапсах у всій центральній нервовій системі та відома як така, що діє на щонайменше два типи рецепторів: іонотропний та метаботропний глутаматні рецептори. Принципова функція іонотропних глутаматних рецепторів полягає в тому, що їх активація формує керовані лігандами іонні канали та, таким чином, безпосередньо опосередковує електричні сигнали нервових клітин, забезпечуючи швидкі та відносно великі зміни електропровідності в постсинаптичних мембранах. Метаботропні глутаматні рецептори (mGluR) контролюють електричні сигнали опосередковано шляхом впливу на внутрішньоклітинні метаболічні процеси через G-білки. Зміни в постсинаптичній клітині, які опосередковані mGluR, є відповідно відносно повільними в часі та не пов'язані з швидкими та великими змінами в проводимості мембран нейронів. [006] Три підтипи іонотропних глутаматних рецепторів були описані, тобто, NMDA, AMPA та каїнатний підтипи. [007] Вісім підтипів метаботропних глутаматних рецепторів були клоновані. Підтипи класифікували в три групи на основі подібностей в послідовностях, та фармакологічних та біохімічних властивостях (Spooren et al., Trends Pharmacol. Sci. 22: 331-337, 2001): mGluрецептори групи I (mGlu1 та mGlu5), mGlu-рецептори групи II (mGlu2 та mGlu3) та mGluрецептори групи III (mGlu4, mGlu6, mGlu7 та mGlu8). [008] Рецептор mGlu5 групи I (або людський, або щурячий) відомий як такий, що містить щонайменше два підтипи "a" та "b". Підтип "b" довший, ніж підтип "a", через альтернативне зрощування ділянки 32-амінокислоти в C-кінцевому (внутрішньоклітинному) домені, на 50 залишків нижче початкового домену. Людський mGlu5b являє собою 1212 амінокислот в довжину, в той час, як "a" формує нестачу амінокислот від 877 до 908 (номер 828 є першою внутрішньоклітинного домена). Щурячий mGlu5b являє собою 1203 амінокислот в довжину, в той час, як "a" формує нестачу амінокислот від 876 до 907 (номер 827 є першою внутрішньоклітинного домена). (Hermans and Challis, Biochem. J. 359: 465-484, 2001). [009] mGlu-рецептори, які належать до сімейства 3 GPCR, характеризуються двома відмінними топологічними доменами: великим позаклітинним N-кінцевим доменом, який містить модуль венериної мухоловки, який відповідає за зв'язування агоніста, та 7-TM доменом плюс внутрішньоклітинний C-кінцевий домен, який включений в активацію рецептора та сполучення G-білку. 1 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 [010] 7-TMD рецепторів mGlu групи I, як було показано, формує карман зв'язування для позитивних та негативних алостеричних модуляторів; негативні ідентифікували завдяки технологіям високопродуктивного скринінгу та діють як неконкурентні антагоністи, які не мають ефекту на зв'язування агоністів. Найбільш цікава властивість цих молекул, на додаток до їх сильної активності, полягає в їх винятковій селективності до підтипу. [011] Область зв'язування 7-TM розташована в кармані, який вистелений TM-III, TM-V, TM-VI та TM-VII; цей сайт відповідає ретинальному карману зв'язування в родопсині. [012] Алостеричні модулятори mGlu5 представляють хвилюючий успіх в демонстрації потенціалу для розробки нових засобів дослідження та терапевтичних засобів, які контролюють активність специфічних підтипів mGluR. [013] Сполуки даного винаходу включають такі, які описані в даному документі як антагоністи mGlu5, які в багатьох випадках є фактично негативними алостеричними модуляторами, які діють в області зв'язування 7-TM. [014] Документ WO 00/63166 розкриває трициклічні похідні карбамінової кислоти, застосовувані для лікування різних захворювань, включаючи нетримання сечі. Похідні розкриті як агоністи або антагоністи рецепторів mGlu групи I з вибірковою дією до mGlu1-рецептора. [015] Документ WO 01/32632 розкриває піримідинові похідні, застосовувані для лікування різних захворювань, включаючи нетримання сечі. Похідні описані як селективні антагоністи mGlu1-рецептора з щонайменше в 10 разів більшою селективністю до mGlu1-рецептора, ніж у mGlu5-рецептора. [016] Документ WO 01/27070 розкриває нові бісарилaцетаміди, застосовувані для лікування нетримання сечі, серед інших станів. Молекули розкриті як агоністи або антагоністи, селективні до mGlu1-рецептора. [017] Патент США №6369222 розкриває похідні гетероциклоазепінілпіримідину, застосовувані для лікування нетримання сечі, серед інших станів. Похідні розкриті як антагоністи mGlu1-рецептора. [018] Вищевказані заявки та патент, отже, розкривають антагоністи mGlu1-рецептора як застосовувані для лікування нетримання сечі. Жодне з посилань, проте, не забезпечує експериментальну підтримку для лікування нетримання сечі, або у пацієнтів-людей, або у тваринній моделі для захворювань нижніх сечових шляхів. [019] Ми тестували активність антагоністів, селективних до mGlu1 та селективних до mGlu5, на щурячій моделі, застосовуваній для визначення активності в нижніх сечових шляхах. Несподівано, хорошу активність знайшли у антагоністів, селективних до mGlu5-рецептора, тоді як два комерційно доступні антагоністи, селективні до mGlu1-рецептора не показали ефект. Антагоніст, селективний до рецепторів mGluR групи II, також не показав ефект в щурячій моделі. Враховуючи ці результати, селективні mGlu5-антагоністи можуть бути ефективними засобами для лікування розладів нижніх сечових шляхів. [020] В даному рівні техніки існує потреба в розробці нових сполук та композицій для лікування розладів нижніх сечових шляхів та для полегшення симптомів, пов'язаних з такими розладами. Винахідники вирішили цю потребу завдяки розробці нових гетероциклічних сполук, які селективні до mGlu5-модуляторів, включаючи селективний mGlu5-антагоніст. Сполуки даного винаходу забезпечують сильне інгібування рефлексу сечовипускання за допомогою нового механізму дії. Опис даного винаходу [021] Даний винахід забезпечує сполуку загальної формули I ,I де: X представляє собою атом кисню або сірки; R1 представляє собою атом вуглецю, азоту, кисню або сірки; 2 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 R1a представляє собою CH-, CH2-, N- або NH-фрагмент; R2 представляє собою валентний зв'язок або CH- або CH2-групу; R3 представляє собою необов'язково заміщену C1-C6алкільну групу, необов'язково заміщену моно-, бі- або трициклічну C1-C13гетероциклічну групу, що містить 1-5 гетероатомів, обраних з N, O та S, необов'язково заміщену моно-, бі- або трициклічну C6-C14арильну групу, необов'язково заміщену C3-C6 циклоалкільну групу або необов'язково заміщену C3-C6циклоалкенільну групу; якщо R1 представляє собою атом вуглецю: R4 представляє собою атом водню, атом галогену, необов'язково заміщену моно- або біциклічну C1-C9гетероциклічну групу, що містить 1-3 гетероатоми, обрані з N, O та S, або необов'язково заміщену моно-, бі- або трициклічну C6-C14арильну групу; R5 представляє собою атом водню або галогену, ціаногрупу або необов'язково заміщений гідрокси, меркапто, аміно, карбамоїл, C1-C6 алкіл або C1-C6алкоксигрупу, або групу формули – C(=O)–R6, де R6 представляє собою необов'язково заміщений C1-C6алкіл або C1-C6 алкоксигрупу, необов'язково заміщену моно- або біциклічну C1-C9 гетероциклічну групу, що містить 1-3 гетероатоми, обрані з N, O та S, або необов'язково заміщену моно-, бі- або трициклічну C6-C14арильну групу; або R4 та R5 разом представляють оксогрупу або необов'язково заміщений метилeн або гідроксііміногрупу; або R4 та R5 разом з R1 представляють собою необов'язково заміщене ненасичене 4-6-членне кільце, що містить від 0 до 3 гетероатомів, обраних з N, O та S; якщо R1 представляє собою атом кисню: R4 та R5 відсутні; якщо R1 представляє собою атом азоту: один з R4 та R5 відсутній, та інший є таким, як визначено вище; якщо R1 представляє собою атом сірки: кожний з R4 та R5 незалежно відсутній або представляє собою оксогрупу; m дорівнює 1, 2 або 3; n дорівнює 1 або 2; якщо n дорівнює 2, або m дорівнює 2 або 3, кільце, що містить R1, може бути конденсованим з необов'язково заміщеним бензольним кільцем; та кожний ---- представляє собою простий або подвійний зв'язок, забезпечуючи, що один подвійний зв'язок подовжується від атома вуглецю, з яким R3-C≡C- зв'язаний, та що жодний атом вуглецю кільця не несе два подвійні зв'язки; та сольвати, гідрати, енантіомери, діастереомери, N-оксиди та фармацевтично прийнятні солі таких сполук. [022] Необов'язкові замісники незалежно обрані з атомів галогенів та груп C 1-C6алкілу, C1C6алкоксі, гідроксі, меркапто, нітро, ціано, оксо, галоген(C1-C6)алкілу, галоген(C1-C6)алкоксі, C1C6алкілтіо, C1-C6алкілсульфонілу, C1-C6алкілкарбонілу, сульфамоїлу, C1-C6алкілсульфамоїлу, ди(C1-C6)алкілсульфамоїлу, (C1-C6)алкоксикарбонілу та (C1-C6)алкілкарбоніл(C1-C6)алкілу, та з груп формул -NR*R*, -C(=O)NR*R*, -A, -O-A, -C(=O)A, -(CH2)q-A, -NR**-A, -C(=O)NR**-A, -NR**C(=O)A та -O-C(=O)A, де кожний R* незалежно представляє собою атом водню або групу C1-C6алкілу, C1-C6алкілкарбонілу, фенілу або бензилу, R** представляє собою атом водню або C1-C6алкільну групу, q представляє собою ціле число від 1 до 6, та A представляє собою фенільну групу або C1-C8 гетероциклічну групу, що містить від 1 до 3 гетероатомів, обраних з N, O та S; причому кожна група A необов'язково заміщена 1-3 групами, незалежно обраними з галогену, гідроксі, ціано, нітро та C1-C6алкілу. [023] Найбільш переважними сполуками за даним винаходом є такі, в яких X представляє собою атом кисню, R1a представляє собою атом азоту, R2 представляє собою зв'язок, та подвійний зв'язок протягується від R1a до атома вуглецю, з яким R3-C≡C- зв'язаний. Проте, сполуки за даним винаходом, в яких X представляє собою атом кисню, R 1a представляє собою CH-групу з подвійним зв'язком, який протягується від R 1a до атома вуглецю, з яким R3-C≡Cзв'язаний, або CH2-групу з простим зв'язком, який протягується від R1a до атома вуглецю, з яким R3-C≡C- зв'язаний, та R2 представляє собою CH2-групу, також переважні. [024] R3 переважно представляє собою алкільну групу, необов'язково заміщену C3C5гетеромоноциклічну групу, що містить 1-3 гетероатоми, обрані з N, O та S, необов'язково заміщену фенільну групу або групу формули –C(=O)–R3, де R3 є таким, як визначено в цьому реченні. Більш переважно, R3 представляє собою групу метилу, ізопропілу, бутилу, фенілу, 3(трет-бутил)-фенілу, 2-хлорфенілу, 3-хлорфенілу, 3-хлор-5-фторфенілу, 2-ціанофенілу, 3ціанофенілу, 3-етоксифенілу, 3-етилфенілу, 2-фторфенілу, 3-фторфенілу, 4-фторфенілу, 3гідроксифенілу, 3-ізопропілфенілу, 3-метоксифенілу, 2-метилфенілу, 3-метилфенілу, 3-(3 3 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 метил-[1,2,4]-оксадіазол-5-іл)-фенілу, 3-нітрофенілу, 3-трифторметоксифенілу, 3трифторметилфенілу, 2-піридилу, 4-хлор-2-піридилу, 5-хлор-2-піридилу, 5-фтор-2-піридилу, 6фтор-2-піридилу, 4-метил-2-піридилу, 6-метокси-3-піридилу, 6-метил-2-піридилу, 4трифторметил-2-піридилу, 3-піридилу, 6-фтор-3-піридилу, 2-фурилу, 2-тієнілу, 3-тієнілу, 2піразинілу, 2-метил-1,3-тіазол-4-ілу або 2-фуроїлу. [025] Якщо R1 представляє собою атом вуглецю, R4 переважно представляє собою атом водню, атом галогену, необов'язково заміщену моноциклічну C3-C5гетероциклічну групу, що містить 1-3 гетероатоми, обрані з N, O та S, або необов'язково заміщену фенільну групу; та R5 переважно представляє собою атом водню або галогену, ціаногрупу або необов'язково заміщений гідроксі, меркапто, аміно, карбамоїл, C1-C6алкіл або C1-C6алкоксігрупу, або групу формули -C(=O)–R6, де R6 представляє собою необов'язково заміщену C1-C6алкільну групу, необов'язково заміщену моноциклічну C3-C5гетероциклічну групу, що містить 1-3 гетероатоми, обрані з N, O та S, або необов'язково заміщену фенільну групу. [026] Якщо R1 представляє собою атом вуглецю, R4 більш переважно представляє собою атом водню або фтору або групу 2-піридилу або 2-піридилметилу, та R5 більш переважно представляє собою атом водню або фтору або ціано-, гідроксі- або етоксикарбонільну групу. [027] Альтернативно, якщо R1 представляє собою атом вуглецю, R4 та R5 разом переважно представляють собою групу оксо, метилeну, дифторметилeну, 2-піридилметилeну, триметилeну, тетраметилeну, етилeндіоксі, пропілeндіоксі, оксіетил, оксипропіл, метилeноксиметилен, гідроксііміно, метоксііміно, 1-карбокси-3-гідрокси-пропоксііміно або 2-оксотетрагідрофуран-3-ілоксііміно. [028] Альтернативно, якщо R1 представляє собою атом вуглецю, R4 та R5 разом переважно представляють собою групу формули –(Yp)–, де p являє собою ціле число від 3 до 5, та кожний Y незалежно представляє собою атом кисню або необов'язково заміщену метилeнову групу, забезпечуючи, що жодні два суміжні Y-фрагменти не являють собою атоми кисню. Наприклад, – (Yp)– може бути -O-(CH2)2-O-, -O-(CH2)3-O-, -O-(CH2)2-, -O-(CH2)3-, -CH2-O-CH2-, -(CH2)3-, (CH2)4-, -(CH2)5- або -CH2CH2CF2CH2CH2-. [029] Якщо R1 представляє собою атом азоту, R4 переважно представляє собою необов'язково заміщену C3-C5 гетеромоноциклічну групу, що містить 1-3 гетероатоми, обрані з N, O та S, з відсутнім R5. Альтернативно, R5 переважно представляє собою алкоксикарбоніл, необов'язково заміщений арилкарбоніл, необов'язково заміщений гетероциклілкарбоніл, карбамоїл, діалкілкарбамоїл, N-алкокси-N-алкілкарбамоїл або необов'язково заміщену гетероциклілкарбамоїльну групу, з відсутнім R4. [030] Якщо R1 представляє собою атом азоту, R4 більш переважно представляє собою групу 3-ціано-2-піразинілу, 3-нітро-2-піридилу або 3-нітро-6-метил-2-піридилу, з відсутнім R5. Альтернативно, R5 більш переважно представляє собою групу етоксикарбонілу, 3-хлорбензоїлу, 2-фуроїлу, 2-оксо-1-імідазолідинілкарбонілу, 3-метилсульфоніл-2-оксо-1імідазолідинілкарбонілу, 4-метил-1-піперазинілкарбонілу, піперидинoкарбонілу, 1піролідинілкарбонілу, карбамоїлу, диметилкарбамоїлу, диетилкарбамоїлу, N-метокси-N-метилкарбамоїлу, N-етил-N-ізопропілкарбамоїлу або 4-піридилкарбамоїлу, з відсутнім R4. Визначення [031] За вийнятком того, де вказано інше, наступні визначення застосовують у всьому даному описі та формулі винаходу. Ці визначення застосовують не зважаючи на те, застосовується вираз сам по собі або в комбінації з іншими виразами. Наприклад, визначення "алкіл" застососвується не тільки до алкілу як такового, але також до алкільних частин алкокси, алкіламіно, алкілтіо, алкілкарбонілу і т.і. Крім того, всі діапазони, описані для хімічних груп, наприклад, діапазони "від 1 до 20 атомів вуглецю" та "C 1-C6алкіл" включають всі комбінації та субкомбінації діапазонів та конкретних чисел атомів вуглецю в них. [032] "Алкіл" означає аліфатичну вуглеводневу групу з прямим ланцюгом або розгалуженим ланцюгом з 1-20 атомами вуглецю в ланцюгу. Переважниі алкільні групи мають 1-12 атомів вуглецю в ланцюгу. Більш переважні алкільні групи мають 1-6 атомів вуглецю в ланцюгу. "Нижчий алкіл" означає алкільну групу з від приблизно 1 до приблизно 6 атомів вуглецю в ланцюгу, який може бути прямим або розгалуженим. Приклади придатних алкільних груп включають метил, етил, н-пропіл, ізопропіл, втор-бутил, н-бутил, та трет-бутил. [033] "Алкеніл" означає аліфатичну вуглеводневу групу з прямим ланцюгом або розгалуженим ланцюгом з щонайменше одним вуглець-вуглецевим подвійним зв'язком та з 2-15 атомами вуглецю в ланцюгу. Переважні алкенільні групи мають 2-12 атомів вуглецю в ланцюгу. Більш переважні алкенільні групи мають 2-6 атомів вуглецю в ланцюгу. "Нижчий алкеніл" означає алкенільну групу з від 2 до приблизно 6 атомів вуглецю в ланцюгу, який може бути прямим або розгалуженим. Приклади придатних алкенільних груп включають етеніл, пропеніл, 4 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 ізопропеніл, н-бутеніл, 1-гексеніл та 3-метилбут-2-еніл. [034] "Алкініл" означає аліфатичну вуглеводневу групу з прямим ланцюгом або розгалуженим ланцюгом з щонайменше одним вуглець-вуглецевим потрійним зв'язком та з 2-15 атомами вуглецю в ланцюгу. Переважні алкінільні групи мають 2-12 атомів вуглецю в ланцюгу. Більш переважні алкінільні групи з 2-6 атомами вуглецю в ланцюгу. "Нижчий алкініл" означає алкінільну групу з від 2 до приблизно 6 атомів вуглецю в ланцюгу, який може бути прямим або розгалуженим. Приклади придатних алкінільних груп включають етиніл, пропініл та 2-бутиніл. [035] "Моно-, бі- або трициклічний арил" означає ароматичну моноциклічну, біциклічну або трициклічну кільцеву систему, що містить 6-14 атомів вуглецю. Бі- та трициклічні арильні групи конденсовані в 2 або 4 положенні або з'єднані в одній точці за допомогою зв'язку або гетероатомного лінкера (O, S, NH або N(C1-C6алкіл) (наприклад, біфеніл, 1-фенілнафтил). Арильна група може бути необов'язково заміщена на кільці одним або декількома замісниками, переважно 1-6 замісниками, які можуть бути однаковими або різними. Приклади придатних арильних груп включають феніл та нафтил. [036] "Моно-, бі- або трициклічна гетероциклічна сполука" означає ароматичну або неароматичну насичену моно-, бі- або трициклічну кільцеву систему з 2-14 кільцевими атомами вуглецю та з 1-5 кільцевими атомами, обраними з N, O та S, окремо або в комбінації. Бі- та трициклічні гетероциклічні групи конденсовані в 2 або 4 положенні або з'єднані в одній точці за допомогою зв'язку або гетероатомного лінкера (O, S, NH або N(C1-C6алкіл). "Моно-, бі- або трициклічна гетероциклічна сполука" може бути необов'язково заміщена на кільці заміщенням доступного водню на кільці одним або декількома замісниками, які можуть бути однаковими або різними. В кільцевій системі немає суміжних атомів кисню та/або сірки. Атом азоту або сірки гетероциклічної сполуки може бути необов'язково окисненим до відповідного N-оксиду, S-оксиду або S-діоксиду. Приклади придатних гетероциклічних сполук включають фураніл, імідазоліл, ізоксазоліл, оксадіазоліл, оксазоліл, піроліл, піридил, піримідил, піридазиніл, тіазоліл, тріазоліл, тетразоліл, тієніл, карбазоліл, бензімідазоліл, бензотієніл, бензофураніл, індоліл, хінолініл, бензотриазоліл, бензотіазоліл, бензооксазоліл, бензімідазоліл, ізохінолініл, ізоіндоліл, акридиніл та бензoізоксазоліл, азиридиніл, піперидиніл, піролідиніл, піперазиніл, тетрагідропіраніл, тетрагідрофураніл, тетрагідротіофеніл, морфолініл та тіоморфолініл. [037] Гетероциклічні сполуки з ароматичними характеристиками можна називати гетероарили або гетероароматичні сполуки. Приклади придатних гетероароматичних сполук включають фураніл, імідазоліл, ізоксазоліл, оксадіазоліл, оксазоліл, піроліл, піридил, піримідил, піридазиніл, тіазоліл, тріазоліл, тетразоліл, тієніл, карбазоліл, бензімідазоліл, бензотієніл, бензофураніл, індоліл, хінолініл, бензотриазоліл, бензотіазоліл, бензооксазоліл, бензімідазоліл, ізохінолініл, ізоіндоліл, акридиніл, бензоізоксазоліл, тетрагідрохінолініл, тетрагідроізохінолініл, 3-фенілпіридин, 3-циклогексилпіридин, 3-(піридин-3-іл)морфолін, 3-фенілізоксазол та 2(піперидин-1-іл)піримідин. [038] "Моно- або біциклічний циклоалкіл" означає моноциклічну або біциклічну вуглецеву кільцеву систему з 3-14 атомами вуглецю, переважно з 3-6 атомами вуглецю. Циклоалкіл може бути необов'язково заміщеним на кільці заміщенням доступного водню на кільці одним або декількома замісниками, які можуть бути однаковими або різними. Приклади придатних моноциклічних циклоалкілів включають циклопропіл, циклопентіл, циклогексил та циклогептил. Приклади придатних багатоциклічних циклоалкілів включають 1-декалініл, норборніл та адамантил. [039] "Циклоалкеніл" має значення відповідне такому циклоалкілу, але з одним або двома подвійними зв'язками в кільці (наприклад, циклогексеніл, циклогексадієн). [040] "Галоген" або "Hal" означає фтор, хлор, бром або йод. Переважними є фтор, хлор або бром, та більш переважними є фтор та хлор. [041] Вираз "ацил", де застосовується окремо або в виразі, такому як "ациламіно", означає радикал, забезпечений залишком після видалення гідроксилу з органічної кислоти. Вираз "ациламіно" відноситься до аміно-радикалу, заміщеного ацильною групою. Прикладом "ациламіно”-радикала є CH3C(=O)-NH-, де амін може бути додатково заміщеним алкілом, арилом або аралкілом. Стереохімія сполук даного винаходу [042] Сполуки формули I можуть мати один або декілька хіральних центрів та, в залежності від природи окремих замісників, вони можуть також мати геометричні ізомери. Ізомери, які відрізняються угрупованням своїх атомів в просторі, називаються "стереоізомери". Стереоізомери, які не є дзеркальними відображеннями один одного, називаються "діастереомери", та ті, які є ненакладеними дзеркальними відображеннями один одного, називаються "енантіомери". Якщо сполука має хіральний центр, пара енантіомерів можлива. 5 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 Енантіомер може характеризуватись абсолютною конфігурацією його асиметричного центру та описано правилами Кана та Прелога для побудови R- та S-послідовностей, або шляхом, яким молекула повертає площину поляризованого світла та визначеного як правообертаючий або лівообертаючий (тобто, як (+) або (-)-ізомер, відповідно). Хіральна сполука може існувати або як окремий енантіомер, або як суміш енантіомерів. Суміш, яка містить рівні співвідношення енантіомерів, називають "рацемічна суміш". Суміш, яка містить нерівні співвідношення енантіомерів, описують як таку, що має "енантіомерний надлишок" (ee) або R, або S-сполуки. Надлишок одного енантіомера в суміші часто описують в % значенні енантіомерного надлишку (% ee), визначеного формулою: % ee = (R) - (S) / (R) + (S) [043] Співвідношення енантіомерів можна також визначити "оптичною чистотою", де ступінь, при якому суміш енантіомерів обертає плoскополяризоване світло, порівняний з окремими оптично чистими R- та S-сполуками. Оптичну чистоту можна визначити за допомогою наступної формули: Оптична чистота = енант.основний / (енант.основний + енант.побічний) [044] Даний винахід включає всі окремі ізомери сполук формули I. Опис або присвоєння імен конкретній сполуці в описі та формулі винаходу має намір включати як окремі енантіомери, так і їх суміші, рацемічні або інші. Способи визначення стереохімії та розділення стереоізомерів добре відомі в даному рівні техніки. [045] Для багатьох застосувань переважно виконувати стереоселективні синтези та/або піддавати продукт реакції придатним етапам очисти так, щоби продукувати головним чином оптично чисті матеріали. Придатні процедури стереоселективного синтезу для отримання оптично чистих матеріалів добре відомі в даному рівні техніки як такі процедури для очистки рацемічних сумішей в оптично чистих фракціях. Фахівці в даній галузі додатково визначать, що сполуки винахіду можуть існувати в поліморфних формах, де сполука здатна кристалізуватись в різних формах. Придатні способи для ідентифікації та відділення поліморфiзмів відомі в даному рівні техніки. [046] Діастереоізомери відрізняються як фізичними властивостями, так і хімічною активністю. Суміш діастереомерів можна розділяти в енантіомерні пари на основі розчинності, кристалізації фракцій або хроматографічних властивостей, наприклад, тонкошарова хроматографія, колонкова хроматографія або ВЕРХ. [047] Очистка комплексних сумішей діастереомерів в енантіомерах типово потребує два етапи. На першому етапі суміш діастереомерів розділяють на енантіомерні пари, як описано вище. На другому етапі енантіомерні пари додатково очищують в композиціях, збагачених одним або іншим енантіомером або більш переважно розкладають в композиціях, що містять чисті енантіомери. Розділення енантіомерів типово потребує реакцію або молекулярну взаємодію з хіральним засобом, наприклад, розчинником або стовпчиковою матрицею. Розділення можна досягти, наприклад, перетворенням суміші енантіомерів, наприклад, рацемічної суміші, в суміші діастереомерів реакцією з чистим енантіомером другого засобу, тобто, засобу розділення. Два отримані діастереомерні продукти можна розділити. Відділені діастереомери потім повертають в чисті енантіомери зміною початкового хімічного перетворення. [048] Розділення енантіомерів може також виконати різницею в їх нековалентному зв'язуванні з хіральною речовиною, наприклад, хроматографією на гомохіральних адсорбентах. Нековалентне зв'язування між енантіомерами та хроматографічними адсорбентами створює діастереомерні комплекси, які призводять до диференційного розділення в рухливому та зв'язаному станах в хроматографічній системі. Дваенантіомери отже проходять через хроматографічну систему, наприклад, колонку, при різних швидкостях, дозволяючи їх розділення. [049] Хіральні колонки для розділення добре відомі в даному рівні техніки та комерційно доступні (наприклад, від MetaChem Technologies Inc., філіалу ANSYS Technologies, Inc., Лейк Форест, Каліфорнія). Енантіомери можна аналізувати та очищати за допомогою, наприклад, хіральних нерухомих фаз (CSP) для ВЕРХ. Хіральні колонки для ВЕРХ типово містять одну форму енантіомерної сполуки, імобілізованої на поверхні сорбенту з діоксиду кремнію. [050] D-фенілгліцин та L-лейцин є прикладами CSP типу I та застосовують комбінації π-π взаємодій, водневих зв'язків, диполь-дипольних взаємодій та стеричних взаємодій для досягнення хірального розпізнавання. Для розкладання в колонці типу I енантіомери, які аналізують, можуть містити функціональну групу, додаткову до такої CSP так, що речовина, яку аналізують, піддається необхідним взаємодіям з CSP. Зразок повинен переважно містити одну з наступних функціональних груп: π-кислота або π-основа, донор та/або акцептор водневого 6 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 зв'язку або амідний диполь. Отримання похідних іноді застосовують для додавання інтерактивних сайтів до таких сполук, у яких вони відсутні. Найбільш поширені похідні включають утворення амідів з амінів та карбонових кислот. [051] MetaChiral ODM™ є прикладом CSP типу II. Первинні механізми для утворення комплексів розчин-CSP проходять через атрактивні взаємодії, але комплекси включення також відіграють важливу роль. Водневе зв'язування, π-π взаємодії та дипольний стекінг важливі для хірального розкладання на MetaChiral™ ODM. Отримання похідних можливо необхідне, якщо молекула розчину не містить групи, потрібні для взаємодій розчин-колонка. Отримання похідних, як правило, для бензидамідів, може потребуватись для деяких сильно полярних молекул, таких як аміни та карбонові кислоти, які інакше будуть інтенсивно взаємодіяти з нерухомою фазою завдяки неспецифічним стереовзаємодіям. [052] Сполуки формули I можна розділяти на діастереомерні пари, наприклад, розділенням колонковою хроматографією або TLC на силікагелі. Ці діастереомерні пари називаються в даному документі діастереомер з верхнім TLC Rf; та діастереомер з нижнім TLC Rf. Діастереомери можна додатково збагачувати конкретним енантіомером або розкладати на окремий енантіомер за допомогою способів, добре відомих в даній області техніки, такими як ті, що описані в даному документі. [053] Відповідну конфігурацію діастереомерних пар можна встановити застосуванням теоретичних моделей або правил (наприклад, правило Крама, модель Фелкіна-Ана) або за допомогою більш надійних просторових моделей, створених компьютерними хімічними програмами. В багатьох випадках ці способи здатні визначати, який діастереомер є енергетично переважним продуктом хімічного перетворення. Альтернативно, відповідну конфігурацію діастереомерних пар можна непрямо визначити знаходженням абсолютних конфігурацій окремого енантіомера в одному (або обох) з діастереомерної пари(пар). [054] Абсолютну конфігурацію стереоцентрів можна визначити дуже добре відомим фахівцям даної галузі техніки способом (наприклад, рентгенографією, круговим дихроїзмом). Визначення абсолютної конфігурації можна також застосовувати для підтвердження можливості прогнозування теоретичних моделей та може бути корисним для продовження застосування цих моделей для подібних молекул, отриманих реакціями з аналогічними механізмами (наприклад, відновлення кетонів та відновне амінування кетонів гідридами). [055] Даний винахід також включає стереоізомери Z-E-типу та їх суміші через те, що R2-R3замісники подвійного зв'язку непрямо зв'язані з кільцем. Додаткові Z-E стереоізомери зустрічаються, якщо m не дорівнює 1, та m та n різні. Правила приоритету Кана-ІнгольдаПрелога застосовують для визначення, який зі стереоізомерів через відповідні положення в площині подвійного зв'язку зв'язаних подвійним зв'язком замісників є Z або E. Стереоoізомер визначають як Z (zusammen = разом), якщо 2 групи найвищого пріоритету лежать на одному боці рівня площини, яка проходить через C=C-зв'язок. Інший стереoізомер позначають як E (entgegen = напроти). [056] Суміш стереоізомерів E-Z-типу можна розділяти (та/або характеризувати) за їх компонентами за допомогою класичного способу очистки який базується на основі різниці хіміко-фізичних властивостей цих сполук. Включеними в цей спосіб є фракційна кристалізація, хроматографію проводять техніками при низькому, середньому або високому тиску, фракційна дистиляція та будь-який інший спосіб, дуже добре відомий фахівцям даної галузі техніки. Похідні сполук даного винаходу [057] Даний винахід додатково включає солі, сольвати, гідрати, N-оксиди, проліки та активні метаболіти сполук формули I. [058] Вираз "солі" може включати солі приєднання кислоти або солі приєднання вільних основ. Для виділення або очистки можливо застосовувати фармацевтично небажані солі. Проте, лише фармацевтично прийнятні, нетоксичні солі застосовують терапевтично, та отже вони переважні. Приклади кислот, які можна застосовувати для формування фармацевтично прийнятних солей додавання кислоти, включають солі, отримані з нетоксичних неорганічних кислот, таких як азотна, фосфорна, сірчана або бромистоводнева, йодистоводнева, фтористоводнева, фосфорна, а також солі, отримані з нетоксичних органічних кислот, таких як аліфатичні моно- та дикарбонові кислоти, фенілзаміщені алканові кислоти, гідроксіалканові кислоти, алкандіові кислоти, ароматичні кислоти, аліфатичні та ароматичні сульфонові кислоти, та оцтова, малеїнова, бурштинова або лимонна кислоти. Приклади таких солей включають нападизілат, безилат, сульфат, піросульфат, бісульфат, сульфіт, бісульфіт, нітрат, фосфат, моногідрофосфат, дигідрофосфат, метафосфат, пірофосфат, хлорид, бромід, йодид, ацетат, трифторацетат, пропіонат, каприлат, ізобутират, оксалат, малонат, сукцинат, суберат, себацат, фумарат, малеат, манделат, бензоат, хлорбензоат, метилбензоат, динітробензоат, фталат, 7 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 бензолсульфонат, толуолсульфонат, фенілацетат, цитрат, лактат, малеат, тартрат, метансульфонат і т.і. Також включені солі амінокислот, такі як аргінат і подібні та глюконат, галактуронат (дивись, наприклад, Berge, et al. "Pharmaceutical Salts, ” J. Pharma. Sci. 1977; 66:1). [059] Фраза "фармацевтично прийнятний", як застосовується у зв'язку з композиціями даного винаходу, стосується молекулярних структур та інших інгредієнтів таких композицій, які є фізіологічно прийнятними та типово не продукують небажаних реакцій при введенні ссавцю (наприклад, людині). Переважно, як застосовується у даному документі, вираз "фармацевтично прийнятний" означає схвалені регулятивним органом федерального уряду або уряду штату або перераховані в Фармакопії США або інших як правило визнаних фармакопій для застосування у ссавців та, конкретніше, у людей. [060] Типово, фармацевтично прийнятна сіль сполуки формули I може бути швидко отримана за допомогою бажаної кислоти або основи, в разі необхідності. Сіль може осаджуватись з розчину та збиратись фільтруванням або може бути виділена випарюванням розчинника. Наприклад, водний розчин кислоти, такої як соляна кислота, можна додати до водної суспензії сполуки формули I та отриману суміш випаровують насухо (ліофілізують) для отримання солі приєднання кислоти як твердої речовини. Альтернативно, сполуку формули I можна розчинити в придатному розчиннику, наприклад, спирті, такому як ізопропанoл, та можна додати кислоту в такому саме розчиннику або іншому придатному розчиннику. Отриману сіль приєднання кислоти можна тоді осаджувати безпосередньо або додаванням менш полярного розчинника, такого як діізопропіловий ефір або гексан, та виділяти фільтруванням. [061] Солі приєднання кислоти сполук формули I можна одержати контактом форми вільної основи з достатньою кількістю бажаної кислоти для одержання солі звичайним чином. Форму вільної основи можна отримати контактом сольової форми з основою та виділенням вільної основи звичайним чином. Форми вільної основи відрізняються від їх відповідних сольових форм деякою мірою конкретними фізичними властивостями, такими як розчинність в полярних розчинниках, але в іншому випадку солі являють собою еквівалент їх відповідній вільній основі для цілей даного винаходу. [062] Також включені як повні, так і неповні солі, а саме солі з 1, 2 або 3, переважно 2, еквівалентами основи на моль кислоти формули I, або солі з 1, 2 або 3 еквіваленти, переважно 1 еквівалентом, кислоти на моль основи формули I. [063] Фармацевтично прийнятні солі приєднання основи формують з металами або амінами, такими як лужні та лужноземельні метали або органічні аміни. Приклади металів, застосовуваних в якості катіонів, представляють собою натрій, калій, магній, кальцій і тому подібне. Приклади придатних амінів представляють собою N, N’-дибензилетилeндіамін, хлорпрокаїн, холін, діетаноламін, дициклогексиламін, етилeндіамін, N-метилглукамін та прокаїн. [064] Солі приєднання основи вказаних кислотних сполук отримують контактом форми вільної кислоти з достатньою кількістю бажаної основи для отримання солі звичайним чином. Форма вільної кислоти може бути утворена контактом сольової форми з кислотою та виділенням вільної кислоти. [065] Сполуки даного винаходу можуть мати як основний, так і кислотний центр, та отже бути в формі цвіттер-іонів або внутрішніх солей. [066] Типово, фармацевтично прийнятну сіль сполуки формули I можна легко одержати за допомогою бажаної кислоти або основи, за необхідності. Сіль можна осаджувати з розчину та збирати фільтрацією або можна виділити випарюванням розчинника. Наприклад, водний розчин кислоти, такої як соляна кислота, можна додати до водної суспензії сполуки формули I та отриману суміш випаровують насухо (ліофілізують) для отримання солі приєднання кислоти у вигляді твердої речовини. Альтернативно, сполуку формули I можна розчинити в придатному розчиннику, наприклад, спирті, такому як ізопропанoл, та кислоту можна додати в такому саме розчиннику або іншому придатному розчиннику. Отриману сіль приєднання кислоти можна потім осаджувати безпосередньо або додаванням менш полярного розчинника, такого як діізопропіловий ефір або гексан, та виділяти фільтрацією. [067] Спеціалісти в даній області техніки органічної хімії оцінять, що багато органічних сполук можуть формувати комплекси з розчинниками, в яких вони реагують або з яких вони осаджуються або кристалізуються. Ці комплекси відомі як "сольвати". Наприклад, комплекс з водою відомий як "гідрат". Сольвати сполуки даного винаходу знаходяться в обсязі даного винаходу. Солі сполуки формули I можуть формувати сольвати (наприклад, гідрати), та даний винахід також включає всі такі сольвати. Значення слова "сольвати" добре відоме фахівцям даної галузі техніки як сполука, сформована взаємодією розчинника та розчина (тобто, сольватація). Техніки отримання сольватів добре описані в даному рівні техніки (дивись, наприклад, Brittain. Polymorphism in Pharmaceutical solids. Marcel Decker, New York, 1999.). 8 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 [068] Даний винахід також включає N-оксиди сполук формули I. Вираз "N-оксид" означає, що 2 для гетероциклів, які містять інший незаміщений sp N-атом, N-атом може нести ковалентно зв'язаний O-атом, тобто, -N(O. Приклади таких гетероциклів, заміщених N-оксидом, включають піридильні N-оксиди, піримідильні N-оксиди, піразинільні N-оксиди та піразолільні N-оксиди. [069] Даний винахід також включає проліки сполук формули I, тобто, сполуки, які вивільняють активний початковий лікарський засіб згідно з формулою I in vivo, якщо їх вводять суб'єкту-ссавцю і т.д. Проліки є фармакологічно активною або більш типово неактивною сполукою, яка перетворюється в фармакологічно активний засіб метаболічним перетворенням. Проліки сполуки формули I отримують модифікацією функціональних груп, присутніх в сполуці формули I, таким чином, що модифікації можуть розщеплюватись in vivo для вивільнення початкової сполуки. In vivo проліки легко піддаються хімічним змінам за фізіологічних умов (наприклад, на них діють фермент(и), який зустрічається в природі), приводячи до вивільнення фармакологічно активного засобу. Проліки включають сполуки формули I, де гідроксі-, аміноабо карбоксигрупа сполуки формули I зв'язана з будь-якою групою, яка може бути розщеплена in vivo для утворення вільної гідроксильної, аміно- або карбоксигрупи, відповідно. Приклади проліків включають складні ефіри (наприклад, похідні ацетату, форміату та бензоату) сполук формули I або будь-яку іншу похідну, яка при дії фізіологічного pH або через дію фермента перетворюється в активний вихідний лікарський засіб. Звичайні процедури вибору та одержання придатних похідних проліків описані в рівні техніки (дивись, наприклад, Bundgaard. Design of Prodrugs. Elsevier, 1985). [070] Проліки можна вводити таким саме чином як і активний інгредієнт, в який вони перетворюються, або їх можна доставити в формі резервуара, наприклад, трансдермального пластира або іншого резервуара, який адаптований для дозволення (забезпеченням фермента або іншого придатного реагента) перетворення проліків в активний інгредієнт повільно в часі, та доставки активного інгредієнта пацієнту. [071] Даний винахід також включає метаболіти. "Метаболіт" сполуки, розкритої в даному документі, являє собою похідну сполуки, яка формується, якщо сполука метаболізується. Вираз "активний метаболіт" стосується біологічно активної похідної сполуки, яка формується, якщо сполука метаболізується. Вираз "метаболізується" стосується суми процесів, якими конкретна речовина змінюється в живому організмі. Словом, всі сполуки, присутні в організмі, управляються ферментами в організмі для отримання енергії та/або для видалення їх з організму. Конкретні ферменти продукують конкретні структурні зміни сполуки. Наприклад, цитохром P450 каталізує різноманітні окисні та відновні реакції, в той час, як уридиндифосфатглюкоронитрансферази каталізують перенос активованої молекули глюкуронової кислоти до ароматичних спиртів, аліфатичних спиртів, карбонових кислот, амінів та вільних сульфгідрильних груп. Додаткову інформацію про метаболізм можна отримати з The Pharmacological Basis of Therapeutics, 9th Edition, McGraw-Hill (1996), pages 11-17. [072] Метаболіти сполук, розкритих в даному документі, можна ідентифікувати або введенням сполук хазяїну, або аналізом зразків тканини з хазяїна, або інкубацією сполук з гепатоцитами in vitro та аналізом отриманих сполук. Обидва способи добре відомі в даному рівні техніки. Застосування сполук даного винаходу для лікування розладів нижніх сечових шляхів [073] Номенклатура симптомів та патологій нижніх сечових шляхів, застосовувана в даному документі, описана в Abrams et al., Neurol. and Urodyn. 21:167-178 (2002) та Andersson et al., Pharmacol. Rev. 56:581-631 (2004). [074] Порушення спорожнювання можна приблизно класифікувати як порушення акумулювання або спорожнювання. Симптоми акумулювання зазнаються під час фази акумулювання міхура та включають збільшену частоту за день, ноктурію (прокидання вночі один або декілька разів для спорожнення), невідкладний позив до сечовипускання (несподіване, нездоланне бажання мочитися, яке складно затримати) та нетримання сечі (будь-яке невільне витікання сечі). Нетримання сечі можна додатково характеризувати відповідно до симптомів. Стресове нетримання сечі є невільним витіканням при навантаженні або напрузі, або при чиханні або кашлі. Невідкладне нетримання сечі є невільним витіканням сечі, яке супроводжується або відбувається одразу після невідкладного позиву до сечовипускання. Змішане нетримання сечі є невільним витіканням сечі, пов'язаним з невідкладним позивом до сечовипускання та також з напругою, навантаженням, чиханням або кашлем. Нетримання сечі через переповнення сечового міхура є невільним витіканням сечі, яке відбувається після того, як місткість сечового міхура була перевищена, наприклад, від розладу до пустого. Енурез також стосується будь-якої невільної втрати сечі. Нічне нетримання являє втрату сечі, яка виникає протягом сну. 9 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 [075] Симптоми спорожнення включають повільний потік, розпилення або розбризкування потоку сечі, преривність потоку (преривність, тобто, зупинення та поновлення потоку сечі під час сечовипускання, коливання (складності при початку сечовипусканні, що приводить до затримки початку спорожнення після того, як особа готова мочитися), напруження та останні краплини (подовжена кінцева частина сечовипускання, якщо потік сповільнився до тонкої струї/капель). [076] Розлади нижніх сечових шляхів можна додатково класифікувати за сукупністю симптомів (тобто, синдром) або за етіологією. Особи, які страждають від синдрому надактивного сечового міхура (OAB), наприклад, типово страждають від симптомів невідкладного позиву до сечовипускання, невідкладного нетримання сечі, підвищеної частоти за день або ноктурії. OAB виникає в результаті надактивності м'яза-стискача, яку називають рухомість м'яза-стискача. Рухомість м'яза-стискача може виникати через неневрологічні патології, такі як камні сечового міхура, захворювання м'язів, інфекції сечових шляхів або побічні ефекти лікарських засобів, або може бути ідіопатичною. [077] Неврогенний надактивний сечовий міхур (або неврогенний сечовий міхур) є типом надактивного сечового міхура, який виникає в результаті надактивності м'яза-стискача, яку називають гіперрефлексія стискача, вторинно до відомих неврологічних розладів. Пацієнти з неврологічними розладами, такими як удар, хвороба Паркінсона, діабет, розсіяний склероз, периферична невропатія або ушкодження спинного мозку, часто страждають від неврогенного надактивного сечового міхура. [078] Цистит (включаючи інтерстиціальний цистит) являє собою розлад нижніх сечових шляхів невідомої етілогії, який головним чином уражує молодих жінок та жінок середнього віку, хоча чоловіки та діти також можуть бути уражені. Симптоми інтерстиціального циститу можуть включати симптоми спорожнювання, підвищену частоту за день, невідкладний позив до сечовипускання, ноктурію або надлобковий або тазовий біль, пов'язаний з та послаблюючий спорожнюванням. Багато пацієнтів з інтерстиціальним циститом також відчувають головні болі, а також проблеми з шлунково-кишковим трактом та шкірою. В деяких випадках інтерстиціальний цистит може також бути пов'язаний з виразками або ушкодженнями сечового міхура. [079] Простатит та простадинія є іншими розладами нижніх сечових шляхів, які, як вважається, вражають приблизно 2-9 % дорослих чоловіків. Простатит є запаленням простати та включає бактеріальний простатит (гострий та хронічний) та небактеріальний простатит. Гострий та хронічний бактеріальні простатити характеризуються запаленням простати та бактеріальною інфекцією передміхурової залози, як правило, зв'язаним з симптомами болю, підвищеної частоти за день та/або невідкладним позивом до сечовипускання. Хронічний бактеріальний простатит відрізняється від гострого бактеріального простатиту періодичною природою розладу. Хронічний небактеріальний простатит характеризується запаленням простати, яке є невідомої етіології, пов'язаної з присутністю надлишкової кількості запальних клітин в секреті предміхурової залози, та зараз не пов'язують з бактеріальною інфекцією предміхурової залози, та, як правило, зв'язане з симптомами болю, підвищеної частоти за день та/або невідкладним позивом до сечовипускання. Простадинія являє собою розлад, який імітує симптоми запалення простати без простатиту, бактеріальної інфекції простати та підвищені рівні запальних клітин в секреті предміхурової залози. Простадинія може бути пов'язана з симптомами болю, підвищеної частоти за день та/або невідкладним позивом до сечовипускання. [080] Доброякісна простатична гіперплазія (BPH) являє собою доброякісне збільшення простати, яке є дуже поширеним серед чоловіків віком за 40 років. BPH як вважають виникає через надлишковий клітинний ріст як залозистих, так і стромальних елементів простати. Симптоми BPH можуть включати підвищену частоту, невідкладний позив до сечовипускання, невідкладне нетримання сечі, ноктурію та симптоми спорожненя, включаючи повільний потік, розпилення або розбризкування потоку сечі, преривність, коливання, напруження та останні краплі. [081] Сполуки за даним винаходом можна застосовувати для лікування вищевказаних захворювань або розладів нижніх сечових шляхів, особливо нервово-м'язових розладів нижніх сечових шляхів, включаючи невідкладний позив до сечовиділення, надактивний сечовий міхур, підвищену частоту сечовипускання, зменшена розтяжність сечового міхура (зменшена місткість сечового міхура), цистит, інтерстиціальний цистит, нетримання, втрату сечі, енурез, дизурію, коливання сечі та складності при спорожненні сечового міхура. Під лікуванням ми розуміємо лікування будь-якого одного або декількох з вищевказаних станів, симптомів та/або синдромів. [082] При лікуванні нервово-м'язових розладів нижніх сечових шляхів сполуки даного винаходу можна вводити окремо або в комбінації з іншим лікарським засобом. Такий інший 10 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 лікарський засіб може бути антимускариновим лікарським засобом, таким як оксибутинін, толтеродін, дарифенацин, соліфенацин, троспій, імідафенацин, фезотеродин або теміверин; α 1адренергічним антагоністом, таким як празозин, доксазозин, теразозин, альфузозин, силодозин або тамсулозин; інгібітором зворотнього захвату серотоніну та/або норадреналіну, таким як дулоксетин, мілнаципран, амоксапін, венлафаксин, дезвенлафаксин, сибутрамін, тезофензин або дезметилсибутрамін; або селективним або неселективним інгібітором COX, таким як ібупрофен, напроксен, беноксапрофен, флурбіпрофен, фенопрофен, кетопрофен, індопрофен, пірпрофен, карпрофен, тіоксапрофен, супрофен, тіапрофенова кислота, флупрофен, індометацин, суліндак, толметін, зомепірак, діклофенак, фенклофенак, ібуфенак, ацетилсаліцилова кислота, піроксикам, теноксикам, набуметон, кеторолак, азапропазон, мефенамова кислота, толфенамова кислота, дифлунізал, ацеметацин, фентіазак, кліданак, меклофенамова кислота, флуфенамова кислота, ніфлумова кислота, флуфенісал, судоксикам, етодолак, саліцилова кислота, бенорилат, ізоксикам, 2-фтор-α-метил-[1,1’-біфеніл]-4-оцтової кислоти 4-(нітроокси)бутиловий складний ефір, мелоксикам, парекоксиб або німесулід. Інші застосування сполук даного винаходу [083] Сполуки за даним винаходом можна також застосовувати для лікування мігрені; для лікування гастроезофагеальної рефлюксної хвороби (GERD); для лікування тривожного розладу; для лікування зловживання; розлади, пов'язані з залежністю від речовини та виводом речовини; для лікування невропатичного больового розладу; та для лікування розладів синдрому ламкої X-хромосоми. Фармацевтичні композиції, які містять сполуку формули I [084] Хоча можливо, що сполуку I можна вводити в якості сипучої речовини, переважно, щоб активний інгредієнт був присутній в фармацевтичному складі, наприклад, де засіб знаходиться в суміші з фармацевтично прийнятним носієм, обраним відповідно до можливого шляху введення та стандартної фармацевтичної практики. [085] Відповідно, даний винахід додатково забезпечує фармацевтичну композицію, що містить сполуку формули I або її сольват, гідрат, енантіомер, діастереомер, N-оксид або фармацевтично прийнятну сіль в суміші з фармацевтично прийнятним носієм. Вираз "носій" стосується розріджувача, наповнювача та/або середовища, з яким активну сполуку вводять. [086] Сполуку формули I можна застосовувати в комбінації іншими терапіями та/або активними засобами. Відповідно, даний винахід забезпечує в додатковому аспекті фармацевтичну композицію, що містить сполуку формули I або її сольват, гідрат, енантіомер, діастереомер, N-оксид або фармацевтично прийнятну сіль, другий активний засіб та фармацевтично прийнятний носій. [087] Фармацевтичні композиції можуть містити на додаток в якості носія будь-яке придатне зв'язуюче, змащувальний засіб, суспендуючий засіб, покриваючий засіб та/або солюбілізуючий засіб. [088] Консерванти, стабілізатори, барвники та ароматизуючі засоби також можна забезпечити в фармацевтичній композиції. Антіоксиданти та суспендуючі засоби можна також застосовувати. [089] Сполуки даного винаходу можна розмелювати за допомогою відомих процедур розмелювання, таких як вологе розмелювання, для отримання розміру часток, придатного для одержання таблеток та для інших типів складів. Дрібнодисперсні (наночастка) препарати сполук даного винаходу можна отримати способами, відомими в даному рівні техніки, наприклад, дивись WO 02/00196. Шляхи введення та стандартні лікарські форми [090] Шляхи введення включають пероральний (наприклад, в вигляді таблетки, капсули або розчину для проковтування), місцевий, через слизову (наприклад, в вигляді назального спрею або аерозолю для інгаляції), назальний, парентеральний (наприклад, в формі для ін'єкції), шлунково-кишковий, інтраспінальний, інтраперитонеальний, внутрішньом'язовий, внутрішньовенний, внутрішньоматковий, внутрішньоочний, інтрадермальний, внутрішньочерепний, інтратрахеальний, інтравагінальний, інтрацеребро-вентрикулярний, інтрацеребральний, підшкірний, очний (включаючи введення в скловидне тіло або інтракамерне), трансдермальний, ректальний, букальний, епідуральний та сублінгвальний. Композиції даного винаходу можна особливо складати для будь-якого з цих шляхів введення. В переважних варіантах здійснення фармацевтичні композиції даного винаходу складені в формі, яка придатна для пероральної доставки. [091] Можуть бути різні вимоги до композиції/складу в залежності від різних систем доставки. Це повинно бути ясним, що не всі сполуки треба вводити однаковим шляхом. Аналогічно, якщо композиція містить більше ніж один активний компонент, тоді ці компоненти можна вводити 11 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 різними шляхами. В якості прикладу, фармацевтичну композицію даного винаходу можна скласти для доставки за допомогою мінінасосу або через слизову, наприклад, як назальний спрей або аерозоль для інгаляції або розчин для проковтування, або парентерально, при якій композицію складають у формі для ін'єкції для доставки, наприклад, внутрішньовенним, внутрішньом'язовим або підшкірним шляхом. Альтернативно, склад можна виконувати для доставки декількома шляхами. [092] Якщо засіб треба доставити через слизову крізь шлунково-кишкову слизову, він має залишатись стабільним під час проходу через шлунково-кишковий тракт; наприклад, він має бути стійким до протеолітичного розпаду, стабільним при кислому pH та стійким до розрихлюючих ефектів жовчі. Наприклад, сполуку формули I можна покрити шаром ентеросолюбільного покриття. Матеріал шару ентеросолюбільного покриття може бути диспергований або розчинений або в воді, або в придатному органічному розчиннику. В якості полімерів шару ентеросолюбільного покриття, одного або декількох, окремо або в комбінації, наступні можуть використовуватися; наприклад, розчини або дисперсії співполімерів метакрилової кислоти, фталат ацетилцелюлози, бутират ацетилцелюлози, фталат гідроксипропілметилцелюлози, сукцинат гідроксипропілметилацетилцелюлози, фталат полівінілацетату, тримелітат ацетилцелюлози, карбоксиметилетилцелюлоза, шелак або інший придатний полімер(и) шару ентеросолюбільного покриття. З екологічних міркувань водний спосіб покриття може бути переважним. В таких водних способах співполімери метакрилової кислоти найбільш переважні. [093] Якщо необхідно, фармацевтичні композиції можна вводити інгаляцією, в формі супозиторію або песарію, місцево в формі лосьону, розчину, крему, мазі або присипки, шляхом застосування трансдермального пластиру, перорально в формі таблеток, які містять наповнювачі, такі як крохмаль або лактоза, або в капсулах або супозиторіях або окремо, або в суміші з наповнювачами, або в формі еліксірів, розчинів або суспензій, які містять ароматизуючі або фарбуючі засоби, або їх можна ввести ін'єкцією парентерально, наприклад, внутрішньовенно, внутрішньом'язово або підшкірно. Для букального або сублінгвального введення композиції можно вводити в формі таблеток або пастилок, які можна скласти звичайним чином. [094] Якщо композицію даного винаходу необхідно вводити парентерально, таке введення включає одне або декілька з: внутрішньовенного, внутрішньоартеріального, внутрішньочеревного, інтратекального, інтравентрикулярного, інтрауретрального, надчеревного, внутрішньочерепного, внутрішньом'язового або підшкірного введення засобу; та/або за допомогою технік інфузії. [095] Фармацевтичні композиції даного винаходу можна вводити парентерально, наприклад, інфузією або ін'єкцією. Фармацевтичні композиції, придатні для ін'єкції або інфузії, можуть бути в формі стерильного водного розчину, дисперсії або стерильного порошку, які містять активний інгредієнт, пристосовані, якщо необхідно, для отримання такого стерильного розчину або дисперсії, придатних для інфузії або ін'єкції. Ці препарати можуть необов'язково бути інкапсульовані в ліпосомах. У всіх випадках кінцевий препарат має бути стерильним, рідким та стабільним за умов отримання та зберігання. Для покращення стабільності при зберіганні, такі препарати мають також містити консервант для запобігання росту мікроорганізмів. Запобігання дії мікроорганізму можна досягти завдяки додаванню різних антибактеріальних та протигрибкових засобів, наприклад, парабен, хлорбутанол або аскорбінова кислота. В багатьох випадках ізотонічні речовини рекомендовані, наприклад, цукри, буфери та хлорид натрію, для гарантування осмотичного тиску, подібного до таких рідин організму, особливо крові. Пролонговану абсорбцію таких ін'єкційних сумішей можна досягти введенням сповільнюючих абсорбцію засобів, таких як алюмінію монoстеарат або желатин. [096] Дисперсії можна отримати в рідкому носії або проміжній сполуці, такій як гліцерин, рідкі поліетиленгліколі, триацетинові масла, та їх суміші. Рідкий носій або проміжна сполука можуть бути розчинником або рідким дисперсним середовищем, яке містить, наприклад, воду, етанол, поліол (наприклад, гліцерин, пропілeнгліколь або подібне), рослинні олії, нетоксичні складні ефіри гліцерину та їх придатні суміші. Придатну плинність можна підтримувати формуванням ліпосом, введенням часток придатного розміру у випадку дисперсій або додаванням поверхнево-активних речовин. [097] Для парентерального введення сполуку краще застосовувати в формі стерильного водного розчину, який може містити інші речовини, наприклад, достатньо солей або глюкози для отримання розчину, ізотонічного крові. Водні розчини повинні бути підходяще буферизовані (переважно до pH від 3 до 9), якщо необхідно. Отримання придатних парентеральних складів за стерильних умов є легко виконуваними стандартними фармацевтичними техніками, добре 12 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 відомими фахівцям даної галузі техніки. [098] Стерильні розчини для ін'єкцій можна отримати змішуванням сполуки формули I з відповідним розчинником та одним або декількома з вищевказаних носіїв, з наступною стерильною фільтрацією. У випадку стерильних порошків, придатних для застосування при отриманні стерильних розчинів для ін'єкцій, переважні способи отримання включають сушку в вакуумі та ліофілізацію, які забезпечують порошкоподібні суміші антагоністів альдостеронових рецепторів та бажаних наповнювачів для наступного отримання стерильних розчинів. [099] Сполуки за даним винаходом можна скласти для застосування в лікарських препаратах для людини або в ветеринарії в вигляді ін'єкції (наприклад, внутрішньовенна болюсна ін'єкція або інфузія або через внутрішньом'язовий, підшкірний або інтратекальний шляхи) та можуть бути представлені в формі однократної дози, в ампулах або інших контейнерах для однократної дози, або в упаковці лікарських засобів для багаторазового застосування, якщо необхідно з доданим консервантом. Композиції для ін'єкції можуть бути в формі суспензій, розчинів або емульсій, в маслянистому або водному середовищах, та можуть містити засоби для складання, такі як суспендуючі, стабілізуючі, солюбілізуючі та/або диспергуючі засоби. Альтернативно, активний інгредієнт може бути в формі стерильного порошку для розбавлення придатним середовищем, наприклад, стерильною, апірогенною водою, перед застосуванням. [0100] Сполуки даного винаходу можна вводити (наприклад, перорально або місцево) в формі таблеток, капсул, супориторіів, еліксирів, розчинів або суспензій, які можуть містити ароматизуючі або фарбуючі засоби, для застосувань з негайним, сповільненим, модифікованим, безперервним, імпульсним або контрольованим вивільненням. [0101] Сполуки даного винаходу можуть також бути представлені для застосування для людей або в ветеринарії в формі, придатній для перорального або букального введення, наприклад, в формі розчинів, гелів, сиропів, рідин для полоскання рота або суспензій, або сухого порошку для змішування з водою або іншим придатним середовищем перед застосуванням, необов'язково з ароматизуючими та фарбуючими засобами. Тверді композиції, такі як таблетки, капсули, коржики, пастилки, пігулки, болюси, порошок, пасти, гранули, кульки або премікси препаратів, можна також застосовувати. Тверді та рідкі композиції для перорального застосування можна отримати згідно зі способами, добре відомими в даному рівні техніки. Такі композиції можуть також містити один або декілька фармацевтично прийнятних носіїв та наповнювачів, які можуть бути в твердій або рідкій формі. [0102] Таблетки можуть містити наповнювачі, такі як мікрокристалічна целюлоза, лактоза, цитрат натрію, карбонат кальцію, двоосновний фосфат кальцію та гліцин, дезінтегранти, такі як крохмаль (переважно кукурудзяний, картопляний або крохмаль тапіоки), натрію крохмальгліколят, кроскармелоза натрію та конкретні комплексні силікати та зв'язуючі грануляції, такі як полівінілпіролідон, гідроксипропілметилцелюлоза (HPMC), гідроксипропілцелюлоза (HPC), цукроза, желатин та камедь. [0103] Додатково можна включити змащуючі засоби, такі як стеарат магнію, стеаринова кислота, гліцерилбегенат та тальк. [0104] Композиції можна вводити перорально, в формі таблеток, мікрочасток, мінітаблеток, капсул, саше швидкого або контрольованого вивільнення та пероральних розчинів або суспензій, або порошків для їх отримання. На додаток до нових твердих форм пантопразолу даного винаходу в якості активної речовини, пероральні перпарати можуть необов'язково містити різні стандартні фармацевтичні носії та наповнювачі, такі як зв'язуючі, заповнювачі, буфери, змащувальні засоби, речовини, які сприяють ковзанню, барвники, дезінтегранти, запашні речовини, підсолоджувачі, поверхнево-активні речовини, антиадгезійні мастила, антиадгезивні засоби та покриття. Деякі наповнювачі можуть мати багато задач в композиціях, наприклад, діють як і зв'язуючі, так і дезінтегранти. [0105] Приклади фармацевтично прийнятних дезінтегрантів для пероральних композицій включають крохмаль, пептизований крохмаль, натрію крохмаль гліколят, натрію карбоксиметилцелюлоза, кроскармелоза натрію, мікрокристалічна целюлоза, альгінати, смоли, поверхнево-активні речовини, шипучі композиції, водні алюмінію силікати та поперечно-зшитий полівінілпіролідон. [0106] Приклади фармацевтично прийнятних зв'язуючих для пероральних композицій включають камедь; похідні целюлози, такі як метилцелюлоза, карбоксиметилцелюлоза, гідроксипропілметилцелюлоза, гідроксипропілцелюлоза або гідроксиетилцелюлоза; желатин, глюкозу, декстрозу, ксилол, поліметакрилати, полівінілпіролідон, сорбіт, крохмаль, пептизований крохмаль, трагакант, ксантанову камедь, альгінати, магнію-алюмінію силікати, поліетиленгліколь або бентоніт. 13 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 [0107] Приклади фармацевтично прийнятних наповнювачів для пероральних композицій включають лактозу, ангідролактозу, лактози моногідрат, цукрозу, декстрозу, маніт, сорбіт, крохмаль, целюлозу (особливо мікрокристалічну целюлозу), дигідро- або ангідрокальцію фосфат, кальцію карбонат та кальцію сульфат. [0108] Приклади фармацевтично прийнятних змащувальних засобів, придатних в композиціях даного винаходу, включають стеарат магнію, тальк, поліетиленгліколь, полімери етилeноксиду, натрію лаурил сульфат, магнію лаурил сульфат, натрію олеат, натрію стeарил фумарат та колоїдний діоксид кремнію. [0109] Приклади придатних фармацевтично прийнятних душистих речовин для пероральних композицій включають синтетичні аромати та природні ароматичні олії, такі як екстракти олій, квітів, фруктів (наприклад, банан, яблуко, морель, персик) та їх комбінації, та подібні аромати. Їх застосування залежить від багатьох факторів, найбільш важливим є органолептична придатність для особин, які будуть приймати фармацевтичні композиції. [0110] Приклади придатних фармацевтично прийнятних барвників для пероральних композицій включають синтетичні та натуральні барвники, такі як титану діоксид, бета-каротин та екстракти шкірки грейпфруту. [0111] Приклади придатних фармацевтично прийнятних покриттів для пероральних композицій, типово застосовуваних для полегшення ковтання, модифікації властивостей вивільнення, покращення зовнішнього вигляду та/або маскування смаку композицій, включають гідроксипропілметилцелюлозу, гідроксипропілцелюлозу та співполімери акрилату-метакрилату. [0112] Приклади фармацевтично прийнятних підсолоджувачів для пероральних композицій включають аспартам, сахарин, сахарин натрію, натрію цикламат, ксилітол, маніт, сорбіт, лактозу та цукрозу. [0113] Приклади фармацевтично прийнятних буферів включають лимонну кислоту, натрію цитрат, натрію бікарбонат, двоосновний натрію фосфат, магнію оксид, кальцію карбонат та магнію гідроксид. [0114] Приклади фармацевтично прийнятних поверхнево-активних речовин включають натрію лаурилсульфат та полісорбати. [0115] Тверді композиції подібного типу можна також використовувати в якості заповнювачів в желатинових капсулах. Переважні наповнювачі при цьому включають лактозу, крохмаль, целюлозу, молочний цукор або високомолекулярні поліетиленгліколі. Для водних суспензій та/або еліксирів засіб можна комбінувати з різними підсолоджуючими або ароматизуючими засобами, фарбуючими речовинами або барвниками, з емульгуючими та/або суспендуючими засобами та з розріджувачами, такими як вода, етанол, пропілeнгліколь та гліцерин, та їх комбінаціями. [0116] Сполуки даного винаходу можна також, наприклад, складати як супозиторії, наприклад, які містять звичайні супозиторні основи, для застосування в лікарських препаратах для людей або ветеринарії або в якості песаріїв, наприклад, які містять звичайні основи для песаріїв. [0117] Сполуки за даним винаходом можна складати для місцевого введення, для застосування в лікарських препаратах для людей та ветеринарії, в формі мазей, кремів, гелів, гідрогелей, лосьонів, розчинів, шампуней, порошків (включаючи спрей або присипки), песаріїв, тампонів, спреїв, розчинів, аерозолів, крапель (наприклад, крапель для очей, вух або носа) або речовин для зрошування [0118] Для застосування місцево на шкірі засіб даного винаходу можна складати в якості придатної мазі, яка містить активну сполуку, суспендовану або розчинену в, наприклад, суміші з одним або декількома з наступного: мінеральне масло, рідкий вазелін, медичний вазелін, пропілeнгліколь, поліоксіетилeну-поліоксипропілeну сполука, емульгуючий віск, сорбітану монoстеарат, поліетиленгліколь, рідкий парафін, полісорбат 60, цетилових складних ефірів віск, цетеариловий спирт, 2-октилдодеканол, бензиловий спирт та вода. Такі композиції можуть також містити інші фармацевтично прийнятні наповнювачі, такі як полімери, олії, рідкі носії, поверхнево-активні речовини, буфери, консерванти, стабілізатори, антіоксиданти, зволожувачі, пом'якшувачі, пігменти та запашні речовини. [0119] Приклади фармацевтично прийнятних полімерів, придатних для таких місцевих композицій, включають акрилові полімери; похідні целюлози, такі як карбоксиметилцелюлоза натрію, метилцелюлоза або гідроксипропілцелюлоза; природні полімери, такі як альгінати, трагакант, пектин, ксантан та цитозан. [0120] Приклади придатних фармацевтично прийнятних олій, які також застосовні, включають мінеральні масла, силіконові масла, жирні кислоти, спирти та гліколі. [0121] Приклади придатних фармацевтично прийнятних рідких носіїв включають воду, 14 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 спирти або гліколі, такі як етанол, ізопропанoл, пропілeнгліколь, гексилeнгліколь, гліцерин та поліетиленгліколь, або їх суміші, в яких псевдополіморф розчинений або диспергований, необов'язково з додаванням нетоксичних аніонних, катіонних або неіонних поверхнево-активних речовин та неорганічних або органічних буферів. [0122] Приклади фармацевтично прийнятних консервантів включають натрію бензоат, аскорбінову кислоту, складні ефіри п-гідроксибензойної кислоти та різні антибактеріальні та протигрибкові засоби, такі як розчинники, наприклад, етанол, пропілeнгліколь, бензиловий спирт, хлорбутанол, четвертинні амонієві солі та парабени (такі як метилпарабен, етилпарабен та пропілпарабен). [0123] Приклади фармацевтично прийнятних стабілізаторів та антіоксидантів включають етилeндіамінтетраоцтову кислоту (EDTA), тіосечовину, токоферол та бутилгідроксианізол. [0124] Приклади фармацевтично прийнятних зволожувачів включають гліцерин, сорбіт, сечовину та поліетиленгліколь. [0125] Приклади фармацевтично прийнятних пом'якшувачів включають мінеральні олії, ізопропілміристат та ізопропілпальмітат. [0126] Сполуки можна вводити також на шкіру або трансдермально, наприклад, шляхом застосуванням пластира для шкіри. [0127] Для офтальмічного застосування сполуки можна складати як тонкодисперсні суспензії в ізотонічному, pH відрегульованому, стерильному сольовому розчині або переважно як розчини в ізотонічному, pH відрегульованому, стерильному сольовому розчині, необов'язково в комбінації з консерванотом, таким як бензилалконію хлорид. [0128] Як вказано, сполуки даного винаходу можна вводити інтраназально або інгаляцією та звичайно доставляють в формі інгалятора сухого порошку або аерозоля для випуску з контейнера під тиском, насоса, розпилювача або небулайзера з застосуванням придатного пропелента, наприклад, дихлордифторметану, трихлорфторметану, дихлортетрафторетану, гідрофторалкану, такого як 1,1,1,2-тетрафторетан (HFA 134AT) або 1,1,1,2,3,3,3гептафторпропан (HFA 227EA), діоксиду вуглецю або іншого придатного газу. У випадку аерозолю під тиском одиницю дозування можна визначити за допомогою клапана для доставки відміряної кількості. Контейнер, насос, розпилювач або небулайзер під тиском можуть містити розчин або суспензію активної сполуки, наприклад, використовуючи суміш етанолу та пропеленту в якості розчинника, який може додатково містити змащувальний засіб, наприклад, сорбітан триолеат. [0129] Капсули та картриджі (зроблені, наприклад, з желатину) для застосування в інгаляторі або інсуфляторі можна скласти так, щоб вони містили порошкову суміш сполуки та придатну порошкову основу, таку як лактоза або крохмаль. [0130] Для місцевого введення інгаляцією сполуки за даним винаходом можна доставляти для застосування у медицині для людей або ветеринарії за допомогою небулайзера. [0131] Фармацевтичні композиції даного винаходу можуть містити від 0,01 до 99 % ваги на об'єм активного матеріалу. Для місцевого введення, наприклад, композиція типово містить 0,0110 %, більш переважно 0,01-1 %, активного матеріалу. [0132] Активні засоби можна також вводитит в формі систем доставки ліпосом, таких як маленьких моноламелярних везикул, великих моноламелярних везикул та багатошарових везикул. Ліпосоми можна сформувати з різноманітних фосфоліпідів, таких як холестерин, стеариламін або фосфатидилхоліни. [0133] Фармацевтичну композицію або стандартну лікарську форму даного винаходу можна вводити в залежності від дозування та режиму введення, визначеного звичайним тестуванням з урахуванням принципів, даних вище, для отримання оптимальної активності при мінімізації токсичності або побічних ефектів для конкретного пацієнта. Проте, таке точне регулювання терапевтичного режиму є звичайним в світлі принципів, наданих в даному документі. [0134] Дозування активних засобів даного винаходу може варіювати відповідно до різноманітних факторів, таких як основні стани захворювання, стан особи, вага, стать та вік, та режим введення. Ефективну кількість для лікування розладу можна легко визначити емпіричними способами, відомими спеціалістам в даній області техніки, наприклад, встановленням матриці дозувань та частот введення та порівняння групи експериментальних елементів або суб'єктів в кожній точці в матриці. Точна кількість, яку необхідно ввести пацієнту, буде варіювати залежно від стану та тяжкості розладу та фізичного стану пацієнта. Помітне покращення будь-якого симптому або параметра може бути визначене спеціалістом в даній області техніки або описане пацієнтом лікарю. Зрозуміло, що будь-яке клінічно або статистично суттєве послаблення або покращення будь-якого симптому або параметра розладів сечових шляхів знаходиться в обсязі даного винаходу. Клінічно суттєве послаблення або покращення 15 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 означає помітний пацієнту та/або лікарю. [0135] Наприклад, один пацієнт може страждати від декількох симптомів дизурії одночасно, таких як, наприклад, невідкладний позив до сечовипускання та перевищена частота сечовипускання, або обидва, та їх можна послабити за допомогою способів даного винаходу. У випадку нетримання будь-яке зменшення частоти або об'єму небажаного випускання сечі розглядають як цілющий ефект даного способу лікування. [0136] Кількість засобу, яку необхідно вводити, може бути в діапазоні між приблизно 0,01 та приблизно 25 мг/кг/день, переважно між приблизно 0,1 та приблизно 10 мг/кг/день та найбільш переважно між 0,2 та приблизно 5 мг/кг/день. Буде зрозуміло, що фармацевтичні склади даного винаходу не мають обов'язково містити усю кількість засобу, який є ефективним у лікуванні розладу, власне, ефективні кількості можуть бути досягнуті введенням декількох доз таких фармацевтичних складів. [0137] В переважному варіанті здійснення даного винаходу сполуки I складені в капсули або таблетки, які переважно містять 10-200 мг сполук даного винаходу, та переважно їх вводять пацієнту в загальній добовій дозі 10-300 мг, переважно 20-150 мг та найбільш переважно приблизно 50 мг, для послаблення нетримання сечі та інших розладів. [0138] Фармацевтична композиція для парентерального введення містить від приблизно 0,01 % до приблизно 100 % за вагою активних засобів даного винаходу, на основі 100 % ваги загальної фармацевтичної композиції. [0139] Загалом, трансдермальні лікарські форми містять від приблизно 0,01 % до приблизно 100 % за вагою активних засобів відносно 100 % загальної ваги лікарської форми. [0140] Фармацевтичну композицію або стандартну лікарську форму можна вводити в однократній добовій дозі, або загальне добове дозування можна вводити подрібненними дозами. До того ж сумісне введення або послідовне введення іншої сполуки для лікування розладу може бути бажаним. Для цієї цілі об'єднані активні діючі речовини складають в просту одиницю дозування. [0141] Для комбінованого лікування, де сполуки знаходяться в окремих лікарських складах, сполуки можна вводити одночасно, або кожну можна вводити з диференційованими інтервалами. Наприклад, сполуку даного винаходу можна вводити вранці та антимускаринову сполуку можна вводити ввечері, або навпаки. Додаткові сполуки можна вводити з конкретними інтервалами також. Порядок введення буде залежати від різноманітних факторів, включаючи вік, вагу, стать та медичний стан пацієнта; тяжкість та етіологію розладів, які треба лікувати, шлях введення, ренальну та печінкову функцію пацієнта, історію хвороби пацієнта та сприйнятливість пацієнта. Визначення порядку введення може бути точно відрегульоване, та таке точне регулювання є звичайним в світлі принципів, наданих в даному документі. Синтез сполук даного винаходу [0142] Сполуки формули I та їх енантіомери, діастереомери, N-оксиди та фармацевтично прийнятні солі можна отримати загальними способами, зазначеними нижче в даному документі, причому вказані способи містять додатковий аспект даного винаходу. [0143] Спеціалістами в даній області техніки буде оцінено, що може бути бажаним застосовувати захищені похідні проміжних сполук, застосовуваних в отриманні сполук I. Захист та зняття захисту з функціональних груп можна виконувати способами, відомими в даному рівні техніки (дивись, наприклад, Green and Wuts Protective Groups in Organic Synthesis. John Wiley та Sons, New York, 1999). Гідроксі- або аміногрупи можна захистити будь-якими гідроксі- або амінозахисною групою. Амінозахисні групи можна видаляти звичайними техніками. Наприклад, ацильні групи, такі як алканоїльні, алкоксикарбонільні та ароїльні групи, можна видалити сольволізом, наприклад, гідролізом за кислотних або основних умов. Арилметоксикарбонільні групи (наприклад, бензилоксикарбоніл) можна розщепити гідрогенолізом в присутності каталізатора, такого як паладій на активованому вугіллі. [0144] Синтез цільових сполук завершують видаленням будь-яких захисних груп, які можуть бути присутні в передостанніх проміжних сполуках за допомогою стандартних технік, добре відомих фахівцям даної галузі техніки. Кінцеві продукти без захисних груп потім очищують, якщо необхідно, за допомогою стандартних технік, таких як хроматографія на силікагелі, ВЕРХ на силікагелі і т.і., та/або перекристалізацією. [0145] Сполуки даного винаходу типово отримують згідно з наступною схемою: 16 UA 110343 C2 5 10 15 20 25 30 35 40 [0146] На схемі 1 "Ak" представляє собою нижчу алкільну групу, та інші змінні є такими, як визначено для загальної формули I або всередині самої схеми. [0147] Циклічні кетони 1 комерційно доступні або їх можна легко отримати стандартними способами, відомими фахівцям даної галузі техніки, наприклад, з піперидону (R1=N) з карбонільною групою, який може бути або може не бути попередньо захищений (наприклад, як кеталь, наприклад, як 1,3-діоксолан) простим нуклеофільним заміщенням активованих галогенарилів, галогеналкілів або галогенгетероарилів, яке можна проводити в придатному розчиннику (такому як н-бутанол, DMF, N-метилпіролідон або N, N-диметилацетамід) при температурі між кімнатною температурою та кипінням обраного розчинника в присутності основи, такої як триетиламін або 4,4-диметиламінопіридин. Реакцію можна проводити також з мікрохвильовим випроміненням в мікрохвильовому апараті для зменшення часу реакції. Альтернативний загальний спосіб одержання піперидонів з неактивованих галогенарилів або галогенгетероарилів (або трифлатів) представлений амінуванням Бухвальда-Хартвіга за допомогою паладієвого каталізатора або амінуваннями, каталізованими іншими металами. Дуже добре відомі процедури відновного амінування можна використовувати, де R4(R5)1 являє собою алкіл. Циклічні кетони 1 реагують з ілідами, наприклад, отриманими додаванням основи (наприклад, LiHMDS або калію трет-бутоксиду в апротонному розчиннику типу THF або діетилового ефіру) до, наприклад, метилтрифенілфосфонію броміду, для забезпечення похідних екзометилeну 2. Похідні метилeну 2, в свою чергу, циклізують за допомогою методики 1,3-диполярного циклоприєднання до похідних алкінілу 3 (Hao-Wei Shih et. al., Тетраhedron letters 49 (2008) 1008-1011, WO 20006/122770). Для цього триалкілсілілпропіоальдегіди оксимів перетворюють in situ (або виділенням проміжних сполук) в відповідні хлор- або бромоксими (наприклад, застосуванням N-бромсукциніміду або N-хлорсукциніміду або натрію гіпохлориту або гіпоброміту або трет-бутилгіпохлориту в придатному розчиннику, такому як дихлорметан або DMF, з або без додавання води), які виділяють або безпосередньо трансформують в реакційній посудині в відповідні нітрилоксиди за допомогою слабкої основи, такої як Na 2CO3, триетиламін або етилмагнію бромід. Нітрилоксиди реагують дуже легко зі сполуками 2 в звичайному розчиннику, такому як дихлорметан або DMF, як правило, при від -78 °C до 0° до кімнатної температури або нагріванні до кипіння обраного розчинника, даючи сполуки 3. [0148] Сілільну захисну групу сполуки 3 потім видаляють обробкою тетрабутиламонію фторидом в THF при температурі у діапазоні від температури навколишнього середовища до кипіння, або гідролізом з основою (K2CO3 або KOH в MeOH), або іншим придатним способом, обраним з тих, які описані в Greene-Wuts (Greene's Protective Groups in Organic Synthesis, 3rd Edition, Peter G. M. Wuts, Theodoura W. Greene 1999, Wiley Interscience page 654-659) та добре відомі спеціалістам в даній області техніки. Отримані ацетиленові сполуки потім трансформують в сполуки 4 їх реакцією з R3-LG з наступною добре відомою процедурою Соногашири (Science of Synthesis, H. Heaney and S. Christie, October 2003, Vol. 3, Page 402 і наступні). В цій процедурі застосовують міді йодид та паладієвий комплекс, обраний з (Ph3P)2PdCl2, (Ph3P)2Pd(OAc)2, (Ph3P)4Pd (які можна також утворити in situ, наприклад, з трифенілфосфіну та Pd(OAc)2), та всі інші паладієві комплекси, вказані в літературі та застосовувані для цього типу реакції, в присутності основи, такої як TEA, DEA, DIPEA, TMA, бутиламін, піперидин. Розчинники вибирають серед THF, DME, DMF, DMA, EtOAc, DMSO, толуолу та інших придатних для цілей реакції; або така саме основа в надлишку може 17 UA 110343 C2 5 10 15 20 25 30 35 40 використовуватися в якості реакційного розчинника. Якщо виконують реакцію в DMF або DME, виділення сполук 4 можна уникнути додаванням тетрабутиламонію фториду або тетрабутиламонію хлориду безпосередньо до реакційного середовища, яке містить 3, перед сполученням (Sorensen, U.S., Pombo-Villar, E. Тетраhedron 2005, 61, 2697-2703). R3-замісники вводять за допомогою арилових або гетероарилових галогенідів (переважно в порядку зменшення - йодид, бромід, хлорид), арилових або гетероарилових трифлатів, алкілгалогенiдів або ацилхлоридів, ароїлхлоридів, гетероароїлхлоридів. Трифлати синтезують за допомогою дуже добре відомого фахівцям в даній галузі техніки способом, наприклад, з фенолів або гідроксіарилів (гетероарилів) за допомогою трифторметансульфонового ангідриду в хлорованому розчиннику або за допомогою N-фенілтрифліміду в толуолі або хлорованого розчинника в присутності або відсутності основи (наприклад, TEA). Обидва сопособи можна прискорити за допомогою мікрохвиль, виконуючи реакцію в мікрохвильовій печі. Іншими придатними групами, що заміщуються, LG для R3-LG є нонафлати, тозилати та калію трифторборати. Де R3 являє собою Ak, альтернативною процедурою для сполучення Соногашири є реакція сполук 4 з літієвою основою (наприклад, бутиллітій або LHDMS) в придатному розчиннику, наприклад, для отримання літійалкінільної похідної, яка в свою чергу реагує з придатним електрофілом, таким як, наприклад, бутил йодид або подібне, в такому саме розчиннику або в альтернативному апротонному розчиннику, такому як толуол, при температурі в діапазоні від -20 °C до кипіння обраного розчинника. [0149] Якщо сполуки 4 отримують такі, в яких Q являє собою захисну групу, вони потребують додаткового сняття захисних груп та N-арилювання/алкілювання або інших типів етапів отримання похідних для забезпечення сполуки I. [0150] Сполуки 4 можна отримати безпосередньою реакцією сполук 2 з відповідними похідними пропіоальдегід оксимів, в яких R3-група заміщує триалкілсілільну групу. [0151] На схемі 2 "Ak" представляє собою групу нижчого алкілу, та останні змінні визначені для загальної формули I або на самій схемі. Схема 2 представляє собою альтернативну процедуру для отримання сполук I, де R3 являє собою Ak. Приводячи в реакцію дибромформальдоксим, як описано вище для отримання сполук 3, можна синтезувати сполуки 5. Бромoксазолін 5 можна додатково алкінілювати застосування алкінів, придатної основи, такої як натрію карбонат, за допомогою Cu/CuI спільного каталізу, як описано детально в експериментальній частині. Якщо Q являє собою захисну групу в отриманих сполуках 6, вони потребують додаткового зняття захисних груп та Nарилювання/алкілювання або інших типів етапів отримання похідних для забезпечення сполук I. [0152] Сполуки 6 можна отримати безпосередньою реакцією сполук 2 з придатними алкілпропіоальдегід оксимами. [0153] Інші спірогетероциклічні проміжні сполуки відмінні від спірооксазолінів можна синтезувати наступними способами, зазначеними в літературі та вказаними в експериментальній частині в якості посилань. [0154] Синтез інших сполук, на даний час не описаний в загальному описі вище, добре 18 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 задокументований в експериментальній частині даного винаходу, яка йде далі. [0155] Вільні основи формули I, їх діастереомери або енантіомери можна перетворювати в відповідні фармацевтично прийнятні солі за стандартних умов, добре відомих в даному рівні техніки. Наприклад, вільну основу розчиняють в придатному органічному розчиннику, такому як метанол, обробленому, наприклад, одним еквівалентом малеїнової або щавелевої кислоти, одним або двома еквівалентами соляної кислоти або метансульфонової кислоти, та потім концентрують в вакуумі для забезпечення відповідної фармацевтично прийнятної солі. Залишок можна потім очистити перекристалізацією з придатного органічного розчинника або суміші органічних розчинників, такої як метанол/діетиловий ефір. [0156] N-оксиди сполук формули I можна синтезувати процедурами простого окиснення, добре відомими фахівцям даної галузі техніки. Приклади [0157] Наступні приклади ілюструють синтез сполук формули I, як описано загалом вище. Ці приклади є лише ілюстративними та не призначені для обмеження обсягу даного винаходу. Реагенти та початкові матеріали легко доступні фахівцю в даній галузі. Приклад 1 3-фенілетиніл-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен 3-фенілпроп-2-іналь оксим (сполука 1a) Суміш фенілпропаргілальдегіду (859 мг, 6,6 ммоль), гідроксиламіну гідрохлориду (4,59 г, 66 ммоль), EtOH (48 мл) та води (12 мл) перемішували при к.т. протягом 24 годин. Реакційну суміш розвели H2O, екстрагували Et2O-EtOAc, промили розсолом та випарили насухо in vacuo, забезпечуючи 0,96 г титульної сполуки (син:анті 1:1) в вигляді в'язкої коричневатої твердої речовини. + MS: [M+H] = 146,11 3-фенілетиніл-8-(трет-бутоксикарбоніл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен (сполука 1b) До розчину сполуки 1a (0,35 г, 2,41 ммоль) в 3 мл DMF, перемішаного при к.т., додали Nхлорсукцинімід (0,386 г, 2,89 ммоль) та розчин ставав помаранчевого кольору. Через 2 години перемішування розчин ставав жовтим, та через додаткові 2 години перемішування його охолоджували до 0 °C, та розчин 1-(трет-бутоксикарбоніл)-4-метилeнпіперидину (143 мг, 0,73 ммоль) в 0,5 мл DMF додавали, з наступним розчином TEA в 0,5 мл DMF. Охолоджувальну баню видаляли та реакційну суміш перемішували при к.т. протягом 2 днів. Потім реакційну суміш розвели холодною водою, екстрагували EtOAc. Екстракти промили розсолом, висушили над Na2SO4, випарювали насухо in vacuo. Неочищений матеріал очистили автоматизованою ® флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір-EtOAc від 95:5 до 7:3), забезпечуючи 210 мг титульного продукту. Вихід: 85,5 %. + MS: [M+H] = 341,16 3-фенілетиніл-1-окса-2,8-діазаспіро[4.5]дец-2-ен (сполука 1c) До розчину сполуки 1b (200 мг, 0,59 ммоль) в CH2Cl2 (12 мл), перемішаної при 0 °C, додали трифтороцтову кислоту (452 мкл, 5,87 ммоль) та реакційну суміш перемішували при 25 °C протягом 24 годин, доки повне перетворення реагуючої речовини не спостерігали за допомогою LC-MS. Воду додали з наступним 3н водн. NaOH для отримання лужного pH. Розділення органічного шару та екстракція водного шару CH2Cl2, промиття розсолом та сушка над Na2SO4 об'єднаних органічних шарів забезпечувало титульну сполуку в вигляді бежевої твердої речовини, застосовуваної на наступному етапі без додаткової очистки. + MS: [M+H] = 241,29 3-фенілетиніл-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Розчин сполуки 1c (50 мг, 0,21 ммоль), 2-хлор-6-метил-3-нітропіридину (39,5 мг, 0,23 ммоль) та триетиламіну (31,9 мкл, 0,23 ммоль) в N, N-диметилацетаміді (1,14 мл) перемішували при к.т. протягом 24 годин та вилили в воду. Водний шар екстрагували EtOAc. Об'єднані екстракти промили водою, висушили над Na2SO4 та випарювали насухо in vacuo. Неочищений продукт ® очистили автоматизованою флеш-хроматографією (SP1 TM – Вiotage), при елююванні з сумішшю петролейного ефіру-Me2CO 95:5. Додаткова очистка з CH2Cl2 в якості елюенту забезпечила 47,7 мг титульної сполуки (67,7 %) в вигляді жовтої твердої речовини. + MS: [M+H] = 377,22 1 H-ЯМР: (CDCl3, δ): 1,90-2,11 (m, 4H), 2,50 (s, 3H), 3,00 (s, 2H), 3,50-3,71 (m, 4H), 6,63 (d, J=8 Гц, 1H), 7,34-7,46 (m, 3H), 7,51-7,57 (m, 2H), 8,11 (d, 8 Гц, 1H). Приклад 2 3-фенілетиніл-8-(3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен 2-(4-метилeн-1-піперидил)-3-нітропіридин (сполука 2a) н-бутиллітій в гексані (2,5 M, 4,93 мл, 12,3 ммоль) додали по краплях за 10 хв. в суспензію 19 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 98 % метилтрифенілфосфонію броміду (4,65 г, 12,8 мммоль) в 40 мл THF, перемішаного при 70 °C. Через 0,5 години розчин 1-(3-нітро-2-піридил)-4-оксо-піперидину (2 г, 8,5 ммоль) в 16 мл THF додали та реакційній суміші дозволили нагрітись до к.т. Після того, як її залишили на ніч, суміш погасили водним насиченим розчином NH4Cl, екстрагували EtOAc, висушили над Na2SO4, та випарювали насухо in vacuo. Неочищений продукт очистили автоматизованою флеш® хроматографією (SP1 TM – Вiotage) при елююванні з градієнтом петролейного ефіру–EtOAc від 1:0 до 9:1, даючи 1,23 г титульної сполуки в вигляді жовтої твердої речовини. + MS: [M+H] = 220,18 3-фенілетиніл-8-(3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали, як описано для сполуки 1b, але за допомогою сполуки 2a замість 1-(трет-бутоксикарбоніл)-4-метилeн-піперидину. Після звичайної обробки суміш ® очистили автоматизованою флеш-хроматографією (SP1 TM – Вiotage) при елююванні з градієнтом петролейний ефір–EtOAc від 95:5 до 7:3, даючи 25 мг титульної сполуки. Вихід: + MS: [M+H] = 363,54 1 H-ЯМР: (CDCl3, δ): 1,90-2,11 (m, 4H), 3,00 (s, 2H), 3,51-3,70 (m, 4H), 6,76-6,83 (m, 1H), 7,347,46 (m, 3H), 7,47-7,51 (m, 2H), 8,14-8,18 (m, 1H), 8,36-8,38 (m, 1H). Приклад 3 3-[(6-метил-2-піридил)-етиніл]-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2ен 6-метил-2-(4-метилен-1-піперидил)-3-нітропіридин (сполука 3a) Титульний продукт синтезували за процедурою, вказаною для сполуки 2a, але замінюючи 1(3-нітро-2-піридил)-4-оксо-піперидин на 1-(6-метил-3-нітро-2-піридил)-4-oксoпіперидин. Вихід: 62 %. + MS: [M+H] = 233,12 N-гідрокси-3-триметилсіліл-проп-2-інімідоїлхлорид (сполука 3b) До розчину 68 г (11,9 ммоль) 3-триметилсілілпроп-2-іналь оксиму [Carreira, Erick M. et al., Organic Letters, Volume 7, Issue 10, 2005, Pages 2011-2014] в 11,9 мл DMF, перемішаного при к.т., додали N-хлорсукцинімід (1,99 г, 14,8 ммоль). Через 4 години перемішування розчин вилили в воду та екстрагували Et2O. Після звичайної обробки залишок (2,09 г) застосовували як такий для наступного етапу. 3-(триметилсілілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен (сполука 3c) Розчин TEA (0,554 мл, 3,85 ммоль) в 9,4 мл diхлорметану додали по краплях в розчин сполуки 3b (1,67 г, 2,57 ммоль) та сполуки 3a (600 мг, 2,57 ммоль) в 42 мл дихлорметану, перемішаного при 0 °C. Потім реакційну суміш перемішували при к.т. протягом 24 годин; потім її розводили холодною водою. Органічний шар промили розсолом, висушили над Na2SO4 та випарювали насухо in vacuo. Неочищений матеріал очистили автоматизованою флеш® хроматографією (SP1 TM – Вiotage; градієнт CH2Cl2-петролейний ефір-EtOAc від 5:5 до 10:0), забезпечуючи 641 мг титульного продукту. Вихід: 67 %. + MS: [M+H] = 273,43 3-[(6-метил-2-піридил)-етиніл]-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2ен Суспензія сполуки 3c (58 мг, 0.16 ммоль), натрію ацетату тригідрат (42,5 мг, 0,31 ммоль), 2бром-6-метилпіридин (26, 8 мг, 0,16 ммоль), тетрабутиламонію фторид (40,8 мг, 0,156 ммоль) та тетракіс(трифенілфосфін)паладій(0) (15,8 мг, 0,014 ммоль) в 2,05 мл DMF, промитий азотом, нагрівали в мікрохвильовій печі (Biotage) при 120 °C протягом 10 хв. Розведення EtOAc, промивання H2O та сушка над Na2SO4 з наступним випарюванням та очисткою залишку ® автоматизованою рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 9:1 до 6:4) забезпечують 17,4 мг (28,5 %) титульної сполуки в вигляді жовтого масла. + MS: [M+H] = 392,33 1 H-ЯМР: (CDCl3, δ): 1,90-2,07 (m, 4H), 2,48 (s, 3H), 2,66 (s, 3H), 3,04 (s, 2H), 3,50-3,68 (m, 4H), 6,62 (d, J=8 Гц, 1H), 7,22-7,26 (m, 1H), 7,42-7,46 (m, 1H), 7,65-7,61 (m, 1H), 8,10 (d, J=8 Гц, 1H). Приклад 4 3-(2-тієнілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, але за допомогою 2-бромтіофену замість 2-бром-6-метилпіридину. Очистка залишку ® автоматизованою рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 9:1 до 6:4). Вихід: 26,7 %. + MS: [M+H] = 383,52 20 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 5 3-(2-піридилетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, але за допомогою 2-йодпіридину замість 2-бром-6-метилпіридину. Очистку залишку ® автоматизованою рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 9:1 до 4:6). Вихід: 49,6 %. + MS: [M+H] = 378,46 1 H-ЯМР: (CDCl3, δ): 1,90-2,09 (m, 4H), 2,49 (s, 3H), 3,03 (s, 2H), 3,51-3,67 (m, 4H), 6,63 (d, J=8 Гц, 1H), 7,36-7,41 (m, 1H), 7,59-7,63 (m, 1H), 7,76-7,82 (m, 1H), 8,11 (d, J=8 Гц, 1H), 8,66-8,69 (m, 1H). Приклад 6 3-(2-фторфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, але за допомогою 2-фторйодбензолу замість 2-бром-6-метилпіридину. Очистка залишку ® автоматизованою рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 95:5 до 7:3). Вихід: 42,6 %. + MS: [M+H] = 395,27 1 H-ЯМР: (CDCl3, δ): 1,90-2,11 (m, 4H), 2,50 (s, 3H), 3,02 (s, 2H), 3,50-3,70 (m, 4H), 6,63 (d, J=8 Гц, 1H), 7,09-7,21 (m, 2H), 7,36-7,45 (m, 1H), 7,49-7,57 (m, 1H), 8,11 (d, J=8 Гц, 1H). Приклад 7 3-(3-фторфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, але за допомогою 3-фторйодбензолу замість 2-бром-6-метилпіридину. Вихід: 42,4 % + MS: [M+H] = 395,41 1 H-ЯМР: (CDCl3, δ): 1,90-2,11 (m, 4H), 2,50 (s, 3H), 2,99 (s, 2H), 3,50-3,70 (m, 4H), 6,63 (d J=8 Гц, 1H), 7,09-7,17 (m, 1H), 7,20-7,27 (m, 1H), 7,30-7,39 (m, 2H), 8,11 (d, 8 Гц, 1H). Приклад 8 3-(4-фторфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 4-фторйодбензолу замість 2-бром-6-метилпіридину. Вихід: 37,7 % + MS: [M+H] = 395,27 1 H-ЯМР: (CDCl3, δ): 1,90-2,10 (m, 4H), 2,50 (s, 3H), 2,99 (s, 2H), 3,50-3,70 (m, 4H), 6,63 (d J=8 Гц, 1H), 7,04-7,13 (m, 2H), 7,50-7,57 (m, 2H), 8,11 (d, J=8 Гц, 1H). Приклад 9 3-(2-фурилетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 2-бромфурану замість 2-бром-6-метилпіридину. Очистка залишку автоматизованою ® рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 95:5 до 6:4). Вихід: 12,6 %. + MS: [M+H] = 367,33 Приклад 10 3-[(2-метил-1,3-тіазол-4-іл)-етиніл]-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 4-бром-2-метилтіазолу замість 2-бром-6-метилпіридину. Очистка залишку ® автоматизованою рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 9:1 до 5:5). Вихід: 17,6 %. + MS: [M+H] = 398,35 Приклад 11 3-(проп-1-ініл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен 3-етиніл-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен (сполука 11a) До розчину сполуки 3c (360 мг, 0,96 ммоль) в 9 мл THF додали тетрабутиламонію фториду гідрат (269 мг, 0,963 ммоль) та реакційну суміш перемішували при к.т. протягом 4 годин. Після того, як його залишили на ніч, погасили водою, екстрагували EtOAc та випарили насухо, ® неочищений матеріал очистили автоматизованою рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 95:5 до 7:3), даючи сполуку 11a (0,231 г, 80 %). + MS: [M+H] = 301,36 3-(проп-1-ініл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен В розчин сполуки 11a (25 мг, 0,83 ммоль) в THF (1,26 мл), який підтримували при перемішуванні при -78 °C, бутиллітій в гексані (2,5 M, 0,04 мл, 0,1 ммоль) додавали по краплях. 21 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 Через 30 хв. додали метилйодид (6,22 мкл, 0,1 ммоль). Холодну баню видалили та помаранчевому розчину дозволили досягти к.т. Після того, як його залишили на ніч, його погасили насиченим водним розчином NH4Cl, екстрагували EtOAc, промили H2O, висушили над Na2SO4 та випарювали насухо in vacuo. Неочищений матеріал очистили автоматизованою ® рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 95:5 до 6:4), даючи 6 мг титульної сполуки. Вихід: 22,9 %. + MS: [M+H] = 315,32 Приклад 12 3-(3-хлорфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 3-хлорйодбензолу замість 2-бром-6-метилпіридину. Очистка залишку ® автоматизованою рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 9:1 до 7:3). Вихід: 55 %. + MS: [M+H] = 411,16 1 H-ЯМР: (CDCl3, δ): 1,90-2,11 (m, 4H), 2,50 (s, 3H), 2,99 (s, 2H), 3,50-3,70 (m, 4H), 6,64 (d, J=8 Гц, 1H), 7,29-7,35 (m, 1H), 7,39-7,45 (m, 2H), 7,53 (m, 1H), 8,11 (d, 8 Гц, 1H). Приклад 13 3-(3-метилфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 3-йодтолуолу замість 2-бром-6-метилпіридину. Жовта тверда речовина. Вихід: 59,6 % + MS: [M+H] = 391,42 1 H-ЯМР: (CDCl3, δ): 1,91-2,11 (m, 4H), 2,37 (s, 3H), 2,51(s, 3H), 2,99 (s, 2H), 3,52-3,70 (m, 4H), 6,64 (d, J=8 Гц, 1H), 7,20-7,27 (m, 2H), 7,29-7,38 (m, 2H), 8,12 (d, J=8 Гц, 1H). Приклад 14 3-(3-метоксифенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 3-метоксийодбензолу замість 2-бром-6-метилпіридину. Жовта тверда речовина. Вихід: 41 % + MS: [M+H] = 407,27 1 H-ЯМР: (CDCl3, δ): 1,90-2,09 (m, 4H), 2,49 (s, 3H), 3,00 (s, 2H), 3,52-3,70 (m, 4H), 3,84 (s, 3H), 6,63 (d, J=8 Гц, 1H), 6,95-7,00 (m, 1H), 7,06-7,08 (m, 1H), 7,12-7,16 (m, 1H), 7,26-7,32(m, 1H), 8,11 (d, J=8 Гц, 1H). Приклад 15 3-(3-ціанофенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 3-йодбензонітрилу замість 2-бром-6-метилпіридину. Очистка залишку ® автоматизованою рідинною флеш-хроматографією (Horizon TM – Biotage) (градієнт петролейний ефір–EtOAc від 95:5 до 5:5). Вихід: 66,5 %. + MS: [M+H] = 402,23 1 H-ЯМР: (CDCl3, δ): 1,90-2,09 (m, 4H), 2,49 (s, 3H), 3,00(s, 2H), 3,50-3,70 (m, 4H), 6,64 (d, J=8 Гц, 1H), 7,49-7,55 (m, 1H), 7,67-7,71 (m, 1H), 7,74-7,78 (m, 1H), 7,81-7,83 (s, 1H), 8,11 (d, J=8 Гц, 1H). Приклад 16 3-(3-тієнілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 3-бромтіофену замість 2-бром-6-метилпіридину. Очистка залишку автоматизованою TM рідинною флеш-хроматографією (Horizon – Biotage) (градієнт петролейний ефір–EtOAc від 7:3 до 3:7). Жовта тверда речовина. Вихід: 66,5 %. + MS: [M+H] = 383,22 1 H-ЯМР: (CDCl3, δ): 1,90-2,01 (m, 4H), 2,49 (s, 3H), 2,98 (s, 2H), 3,50-3,70 (m, 4H), 6,62 (d, J=8 Гц, 1H), 7,19-7,22 (m, 1H), 7,32-7,35 (m, 1H), 7,62-7,63 (m, 1H), 8,11 (d, J=8 Гц, 1H). Приклад 17 3-(3-піридилетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 3-йодпіридину замість 2-бром-6-метилпіридину. Після звичайної обробки ® неочищений матеріал очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 7:3 до 3:7), забезпечуючи титульний продукт в вигляді жовтої твердої речовини. Вихід: 66,7 %. + MS: [M+H] = 378,27 22 UA 110343 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 H-ЯМР: (CDCl3, δ): 1,90-2,09 (m, 4H), 2,49 (s, 3H), 3,01(s, 2H), 3,50-3,70 (m, 4H), 6,63 (d, J=8 Гц, 1H), 7,33-7,38 (m, 1H), 7,83-7,87 (m, 1H), 8,11 (d, J=8 Гц, 1H), 8,63-8,65 (m, 1H), 8,78-7,80 (s, 1H). Приклад 18 3-{3-(3-метил-[1,2,4]оксадіазол-5-іл)-фенілетиніл}-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 5-(3-бром-феніл)-3-метил-[1,2,4]оксадіазолу замість 2-бром-6-метилпіридину. Після звичайної обробки неочищений матеріал очистили автоматизованою флеш-хроматографією ® (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 95:5 до 6:4), забезпечуючи титульний продукт в вигляді жовтої твердої речовини. Вихід: 33,8 %. + MS: [M+H] = 459,11 1 H-ЯМР: (CDCl3, δ): 1,92-2,11 (m, 4H), 2,50-2,52 (m, 6H), 3,01(s, 2H), 3,52-3,70 (m, 4H), 6,64 (d, J=8 Гц, 1H), 7,54-7,59 (m, 1H), 7,72-7,76 (m, 1H), 8,10-8,17 (m, 2H), 8,29-8,31 (m, 1H). Приклад 19 3-(3-метилбут-1-иніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діаза-спіро[4.5]дец-2-ен 3-бром-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен (сполука 19a) Суспензія 6-метил-2-(4-метилeн-1-піперидил)-3-нітропіридину (сполука 3a, 350 мг, 1,5 ммоль), натрію карбонату (1,26 г, 15 ммоль) та дибромформальдоксиму (608 мг, 3 ммоль) в 25 мл EtOAc перемішували при к.т. протягом 2 днів. Потім реакційну суміш промили водою, висушили над натрію сульфатом та випарювали насухо in vacuo. Неочищений матеріал ® очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 9:1 до 6:4), даючи 377 мг титульного продукту. Вихід: 70,8 %. + MS: [M+H] = 356,41 3-(3-метилбут-1-иніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діаза-спіро[4.5]дец-2-ен Суміш сполуки 19a (50 мг, 0,141 ммоль), 3-метил-1-бутину (48 мг, 0,705 ммоль), натрію карбонату (74,6 мг, 0,704 ммоль) та Cu (44,8 мг, 0,705 ммоль) нагрівали в запаяній посудині при 120 °C протягом 32 годин, додаючи кожні 8 годин додаткові рівні кількості кількостей 3-метил-1бутину, натрію карбонату та Cu. Потім суміш охолоджували, додавали CH2Cl2, фільтрували на целіті та випарювали насухо in vacuo. Залишок очистили автоматизованою флеш® хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 95:5 до 75:25, потім ізократичним петролейним ефіром - EtOAc від 9:1, даючи 16 мг титульного продукту. Вихід: 33,1 %. + MS: [M+H] = 343,20 1 H-ЯМР: (CDCl3, δ): 1,26 (d, 6H, J=8 Гц), 1,86-2,05 (m, 4H), 2,49 (s, 3H), 2,73-2,81 (m, 1H), 2,86 (s, 2H), 3,48-3,65 (m, 4H), 6,62 (d, J=8 Гц, 1H), 8,10 (d, J=8 Гц, 1H). Приклад 20 3-(гекс-1-иніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт синтезували за способом, описаним для сполуки прикладу 19, але замінюючи 3-метил-1-бутин гекс-1-ином. Залишок очистили автоматизованою флеш® хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 95:5 до 85:15), даючи 7,8 мг титульного продукту. Вихід: 27,9 %. + MS: [M+H] = 357,27 1 H-ЯМР: (CDCl3, δ): 0,95-0,99 (m, 3H), 1,26-1,65 (m, 4H), 1,86-2,03 (m, 4H), 2,38-2,45 (m, 2H), 2,48 (s, 3H), 2,86 (s, 2H), 3,48-3,65 (m, 4H), 6,61 (d, J=8 Гц, 1H), 8,10 (d, 8 Гц, 1H). Приклад 21 3-(2-ціанофенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки прикладу 3, за допомогою 2-бромбензонітрилу замість 2-бром-6-метилпіридину. Після звичайної обробки ® неочищений матеріал очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 9:1 до 4:6), забезпечуючи титульний продукт в вигляді жовтого масла. Вихід: 74,8 %. + MS: [M+H] = 402,08 1 H-ЯМР: (CDCl3, δ): 1,90-2,11 (m, 4H), 2,49 (s, 3H), 3,06 (s, 2H), 3,50-3,70 (m, 4H), 6,63 (d, J=8 Гц, 1H), 7,48-7,54 (m, 1H), 7,60-7,74 (m, 3H), 8,11 (d, J=8 Гц, 1H). Приклад 22 3-(3-хлорфенілетиніл)-8-(3-ціано-2-піразиніл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен 3-триметилсілілетиніл-8-(трет-бутоксикарбоніл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен (Сполука 22a) Титульну сполуку синтезували згідно зі способом, вказаним для сполуки 3c за допомогою 1 23 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 (трет-бутоксикарбоніл)-4-метилeнпіперидину замість сполуки 3a. Після звичайної обробки ® неочищений матеріал очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 95:5 до 6:4), забезпечуючи титульний продукт в вигляді білої твердої речовини. Вихід: 43,3 %. + MS: [M+H] = 337,13 3-(3-хлорфенілетиніл)-8-(трет-бутоксикарбоніл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен (Сполука 22b) Титульну сполуку синтезували згідно зі способом, вказаним для сполуки з прикладу 3, замінюючи 2-бром-6-метилпіридин 1-хлор-3-йодбензолом та сполуку 3c сполукою 22a. Після звичайної обробки неочищений матеріал очистили автоматизованою флеш-хроматографією ® (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 95:5 до 6:4), забезпечуючи титульний продукт в вигляді білої твердої речовини. Вихід: 76,9 %. + MS: [M+H] = 375,14 3-(3-хлорфенілетиніл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен (Сполука 22c) Титульну сполуку синтезували згідно зі способом, вказаним для сполуки 1c, замінюючи сполуку 1b сполукою 22c. Неочищений залишок застосовували без додаткової очистки в наступній реакції. Вихід: 90,4 %. + MS: [M+H] = 275,12 3-(3-хлорфенілетиніл)-8-(3-ціано-2-піразиніл)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульну сполуку отримували згідно зі способом, описаним для сполуки з прикладу 1, замінюючи сполуку 1c сполукою 22d та 2-хлор-6-метил-3-нітропіридин 2-хлор-3-ціанопіразином. Коричневате в'язке масло. Вихід: 83,3 %. + MS: [M+H] = 378,14 1 H-ЯМР: (CDCl3, δ): 1,90-2,00 (m, 2H), 2,10-2,15 (m, 2H), 2,99 (s, 2H), 3,65-3,78 (m, 2H), 4,204,27 (m, 2H), 7,29-7,35 (m, 1H), 7,39-7,45 (m, 2H), 7,54 (s, 1H), 8,05 (s, 1H), 8,28 (s, 1H). Приклад 23 3-(2-метилфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульну сполуку отримали згідно з процедурою, вказаною для сполуки з прикладу 3, замінюючи 2-бром-6-метилпіридин 2-бромтолуолом. Після звичайної обробки неочищений ® матеріал очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 95:5 до 8:2), забезпечуючи титульний продукт в вигляді жовтої твердої речовини. Вихід: 29,6 %. + MS: [M+H] = 391,09 1 H-ЯМР: (CDCl3, δ): 1,90-2,11 (m, 4H), 2,46-2,50 (2s, 6H), 3,01 (s, 2H), 3,50-3,70 (m, 4H), 6,63 (d J=8 Гц, 1H), 7,18-7,34 (m, 3H), 7,48-7,52 (m, 1H), 8,11 (d, J=8 Гц, 1H). Приклад 24 3-(2-хлорфенілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульний продукт отримали за процедурою, вказаною вище для сполуки з прикладу 3, за допомогою 1-хлор-2-йодбензолу замість 2-бром-6-метилпіридину. Після звичайної обробки, ® неочищений матеріал очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 95:5 до 7:3), забезпечуючи титульний продукт в вигляді жовтого масла. Вихід: 57,2 %. + MS: [M+H] = 410,97 1 H-ЯМР: (CDCl3, δ): 1,90-2,11 (m, 4H), 2,49 (s, 3H), 3,03 (s, 2H), 3,50-3,70 (m, 4H), 6,63 (d J=8 Гц, 1H), 7,26-7,38 (m, 2H), 7,44-7,48 (m, 1H), 7,56-7,60 (m, 1H), 8,11 (d, J=8 Гц, 1H). Приклад 25 3-(2-піразинілетиніл)-8-(6-метил-3-нітро-2-піридил)-1-окса-2,8-діазаспіро[4.5]дец-2-ен Титульну сполуку отримували згідно з процедурою, вказаною для сполуки з прикладу 3, але замінюючи 2-бром-6-метилпіридин 2-йодпіразином. Після звичайної обробки неочищений ® матеріал очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 8:2 до 3:7), забезпечуючи титульний продукт в вигляді жовтої твердої речовини. Вихід: 28,1 %. + MS: [M+H] = 379, 22 1 H-ЯМР: (CDCl3, δ): 1,93-2,11 (m, 4H), 2,51 (s, 3H),3,03 (s, 2H), 3,51-3,71 (m, 4H), 6,64 (d J=8 Гц, 1H), 8,12 (d, J=8 Гц, 1H), 8,60 (dd, J=16 Гц, 4Гц, 2H), 8,80 (s, 1H). Приклад 26 3-фенілетиніл-8-(6-метил-3-нітро-2-піридил)-1-окса-8-азаспіро[4.5]дец-3-ен 3-гідроксі-3-фенілетиніл-8-етоксикарбоніл-1-окса-8-азаспіро[4.5]декан (сполука 26a) До розчину 82 мг (0,362 ммоль) етил 3-оксо-1-окса-8-азаспіро[4.5]декан-8-карбоксилату [Edwin S. C. Wu et al., J. Med. Chem., 1995, 38 (9), pp 1558-1570] в THF (4 мл) додали по краплях 24 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 1M розчин фенілетинілмагнію броміду в THF (0,724 мл, 0,724 ммоль), перемішували при к.т. в безводній атмосфері азоту. Реакційну суміш перемішували при к.т. протягом 4 годин, потім при 60 °C протягом 6 годин, потім її погасили насиченим водним розчином амонію хлориду, екстрагували EtOAc. Об'єднані органічні шари промили розсолом, висушили над натрію сульфатом та випарювали насухо in vacuo. Неочищений матеріал очистили автоматизованою ® флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 75:25 до 4:6), забезпечуючи титульний продукт в вигляді жовтої твердої речовини. Вихід: 87,2 %. + MS: [M+H] = 330,33 3-фенілетиніл-8-етоксикарбоніл-1-окса-8-азаспіро[4.5]дец-3-ен (сполука 26b) До розчину сполуки 26a (93 мг, 0,282 ммоль), перемішаної в піридині (4 мл), при 0 °C додали тіонілхлорид (0,103 мл, 1,141 ммоль) та реакційну суміш перемішували при від 0 °C до к.т. протягом 2 годин. Потім її вилили в воду, підкислили 1M HCl та екстрагували хлороформом. Органічні шари об'єднали, промили розсолом, висушили над натрію сульфатом та випарювали насухо для забезпечення неочищеного матеріала, який очистили автоматизованою флеш® хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 92:8 до 75:25) для отримання 18 мг титульної сполуки. + MS: [M+H] = 312,34 3-фенілетиніл-1-окса-8-азаспіро[4.5]дец-3-ен (сполука 26c) Суміш сполуки 26b (25 мг, 0,803 ммоль), KOH (80 мг, 1,43 ммоль), води (2 мл) та MeOH (4 мл) перемішували при кипінні протягом 2 годин. Потім її екстрагували EtOAc. Органічний шар промили розсолом, висушили над натрію сульфатом та випарювали насухо in vacuo. Неочищений залишок (19,2 мг) застососвували без будь-якого типу очистки на наступному етапі. + MS: [M+H] = 240,10 3-фенілетиніл-8-(6-метил-3-нітро-2-піридил)-1-окса-8-азаспіро[4.5]дец-3-ен Титульну сполуку отримували згідно зі способом, описаним для сполуки з прикладу 1, замінюючи сполуку 1c сполукою 26c. Неочищений матеріал очистили автоматизованою флеш® хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 98:2 до 9:1) для отримання 8 мг титульної сполуки. Вихід: 51 % + MS: [M+H] = 376,14 1 H-ЯМР: (CDCl3, δ): 1,75-1,87 (m, 2H), 1,87-1,98 (m, 2H), 2,48 (s, 3H), 3,49 (ddd, J=13,39, 10,70, 3,06 Гц, 2H), 3,68 (dt, J=13,45, 4,16 Гц, 2H), 4,76 (d, J=2,20 Гц, 2H), 6,13 (t, J=2,20 Гц, 1H), 6,58 (d, J=8,31 Гц, 1H), 7,32-7,40 (m, 3 H), 7,43-7,50 (m, 2H), 8,08 (d, J=8,07 Гц, 1H). Приклад 27 3-(3-хлорфенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.4]нон-2-ен 1-(трет-бутоксикарбоніл)-3-метилene-піролідин (сполука 27a) Титульну сполуку синтезували згідно зі способом, описаним вище для сполуки 2a за допомогою 1-(трет-бутоксикарбоніл)-3-піролідинoну замість 1-(3-нітро-2-піридил)-4оксопіперидину. Після звичайної обробки неочищений продукт очистили автоматизованою ® флеш-хроматографією (Horizon TM – Biotage), елюючи градієнтом петролейний ефір – EtOAc від 95:5 до 7:3, даючи титульну сполуку в вигляді коричневатого масла. Вихід: 75,8 %. + MS: [M+H] = 184,53 3-триметилсілілетиніл-7-(трет-бутоксикарбоніл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен (сполука 27b) Титульну сполуку синтезували згідно зі способом, описаним вище для сполуки 3c за допомогою сполуки 27a замість сполуки 3a. Після звичайної обробки неочищений продукт ® очистили автоматизованою флеш-хроматографією (Horizon TM – Biotage), за допомогою елюювання градієнтом петролейний ефір – EtOAc від 95:5 до 75:25, даючи титульну сполуку. Вихід: 82,9 %. + MS: [M+H] = 323,45 3-(3-хлорфенілетиніл)-7-(трет-бутоксикарбоніл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен (сполука 27c) Титульну сполуку отримали згідно з процедурою, вказаною для сполуки з прикладу 3, за допомогою 1-хлор-3-йодбензолу замість 2-бром-6-метилпіридину. Після звичайної обробки ® неочищений матеріал очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 95:5 до 6:4), забезпечуючи титульний продукт в вигляді жовтого масла. Вихід: 14 %. + MS: [M+H] = 361,13 3-(3-хлорфенілетиніл)-1-окса-2,7-діазаспіро[4.4]нон-2-ен (сполука 27d) Титульну сполуку синтезували згідно зі способом, вказаним для сполуки 1c, але замінюючи 25 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 сполуку 27c на сполуку 1b. Неочищений залишок застосовували без додаткової очистки в наступній реакції. Вихід: + MS: [M+H] = 261,11 3-(3-хлорфенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.4]нон-2-ен Титульну сполуку отримували згідно зі способом, описаним для сполуки прикладу 1, замінюючи сполуку 27d на сполуку 1c. Неочищений матеріал очистили автоматизованою флеш® хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - ацетон від 95:5 до 9:1) для отримання титульної сполуки в вигляді в'язкого жовтого масла. Вихід: 68,5 %. 1 H-ЯМР: (CDCl3, δ): 2,13-2,25 (m, 1H), 2,46 (dd, J=12,84, 6,48 Гц, 1H), 2,52 (s, 3H), 3,17-3,34 (m, 2H), 3,42 (d, J=12,47 Гц, 1H), 3,69 (t, J=9,78 Гц, 1H, ) 3,82 (d, J=12,47 Гц, 1H), 3,98 (td, J=10,94, 6,97 Гц, 1H), 6,61 (d, J=8,07 Гц, 1H), 7,30-7,36 (m, 1H, ) 7,37-7,45 (m, 2H), 7,53 (s, 1H), 8,07 (d, J=8,31 Гц, 1H). Приклад 28 3-(3-хлорфенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.3]окт-2-ен 1-(трет-бутоксикарбоніл)-3-метилeназетидин (сполука 28a) До суспензії метилтрифенілфосфонію броміду (1,56 г, 4,37 ммоль) в 30 мл Et2O, перемішаної при 0 °C, додали калію трет-бутилaт (0,459 г, 4,09 ммоль). Після 0,5 години холодну баню видалили та суміш перемішували протягом 1 години при к.т. Потім її охолоджували в водно-льодовій бані та 1-(трет-бутоксикарбоніл)-3-азетидинон (500 мг, 2,92 ммоль) додали. Холодну баню видалили. Після того, як її залишили на ніч, реакційну суміш погасили насиченим розчином NH4Cl в воді, екстрагували Et2O, висушили над Na2SO4, випарювали насухо in vacuo розчинник. Залишковий неочищений матеріал очистили ® автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір ацетон від 10:0 до 7:3) для отримання титульної сполуки (426 мг) в вигляді в'язкого безкольорового масла. Вихід: 86,2 %. + MS: [M+H] = 170,45 3-триметилсілілетиніл-7-(трет-бутоксикарбоніл)-1-окса-2,7-діазаспіро[4.3]окт-2-ен (сполука 28b) Титульну сполуку синтезували згідно зі способом, описаним вище для сполуки 3c, за допомогою сполуки 28a замість сполуки 3a. Після звичайної обробки неочищений продукт ® очистили автоматизованою флеш-хроматографією (Horizon TM – Biotage) за допомогою елюювання градієнтом петролейний ефір – EtOAc від 95:5 до 6:4, отримуюючи титульну сполуку. Вихід: 62 %. + MS: [M+H] = 309,16 3-(3-хлорфенілетиніл)-7-(трет-бутоксикарбоніл)-1-окса-2,7-діазаспіро[4.3]окт-2-ен (сполука 28c) Титульну сполуку отримали згідно з процедурою, вказаною для сполуки прикладу 3, за допомогою 1-хлор-3-йодбензолу замість 2-бром-6-метилпіридину. Після звичайної обробки ® неочищений матеріал очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір - EtOAc від 8:2 до 65:35), забезпечуючи титульний продукт в вигляді жовтого масла. Вихід: 24,3 %. + MS: [M+H] = 347,09 3-(3-хлорфенілетиніл)-1-окса-2,7-діазаспіро[4.3]окт-2-ен (сполука 28d) Титульну сполуку синтезували згідно зі способом, вказаним для сполуки 1c, але замінюючи сполуку 1b сполукою 28c. Неочищений залишок застосовували без додаткової очистки на наступному етапі реакції. + MS: [M+H] = 247,13 3-(3-хлорфенілетиніл)-7-(6-метил-3-нітро-2-піридил)-1-окса-2,7-діазаспіро[4.3]окт-2-ен Титульну сполуку отримували згідно зі способом, описаним для сполуки прикладу 1, але замінюючи сполуку 1c сполукою 28d. Неочищений матеріал очистили автоматизованою флеш® хроматографією (SP1 TM – Biotage; петролейний ефір – дихлорметан 1:9) для отримання титульної сполуки в вигляді в'язкого жовтого масла. Вихід: 68,5 % + MS: [M+H] = 383,08 1 H-ЯМР: (CDCl3, δ): 2,51 (s, 3H), 3,49 (s, 2H), 4,38 (d, J=10,76 Гц, 2H), 4,49 (d, J=11,00 Гц, 2H), 6,65 (d, J=8,31 Гц, 1H), 7,33 (t, J=8,10 Гц, 1H), 7,42 (t, J=8,07 Гц, 2H),7,54 (s, 1H), 8,17 (d, J=8,31 Гц, 1H). Приклад 29 та 30 4-фенілетиніл-9-(6-метил-3-нітро-2-піридил)-1-окса-9-азаспіро[5.5]ундец-4-ен та 4фенілетиніл-9-(6-метил-3-нітро-2-піридил)-1-окса-9-азаспіро[5.5]ундец-3-ен 26 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 4-метилeн-9-(трет-бутоксикарбоніл)-1-окса-9-азаспіро[5.5]ундекан (сполука 29a) До розчину 1-Boc-піперидону (2,39 г, 12 ммоль) та етокситриметилсилану (3,75 мл, 24 ммоль) в 80 мл CCl4 при перемішуванні при 0 °C додали триметилсіліл трифторметилсульфонат (217 мкл, 1,2 ммоль) та триметил-(2-метилeн-4триметилсілілoксибутил)-силан (E. I. Marko et al., Journal of Organic Chemistry, 1992, 57, 22112213), розчинені в 23 мл CCl4. Після перемішування при 0-5 °C протягом 6 годин та залишаючи протягом ночі при 0 °C, реакційну суміш промили водою, висушили над Na2SO4, відфільтрували та розчинник випарювали насухо in vacuo. Останні 6,5 г безкольорового масла очистили ® автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір – EtOAc від 99:1 до 85:15) для отримання 3,2 г титульної сполуки в вигляді безкольорового масла. Вихід: 100 %. + MS: [M+H] = 268,62 4-оксо-9-(трет-бутоксикарбоніл)-1-окса-9-азаспіро[5.5]ундекан (сполука 29b) До розчину сполуки 29a (1,6 г, 5,99 ммоль) в суміші діоксан–вода (32,9 мл та 11 мл, відповідно) при перемішуванні при к.т. додали 4 % розчиненого осмію тетроксиду в воді (0,762 мкл, 0,125 ммоль). Після 2 годин додали порційно розмелений натрію метаперіодат (2,56 г, 12 ммоль), забезпечуючи суспензію, яка прагне стати вітло-сірою з коричневатої. Через 4 години H2O додали, екстрагуючи EtOAc, промиваючи H2O, висушуючи над Na2SO4, випарюючи розчинник насухо. Залишкову темно-жовту напівтверду речовину очистили автоматизованою ® флеш-хроматографією (SP1 TM – Biotage; петролейний ефір – EtOAc 7:3) для отримання 0,96 г титульної сполуки в вигляді сірої твердої речовини. Вихід: 59,5 % + MS: [M+H] = 270,33 4-гідроксі-4-фенілетиніл-9-(трет-бутоксикарбоніл)-1-окса-9-азаспіро[5.5]ундекан (сполука 29c) Титульну сполуку отримали згідно зі способом, вказаним вище для сполуки 26a, замінюючи етил 3-оксо-1-окса-8-азаспіро[4.5]декан-8-карбоксилат сполукою 29b. Після звичайної обробки ® маслянистий залишок очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір – EtOAc від 9:1 до 6:4) для отримання 0,96 г титульної сполуки в вигляді сірої твердої речовини. Вихід: 57,3 % + MS: [M+H] = 372,14 4-фенілетиніл-1-окса-9-азаспіро[5.5]ундец-3-ен та 4-фенілетиніл-1-окса-9азаспіро[5.5]ундец-4-ен (сполуки 29d) Титульні сполуки отримали згідно зі способом, вказаним в даному документі для сполуки 26c, замінюючи сполуку 26b сполукою 29c. Після звичайної обробки масло, що залишилось, ® очистили автоматизованою флеш-хроматографією (SP1 TM – Biotage; градієнт петролейний ефір – EtOAc від 9:1 до 8:2) для отримання 0,49 г (33,6 %) титульних сполук в вигляді коричневатого масла, яке застосовують на наступному етапі без розділення. + MS: [M+H] = 254,17 4-фенілетиніл-9-(6-метил-3-нітро-2-піридил)-1-окса-9-азаспіро[5.5]ундец-4-ен та 4фенілетиніл-9-(6-метил-3-нітро-2-піридил)-1-окса-9-азаспіро[5.5]ундец-3-ен Титульні сполуки отримали згідно зі способом, описаним для сполуки прикладу 1, замінюючи сполуку 1c сполуками 29d. Неочищений матеріал очистили автоматизованою флеш® хроматографією (SP1 TM – Biotage; градієнт петролейний ефір – CH2Cl2 від 4:6 до 3:7) для отримання 5 мг сполуки прикладу 29 та 1 мг сполуки прикладу 30. Приклад 29 + MS: [M+H] = 390,29 1 H-ЯМР: (CDCl3, δ): 1,73-1,90 (m, 4H), 2,32-2,39 (m, 2H), 2,47 (s, 3H), 3,38-3,50 (m, 2H), 3,603,72 (m, 2H), 3,87 (t, J=5,38 Гц, 2H), 6,07 (s, 1H), 6,57 (d, J=8,31 Гц, 1H), 7,30-7,37 (m, 3H), 7,427,50 (m, 2H), 8,08 (d, J=8,07 Гц, 1H). Приклад 30 + MS: [M+H] = 390,16 1 H-ЯМР: (CDCl3, δ): 1,69-1,79 (m, 2H), 1,95 (d, J=13,20 Гц, 2H), 2,26 (d, J=1,96 Гц, 2H), 2,48 (s, 3H), 3,36-3,50 (m, 2H), 3,58-3,70 (m, 2H), 4,30 (d, J=2,69 Гц, 2H), 6,20 (br, s, 1H), 6,58 (d, J=8,31 Гц, 1H), 7,31-7,41 (m, 3H), 7,45 (dd, J=6,60, 2,93 Гц, 2H), 8,08 (d, J=8,31 Гц, 1H). Приклад 31 3-(3-хлорфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен 8-метилeн-1,4-діоксаспіро[4.5]декан (сполука 31a) Титульну сполуку отримали згідно зі способом, вказаним вище для сполуки 2a, за допомогою літій-біс-триметилсіліламіду замість бутиллітію та проведення реакції при -20 °C. В якості початкового матеріалу 1,4-диоксаспіро[4.5]декан-8-он замінили 1-(3-нітро-2-піридил)-4 27 UA 110343 C2 5 10 15 20 25 30 35 40 45 50 55 60 oксoпіперидином. Після звичайної обробки залишок очистили автоматизованою флеш® хроматографією (Horizon TM – Biotage; петролейний ефір – EtOAc 95:5) для отримання титульної сполуки в якості рідкого безкольорового масла. Вихід: 99,3 %. + MS: [M+H] = 155,13 3-триметилсілілетиніл-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен (сполука 31b) Титульну сполуку синтезували за допомогою способу, вказаного в даному документі для сполуки 3c, за допомогою сполуки 31a замість сполуки 3a. Після звичайної обробки залишок ® очистили автоматизованою флеш-хроматографією (Horizon TM – Biotage; градієнт петролейний ефір – EtOAc від 98:2 до 9:1) для отримання титульної сполуки. 3-(3-хлорфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен Титульну сполуку отримали згідно зі способом, вказаним вище для сполуки прикладу 3, але замінюючи 2-бром-6-метилпіридин 1-хлор-3-йодбензолом. Після звичайної обробки залишок ® очистили автоматизованою флеш-хроматографією (Horizon TM – Biotage; петролейний ефір – EtOAc 85:15) для отримання титульної сполуки в вигляді сірої твердої речовини. Вихід: 80,1 %. Альтернативна процедура 1-хлор-3-(3,3-діетоксипроп-1-ініл)-бензол (сполука 31c) Суміш 1-хлор-3-йодбензолу (4 г, 16,8 ммоль), пропаргілальдегіддіетилацеталю (2,66 мл, 18,5 ммоль), біс(трифенілфосфін)паладію(II) дихлориду (295 мг, 0,42 ммоль), міді йодиду (160 мг, 0,84 ммоль) та триетиламіну (60 мл) перемішували при к.т. протягом 3 годин. Через 4 години реакційну суміш погасили H2O та екстрагували EtOAc. Екстракти промили розсолом, висушили над Na2SO4, та випарювали насухо in vacuo. Залишок очистили автоматизованою флеш® хроматографією (Horizon TM – Biotage; петролейний ефір – EtOAc 97:3) для отримання 4 г титульної сполуки в вигляді рідкого жовтуватого масла. Вихід: 100 %. + MS: [M+H] = 239,32 3-(3-хлорфеніл)-проп-2-іналь (сполука 31d) 38,8 мл води та 7,7 мл трифтороцтової кислоти додали до розчину сполуки 31c (4 г, 16,7 ммоль) в CH2Cl2. Через 4 години при перемішуванні, додаткові 4 екв. трифтороцтової кислоти додали. Через 24 години перетворення закінчилось, 2 шари розділили, органічний шар промили водою, висушили над Na2SO4 та випарювали насухо in vacuo для забезпечення титульної сполуки в вигляді жовто-коричневатого масла, яке застосовували на наступному етапі без додаткової очистки. + MS: [M+H] = 165,35 3-(3-хлорфеніл)-проп-2-іналю оксим (сполука 31e) Титульну сполуку отримали згідно зі способом, описаним вище для сполуки 1a, за допомогою сполуки 31d замість фенілпропаргілальдегіду. Світлий коричневий залишок застосовували на наступному етапі без додаткової очистки. Вихід: 96,4 %. + MS: [M+H] = 180,16 3-(3-хлорфеніл)-N-гідроксипроп-2-інімідоїлхлорид (сполука 31f) Титульну сполуку отримали згідно зі способом, описаним в даному документі для сполуки 3b, за допомогою сполуки 31e замість 3-триметилсілілпроп-2-іналю оксиму. Світлий коричневий залишок застосовували на наступному етапі без додаткової очистки. Вихід: 96,4 %. 3-(3-хлорфенілетиніл)-1,9,12-триокса-2-азадиспіро[4.2.4.2]тетрадец-2-ен Титульну сполуку отримали згідно з процедурою, описаною для сполуки 3c, за допомогою сполуки 31f замість сполуки 3b та сполуки 31a замість сполуки 3a. Після звичайної обробки ® залишок очистили автоматизованою флеш-хроматографією (Horizon TM – Biotage; градієнт петролейний ефір – ацетон від 95:5 до 9:1) для отримання титульної сполуки в вигляді сірої твердої речовини. Вихід: 64,8 % + MS: [M+H] = 332,14 1 H-ЯМР: (CDCl3, δ): 1,63-1,74 (m, 2H), 1,88 (dd, J=13,94, 2,45 Гц, 2H),1,96-2,10 (m, 4H), 2,92 (s, 2H), 3,92-4,05 (m, 4H), 7,32 (d, J=7,58 Гц, 1H), 7,35-7,44 (m, 2H), 7,52 (s, 1H). Приклад 32 3-(3-хлорфенілетиніл)-8-оксо-1-окса-2-азаспіро[4.5]дец-2-ен Розчин сполуки прикладу 31 (0,76 г, 2,3 ммоль) в 5 мл трифтороцтової кислоти розвели водою (0,21 мл) та перемішували при 0-4 °C протягом 4 годин, підлужували 3н NaOH, екстрагували EtOAc, промили водою, висушили над Na2SO4 та випарювали насухо in vacuo для забезпечення титульної сполуки в вигляді жовто-коричневатого масла. Залишок очистили ® автоматизованою флеш-хроматографією (Horizon TM – Biotage; петролейний ефір – EtOAc 8:2) для отримання титульної сполуки в вигляді сірої твердої речовини. Вихід: 53,8 % + MS: [M+H] = 288,14 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNovel spiroheterocyclic compounds as mglu5 antagonists
Автори англійськоюLeonardi, Amedeo, Motta, Gianni, Riva, Carlo, Guarneri, Luciano, Graziani, Davide, de Toma, Carlo, Karamfilova, Katia Dimitrova
Автори російськоюЛеонарди Амедео, Мотта Джианни, Рива Карло, Гуарнери Лучиано, Гразиани Давиде, дэ Тома Карло, Карамфилова Катя Димитрова
МПК / Мітки
МПК: A61P 13/02, C07D 491/10, A61K 31/438, C07D 498/10
Мітки: сполуки, антагоністи, спірогетероциклічні, mglu5
Код посилання
<a href="https://ua.patents.su/64-110343-spirogeterociklichni-spoluki-yak-antagonisti-mglu5.html" target="_blank" rel="follow" title="База патентів України">Спірогетероциклічні сполуки як антагоністи mglu5</a>
Попередній патент: Ксантанова камедь з високою швидкістю гідратування та високою в’язкістю
Наступний патент: Підгузок одноразового використання
Випадковий патент: Спосіб корекції системних порушень метаболізму оксиду азоту у хворих на бронхіальну астму












