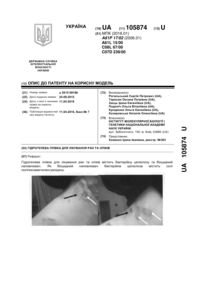
Гідрогелева плівка для лікування ран та опіків
Номер патенту: 105874
Опубліковано: 11.04.2016
Автори: Подоліч Ольга Віталіївна, Кухаренко Ольга Євгенівна, Рогальський Сергій Петрович, Заєць Ірина Євгеніївна, Тарасюк Оксана Петрівна, Козировська Наталія Олексіївна
Формула / Реферат
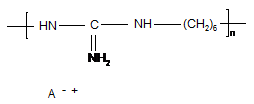
Гідрогелева плівка для лікування ран та опіків, що містить бактерійну целюлозу та біоцидний наповнювач, яка відрізняється тим, що як біоцидний наповнювач бактерійна целюлоза містить солі полігексаметиленгуанідину загальної формули
 ,
,
де А - залишок кислоти, що вибраний з групи, що складається з соляної, фосфорної, вугільної, оцтової, лимонної, сорбінової та глюконової кислот.
Текст
Реферат: Гідрогелева плівка для лікування ран та опіків містить бактерійну целюлозу та біоцидний наповнювач. Як біоцидний наповнювач бактерійна целюлоза містить солі полігексаметиленгуанідину. UA 105874 U (12) UA 105874 U UA 105874 U 5 10 15 20 25 30 35 40 45 50 55 Корисна модель належить до загальної органічної хімії та мікробіології і стосується гідрогелевої плівки для лікування ран та опіків, що містить бактерійну целюлозу та біоцидний наповнювач, і може бути використана як перев'язувальний матеріал в медицині. Бактерійна целюлоза (БЦ) є натуральним гідрогелем, синтезованим бактеріями роду Komagataeibacter (у минулому Gluconacetobacter) [1]. Хоча за хімічною будовою БЦ тотожна до рослинної, вона має ряд унікальних морфологічних і фізико-хімічних властивостей, які зумовлюють перспективність її використання в різноманітних галузях. На відміну від рослинної целюлози, БЦ є хімічно чистою і не містить домішок лігніну і пектину. Структура БЦ має вигляд сітки нерегулярної будови і утворена нанофібрилами, які мають товщину в діапазоні 70-150 нм, що майже у 100 разів менше від товщини волокон рослинної целюлози [2]. Нанофібрилярна структура БЦ зумовлює її високу кристалічність і механічну міцність, велику питому площу поверхні і мікропористу структуру, завдяки чому плівки БЦ мають високу водоутримуючу здатність (до 99 %), а також сорбційну здатність відносно полярних сполук [2-4]. БЦ вважається надзвичайно перспективним матеріалом для застосування у біомедичній галузі (перев'язувальні матеріали і тимчасові замінники шкіри для лікування ран і опіків), оскільки має високу еластичність у вологому стані, хорошу адгезію до поверхні ран і може бути легко насичена різноманітними антибіотиками. Крім того, БЦ є неалергенною і придатна до стерилізації усіма звичайними методами [2, 3, 5, 6]. Слід зазначити, що БЦ не має власної антимікробної активності, яка є необхідною для застосування як перев'язувального матеріалу для запобігання мікробному поширенню на поверхні ран і відповідно ризику виникнення інфекцій. Описано антимікробні композитні плівки на основі БЦ, модифікованої наночастинками срібла, які проявляють високу активність проти грампозитивних і грамнегативних бактерій [7]. Модифікацією БЦ природним полімерним біоцидом хітозаном отримано плівки з бактеріостатичною активністю по відношенню до грампозитивних і грамнегативних бактерій і бактерицидною активністю до грампозитивних тесткультур [8]. Однак, слід зазначити, що такі біоцидні домішки, як наносрібло і хітозан мають високу вартість, а їх введення в БЦ є досить складним з практичної точки зору. Відомі більш дешеві та простіші у виготовленні антимікробні плівки БЦ, насичені катіон-активним біоцидом бензалконій хлоридом [9]. Однак такий матеріал проявляє високу активність лише проти грампозитивних бактерій, залишаючись недостатньо стійким до дії грамнегативних (Escherichia coli), які спричинюють інфекційні захворювання [9]. Таким чином, важливими проблемами застосування БЦ як перев'язувального матеріалу в медицині є висока вартість біоцидів, які застосовуються для надання антимікробних властивостей, складність їх введення в плівки целюлози, а також недостатньо широкий спектр антимікробної активності таких матеріалів. Відомий засіб для догляду за шкірою, що містить гліцерин, емульгатор, масляний екстракт лікарської рослини, водно-спирто-гліцеринового екстракту шипшини, солянокислого полігексаметиленгуанідину, поліетиленгліколю та інших компонентів (Патент РФ № 2106859, 6 МПК : А61K7/48, А61K7/40, "опублікований: 20.03.1998 р.) [10]. Відомий спосіб стерилізації медичних приладів шляхом антисептичної обробки їх поверхні розчином ПГМГ-гідрохлориду (Патент України № 70215, МПК (2006): A61L2/16, опубліковано: 15.09.2004, бюл. № 9) [11]. Відомий гель гігієнічний для догляду за шкірою, який включає солі ПГМГ в поєднанні з четвертинними амонієвими солями, поліетиленгліколем і вітамінної складової (Патент РФ № 7 2225202, МПК : А61K31/395, А61K7/48, опублікований: 10.03.2004 р.) [12]. Однак у вищезазначених засобах солі ПГМГ застосовуються в рідкій, гелевій формі, що є незручним для лікування ран та опіків. В основу корисної моделі поставлено задачу створити гідрогелеву плівку для лікування ран та опіків, яка б містила бактерійну целюлозу та біоцидний наповнювач, яку б легко можна було вводити в плівки целюлози простими і економічними методами, та яка буде мати широкий спектр антимікробної дії, тобто, створити нову форму застосування ПГМГ у вигляді лікувальної плівки для лікування ран та опіків. Поставлена задача вирішується пропонованою гідрогелевою плівкою для лікування ран та опіків, що містить бактерійну целюлозу та біоцидний наповнювач, згідно з корисною моделлю, як біоцидний наповнювач вона містить солі полігексаметиленгуанідину загальної формули 1 UA 105874 U C HN NH (CH2)6 n NH2 A - + 5 10 15 20 25 30 35 40 , де А - залишок кислоти, що вибраний з групи, що складається з соляної, фосфорної, вугільної, оцтової, лимонної, сорбінової та глюконової кислот. Наведені вище солі ПГМГ є катіонактивними поліелектролітами, які давно застосовують як основи для біоцидних композицій, ефективних проти багатьох патогенних мікроорганізмів. Перевагами таких полімерних біоцидів є поєднання низької токсичності, біодеструктивності і широкого спектра антимікробної активності проти грампозитивних і грамнегативних бактерій, грибів, вірусів, водоростей [11]. В запропонованій корисній моделі встановлено, що гідрогелеві плівки БЦ можуть бути легко насичені солями ПГМГ з їх водних розчинів, які містять 0,1-1 % відповідної солі ПГМГ. Композитні плівки БЦ-ПГМГ проявляють високу антимікробну активність по відношенню до грампозитивних і грамнегативних бактерій, дріжджів і біоплівок. Суть пропонованої корисної моделі пояснюється графічним матеріалом, де представлено застосування заявлених гідрогелевих плівок (білі стрілки) для лікування ранових поверхонь після видалення кератом у пацієнтки у клініці у порівнянні з вазеліновими серветками (чорна стрілка), що традиційно застосовуються у клініці. Відомості, що підтверджують можливість реалізації корисної моделі. 1. Отримання бактерійної целюлози Культуру Komagataeibacter intermedius IMBG291 вирощували в рідкому середовищі HS (Hestrin-Schramm Medium) [13] при температурі 29 °C продовж 2 діб. Для забезпечення її високої активності було здійснено два пасажі без зміни умов та часу культивування. Прискорення синтезу целюлози бактеріями K. intermedius здійснювалось за рахунок вирощування спільно з культурою дріжджів Zygosaccharomyces bailii IMBG292. Для забезпечення сприятливих умов формування плівки внаслідок розвитку штучної асоціації K. intermedius та Ζ bailii використовували дводобові культури. Умови культивування та склад середовища при цьому залишалися сталими. З метою отримання швидкого розвитку Ζ bailii, їх попередньо вирощували на твердому середовищі YPD (Yeast Extract Peptone Dextrose Medium): 10 r дріжджового екстракту, 20 г пептону, 20 г мікробіологічного агару на 1 л дистильованої води. Час культивування складав 2 доби при температурі 29 °C. Наступний пасаж здійснювався на рідке середовище HS з метою адаптації дріжджової культури до росту за умов пониженого показника рН. Загалом асоціація K. intermedius та Ζ bailii вирощувалася 7 діб. Після чого отримана плівка бактерійної целюлози оцінювалася з точки зору якісних показників. Таких як: товщина, міцність та однорідність по всій площі поверхні, відсутність прогалин та недоліків. За результатами візуального огляду отримана целюлозна плівка відповідала пред'явленим критеріям якості при товщині 4 мм. Очищення плівки від клітин, контроль Після 7-діб культивування, плівки БЦ, сформовані K. intermedius, було вилучено з культуральної рідини та промито стерильною дистильованою водою, щоб видалити компоненти середовища. Відповідно до [14] було виконано двоетапну очистку плівок. Спочатку плівки БЦ прогрівали при температурі 100±5 °C у 2,0 % розчині додецилсульфату натрію протягом 3 год., промивали дистильованою водою, а потім прогрівали при температурі 100±5 °C у 4,0 % розчині NaOH протягом 1,5 год., щоб видалити інкорпоровані клітини мікроорганізмів та їх залишки. 2. Синтез полімерного біоциду ПГМГ гідрохлориду 45 140 - 200 oC H2N Cl - + C NH2 + H2N (CH2)6 NH2 HN - NH3 C NH (CH2)6 n NH2 NH2 Cl - + ПГМГ гідрохлорид Суміш гуанідину гідрохлориду (20 г, 0,208 моль) і гексаметилендіаміну (24,1 г, 0,208 моль) помішували в круглодонну колбу ємністю 250 мл, оснащену магнітною мішалкою. Реакційну 2 UA 105874 U 5 10 15 20 суміш нагрівали до 100 °C і перемішували протягом 4 годин, після чого температуру реакції поступово підвищували і проводили реакцію 4 години при 130-140 °C, 4 години при 180 °C і 3 години при 200 °C до утворення в'язкого розплаву. Після охолодження суміші до кімнатної температури отримували склоподібний аморфний полімер, який розчиняли в 200 мл води і осаджували додаванням 100 мл насиченого водного розчину хлориду натрію. Пастоподібний осад відділяли декантацією і сушили при 140 °C протягом 24 годин, після чого подрібнювали отриманий крихкий продукт у фарфоровій ступці. Характеристична в'язкість синтезованого полімеру ПГМГ-С1, визначена в 0,1 н розчині NaCl при 25 °C, становить 0,09 дл/г. 1 Н ЯМР (300 мГц, ДМСО-De):δ = 1,32-1,47 (м, 8Н, (СН2)4,), 3.17 (м, 4Н, (NH-СH2), 7,1-8,1 (м, + 4Н, C-NH-C, C=NH2 ). -1 -1 -1 -1 ІЧ (KВr): 3280 см (ν ΝΗ), 3150 см (δ ΝΗ), 2924 см (asCH2), 2853 см (SCH2), 1528-1697 -1 см (ν C=N). Знайдено, %: С 47,1, Η 8,7, Ν 24,1, Сl 20,0 (C7H16N3Cl)x(177,5)x Обчислено, %: С 47,4, Η 9,1, Ν 23,8, Сl 19,8. 3. Отримання гідрогелевих плівок Очищені гідрогелеві плівки БЦ уміщували у водні розчини полімерного біоциду ПГМГ гідрохлориду з концентрацією 1,0 % на 24 і 72 години, після чого промивали дистильованою водою, видаляли надлишкову вологу за допомогою фільтрувального паперу і вирізали диски діаметром 10 мм, які використовували для дослідження антимікробної активності. Для встановлення вмісту ПГМГ гідрохлориду в плівках БЦ їх сушили при 100-130 °C до постійної ваги, після чого встановлювали елементним аналізом вміст хлору. Таблиця 1 Дані елементного аналізу зразків бактерійної целюлози (БЦ) після витримки в розчинах полігексаметиленгуанідину (ПГМГ) гідрохлориду протягом 72 годин Зразок 30 35 Сl, % БЦ-1 БЦ-2 БЦ-3 25 Розчин ПГМГ гідрохлориду, % 0,1 0,5 1,0 2,17 6,81 10,21 Вміст ПГМГ гідрохлориду в сухій плівці БЦ, % 10,9 34,1 51,1 Дані таблиці 1 вказують на високе насичення гідрогелевих плівок БЦ полімерним біоцидом ПГМГ гідрохлоридом із його розведених водних розчинів. 4. Антимікробні властивості гідрогелевих плівок Антимікробні властивості оцінювали шляхом кількісного визначення мінімальної інгібуючої концентрації біоциду. Плівки, наповнені різними концентраціями ПГМГ-Сl були здатні пригнічувати ріст всіх тестованих мікроорганізмів (таблиця 2). Чутливість до плівки варіювала у бактерій і дріжджів, як це було видно на діаметрами пригнічення росту тест-культур на агаровому середовищі і залежала від концентрації ПГМГ-Сl у плівці. Зокрема, плівка, просякнута ПГМГ-Сl (1,0 % розчин) інгібує ріст бактерій, що видно за розміром зон 18,0-22,0 мм, на відміну від нативної плівки, що не пригнічувала ріст мікроорганізмів. Стабільна антимікробну активність спостерігалася протягом не менше 12 місяців протягом зберігання БЦ/ПГМГ-Сl у вологому стані. 3 UA 105874 U Таблиця 2 Розмір зон просвітлення навколо композиту бактерійної целюлози і ПГМГ-Сl на тлі тест-культур, мм Концентрація полігексаметиленгуанідину гірохлориду у плівці бактерійної целюлози, % 1,0 0,5 0,1 Бактерії Xantomonas campestris 22,0 16,0 15,0 Komagate ibacter xylinus 20,0 16,0 14,0 Bacillus subtilis 18,0 16,0 14,0 Klebsiella pneumonia 19,0 19,0 14,0 Pseudomonas syrinsae 20,0 20,0 16,0 Staphylococcus aureus 20,0 20,0 15,0 Дріжджі Pichia galeiformis 21,0 21,0 14,0 Dekkera anomala 22,0 22,0 17,0 Zygosaccharomyces bailii 22,0 22,0 14,0 Штами 5 10 15 20 25 30 35 40 5. Тестування заявлених гідрогелевих плівок на ранових поверхнях Тестування проводили на свіжих та інфікованих ранових поверхнях, отриманих після видалення кератом лазером. Після обробки ран перекисом водню, на поверхню накладали заявлені гідрогелеві плівки або комерційну вазелінову серветку (див. рис.). Плівки БЦ/ПГМГ щільно закривали рану і відпадали через 4-5 діб, не залишаючи рубців. Серветки ж трималися на поверхні рани недовго, тому рани потребували додаткової уваги, тобто лікування і витрат. Після епітелізації тканини кірка на ранах, покритих серветками, відпадала через 6-7 діб, тобто пізніше на 1-2 доби від ран, покритих гідрогелевими плівками. Перелік посилань 1. Yamanaka S. Watanabe К, Kitamura N, Iguchi Μ, Mitsuhasi S, Nishi Y, Uryu M. The Structure and Mechanical Properties of Sheets Prepared from Bacterial Cellulose. J. Mater. Sci. 1989,24:31413145. 2. Czaja W., Krystynowicz Α., Bielecki S., Brown R.M. Microbial cellulose-the natural power to heal wounds. Biomaterials 2006, 27: 145-151. 3. Klemm D., Schumann D., Udhardt U., Marsch S. Bacterial synthesized cellulose artificial blood vessels for microsurgery. Progr. Polym. Sci. 2001, 26(9): 1561-1603. 4. Ul-Islam M, Khan Т., Park.Т.К. Water holding and release properties of bacterial cellulose obtained by in situ and ex situ modification. Carbohydr. Polym. 2012, 88: 596-603. 5. Fontana J.D., de Souza A.M., Fontana C.K., Torriani I.L., Moreschi J.C., Gallotti B.J., de Souza S.J., Narcisco G.P., Bichara J.A., Farah L.F.X. Acetobacter Cellulose Pellicle as a Temporary Skin Substitute. Appl. Biochem. Biotechnol. 1990, 24/25: 253-263. 6. Jonas R., Farah L.H. Production and applications of microbial cellulose. Polym. Degrad. Stab. 1998,59: 101-106. 7. Maneerung T, Tokura S, Rujiravanit R. Impregnation of silver nanoparticles into bacterial cellulose for antimicrobial wound dressing. Carbohydr. Polym. 2008, 72: 43-51. 8. Ciechanska, D. Multifunctional bacterial cellulose/chitosan composite materials for medical applications. Fibres&Textiles in Eastern Europe 2004, 12(4), 69-72, 9. Kim J., Cai Z., Lee H.S., Choi G.S., Lee D.H., Jo С Preparation and characterization of a bacterial cellulose/chitosan composite for potential biomedical application·. J. Polym. Res. 2011, 18(4): 739-744. 10. Сенявина Н.К.; Тарасов А.В.; Черных И.Н.; Петухов В.А.; Секретев А.Г.; Кожевников Б.Е.; Гордиевский А.А.; Бабаев В.В.; Давыдова В.Н.; Ли С.К.; Сорокин Н.И. Средство для ухода за кожей. RU 2106859 (1998). 11. Морозова Н. С, Куцевляк С. В. Спосіб стерилізації медичних приладів. UA 70215 (2004). 12. Бородкина Т. В., Бежанишвили А. Е., Панченко С. С. Гель гигиенический. RU 2225202 (2004). 13. Hestrin S., Schramm M. Synthesis of cellulose by Acetobacter xylinum. Preparation of freezedried cells capable of polymerizing glucose to cellulose. Biochem. J., 1954, 58(2): 345-352. 4 UA 105874 U 14. Sakairi N., Asano H., Ogawa M., Nishi N. and Tokura S. A method for direct harvest of bacterial cellulose filaments during continuous cultivation of Acetobacter xylinum//Carbohydrate Polymers 35 (1998) 233-237. 5 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 10 Гідрогелева плівка для лікування ран та опіків, що містить бактерійну целюлозу та біоцидний наповнювач, яка відрізняється тим, що як біоцидний наповнювач бактерійна целюлоза містить солі полігексаметиленгуанідину загальної формули C HN NH (CH2)6 n NH2 A - + , де А - залишок кислоти, що вибраний з групи, що складається з соляної, фосфорної, вугільної, оцтової, лимонної, сорбінової та глюконової кислот. 15 Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
Назва патенту англійськоюHydrogel film for healing wounds and burns
Автори англійськоюRohalskyi Serhii Petrovych, Tarasiuk Oksana Petrivna, Zaiets Iryna Yevhenivna, Podolich Olha Vitaliivna, Kukharenko Olha Yevhenivna, Kozyrovska Nataliia Oleksiivna
Назва патенту російськоюГидрогелевая пленка для лечения ран и ожогов
Автори російськоюРогальский Сергей Петрович, Тарасюк Оксана Петровна, Заяц Ирина Евгеньевна, Подолич Ольга Витальевна, Кухаренко Ольга Евгеньевна, Козыровская Наталья Алексеевна
МПК / Мітки
МПК: C08L 67/00, A61L 15/00, A61P 17/02, C07D 239/00
Мітки: ран, опіків, плівка, гідрогелева, лікування
Код посилання
<a href="https://ua.patents.su/7-105874-gidrogeleva-plivka-dlya-likuvannya-ran-ta-opikiv.html" target="_blank" rel="follow" title="База патентів України">Гідрогелева плівка для лікування ран та опіків</a>
Попередній патент: Спосіб степлерної гемороїдектомії з деартеризацією гемороїдальних вузлів та мукопексією
Наступний патент: Портативний прилад для електротерапії та стимуляції
Випадковий патент: Таблетка з плівковим покриттям, яка містить екстракт листя червоного винограду