25,27-ди-(5-тіо-октилокси)калікс[4]арен-краун-6
Номер патенту: 107468
Опубліковано: 10.06.2016
Автори: Саяпіна Ольга Ярославівна, Дзядевич Сергій Вікторович, Кальченко Віталій Іванович, Харченко Сергій Григорович, Вишневський Сергій Григорович
Формула / Реферат
25,27-ди-(5-тіо-октилокси)калікс[4]арен-краун-6 формули:
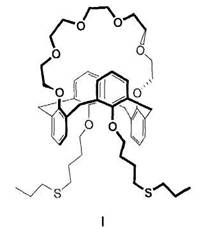 Сполука І.
Сполука І.
Текст
Реферат: 25,27-Ди-(5-тіо-октилокси)калікс[4]арен-краун-6 формули: Сполука І. UA 107468 U (12) UA 107468 U UA 107468 U Корисна модель належить до органічної хімії, а саме до нової сполуки 25,27-ди-(5-тіооктилокси)калікс[4]арен-краун-6 формули І 5 10 15 20 25 30 , яка містить на верхньому вінці макроциклу структурний фрагмент краун-етеру, здатний до селективного комплексоутворення з катіонами лужних металів і амонієвими катіонами, та на нижньому вінці реакційноздатні діалкілсульфідні групи, здатні до хімічного зв'язування з поверхнею атомарного золота. Каліксарен І може знайти застосування при створенні золотих мікрочипів хемо- та біосенсорів, придатних для аналітичного визначення катіонів цезію, біогенних амонієвих катіонів, амінокислот, пептидів, протеїнів. Найближчими структурними аналогами сполуки І, яка заявляється, є 25,27-ди(октилокси)калікс[4]арен-краун-6 формули II [1,2], котрий містить краун-етерний фрагмент, а також 25,26,27,28-тетракіс-(4-меркаптобутокси)-калікс[4]арен формули III [3], котрий містить на нижньому вінці макроциклу тіольні групи. , . Калікс[4]краун-етер II та його похідні широко застосовуються для зв'язування та вилучення радіоактивного цезію з відпрацьованого ядерного палива, аналітичного визначення біогенних амонієвих катіонів, амінокислот, пептидів, протеїнів [4,5,6,7,8,9,10]. Проте, 25,27-ди(октилокси)калікс[4]арен-краун-6 II не містить функціональних груп, за допомогою яких він може хімічно зв'язуватись з золотою поверхнею мікрочипів хемо- та біосенсорів. Калікс[4]арен III, функціоналізований 4-меркаптобутоксильними групами, здатний до хімічної адгезії на поверхні атомарного золота [3]. Разом з тим, сполука є інертною до катіонів лужних металів, амонієвих катіонів, амінокислот, пептидів, протеїнів. Задачею корисної моделі є пошук серед похідних калікс[4]арен-краун-6 сполук, які можуть розпізнавати і зв'язувати біогенні амонієві катіони, амінокислоти, пептиди, протеїни, та містити реакційноздатні групи, які можуть забезпечити хімічне зв'язування з поверхнею атомарного золота мікрочипів. Такі каліксарени можуть знайти застосування як хемо- та біосенсори в біології та медицині. Зазначена мета реалізується шляхом синтезу 25,27-ди-(5-тіо-октилокси)калікс[4]арен-краун6 І, який включає три стадії, виходячи і комерційно доступного тетрагідроксикалікс[4]арену IV. 1 UA 107468 U На першій стадії алкілуванням тетрагідроксикалікс[4]арену IV 1,4-дихлорбутаном в диметилформаміді за присутності карбонату калію та каталітичної кількості йодиду калію отримують 25,27-ди-(4-хлоробутокси)калікс[4]арен V в конформації конус (схема 1). Схема 1 5 10 15 . Конформація конус сполуки V підтверджується наявністю дублета дублетів спінової АВсистеми аксіального (4,26 м.ч., 4Н, J=12 Гц) та екваторіального (3,40 м.ч., 4Н, J=12 Гц) протонів метиленових зв'язок макроциклу в спектрі ПМР. На другій стадії реакцією циклізації ди-(4-хлоробутокси)калікс[4]арену V з дитозилатом пентаетиленгліколю за присутності карбонату цезію в розчині ацетонітрилу отримують 25,27-ди(4-хлоробутокси)калікс[4]арен-краун-6 VI (схема 2). На цій стадії під впливом темплатного ефекту катіону цезію конформація конус сполуки V трансформується в конформацію 1,3альтернат сполуки VI. Схема 2 . Кінцевий продукт 25,27-ди-(5-тіо-октилокси)калікс[4]арен-краун-6 І отримують заміщенням атомів хлору сполуки VI на пропілсульфідні угруповання реакцією з пропілмеркаптаном в розчині тетрагідрофурану за присутності гідриду натрію (схема 3). Схема 3 . 20 Винахід ілюструється наступними прикладами. Приклад 1. 2 UA 107468 U 5 10 15 20 25 30 35 40 45 50 55 Синтез 25,27-ди-4-хлоробутоксикалікс[4]арену V. До 2,0 г (4,7 ммоля) калікс[4]арену IV додають 2,0 г (14,47 ммоля) карбонату калію та 20 мл диметилформаміду. Реакційну суміш перемішують при кімнатній температурі, потім додають 3,5 г (27,6 ммоль) 1,4-дихлорбутану та 0,2 г (1,2 ммоль) йодиду калію та витримують реакційну суміш при 75-80 °C протягом 48 годин. Охолоджують до кімнатної температури, додають 100 мл води, екстрагують 200 мл хлороформу, органічний шар промивають 20 мл 0,5 N соляної кислоти та 100 мл води. Органічний шар сушать над сульфатом натрію. Видаляють розчинник при пониженому тиску. Залишок кристалізуюсь з н-бутилового спирту. Осад, що утворився, відфільтровують. Отримують безбарвну кристалічну речовину. Вихід 1,32 г (45,6 %). Т.топл. 175-176 °C. 1 Спектр ЯМР H (CDCl3, 300 МГц) δ, м.д.: 2,24 (м, 4H, -СН2-СН2-), 3,40 (д, 4Н, Аr-СН2екв-Аr), 3,78 (т, 4Н, -СН2-Сl), 4,03 (т, 8Н, -СН2-ОАr),), 4,26 (д, 4Н, Аr-СН2акс-Аr), 6,72 (д. т, 4Н, АrН), 6,99 (д. д, 8Н, АrН), 8,01 (с, 2Н, ОН). Обчислено, %: С 71,39; Η 6,32; Сl 11,70. С 36Н38Сl2О4. Знайдено, %: С 71,47; Η 6,45; Сl 11,58. Приклад 2. Синтез 25,27-ди-(4-хлоробутокси)каліксІ4]арен-крауну-6 VI До 1,0 г (1,65 ммоля) 25,27-ди-4-хлоробутоксикалікс[4]арену V додають 50 мл ацетонітрилу, нагрівають реакційну суміш до температури 75-80 °C і додають 1,2 г (3,68 ммоля) карбонату цезію. Через 30 хвилин додають 1,2 г (2,20 ммоль) дитозилату пентаетиленгліколю. Витримують реакційну суміш при 90-95 °C протягом 48 годин. Охолоджують до кімнатної температури, відфільтровують надлишок карбонату цезію та тозилат цезію, що утворився, розчинник видаляють при пониженому тиску. Додають 200 мл хлороформу, органічний шар промивають 20 мл 2 N соляної кислоти та 50 мл води. Органічний шар сушать над сульфатом натрію. Видаляють розчинник при пониженому тиску. Залишок очищають колонковою хроматографією. Кристалізують із н-бутилового спирту. Отримують безбарвну кристалічну речовину. Вихід 0,35 г (43,3 %). Т.топл. 115-116 °C. 1 Спектр ЯМР H (CDCl3, 300 МГц) δ, м.д.: 1,41-1,58 (м, 4Н, -СН2-СН2), 3,58 (т 16Н, АrО-СH2СH2-), 3,38-3,81 (м, 20Н, АrО-СН2-СН2 -О-), 6,84 (д. т, 4Н кожен, АrН), 7,08-7,11 (д. д, 8Н, АrН). Обчислено, %: С 68,39; Η 6,99; Сl 8,78. С46Н56 Сl2О8. Знайдено, %: С 70,07; Η 4,86; Сl 8,65. Приклад 3. Синтез 25,27-ди-(5-тіо-октилокси)калікс[4]арен-краун-6 І До 0,30 г (1,65 ммоля) 25,27-ди-(4-хлоробутокси)калікс[4]арен-краун-6 VI додають 10 мл тетрагідрофурану, охолоджують реакційну суміш до -10 °C і додають 0,145 г (3,0 ммоля) гідриду натрію. Через 30 хвилин додають 0,226 г (3,0 ммоль) н-пропілмеркаптану. Витримують реакційну суміш при 70-75 °C протягом 6 годин. Охолоджують до кімнатної температури, розчинник видаляють при пониженому тиску. Додають 50 мл хлороформу, органічний шар промивають 20 мл 1 N соляної кислоти та 50 мл води, сушать над сульфатом натрію. Видаляють розчинник при пониженому тиску. Залишок очищають колонковою хроматографією. Вихід 0,16 г (48,6 %). Густа олія. 1 Спектр ЯМР H (CDCl3, 300 МГц) δ, м.д.: 1,04 (τ, 6Н, СН3), 1,37-1,45 (м, 4Н, -СН2-СН2), 1,611,66 (м, 4Н, -СН2-СН2), 2,46-2,54 (м, 8Н, -S-CH2), 3,72 (с, 4Н, -Аr-ОСН2), 3,79 (с, 8Н, Аr-СН2-Аr), 1,58-1,64 (м, 4Н, -СН2-СН2), 3,58 (т, 4Н, АrO-СН2-СН2-), 3,38-3,79 (м, 16Н, АrO-СН2-СН2-О-), 6,826,84 (д. т, 4Н, АrН), 7,03-7,10 (д. д, 8Н, АrН). Обчислено, %: С 70,38; Η 7,95; S 7,23. C 52H70O8S2. Знайдено, %: С 70,54; Η 8,06; S 7,15. Приклад 4. Нанесення каліксарену І на поверхню золота (фіг. 1) Чутливу поверхню мікрочипа - пару золотих зустрічно-штирьових електродів витримують протягом 1-2 хвилин в щойно приготованому розчині, що містить 3 мл пероксиду водню (концентрація 35 %) та 7 мл сірчаної кислоти (концентрація 98 %). Після чого чутливу поверхню мікрочипа промивають у бістильованій воді, висушують на повітрі та обробляють концентрованим розчином етилового спирту. До 1 мг одержаного краун-етеру І додають в атмосфері аргону 1 мл толуену та перемішують до одержання гомогенної суміші (далі композиції). На пару золотих зустрічно-штирьових електродів, розміщених горизонтально до робочої поверхні, наносять краплину композиції об'ємом 0,5 мкл та залишають при кімнатній температурі на 60 хвилин. Після цього етап нанесення композиції повторюють ще двічі. Після чого мікрочип залишають при кімнатній температурі на 60 хвилин, потім витримують при температурі +4 °C 24 години. Далі мікрочип закріпляють в тримачі електродів, помішують його в комірку заповнену буферним розчином складу КН2РO4-NaH2PO4, і витримують протягом 30 хвилин, за умов постійного перемішування, з метою відмивання поверхні золота від сполуки І, 3 UA 107468 U яка не зв'язалась з поверхнею. Мікрочип, модифікований сполукою І зберігають в сухому стані при температурі +4 °C до моменту подальшого використання. 5 10 15 20 25 30 Джерела інформації: [1] R. Ungaro, A. Casnati, F. Ugozzoli, A. Pochini, J.-F. Dozol, С. Hill, H. Rouquette. 1,3Dialkoxycalix[4]arenecrown-6 in 1,3-alternate configuration: cesium-selective ligands that exploit cation-arene interations. Angew. Chem. Int. Ed. Engl. - 1994. - Vol. 33. - P. 1506-1509. [2] A. Casnati, A. Pochini, R. Ungaro, F. Ugozzoli, F. Arnaud, S. Fanni, M.-J. Schwing, Richard J. M. Egberink, F. de Jong, David N. Reinhoudt. Synthesis, complexation, and membrane transport studies of 1,3-alternate calix[4]arene-crown-6 conformers: a new class of cesium selective ionophores. J. Am. Chem. Soc. - 1995. - Vol. 117. - Ρ. 2767-2777. [3] J.-M. Ha, A. Katz, A. B. Drapailo, V. I. Kalchenko. Mercaptocalixarene-capped gold nanoparticles via postsynthetic modification and direct synthesis: effect of calixarene cavity-metal interactions. J. Phys. Chem. С - 2009. - Vol. 113. - P. 1137-1142. [4] B. A. Moyer. Complexation and Transport. G. W. Gokel, J. L. Atwood, J. E. D. Davies, D. D. MacNicol, F. Vogtle, J.-M. Lehn (Eds.). Molecular recognition: receptors for cationic guests. Comprehensive Supramolecular Chemistry. Pergamon. Elsevier. Oxford. - 1996. - P. 377-416. [5] V. Kumar, J. N. Sharma, P. V. Achuthan, R. C. Hubli. Selective separation of cesium from simulated high level waste solution using 1,3-dioctyloxy calix[4]arene-benzo-crown-6. J. Radioanal. Nucl. Chem. - 2014. - Vol. 299. - P. 1547-1553. [6] J. F. Dozol, N. Simon, V. Lamare, H. Rouquette, S. Eymard, B. Tournois, D. De Mark, R. M. Macias. A solution for cesium removal from high-salinity acidic or alkaline liquid waste: the crown calix[4]arenes. Sep. Sci. Technol. - 1999. - Vol. 34. - P. 877-909. [7] S. Safi, Z. Asfari, L. Ehret-Sabatier, M. Leroy, A. Hagége. Synthesis and characterization of immunogens based on calix[4]arene-crown-6 for the generation of antibodies directed towards cesium ions. Bioconjug. Chem. - 2006. - Vol. 17. - P. 1346-1350. [8] T. Katsu, M. Matsumoto. Discrimination of methyl ammonium from organic ammonium ions using ion-selective electrodes based on calix[4]arene-crown-6 conjugates. Analytical Science. - 2001. - Vol. 17. - P. 721-725. [9] F. Botha, J. Budka, V. Eigner, O. Hudecek, L. Vrzal, I. Cisarova, P. Lhotak. Recognition of chiral anions using calix[4]arene-based ureido receptor in the 1,3-alternate conformation. Tetrahedron. - 2014. - Vol. 70. - P. 477-483. [10] S. B. Nimse, T. Kim. Biological application of functionalized calixarenes. Chem. Soc. Rev. 2013. - Vol. 42. - P. 366-386. 35 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 25,27-Ди-(5-тіо-октилокси)калікс[4]арен-краун-6 формули: 40 Сполука І. 4 UA 107468 U Комп’ютерна верстка О. Гергіль Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07C 15/00
Мітки: 25,27-ди-(5-тіо-октилокси)калікс[4]арен-краун-6
Код посилання
<a href="https://ua.patents.su/7-107468-2527-di-5-tio-oktiloksikaliks4aren-kraun-6.html" target="_blank" rel="follow" title="База патентів України">25,27-ди-(5-тіо-октилокси)калікс[4]арен-краун-6</a>
Попередній патент: Установка для зварювання та рихтування карданних валів
Наступний патент: Захисна рукавичка
Випадковий патент: Тетрагідропіридини як пестициди, композиція, спосіб її приготування та спосіб боротьби із шкідниками











