Креатин фосфат і його фармацевтично прийнятні солі для лікування пухлин та фармацевтична композиція, що має протипухлинну активність
Формула / Реферат
1. Применение по крайней мере одного соединения, выбранного из креатин фосфата и его фармацевтически приемлемых солей, для ингибирования или снижения роста опухоли у млекопитающих.
2. Применение в соответствии с п.1, в котором фармацевтически приемлемой солью является натриевая соль.
3. Фармацевтическая композиция для ингибирования или снижения роста опухоли у млекопитающих, содержащая активное начало и фармацевтический приемлемый носитель, отличающаяся тем, что активное начало выбрано из креатин фосфата и его фармацевтически приемлемых солей в количестве от 0,1 до 50 г на композицию.
4. Фармацевтическая композиция в соответствии с п.3, в которой фармацевтически риемлемой солью является натриевая соль.
5. Фармацевтическая композиция в соответствии с п.3, в инъекционной форме.
Текст
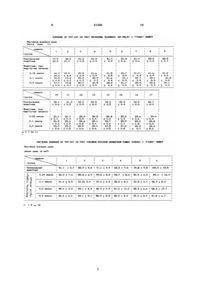
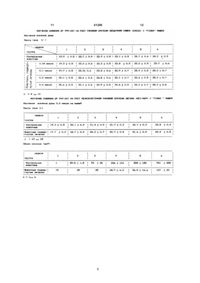
1. Применение по крайней мере одного соединения, выбранного из креатин фосфата и его фармацевтически приемлемых солей, для ингибирования или снижения роста опухоли у млекопитающих. 3 41285 4 слоты в смеси с аденозинтрифосфорной кислотой - сорбит; (АТф). Эти препараты предназначены для лече- фосфатный буфер, содержащий безводный втония и профилактики повреждения, вызванного ричный кислый фосфат натрия/первичный кислый ишемией клеток. фосфа т натрия; Документ US-4 769 318 относится к раство- нитратный буфер, содержащий цитрат нарам, содержащим различные производные фострия/лимонную кислоту; фоенолпировиноградной кислоты. Эти растворы - лактатный буфер, содержащий лактат натрия/ предназначены для консервирования крови. молочную кислоту; Наконец, в документе ЕР-А-239-357 описано - хлористый натрий. применение мононатриевой соли фосфоенолпиВ нашем предпочтительном примере осущеровиноградной кислоты для лечения заболевания ствления изобретения активный компонент можно сердца и почек, связанного с ишемией. разбавить реконструирующим растворителем, Было обнаружено, и это является основой насовместимым со способом введения препарата. стоящего изобретения, что соединения, имеющие Применяют хорошо известные реконструифосфоамидную связь или фосфатн ую связь энорующие растворители, примерами которых являла, обладают ценными, неизвестными фармакоются: логическими свойствами, в частности заметно - вода для инъецируемых препаратов; проявляемой противоопухолевой активностью. - 0,9%-ный раствор NaCl; Таким образом, настоящее изобретение отно- 5-15%-мый раствор глюкозы; сится в основном к применению по меньшей мере - 10-30%-ный раствор маннита; одного соединения, имеющего обогащенную энер- 20-30%-ный раствор сорбита; гией связь (фосфамидную связь или фосфатную - раствор тринатриевой соли лимонной кислоты. связь энола), для получения фармацевтических Цель настоящего изобретения является также препаратов, предназначенных для лечения опухоспособ лечения опухолей у людей введением телей. рапевтически эффективного количества, по меньВ одном типичном предпочтительном примере шей мере одного соединения, имеющего фососуществления изобретения в качестве соединефоамидную связь или фосфатную связь энола. ния, имеющего обогащенную энергией связь, приФармакологические свойства соединений, меняют фосфатокреатин и его фармацевтически имеющих, фосфамидную связь или фосфатную пригодные соли, в частности, натриевые соли. связь энола были показаны проведением различВ другом примере соединением, имеющим ных исследований для оценки действия фосфокобогащенную энергией связь, является фосфоереатина на различные опухолевые клетки. нолпировиноградная кислота и ее фармацевтичеДействие это неоспоримо обусловлено приски пригодные соли, в частности натриевые соли. сутствием фосфамидной связи в его молекуле. Фармацевтические препараты, полученные в Дополнительные опыты с фосфоноенолпиросоответствии с настоящим изобретением, особенвиноградной кислотой показывают, что аналогично пригодны для лечения свежих опухолей или ные фармакологические свойства можно достичь опухолей, которые оказались устойчивыми к хипри применении соединений, имеющих фосфатмиотерапии, например аденокарцином (ободочной ную связь энола. кишки, поджелудочной железы, желудка, бронхов, Экспериментальные протоколы и результаты почек, молочной железы, матки, яичников); эпипозволившие показать фармакологические свойдермоидных карцином (верхнего дыхательного ства соединений, имеющих фосфомидную связь пищеварительного тракта, бронхов, мочевых пуили фосфатн ую связь энола, приведены ниже. тей, заднего прохода, кожи); злокачественной ме1. Способ ланомы; саркомы мягких тканей; лейкемии; лим1.1. Принцип изобретения фом и множественной миеломы. Образование опухолей у "голой" мыши вызыЭти фармацевтические препараты будут привали подкожным инокулированием раковых клеготовлять обычными способами и вводить внутриток. Через неделю после инокулирования внутривенно, в форме пилюли или препарата для пребрюшной инъекцией вводили фосфокреатин, рывистой или непрерывной перфузии, обозначенный далее как UP-999-247, или NaCl. В внутриартериально, внутрибрюшинно или внутрипроцессе лечения животных взвешивали и размер мышечно в дозах от 50 мг до 5 г/кг тела на 24 ч. опухоли измеряли каждую неделю. В соответствии с одной из характеристик на1.2. Ме тодика стоящего изобретения фармацевтический препа1.2.1. Развитие рака человека у "голых" мырат выпускается в виде доз на один прием. шей Предпочтительная дозрованная единица соЧетырехнедельных "голых" мышей штамма держит 0,1 - 50 г активного компонента. Swiss выращивали в изоляторе (стерильная среВ предпочтительном варианте препарат выда) под давлением. пускают в виде инъецируемого препарата, содерЛинии раковых клеток человека, а именно Сажащего 0,1-50 г активного компонента. со2 (ободочной кишки), SK-MEL5 (меланомы), СаВ одном предпочтительном примере осущестраn-1 ( поджелудочной железы) и NCI-H69 (мелковления изобретения активный компонент разбавклеточного рака легких), культивировали в лен наполнителем, совместимым со способом различных средах, содержащих 10-20% сыворотки введения препарата. Применяют хорошо известплода теленка и 1% неосновных аминокислот. ные наполнители, примерами которых являются : 5 х 106 (SK-MEL5), 9 х 106 (Сасо2), 2 х 105 (Са- маннит; раn-1) и 2,3 х 106 (NCI-H69) клеток d забуферен 2 5 41285 6 ном фосфатном физиологическом растворе иноку ответствовали экспериментальному периоду. пировали в правый бок каждой мыши. Операцию Биохимические и гематологические измерения проводили в камере в стерильных условиях. проводили на плазме и крови, отобранных после Каждую неделю после инокулирования животнадреза животных. ных взвешивали и измеряли у них опухоль штанВ описанных экспериментальных условия х генциркулем. фосфокреатин не вызывал летального исхода. Объем опухоли (полуэллипсоидной) подсчиНаблюдаемое отклонение относится к группе тывали при помощи следующей формулы животных, которым ввели самые высокие дозы, (DETHLEFSENL.A., PRNITT I.M.S., MENDELSOHN вызывающие умеренное повышение содержания M.L. Анализ кривых роста опухолей, J.Natl. Cancer трансаминазы и натрия и понижение содержания Institute, 1968.40, 368-408, RADULOVIC S., MILLER щелочных фосфатов и элементов крови. G. ,SCHALL Y A. V. Ингибирование роста ксенотДругие изменения находятся в соответствии с расплантантантов рака ободочной кишки человека колебаниями , обычно наблюдаемыми у крыс. НТ-29 в "голых" мышах лечением анатагонистом Фосфокреатин проявляет прекрасную биолопептида, высвобождающего бомбезин/гастрин гическую толетарность при дозах до 2400 мг/кг, (RC-3095). Canser Res., 1991, 51, 6006-6009): введенных внутривенно. Подобным образом, фосфоенолпировиноширина´ длина´ высота ´p Объем опухоли = градная кислота имеет хорошую биологическую 6 толерантность при введении крысам в дозах до 50 1.2.2. Поучение влияния UP 999-247 на рост мг/кг и не индуцирует летальный исход. опухоли Некоторые примеры фармацевтических преЛечение начинают через 7 дней после инокупаратов на основе соединения, имеющего фослирования путем внутрибрюшинной инъекции UP фамидную связь или фосфатную связь энола, 999-247 (группа, подвергнутая лечению) или изобудут приведены ниже. тонического раствора (контрольная группа). КажФосфокреатин может быть в виде готового к дая группа содержит 10-15 мышей. Животные, применению стерильного раствора или в виде индивидуально индентифицированные татуировстерильного порошка или лиофилизатора. В этом кой на спине, разделяют по макролоновым камеслучае можно применять наполнитель без фармарам. кологической активности. В качестве наполнителя Продолжительность лечения зависит от цели применяют лактозу, маннит, фосфа тный буфер, лечения для каждой изучаемой серии. содержащий безводный первичный кислый фосПосле окончания лечения опухоли удаляют и фат натрия/вторичный кислый фосфат натрия, закрепляют в фиксаторе Bouin для патологоананитратный буфер, содержащий цитрат натомического анализа. трия/лимонную кислоту, молочный буфер, содер1.2.3. Схема введения жащий лактат натрия/молочную кислоту, хлорисИзучаемый продукт применяют в 0,9%- ном тый натрий или смесь этих наполнителей в любых растворе NaCl. Его стерилизуют при помощи 0,2 пропорциях. Наполнитель применяют хорошо измкм фильтра. Раствор вводят внутрибрюшинно в вестным способом. количестве 1 мл на мышь. В качестве реконструирующего растворителя Контрольным животным вводят 1 мм 0,9Х-ного используют либо инъекционные растворители для раствора хлористого натрия. обычного применения (0.9%-ный раствор NaCl, Схема дозирования предусматривает инъеци5%-ный или 15%-ный раствор глюкозы, 20-30%рование 0,04 ммоля, 0,1 ммоля, 0,2 ммоля и 0,4 ный раствор сорбита, раствор тринатриевой соли ммоля UP 999-247 каждой мыши. лимонной кислоты или инъецируемый препарат) Эти дозы выбраны соответственно максиили любой другой обычно применяемый раствомальной дозе, которую можно вводить внутриритель для перфузии. брюшинно, и соответственно концентрация плазфармацевтический препарат рекомендуется мы, определенной заранее в применять в виде стерильного лиофилизатора, фармококинетических исследованиях. содержащего 25 г фосфокреатина, реконструиро1.2.4. Выражение результатов ванного 100 мл 0,9%-ного раствора хлористого Из полученных измерением отдельных велинатрия. чин рассчитаны следующие параметры! Пример 1: - Масса тела в г, (среднее значение ± стандартное отклонение), измеряемая каждую неденитратный буфер рН 7 лю. лимонная кислота 0,0329% - объем опухоли в мм 3 (среднее значение ± Na2HPO4 • 2Н2О 0,253% стандартное отклонение), намеряемый каждую глюкоза 5% неделю. вода для инъецируемого 2. РЕЗУЛЬТАТЫ препарата gsg 100% Результаты представлены в помещенных ниЕсли применяют лиофилизат, то для инъециже таблицах. Полученные результаты указывают руемых препаратов растворителем служит вода. на ингибирования роста опухоли после введение Пример 2: фосфокреатина "голым" мышам с различными установленными опухолями человека. фосфа тный буфер рН 7,2 Ингибирование зависит от дозы соединения. Na2HPO4 • 2Н2О 0,758% Изменение массы и поведение животных соNaH2PO4 0,184% 3 7 NaCl вода для инъецируемого препарата 41285 8 Пример 4: глюкоза 5% вода для инъецируемого препарата gsg 100% Если применяют лиофилизат, то раствортелем для инъецируемых препаратов служит вода. Пример 5: 0,44% gsg 100% Пример 3: маннит вода для инъецируемого препарата gsg 100% KH2PO4 Na2HPO4 • 2Н2О глюкоза вода для инъецируемого препарата Если применяют лиофилизат, то растворителем для инъецируемых препаратов служит вода. 4 0,178 0,953% 2% gsg 100% 9 41285 5 10 11 41285 6 12 13 41285 14 ________________________________________________________ ДП "Український інститут промислової власності" (Укрпатент) Україна, 01133, Київ-133, бульв. Лесі Українки, 26 (044) 295-81-42, 295-61-97 __________________________________________________________ Підписано до друку ________ 2001 р. Формат 60х84 1/8. Обсяг ______ обл.-вид. арк. Тираж 50 прим. Зам._______ ____________________________________________________________ УкрІНТЕІ, 03680, Київ-39 МСП, вул. Горького, 180. (044) 268-25-22 ___________________________________________________________ 7
ДивитисяДодаткова інформація
Назва патенту англійськоюCreatine phosphate and pharmaceutically acceptable salts thereof for cancer treatment and pharmaceutical composition possessing anticancer activity
Автори англійськоюNICOLE BRU, VICTOR IZRAEL
Назва патенту російськоюКреатин фосфат и его фармацевтически приемлемые соли для лечения опухолей и фармацевтическая композиция с противоопухолевой активностью
Автори російськоюБру Николь, Израэль Виктор
МПК / Мітки
МПК: A61K 31/66, A61P 35/00
Мітки: пухлин, фармацевтично, композиція, солі, активність, прийнятні, фармацевтична, лікування, протипухлинну, фосфат, має, креатин
Код посилання
<a href="https://ua.patents.su/7-41285-kreatin-fosfat-i-jjogo-farmacevtichno-prijjnyatni-soli-dlya-likuvannya-pukhlin-ta-farmacevtichna-kompoziciya-shho-maeh-protipukhlinnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Креатин фосфат і його фармацевтично прийнятні солі для лікування пухлин та фармацевтична композиція, що має протипухлинну активність</a>
Наступний патент: Композиційний матеріал для покрить
Випадковий патент: Спосіб визначення антиоксидантної активності біологічно активних сполук (бас)