Спосіб одержання 3-n,n-дициклобутиламіно-8-фтор-3,4-дигідро-2н-1-бензопіран-5-карбоксаміду в вигляді рацемічної сполуки або r- чи s-енантіомерів та проміжні сполуки
Формула / Реферат
Спосіб одержання рацемічної сполуки формули (І)
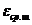 , (І)
, (І)
її R-енантіомера (формула R-(І))
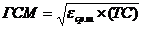 R-(І)
R-(І)
та її S-енантіомера (формула S-(І))
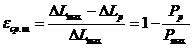 , S-(І)
, S-(І)
та їх фармацевтично прийнятної солі та/або сольвату, який включає наступні реакційні стадії:
а) етерифікація сполуки (II) з одержанням сполуки (ІІІ)
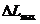 , (II)
, (II)
де R – С1-С4 алкіл,
![]()
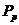 , (III)
, (III)
b) пропаргілування сполуки (III) у присутності основи з одержанням сполуки (IV)
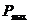 , (IV)
, (IV)
с) нагрівання сполуки (IV) з одержанням сполуки (V)
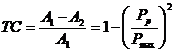 , (V)
, (V)
d) гідроліз сполуки (V) у присутності основного або кислотного каталізатора з одержанням сполуки (VI)
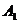 , (VI)
, (VI)
е) взаємодія сполуки (VI) з оксалілхлоридом або тіонілхлоридом з наступною обробкою аміаком з одержанням сполуки (VII)
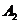 , (VII)
, (VII)
f) взаємодія сполуки (VII) з йодом або нітритною сіллю з одержанням сполуки (VIII)
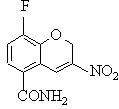 , (VIII)
, (VIII)
g) взаємодія сполуки (VIII) з відновником з одержанням сполуки (IX)
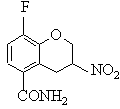 , (IX)
, (IX)
h) відновлення сполуки (IX) з одержанням сполуки (X)
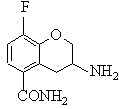 , (X)
, (X)
і) якщо є бажаним (R)- або (S)-енантіомер сполуки (І), взаємодія сполуки (X) з відповідним чистим енантіомером хіральної кислоти з наступною фракційною кристалізацією та обробкою одержаної солі основою з одержанням сполуки (R)-(XI)
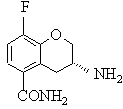 R-(ХІ)
R-(ХІ)
або S-(XI)
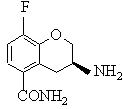 , S-(ХІ)
, S-(ХІ)
j) алкілування сполук R-(XI) або S-(XI) з одержанням сполук формули R-(I) або S-(I) відповідно або алкілування сполуки (X) з одержанням рацемічної сполуки формули (І),
k) необов'язково обробка сполук, одержаних на стадії j) традиційним способом з одержанням їхньої солі або сольвату.
2. Спосіб за п. 1, який відрізняється тим, що стадію а) етерифікації здійснюють з використанням триалкілортоформіату.
3. Спосіб за п. 2, який відрізняється тим, що триалкілортоформіатом є триметилортоформіат.
4. Спосіб за п. 1, який відрізняється тим, що стадію b) пропаргілування здійснюють з використанням пропаргілброміду.
5. Спосіб за п. 1, який відрізняється тим, що стадію с) нагрівання здійснюють у присутності ароматичного розчинника, наприклад діетиланіліну.
6. Спосіб за п. 1, який відрізняється тим, що використовуваним на стадії d) каталізатором є гідроксид натрію.
7. Спосіб за п. 1, який відрізняється тим, що використовуваною на стадії f) нітритною сіллю є нітрит натрію.
8. Спосіб за п. 1, який відрізняється тим, що використовуваним на стадії g) відновником є боргідрид натрію.
9. Спосіб за п. 1, який відрізняється тим, що як хіральну кислоту на стадії і) використовують L-(+)-винну кислоту з одержанням сполуки R-(XI).
10. Спосіб за п. 1, який відрізняється тим, що стадію j) алкілування здійснюють відновним амінуванням циклобутанону в присутності відновника.
11. Спосіб за п. 10, який відрізняється тим, що відновником є ціанборгідрид натрію.
12. Сполука формули (V)
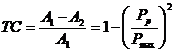 , (V)
, (V)
де R означає С1-С4 алкіл.
13. Сполука формули (VII)
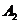 (VII)
(VII)
14. Сполука формули (X)
 (X)
(X)
15. Сполука формули (VIII)
 (VIII)
(VIII)
16. Сполука формули (IX)
 . (IX)
. (IX)
Текст
Спосіб одержання рацемічної сполуки форму ли (І) F ОН ОН , (III) де R - Сі-С4 алкіл, Ь) пропарплування сполуки (III) у присутності основи з одержанням сполуки (IV) F О и R-енантюмера (формула R-( F с) нагрівання сполуки (IV) з одержанням сполуки (V) F О. (О та и S-енантюмера (формула S-( F d) гідроліз сполуки (V) у присутності основного або кислотного каталізатора з одержанням сполуки (VI) F О. та їх фармацевтично прийнятної солі та/або сольвату, який включає наступні реакційні стадії а) етерифікація сполуки (II) з одержанням сполуки (III) .(VI) є) взаємодія сполуки (VI) з оксалілхлоридом або тюнілхлоридом з наступною обробкою аміаком з одержанням сполуки (VII) 61949 стадії j) традиційним способом з одержанням їхньої солі або сольвату 2 Спосіб за п 1, який відрізняється тим, що стадію а) етерифікації здійснюють з використанням триалкілортоформіату 3 Спосіб за п 2, який відрізняється тим, що триалкілортоформіатом є триметилортоформіат 4 Спосіб за п 1, який відрізняється тим, що стадію Ь) пропарплування здійснюють з використанf) взаємодія сполуки (VII) з йодом або нітритною ням пропарплброміду сіллю з одержанням сполуки (VIII) 5 Спосіб за п 1, який відрізняється тим, що стаF дію с) нагрівання здійснюють у присутності ароматичного розчинника, наприклад діетиланіліну О. 6 Спосіб за п 1, який відрізняється тим, що використовуваним на стадії d) каталізатором є гідроNOксид натрію 7 Спосіб за п 1, який відрізняється тим, що ви:ONH 2 користовуваною на стадії f) нітритною сіллю є ніт, (viii) рит натрію g) взаємодія сполуки (VIII) з відновником з одер8 Спосіб за п 1, який відрізняється тим, що вижанням сполуки (IX) користовуваним на стадії д) ВІДНОВНИКОМ Є борпдF рид натрію 9 Спосіб за п 1, який відрізняється тим, що як О. хіральну кислоту на стадії і) використовують !_-(+)винну кислоту з одержанням сполуки R-(XI) NO10 Спосіб за п 1, який відрізняється тим, що стадію]) алкілування здійснюють відновним аміну:ONH2 ванням циклобутанону в присутності відновника , (їх) 11 Спосіб за п 10, який відрізняється тим, що h) відновлення сполуки (IX) з одержанням сполуки відновником є ціанборпдрид натрію 12 Сполука формули (V) F О. NH, 12 , (X) і) ЯКЩО Є бажаним (R)- або (З)-енантюмер сполуки (І), взаємодія сполуки (X) з ВІДПОВІДНИМ ЧИСТИМ енантюмером хіральної кислоти з наступною фракційною кристалізацією та обробкою одержаної солі основою з одержанням сполуки (R)-(XI) F .00 де R означає С1-С4 алкіл 13 Сполука формули (VII) F О. О. "" NH (VII) 14 Сполука формули (X) F О. або S-(XI) F NH, О. : O N H1 2 NH:ONH 2 (X) 15 Сполука формули (VIII) , s-cxi) j) алкілування сполук R-(XI) або S-(XI) з одержанням сполук формули R-(l) або S-(l) ВІДПОВІДНО або алкілування сполуки (X) з одержанням рацемічної сполуки формули (І), к) необов'язково обробка сполук, одержаних на 61949 NO NO:ONH 2 (VIII) (IX) 16 Сполука формули (IX) Даний винахід відноситься до нового способу одержання 3-М,г\І-дициклобутиламіно-8-фтор-3,4дипдро-2Н-1 -бензопіран-5-карбоксаміду, особливо (Р)-3-І\І,І\І-дициклобутиламіно-8-фтор-3,4-дипдро2Н-1-бензопіран-5-карбоксаміду та до нових проміжних продуктів, одержуваних у ході цього процесу (Р)-3-М,г\І-дициклобутиламіно-8-фтор-3,4дипдро-2Н-1-бензопіран-5-карбоксамід розкрито у WO95/11891, де також описано спосіб одержання розглянутої сполуки Зазначений спосіб включає ряд стадій реакції Атом фтору вводять у бензопіранове кільце селективним бромуванням у 8-е положення з наступним г\І,г\І-дибензилюванням, із наступною реакцією галогенлітієвого обміну в отриманій бромвмісній сполуці та реакції з ВІДПОВІДНИМ агентом, який фторує Отриманий (R)-3-N,NДибензиламшо-8-фтор-5-метокси-3,4-дипдро-2Н1-бензопіран потім дибензилюють, N,Nдіалкілують реакцією відбудовного алкілування з циклобутаноном, деметилюють та каталітично перетворюють, використовуючи перехідний метал, монооксид вуглецю та ВІДПОВІДНИЙ спирт, у проміжний алкіл (Р)-3-М,г\І-дициклобутиламіно-8-фтор3,4-дипдро-2Н-1-бензопіран-5-карбоксилат Гідроліз складного ефіру до карбонової кислоти з наступною обробкою кислоти тюнілхлоридом дає хлорангідрид кислоти, який при обробці аміаком дає бажаний (Р)-3-М,г\І-дициклобутиламіно-8фтор-3,4-дипдро-2Н-1-бензопіран-5-карбоксамід Однак, незважаючи на наявність зазначених методів та іншої інформації, усе ще є потреба в нових, більш зручних та ефективних способах виробництва (Р)-3-М,г\І-дициклобутиламіно-8-фтор3,4-дипдро-2Н-1-бензопіран-5-карбоксаміду Спосіб одержання ^)-3-г\І,г\І-дициклобутиламшо-8-фтор-3,4-дипдро-2Н-1-бензопіран-5карбоксаміду даного винаходу має переваги з технічної точки зору в порівнянні зі способом, описаним yWO95/11891 У заявленому способі використовують вихідний матеріал, що має фторозаміщення в потрібному положенні, що не вимагає проведення небажаної стадії фторування Введення фтору ВІДПОВІДНО до традиційного процесу вимагає низьких температур для обробки ЛІТІЄМ та проведення реакції з дорогим, шкідливим і, можливо, навіть токсичним агентом , що фторує Крім того, реакція призводить до отримання як побічного продукту значної КІЛЬКОСТІ (R)-3-N,Nдициклобутиламіно-5-метокси-3,4-дипдро-2Н-1 бензопірану, який повинний бути відділений від бажаного фторовмісного кінцевого продукту методом дорогої та технічно складної хроматографії Спосіб даного винаходу є комерційно більш вигідним, ніж спосіб, відомий з WO95/11891 Даний винахід стосується нового способу одержання рацемічної сполуки (R)-3-N,Nдициклобутиламіно-8-фтор-3,4-дипдро-2Н-1бензопіран-5-карбоксаміду, який має формулу (І), його R-енантюмеру (формула R-(l)) та його Sенантюмеру (формула S-( та їх фармацевтично прийнятних солей та/або сольватів Новий шлях синтезу для виробництва сполук, що мають формули (1), R-(l) та S-(l) приводиться нижче Основним важливим способом є спосіб виробництва ^)-3-М,г\І-дициклобутиламіно-8фтор-3,4-дипдро-2Н-1-бензопіран-5-карбоксаміду Вихідний матеріал сполуки (II) може бути придбаний наприклад, в компанії Frmton Laboratories, Іпс США ВІДПОВІДНО ДО способу даного винаходу, сполука (III), в якій R являє собою С1-С4 алкіл, наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, т-бутил, одержують (а) етерифікацією сполуки (II) триалкілортоформіатом в безводному розчиннику, такому як ВІДПОВІДНИЙ алкіловий спирт Етерифікація каталізується кислотою, такою як H2SO4, при температурі в діапазоні від 0°С до 100°С Реакція може бути також проведена з використанням інших методів етерифікації, таких, як нагрівання сполуки (II) до температури в діапазоні від 40°С до 100°С у відповідному спирті, такому як метанол, етанол або пропанол, у присутності кислоти, такої як H2SO4 Карбонова кислота (III) може бути також захищена за допомогою інших захисних груп, відомих фахівцям у даній області, див , наприклад Protective Groups in Organic Synthesis, Second Edition, Theodora W Green and Peter G H Wuts, John Wiley&Sons, Inc , 1991 F Г OH (it) CCLK Сполуку (IV) одержують (b) алкілуванням сполуки (III) галогенідами пропал плу, наприклад, бромідами, хлоридами або йодидами, або пропаппловим спиртом, активованим у вигляді сульфонату, наприклад, п-толуолсульфонату в органічному розчиннику в присутності основи при температурі в діапазоні від 20°С до 100°С Прикладами основ, що можуть використовуватися, є карбонати, такі як карбонат натрію та карбонат калію, або аміни, такі як триалкіламіни, наприклад, триетиламш, хоча фахівцям у даній області ВІДОМІ ІНШІ прийнятні основи Переважно використовують карбонат калію Органічний розчинник може бути обраний з ацетону, ізобутилметилкетону, ацетонітрилу та толуолу, але можуть також застосовуватися й ІНШІ органічні розчинники, ВІДОМІ фахівцям в даній області Переважно використовують ацетон 61949 8 кількостей кислот або основ, наприклад, гідроксиду натрію, гідроксиду калію, гідроксиду ЛІТІЮ, сірчаної кислоти, соляної кислоти або сульфонової кислоти Можуть використовуватися також ІНШІ каталізатори, ВІДОМІ фахівцям у даній області Розчинник може бути обраний із спирту, води або толуолу, або їхньої суміші, а також з інших прийнятних розчинників, відомих фахівцям у даній області Сполука (VII) може бути також отримана шляхом взаємодії сполуки (V) із ВІДПОВІДНИМ амідом, наприклад, формамідом, по реакції трансамідування в присутності ВІДПОВІДНОГО каталізатора, наприклад, ціаніду F F F (IV) CX C. R Сполуку (V) одержують (с) нагріванням сполуки (IV) у чистому вигляді або у відповідному ароматичному розчиннику, такому як діетиланілін, диметиланілін, дифеніловий ефір або в ароматичному розчиннику, наприклад, у толуолі або ксилолі, при підвищеному тиску або в насиченому вищому вуглеводні, наприклад, ундекані або додекані при температурі в діапазоні від 150°С до 250°С, переважно в діапазоні температур від 210°Сдо230°С (VM) CONH, Сполуку (VIII) одержують (f) шляхом взаємодії сполуки (VII) із йодом або іншими агентами, що йодують, наприклад, монохлоридом йоду та нітритної солі, такої як нітрит срібла, нітрит натрію, або нітрит тетрабутиламонію в органічному розчиннику, такому як етилацетат, етанол, етиленгліколь, тетрапдрофуран, моно- або диглим або метанол та їхня суміш, у присутності або у відсутність води, у діапазоні температур від 0°С до 100°С F F (Vlli) Сполуку (VI) одержують (d) гідролізом в присутність основи або кислоти в суміші органічного розчинника та води при температурі в діапазоні від 20°С до 100°С Органічний розчинник може бути обраний з метанолу, етанолу етиленгліколю та їхніх сумішей, однак, можуть бути використані й ІНШІ розчинники або суміші розчинників, ВІДОМІ фахівцям у даній області Переважно використовують метанол Можуть бути використані різні основи, такі як гідроксид натрію, гідроксид калію або гідроксид ЛІТІЮ, або кислота, така, як соляна кислота, сірчана кислота або тр и фтор метан сул ьфонова кислота Сполуку (VII) одержують (е(і)) шляхом взаємодії сполуки (VI) при температурі в діапазоні від 0°С до 100°С з оксалілхлоридом або тюнілхлоридом в присутності або без органічного розчинника або суміші органічних розчинників, з проведенням потім реакції з аміаком або гідроксидом амонію Органічним розчинником, використовуваним у даній реакції може бути метиленхлорид, етилацетат або толуол, або їхні суміші Сполука (VII) може бути також отримана (е(м)) шляхом взаємодії сполуки (V) з аміаком у відповідному розчиннику в діапазоні температур від 20°С до 200°С під тиском або без підвищення тиску Реакція може бути проведена в присутності або у відсутності каталітичних CONH CONH, Сполуку (IX) одержують (д) шляхом взаємодії сполуки (VIII) з відновником, таким як борпдрид натрію, ціанборпдрид натрію, алюмопдрид ЛІТІЮ або інший придатний відновник, у присутності етиленгліколю або силікатів органічного розчинника, такого, як етилацетат, метиленхлорид, метанол або етанол, у присутності або у відсутності води та/або оцтової кислоти при температурі від -20°С до 100°С, переважно в діапазоні температур від 0° до 20°С Р F N 0 , C O N H C Q N H , Сполуку (X) одержують (п) шляхом відновлення сполуки (IX), наприклад, цинком та соляною кислотою в оцтовій кислоті в діапазоні температур від 20°С до 150°С або шляхом пдрогенування в присутності каталізатора, такого, як платина, паладій або нікель Ренея та газоподібного водню в органічному розчиннику, такому як тетрапдрофуран, етилацетат, нижний спирт або їхня суміш, переважно в присутності кислоти, наприклад, соляної кислоти в діапазоні температур від -20°С до 61949 100°С Можуть використовуватися також ІНШІ ВІД 10 ПОВІДНІ ВІДНОВНИКИ, ВІДОМІ фахівцям у даній облас ті F F (ЇХ) h CONH, (Р)-енантіомер сполуки (XI) одержують ВІДПОВІДНО до відомих методів, таких як фракційна кристалізація діастереомерних солей Діастереомерну сіль одержують (і) ШЛЯХОМ обробки сполуки (X) чистим енантюмером хіральної кислоти, такої як карбонова кислота або сульфонова кислота, у відповідному розчиннику, такому як метанол, етанол, етилацетат або вода, хоча можуть використовуватися й ІНШІ розчинники та/або суміші розчинників, ВІДОМІ фахівцям у даній області Кислота може бути обрана з чистих енантюмерів винної кислоти, мигдальної кислоти та камфанової кислоти, але можуть використовуватися й ІНШІ КИСЛОТИ, ВІДОМІ фахівцям у даній області Переважно використовують І_-(+)-винну кислоту Чисту сполуку R(XI) одержують шляхом обробки солі основою, такою, як карбонат натрію, карбонат калію, гідроксид кальцію, гідроксид натрію або аміак, та екстрагують ВІДПОВІДНИМ органічним розчинником, наприклад, діетиловим ефіром (З)-енантюмер сполуки (XI) одержують за методикою (і), описаною для сполуки R-(XI), використовуючи кислоту, енантюмерно протилежну застосовуваній для одержання R-(XI) Переважно використовують Р-(-)-винну кислоту Сполуки (І), R-(l) та S-(l) одержують Q) шляхом алкілування сполук (X), R-(XI) та S-(XI) за допомогою ВІДПОВІДНИХ відомих методів, таких як відновлювальне алкілування з використанням циклобутанону, у присутності відновника, такого як борпдрид натрію, ціанборпдрид натрію або каталізатора гідрування, такого як паладій або платина, у присутності водню, в органічному розчиннику, такому як метанол, етанол, толуол, оцтова кислота або етилацетат, або їхня суміш Альтернативно, сполуки (І), R-(l) та S-(l) можуть бути отримані (j) шляхом алкілування сполук (X), R-(XI) та S-(XI), ВІДПОВІДНО, алкілуючим агентом, таким, як циклобутил галогенід або мезилат, або тозилат циклобутанолу, у відповідному органічному розчиннику в присутності основи та/або каталізатора Органічний розчинник може бути обраний з ацетонітрилу або етанолу, а також інших прийнятних розчинників, що ВІДОМІ фахівцям у даній області Основа може бути обрана з карбонату натрію, карбонату калію або триетиламшу, а також з інших можливих основ, які ВІДОМІ фахівцям у даній області Каталізатор являє собою йод, переважно, йодид натрію CN, DH у Сіль сполук (І), R-(0 та S-(l) може бути отримана з використанням традиційних методів Даний винахід відноситься також до нових проміжних продуктів, а саме до проміжних продуктів формул (ІІІ)-(Х) R-(XI) та S-(XI) Особливо кращими проміжними продуктами є наступні проміжніпродукти сполука формули (V) де R означає С1-С4 алкіл, сполука формули сполука формули (X) Даний винахід пояснюється більш детально за допомогою наступних прикладів ПРИКЛАД 1 Одержання метилу 4-Фтор-З-пдроксибензоату (Сполука (III)) 4-фтор-З-пдроксибензойну кислоту (20,0г, 0,13 моль 5 розчиняють в безводному метанолі (160мл), змішують з триметилортоформіатом (25мл) та потім додають концентровану H2SO4 (Змл) та реакційну суміш нагрівають до 40-55°С протягом ночі Половину розчинника видаляють у вакуумі, отриманий розчин виливають у суміш лід/НгО та продукт екстрагують ДВІЧІ діетиловим ефіром Об'єднані ефірні фази промивають ДВІЧІ НгО, обробляють холодним розчином насиченого ІЧаНСОз, обробляють насиченим сольовим розчином, висушують MgSO4, фільтрують та розчинник видаляють у вакуумі з одержанням 21,6г (99% ви 12 11 61949 хід) білої твердої речовини як цільової сполуки чинник видаляють у вакуумі з одержанням 6,64г (тпл 93,5-94,5°С) (97% вихід) жовтуватої твердої речовини (висушують в ексикаторі над Р2О5) як цільової сполуки Мас-спектр (70eV) m/z (відносна інтенсивність) + (тпл 224-226°С) 170 (44, М ), 139 (100), 111 (83), 83(83), 82(16), 81(11), 63(11), 57(24) Мас-спектр (70eV) m/z (відносна інтенсивність) + 194 (93, М ), 193 (100), 149 (56), 148 (68), 120 (13), ПРИКЛАД 2 88 (25), 75 (28), 74 (21), 60 (12) Одержання метил 4-Фтор-Зпропарплоксибензоату (Сполука (IV)) ПРИКЛАД 5 Метил 4-фтор-З-пдроксибензоат (20,0мл, Одержання 8-фтор-2Н-1-бензопіран-50,118 моль) розчиняють у безводному ацетоні карбоксаміду (Сполука (VII)) (450мл), змішують з пропарплбромідом (26,2г, До 8-фтор-2Н-1-бензопіран-5-карбоновой кис0,177 моль) та потім додають порошкоподібний лоти додають тюнілхлорид (60мл) та розчин переК2СО3 (32,4г, 0,236 моль) та реакційну суміш пемішують при кімнатній температурі протягом ночі ремішують протягом ночі при кімнатній температуНадлишок тюнілхлориду видаляють у вакуумі, дорі Реакційну суміш фільтрують та розчинник видають безводний толуол та розчинник видаляють даляють у вакуумі Залишок розчиняють у у вакуумі Хлорангідрид кислоти розчиняють у медіетиловому ефірі, промивають 4 рази НгО, обротиленхлориді (60мл) та додають краплинами до бляють насиченим сольовим розчином, висушують охолодженого розчину (крижана баня) концентроMgSO4, фільтрують та розчинник видаляють у ваваного аміаку (60мл) Реакційну суміш перемішукуумі з одержанням як цільової сполуки 25,5г ють при кімнатній температурі протягом ЗО хвилин (100% вихід) забарвленої у світло-абрикосовий До реакційної суміші додають етилацетат та відоколір твердої речовини (тпл 60,5-61,5°С) кремлюють органічну фазу Водну фазу повторно екстрагують сумішшю метиленхлориМас-спектр (70eV) m/z (відносна інтенсивність) ду/етилацетату та об'єднані органічні фази вису208 (27, М+), 207 (100), 193 (22), 177 (20), 149 (50), шують MgSO4, фільтрують, та розчинник видаля82(21), 81 (10) ють у вакуумі з одержанням 1,91г (98% вихід) білої ПРИКЛАД З твердої речовини як цільової сполуки (тпл 194,5Одержання метил 8-фтор-2Н-1-бензопіран-5195,0°С) карбоксилату (Сполука (V)) Метил 4-фтор-З-пропарплоксибензоату (140,0г, 67,2 ммоль) змішують із N,Nдіетиланіліном та реакційну суміш нагрівають до 220°С протягом 5 годин Забарвлену в чорний колір реакційну суміш охолоджують, розчиняють у діетиловому ефірі (600мл) та промивають 2М НСІ, порціями по 1л Промивні води екстрагують повторно діетиловим ефіром, об'єднані ефірні фази промивають НгО до нейтральної реакції, обробляють насиченим сольовим розчином, висушують MgSO4, фільтрують та розчинник видаляють у вакуумі з одержанням темно-коричневого неочищеного залишку Неочищену тверду речовину хроматографують на силікагелі (елюент метиленхлорид/чотирихлористий вуглець 11) з одержанням 11,9г (85% вихід) бурувато-жовтої твердої речовини як цільової сполуки (т пл 73,574,5°С) Мас-спектр (70eV) m/z (відносна інтенсивність) 208 (65, М+), 207 (42), 194 (12), 193 (100), 177 (32), 149(10), 148(12) ПРИКЛАД 4 Одержання 8-фтор-2Н-1-бензопіран-5карбонової кислоти (Сполука (VI)) Метил 8-фтор-2Н-1-бензопіран-5-карбоксилат (7,36г, 35,4 ммоль) розчиняють в абсолютному етанолі (220мл), додають NaOH (2,0г, 49,6 ммоль) у НгО (25мл) та реакційну суміш кип'ятять із зворотним холодильником протягом 1,5 годин Потім реакційну суміш охолоджують та розчинник видаляють у вакуумі Жовту тверду речовину розчиняють у НгО (150мл), додають активоване вугілля та суміш фільтрують Отриману злегка забарвлену рідину промивають діетиловим ефіром, водяний розчин підкислюють за допомогою 2М НСІ, та продукт ДВІЧІ екстрагують етилацетатом Об'єднані органічні порції обробляють насиченим сольовим розчином, висушують MgSO4, фільтрують та роз Мас-спектр (70eV) m/z (відносна інтенсивність) 193 (51, М+), 192 (19), 176 (11), 175 (33), 174 (100), 149 (20), 148 (38), 101 (14), 75 (17) ПРИКЛАД 6 Одержання 5-фтор-2Н-1-бензопіран-5карбоксаміду (Сполука (VIII) До розчину 8-фтор-3-нітро-2Н-1-бензопіран-5карбоксаміду (4,46г, 23,1 ммоль) в етилацетаті (220мл) додають етиленгліколь (4,0мл) та розчин нітриту натрію (6,52г, 92,4 ммоль) в НгО (11мл) і потім йод (9,0г, 34,7 ммоль) Реакційну суміш кип'ятять із зворотним холодильником протягом 24 годин та в цей період додають НгО (2,2мл) та етиленгліколь (4,0мл) порціями Реакційну суміш охолоджують, розбавляють етилацетатом, промивають 5% розчином NaSO4, обробляють насиченим сольовим розчином, висушують MgSO4, фільтрують та розчинник видаляють у вакуумі з одержанням неочищеної жовтої твердої речовини Тверду речовину повторно кристалізують з абсолютного етанолу з одержанням 1,3г (24% вихід) блискучих жовтих кристалів як цільової сполуки (т пл 227,8228,2Х) Мас-спектр (70eV) m/z (відносна інтенсивність) 238 (57, М+), 221 (100), 192 (71), 191 (46), 190 (10), 148(14), 109(16), 94(12) ПРИКЛАД 7 Одержання 8-Фтор-3-нітро-3,4-дипдро-2Н-1бензопіран-5-карбоксаміду (Сполука (IX)) 8-фтор-3-нітро-2Н-1-бензопіран-5-карбоксамід (730мг, 3,1 ммоль) перемішують у вигляді суспензії в хлороформі (75мл) в ізопропіловому спирті (25мл) До перемішуваної суміші додають силікагель (2,2г, 230-400 меш ASTM) та потім порціями протягом 15 хвилин - порошкоподібний борпдрид натрію (255мг, 6,2 ммоль) Після завершення додавання реакційну суміш перемішують протягом 20 хвилин та реакцію гасять додаванням оцтової 14 13 61949 кислоти (2мл) і перемішують ще ЗО хвилин Відфіповітрі з одержанням 1,4г вільної основи у вигляді льтровують нерозчинний матеріал та розчинник білих кристалів (т пл 196°С розклад ) 23 видаляють у вакуумі Залишок розподіляють між [a] D-43° (з 0,005, МеОН) етилацетатом і водою Водну фазу екстрагують Мас-спектр (70 еВ) m/z (відносна інтенсив+ етилацетатом, об'єднані етилацетатні фази оброність) 210 (5, М ), 194 (31), 193 (100), 192(13), бляють насиченим сольовим розчином, висушують 178(17), 148(11) MgSO4, фільтрують та розчинник видаляють у ваПРИКЛАД 10 куумі з одержанням 0,67г (91% вихід) жовтуватоОтримання (3)-3-амшо-8-фтор-3,4-дипдро-2Нбілої твердої речовини як цільової сполуки (т пл 1-бензопіран-5-карбоксаміду (Сполука S-(XI) 191,0-191,5°С) (З)-енантюмер, отриманий з маточного розчиМас-спектр (70eV) m/z (відносна інтенсивність) ну після попереднього розділення та видалення + 240 (1, М ), 195 (17), 194 (100), 193 (17), 177 (26), основи (4г, 19 ммоль), розчиняють у метанолі 151 (44), 149 (27), 148 (18), 123 (23), 103 (48), 102 (20мл) та додають розчин Р-(-)-винноі кислоти (Зг, (11), 101 (29), 96 (13), 95 (15), 94 (11), 88 (41), 83 20 ммоль), розчиненої в 20мл метанолу (20мл) (14), 77 (25), 76 (11), 75 (39), 74 (23), 70 (10), 63 Отриману кристалічну тверду речовину фільтру(11), 60(11), 51 (17), 50(10) ють та повторно кристалізують з розчину 40% етанолу у воді (ЮОмл) Одержують Зг безбарвних ПРИКЛАД 8 кристалів (т пл 173°С розклад ) Одержання 3-амшо-8-Фтор-3,4-дипдро-2Н-1бензопіран-5-карбоксаміду (Сполука (X)) [a]23D-90° (з 0,005, Н2О) Вільну основу одер8-фтор-3-нітро-3,4-дипдро-2Н-1-бензопіран-5жують тим же самим способом, що і (R)карбоксамід (9,0г, 37,5 ммоль) розчиняють у тетенантюмер, з виходом 1г білих кристалів (т пл рапдрофурані (ЮОмл) та абсолютному етанолі 197°С розклад) (400мл) та поміщають в умови пдрогенування при [a]23D+44° (з 0,005, МеОН) атмосферному тиску з використанням нікелю РеМас-спектр (70eV) m/z (відносна інтенсивність) нея (W-2,9r) при кімнатній температурі Реакцію 210 (4, М+), 194 (32), 193 (100), 192 (12), 178(16) припиняють через 48 годин, через зазначений час ПРИКЛАДИ відфільтровують каталізатор, промивають суміш Одержання (Р)-3-г\І,г\І-дициклобутиламіно-8гарячим етанолом та об'єднані розчинники видафтор-3,4-дипдро-2Н-1-бензопіран-5-карбоксаміду ляють у вакуумі з одержанням 7,8г (99% вихід) (Сполука R-(lj) жовтувато-білої твердої речовини Частину її по(Р)-3-амшо-8-фтор-3,4-дипдро-2Н-1вторно кристалізують з етилацетату з одержанням бензопіран-5-карбоксамід (0,5г, 2,4 ммоль) розчибілих кристалів як цільової сполуки (т пл 187няють у безводному метанолі (Юмл), та до зазна188°С) ченого розчину додають перемішуваний розчин Мас-спектр (70eV) m/z (відносна інтенсивність) НОАс (140 мг, 2,4 ммоль), циклобутанону (0,5г, 7 210 (6, М+), 194 (ЗО), 193 (100), 192(20), 178(12) ммоль) та NaCNBbb (0,3г, 5 ммоль) Суміш переПРИКЛАД 9 мішують при кімнатній температурі протягом ночі Отримання (Р)-3-амшо-8-фтор-3,4,-дипдро-2НРеакційну суміш нагрівають до 60°С та додають 1-бензопіран-5-карбоксаміду (Сполука R-(XI) порціями протягом 6 днів додаткову КІЛЬКІСТЬ циклобутанону (0,8г, 11 ммоль), NaCNBH3 (200мг, 3,2 І_-(+)-винну кислоту (7г, 47 ммоль) розчиняють ммоль) і НОАс (ЮОмг, 1,4 ммоль) Розчин випау суміші 30% етанолу у воді (ЗООмл) та нагрівають рюють у вакуумі, залишок перемішують з 2М роздо кипіння Додають рацемічний амін формули (X) чину NH3 і потім екстрагують ДВІЧІ етилацетатом (8г, 38 ммоль) Розчин повільно охолоджують до Об'єднані етилацетатні порції сушать над Na2SO4, кімнатної температури Осад фільтрують та профільтрують та розчинник видаляють у вакуумі, з мивають етанолом з одержанням 4,7г (65%) злегка одержанням неочищеного залишку Хроматогракоричневих кристалів, (т пл 175°С) фія на силікагелі (елюент етилацетат) дає 0,5г [a]23D+67°(3 0,01,H2O) (82%) цільової сполуки у вигляді білих кристалів Вільну основу отримують додаванням розчину (тлл 138-139°С) ЫагСОз до суспензії тартрату в етанолі Суміш фільтрують та розчинник видаляють у вакуумі [a]23D-134°(3 0,006, CH2CI2) Залишок розчиняють у 200мл киплячого етилацеМас-спектр (70eV) m/z (відносна інтенсивність) тату/етанолу (95 5) та фільтрують крізь целіт Роз318 (З, М+), 193 (55), 177 (11), 176 (21), 149 (18), чин випарюють доти, поки не починається криста148 (31), 98 (54), 70 (100), 69 (40), 68 (11), 55 (40), лізація продукту та з цього моменту повільно 54 (34), 44(17), 42 (19), 41 (59), 39 (29) доводять до кімнатної температури Осад відфільтровують, промивають етилацетатом та сушать на Комп'ютерна верстка О Воробей Підписне Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійськоюA new process
Автори англійськоюJohansson Lars
Назва патенту російськоюНовый способ
Автори російськоюЙоханссон Ларс
МПК / Мітки
МПК: A61K 31/352, C07D 311/58
Мітки: спосіб, 3-n,n-дициклобутиламіно-8-фтор-3,4-дигідро-2н-1-бензопіран-5-карбоксаміду, вигляді, проміжні, одержання, рацемічної, сполуки, s)-енантіомерів
Код посилання
<a href="https://ua.patents.su/7-61949-sposib-oderzhannya-3-nn-diciklobutilamino-8-ftor-34-digidro-2n-1-benzopiran-5-karboksamidu-v-viglyadi-racemichno-spoluki-abo-r-chi-s-enantiomeriv-ta-promizhni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 3-n,n-дициклобутиламіно-8-фтор-3,4-дигідро-2н-1-бензопіран-5-карбоксаміду в вигляді рацемічної сполуки або r- чи s-енантіомерів та проміжні сполуки</a>
Попередній патент: Спосіб одержання гідравлічного в’яжучого
Наступний патент: Бальзам “чари діброви”
Випадковий патент: Ортез на нижню кінцівку











