[(1-феніл-5-форміл-1н-імідазол-4-іл)тіо]оцтова кислота та її 5-алкенілпохідні, які виявляють антиоксидантну активність
Номер патенту: 68451
Опубліковано: 26.03.2012
Автори: Вовк Михайло Володимирович, Чорноус Віталій Олександрович, Яремій Ірина Миколаївна, Паламар Аліна Олександрівна
Формула / Реферат
[(1-Феніл-5-форміл-1H-імідазол-4-іл)тіо]оцтова кислота та її 5-алкенілпохідні загальної формули
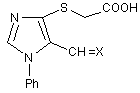
де Х=О (І), ![]() (ІІ),
(ІІ), 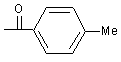 (III),
(III), 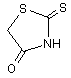 (IV),
(IV), 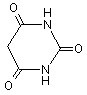 (V),
(V),
які виявляють антиоксидантну активність.
Текст
Реферат: [(1-Феніл-5-форміл-1H-імідазол-4-іл)тіо]оцтова кислота та її 5-алкенілпохідні загальної формули S N N COOH CH =X Ph O S S H N O CN CN (ІІ), де Х=О (І), які виявляють антиоксидантну активність. O NH Me (III), O (IV), O N H (V), UA 68451 U (12) UA 68451 U UA 68451 U Корисна модель належить до органічної хімії, а саме до нової [(1-феніл-5-форміл-1Hімідазо-4-іл)тіо]оцтової кислоти та її 5-алкенільних похідних загальної формули : S N N COOH CH =X Ph O S O CN CN (ІІ), 5 10 15 20 Me 30 35 40 45 NH Me H N O N H де Х=О (І), (ІІІ), O (IV), O (V). Запропоновані нові сполуки, спосіб їх отримання, властивості і застосування в науковій літературі та патентних виданнях не описані. Хронічні захворювання печінки обумовлені впливом різноманітних екзота ендогенних факторів [1-3] і супроводжуються запальними процесами. При виникненні хронічної печінкової патології порушується проникність мембран гепатоцитів, їх осмотичні властивості, білковосинтетична функція та гемодинаміка [1, 4]. З'ясовано, що такі патологічні зміни виникають внаслідок процесів вільнорадикального окиснення ліпідів. Це супроводжується надмірним утворенням вільних радикалів, які ініціюють пероксидне окиснення поліненасичених жирних кислот, пошкодження ліпідних компонентів біологічних мембран та внутрішньоклітинної структури гепатоцитів. При цьому антиоксидантна система, яка нейтралізує вплив вільних радикалів, у хворих на хронічний гепатит перебуває у пригніченому стані. Проблема лікування хронічних захворювань печінки є однією із найскладніших у гастроентерології, що викликано значними змінами функції та структури печінкової тканини. Класичними препаратами для лікування хронічних захворювань печінки є як рослинні, так і синтетичні гепатопротектори. В останні роки пошук нових синтетичних антиоксидантів стає актуальною хімічною та фармацевтичною проблемою [5]. Найближчим аналогом за фармакологічною дією сполук, які заявляються, є вітчизняний препарат Тіотриазолін формули: N 25 S N N H S COO + H2N O Цей лікарський засіб має широкий спектр дії та виявляє антиоксидантну, гепатозахисну, кардіопротекторну, протиішемічну, мембраностабілізуючу, імуномодулюючу, протизапальну, антиаритмічну та нейропротекторну активність, що дозволяє використовувати його у гепатології, кардіології, гінекології, неврології, педіатрії та хірургії. Він входить до переліку препаратів при комплексній терапії гепатитів різного генезу, інфаркту міокарда, стенокардії, інсульту тощо [6]. Експериментальні дослідження останніх років підтвердили ефективність застосування Тіотриазоліну при різноманітних ураженнях печінки (тетрацикліновому та ізоніазидрифампіциновому, доксорубіциновому, алкогольному) завдяки антиоксидантному впливу та запобіганню проявам цитолізу [7-9]. Значна антиоксидантна активність препарату, виявлена при моделюваннях різних патологічних процесів, свідчить, що однією із складових механізму антиоксидантної дії Тіотриазоліну є його здатність «захоплювати» активні форми кисню (АФК) [6]. У дослідах in vivo -5 -7 було встановлено, що Тіотриазолін у діапазоні концентрацій 10 -10 М знижує концентрацію ˉ АФК, зокрема, супероксидного аніон-радикала (О2 ˉ) і пероксинітриту (ONOO ) [11-13]. Неймовірніше, що така дія Тіотриазоліну проявляється завдяки наявності в структурі тіольної групи, що надає всій молекулі високих відновлювальних властивостей. Разом з тим, передозування Тіотриазоліну [14] в деяких випадках може приводити до загальної слабкості, головокружіння, тахікардії, задишки і навіть задухи. Враховуючи достатньо високі рекомендовані дози Тіотриазоліну (1% розчин), доцільним є пошук нових синтетичних антиоксидантів, які виявляють більшу ефективність при цій же концентрації, що дозволить знизити величину лікувальної дози і зменшить ризики передозування. Задача корисної моделі є дизайн та синтез нових ефективних сполук з вираженими антиоксидантними властивостями. Поставлена задача вирішується синтезом нової [(1-феніл-5-форміл-1Н-імідазо-4іл)тіо]оцтової кислоти та її 5-алкенілпохідних. 1 UA 68451 U 5 10 Для одержання зазначених сполук нами розроблена препаративно зручна схема, яка базується на використанні доступного 1-феніл-4-хлоро-5-формілімідазолу [15]. При його нагріванні з тіогліколевою кислотою в етанолі впродовж 2 год. в присутності гідроксиду натрію як основи утворюється [(1-феніл-5-форміл-1H-імідазол-4-іл)тіо] оцтова кислота (І) з виходом 78 %. Проведення реакції в достатньо м'яких умовах дозволяє отримати продукт заміщення хлору на фрагмент тіогліколевої кислоти із збереженням альдегідної групи. Синтетичний потенціал альдегідної групи синтезованої кислоти було використано для отримання ряду її структурних аналогів, функціоналізованих в положенні 5 фармакоактивними алкенільними, в тому числі і гетерилзаміщеними, угрупованнями. Показано, що [(1-феніл-5форміл-1H-імідазол-4-іл)тіо] оцтова кислота при взаємодії з ациклічними та гетероциклічними СН-кислотами в етанольному розчині в умовах основного каталізу перетворюється у відповідні 5-алкіліденопохідні (II-V) з виходами 68-73 %. Cl HS N N Ph CH=O COOH S N N COOH CH=O H2X S N COOH CH=X N Ph Ph ІІ-V I O S S H N O CN CN 15 20 25 30 35 40 45 50 NH Me O N H де Х=О (І), (ІІ), (ІІІ), O (IV), O (V). Схема ілюструється прикладами синтезу цільових сполук, структура яких підтверджена 1 13 аналітичними даними та результатами вимірів ІЧ - та ЯМР Н і С спектрів. Приклад 1. [(1-Феніл-5-форміл-1H-імідазол-4-іл)тіо]оцтова кислота (І). До розчину 1.2 г (0,021 моль) КОН у 20 мл етанолу прикапують 1 г (0,011 моль) тіогліколевої кислоти, додають 2 г (0,01 моль) альдегіду і кип'ятять 2 год. Реакційну суміш охолоджують, розчинник випаровують у вакуумі, до залишку додають 50 мл 5 %-ного розчину КОН, відфільтровують незначний залишок. Фільтрат підкислюють 10 % НСl до рН=5-6. Отриманий осад відфільтровують, і сушать на повітрі. Вихід -1 1 83 %, т. топл. 137-139 °C. ІЧ-спектр, см : 1700 (С=О), 2540-2880 (СООН). Спектр ЯМР Н, δ, 2 м.ч.: 4.00 с (2Н, СН2), 7.56-7.63 м ( 5НAr), 8.25 с (1Н, Н ), 9.59 с (1Н, СН=O), 12.74 ш.с. (1Н. 13 5 СООН). Спектр ЯМР С, δ, м.ч.: 32.61 (СН2), 125.39 (СAr), 126.29 (С ), 129.02 (СAr), 129.50 (САr), 2 4 134.62 (СAr), 142.21 (С ), 147.84 (С ), 170.12 (СООН), 177.58 (СН=O). Знайдено, %: С 54.87; Н 3.80; N 10.73. C12H10N2O3S. Вирахувано, %: С 54.95; Н 3.84; N 10.68. Синтез 5-алкенілпохідних [(1-феніл-5-форміл-1H-імідазол-4-іл)тіо]оцтової кислот (II-V). До розчину 0,53 г (0.002 моль) сполуки І у 20 мл етанолу додають (0,002 моль) відповідної СНкислоти, 1 кр піперидину і кип'ятять 4 год. Охолоджують, отриману реакційну суміш розводять рівною кількістю води, підкислюють 10% НСl до рН=5-6. Осад відфільтровують. Сушать і кристалізують з 70%-ного водного етанолу. Приклад 2. {[5-(2,2-Диціаноетеніл)-1-феніл-1H-імідазол-4-іл]тіо}оцтова кислота (II). Вихід 73 %, т. топл. -1 1 165-167 °C. ІЧ-спектр, см : 1655(С=С), 2210 (C=N), 2490-2820 (СООН). Спектр ЯМР Н, δ, м.ч.: 2 4.09 с (2Н, СН2), 7.54-7.62 м (5НAr), 8.08 с (1Н, Н ), 8.71 с (1Н, СН=). Знайдено, %: С 57.98; Н + 3.21; N 18.09. [М+1] 311. C15H10N4O2S. Вирахувано, % : С 58.06; Н 3.25; N 18.05. М 310.34. Приклад 3. {[5-[3-(4-Метилфеніл)-3-оксо-1-пропеніл]-1-феніл-1H-мідазол-4-іл]тіо}оцтова кислота (III). -1 1 Вихід 69 %, т. топл. 173-175 °C. ІЧ-спектр, см : 1730 (С=О), 2450-2810 (СООН). Спектр ЯМР Н, 2 δ, м.ч.: 2.39 с (3Н, СН3), 4.07 с (2Н, СН2), 7.22-7.78 м (9НAr + 2СН=), 8.23 с (1Н, Н ), 12.81 ш.с (1Н, + СООН). Знайдено, %: С 66.60; Н 4.76; N 7.43. [М+1] 379. C21H18N2O3S. Вирахувано, %: С 66.65; Н 4.79; N 7.40. М 378.45. Приклад 4. {[5-[(4-Оксо-5-тіазолідиніліден)метил]-1-феніл-1H-імідазол-4-іл]тіо}оцтова кислота (IV). Вихід -1 70 %, т. топл. 240-242 °C. ІЧ-спектр, см : 1660 (С=С), 1690 (С=О), 2470-2855 (СООН), 3290 (N1 2 H). Спектр ЯМР H, δ, м.ч.: 3.99 с (2Н, СН2), 7.12 с (1Н, СН=), 7.49-7.61 м (5НAr), 8.30 с (1Н, Н ), + 12.84 ш.с (1Н, NH), 13.55 ш.с (1Н, СООН). Знайдено, %: С 47.70; Н 2.91; N 11.15. [М+1] 378. C15H11N3O3S3. Вирахувано, %: С 47.73; Н 2.93; N 11.13. М 377.47. Приклад 5. {[1-Феніл-5-[(тетрагідро-2,4,6-триоксо-5(2H)-піримідиніліден)-метил]-1Н-імідазол-4-1 іл]тіо}оцтова кислота (V). Вихід 71 %, т. топл. 245-247 °C. ІЧ-спектр, см : 1640 (С=С), 1690-1710 1 (С=О), 2445-2870 (СООН). Спектр ЯМР Н, δ, м.ч.: 3.96 с ( 2Н, СН2), 7.46-7.61 м (5НAr), 7.69 с 2 UA 68451 U 2 5 10 15 20 25 (СН=), 8.49 с (1Н, Н ), 11.13 с (1Н, NH), 11.33 с (1Н, NH), 12.73 м (1Н, СООН). Знайдено, %: С + 51.59; H 3.22; N 15.09. [M+l] 373. C16H12N4O2S. Вирахувано, %: С 51.61; Н 3.25; N 15.05. М 372.36. Приклад 6. Визначення антиоксидантної активності [(1-феніл-5-форміл-1Н-імідазо-4іл)тіо]оцтової кислоти та її 5-алкенілпохідних. Антиоксидантну активність сполук в дослідженнях in vitro визначали за їх здатністю 2+ інгібувати індуковане Fе -аскорбатзалежне пероксидне окиснення ліпідів (ПОЛ) (зменшення у досліджуваних пробах вмісту малонового альдегіду (МА) - одного з кінцевих продуктів ПОЛ). Вміст МА в пробах визначали за реакцією з тіобарбітуровою кислотою (ТК) [16]. Вивчення антиоксидантної активності сполук в системі in vivo проводили на загальновідомій моделі тетрахлорметанового гепатиту в щурів, який викликали шляхом дворазового (через день) внутрішньошлункового введення тваринам CCl4 із розрахунку 0,25 мл/100 г маси щура у вигляді 50%-ного олійного розчину [16]. Дослідні тварини були розділено на чотири групи: І контрольна (інтактні щури); II - тварини інтоксиковані CCl4; III - щури, яким на фоні інтоксикації CCl4 упродовж 7 днів вводили сполуку 6 (100 мг/кг); IV - щури, яким на фоні інтоксикації ССl4 упродовж 7 днів вводили Тіотриазолін (100 мг/кг). Тварин забивали декапітацією під легким ефірним наркозом. Кров відбирали в присутності гепарину. У плазмі крові щурів визначали вміст окисно-модифікованих білків (ОМБ), вільних HS-груп і загальну антиоксидантну активність (АОА); в еритроцитах крові визначали вміст МА, глутатіону відновленого (Г-SH) та активності каталази (КАТ) за загальноприйнятими методиками описаними в роботі [16]. Дослідження антиоксидантної активності синтезованих сполук in vitro показало, що в -1 -3 діапазоні концентрацій 10 -10 всі сполуки є активними. Найбільшу антиоксидантну активність -2 в системі in vitro виявили сполуки І, ІІІ та IV, які при концентрації 10 моль/л мають вищі показники загальної антиоксидантної активності порівняно з Тіотриазоліном відповідно на 5,7%, 3,9% та 5,6%. Таблиця 1 Антиоксидантна активність синтезованих сполук in vitro (у % від контролю) Конц. моль/л -1 1×10 -1 5×10 -2 1×10 -2 5×10 -3 1×10 І 63.2 69.2 80.2 81.5 81.3 Антиоксидантна активність (% від контролю) II ІІІ IV V Тіотриазолін 80.4 66.2 67.7 73.1 65.4 79.1 71.2 75.8 73.3 71.9 78.4 78.2 80.1 73.5 74.5 80.4 80.2 79.0 72.3 76.9 82.1 79.0 81.7 71.2 78.3 Вивчення антиоксидантної дії in vivo на прикладі сполуки І при експериментальному токсичному гепатиті підтверджує потенційну активність всієї серії (табл. 2). 30 Таблиця 2 Вплив сполуки І на показники оксидантно-антиоксидантного гомеостазу в крові щурів за умов токсичного гепатиту ((М±m; n=5-7)) Показники/групи щурів МА, мкмоль/л ОМБ, о.о.г/мл АОА, % Вільні HS-групи, мкмоль/мл Г-SH, мкмоль/мл КАТ, мкмоль/хв·л Контроль (інтактні щури) 13,06±1,21 1,42±0,11 80,3±7,4 ССl4 ССl4+ сполука І ССl4+тіотриазолін 18,85±1,7* 1,92±0,17* 54,4±5,2* 16,35±1,51 1,47±0,14 78,3±6,5 16,30±1,62* 1,67±0,12* 77,1±7,1 0,85±0,05 0,62±0,04* 0,83±0,07 0,89±0,07 1,05±0,08 26,3±2,1 0,80±0,05* 21,3±1,9* 1,15±0,09 25,8±2,4 1,23±0,08* 24,7±1,8 Примітка: * - зміни достовірні порівняно з контролем (Р ≤ 0,05). Токсичний тетрахлорметановий гепатит у щурів приводить до суттєвих порушень оксидантно-антиоксидантної рівноваги. Так, у проведеному нами експерименті, в тварин з ССl4 3 UA 68451 U 5 10 15 20 25 30 35 40 45 50 індукованим гепатитом зріс вміст МА в еритроцитах крові та ОМБ в плазмі крові на 44 і 35% відповідно порівняно з показниками інтактних щурів. Посилення процесів ВРОЛ і ОМБ у організмі гепатитних щурів супроводжувалося пригніченням функціонування систем антиоксидантного захисту, на що вказує зниження, порівняно з показниками інтактних тварин, в плазмі щурів загальної АОА і вмісту вільних HS-груп (на 32 і 30,3%) та в еритроцитах крові вмісту Г-SH та активності каталази (на 24% і 19%). Поєднана дія тетрахлоретану і сполуки І нормалізувала стан оксидантно-антиоксидантної системи і за деякими показниками показала кращі результати ніж тіотриазолін. Зокрема, вміст ОМБ в плазмі крові досліджуваних тварин знизився до 1,47 о.о.г/мл, що на 14% перевищив показники, отримані при використанні тіотриазоліну. Величина загальної АОА сполуки І була вищою ніж величина АОА тіотриазоліну і практично дорівнювала величині загальної АОА контрольної групи тварин. Ці дані вказують на здатність досліджуваного класу сполук більш ефективно пригнічувати процеси ВРОЛ і біополімерів, зокрема ОМБ. У плазмі крові тварин цієї групи також нормалізувався вміст вільних HS-груп, а у еритроцитах крові тварин, які на фоні гепатиту отримували сполуку І - показники Г-SH і активності КАТ. Таким чином результати дослідження біологічних властивостей [(1-феніл-5-форміл-1Hімідазол-4-іл)тіо]оцтової кислоти свідчать, що в експериментах in vitro та in vivo вказана речовина характеризується вираженою антиоксидантною активністю. Введення в її структуру функціональних алкенільних фрагментів в цілому посилює антиоксидантну дію і дозволяє кваліфікувати цей тип сполук як новий клас антиоксидантів гетероциклічного ряду. Джерела інформації: 1. Губергріц Н. Б. Хронічні гепатити і цирози печінки. Сучасні класифікація, діагностика, лікування. - Донецьк : ТОВ «Лебідь», 2002. - 158 с. 2. Подымова С. Д. Болезни печени.- М.: Медицина, 1993. - 544 с. 3. Харченко Н. В. Хронические гепатиты: достижения, нерешенные проблемы // Сучасна гастроентерологія. - 2000. - № 1. - С. 50-53. 4. Бабак О. Я. Эффективность использования препарата циброгинин в терапии хронических гепатитов // Сучасна гастроентерологія і гепатологія, 2001.- № 1. - С. 64-65. 5. Омельянчик Л. О., Генчева В. І., Федоряк Д. М., Бражко О. А., Завгородній М. П., Лабенська І. Б., Корнет Н. Н. Пошук біорегуляторів з антиоксидантною дією серед S-похідних 4меркаптохінолінів // Ukrainica Bioorganica Acta.- 2007.- Т.2.- С. 17-24. 6. Бєленічев І. Ф., Мазур І. А., Волошин М. А., Горчакова Н. О., Чекман І. С. // Новости медицины и фармации в Украине. - 2007. - № 2. - С. 206-210. //http://novosti.mifua.com/archive/issue-3396/article-3421 7. Гудивок Я. С., Голубєва М. Г. // Ліки України. - 2005. - Додаток: 36. наук, праць І Націон. конгресу лікарів внутрішньої медицини. - С. 41. 8. Гудивок Я. С., Купновицька І. Г., Голубєва М. Г. // Вісн. фармакол. та фармації. - 2005. - № 7. - С. 7-9. 9. Стародуб Є. М., Самогальська О. Є. Використання антиоксидантів у лікуванні хронічних захворювань печінки. Новости медицины и фармации. - 2007. - № 2. - С. 226- 230. 10. Тиотриазолин / И. А. Мазур, Н. А. Волошин, И. С. Чекман та ін. - Львов: Наутилус, 2005. 156 с. 11.Беленичев И. Ф., Мазур И. А., Коваленко С. И. // Акт. питання фармац. та мед. науки і практики. - 2002. - Вип. VIII. - С. 43-48. 12. Бєленічев І. Ф., Коваленко С. І., Мазур І. А. та ін. // Ліки. - 2001. - № 5. - С. 28-36. 13. Бєленічев І. Ф., Кучеренко Л. І., Мазур І. А. // Експер. фізіол. та біохімія. - 2002. - № 12. С. 24-29. 14. http://compendium.com.ua/info/7043. 15. Чорноус В. А., Братенко М. К., Вовк М. В. Полифункциональные имидазолы. I. Синтез 1замещенных 4-хлор-1H-имидазол-5-карбальдегидов по Вильсмайеру-Хааку // Журн. орган. Химии. - 2009. - Т.45, № 8. - С. 1219-1222. 16. Давидова Н. В. Біохімічні механізми антиоксидантної дії екстракту родіоли рідкого: дис. ...канд. мед. наук: 03.00.04 / Давидова Наталія Валентинівна. - К., 2005. - 182 с. 55 4 UA 68451 U ФОРМУЛА КОРИСНОЇ МОДЕЛІ [(1-Феніл-5-форміл-1H-імідазол-4-іл)тіо]оцтова кислота та її 5-алкенілпохідні загальної формули S N N COOH CH =X Ph , O S S H N O 5 CN CN (ІІ), де Х=О (І), які виявляють антиоксидантну активність. O NH Me (III), O (IV), O N H (V), Комп’ютерна верстка Л. Купенко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
Назва патенту англійською[(1-phenyl-5-formyl-1h-imidasol-4-yl)thio]acetic acid and 5-alkenyl derivatives thereof possessing antioxidant activity
Автори англійськоюVovk Mykhailo Volodymyrovych, Chornous Vitalii Oleksandrovych, Palamar Alina Oleksandrivna, Yaremii Iryna Mykolaivna
Назва патенту російською[(1-фенил-5-формил-1h-имидазол-4-ил)тио]уксусная кислота и ее 5-алкенилпроизводные, проявляющие антиоксидантную активность
Автори російськоюВовк Михаил Владимирович, Черноус Виталий Александрович, Паламар Алина Александровна, Яремий Ирина Николаевна
МПК / Мітки
МПК: A61K 31/00, C07D 233/00
Мітки: кислота, активність, 5-алкенілпохідні, 1-феніл-5-форміл-1н-імідазол-4-іл)тіо]оцтова, антиоксидантну, виявляють
Код посилання
<a href="https://ua.patents.su/7-68451-1-fenil-5-formil-1n-imidazol-4-iltiooctova-kislota-ta-5-alkenilpokhidni-yaki-viyavlyayut-antioksidantnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">[(1-феніл-5-форміл-1н-імідазол-4-іл)тіо]оцтова кислота та її 5-алкенілпохідні, які виявляють антиоксидантну активність</a>
Попередній патент: Оптичний кабель, вбудований у грозозахисний трос
Наступний патент: Гра “полюси”
Випадковий патент: Спосіб розігрівання і нижнього зливання із залізничних вагонів-цистерн застиглих продуктів











