2-(хіназолін-4-ілтіо)бутанова кислота, що проявляє антирадикальну, антиоксидантну та гепатопротекторну активність
Номер патенту: 16242
Опубліковано: 17.07.2006
Автори: Горюшко Ганна Герасимівна, Бєленічев Ігор Федорович, Губський Юрій Іванович, Коваленко Сергій Іванович, Левицький Євген Леонідович, Авраменко Антоніна Іванівна, Нікітін Владислав Олександрович
Формула / Реферат
2-(хіназолін-4-ілтіо)бутанова кислота формули:
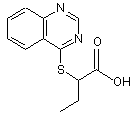 ,
,
що проявляє антиоксидантну, антирадикальну та гепатопротекторну активність.
Текст
УКРАЇНА (19) UA (11) 16242 (13) U (51) МПК C07D 239/72 (2006.01) A61P 39/06 (2006.01) A61P 1/16 (2006.01) МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ОПИС ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ видається під відповідальність власника патенту ДО ДЕКЛАРАЦІЙНОГО ПАТЕНТУ НА КОРИСНУ МОДЕЛЬ (54) 2-(ХІНАЗОЛІН-4-ІЛТІО)БУТАНОВА КИСЛОТА, ЩО ПРОЯВЛЯЄ АНТИРАДИКАЛЬНУ, АНТИОКСИДАНТНУ ТА ГЕПАТОПРОТЕКТОРНУ АКТИВНІСТЬ 1 2 O S * O OH Відомі структурні аналоги: похідні S-(4хіназоліл)-меркаптооцтової кислоти, що проявляють антиоксидантну, антирадикальну та протисудомну активність [Бєленічев І.Ф., Коваленко C.I., Карпенко О.В. Дослідження антиоксидантної та антирадикальної активності іліденгідразидів S-(4хіназоліл)-меркапто-оцтової кислоти in vitro та в умовах модельних судом // Клінічна фармація. N O S OH S N R3 N R R=H, СН3; R1 =H, ОН, ОСН3, СООН; R2 = Н, OCH3; R3=Н, ОН, ОСН3 Недоліком відомих структурних аналогів є те, що вони не проявляють гепатопротекторної активності. Найбільш близькою до сполуки, що заявляється, є 2-(хіназолін-4-ілтіо)-етанова кислота [Белєнічев І.Ф., Коваленко C.I., Бражко О.А., Карпенко О.В. Дослідження антиоксидантної дії хіназоліл-4(хіноліл-4)-тіо- ( )карбонових кислот та їх похідних в умовах ініціювання вільно-радикальних про (13) 16242 R1 N O (11) 2003. - Т.7, №1. - С.53-57; Дунаев В.В., Беленичев И.О., Коваленко С.И., Карпенко А.В. Изучение антиоксидантной активности бензилиденгидразидов S-(4-хиназолил)-меркаптоуксусной кислоты на модели "нитрозирующего стресса" in vitro // Экспериментальная и клиническая фармакология 2004. - Т.67, №3. - С.69-72.], формули: N R2 U , що проявляє антиоксидантну, антирадикальну та гепатопротекторну активність. UA Корисна модель відноситься до біологічно активних сполук і може бути використаною у фармації та медицині. Відомий лікарський препарат - тіотриазолін (який в своїй структурі містить залишок карбоксіалкільної групи, що зв'язана із азагетероциклом через екзоциклічний атом сірки), який застосовується у медичній практиці як препарат, що проявляє антиоксидантну та гепатопротекторну активність. [Тиотриазолин: фармакологические аспекты и клиническое применение. Мазур И.А., Волошин Н.А., Чекман И.С. и др. - Запорожье-Львов: "НАУТІЛУС", 2005. - 156с.], формули: N N N N (19) (21) u200605441 (22) 18.05.2006 (24) 17.07.2006 (46) 17.07.2006, Бюл. № 7, 2006 р. (72) Нікітін Владислав Олександрович, Авраменко Антоніна Іванівна, Коваленко Сергій Іванович, Бєленічев Ігор Федорович, Губський Юрій Іванович, Левицький Євген Леонідович, Горюшко Ганна Герасимівна (73) Коваленко Сергій Іванович, Бєленічев Ігор Федорович (57) 2-(хіназолін-4-ілтіо)бутанова кислота формули: 3 16242 цесів in vitro та моделюванні ішемії головного мозку // Ліки. - 2001. - №5-6. - С.28-33]; 4 N Вплив ( )-[S-(4хіназоліл)]тіоалкілкарбонових кислот та їх солей на картину судом, викликаних тіосемікарбазидом [Л.Ф. Беленичев, С.І.Коваленко, А.В. Карпенко та ін. // Ліки. - 2002. - №5-6. - С.75-81; Синтез, фізико N O S OH хімічні властивості ( )-[S-(4-хіназоліл)-, (4хіноліл)тіоалкілкарбонових кислот та їх ефірів /C.I. Коваленко, О.А. Бражко, І.А. Мазур та ін. // Фізіологічно активні речовини. -2002. - №2(34). - 15-19; Дослідження антирадикальних властивостей Sкарбоксіалкільних похідних 4-тіохіназоліну в дослідах in vitro у системі утворення оксиду азоту / C.I. Коваленко, І.Ф. Бєленічев, О.В. Карпенко та ін. // Ліки. - 2003. - №1-2. - С.68-72], формули: N Одержують наведену сполуку (НКС-153) взаємодією 4-тіохіназоліну з 2-бромбутановою кислотою у водному розчині гідроксиду натрію (еквімолярна концентрація) (схема). Br OH N N O N N O S OH SH Приклад: 1,62г (0,01моль) 4-тіохіназоліну розчиняють у 10мл 1М розчину гідроксиду натрію при нагріванні, до отриманого розчину додають 1,67г (0,01моль) 2-бромбутанової кислоти і реакційну суміш кип'ятять до нейтрального рН середовища. Розчин охолоджують, підкислюють до рН 3-4, утворений осад відфільтровують і сушать. Одержують цільовий продукт з виходом 65-75%. Синтезована сполука - світло-жовта кристалічна речовина з Т.плав. 174-176°С, розчинна у спирті, діоксані, диметилформаміді, лугах, нерозчинна у воді. Для аналізу очищена переосадженням. Знайдено, %: N 11,30; Вирахувано, %: N 11,28. C12H12N2O2S. Будова сполуки НКС-153 також доведена ІЧ-, ПМР-спектрами та масспектрометрично (таблиця). N O S OH Недоліком найближчого аналогу є те, що він також не проявляє гепатопротекторну активність. Таким чином, в основу корисної моделі поставлена задача створення нової біологічно активної сполуки серед похідних 4-тіохіназоліну, що проявляє антиоксидантну, антирадикальну та гепатопротекторну активність. Вирішення даної задачі забезпечує похідне 4тіохіназоліну, а саме 2-(хіназолін-4-ілтіо)бутанова кислота (НКС-153), яка проявляє антиоксидантну, антирадикальну та гепатопротекторну активність, формули: Таблиця Вид дослідження 1НЯМР, (ррm), ІЧ, (см-1) Мас, m/z (a.o.) Результати 2 13.035 (с, 1Н, СООН); 9.004 (с, 1Н, Н xін); 8.133 (д, 2Н, Н5хін); 8,005(м, 2Н,Н7хін-Н8хін); 7.761 (т, 1Н, Н6хін); 4.789 (т, 1Н,S-СН);1.999(м,2Н,СН2)1,067(т,3Н,СН3) 1730-1650 см-1 ( CO), 680-620 см-1 ( СH2-S-.) 249, 215,204,162,129,102,76. ПМР-спектри знімались на спектрофотометрі ядерного магнітного резонансу "Varian VXR-300", розчинник DMSO-D6, внутрішній стандарт - тетраметилсилан. ІЧ-спектри сполук знімалися у таблетках калію броміду (концентрація речовини 1%) на спектрофотометрі Specord M-80 в області 4000500см-1 (умови сканування: щільова програма 3,0, постійна часу - =3с, час сканування 33хв.). Таблетки готувались спільним розтиранням 200мг калію броміду і 2мг досліджуваної сполуки з наступним пресуванням. Мас-спектр зареєстровано на приладі Varian 1200L, іонізація здійснюється електронним ударом (70eV) при прямому введенні зразка. Температура іонного джерела 200°С; нагрівання відбувається від 25°С до 390°С зі швидкістю 300°С/хв. На першому етапі проведений первинний фармакологічний скринінг методами in vitro для оцін ки антиоксидантної активності. Оцінку антиоксидантної (АОА) та антирадикальної (АРА) активності сполук у дослідах in vitro проводили на п'яти моделях ініціювання вільно-радикального окислювання (ВРО): оцінка АОА при ферментативному і неферментативному ініціюванні та оцінка АРА по інгібуванню супероксид-, пероксинітритрадикалу та стабільної форми радикалу дифенілпікрилгідразину (ДФПГ). Перша модель (ферментативне ініціювання) характеризує АОА сполук на всіх етапах розвитку ВРО [Методи оцінки антиоксидантних властивостей фізіологічне активних речовин при ініціюванні вільно-радикальних процесів у дослідах in vitro /Губський Ю.І., Дунаев В.В., Бєленічев І.Ф. та ін.// Метод, реком. - Київ: Державний Фармакологічний центр МОЗ України, 2002. - 26с.]. Вільнорадикальні процеси запускали ферментативним 5 16242 6 шляхом, додаванням нікотинаЧетверту модель - оцінку АРА синтезованих мідаденіндинуклеотидфосфату відновленого сполук оцінювали використовуючи метод in vitro по (НАДФхH+) у гомогенат тканин головного мозку інгібіюванню активних форм NО [Методи оцінки щурів лінії Вістар. АОА визначали спектрофотомеантиоксидантних властивостей фізіологічно активтрично по вмісту біомаркеру ВРО - малонового них речовин при ініціюванні вільно-радикальних діальдегіду (МДА) після його взаємодії з тіобарбіпроцесів у дослідах in vitro / Губський Ю.І., Дунаев туровою кислотою. В.В., Бєленічев І.Ф. та ін. // Метод, реком. - Київ: Друга модель (Fе2+-залежного ВРО) провоДержавний Фармакологічний центр МОЗ України, диться у суспензії яйцевих ліпопротеїдів [Методи 2002. - 26с.]. Індукцію NO здійснювали при дії на оцінки антиоксидантних властивостей фізіологічно проби з нітропрусидом натрію світла від джерела активних речовин при ініціюванні вільнопотужністю 300Вт з довжиною хвилі 425нм. Ефекрадикальних процесів у дослідах in vitro I Губський тивність гальмування утворення NO тестували по Ю.І., Дунаев В.В., Бєленічев І.Ф. та ін.// Метод, інгібіюванню окиснення аскорбінової кислоти. АРА реком. - Київ: Державний Фармакологічний центр виражали у відсотках інгібіювання окиснення аскоМОЗ України, 2002. - 26с.]. Ця модель характерирбату. зує антиоксидантні властивості речовин на кінцеП'яту модель - оцінку АРА синтезованих сповому етапі ВРО, де вільно-радикальні процеси лук у дослідах in vitro проводили по інгібуванню відбуваються неферментативним шляхом. АОА стабільної форми радикалу дифенілпікрилгідразивизначали спектрофотометрично по вмісту біоману (ДФПГ) [Губський Ю.І., Левицький Є.Л. Перекиркеру ВРО - МДА після його взаємодії з тіобарбісно-антиоксидантний механізм регуляції активностуровою кислотою. ті хроматину //Журн. АМН України. - 1997. - Т.3, Третя модель - модель оцінки АРА синтезова№2. - С.275-282]. них сполук по інгібуванню активної форми кисню Дослідження АОА на моделях in vitro при фе(супероксидрадикал), яка моделюється у реакціях рментативному та неферментативному ініціюванні ауто-окислення адреналіну в адренохром у луж- показало (табл. 1), що сполука НН-153 проявляє ному середовищі [Методи оцінки антиоксидантних високу активність, яка перевищує активність етавластивостей фізіологічне активних речовин при лонів порівняння дибунолу та унітіолу на 9,9% і ініціюванні вільно-радикальних процесів у дослі49,4% відповідно. Крім того, НКС-153 виявилась дах in vitro" /Губський Ю.І., Дунаев В.В., Бєленічев більш ефективною у порівнянні з препаратом "ТіоІ.Ф. та ін.// Метод, реком. - Київ: Державний Фартриазолін" на моделі неферментативного ініціюмакологічний центр МОЗ України, 2002. - 26с.].вання ВРО, перевищує активність лікарського преАОА визначали спектрофотометричне) по гальмупарату на 14,35%. ванню утворення супероксидрадикалу досліджуваними речовинами. Таблиця 1 Антиоксидантна активність синтезованих сполук у дослідах in vitro (%) Сполуки* НКС-153 Дибунол -Токоферолу ацетат Тіотриазолін Метіонін Унітіол Ферментативне ініціювання ВРО 35,1 25,2 10,16 Неферментативне ініціювання ВРО 68,0 53,65 16,2 18,6 Примітки: * - дибунол, -токоферолу ацетат, тіотриазолін, метіонін, унітіол, НКС-153 вводили у дозах 10-7 М відповідно моделям ВРО. Одержані результати антирадикальної активості (табл.2). вказують на те, що всі досліджувані сполуки володіють АРА різної тропності до відповідних радикалів. Так, необхідно відмітити, що NC153 у методах in vitro на різних моделях проявляє значну активність, яка перевищує активність еталонного препарату "Тіотриазолін" на моделі інгібування ДФПГ і наближається за силою дії до еталонних препаратів сечовини та N-ацетилцистеїну. 7 16242 8 Таблиця 2 Антирадикальна активність сполук щодо різних видів радикалів (%) Сполука* NKC-153 Дибунол Тіотриазолін Сечовина N-Ацетилцистеїн ДФПГ 21.2 81.9 13.7 інігібування супероксидрадикалу 30.0 35.0 інгібування пероксинітритрадикалу 42.3 62.2 Примітки: * - дибунол, тіотриазолін, сечовину та N-ацетилцистеїн, НКС-153 вводили у дозах 10-7 М відповідно моделям ВРО. тестування сполук у концентрації 10-5М не продемонструвало наявності антиокислювальних властивостей у зазначеної сполуки, а спостерігалося лише незначне зниження швидкості накопичення продуктів ВРО у препаратів порівняння - іонолу та -токоферолу, а тіотриазолін у цій концентрації був неефективний (табл. 3). При тестуванні сполук у концентрації на рівні 10-4М спостерігається тенденція до зниження утворення продуктів окислення за умов НК, АЗП та НЗП (табл. 3). Так, НКС-153 у зазначеній концентрації призводить до зниження швидкості накопичення МДА тільки за умов АЗП та НЗП. Слід зауважити, що за умов даної моделі тіотриазолін впливає на швидкість накопичення продуктів ВРО лише за умов НК та у найвищій концентрації. Наступним етапом досліджень було вивчення АОА сполуки НКС-153 за показниками швидкості накопичення МДА на моделі неініційованого та індукованого ВРО в ізольованих мембранах ендоплазматичного ретикулуму (ЕР) клітин печінки інтактних щурів. Для визначення швидкості накопичення МДА в ізольованих мембранах ендоплазматичного ретикулуму (ЕР) клітин печінки інтактних щурів в НАДФН (НЗП) та аскорбат (АЗП) індукованих системах ВРО, а також у неіндукованому контролі (НК) використовували метод [Губський Ю.І., Левицький Є.Л. Перекисноантиоксидантний механізм регуляції активності хроматину // Журн. АМН України. -1997. - Т.3, №2. - С.275-282]. Вплив НКС-153 на швидкість накопичення продуктів окислення досліджували у концентраціях 10-5-10-3 М у системах НК, АЗП та НЗП. Вибіркове Таблиця 3 Вплив досліджуваних сполук на швидкість накопичення МДА ізольованими мембранами ЕР печінки інтактних щурів (% до контролю) Сполуки, 10-4 М Контроль NC-109 ТХ-27 НКС-153 Дибунол Тіотриазолін -токоферол Примітка. *- р НК 100 104,2 108,46 102,4 58,98* 85,73 52,54* Системи ВРО АЗП 100 105,3 89,29 99,24 30,95* 103,59 40,46* НЗП 100 100,8 90,2 98,50 50,60* 101,21 53,21* 0,05 (по відношенню до контролю). АОА синтезованих сполук також вивчали за умов in vitro на ізольованих фракціях ядерного хроматину (репресованого - РХ та транскрапційно активного - TAX) клітин печінки інтактних та отруєних ТХМ щурів. Для визначення швидкості накопичення МДА у фракціях хроматину в НАДФН (НЗП) та аскорбат (АЗП) індукованих системах ВРО, а також у неіндукованому контролі (НК) використовували наступні методи [Взаємодія нових похідних піридинкарбонових кислот з ізольованими фракціями ядерного хроматину клітин печінки інтактних та отруєних тетрахлорметаном щурів / Губський Ю.І., Левицький Є.Л., Горюшко Г.Г. и др. // Совр. пробл. токсикол. - 2002. - №2. - С. 26-33; Левицкий Е.Л., Губский Ю.И. Свободно-радикальные повреждения ядерного генетического аппарата клетки // Укр.биохим.журн. - 1994. - Т.66, №4. - С.18-30] з деякими модифікаціями. Розрахунок проводили за коефіцієнтом молярної екстинкції 1,56х105 М-1см-1. Результати виражали в нмоль/мг білка хроматину. Значення НЗП та АЗП одержували відніманням від сумарної величини значення концентрації МДА в неініційованому контролі. Розраховували також значення чутливої до нагрівання складової НЗП 9 16242 10 шляхом віднімання від сумарної величини НЗП няння при АЗП та конкурувала з ними при НЗП значення активності, що залишається після кип'я(табл. 4). У TAX при НЗП активність виявляють тіння зразків протягом 7 хв. сполуки НКС-153 і препарат порівняння Із результатів досліджень видно (табл. 4), що у токоферол (інгібування ВРО на 16,2%, 18,5%, відрепресованому хроматині інтактних тварин сполуповідно), тоді як інші досліджувані сполуки виявика НКС-153 інгібує майже на 34% швидкість наколись менш ефективними. Проте, НКС-153 поступичення МДА у системі НК, перевищуючи при пається за своєю активністю еталонам порівняння цьому активність еталонних антиоксидантів та у системах НК та АЗП. тіотриазоліну. Важливо відзначити, що сполука НКС-153 перевищувала активність еталонів порівТаблиця 4 Визначення швидкості накопичення МДА у фракціях хроматину печінки інтактних щурів при додаванні досліджуваних сполук у концентрації 10-5 (in vitro, у % до контролю) Показники НЗП НЗП, АЗП НК Контроль 100,00 100,00 100,00 100,00 Дибунол 83,68 87,48 81,94 74,03 НЗП НЗП, АЗП НК 100,00 100,00 100,00 100,00 85,35 82,29 78,12 81,56 У фракції РХ щурів з токсичним ураженням печінки у системі НЗП найбільшу активність проявляють -токоферол і дибунол, але і сполука НКС-153 наближається по швидкості накопичення МДА до тіотриазоліну (табл. 5). При АЗП найбільш РХ Тіотриазолін 81,63 84,79 101,52 81,38 TAX 89,06 89,84 94,15 74,28 -токоферол 86,94 87,09 84,02 78,11 81,65 82,81 100,00 67,01* NKC-153 83,63 82,76 76,17 65,99 83,82 78,13 115,27 84,94 активними виявились дибунол і тіотриазолін (інгібування ВРО на 23,2% і 24,3% відповідно). Сполука НКС-153 виявилась найбільш активною у системі НК ВРО, зменшуючи швидкість накопичення МДА на 18,07% відносно контролю (табл. 5). Таблиця 5 Визначення швидкості накопичення МДА у фракціях хроматину печінки отруєних ТХМ щурів при додаванні досліджуваних сполук у концентрації 10-5 (in vitro, у % до контролю) РХ Показники НЗП НЗП, АЗП НК НЗП НЗП, АЗП НК Контроль 100,00 100,00 100,00 100,00 Дибунол 83,98 85,36 76,82 104,60 100,00 100,00 100,00 100,00 91,28 93,57 69,75 88,39 В скринінгових дослідженнях на моделі in vitro на ізольованих фракціях ядерного хроматину (РХ та TAX) клітин печінки інтактних та отруєних ТХМ щурів показано, що сполука НКС-153 за своєю активністю не поступається тіотриазоліну та дибунолу, а за деякими показниками конкурує з токоферолом. Дослідження гепатопротекторної активності проведені на щурах лінії Вістар масою тіла 200220г, які утримувались на стандартному раціоні віварію. В процесі роботи використано 18 тварин. Тварини були розділені на 6 груп: перша група інтактні тварини, друга група - тварини з токсичним ураженням печінки (контрольна група). Токсичне Тіотриазолін 92,04 93,12 75,71 88,66 TAX 91,87 96,62 73,81 77,94 -токоферол 87,40 88,20 100,11 88,40 92,97 94,54 78,75 76,62 НКС-153 92,62 94,82 96,87 81,93 90,29 92,25 82,39 71,63 ураження печінки (ТУП) викликали шляхом введення 50% масляного розчину тетрахлорметану (ТХМ) у дозі 1мл на 100г маси тіла експериментальних тварин два рази на добу протягом 3 діб. Третя група - тварини з ТУП, яким вводили НКС153, четверта група - тварини з ТУП, яким вводили відомий гепатопротекторний та антиоксидантний препарат "Тіотриазолін" [Тиотриазолин: фармакологические аспекты и клиническое применение. Мазур И.А., Волошин НА., Чекман И.С. и др. - Запорожье-Львов: "НАУТІЛУС!", 2005. - 156с]. Сполука НКС-153 та препарат "Тіотриазолін" вводили у дозах 50мг/кг, внутрішньоочеревинно, за годину перед введенням ТХМ. 11 16242 12 Тварин виводили із експерименту через 24 гокації організму проводили шляхом визначення дини після останнього введення ТХМ під етаміналактивності маркерних ферментів аспарагінамінотнатрієвим наркозом (40 мг/кг). Дослідження функрансферази (АсАТ), аланінамінотрансферази ціонального стану антиоксидантної системи про(АлАТ) та за тимоловою пробою у ГП [Меньшиков водили шляхом визначення активності каталази у В.В. Клинико-лабораторная диагностика. М.: "Меплазмі крові (ПК) та гомогенаті печінки (ГП) [Кородицина", 1986. - 325с]. Результати досліджень підлюк М.А. Способ определения активности каталадавали статистичному аналізу [Державна Фармазы // Лаб. дело. - 1988. - №1. - С.16-19), конценткопея України / ДП "Науково-експертний рації стабільних метаболітів NO (Уразаева А.Х., фармакопейний центр". - 1-е вид. - Харків: "РІРЕГ", Зефиров А.Л. Физиологическая роль оксида азота 2001. - Доповнення 1. - 2004. - 520с]. // Успехи физиол. наук. - 1999. - №30 (1). - С.54-72; При моделюванні експерименту за умов in vivo Monocada S., Palmer R.M., Higgs E.A. Nitric oxyde: нами досліджена виживаємість тварин у різні терphysiology, pathophysiology and pharmacology // міни експерименту. Так, результати показали Pharmacol. Rev. - 1991. - Vol.43. - P.109-142], а (табл. 6), що в групі тварин з ТУП (контрольна грутакож за ступенем окисної модифікації білка па) виживаємість складала 50% на 3 добу експе(OМБ) [Halliwell В. Free Radicals Biology Medicine. рименту. Так, при введенні сполук НКС-153 і тіотOxford Press, 1999. - 248p] як одних з ранніх марриазоліну виживаємість щурів з патологією керів ВРО в організмі. Оцінку ендогенної інтоксискладала 83,3%. Таблиця 6 Виживаємість тварин з ТУП Групи тварин Всього тварин Тварини з ТУП (контроль) Тварини з ТУП + тіотриазолін Тварини з ТУП + НКС-153 6 6 6 Виживаємість експериментутварин на 3 добу Кількість від загального числа %, від загального числа 3 50,0 5 83,33 5 83,33 Проведені біохімічні дослідження показали, що у тварин з ТУП активуються процеси ВРО, зокрема відзначалося підвищення концентрації продуктів взаємодії 2,4-динітрофенілгідразину з карбонільними (274нм) та карбоксильними (363нм) групами у ПК як при спонтанній ОМБ у 2,26 і 1,84 рази відповідно, так і при ініційованій ОМБ у 1,99 і 2,54 рази відносно інтактної групи (табл. 6). Крім того, при ОМБ відбувається інтенсивне утворення низькомолекулярних компонентів ( =254, 272, 280нм) у ПК як при спонтанному, так і ініційованому процесі ВРО у порівнянні з інтактом (табл. 7). Введення тваринам тіотриазоліну та сполуки НКС-153 приводило до достовірного зниження концентрації стабільних метаболітів і ступеня дефрагментації білка у ПК. Найбільш позитивні зміни були у експериментальних групах, що отримували сполуку НКС-153. Так, зазначені сполуки перевищували активність еталону порівняння тіотриазоліну при спонтанному та ініційованому OМБ. Таблиця 7 ОМБ у плазмі крові (од/гр/білка) щурів з ТУП Група тварин Показники 254 нм Спонтанна 272 нм ОМБ 280 нм 254 нм Ініційована 272 нм ОМБ 280 нм Спонтанна 274 нм ОМБ 363 нм Ініційована 274нм ОМБ 363 нм Інтактна 0,063±0,003 0,041 ±0,002 0,035±0,004 0,350±0,009 0,211±0,007 0,163±0,008 0,081 ±0,005 0,067±0,003 0,193 ±0,005 0,080±0,004 Тварини з ТУП (контроль) 0,255±0,01 0,193±0,015 0,158±0,028 0,555±0,024 0,483±0,03 0,415±0,027 0,183±0,009 0,123±0,008 0,384±0,010 0,203±0,009 Тварини з ТУП + НКС-153 0,143±0,005* 0,10±0,002* 0,080±0,004* 0,475±0,004* 0,371±0,005* 0,311±0,008* 0,123±0,007* 0,10±0,006* 0,221±0,009* 0,19±0,007* Тварини з ТУП + тіотриазолін 0,150±0,006* 0,110±0,002* 0,09±0,005* 0,521±0,006* 0,398±0,003* 0,341±0,009* 0,138±0,008* 0,120±0,005* 0,231±0,012 0,188±0,006* Примітка: * - р
ДивитисяДодаткова інформація
Назва патенту англійською2-(quinazoline-4-ylthio)butane acid, which reveals antioxidant, antiradical and hepatoprotector activity.
Автори англійськоюNikitin Vladislav Oleksandrovich, Kovalenko Serhii Ivanovych, Bielenichev Ihor Fedorovych, Hubskyi Yurii Ivanovych, Levytskyi Yevhen Leonidovych, Horiushko Hanna Herasymivna
Назва патенту російською2-(хиназолин-4-илтио)бутановая кислота, которая проявляет антирадикальную, антиоксидантную и гепатопротекторную активность
Автори російськоюНикитин Владислав Александрович, Коваленко Сергей Иванович, Беленичев Игорь Федорович, Губский Юрий Иванович, Левицкий Евгений Леонидович, Горюшко Анна Герасимовна
МПК / Мітки
МПК: C07D 239/72, A61P 39/06, A61P 1/16
Мітки: активність, 2-(хіназолін-4-ілтіо)бутанова, гепатопротекторну, кислота, проявляє, антирадикальну, антиоксидантну
Код посилання
<a href="https://ua.patents.su/8-16242-2-khinazolin-4-iltiobutanova-kislota-shho-proyavlyaeh-antiradikalnu-antioksidantnu-ta-gepatoprotektornu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">2-(хіназолін-4-ілтіо)бутанова кислота, що проявляє антирадикальну, антиоксидантну та гепатопротекторну активність</a>
Попередній патент: Пристрій для розігріву вантажів, що змерзлися, в залізничних вагонах
Наступний патент: Спосіб представлення візуальної інформації рекламного та/або пізнавального характеру
Випадковий патент: П'єзоелектричний двигун