Спосіб одержання заміщених 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1н-ксантен-1-онів
Номер патенту: 77599
Опубліковано: 25.02.2013
Автори: Чебанов Валентин Анатолійович, Афанасіаді Людмила Михайлівна, Ткаченко Володимир Володимирович, Муравйова Олена Олександрівна, Десенко Сергій Михайлович, Руденко Роман Володимирович
Формула / Реферат
Спосіб одержання заміщених 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-онів формули
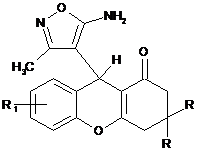 ,
,
де: R=Н, СН3, 4-СlС6Н4
R1=Н, 7-Сl, 7-Br, 7-NO2, 5-OCH3,
який включає конденсацію еквімолярних кількостей 5-аміно-3-метилізоксазолу з R1-заміщеними 2-гідроксибензальдегідами і відповідними R-заміщеними циклогексан-1,3-діонами в розчиннику, після чого цільовий продукт промивають ацетоном, який відрізняється тим, що як розчинник використовують воду, а реакцію конденсації ведуть при температурі 140 °C протягом 5-10 хвилин при мікрохвильовому опроміненні до утворення цільового продукту.
Текст
Реферат: Спосіб одержання заміщених 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1онів формули O NH2 N H H3 C O де: R=Н, СН3, 4-СlС6Н4 R1=Н, 7-Сl, 7-Br, 7-NO2, 5-OCH3, R1 R O R , включає конденсацію еквімолярних кількостей 5-аміно-3-метилізоксазолу з R1-заміщеними 2гідроксибензальдегідами і відповідними R-заміщеними циклогексан-1,3-діонами в розчиннику, після чого цільовий продукт промивають ацетоном. Як розчинник використовують воду, а реакцію конденсації ведуть при температурі 140 °C протягом 5-10 хвилин при мікрохвильовому опроміненні до утворення цільового продукту. UA 77599 U (12) UA 77599 U UA 77599 U Корисна модель належить до галузі хімії і являє собою спосіб одержання заміщених 9-(5аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-онів загальної формули 1. O NH2 N H H3C O де R=Н, СН3, 4-СlС6Н4 R1=Н, 7-Сl, 7-Br, 7-NO2, 5-OCH3. R1 R O 5 10 15 20 25 30 35 1 R , Ці сполуки - складні азотовмісні речовини, що виконують важливу роль у біоенергетиці людського організму. До фармакофорних груп, введення яких у молекули потенційних лікарських препаратів надає їм певної біологічної активності, відносять бензопірановий і ксантиновий цикли. Ці фрагменти входять до складу багатьох природних продуктів з антибактеріальною [К.P. Chitre et al., Orient. J. Chem., 20, 377 (2004)], антиоксидантною [Т.Т. Wei et al., Biochem. Pharm., 66, 83 (2003)], антиалергійною активністю |Eur. Pat. 1273578 (2003)]. Ксантенові похідні мають протизапальну активність [J.P. Poupelin et al., Eur. J. Med. Chem., 13, 67 (1978)], є антагоністами для лікарських стійких ліній лейкемії [Н.Т. Nguyen et al., J. Nat. Prod., 72, 527 (2009)]. Як флуоресцентні матеріали вони використовуються як барвники [Красовицкий Б.М., Болотин Б.М. Органические люминофоры. - М.: Химия, 1984], активних лазерних середовищ [М. Ahmad et al., J. Phys. D: Appl. Phys., 35, 1473 (2002)], флуоресцентних індикаторів [J. Lin et al., Bioorg. Med. Chem. Lett., 11, 2903 (2001)]. Використання таких сполук як біологічно активних речовин потребує постійного удосконалення методів їх одержання, підвищення ступеня чистоти, простоти і доступності синтезу. Крім того, в останні роки особливу увагу в синтетичній органічній хімії приділяють зеленій хімії. Нові схеми хімічних реакцій і процесів, які розробляються в багатьох лабораторіях світу, покликані кардинально скоротити вплив на навколишнє середовище великотоннажних хімічних виробництв. Хімічні ризики, що неминуче виникають при використанні агресивних середовищ, виробничники традиційно намагаються зменшити, обмежуючи контакти працівників з цими речовинами. У той же час, зелена хімія передбачає іншу стратегію - вдумливий відбір вихідних матеріалів і схем процесів, який взагалі виключає використання шкідливих речовин. Таким чином, зелена хімія - це свого роду мистецтво, що дозволяє не просто отримати потрібну речовину, але отримати його таким шляхом, який, в ідеалі, не шкодить навколишньому середовищу на всіх стадіях свого отримання. Послідовне використання принципів зеленої хімії приводить до зниження витрат на виробництво, хоча б тому, що не потрібно вводити стадії знищення і переробки шкідливих побічних продуктів, використаних розчинників та інших відходів, - оскільки їх просто не утворюється. Скорочення числа стадій веде до економії енергії, і це теж позитивно позначається на екологічній та економічній оцінці виробництва. Тому, в останні роки особливу увагу в синтетичній органічній хімії приділяють реакціям, що проходять у водних середовищах. Відомий спосіб одержання структурного аналога сполук формули 1-10,10-диметил-7-феніл10,11-дигідро-7Н-бензо[с]ксантен-8(9Н)-ону формули 2 [Jianjun Li, Lingmei Lu et al., Tetrahedron Lett., 51, 2434-2437 (2010)]. Ph O CH3 O 2 CH3 . Спосіб одержання є одностадійним і здійснюється за схемою: 1 UA 77599 U Ph O O OH пролінтрифлат + Ph O + CH3 O 5 10 15 CH3 . До суміші рівномолярних кількостей 1-нафтолу (1,0 ммоль), бензальдегіду (1,0 ммоль) і 5,5диметилциклогексан-1,3-діону (1,0 ммоль) в 2 мл води додають як каталізатор пролінтрифлат (0,1 ммоль). Суміш кип'ятять 5 годин. Перебіг реакції контролюють тонкошаровою хроматографією. Суміш, що утворилася, екстрагують етилацетатом (3 рази по 10 мл). Органічний шар сушать над безводним натрію сульфатом і випарюють, технічний продукт очищають хроматографічно (елюент - суміш етилацетату і петролейного ефіру 1:10) і одержують 10,10-диметил-7-феніл-10,11-дигідро-7Н-бензо[с]ксантен-8(9Н)-он (безбарвні кристали з т. пл. 155.7-156.9 °C). Вихід 79 %. Недоліками відомого способу одержання сполуки формули 2 є тривалий час технологічного процесу одержання (приблизно 5-9 годин з урахуванням екстракції, випарювання розчинника, хроматографічної очистки суміші над безводним натрію сульфатом), невисокий вихід реакції (79 %), необхідність очистки кінцевого продукту, можливість модифікації хімічної структури лише за варіюванням альдегідної складової. Крім того, використання як каталізатора пролінтрифлату, який не випускається вітчизняною промисловістю і дорого коштує, також можна віднести до недоліків способу одержання сполуки формули 2. Відомий спосіб одержання структурного аналога сполук формули 1-3-заміщених 2-аміно-7,7диметил-5-оксо-4-арил-4,6,7,8-тетрагідро-5Н-хроменів загальної формули 3 [Sunita В. Bandgar et al, Australian J. Chem., 60, 305-307 (2007)1. O Ar де: Ar=C6H5, 4-Cl-C6H4, 4-Br-C6H4, 4-CH3-C6H4 та ін., R=CN, COOEt, CONH2 та ін. R 3 H3C NH2 O H3C , Спосіб одержання сполук формули 3 реалізується за схемою: 20 O O Ar R H2O Ph O + RCH2CN + O 25 30 CH3 O CH3 CH3 H3C CH3 H3C O NH2 . Суміш рівномолярних кількостей ароматичного альдегіду, димедону (5,5диметилциклогексан-1,3-діону) і подвійної кількості відповідного похідного малонової кислоти в 10 мл води нагрівають протягом 1,5-4 годин в залежності від замісника в альдегідній компоненті. Реакцію контролюють тонкошаровою хроматографією. Після охолодження (на льоду) і фільтрації одержують чисті кінцеві продукти з кількісними виходами. В деяких випадках використовують перекристалізацію із етанолу. Недоліком відомого способу одержання сполуки формули 3 є тривалий процес, який потребує великих енерговитрат. Відомий спосіб одержання заміщених 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро1Н-ксантен-1-онів формули 1 [заявка України на винахід № а201205845 від 14.05.12, C07D 311/00]: 2 UA 77599 U O NH2 N O H H3C де R=Н, СН3, 4-СlС6Н4 R1=Н, 7-Сl, 7-Br, 7-NO2, 5-OCH3. R1 R O R 1 , Спосіб одержання сполук формули 1 реалізується за схемою: O NH2 N O OH H3C DMF N O 5 10 15 20 25 30 35 40 R + NH2 O O + O R H H3C R1 R1 R O R . Еквімолярні кількості 5-аміно-3-метилізоксазолу, відповідного Rr заміщеного 2гідроксибензальдегіду і R-заміщеного циклогексан-1,3-діону кип'ятять у диметилформаміді протягом 2-3 хвилин. Охолоджену масу розбавляють ацетоном, відфільтровують осад, промивають ацетоном, сушать. Виходи продукту становлять 50-63 %. Недоліком відомого способу одержання сполуки формули 1 є низькі виходи реакції. Останній з наведених аналогів за кількістю загальних ознак вибраний як прототип. В основу корисної моделі поставлено задачу розробки простого способу одержання заміщених 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-онів, в якому за рахунок зміни умов проведення синтезу можна спростити процес і значно збільшити вихід кінцевого продукту. Рішення поставленої задачі забезпечується тим, що у способі одержання заміщених 9-(5аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1H-ксантен-1-онів, що включає конденсацію еквімолярних кількостей 5-аміно-3-метилізоксазолу з відповідними R-заміщеними циклогексан1,3-діонами і R1-заміщеними 2-гідроксибензальдегідами в розчиннику, після чого цільовий продукт промивають ацетоном, згідно з корисною моделлю, як розчинник використовують воду, а реакцію конденсації ведуть при температурі 140 °C протягом 5-10 хвилин при мікрохвильовому опроміненні до утворення цільового продукту. Хімічну структуру сполук формули 1 за цим способом легко модифікувати, використовуючи різні заміщені 2-гідроксибензальдегіду і циклогексан-1,3-діону. Це дає можливість розширювати асортимент перспективних речовин даної структури з різною біологічною активністю. Вибір компонентів реакції конденсації і розчинника для реакції (води) дозволяє здійснити однореакторний, багатокомпонентний синтез в одну стадію протягом 5-10 хвилин у мікрохвильовому реакторі. За способом, що заявляється, заміщені 9-(5-аміно-3-метилізоксазол4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1-онів одержують в реакції, що не каталізується, з високими виходами. Проведення реакції при мікрохвильовому опроміненні забезпечує високу швидкість її протікання без застосування каталізаторів, що приводить до мінімальної тривалості (5-10 хвилин) одностадійного технологічного процесу у порівнянні з умовами синтезу відомих структурних аналогів. Це дозволяє при необхідності швидко розробити методику синтезу таких сполук в умовах промислового мікрохвильового реактора. Проведення реакції конденсації менше 5 хвилин є недоцільним, оскільки залишаються вихідні реагенти, що не прореагували, а більше 10 хвилин приводить до невиправдано великих енерговиграт. Експериментальним варіюванням температурного режиму реакції було встановлено, що температура 140 °C в умовах закритого мікрохвильового реактора є оптимальною, при якій цільові продукти можна одержувати з високими виходами. Усі сполуки, що одержані за 1 способом, який заявляється, ідентифіковано за допомогою H ЯМР-спектроскопії. У таблиці 1 дано порівняльні характеристики способу, що заявляється, і способів одержання відомих аналогів. У таблиці 2 наведено характеристики деяких основних продуктів реакції, які одержано за способом, що заявляється. 3 UA 77599 U Спосіб, що заявляється, здійснюється за схемою: O NH2 N O H3C + N O 5 10 15 20 25 30 35 40 45 50 O NH2 R O R + R1 H2O MW 140 0C OH H H3C O R1 R O R . Суміш 0,01 моль R-заміщеного циклогексан-1,3-діону, 0,01 моль R1-заміщеного 2гідроксибензальдегіду і 0,01 моль 5-аміно-3-метилізоксазолу суспендують у 5 мл води і нагрівають при 140 °C у закритій посудині у мікрохвильовому реакторі при перемішуванні протягом 5-10 хвилин. Після охолодження осад, що випав, відфільтровують, сушать. Нижче наведено приклади конкретного виконання. Приклад 1. Одержання 9-(5-аміно-3-метилізоксазол-4-іл)-7-бромо-3,3-диметил-2,3,4,9тетрагідро-1 Н-ксантен-1-ону. Суміш 0,98 г (0,01 моль) 5-аміно-3-метилізоксазолу, 1,40 г (0.01 моль) 5,5диметилциклогексан-1,3-діону і 2,01 г (0,01 моль) 2-гідрокси-5-бромобензальдегіду суспендують у 5 мл води і нагрівають при 140 °C у закритій посудині у мікрохвильовому реакторі при перемішуванні протягом 5 хвилин. Реакційну масу охолоджують до кімнатної температури. Осад, що випав, відфільтровують, промивають ацетоном, сушать. Вихід 3,34 г (83 %); т. пл. 222-224 °C. 1 Спектр ЯМР H (ДМС0-d6; δ, м.ч.): 1,00 (с; 3Н), 1,02 (с; 3Н), 1,62 (с; 3Н), 2,24 (дд; 2Н), 2,58 (дд; 2Н), 4,74 (с; 1Н), 6,48 (с; 2Н), 6,7-7,3 (м; 3Н). Приклад 2. Одержання 9-(5-аміно-3-метилізоксазол-4-іл)-7-нітро-2,3,4,9-тетрагідро-1Нксантен-1-ону. Суміш 0,98 г (0,01 моль) 5-аміно-3-метилізоксазолу, 1,12 г (0,01 моль) циклогексан-1,3-діону і 1,67 г (0,01 моль) 2-гідрокси-5-нітробензальдегіду суспендують у 5 мл води і нагрівають при 140 °C у закритій посудині у мікрохвильовому реакторі при перемішуванні протягом 7 хвилин. Реакційну масу охолоджують до кімнатної температури. Осад, що випав, відфільтровують, промивають ацетоном, сушать. Вихід 3,10 г (91 %); т. пл. 214-216 °C. 1 Спектр ЯМР H (ДМСО-d6; δ, м.ч.): 1,63 (с; 311), 1,87 (м; 211), 2,32 (м; 2Н), 2,64 (м; 2Н), 4,73 (с; 1Н), 6,52 (с; 2Н), 6,9-7,5 (м; 3H). Приклад 3. Одержання 9-(5-аміно-3-метилізоксазол-4-іл)-5-метокси-3,3-диметил-2,3,4,9тетрагідро-1Н-ксантен-1-ону. Суміш 0,98 г (0,01 моль) 5-аміно-3-метилізоксазолу, 1,40 г (0,01 моль) 5,5диметилциклогексан-1,3-діону і 1,52 г (0,01 моль) 2-гідрокси-3-метоксибензальдегіду суспендують у 5 мл води і нагрівають при 140 °C у закритій посудині у мікрохвильовому реакторі при перемішуванні протягом 10 хвилин. Реакційну масу охолоджують до кімнатної температури. Осад, що випав, відфільтровують, промивають ацетоном, сушать. Вихід 3,01 г (85 %); т. пл. 210-212 °C. 1 Спектр ЯМР H (ДМСО-d6; δ, м.ч.): 0,99 (с; 3Н). 1,02 (с; 3Н), 1.62 (с; 3Н), 2,21 (дд; 2Н), 2,56 (дд; 2Н), 3,79 (с; 3Н), 4,76 (с; 1Н), 6,36 (с; 2Н), 6,5-7,1 (м; 3Н). Як видно із тексту матеріалів, що заявляються, технічне рішення, що пропонується, має наступні переваги: - тривалість синтезу складає 5-10 хвилин (за аналогом формули 2-5-9 годин, за аналогом формули 3-1,5-4 години); - за запропонованим способом можна одержувати велику кількість сполук, як R-заміщених у положенні 3, так і R1-заміщених у положеннях 5 і 6 ксантенового фрагмента, що дозволяє значно розширити асортимент потенційно біологічно активних речовин; - спосіб, що заявляється, дає можливість синтезувати будь-які кількості кінцевих продуктів, виходячи з відповідних кількостей вихідних речовин; - спосіб, що заявляється, менш енергоємний, ніж способи одержання аналогів 2 і 3. Можливість широкої модифікації структури заміщених 2,3,4,9-тетрагідро-1Н-ксантен-1-онів та синтезу широкого ряду сполук за способом, що заявляється, припускає, що спосіб знайде широке застосування як у лабораторії, так і у виробничій практиці. 4 UA 77599 U Таблиця 1 Розчинник Спосіб, що заявляється Спосіб одержання аналога формули 2 Спосіб одержання аналога формули 3 Спосіб одержання аналога формули 1 вода Умови синтезу MW 140 °C Час реакції Каталізатор 5-10 хвилин не потрібен вода 100 °C 5-9 годин пролінтрифлат вода 100 °C 1.5-4 години не потрібен ДМФА 150 °C 2-3 хвилини не потрібен Таблиця 2 1 № з/п R R1 Т. пл., °C Вихід, % 1 Η 7-Сl 204-206 85 2 Η 5-ОСН3 196-198 88 3 СН3 7-ΝΟ2 223-225 94 4 СН3 Η 185-187 90 Спектр ЯМР H (ДМСО-d6; δ, м.ч.) 1,63 (с; 3Н), 1,87 (м; 2Н), 2,32 (м; 2Н), 2,64 (м; 2Н), 4,73 (с; 1Н), 6,52 (с; 2Н), 6,97,5 (м; 3Н) 1,62 (с; 3Н), 1,85 (м; 2Н), 2,30 (м; 2Н), 2,63 (м; 2Н), 3,80 (с; 33Н), 4,78 (с; 1Н), 6,38 (с; 2Н), 6,8-7,1 (м; 3Н) 1,02 (с; 3Н), 1,05 (с; 3Н), 1,63 (с; 3Н), 2,31 (дд; 2Н), 2,65 (дд; 2Н), 4,90 (с; 1Н), 6,54 (с; 2Н), 7,2-7,8 (м; 3Н) 1,00 (с; 3Н), 1,02 (с; 3Н), 1,63 (с; 3Н), 2,30 (дд; 2Н), 2,62 (дд; 2Н), 4,71 (с; 1Н), 6,46 (с; 2Н), 6,7-7,0 (м; 4H) ФОРМУЛА КОРИСНОЇ МОДЕЛІ 5 Спосіб одержання заміщених 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1Н-ксантен-1онів формули O NH2 N H H3 C O де: R=Н, СН3, 4-СlС6Н4 R1=Н, 7-Сl, 7-Br, 7-NO2, 5-OCH3, R1 R O 10 R , який включає конденсацію еквімолярних кількостей 5-аміно-3-метилізоксазолу з R1-заміщеними 2-гідроксибензальдегідами і відповідними R-заміщеними циклогексан-1,3-діонами в розчиннику, після чого цільовий продукт промивають ацетоном, який відрізняється тим, що як розчинник використовують воду, а реакцію конденсації ведуть при температурі 140 °C протягом 5-10 хвилин при мікрохвильовому опроміненні до утворення цільового продукту. Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of substituted 9-(5-amino-3-methylisoxazol-4-yl)-2,3,4,9-tetrahydro-1h-xantene-1-ones
Автори англійськоюRudenko Roman Volodymyrovych, Muraviova Olena Oleksandrivna, Chebanov Valentyn Anatoliiovych, Desenko Serhii Mykhailovych, Afanasiadi Liudmyla Mykhailivna, Tkachenko Volodymyr Volodymyrovych
Назва патенту російськоюСпособ получения замещенных 9-(5-амино-3-метилизоксазол-4-ил)-2,3,4,9-тетрагидро-1н-ксантен-1-онов
Автори російськоюРуденко Роман Владимирович, Муравьева Алена Александровна, Чебанов Валентин Анатольевич, Десенко Сергей Михайлович, Афанасиади Людмила Михайловна, Ткаченко Владимир Владимирович
МПК / Мітки
МПК: C07D 311/00
Мітки: спосіб, заміщених, одержання, 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1н-ксантен-1-онів
Код посилання
<a href="https://ua.patents.su/7-77599-sposib-oderzhannya-zamishhenikh-9-5-amino-3-metilizoksazol-4-il-2349-tetragidro-1n-ksanten-1-oniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання заміщених 9-(5-аміно-3-метилізоксазол-4-іл)-2,3,4,9-тетрагідро-1н-ксантен-1-онів</a>
Попередній патент: Спосіб виробництва крепованого вбирного паперу санітарно-гігієнічного призначення
Наступний патент: Спосіб визначення кількісного вмісту вірусу інфекційної анемії коней на основі мікрометоду бляшкоутворення
Випадковий патент: Труба дренажна











