Проміжні сполуки для отримання похідних феноксіоцтової кислоти і спосіб їх одержання
Номер патенту: 79498
Опубліковано: 25.06.2007
Автори: Танака Нобуюкі, Мукаяма Харунобу, Кобаясі Дзуніті, Тамаі Тецуро, Ісікава Такехіро, Акахане Сатосі, Харада Хірому
Формула / Реферат
1. Сполука, представлена загальною формулою (І):
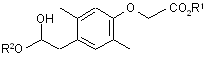 , (I)
, (I)
де кожний з R1 і R2 незалежно являє собою нижчу алкільну групу.
2. Сполука за п. 1, де R1 і R2 являють собою етильну групу.
3. Спосіб отримання сполуки, представленої загальною формулою (І):
 , (I)
, (I)
де кожний з R1 і R2 незалежно являє собою нижчу алкільну групу, при якому проводять стадії:
(a) обробки сполуки формули (II):
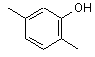 (II)
(II)
сполукою, представленою загальною формулою (III):
 , (III)
, (III)
де R3 являє собою нижчу алкільну групу, з утворенням сполуки, представленої загальною формулою (IV):
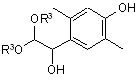 , (IV)
, (IV)
де R3 має вказане вище значення;
(b) обробки вказаної сполуки, представленої загальною формулою (IV), сполукою, представленою загальною формулою (V):
ZCH2CO2R1 , (V)
де Ζ являє собою атом хлору, брому або йоду і R1 має вказане вище значення, з утворенням сполуки, представленої загальною формулою (VI):
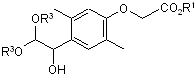 , (VI)
, (VI)
де R1 і R3 мають вказані вище значення;
(c) відновлення вказаної сполуки, представленої загальною формулою (VI), з утворенням сполуки, представленої загальною формулою (VII):
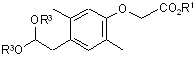 , (VII)
, (VII)
де R1 і R3 мають вказані вище значення;
(d) гідролізу вказаної сполуки, представленої загальною формулою (VII), з утворенням сполуки, представленої загальною формулою (VIII):
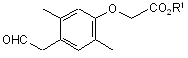 , (VIII)
, (VIII)
де R1 має вказане вище значення; і
(e) обробки вказаної сполуки, представленої загальною формулою (VIII), R2-OН, де R2 має вказане вище значення.
4. Спосіб за п. 3, де R1 і R2 являють собою етильну групу і R3 являє собою метильну групу.
5. Сполука, представлена загальною формулою (IV):
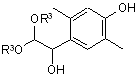 , (IV)
, (IV)
де R3 являє собою нижчу алкільну групу.
6. Сполука за п. 5, де R3 являє собою метильну групу.
7. Сполука, представлена загальною формулою (VI):
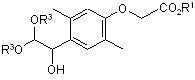 , (VI)
, (VI)
де кожний з R1 і R3 являє собою незалежно нижчу алкільну групу.
8. Сполука, представлена загальною формулою (VII):
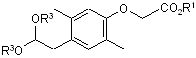 , (VII)
, (VII)
де кожний з R1 і R3 являє собою незалежно нижчу алкільну групу.
9. Сполука за п. 7 або 8, де R1 являє собою етильну групу і R3 являє собою метильну групу.
10. Сполука, представлена загальною формулою (VIII):
 , (VIII)
, (VIII)
де R1 являє собою нижчу алкільну групу.
11. Сполука за п. 10, де R1 являє собою етильну групу.
12. Спосіб отримання сполуки, представленої загальною формулою (X):
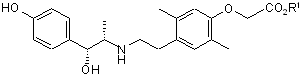 , (X)
, (X)
або її фармацевтично прийнятної солі, де R1 являє собою нижчу алкільну групу, який включає стадію обробки сполуки, представленої загальною формулою (І):
 , (I)
, (I)
де R має вказане вище значення і R2 являє собою нижчу алкільну групу, сполукою, представленою формулою (IX):
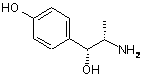 , (IX)
, (IX)
в присутності відновлювального агента і після цього необов'язкового утворення фармацевтично прийнятної солі вказаної сполуки (X).
13. Спосіб за п. 12, де R1 і R2 являють собою етильну групу.
Текст
1. Сполука, представлена загальною формулою (І): O CO2R1 OH (I) 2O R , 3 79498 де R1 має вказане вище значення; і (e) обробки вказаної сполуки, представленої загальною формулою (VIII), R2-OН, де R2 має вказане вище значення. 4. Спосіб за п. 3, де R 1 і R2 являють собою етильну груп у і R3 являє собою метильну груп у. 5. Сполука, представлена загальною формулою (IV): OH OR3 4 CO2 R1 O (VIII) OHC , де R1 являє собою нижчу алкільну гр упу. 11. Сполука за п. 10, де R1 являє собою етильну груп у. 12. Спосіб отримання сполуки, представленої загальною формулою (X): HO O (IV) R3O OH , де R3 являє собою нижчу алкільну гр упу. 6. Сполука за п. 5, де R 3 являє собою метильну груп у. 7. Сполука, представлена загальною формулою (VI): CO2R 1 O OR 3 (VI) R 3O OH , де кожний з R1 і R3 являє собою незалежно нижчу алкільну гр упу. 8. Сполука, представлена загальною формулою (VII): CO2R 1 O OR 3 (VII) R 3O , де кожний з R1 і R3 являє собою незалежно нижчу алкільну гр упу. 9. Сполука за п. 7 або 8, де R 1 являє собою етильну гр уп у і R3 являє собою метильну груп у. 10. Сполука, представлена загальною формулою (VIII): CO2 R1 (X) N H OH , або її фармацевтично прийнятної солі, де R1 являє собою нижчу алкільну груп у, який включає стадію обробки сполуки, представленої загальною формулою (І): O CO2R1 OH (I) R2O , де R має вказане вище значення і R2 являє собою нижчу алкільну гр упу, сполукою, представленою формулою (IX): HO NH 2 (IX) OH , в присутності відновлювального агента і після цього необов'язкового утворення фармацевтично прийнятної солі вказаної сполуки (X). 13. Спосіб за п. 12, де R1 і R2 являють собою етильну груп у. Даний винахід пропонує нові проміжні сполуки для отримання похідного феноксіоцтової кислоти, представленого загальною формулою (X): алкілуючим агентом, представленим загальною формулою (XI): де R1 являє собою нижчу алкільну груп у, або його фармацевтично прийнятних солей, яке володіє рЗ-адренорецептор-стимулюючою активністю і є придатним для лікування або профілактики ожиріння, гіперглікемії, захворювань, викликаних кишковою гіперкінезією, полакіурії, нетримання сечі, депресії або жовчного конкременту. Даний винахід пропонує також спосіб отримання вказаних проміжних продуктів і спосіб використання вказаних проміжних продуктів. В [WO2000/02846] описаний спосіб отримання похідного феноксіоцтової кислоти, представленого загальною формулою (X), який включає стадію обробки аміну загальної формули (IX): де R4 являє собою нижчу алкоксигрупу, R5 і R6 являють собою нижчу алкільну групу, Y являє собою відхідну гр упу, таку як птолуолсульфонілоксигрупу або метансульфонільну гр упу, а том хлору, брому або йоду і тому подібне, в присутності або за відсутності основи. Однак, в [WO2000/02846] не вивчається і не пропонується сполука, представлена загальною формулою (І) даного винаходу. Автори даного винаходу інтенсивно досліджували новий проміжний продукт, який може бути 5 79498 зручним чином і з високим виходом перетворений в похідне феноксіоцтової кислоти загальної формули (X) або його фармацевтично прийнятну сіль, і виявили, що похідне феноксіоцтової кислоти (X) може бути отримане з нової напівацетальної сполуки, представленої загальною формулою (І), з дуже високим виходом. Крім того, авторами даного винаходу виявлений спосіб отримання напівацетальної сполуки (І) з 2,5-ксиленолу за допомогою відповідних процедур. На основі цих відкриттів був досягнутий даний винахід. Отже, даний винахід пропонує: (1) сполуку, представлену загальною формулою (І): де кожний з R1 і R2 незалежно являє собою нижчу алкільну гр упу; (2) сполуку за вищезгаданим пунктом (1), де R1 і R2 являє собою етильну гр упу; (3) спосіб отримання сполуки, представленої загальною формулою (І): де кожний з R і R незалежно являє собою нижчу алкільну гр упу, який включає стадії: (а) обробки сполуки, представленої формулою (II): сполукою, представленою загальною формулою (III): де R3 являє собою нижчу алкільну груп у, з утворенням сполуки, представленої загальною формулою (IV): де R3 має вказане вище значення; (b) обробки вказаної сполуки, представленої загальною формулою (IV), сполукою, представленою загальною формулою (V): де Z являє собою атом хлору, брому або йоду і R1 має вказане вище значення, з утворенням сполуки, представленої загальною формулою (VI): де R1 і R3 мають вказані вище значення; (с) відновлення вказаної сполуки, представленої загальною формулою (VI), з утворенням сполуки, представленої загальною формулою (VII): де R1 і R3 мають вказані вище значення; 6 (d) гідролізу вказаної сполуки, представленої загальною формулою (VII), з утворенням сполуки, представленої загальною формулою (VIII): де R1 має вказане вище значення; і (є) обробки вказаної сполуки, представленої загальною формулою (VIII), R2-ОН, де R2 має вказане вище значення; (4) спосіб за вищезгаданим пунктом (3), де R1 і 2 R являють собою етильну груп у і R3 являє собою метильну груп у; (5) сполуку, представлену загальною формулою (IV): де R3 являє собою нижчу алкільну гр упу; (6) сполуку за вищезгаданим пунктом (5), де R3 являє собою метильну груп у; (7) сполуку, представлену загальною формулою (VI): де кожний з R1 і R3 являє собою незалежно нижчу алкільну групу; (8) сполуку, представлену загальною формулою (VII): де кожний з R1 і R3 являє собою незалежно нижчу алкільну гр упу; (9) сполуку за вищезгаданим пунктом (7) або (8), де R1 являє собою етильну груп у і R 3 являє собою метильну груп у; (10) сполуку, представлену загальною формулою (VIII): де R1 являє собою нижчу алкільну гр упу; (11) сполуку за пунктом 10, де R 1 являє собою етильну груп у; (12) спосіб отримання сполуки, представленої загальною формулою (X): або її фармацевтично прийнятної солі, де R1 являє собою нижчу алкільну групу, який включає стадію обробки сполуки, представленої загальною формулою (І): де R має вказане вище значення і R являє собою нижчу алкільну групу, сполукою, представленою формулою (IX): 7 79498 в присутності відновлювального агента і після цього необов'язкового утворення фармацевтично прийнятної солі вказаної сполуки (X); (13) спосіб за вказаним пунктом (12), де R iR являють собою етильну груп у. У даному винаході термін «нижча алкільна група» відноситься до алкільної групи з нерозгалуженим або розгалуженим ланцюгом, що має від 1 до 6 атомів вуглецю, такої як метильна, етильна, пропільна, ізопропільна, бутильна, ізобутильна, втор-бутильна група і тому подібне. Сполука, представлена загальною формулою (І) даного винаходу, може бути отримана за допомогою стадій від (а) до (є), як показано на наступній схемі. де R1, R2, R3 і Z мають вказані вище значення. (Стадія а) Похідне фенолу, представлене загальною формулою (IV), може бути отримане обробкою 2,5ксиленолу, представленого формулою (II), сполукою, представленою загальною формулою (III), в присутності водного розчину гідроксиду лужного металу, такого як водний розчин гідроксиду натрію. Кількість сполуки (III) і гідроксиду лужного металу звичайно використовують в діапазоні приблизно від 1 до приблизно 3 молярних еквівалентів, рахуючи на 1 моль 2,5-ксиленолу (II). Реакцію звичайно проводять при температурі приблизно від 10 до приблизно 70°С протягом періоду 1-10 годин. Після закінчення реакції реакційний розчин нейтралізують розбавленою кислотою, такою як розбавлена хлористоводнева кислота. Після цього кристали, які осаджуються, фільтрують і сушать, отримуючи при цьому похідне фенолу загальної формули (IV). (Стадія b) Похідне фенолу (IV) обробляють ефіром галогеноцтової кислоти загальної формули (V) в присутності основи в інертному розчиннику, отримуючи при цьому сполуку, представлену загальною формулою (VI). Інертні розчинники, що використовуються в реакції, включають в себе простий ефір, такий як тетрагідрофуран або тому подібне, кетони, такі: як ацетон, метилетилкетон або тому подібне, ацетонітрил, N,N-диметилформамід, N,Nдиметилацетамід або тому подібне. Розчинники можна використати окремо або у вигляді суміші двох або більше за розчинників. Основа, що вико 8 ристовується в реакції, включає в себе карбонат натрію, карбонат калію, карбонат цезію або тому подібне. Ефір галогеноцтової кислоти (V) включає в себе CICH2CO2R1, BrCH2CO2R1 або ICH2CO2R1. Кількість галогеноцтової кислоти (V) і основи використовують звичайно в діапазоні приблизно від 1 до приблизно 5 молярних еквівалентів на основі 1 моля похідного фенолу (IV). Ефір галогеноцтової кислоти (V) і основу звичайно використовують в еквімолярній кількості, але будь-який з них може бути використаний в надлишку. Реакцію звичайно проводять при температурі приблизно від 0 до приблизно 100°С протягом періоду 1-24 годин. Після закінчення реакції, екстракції реакційної суміші і додаткового концентрування звичайними методами отримують сполуку загальної формули (VI). (Стадія с) Відновлення сполуки (VI) з використанням відновлювального агента в інертному розчиннику дає ацетальне похідне, представлене загальною формулою (VII). Інертні розчинники, що використовуються в реакції, включають в себе простий ефір, такий як тетрагідрофуран, 1,2-диметоксіетан, діоксан або тому подібне, ефір органічних карбонових кислот, такий як етилацетат або тому подібне, ацетонітрил або тому подібне. Розчинники можуть бути використані окремо або у вигляді суміші двох або більше розчинників. Відновлювальні агенти, що використовуються в реакції, включають в себе систему йодиду натрію і триалкілхлорсилану, такого як хлортриметилсилан, хлортриетилсилан, трет-бутилдиметилхлорсилан або тому подібне, які звичайно використовують в кількості приблизно від 2 до приблизно 6 молярних еквівалентів, з розрахунку на 1 моль сполуки (VI). Реакцію звичайно проводять при температурі приблизно від -30 до приблизно 30°С протягом періоду від 10 хвилин до 12 годин. Після закінчення реакції, екстракції реакційної суміші і додаткового концентрування звичайними процедурами отримують ацетальне похідне загальної формули (VII). (Стадія d) Гідроліз ацетального похідного (VII) з використанням кислоти у прийнятному розчиннику дає альдегідне похідне, представлене загальною формулою (VIII). Розчинник, що використовується в реакції гідролізу, включає в себе простий ефір, такий як тетрагідрофуран, 1,2-диметоксіетан, діоксан або тому подібне, кетон, такі як ацетон або тому подібне, ацетонітрил або тому подібне. Розчинники можуть бути використані окремо або у вигляді суміші дво х або більше розчинників. Розчинники можуть бути також використані в комбінації з водою. Кислота, що використовується в реакції, включає в себе 5-20% перхлорної кислоти, 110% хлористоводневої кислоти, 1-10% сірчаної кислоти, п-толуолсульфонової кислоти, трифтороцтової кислоти або тому подібне, її звичайно використовують в кількості приблизно від 0,1 до приблизно 2,5 молярних еквівалентів з розрахунку на 1 моль ацетального похідного (VII). Реакцію гідролізу звичайно проводять при температурі приблизно від 0 до приблизно 50°С протягом періоду 0,524 годин. Після закінчення реакції, екстракції реак 9 79498 ційної суміші і додаткового концентрування звичайними процедурами отримують похідне альдегіду (VIII). (Стадія е) Похідне напівацеталю, представлене загальною формулою (І) даного винаходу, може бути отримане обробкою альдегіду (VIII) R2OH, необов'язково в присутності кислоти, такої як оцтова кислота або тому подібне. Реакція приєднання R2OH до похідного альдегіду (VIII) протікає швидко, і подальша кристалізація з прийнятного розчинника дає похідне напівацеталю загальної формули (І). Кількість R2OH звичайно використовують в діапазоні приблизно від 1 до приблизно 10 молярних еквівалентів, з розрахунку на 1 моль альдегіду (VIII). У разі використання кислоти, її звичайно застосовують в кількості приблизно від 0,01 до приблизно 0,1 молярних еквівалентів, з розрахунку на 1 моль альдегіду (VIII). Розчинники для кристалізації включають в себе змішаний розчинник R2OH в комбінації з н-гексаном, н-гептаном, циклогексаном або тому подібне. Похідне напівацеталю (І) виявляє хороші кристалічні властивості і може зберігатися при певній умові, наприклад, при температурі, нижчій за 10°С, протягом тривалого періоду часу. Відповідно до цього, напівацеталь є прийнятним для промислового отримання. Спосіб отримання похідного феноксіоцтової кислоти загальної формули (X), який є застосовним як лікарський засіб, з використанням похідного напівацеталю загальної формули (І) детально описується в наступній схемі. де R1 і R2 мають вказані вище значення. Похідне феноксіоцтової кислоти, представлене загальною формулою (X), може бути отримане обробкою похідного напівацеталю загальної формули (І) аміном формули (IX) в присутності відновлювального агента в інертному розчиннику. Інертні розчинники, що використовуються в реакції, включають в себе простий ефір, такий як тетрагідрофуран, 1,2-диметоксіетан, діоксан або тому подібне, галогеновані вуглеводні, такі як метиленхлорид, 1,2-дихлоретан або тому подібне, органічні карбонові кислоти, такі як оцтова кислота або тому подібне, вуглеводні, такі як толуол або тому подібне, спирти, такі як метанол, етанол або тому подібне, ацетонітрил або тому подібне. Розчинники можуть бути використані окремо або у вигляді суміші двох або більше розчинників. Відновлювальні агенти, що використовуються в реакції, включають в себе гідроборани лужних металів, такі як NaBH4, NaBH3CN, NaBH(OAc)3, NaBH(OMe)3 або тому подібне, борани, такі як ВН3•піридин, ВН3•N,Nдіетиланілін або тому подібне. Якщо необхідно, ці відновлювальні агенти можуть бути використані необов'язково в присутності кислоти, такої як оцтова кислота, п-толуолсульфонова кислота, метансульфонова кислота, сірчана кислота, хлористоводнева кислота, або основи, такої як триетиламін або тому подібне. У альтернативному випадку, реакція може бути проведена в атмосфері водню в 10 присутності металевого каталізатора, такого як 510% паладій на вугіллі, нікель Ренея, оксид платини, паладієва чернь, 10% платина на вугіллі (сульфурована) або тому подібне. У разі використання гідроборанів лужних металів або боранів як відновлювального агенту, такий відновлювальний агент використовують звичайно в діапазоні приблизно від 0,5 до приблизно 5 молярних еквівалентів з розрахунку на 1 моль похідного напівацеталю (І). Реакцію проводять звичайно при температурі приблизно від 0 до приблизно 60°С протягом періоду 1-48 годин. Після закінчення реакції, якщо потрібно, нерозчинні матеріали відфільтровують і реакційну суміш екстрагують і додатково концентрують звичайними процедурами, отримуючи при цьому похідне феноксіоцтової кислоти загальної формули (X). У альтернативному випадку, реакція може бути проведена обробкою аміну (IX) альдегідом загальної формули (VIII) замість похідного напівацеталю (І). Похідне феноксіоцтової кислоти (X) може бути необов'язково перетворене в його фармацевтично прийнятну кислотно-адитивну сіль загальноприйнятими способами. Приклади таких солей включають в себе кислотно-адитивні солі, утворені з мінеральними кислотами, такими як хлористоводнева кислота, бромистоводнева кислота, йодистоводнева кислота, сірчана кислота, фосфорна кислота і тому подібне; кислотно-адитивні солі, утворені з органічними кислотами, такими як мурашина кислота, оцтова кислота, метансульфонова кислота, бензолсульфонова кислота, птолуолсульфонова кислота, пропіонова кислота, лимонна кислота, янтарна кислота, винна кислота, фумарова кислота, масляна кислота, щавлева кислота, малонова кислота, малеїнова кислота, молочна кислота, яблучна кислота, вугільна кислота, глутамінова кислота, аспарагінова кислота і тому подібне. Амін, представлений формулою (IX), може бути отриманий розділенням на оптичні ізомери комерційно доступної енантіомерної суміші аміну загальноприйнятими способами. У альтернативному випадку амін (IX) може бути отриманий методами, що описуються в [J. Med. Chem., 1997, 20 (7), p. 978-981]. Сполука, представлена загальною формулою (І) даного винаходу, її напівпродукти синтезу (IV), (VI), (VII) і (VIII), а також похідне феноксіоцтової кислоти загальної формули (X) можуть бути необов'язково виділені або очищені за допомогою стандартних способів виділення або очищення, таких як екстракція розчинником, перекристалізація, хроматографія і тому подібне. Приклади Наступні приклади ілюструють винахід більш детально. Однак, повинно бути зрозуміло, що вони не повинні ніяким чином розглядатися, як обмежуючі об'єм винаходу. Приклад 1 4-(1 -Гідрокси-2,2-диметоксіетил)2,5-диметилфенол Суспензію водного розчину 5,2% гідроксиду натрію (630г), 2,5-ксиленолу (100г), водного розчину 60% диметилацеталю гліоксалю (213г) і води (200г) нагрівають при 55°С протягом 5 годин з пе 11 79498 ремішуванням. Реакційну суміш охолоджують на крижаній бані і до суміші додають послідовно ацетонітрил (90г) і 7,4% хлористоводневу кислоту (380г). Кристали, які осаджуються, фільтрують, отримуючи при цьому 4-(1-гідрокси-2,2диметоксіетил)-2,5-диметилфенол (150г). 1Н ЯМР (ДМСО-d6) d ч/млн: 2,06 (3Н, с), 2,15 (3Н, с), 3,08 (3Н, с), 3,35 (3Н, с), 4,23 (1Н, д, J=6,7Гц), 4,55 (1Н, дд, J=6,7, 4,4Гц), 4,96 (1H, д, J=4, 4Гц), 6,49 (1H, с), 7,03 (1Н, с), 8,96 (1Н, с). Приклад 2 Етил-2-[4-(1-гідрокси-2,2диметоксіетил)-2,5-диметилфенокси]ацетат До N,N-диметилформаміду (81г) додають 4-(1гідрокси-2,2-диметоксіетил)-2,5-диметилфенол (20,0г), карбонат калію (15,8г) і етилхлорацетат (12,4г) при кімнатній температурі при перемішуванні. Суміш перемішують при кімнатній температурі протягом години і потім перемішують при 71 °С протягом 2 годин. Реакційну суміш розбавляють етилацетатом, промивають водою і насиченим розчином солі і сушать над безводним сульфатом натрію. Органічний шар концентрують при зниженому тиску і до залишку додають суміш етилацетату і гексану. Осаджені кристали збирають фільтруванням, отримуючи при цьому етил-2-[4-(1-гідрокси-2,2диметоксіетил)-2,5-диметилфенокси]ацетат (21,3г). 1Н Я МР (CDCl3) d ч/млн: 1,28 (3Н, т, J=7, 1Гц), 2,26 (3Н, с), 2,32 (3Н, с), 2,54 (1H, д, J=2,3Гц), 3,22 (3Н, с), 3,50 (3Н, с), 4,27 (2Н, кв, J=7,1Гц), 4,32 (1Н, д, J=6,6Гц), 4,61 (2Н, с), 4,80 (1Н, дд, J=6,6, 2,3Гц), 6,48 (1H, с), 7,25 (1H, с). Приклад 3 Етил-2-[4-(2,2-диметоксіетил)-2,5-диметилфенокси]ацетат До суспензії йодиду натрію (72г), що перемішується, і хлортриметилсилану (52г) в ацетонітрилі (180г) додають по краплях розчин етил-2-[4-(1гідрокси-2,2-диметоксіетил)-2,5диметилфенокси]ацетату (50г) в ацетонітрилі (80мг) на бані з льодом і сіллю. Суміш перемішують протягом 30 хвилин і потім додають толуол (400мг) і піридин (25мг). Реакційну суміш промивають послідовно водним розчином тіосульфату натрію, водним розчином лимонної кислоти, водним розчином бікарбонату натрію і насиченим розчином солі. Органічний шар сушать над безводним сульфатом натрію і концентрують при зниженому тиску, отримуючи при цьому етил-2-[4-(2,2диметоксіетил)-2, 5-диметилфенокси] ацетат (43 г). 1Н ЯМР (CDCl3) d ч/млн: 1,30 (3Н, т, J=7,1Гц), 2,24 (3Н, с), 2,27 (3Н, с), 2,82 (2Н, д, J=5,6Гц), 3,33 (6Н, с), 4,27 (2Н, кв, J=7,1Гц), 4,47 (1Н, т, J=5,6Гц), 4,60-(2Н, с), 6,50 (1Н, с), 6,97 (1H, с). Приклад 4 Етил-2-[4-(2-формілметил)-2,5-диметилфенокси] ацетат Етил-2-[4-(2,2-диметоксіетил)-2,5-диметилфенокси]ацетат (23,7г) розчиняють в ацетонітрилі (110г) при перемішуванні і додають 10% перхлорну кислоту (120г), потім суміш перемішують протягом години при кімнатній температурі. Реакційну суміш розподіляють між толуолом (190г) і водою (120г). Органічний шар промивають послідовно водою, водним розчином бікарбонату натрію і на 12 сиченим розчином солі і сушать над безводним сульфатом натрію з подальшим концентруванням при зниженому тиску. Після розчинення залишку в етанолі (96г) розчинник видаляють при зниженому тиску. Залишок знов розчиняють етанолом (96 г) і розчинник видаляють при зниженому тиску, отримуючи при цьому етил-2-[4-(2-формілметил)-2,5диметилфенокси] ацетат (20,8 г). 1Н ЯМР (CDCl3) d ч/млн: 1,30 (3Н, т, J=7,1Гц), 2,20, (3Н, с), 2,25 (3Н, с), 3,59 (2Н, д, J=2,4Гц), 4,27 (2Н, кв, J=7,1Гц), 4,62 (2H, с), 6,56 (1Н, с), 6,94 (1H, с), 9,66 (1H, т, J=2,4Гц). Приклад 5 Етил-2-[4-(2-етокси-2-гідроксіетил)-2,5-диметилфенокси]ацетат Етил-2-[4-(2,2-диметоксіетил)-2,5-диметилфенокси]ацетат (43г) розчиняють в ацетонітрилі (190г) при перемішуванні. До розчину, що утворився, додають 10% перхлорну кислоту (216г) і суміш перемішують протягом години при кімнатній температурі. Реакційну суміш розподіляють між толуолом (340г) і водою (200г). Органічний шар промивають послідовно водою, водним розчином бікарбонату натрію і насиченим розчином солі і сушать над безводним сульфатом натрію з подальшим концентруванням при зниженому тиску. Залишок розчиняють в етанолі (180г) і розчинник видаляють при зниженому тиску. Залишок розчиняють гексаном (86г) і етанолом (37г). Після додання затравкових кристалів розчин перемішують при 0-10°С протягом 2 годин. Додають гексан (220г) і суспензію, що утворилася, перемішують при 0-10°С протягом 2 годин. Осаджені кристали фільтрують, отримуючи при цьому етил-2-[4-(2етокси-2-гідроксіетил)-2,5-диметилфенокси]ацетат (21 г). 1H ЯМР (ДМСО-d6) d ч/млн: 1,06 (3Н, т, J=7,0Гц), 1,21 (3Н, т, J=7=1Гц), 2,11 (3Н, с), 2,19 (3Н, с), 2,50-2,80 (2Н, м), 3,20-3,40 (1Н, м), 3,603,70 (1Н, м), 4,16 (2Н, кв, J=7,1Гц), 4,50-4,70 (1H, м), 4,73 (2H, с), 5,98 (1Н, д, J=7,6Гц), 6,59 (1Н, с), 6,93 (1H, с). Приклад 6 Етил-(-)-2-[4-[2-[[(18,2К)-2-гідрокси-2-(4-гідроксифеніл)-1-метилетил]аміно]етил]-2,5-диметилфенокси]ацетат Суспензію етил-2-[4-(2-етокси-2-гідроксіетил)2,5-диметилфенокси]ацетату (5,4г), 10% паладію на вугіллі (50% вологи, 1,4г), (lR,2S)-2-аміно-1-(4гідроксифеніл)пропан-1-олу (3,0г) і тетрагідрофурану (30г) перемішують в атмосфері водню при 40°С протягом 3 годин. Після видалення каталізатора фільтруванням фільтрат концентрують при зниженому тиску. Залишок розчиняють в толуолі і промивають послідовно водою, водним розчином бікарбонату натрію і насиченим розчином солі. Органічний шар сушать над безводним сульфатом натрію і розчинник видаляють при зниженому тиску, отримуючи при цьому етил(-)-2-[4-[2-[[(1S,2R)-2гідрокси-2-(4-гідроксифеніл)-1-метилетил]аміно] етил]-2,5-диметилфенокси]ацетат (7,3г). 1Н ЯМР (CDCl3) d ч/млн: 0,98 (3Н, д, J=6,4Гц), 1,34 (3Н, т, J=7,1Гц), 2,18 (3Н, с), 2,22 (3Н, с), 2,60-3,00 (5Н, м), 4,31 (2Н, кв, J=7,1Гц), 4,49 (1Н, д, J=5,6Гц), 4,62 (2Н, с), 6,41 (1H, с), 6,69 (2Н, д, J=8,5Гц), 6,78 (1H, с), 7,05 (2Н, д, J=8,5Гц). 13 79498 Приклад 7 Гідрохлорид етил-(-)-2-[4-[2-[[(1S,2R)-2гідрокси-2-(4-гідроксифеніл)-1-метилетил]аміно] етил]-2,5-диметилфенокси]ацетату Суспензію етил-2-[4-(2-етокси-2-гідроксіетил)2,5-диметилфенокси]ацетату (68,7г), 10% паладію на вугіллі (50% вологи, 17г), (1R, 2S)-2-аміно-1-(4гідроксифеніл) пропан-1-олу (38,0г) і тетрагідрофурану (380г) перемішують в атмосфері водню при 40°С протягом 5 годин. Після видалення каталізатора фільтруванням, фільтрат концентрують при зниженому тиску. Залишок розчиняють в толуолі і послідовно промивають водою, водним розчином бікарбонату натрію і насиченим розчином солі. Органічний шар суша ть над безводним сульфатом натрію і розчинник видаляють при зниженому тиску. Залишок розчиняють в толуолі (200г) і етанолі (21г) і по краплях додають 20% мас. розчин хлориду водню в етанолі (37,3г). Осаджені кристали фільтрують, отримуючи при цьому гідрохлорид етил-(-)-2-[4-[2-[[(1S,2R)-2-пдрокси-2(4-гідроксифеніл)-1-метилетил]аміно]етил]-2,5 Комп’ютерна в ерстка В. Клюкін 14 диметилфенокси]ацетату (70,2 г). 1Н Я МР (ДМСОd6) d ч/млн: 0,96 (3Н, д, J=6,6Гц), 1,21 (3Н, т, J=7,1Гц), 2,15 (3Н, с), 2,25 (3Н, с), 2,8-3,2 (4Н, м), 4,16 (2Н, кв, J=7,1Гц), 4,76 (2Н, с), 4,9-5,1 (1Н, м), 5,8-6,0 (1H, м), 6,68 (1H, с), 6,76 (2Н, д, J=8,5Гц), 6,96 (1H, с), 7,17 (2Н, д, J=8,5Гц), 8,5-9,0 (2Н, ушир.), 9,41 (1Н, с). За допомогою похідного напівацеталю, представленого загальною формулою (І) даного винаходу, по хідне феноксіоцтової кислоти загальної формули (X) або його фармацевтично прийнятна сіль може бути отримане з комерційно доступного 2,5-ксиленолу з високим виходом і за допомогою відповідних процедур. Отже, вказане похідне напівацеталю (І) є корисним як проміжне для отримання лікарського засобу для лікування або профілактики ожиріння, гіперглікемії, захворювань, викликаних кишковою гіперкінезією, полакіурії, нетримання сечі, депресії або жовчного конкременту. Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюIntermediates for preparation of phenoxy-acetic derivates and processes of their preparation
Назва патенту російськоюПромежуточные соединения для получения производных феноксиуксусной кислоты и способ их получения
МПК / Мітки
МПК: C07C 217/60, C07C 67/31, C07C 69/712, C07C 43/315, C07C 69/736, C07C 43/178
Мітки: кислоти, похідних, отримання, проміжні, сполуки, спосіб, одержання, феноксіоцтової
Код посилання
<a href="https://ua.patents.su/7-79498-promizhni-spoluki-dlya-otrimannya-pokhidnikh-fenoksioctovo-kisloti-i-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Проміжні сполуки для отримання похідних феноксіоцтової кислоти і спосіб їх одержання</a>
Попередній патент: Підшипниковий вузол
Наступний патент: Спосіб електронно-променевого переплаву губчастого активного металу
Випадковий патент: Спосіб лікування пневмонії на тлі лейкозів глутоксимом











