Спосіб отримання спіропохідних 1,2-дифенілпіразолідин-3,5-діонів реакціями метатезису з закриттям циклу
Номер патенту: 94044
Опубліковано: 27.10.2014
Автори: Головатюк Володимир Миколайович, Кашковський Володимир Ілліч, Безуглий Юрій Віталійович
Формула / Реферат
Спосіб отримання спіропохідних 1,2-дифенілпіразолідин-3,5-діонів, який полягає в проведенні реакцій метатезису з закриттям циклу на 4,4-діалкеніл-1,2-дифенілпіразолідин-3,5-діонах, причому реакція проходить за участю 3 мольн. % рутенійвмісного карбенового каталізатора Грабса II в сухому дихлорометані за температури 42 °C протягом 2 годин, що дозволяє одержати спіроалкенільні піразолідиндіони з високими виходами (70-90 %), які можуть бути потенційними біологічно активними речовинами чи напівпродуктами для їх одержання.
Текст
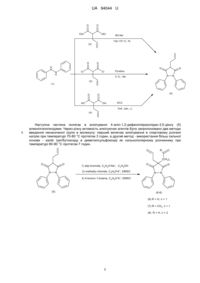
Реферат: Спосіб отримання спіропохідних 1,2-дифенілпіразолідин-3,5-діонів полягає в проведенні реакцій метатезису з закриттям циклу на 4,4-діалкеніл-1,2-дифенілпіразолідин-3,5-діонах. Причому реакція проходить за участю 3 мольн. % рутенійвмісного карбенового каталізатора Грабса II в сухому дихлорометані за температури 42 °C протягом 2 годин, що дозволяє одержати спіроалкенільні піразолідиндіони з високими виходами (70-90 %), які можуть бути потенційними біологічно активними речовинами чи напівпродуктами для їх одержання. UA 94044 U (54) СПОСІБ ОТРИМАННЯ СПІРОПОХІДНИХ 1,2-ДИФЕНІЛПІРАЗОЛІДИН-3,5-ДІОНІВ РЕАКЦІЯМИ МЕТАТЕЗИСУ З ЗАКРИТТЯМ ЦИКЛУ UA 94044 U UA 94044 U 5 10 Корисна модель належить до органічної та металоорганічної хімії, а саме - до способу отримання нових спіропохідних 1,2-дифенілпіразолідин-3,5-діонів, які можуть проявляти біологічну активність і виступати як потенційно активні біологічні та фармацевтичні препарати. Велика кількість сполук, які включають в себе різноманітні фрагменти піразолідин-3,5діонового циклу з різними лінійними замісниками в 4-му положенні - це препарати, що широко застосовуються в медицині, ветеринарії та біології. Наприклад, всесвітньо відомий фармацевтичний препарат "Фенілбутазон" (4-бутил-1,2дифенілпіразолідин-3,5-діон), що є нестероїдним протизапальним препаратом з групи піразолідиндіонів, які мають протизапальну, жаропонижаючу та знеболюючу дію, синтезують конденсацією н-бутилдіетилмалонату з гідразобензеном за наявності алкоголяту натрію в абсолютному спирті [1]. O O N O N N Phenylbutazone 15 20 25 30 35 O N Feprazone Іншим прикладом речовин даного класу може виступати лікарський засіб "Фепразон", який проявляє протизапальні властивості при захворюванні суглобів опорно-рухового апарату та м'язів [2]. Найбільш близькою за будовою до наших об'єктів є така сполука, як 1-фенілпіразолідин-4спіроциклопропан-3,5-діон, що була синтезована конденсацією фенілгідразину з циклопропанмалоновим естером [3]. В той же час слід відмітити, що ненасичені п'яти- і шестичленні спіроциклічні піразолідін-3,5-діонів на сьогоднішній день в літературі не описані, як і не описані методи одержання. Суть корисної моделі полягає в розробці ефективного способу отримання нових спіроциклічних похідних 1,2-дифенілпіразолідин-3,5-діонів за допомогою реакцій метатезису з закриттям циклу. Задача корисної моделі вирішується застосуванням способу синтезу спіропохідних 1,2дифенілпіразолідин-3,5-діонів, що полягає в проведенні реакцій метатезису з закриттям циклу 4,4-діалкеніл-1,2-дифенілпіразолідин-3,5-діонів, причому реакції проходять за участю 3 мольн. % рутенійвмісного карбенового каталізатори Грабса II в сухому дихлорометані за температури 42 °C протягом 2 годин, що дозволяє отримати спіроалкенільні піразолідиндіони з високими виходами (70-90 %), які можуть виступати потенційними біологічно активними речовинами чи напівпродуктами для їх одержання. На першому етапі синтезу одержують алілпіразолідиновий цикл (5) прямою дією діетилового естеру алілмалонової кислоти (2) на гідразобензен (1) в присутності метоксиду чи ізопропоксиду натрію при високій температурі, а також шляхом ацилювання гідразобензену (1) дихлорангідридом алілмалонової кислоти (3) в присутності піридину як м'якої основи, або конденсацією малонової кислоти (4) з вихідним гідразобензеном (1) в присутності водовіднімаючого агента дициклогексилкарбодиіміду. 1 UA 94044 U O O EtO OEt RO-Na+ 130-170 oC, 7h (2) O H N O O Cl N H Cl O Pyridine N 0 oC, 19h N (3) (1) O HO (5) O OH DCC THF, 24h, r.t. (4) 5 Наступна частина полягає в алкілуванні 4-аліл-1,2-дифенілпіразолідин-3,5-діону (5) алкенілгалогенідами. Через різну активність алкілуючих агентів було запропоновано два методи введення ненасиченої групи в молекулу: перший включає алкілування в спиртовому розчині натрію при температурі 70-80 °C протягом 3 годин, а другий метод - використання більш сильної основи - калій третбутоксиду в диметилсульфоксиді як сильнополярному розчиннику при температурі 80-90 °C протягом 7 годин. R (CH2)n O O N N 1) allyl bromide, C2H5O-Na+, C2H5OH 2) methallyi chloride, C4H9O-K+, DMSO 3) 4-bromo-1-butene, C4H9 (5) O-K+, O O N N DMSO (6-8) (6) R = H, n = 1 (7) R = CH3, n = 1 (8) R = H, n = 2 2 UA 94044 U R (CH2)n O O N O 1) allyl bromide, C2H5O-Na+, C2H5OH 2) methallyi chloride, C4H9O-K+, DMSO N 3) 4-bromo-1-butene, C4H9 O-K+, O N N DMSO (5) (6-8) (6) R = H, n = 1 (7) R = CH3, n = 1 (8) R = H, n = 2 5 10 Обидва методи дозволяють отримати діалкенілвмісні піразолідиндіони (6-8) з виходами в межах 70-80 % та використовувати їх в подальшому без додаткової очистки. Спіропохідні піразолідиндіону (9-11) одержують шляхом реакції метатезису з закриттям циклу діалкеніл-1,2-дифенілпіразолідин-3,5-діонів (6-8) на рутенійкарбенових каталізаторах метатезису. В результаті досліджень визначено оптимальний каталізатор та оптимальні умови проведення процесу. Ним виявився рутенійкарбеновий комплекс - 1,3-біс(2,6-диметилфенил)-2імідазолідиніліден)дихлоро(фенілметилен)-(трициклогексилфосфін)рутенію - каталізатор типу Грабса другого покоління (12), а реакція проходить в розчині сухого дихлорометану в атмосфері сухого аргону при температурі 42 °C протягом 2 годин при концентрації каталізатора 3 мольн. %. R R (CH2)n O O N N (CH2)n Grubbs-II O - C2H4 O N (6-8) N (9-11) (9) R = H, n = 1 (10) R = CH3, n = 1 N Cl Cl (11) R = H, n = 2 N Ru Cy3P Grubbs-II generation catalyst (12) 15 Продукти метатезису відділяють від каталізатора методом колонкової хроматографії та ідентифікують за допомогою методу ядерного магнітного резонансу на ядрах Гідрогену. Корисна модель пояснюється декількома прикладами. 3 UA 94044 U 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 1. Одержання 4-аліл-1,2-дифенілпіразолідин-3,5-діону (5) амінолізом гідразобензену (1) алілдіетилмалонатом (2). Попередньо приготовлений розчин 1,2 г (52,5 ммоль) натрію в 40 мл абсолютного метанолу поміщають в суху ампулу на 100 мл, після чого додають 5,4 г (27,1 ммоль) алілдіетилмалонату (2) і 5 г (27,1 ммоль) гідразобензену (1). Ампулу запаюють і нагрівають на масляній бані 7 годин, поступово підвищуючи температуру від 130 до 170 °C. Дану температуру витримують ще 2 години, реакційну масу виливають в воду, екстрагують 2 рази діетиловим етером і, відділивши етерний шар, підкислюють водний залишок 10 % розчином соляної кислоти до слабокислого середовища. Кристали продукту, що випали, відфільтровують, промивають до нейтральної реакції та перекристалізовують з етанолу. Речовина являє собою білі кристали масою 5,1 г (64,8 %). Т. пл=130-132 °C. Приклад 2. Одержання 4-аліл-1,2-дифенілпіразолідин-3,5-діону (5) ацилюванням гідразобензену (1) дихлороангідридом алілмалонової кислоти (3). До охолодженого до 0 °C розчину 5 г (27,1 ммоль) гідразобензену (1) в 40 мл сухого дихлорометану додають 4,7 мл абсолютного піридину, після чого при інтенсивному перемішуванні повільно прикапують 4,9 г (27,1 ммоль) дихлороангідрид алілмалонової кислоти (3) з такою швидкістю, щоб температура реакційної маси не перевищувала 5 °C. Перемішування продовжують протягом 12 годин за нормальних умов, після чого суміш висаджують п'ятикратною кількістю підкисленої води, а осад, що випав, відфільтровують, промивають холодною водою та перекристалізовують з етилового спирту. Вихід продукту складає 6,7 г (85 %). Приклад 3. Одержання 4-аліл-1,2-дифенілпіразолідин-3,5-діону (5) конденсацією гідразобензену (1) з алілмалоновою кислотою (4) за допомогою водовіднімаючого агенту. До охолодженого до 0 °C розчину 5 г (27,1ммоль) гідразобензену (1) та 3,88 г (27,1 ммоль) алілмалонової кислоти (4) в 50 мл сухого дихлорометану при перемішуванні додають порціями 11,2 г (54,2 ммоль) дициклогексилкарбодііміду, підтримуючи температуру в межах 5-10 °C, після чого залишають на ніч. На наступний день дициклогексилсечовину відфільтровують, маточний розчин упарюють при низькому тиску і залишок кристалізують з етанолу. Вихід продукту складає 6,3 г (79 %). Приклад 4. Синтез 4,4-діаліл-1,2-дифенілпіразолідин-3,5-діону (6). 0,4 г (1,7 ммоль) металічного натрію розчиняють в 10 мл абсолютного етанолу, після чого додають 0,5 г (1,7 ммоль) 4-аліл-1,2-дифенілпіразолідин-3,5-діону (5), 10 хвилин перемішують за кімнатної температури та додають 0,2 мл (2,3 ммоль) алілброміду. Після 30 хвилин перемішування реакційну масу кип'ятять 2 години, натрій бромід відфільтровують, спирт упарюють та отриманий маслоподібний продукт подають в подальшу реакцію метатезису без додаткової очистки. Вихід продукту (6) становить 0,51 г (91 %). Приклад 5. Синтез 4-аліл-4(2-метилпроп-2-ен-1-іл)-1,2-дифенілпіразолідин-3,5-діону (7). 0,5 г (1,7 ммоль) 4-аліл-1,2-дифенілпіразолідин-3,5-діону (5) розчиняють в 5 мл абсолютного диметилсульфоксиду, додають 0,2 г (1,7 ммоль) калій третбутоксиду, перемішують при 50 °C 20 хвилин і додають 0,2 мл (2,2 ммоль) 2-метил-3-хлор-1-пропену (металілхлорид). Піднімають температуру до 70 °C і при перемішуванні ведуть синтез протягом 8 годин. Далі реакційну масу висаджують водою, екстрагують 2 рази етилацетатом, органічну фазу сушать над безводним сульфатом натрію, відфільтровують, упарюють при пониженому тиску і залишковий маслоподібний продукт подають далі в реакцію метатезису з закриттям циклу. Вихід продукту (7) становить 0,49 г (84 %). Приклад 6. Синтез 4-аліл-4-бут-3-ен-1-іл-1,2-дифенілпіразолідин-3,5-діону (8). До розчину 0,5 г (1,7 ммоль) 4-аліл-1,2-піразолідин-3,5-діону (5) в абсолютному диметил сульфоксиді (4 мл) додають 0,2 г (1,7 ммоль) калій третбутоксиду та перемішують при 50 °C 20 хвилин. Далі, додавши 0,22 мл (2,2 ммоль) 4-бром-1-бутену, ведуть синтез при 70 °C протягом 17 годин. Виділення продукту реакції проводять аналогічно прикладу 5. Вихід продукту (8) становить 0,45 г (77 %). Приклад 7. Одержання 2,3-дифеніл-2,3-діазоспіро[4,4]нон-7-ен-1,4-діону (9) реакцією метатезису із закриттям циклу. В колбу Шленка поміщають 0,5г (1,5 ммоль) вихідного 4,4-діаліл-1,2-дифеніл-піразолідин3,5-діона (6), потім розчиняють в 10 мл сухого дихлорометану, насичують систему сухим аргоном та додають 37 мг (0,045 ммоль) каталізатора Грабса II (12), після чого реакцію проводять при 42 °C протягом 2 годин. Далі розчинник упарюють і продукт метатезису очищують методом колонкової хроматографії на носії силікагелі в системі дихлорометангексан (1:1). Після упарювання розчинників маслоподібний залишок затирають з гексану. Отримують білу кристалічну речовину з виходом 0,41г (91 %). 4 UA 94044 U 5 10 15 20 25 30 (H)NMR 1Н (400 МГц CDCl3) 3.04 (4Н, с), 5.74 (2Н, с), 7.19 (2Н, т), 7,32-7,35 (8Н, м). Приклад 8. Синтез 7-метил-2,3-дифеніл-2,3-діазоспіро[4,4]нон-7-ен-1,4-діону (10) реакцією метатезису із закриттям циклу. Розчин 0,52 г (1,5 ммоль) 4-аліл-4(2-метилпроп-2-ен-1-іл)-1,2-дифенілпіразолідин-3,5-діону (7) в 10 мл сухого дихлорометану в колбі Шленка продувають сухим аргоном і, додавши 0,045 ммоль (3 мольн. %) каталізатора Грабса II (12), кип'ятять реакційну суміш 2 години. Далі після упарювання розчинника продукт був виділений аналогічно прикладу 7. Маса продукту складає 0,38 г, що відповідає виходу 79,6 % від теоретичного. (H)NMR 1Н (400 МГц CDCl3) 1.79 (ЗН, с), 2.91 (2Н, с), 2.99 (2Н, с), 5,33 (1Н, м) 7.18 (2Н, т), 7.27-7.33 (8Н, м). Приклад 9. Одержання 2,3-дифеніл-2,3-діазоспіро[4,5]дек-7-ен-1,4-діону (11) реакцією метатезису із закриттям циклу. 0,52 г (1,5 ммоль) 4-аліл-4-бут-3-ен-1-іл-1,2-дифенілпіразолідин-3,5-діону (8) розчиняють в колбі Шленка в 10 мл дихлорометану, після чого додають 3 мольн. % каталізатора Грабса II (12) і проводять реакцію в інертній атмосфері при 42 °C протягом 2 годин. Виділення продукту реакції аналогічно прикладу 7. Вихід продукту реакції 0,34 г (71,2 %). (H)NMR 1Н (400 МГц CDCl3) 2.06 (2Н, м), 2.39 (2Н, т), 2.50 (2Н, д), 5,33 (1H, м) 5.76 (1Н, т), 5,92 (1Н, т), 7.18 (2Н, т), 7.30-7.36 (8Н, м). Таким чином, синтезовано нові ненасичені спіроциклічні похідні піразолідиндіонів реакціями метатезису із закриттям циклу на рутенійкарбеновому каталізаторі Грабса другого покоління, які можуть виступати як потенційні біологічно активні речовини чи напівпродукти для їх одержання. Згідно з даними комп'ютерного аналізу, проведеного програмою Prediction of Activity Spectra for Substances, одержані сполуки з високою ймовірністю можуть бути інгібіторами L-глутамат оксидази, інгібіторами тестостерон-17бета-дегідрогенази (НАДФ+), антагоністами нікотин альфа2бета2 рецептора, протизапальними засобами. Джерела інформації: 1. Рубцов М.В., Байчиков А.Г. Синтетические химико-фармацевтические препараты. - М., 1971. - С. 162. 2. Toxicology and applied pharmacology, (1982), 64 (2), 255-270. 3. J. Chem. Soc, Perkin Trans. 1, 1990, № 11, p. 3137-3144. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 35 Спосіб отримання спіропохідних 1,2-дифенілпіразолідин-3,5-діонів, який полягає в проведенні реакцій метатезису з закриттям циклу на 4,4-діалкеніл-1,2-дифенілпіразолідин-3,5-діонах, причому реакція проходить за участю 3 мольн. % рутенійвмісного карбенового каталізатора Грабса II в сухому дихлорометані за температури 42 °C протягом 2 годин, що дозволяє одержати спіроалкенільні піразолідиндіони з високими виходами (70-90 %), які можуть бути потенційними біологічно активними речовинами чи напівпродуктами для їх одержання. 40 Комп’ютерна верстка І. Мироненко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
Автори англійськоюBezuhlyi Yurii Vitaliiovych, Kashkovskii Volodymyr Illich
Автори російськоюБезуглый Юрий Витальевич, Кашковский Владимир Ильич
МПК / Мітки
МПК: C07D 231/04
Мітки: циклу, отримання, спосіб, 1,2-дифенілпіразолідин-3,5-діонів, реакціями, спіропохідних, закриттям, метатезису
Код посилання
<a href="https://ua.patents.su/7-94044-sposib-otrimannya-spiropokhidnikh-12-difenilpirazolidin-35-dioniv-reakciyami-metatezisu-z-zakrittyam-ciklu.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання спіропохідних 1,2-дифенілпіразолідин-3,5-діонів реакціями метатезису з закриттям циклу</a>
Попередній патент: Спосіб випробування гасника коливань
Наступний патент: Головка для формування регулярних мікрорельєфів вібраційним обкочуванням
Випадковий патент: Спосіб діагностики холедохолітіазу