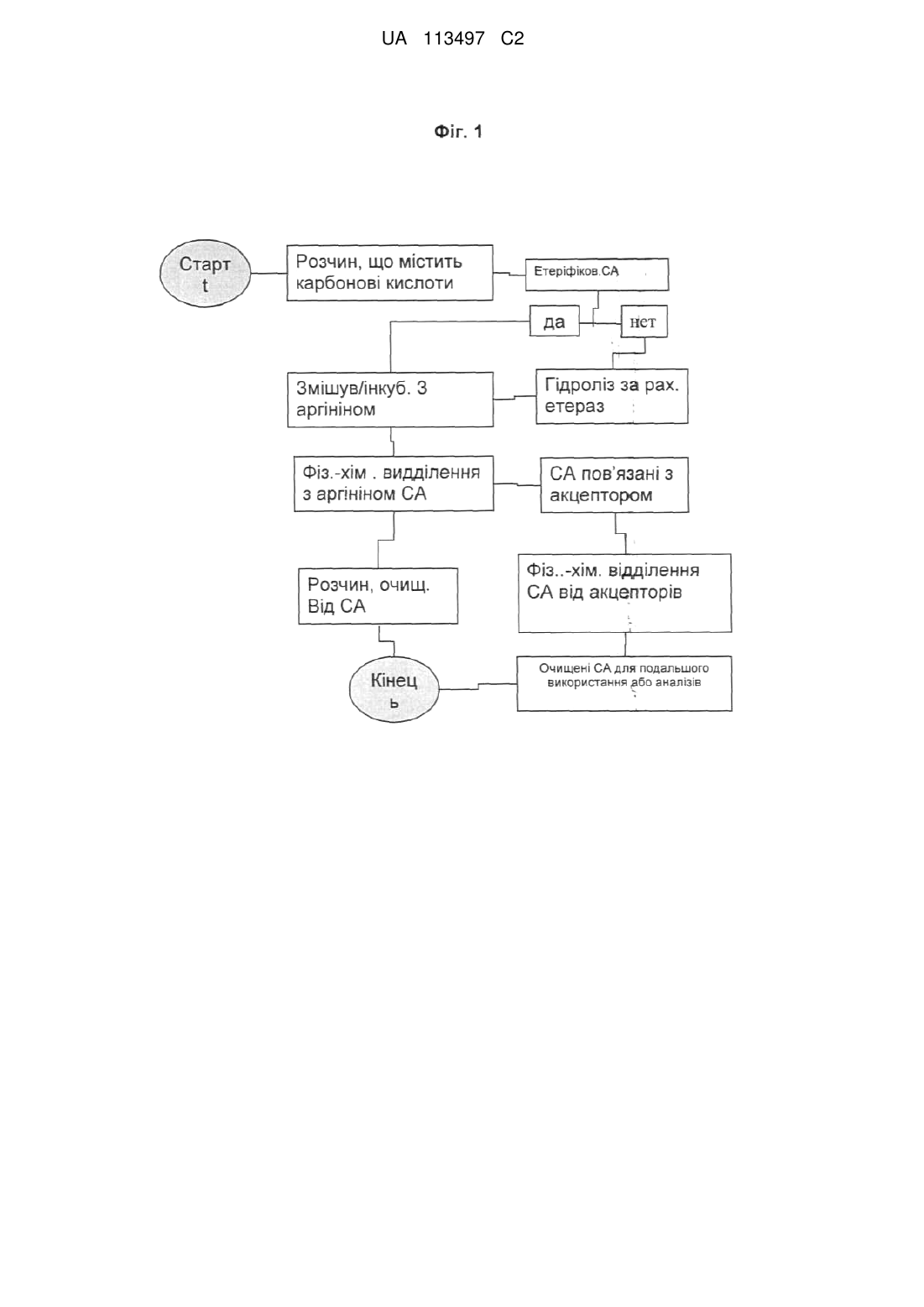
Спосіб солюбілізації і виділення карбонових кислот з використанням солюбілізуючих сполук
Формула / Реферат
1. Спосіб солюбілізації і видалення карбонових кислот з використанням солюбілізуючих сполук з водних або органічних середовищ, емульсій, суспензій, що утворюються при лікарській терапії, в аналітичних методах медицини, в аналітичних методах харчової промисловості, при промисловій переробці продуктів харчування, при промисловій переробці олій, при аналізах олій, при промисловій переробці палива, при модифікації хімічних і фізико-хімічних реакцій, для солюбілізації погано розчинних молекул, в аналітичних методах фармацевтичної чи хімічної промисловості або науки, для видалення карбонових кислот із стічних вод після приватних, комерційних чи промислових чисток, для видалення карбонових кислот з біореакторних процесів, при органожелюванні або наноемульсифікації карбонових кислот, де зазначена солюбілізуюча сполука містить щонайменше одну амідиногрупу і/або щонайменше одну гуанідиногрупу і де солюбілізуюча сполука має коефіцієнт розділення суміші н-октанол-вода KOW < 6,30, причому застосування зазначеної солюбілізуючої сполуки призводить до мікро- або наноемульсії із зазначених карбонових кислот і забезпечує їх розділення за допомогою комплексоутворення, адсорбції, абсорбції, дифузії, осмосу, діалізу, фільтрації, нанофільтрації, перегонки, флюїдної екстракції рідини або надкритичної флюїдної екстракції, використовуючи градієнт концентрації, термічний градієнт, електричний градієнт, фізико-хімічний градієнт або їх комбінації, і де вказаний спосіб включає наступні стадії:
і) одержання розчину або емульсії, або суспензії, що містять карбонові кислоти;
іі) додавання щонайменше еквімолярних кількостей щонайменше однієї солюбілізуючої сполуки;
ііі) виділення солюбілізованих карбонових кислот з розчину або емульсії, або суспензії шляхом фазового розділення, фільтрації, нанофільтрації, діалізу, абсорбції, комплексоутворення, електрофорезу, випаровування, дистиляції та/або екстракції.
2. Спосіб за п. 1, де стадію ііі) здійснюють, використовуючи один з наступних способів виділення або їх комбінації: проходження карбонових кислот роздільно або разом з щонайменше однією солюбілізуючою сполукою через розділову мембрану або трубку, або порожнистий капілярний блок під дією концентраційного градієнта, термічного градієнта, фізико-хімічного градієнта, пневматичного градієнта, електричного градієнта або їх комбінації; або здійснення фазового розділення шляхом комбінування двох або більше середовищ, що забезпечують фазовий поділ; або проходження карбонових кислот разом з щонайменше однією солюбілізуючою сполукою через поверхню розділу фаз, що забезпечує проходження зазначених карбонових кислот та зазначеної щонайменше однієї солюбілізуючої сполуки за рахунок створення концентраційного градієнта, термічного градієнта, фізико-хімічного градієнта, пневматичного градієнта, електричного градієнта або їх комбінації, де поверхня розділу фаз складається з гелю, органогелю або твердого матеріалу, або їх комбінації; або фільтрації карбонових кислот, використовуючи щонайменше одну солюбілізуючу сполуку; або нанофільтрації карбонових кислот, використовуючи щонайменше одну солюбілізуючу сполуку; або діалізу карбонових кислот, використовуючи щонайменше одну солюбілізуючу сполуку; або адсорбції карбонових кислот, використовуючи щонайменше одну солюбілізуючу сполуку; або комплексоутворення карбонових кислот, використовуючи щонайменше одну солюбілізуючу сполуку; або дистиляції карбонових кислот, використовуючи щонайменше одну солюбілізуючу сполуку; або виділення карбонових кислот, використовуючи щонайменше одну солюбілізуючу сполуку, шляхом надкритичної рідинної екстракції.
3. Спосіб за п. 1, що включає наступні стадії:
а) одержання зазначеного розчину шляхом зменшення іонної сили, використовуючи комплексоутворення, адсорбцію, виділення або діаліз пов'язаних або непов'язаних катіонів та аніонів;
b) коригування значення рН розчину шляхом додавання кислоти або основи;
с1) коригування молярності солюбілізуючої сполуки таким чином, щоб вона була в інтервалі від 1:10 до 20:1 по відношенню до розрахункової концентрації карбонових кислот, що підлягають солюбілізації; та
d) додавання вказаної солюбілізуючої сполуки у твердій формі або в розчині до зазначеного водного або органічного розчину, що містить карбонові кислоти для утворення мікро- або наноемульсії;
необов'язково включає будь-яку зі стадій:
а1) вивільнення карбонових кислот, пов'язаних за допомогою комплексоутворення або ковалентного зв'язування
с2) якщо солюбілізуючу сполуку вводять в розчин, то коригування значення рН зазначеного розчину з метою оптимізації сумісності та умов реакції з карбоновими кислотами, що підлягають солюбілізації, використовуючи підкислення або підлуження;
е) додавання естераз, гідролаз або комплексоутворюючого агента;
f) додавання до розчину води та/або співрозчинника; та/або
g) оптимізація умов реакції шляхом нагрівання та/або змішування розчину, в результаті чого утворюється або поліпшується мікро- або наноемульсія.
4. Спосіб за п. 3, що включає додаткові стадії після стадії g):
g2) подачу реакційного розчину з першої камери в другу камеру першого діалізатора через розділову панель, використовуючи спосіб нанофільтрації, за рахунок створення концентраційного градієнта, хімічного градієнта, пневматичного градієнта, електричного градієнта або їх комбінацій;
необов'язково включає стадії:
h) видалення асоціатів карбонової кислоти та солюбілізуючої сполуки з фільтраційного розчину за рахунок конвекції акцепторного розчину, що подається через вхідний отвір у вказану другу камеру і надання можливості витікати через вихідний отвір зазначеної другої камери; та
і) видалення очищеного розчину з вказаної другої камери через наступний випускний отвір.
5. Спосіб за п. 3, де водний розчин являє собою ех vivo зразок крові суб'єкта, з крові якого необхідно видалити мікро- та/або наноемульсії жирних кислот, додатково включає наступні стадії g1) - m) після стадії g):
g1) вивільнення етерифікованих жирних кислот у крові суб'єкта, використовуючи гідролази, іммобілізовані на матеріалі підкладки всередині першої камери, в результаті чого утворюються мікро- або наноемульсії;
h) перекачування фільтраційного розчину з другої камери в першу камеру другого діалізатора;
і) подачі розчину, що містить карбонову кислоту, з вказаної першої камери другого діалізатора в другу камеру другого діалізатора через другу розділову панель за рахунок створення концентраційного градієнта, хімічного градієнта, пневматичного градієнта, електричного градієнта або їх комбінації;
j) видалення асоціатів карбонової кислоти та солюбілізуючої сполуки, що проходять через вказану другу розділову панель, за рахунок циркуляції третього порядку;
к) перекачування акцепторного розчину карбонової кислоти з контейнера для зберігання акцепторного розчину в зазначену другу камеру другого діалізатора;
l) видалення акцепторного розчину з карбоновою кислотою в контейнер для зберігання стічних вод; і
m) повернення очищеного розчину, що містить солюбілізуючу сполуку, що покидає зазначену першу камеру другого діалізатора, на вхідний отвір вказаної другої камери першого діалізатора.
6. Спосіб за п. 5, де спосіб поєднаний з діалізом, гемофільтрацією, гемоперфузією, виділенням плазми, центрифугуванням, плазмаферезом, каскадною фільтрацією і термофільтрацією.
7. Спосіб за п. 5 або 6, де ефективність виділення підвищують шляхом додаткового гідролізу етерифікованих жирних кислот, посиленням ліполізу та/або використання сайту аспірації центральної венозної крові для очищення крові.
8. Спосіб за будь-яким з пп. 5-7, де медичні показання для застосування зазначеного способу вибирають з цукрового діабету, метаболічного синдрому, надмірної ваги, ожиріння, артеріальної гіпертонії, гіпертригліцеридемії, гіперхолістеринемії, гіперурінемії, целюліту, атеросклерозу, жирового метаморфозу печінки, ліпоматозу, шлуночкової екстрасистолії, шлуночкової тахікардії і суправентрикулярної фібриляції.
9. Спосіб за будь-яким з пп. 1-4, де підлягає очищенню розчин, одержаний з рослин, живих організмів, викопних матеріалів, природних або синтетичних реакційних сумішей.
10. Спосіб за будь-яким з п. 1-9, де принаймні одну солюбілізуючу сполуку додають до емульсії, розчину або суспензії, що містить карбонові кислоти, для використання зазначеної мікро- або наноемульсії карбонових кислот для вивільнення, руйнування комплексу, реакції, агрегації, комплексоутворення, коагуляції, флокуляції, седиментації або виділення комплексів, що містять карбонові кислоти.
11. Спосіб за будь-яким з пп. 1-10, де мікро- або наноемульсії карбонових кислот використовують для ослаблення фізико-хімічних чи хімічних реакцій, забезпечення можливості або посилення захоплення і транспорту продуктів реакцій або їх компонентів у процесах біологічних чи хімічних реакцій, відділення, солюбілізації, вивільнення, конвертування, транспорту речовин за рахунок захоплення бульбашками або забезпечення можливості, або посилення проникнення емульгованих карбонових кислот через гідрофільне або амфіфільне середовище або тверду речовину.
Текст
Реферат: Винахід стосується способу солюбілізації і видалення карбонових кислот, особливо жирних кислот, з олій, жирів, водних емульсій, водних середовищ та органічних розчинів, де солюбілізуюча сполука містить щонайменше одну амідиногрупу і/або одну гуанідиногрупу. UA 113497 C2 (12) UA 113497 C2 UA 113497 C2 5 10 15 20 25 30 35 40 45 50 55 60 A. Відомий рівень техніки Запропонований винахід відноситься до солюбілізуючих сполук, до пристрою і до способу солюбілізації і видалення карбонових кислот, і особливо жирних кислот, з олій, жирів, водних емульсій, водних або органічних розчинів. Пристрої, що використовуються в способі винаходу, можна використовувати для виділення карбонових кислот з олій, жирів, водних емульсій, ліпофільних середовищ, водних середовищ або органічних розчинів, відповідно, тим самим, змінюючи умови їх реакцій. Одне із застосувань являє собою пристрій для видалення жирних кислот з крові нужденного в цьому суб'єкта. Вказаний пристрій можна використовувати далі для аналітичних, відповідно діагностичних, цілей, для визначення концентрацій жирних кислот в корпоральних рідинах суб'єктів, в їжі або у фармацевтичних препаратах. Крім того, вказаний спосіб можна застосовувати для видалення залишків карбонових кислот у промислових розчинах, наприклад, що утворюються в харчовій або нафтопереробній промисловості. Взагалі жирні кислоти являють собою високо ліпофільні молекули, які погано розчиняються у водних розчинах. Тому тільки невеликі концентрації жирних кислот можна солюбілізувати у водних розчинах, хоча всі молекули жирних кислот, що перевищують таку концентрацію, присутні у формі міцел, утворюють емульсії за рахунок фазового розділення, або виявляються адсорбованими на стінках контейнера і/або на інших ліпофільних або амфіфільних молекулах, таких як білки в розчині. При концентрації, що перевищує критичну концентрацію міцел (ККМ) етерифікованих і неетеріфіцірованих карбонових кислот, концентрація вільних жирних кислот у водному середовищі залишається незмінною. Жирні кислоти мають тенденцію утворювати емульсії у водних середовищах. У присутності білків або клітинних структур жирні кислоти можуть ними адсорбуватися або адсорбуватися на них. Солюбілізація таких іммобілізованих жирних кислот залежить, головним чином, від критичної концентрації міцел (ККМ) жирних кислот в навколишньому водному середовищі. Емульгатори і детергенти здатні підвищити ККМ гідрофобних речовин, і таким чином сприяти відділенню іммобілізованих ліпофільних молекул. Такі емульгатори і детергенти можуть перетворити емульсії в міні-, мікро-або наноемульсії. Таким чином, площа контакту солюбілізованих жирних кислот з водною фазою збільшується. Це забезпечує кращу здатність до виділення і екстрагірованню солюбілізованих жирних кислот. Це також підвищує реакційну здатність у відношенні інших молекул. Емульсії етерифікованих і неетеріфіцірованих жирних кислот з водним середовищем можна повністю виділити тільки за допомогою органічного розчинника. Без допомоги мембрани цього можна досягти тільки шляхом перенесення жирних кислот в органічну фазу, змішуючи з органічним розчинником. Екстрагування можливо також за рахунок адсорбції на акцептор. У присутності адсорбуючих молекул, таких як білки, виділення жирних кислот в емульсії або суспензії за рахунок розділення фаз або екстрагування часто є неповним. Крім того, ефективність такого способу обмежена, і зазвичай він не пристосований для он-лайн (безперервного) процесу. При фільтруванні таких емульсій водну фракцію можна відфільтрувати майже повністю. Однак, також гідрофільні молекули, особливо великі білки, утримуються і виділяються разом з органічною фазою. Поділ молекул можна здійснити, використовуючи хроматографічні способи. Такі способи, однак, займають багато часу і обмежені по продуктивності. Іншим способом виділення карбонових кислот з водних або органічних середовищ є дистиляція. Проте, такий спосіб вимагає великих енергетичних витрат і може викликати ізомеризацію карбонових кислот або денатуріровання органічних компонентів всередині середовища. Наступним способом є омилення. Додані солі часто буває важко видалити з органіки також як з водних розчинів під час подальшої обробки. Таким чином, існує необхідність у способі безперервного і селективного екстрагування жирних кислот з емульсії водних або органічних розчинів. Метою цього винаходу є створення простого, швидкого і біосумісного способу виділення жирних кислот з водних емульсій чи органічних середовищ. Несподівано було виявлено, що цієї мети можна досягти, додаючи солюбілізуючу сполуку до водних емульсій чи до водних середовищ, таких як кров, ліпофільні середовища або органічні середовища, що містять карбонові кислоти або суміші карбонових кислот з іншими органофільними молекулами. Солюбілізуючу сполуку запропонованого винаходу, що має певні в описі характеристики, здатні солюбілізувати карбонові кислоти і перетворити емульговані карбонові кислоти в макро- або наноемульсії, що дозволяє здійснити виділення за допомогою способів поділу, таких як діаліз, фільтрування та електрофорез. Вказану задачу вирішують, слідуючи технічним вказівкам незалежних пунктів формули запропонованого винаходу. 1 UA 113497 C2 5 10 15 20 25 30 35 40 45 50 55 60 Подальші корисні втілення запропонованого винаходу випливають з залежних пунктів формули винаходу, опису та прикладів. Жирні кислоти Зазвичай жирні кислоти складаються з карбоксильної кінцевої групи і довгого аліфатичного ланцюжка. В залежності від присутності подвійних зв'язків їх підрозділяють на насичені чи ненасичені жирні кислоти. В літературі існують різні визначення жирних кислот. В одному з визначень зазначено, що карбонові кислоти, що містять 4 атоми вуглецю або більше, розглядають як жирні кислоти. Проте природні жирні кислоти містять щонайменше 8 атомів вуглецю. У цих атомів вуглецю щонайменше одна нітрогрупа може заміщати атом (атоми) водню, і перетворювати їх на нітро-жирні кислоти. Також нітро-жирні кислоти можуть мати інші заступники, такі як перераховані вище. Прикладами нерозгалужених насичених жирних кислот є октанова кислота (каприлова кислота), деканова кислота (капринова кислота), додеканова кислота (лауринова кислота), тетрадеканова кислота (міристинова кислота), гексадеканова кислота (пальмітинова кислота), гептадеканова кислота (маргаринова кислота), октадеканова кислота (стеаринова кислота), ейкозанова кислота (арахідінова кислота), докозанова кислота (бегенова кислота) і тетракозанова кислота (лігноцеринова кислота). У відповідності з цим винаходом кращою підгрупою, що підлягає виділенню насичених жирних кислот є міристинова кислота, пальмітинова кислота і стеаринова кислота. Прикладами моноолефінових жирних кислот є цис-9-тетрадеценова кислота (мірістолеінова кислота), цис-9-гексадеценова кислота (пальмітолеінова кислота), цис-6-гексадеценова кислота (сальпенова кислота), цис-6-октадеценова кислота (петроселинова кислота), цис-9октадеценова кислота (олеїнова кислота), цис-11-октадеценова кислота (вакценова кислота), 12-гідрокси-9-цис-октадеценова кислота (ріцінолеінова кислота), цис-9-ейкозенова кислота (гадолеінова кислота), цис-11-ейкозенова кислота (гондоєва кислота), цис-13-докозенова кислота (ерукова кислота), цис-15-тетракозенова кислота (нервонова кислота), t9-октадеценова кислота (елаідінова кислота), t11-октадеценова кислота (t-вакценова кислота) і t3гексадеценова кислота. У відповідності з цим винаходом кращою підгрупою, що підлягає виділенню ненасичених жирних кислот є транс-ізомери t9-октадеценової кислоти, t11октадеценової кислоти, і t3-гексадеценової кислоти. Прикладами поліолефінових жирних кислот є 9,12-октадекадієнова кислота (лінолеінова кислота), 6,9,12-октадекатрієнова кислота (γ-лінолеінова кислота), 8,11,14-ейкозатрієнова кислота (дігомі-γ-лінолеінова кислота), 5,8,11,14-ейкозатрієнова кислота (арахідонова кислота), 7,10,13,16-докозатетраєнова кислота, 4,7,10,13,16-докозапентаєнова кислота, 9,12,15октадекатрієнова кислота (α-ліноленова кислота), 6,9,12,15-октадекатетраєнова кислота (стеарідонова кислота), 8,11,14,17-ейкозатетраєнова кислота, 5,8,11,14,17-ейкозапентаєнова кислота (EPA), 7,10,13,16,19-докозапентаєнова кислота (DPA), 4,7,10,13,16,19-докозагексаєнова кислота (DHA), 5,8,11-ейкозатрієнова кислота (медова кислота), 9c, 11t, 13t-елеостеарінова кислота, 8t, 10t, 12c-календова кислота, 9c, 11t, 13c-катальпова кислота, 4,7,9,11,13,16,19докозагептадеканова кислота (стеллагептаєнова кислота), таксолева кислота, піноленова кислота і сціадонова кислота. У відповідності з цим винаходом кращою підгрупою, що підлягає виділенню ненасичених жирних кислот є транс-ізомери ліноленової кислоти, γ-ліноленової кислоти, EPA і DPA. Прикладами ацетиленових жирних кислот є 6-октадецинова кислота (винна кислота), t11октадецен-9-інова кислота (санталбова або хіменова кислота),9-октадецинова кислота (стеаролова кислота), 6-октадецен-9-інова кислота (6,9-октадеценінова кислота), t10гептадецен-8-інова кислота (піровиноградна кислота), 9-октадецен-12-інова кислота (крепенова кислота), t7,t11-октадекадіен-9-інова кислота (хеістерінова кислота), t8,t10-октадекадіен-12інова кислота, 5,8,11,14-ейкозатетраінова кислота (ETYA). Слід зазначити, що відповідно до цього винаходу також і основи, відповідно і солі, вищевказаних жирних кислот повинні ставитися до групи під загальною назвою жирні кислоти або вільні жирні кислоти. Прикладами придатних органічних і неорганічних основ для утворення солей є основи, отримані з іонів металів, наприклад, алюмінію, іонів лужних металів, таких як натрій або калій, іонів лужноземельних металів, таких як кальцій або магній, або іонів солей аміну або гідроксидів лужних або лужноземельних металів, - карбонатів або-бікарбонатів. Приклади включають водний гідроксид натрію, гідроксид літію, карбонат калію, аміак та бікарбонат натрію, солі амонію, первинні, вторинні і третинні аміни, такі як, наприклад, нижчі алкіламіни, такі як метиламін, трет-бутиламін, прокаїн, етаноламін, арілалкіламіни, такі як дібензіламін і N,N-дібензілетілендіамін, нижчі алкілпіперідіни, такі як N-етілпіперідін, ціклоалкіламіни, такі як циклогексиламін або дициклогексиламін, морфолін, глюкамін, N-метил-і 2 UA 113497 C2 5 10 15 20 25 30 35 40 45 50 55 Ν,Ν-діметилглюкамін, 1-адамантіламін, бензатіен, або солі, отримані з амінокислот, таких як лізин, орнітин, або аміди органічних нейтральних або кислотних амінокислот або тому подібне. Наступні карбонові кислоти є переважними прикладами жирних кислот: октанова кислота (каприлова кислота), деканова кислота (капрінова кислота), додеканова кислота (лаурілової кислоти),тетрадеканова кислота (міристинова кислота), гексадеканова кислота (пальмітинова кислота), гептадеканова кислота (маргаринова кислота), октадеканова кислота (стеаринова кислота), ейкозанова кислота (арахідінова кислота), докозанова кислота (бегенова кислота), тетракозанова кислота (лігноцеринова кислота), цис-9-тетрадеценова кислота (мірістолеінова кислота), цис-9-гексадеценова кислота (мірістолеінова кислота) цис-6-октадеценова кислота (петроселінова кислота), цис-9-октадеценова кислота (олеїнова кислота), цис-11-октадеценова кислота (вакценова кислота), цис-9-ейкозенова кислота (гадолеінова кислота), цис-11ейкозенова кислота (гондоєва кислота), цис-13-докозенова кислота (ерукова кислота), цис-15тетракозенова кислота (ацетерукова кислота), t9-октадеценова кислота (елаідінова кислота), t11-октадеценова кислота (t-вакценова кислота), t3-гексадеценова кислота, 9,12октадекадієнова кислота (ліноленова кислота), 6,9,12-октадекатриєнова кислота (γ-ліноленова кислота), 8,11,14-ейкозатрієнова кислота (дігомі-y-ліноленова кислота), 5,8,11,14ейкозатетраєнова кислота (арахідонова кислота), 7,10,13,16-докозатетраєнова кислота, 4,7,10,13,16-докозапентаєнова кислота, 9,12,15-октадекатрієнова кислота (α-ліноленова кислота), 6,9,12,15-октадекатетраєнова кислота (стеарідонова кислота), 8,11,14,17ейкозатетраєнова кислота, 5,8,11,14,17-ейкозапентаєнова кислота (EPA), 7,10,13,16,19докозапентаєнова кислота (DPA), 4,7,10,13,16,19-докозагексаєнова кислота (DHA), 5,8,11ейкозатрієнова кислота (медова кислота), 9c, 11t, 13t-елеостеарінова кислота, 8t, 10t, 12cкалендова кислота, 9c, 11t, 13c-катальпова кислота, 4,7,9,11,13,16,19-докозагептадеканова кислота (стеллагептаєнова кислота), таксолеінова кислота, піноленова кислота, сціадонова кислота, 6-октадеценова кислота (винна кислота), t11-октадецен-9-інова кислота (санталбова або ксіменінова кислота), 9-октадецноєва кислота (стеаролова кислота), 6-октадецен-9-інова кислота (6,9-октадеценіноева кислота), t10-гептадецен-8-інова кислота (піровиноградна кислота), 9-октадецен-12-інова кислота (крепенінова кислота), t7,t11-октадекадіен-9-інова кислота (хеістерова кислота), t8,t10-октадекадіен-12-інова кислота, 5,8,11,14-ейкозатетраіноева кислота (ETYA), елеоoстеарінова кислота, календова кислота, катальпова кислота, стеллагептаєнова кислота, таксолеінова кислота, ретинова кислота, ізопальмітінова кислота, пристанова кислота, фітанова кислота, 11,12-метиленоктадеканова кислота, 9,10метиленгексадеканова кислота, коронарова кислота, (R, S)-ліпоєва кислота, (S)-ліпоєва кислота, (R)-ліпоєва кислота, 6,8-біс(метилсульфаніл) октанова кислота, 4,6біс(метилсульфаніл)гексанова кислота, 2,4-біс(метилсульфаніл)бутанова кислота, 1,2дітіоланкарбонова кислота, (R, S)-6,8-дітіаноктанова кислота, (R)-6,8-дітіаноктанова кислота, (S)-6,8-дітіаноктанова кислота, церебронова кислота, гідроксіацетерукова кислота, ріцінолеінова кислота, лескверолова кислота, брассілова кислота і тапсієва кислота. Жирні кислоти в крові У ссавців жирні кислоти служать фізіологічно важливими енергетичними речовинами і відіграють ключову роль в енергетичному метаболізмі. Крім того, вони є важливими субстратами для синтезу мембранних фосфоліпідів і біологічно активних агентів, таких як ейкозаноїди і лейкотрієни. Організм ссавців в значній мірі залежить від жирних кислот, як постачальників хімічно акумульованої енергії, будівельних блоків клітинних мембран і для передачі сигналів. Основним джерелом жирних кислот є харчові ліпіди, переварені в шлунковокишковому тракті завдяки каталітичній дії гідролітичних ферментів підшлункової залози. Частина жирних кислот виробляється печінкою, що запасає вуглеводи в якості субстрату. Однак великий відсоток жирних кислот зберігається в жирових клітинах (адипоцитах), що включають адіпозну тканину у формі тріацілгліцеріна. Концентрація етерифікованих і неетерофіцірованних жирних кислот у крові залежить від декількох факторів, таких як засвоєння їжі або виділення з адіпозної тканини. Жирні кислоти можуть бути пов'язані з іншими молекулами або приєднані до інших молекул, таким як тригліцериди чи фосфоліпіди, або до невеликого відсотку жирних кислот, що залишилися непов'язаними. У будь-якому випадку жирні кислоти нерозчинні у воді і повинні бути пов'язані з розчинним у воді компонентом для транспорту в організмі. Транспорт жирних кислот в організмі здійснюється за рахунок лімфатичної та судинної систем. В основному існують дві транспортні форми: жирні кислоти можуть переноситися як триацилгліцерини, які являють собою основний компонент циркулюючих ліпобілків, таких як хіломікрони і ліпобілкі дуже низької щільності, або як неетерифіцировані жирні кислоти, які зв'язані з білками плазми, зокрема з альбуміном 3 UA 113497 C2 5 10 15 20 25 30 35 40 45 50 55 60 плазми. Вільні жирні кислоти, які ні з чим не пов'язані, мають дуже низьку розчинність, і присутні тільки в дуже низьких концентраціях. Склад, розподіл і концентрації жирних кислот у крові людини можуть сильно відрізнятися, і складаються з суми різних фракцій плазми: ефіри холестерину, фосфоліпіди і триацилгліцерини, також як пов'язані з альбуміном жирні кислоти. Насичені жирні кислоти в крові людини представлені в основному миристиновою кислотою (14:0), пальмітиновою кислотою (16:0) та стеариновою кислотою (18:0). Основний тип мононенасичених жирних кислот належить до групи, що складається з олеїнової кислоти (18:1) і пальмітолеінової кислоти (16:1). Поліненасичені омега-3 жирні кислоти включають ліноленову кислоту (18:3), ейкозапентаєнову кислоту (20:5), докозапентаєнову кислоту (22:5) і докозагексаєнову кислоту (22:6). Поліненасичені омега-6 жирні кислоти включають в основному ліноленову кислоту (18:2), ейкозадієнову кислоту (20:2), дігомогаммаліноленову кислоту (20:3), арахідонову кислоту (20:4), адренову кислоту (22:4) і докозапентаєнову кислоту (22:5). Концентрації інших жирних кислот зазвичай дуже низькі в цільній крові, але можуть мінятися залежно від генетики, харчування і способу життя. Концентрації жирних кислот у крові підвищені у страждаючих ожирінням пацієнтів, і вносять внесок у діабет 2 типу, гепатичний стеатоз і деякі серцево-судинні порушення, такі як атеросклероз. Була з'ясована патогенетична роль жирних кислот у розвитку атеросклерозу і пов'язаних з ним таких захворювань, як церебральні, міокардіальні, ниркові, еректильні дисфункціі. Без претензій на повноту, далі будуть досліджені деякі аспекти. Було виявлено, що підвищення вмісту жирних кислот відповідає за збільшення утворення реакційно здатних кисневих радикалів, що викликає ендотеліальну дисфункцію, яку можна послабити, використовуючи антиоксидант. (Pleiner et al., FFA-induced endothelial dysfunction can be corrected by vitamin C.J Clin Endocrinol Metab 2002, 87, 2913-7). Зазначений ефект посилюється за рахунок транс-жирних кислот, які, як припускають, володіють додатковими шкідливими ефектами (Lopez Garcia et al., Consumption of trans-fatty acids is related to plasma biomarkers of inflammation and endothelial dysfunction. J Nutr 2005, 135, 562-566; Mozaffarian et al., Health effects of trans-fatty acids: experimental and observational evidence. Eur J Clin Nutr 2009, 63 Suppl 2, S5-21). Їх звинувачують в підвищенні кров'яного тиску, і було виявлено, що вони є патогенетичним чинником виникнення артеріальної гіпертонії (Zheng et al., Plasma fatty acid composition and 6-year incidence of hypertension in middle-aged adults: the Atherosclerosis Risk in Communities (ARIC) Study. Am J Epidemiol 1999, 150, 492-500). Було виявлено, що транс-жирні кислоти підвищують ризик інфаркту міокарда та несподіваної зупинки серця (Ascherio et al., Trans-fatty acids intake and risk of myocardial infarction. Circulation 1994, 89, 94-101; Baylin et al., High 18:2 Trans-fatty acids in adipose tissue are associated with increased risk of nonfatal acute myocardial infarction in Costa Rican adults. J Nutr 2003, 133, 1186-1191). Поряд з постійним збільшенням концентрації жирних кислот у крові, вони відповідальні за резистентність до інсуліну і розвиток цукрового діабету (Krachler et al., Fatty acid profile of the erythrocyte membrane preceding development of type 2 diabetes mellitus. Nutr Metab Cardiovasc Dis 2008, 18, 503-510; Lionetti et al., From chronic overnutrition to insulin resistance: the role of fat-storing capacity and inflammation. Nutr Metab Cardiovasc Dis 2009, 19, 146-152; Yu et al., Mechanism by which fatty acids inhibit insulin activation of insulin receptor substrate-1 (IRS-1)-associated phosphatidylinositol 3-kinase activity in muscle. J Biol Chem 2002, 277, 50230-50236). В даний час вважають, що підвищений оборот жирних кислот, як результат хронічного переїдання, є найбільш важливим патологічним механізмом у розвитку більшості звичайних захворювань у промислових країнах (Bays, "Sick fat", metabolic disease, and atherosclerosis. Am J Med 2009, 122, S26-37). Медичного лікування для ефективного зниження надмірної ваги не існує (Aronne et al., When prevention fails: obesity treatment strategies. Am J Med 2009, 122, S24-32). Однак, можна знайти повних людей, яким вдалося знизити масу тіла, і таким чином значно зменшити можливість захворювань, що викликаються жирними кислотами (Lien et al., The STEDMAN project: biophysical, biochemical and metabolic effects of a behavioral weight loss intervention during weight loss, maintenance, and regain. Omics 2009, 13, 2135; Schenk et al., Improved insulin sensitivity after weight loss and exercise training is mediated by a reduction in plasma fatty acids mobilizatioN,Not enhanced oxidative capacity. J Physiol 2009, 587, 4949-4961). Тому бажано створити пристрій для ефективного зниження повної кількості жирних кислот і переважно кислот з підвищеною патогенічностю. Було виявлено, що хірургічне видалення підшкірної адіпозної тканини є неефективним щодо зменшення концентрації або кількісного вмісту циркулюючих жирних кислот. Видалення фракції 4 UA 113497 C2 5 10 15 20 25 30 35 40 45 50 55 60 ліпопротеїнів з високою концентрацією холестерину шляхом безпосередньої адсорбції з крові можна здійснити, використовуючи адсорбцію або фільтрацію зазначених частинок. Такі процедури для он-лайн очищення крові називають LDL аферезом. Хоча вони створені для зниження вмісту LDL холестерину, вони також адсорбують тригліцериди. Однак, кількість тригліцеридів, що екстрагуються недостатньо для зниження вмісту жирних кислот в організмі. Вміст жирних кислот в крові є низьким в голодному стані в спокої. Однак спостерігається значне підвищення під час ліполізу (див. далі). Через нерозчинність у водному середовищі транспорт неетерифікованих жирних кислот здійснюється білками і клітинними структурами (Spector et al., Utilization of long-chain free fatty acids by human platelets. J Clin Invest 1970, 49, 1489-1496). Основним транспортним білком крові є альбумін. Було документально встановлено наявність щонайменше 10 специфічних сайтів зв'язування жирних кислот. Однак здатність зв'язування може різко зрости за рахунок утворення міцелярних структур з жирними кислотами в умовах надлишку жирних кислот або інших ліпідів (Schubiger et al., Mixed micelles: a new problem-free 123 solution for omega- l-heptadecanoic acid in comparison. Nuklearmedizin 1984, 23, 27-28). При молярності альбуміну близько 600 мкмоль/л буде спостерігатися зв'язувальна здатність щонайменше 0,006 моль/л для жирних кислот, що відповідає приблизно 0,0035 кг/л (Berk and Stump, Mechanisms of cellular uptake of long chain free fatty acids. Mol Cell Biochem 1999, 192, 1731). Крім того, жирні кислоти переносяться в етерифікованій формі, як моно-, ди- або триацилгліцерини. Концентрація в сироватці в голодному стані значно змінюється. Однак загальновизнані нормальні значення повинні бути нижче 150 мг/дл (1,7 моль/л). Після прийому їжі або під час тренування концентрація може зрости в кілька разів і навіть може перевищити 1000 мг/дл (11,3 ммоль/л). Існують лише мізерні повідомлення, в яких досліджують відмінності у вмісті ліпідів в різних сайтах всередині циркуляції. У зазначених дослідженнях було виявлено, що значно вищі значення для жирних кислот і тригліцеридів існують в центральній венозній системі (Vena cava) в порівнянні з іншими вивченими сайтами. (Wiese et al., Lipid composition of the vascular system during infancy, childhood, and young adulthood, J. Lipid Res. 1967, 8, 312-320; Zauner et al., Pulmonary arterial-venous differences in lipids and lipid metabolites. Respiration 1985, 47, 214-219). Відсутні повідомлення про зміни вмісту ліпідів в центральній венозній системі під час тренувань і при індукованому ліполізі. В даний час було виявлено, що під час фізичних тренувань вміст ліпідів різко зростає в центральних абдомінальних венах, демонструючи різницю, що збільшується в вмісті ліпідів в центральному і периферичному сайтах доступів, як розкрито далі. Таким чином, зменшення вмісту жирних кислот у крові з використанням розкритих в описі способів і пристроїв і солюбілізуючих сполук можна використовувати для лікування зазначених вище захворювань, пов'язаних з підвищеним рівнем вмісту жирних кислот у крові або в організмі. Таким чином даний винахід відноситься до лікування та профілактики захворювань, викликаних жирними кислотами, таких як діабет 2 типу, печінковий стеатоз, серцево-судинні захворювання, такі як артеріальна гіпертонія, інфаркт міокарда, удар, несподівана смерть від інфаркту, атеросклероз, захворювання, пов'язані з атеросклерозом, такі як церебральна, міокардіальна, ниркова і еректильна дисфункції, також як до зниження ваги і до зниження вмісту холестерину і також до профілактики резистентності до інсуліну і профілактиці розвитку цукрового діабету, за рахунок використання розкритих у винаході солюбілізуючих сполук для видалення жирних кислот з крові. Ліполіз Плазмові жирні кислоти являють собою важливий енергетичний субстрат. Доступність жирних кислот визначають переважно по їх мобілізації зі сховищ тріацілгліцеріна в адіпозній тканині в процесі ліполізу. У людини ліполіз адіпозної тканини регулюється низкою гормональних, паракрінних і/або автокрінних сигналів. Основні гормональні сигнали можуть бути представлені катехоламінами, інсуліном, гормоном росту, натрійуретичними пептидами, тироксином та деякими адіпоцітокінами (Stich and Berlan, Phisiological regulation of NEFA availability: lypolysis pathway. Proc Nutr Soc 2004, 63, 369-374). Абсолютно рівні і відносна важливість і внесок зазначених сигналів змінюються в різних фізіологічних ситуаціях, причому харчування і фізичні вправи є основними фізіологічними змінними, які впливають на систему гормональних сигналів. Сімейство ферментів, званих ліпазами, з різними функціями відповідає за руйнування тригліцеридів, що знаходяться всередині жирових клітин для зберігання енергії. Вуглеводні і жирні кислоти являють собою основні енергоресурси для м'язових скорочень. Під час вправ ліполіз вивільняє 7,1 + / - 1,2 макромол хв (-1) кг (-1) ваги тіла, що призводить до виділення жирних кислот порядку 4200 мкмоль на годину у людини вагою 100 кг, що 5 UA 113497 C2 5 10 15 20 25 30 35 40 45 50 55 60 еквівалентно 0,15 кг жирних кислот (Coggan et al., Fat metabolism during high-intensity exercise in endurance-trained and untrained men. Metabolism 2000, 49, 122-128). Однак стимуляція ліполізу фармакологічним втручанням і/або локальними фізичними заходами може далі підвищити ліполітичну здатність. Ліполіз підвищується аж до триразового за рахунок систематичного застосування природних рецепторних агоністів або лікарських засобів (Riis et al., Elevated regional lypolysis in hyperthyroidism. J Clin Endocrinol Metab 2002, 87, 4747-4753; Barbe et al., In situ assessment of the role of the beta 1-, beta 2- і beta 3-adrenoceptors in the control of lypolysis and nutritive blood flow in human subcutaneous adipose tissue. Br J Pharmacol 1996, 117, 907-913). Агоністи адренорецепторів, що демонструють стимулювання ліполізу: адреналін, норадреналін, ізопреналін, ефедрин, ізопротеріол, салбутамол, теофілін, фенотерол або ціпреналін, та ін. Ліполітичні ефекти були також описані для фізичних змін жирової тканини. Дослідники виявили, що ультразвук володіє розріджуючим ефектом відносно адіпозної тканини, що призводить до зменшення вмісту жирової тканини, якщо це здійснюється за час голодування (Faga et al., Ultra sound-assisted lypolysis of the omentum in dwarf pigs. Aesthetic Plast Surg 2002, 26, 193-196; Miwa et al., Effect of Ultra sound application on fat mobilization. Pathophysiology 2002, 9, 13). Хоча для всіх вищевикладених вимірювань посилення ліполізу було документовано, вимірюваний вплив на концентрації неетерифікованих жирних кислот було маленьким. У пілотному дослідженні було виявлено, що після стимуляції ліполізу вміст жирних кислот істотно підвищується, якщо його вимірюють, використовуючи спосіб запропонованого винаходу для солюбілізації жирних кислот. Крім того, було виявлено, що вміст жирних кислот набагато вище в абдомінальній венозній системі, ніж в периферичній циркуляції. Цей факт виявився несподіваним, оскільки він не спостерігався в дослідженнях на тваринах, при вимірюванні зразків крові з різних ділянок, взятих одночасно. Тому стимуляція ліполізу під час здійснення очищення крові від жирних кислот за способом запропонованого винаходу і використання центральної абдомінальної вени в якості сайту доступу є кращим варіантом запропонованого винаходу. Частину, що екстрагується можна збільшити якщо вміст етерифікованих і неетерифікованих жирних кислот, що транспортуються в крові можна підвищити, здійснюючи зазначений спосіб. Несподівано виявилося, що завдання можна вирішити, посилюючи ліполіз способом заявленого винаходу. Сольватація і адгезія жирних кислот у водному середовищі Розчинність карбонових кислот у воді мінімальна, якщо довжина вуглеводного ланцюжка перевищує 4 атома вуглецю і у відсутності гідроксильних (-OH) груп, карбоксильних (-COOH) груп або інших полярних або заряджених груп і/або при введенні алкільних заступників або інших ліпофільних груп. Розчинність можна підвищити, використовуючи детергенти, які проникають в міцели жирних кислот, знижуючи тим самим їх стабільність, зменшуючи їх розміри і збільшуючи число вільних молекул жирних кислот у водному середовищі. Як вільні жирні кислоти, так і міцели мають тенденцію зв'язуватися з ліпотропними структурами. Серед них можна вказати вуглець, метали, кераміку, природні та синтетичні полімери. Крім того, органічні структури містять ліпофільні ділянки, причому деякі з них, сконструйовані спеціально для того, щоб зв'язувати жирні кислоти, які утворюють мембранні або ліпідні транспортні білки. Просторові сайти зв'язування представлені головним чином гідрофобними амінокислотами. У крові ліпіди електростатично пов'язані зі спеціалізованими транспортними білками. Жирні кислоти головним чином, переносяться альбуміном. Зв'язування жирних кислот з молекулами альбуміну засновано також на силах електростатичної взаємодії, які локалізовані в гідрофобних кишенях. Енергія зв'язування таких кишень змінюється, однак pKa для всіх з них істотно вище, ніж CMC жирних кислот. Тому жирні кислоти залишаються в навколишньому середовищі навіть після повного видалення вільних жирних кислот. Було виявлено, що відділення жирних кислот від альбуміну є майже повним, якщо використовують органічні розчинники для їх вивільнення, через їх краще розчинення в органічних розчинниках. Однак, такі розчинники змінюють структуру білків, роблячи їх непридатними для подальшого процесу або використання в живому організмі. Для використання альбуміну для медичних або інших цілей необхідно зменшити вміст в них жирних кислот, не змінюючи при цьому структури і функціональності альбуміну. Вказану задачу можна вирішити шляхом активування частинок вуглецю, які мають більш високу здатність до зв'язування з жирними кислотами, ніж з альбуміном. Однак зазначений процес потребує додаткової стадії очищення альбуміну. Тому аж до теперішнього часу не існувало способу, який дозволив би швидко звільнити і солюбілізувати всі молекули, що містяться в 6 UA 113497 C2 5 10 15 20 25 30 35 40 45 50 55 60 молекулах альбуміну жирні кислоти у водному середовищі, який не змінює ультраструктуру та функції молекул альбуміну. Карбонові кислоти також переносяться в бульбашках фосфоліпідів. Електростатичні взаємодії між вуглеводневим ланцюжком карбонових кислот і ланцюжком фосфоліпідів утримують карбонові кислоти від дифузії у навколишнє водне середовище. З необхідними поправками це застосовно також до інших органічних розчинів, біомаси або органічних стічних вод. В органічних розчинах, призначених для подальшої модифікації, очищення або використання, де бажано не використовувати органічний розчинник, бажаний альтернативний біосумісний спосіб. До цих пір такий спосіб відсутній. Несподівано виявилося, що цієї мети можна досягти, використовуючи щонайменше одну солюбілізуючу сполуку, як розкрито в описі, що включає щонайменше один амідінофрагмент і/або щонайменше один гуанідинофрагмент, і особливо солюбілізуючі сполуки загальної формули (I), (II) і (III) і найбільш переважно аргінін і його похідні. Карбонові кислоти, що підлягають видаленню зазвичай містяться у водному середовищі або у водних розчинах, таких як кров або плазма крові, або у водних емульсіях, таких як молоко, або в органічному середовищі, таких як паливо, газ, біо-дизельне паливо, газолін, бензин і тому подібні, або в оліях, таких як рослинні масла, такі як льняна олія, горіхова олія, оліфа, олія енотери, олія соняшнику, олія насіння соняшнику, соєва олія, рапсова олія, оливкова олія, оливкова олія першого віджиму, пальмова олія, олія пальмових кісточок, арахісова олія, бавовняна олія, кокосова олія, кукурудзяна олія, олія виноградних кісточок, олія фундука, рисова олія, сафлорова олія, кунжутна олія, також як тваринні масла, такі як риб'ячий жир, або що містяться в жирах, таких як вершкова олія, олеомаргарін або маргарин. У разі, якщо карбонові кислоти знаходяться у воді, водному середовищі, водній емульсії або у водній суспензії, щонайменше одну солюбілізуючу сполуку можна безпосередньо додати до водного середовища, емульсії або суспензії, або принаймні одну солюбілізуючу сполуку можна розчинити у воді, і отриманий водний розчин можна додати до водного середовища, емульсії або суспензії, що містить карбонові кислоти. Після такого додавання відбувається утворення наноемульсії і/або мікроемульсій. У разі, якщо карбонові кислоти знаходяться в органічному середовищі або ліпофільному органічному середовищі, солюбілізуючу сполуку розчиняють у воді, і отриманий розчин солюбілізуючої сполуки у воді додають до органічного середовища. Утворюється двофазна суміш, і карбонові кислоти переходять у водну фазу. Вважають, що утворюється комплекс чи агрегат однієї молекули карбонової кислоти з однією молекулою солюбілізуючої сполуки або їх димер або тример, що робить карбонову кислоту розчинною у воді. Таким чином, переважно, перемішувати або струшувати двофазні суміші, що складаються з органічного і водного шару, для забезпечення інтенсивного перемішування зазначених двох шарів. Карбонові кислоти, що містяться у водній фазі, можна видалити, використовуючи фазовий поділ. При бажанні, спосіб екстрагування можна повторити. У разі, якщо карбонові кислоти знаходяться в маслі або жирі, солюбілізуючі сполуки розчиняють у воді і одержаний розчин солюбілізуючої сполуки у воді додають до масла або жиру. При бажанні, органічний розчинник можна додавати в олію або жир для зменшення в'язкості масла або жиру, щоб краще можна було перемішувати олію або жир. У разі, якщо карбонові кислоти знаходяться в маслі або жирі, солюбілізуючу сполуку розчиняють у воді і одержаний розчин солюбілізуючої сполуки у воді додають до масла або жиру. При бажанні, органічний розчинник можна додавати в олію або жир для зменшення в'язкості масла або жиру, щоб забезпечити краще перемішування масла або жиру. Суміш масла або жиру і водного розчину солюбілізуючої сполуки перемішують. Карбонові кислоти переходять у водну фазу, і водну фазу можна видалити, використовуючи декантування або фазовий поділ. При бажанні процес екстрагування можна повторювати кілька разів. Таким чином, даний винахід також відноситься до водної мікроемульсії та/або водної наноемульсії, що містить щонайменше одну солюбілізуючу сполуку і щонайменше одну карбонову кислоту в мікроемульгованій або в наноемульгованій формі. Якщо солюбілізуючу сполуку використовують в надлишку порядку 1,2-2,8, переважно 1,5-2,5, і більш переважно в надлишку 1,7-2,3 молярних еквівалентів, виявляється можливим видалити більш ніж 90 % карбонових кислот за одну стадію екстрагування. Якщо стадію екстрагування повторюють двічі, можна видалити аж до 99 % карбонових кислот. Карбонові кислоти, які можна видалити являють собою карбонові кислоти, що містять більше ніж 5 атомів вуглецю, більш переважно більш ніж 7 атомів вуглецю, і особливо переважно більш ніж 9 атомів вуглецю. Переважно, щоб зазначені карбонові кислоти представляли собою жирні кислоти, як розкрито в описі, хоча способом запропонованого винаходу можна також видаляти інші ліпофільні сполуки, що містять карбоксильну групу або 7 UA 113497 C2 5 10 15 20 25 30 35 40 45 50 55 60 групу карбонової кислоти, такі як лікарські засоби або токсини. Однією з карбонових кислот, яка однозначно виключена з цього винаходу, є напроксен. Крім того, метою даного винаходу не є створення способів і сполук або пристроїв для солюбілізації лікарських препаратів з метою одержання галенових композицій. Особливо переважні видалення і солюбілізація нафтенових кислот з олій, бензину, газу та палива. З карбонових кислот найбільш переважні такі карбонові кислоти, які містять подвійні і/або потрійні зв'язки, такі як ненасичені і поліненасичені жирні кислоти. Ще більш кращі фізіологічні карбонові кислоти, і особливо такі фізіологічні карбонові кислоти, які знаходяться в організмах людей. Для промислових цілей ненасичені жирні кислоти переважно видаляють і солюбілізіують з вихідних матеріалів, таких як масла і жири, тоді як для медичних цілей зазначені насичені жирні кислоти переважно видаляють з крові пацієнта. Крім того, кращі такі карбонові кислоти, які зустрічаються в оліях та жирах вищевказаних джерел, особливо тварин, таких як риби, в кукурудзі, оливках, зерні, сільсько-господарських продуктах, рисі, сої і тому подібних. У разі, якщо карбонові кислоти, які необхідно видалити з органічних середовищ, таких як жири, віск, масла, паливо, бензин і тому подібні, що знаходяться в етерифікованій формі (тобто пов'язані в ефірах), стадію омилення можна здійснити до здійснення стадії видалення та солюбілізації запропонованого винаходу. Таке омилення переважно здійснюють у суміші розчинників, що складається з води і щонайменше другого розчинника, що змішується з водою. Іншими переважними карбоновими кислотами є перфторкарбонові кислоти, такі як перфторпропіонова кислота, перфтороктанова кислота (PFOA), перфтордеканова кислота, перфтордодеканова кислота, перфторгексадеканова кислота, також як інші перфторкарбонові кислоти і профірінова кислота. Запропонований винахід також відноситься до солюбілізації, відповідно до видалення, ароматичних карбонових кислот, що належать до вищевказаних цільових груп, таких як бензойна кислота, 4-амінобензойна кислота, антранілова кислота, бензилова кислота, корична кислота, саліцилова кислота, фенилуксусна кислота, 4-метоксіфенілуксусна кислота, галлиєва кислота, фталева кислота, терефталева кислота, абієтинова кислота, біцінхонінова кислота, хінна кислота, хорізмова кислота, клавуланова кислота, фузарова кислота, фузідова кислота, сечова кислота, гіпурова кислота, іботенова кислота, індол-3-оцтова кислота, мигдальна кислота, стіфнінова кислота, уснінова кислота, абсцизова кислота, тропова кислота, бензохінонтетракарбонова кислота, босвелева кислота, кофеїнова кислота, кармінова кислота, хенодеоксіхолева кислота, кумаринова кислота, кромогліцієва кислота, цинарин, меклофенамова кислота, 2,4-дихлорфеноксиуксусна кислота, домоєва кислота, піпемідинова кислота, ферулова кислота, 5-гідроксіферулова кислота, ізофталева кислота, мефенамова кислота, метахлорпероксібензойна кислота, пероксібензойна кислота, протокатехова кислота, налідіксова кислота, сінапова кислота, сукрононова кислота. Особливо переважні видалення і солюбілізація з крові карбонових кислот, які призводять до різних захворювань, що викликається і/або пов'язаним з підвищеним і/або небезпечним рівнем таких карбонових кислот, і особливо жирних кислот. Карбонові кислоти є, переважно, ліпофільними і, переважно, мають коефіцієнт поділу н-октанол - вода (також відомий як log KOW або коефіцієнт поділу октанол-вода) >2,0, переважно >3,0, і більш переважно >4,0. (Наприклад: log KOW оцтової кислоти дорівнює 0,17, масляної кислоти дорівнює 0,79, октанової кислоти дорівнює 3,05 і деканової кислоти дорівнює 4,09). Переважно також, щоб карбонові кислоти, що підлягають видаленню, мали значення pKs >4,85, переважно >4,87 (наприклад: оцтова кислота має pKs 4,76, масляна кислота 4,82, пентанова кислота 4,84 і октанова кислота 4,89). Таким чином в запропонованому винаході запропонований спосіб виділення карбонових кислот, які зовсім не розчиняються у воді або погано розчиняються у воді, і які можна солюбілізувати у воді за допомогою розкритих у винаході солюбілізуючих з'єднань, переважно, у формі нано- або мікроемульсій. Після переходу в водну фазу, жирні кислоти можна видалити різними розкритими в описі способами. Таким чином, даний винахід відноситься до використання солюбілізуючих сполук для солюбілізації карбонових кислот у водних або органічних середовищах, де зазначена солюбілізуюча сполука містить щонайменше одну амідіногрупу і/або щонайменше одну гуанідиногрупу, і де зазначена сполука має коефіцієнт поділу н-октанол - вода KOW
ДивитисяДодаткова інформація
Назва патенту англійськоюDevice and method for solubilizing, separating, removing and reacting carboxylic acids in oils, fats, aqueous or organic solutions by means of micro- or nanoemulsification
Автори англійськоюDitz, Ulrich
Автори російськоюДитц Ульрих
МПК / Мітки
МПК: C07B 63/04
Мітки: солюбілізації, використанням, карбонових, виділення, солюбілізуючих, кислот, спосіб, сполук
Код посилання
<a href="https://ua.patents.su/71-113497-sposib-solyubilizaci-i-vidilennya-karbonovikh-kislot-z-vikoristannyam-solyubilizuyuchikh-spoluk.html" target="_blank" rel="follow" title="База патентів України">Спосіб солюбілізації і виділення карбонових кислот з використанням солюбілізуючих сполук</a>
Попередній патент: Вектор і спосіб підвищення стійкості до інфекції, що викликається campylobacter
Наступний патент: Фосфінові ліганди для каталітичних реакцій
Випадковий патент: Спосіб лікування та профілактики звичного вивиху плеча