5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5н-тіазоло[4,5-d]піридазинон-4, що має протипухлинні властивості
Номер патенту: 118861
Опубліковано: 28.08.2017
Автори: Демченко Сергій Анатолійович, Бобкова Людмила Станіславівна, Суховєєв Володимир Володимирович, Суховєєв Олександр Володимирович, Демченко Анатолій Михайлович
Формула / Реферат
5-Бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5Н-тіазоло [4,5-d] піридазинон-4
 ,
,
що має протипухлинні властивості.
Текст
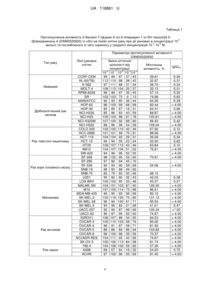
Реферат: 5-Бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5Н-тіазоло [4,5-d]піридазинон-4. Має протипухлинні властивості. UA 118861 U (12) UA 118861 U UA 118861 U Корисна модель належить до органічної, фармацевтичної хімії та медицини, а саме до одержання біологічно активного 5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5H-тіазоло[4,5d]піридазинону-4 (DAM0020930), що має формулу: O N N N N S O DAM0020930 5 10 15 20 25 30 Зазначена сполука проявляє протипухлинну активність та може бути використана при лікуванні лейкемії, клітин раку товстого кишечнику, меланоми та простати. Фармакотерапію пухлинної патології все ширше застосовують у клінічній практиці. У процесі лікування кожного онкологічного хворого розглядається питання щодо можливості та доцільності застосування хіміотерапії. Число пухлинних захворювань, при яких хіміотерапія може сприяти повному виліковуванню, невелика. До них належать лімфогранулематоз, гемобластози, злоякісні герміногенні пухлини, рак передміхурової залози, яєчників і сечового міхура, мієломни, гострі лейкози, дрібноклітинний рак легенів та деякі інші. На регресію пухлини з можливим продовженням життя можна розраховувати у 20-50 % хворих на рак шлунку, меланому, рак молочної залози, тіла матки, плоскоклітинний рак голови та шиї, саркому. Але малочутливими до хіміотерапії є рак щитовидної залози, печінки, підшлункової залози, нирок, шийки матки і піхви [1]. Тому розробка нових протибластомних засобів є нагальною проблемою сучасної фармацевтичної хімії. Усі протипухлинні синтетичні препарати поділяють на ряд груп, а саме: алкілуючі засоби та антиметаболіти. До алкілуючих засобів належать похідні хлоретил аміну, етиленіміну, метансульфонової кислоти, нітрозосечовини та сполуки платини. До антиметаболітів антагоністи фолієвої кислоти, антагоністи пурину та піримідину [2]. Еталоном для порівняння протипухлинної активності заявленої сполуки використано препарат з групи антагоністів піримідину - 5-фторурацил. Зазначений антибластомний засіб пригнічує процес ділення ракових клітин, блокуючи синтез ДНК. Він пригнічує ріст і розвиток пухлин, а також гемопоез. 5-Фторурацил використовують при лікуванні меланоми, раку товстого кишечнику, прямої кишки, раку молочної залози, шлунка, печінки, карциноми ендометрії, раку яєчників та сечового міхура. При застосуванні препарату може спостерігатися пригнічення кровотворення, центральної нервової системи, порушення серцево-судинної, травної та репродуктивної систем, дерматологічні та алергічні реакції [3]. Аналогом за структурою є протипухлинний лікарський засіб іміфос, який є похідним тіазолідину - азирідинілметилтіазолідинілфосфіноксид [4]: S CH3 N N P N O 35 40 Іміфос є алкілувальною сполукою, що пригнічує розвиток проліферуючої, включаючи злоякісну, тканини за рахунок порушення обміну нуклеїнових кислот і блокування мітотичного ділення клітин. Його застосовують для лікування хворих на еритремію, яка обумовлена розростанням клітин кісткового мозку та появою в кровеносному руслі значного числа формених елементів крові тощо. При застосуванні іміфосу може розвиватися лейкопенія (знижений вміст лейкоцитів в крові), тромбоцитопенія (зменшення числа тромбоцитів в крові) та алергічні реакції, що є показаннями, щоб відмінити препарат. Протипоказаннями для застосування препарату також є анемія, кахексія, серцево-судинна недостатність, порушення функції печінки, підвищена чутливість до іміфосу. 1 UA 118861 U 5 10 15 20 Підвищення ефективності хіміотерапії пухлинної хвороби в першу чергу пов'язано зі створенням нових, ефективних протипухлинних препаратів [5]. В основу патенту на корисну модель поставлена задача пошуку нової речовини, що проявляє високу протипухлинну активність - здатність пригнічувати ріст клітин раку відносно лейкемії, товстого кишківника, меланоми та простати. Поставлена задача вирішується шляхом синтезу нової хімічної речовини -5-бензил-7(фуран-2-іл)-2-піперидин-1-іл-5Н-тіазоло[4,5-d]піридазинону-4 (DAM0020930). Заявлену сполуку одержують у декілька стадій (схема 1). Ключовий ізотіоцінатоєстер 2 синтезований по модифікованій нами відомій методиці [6], із етилхлорформіату як каталізатора. Піперидин-1-карботіоамід 4 був одержаний при конденсації піперидину та сухого роданіду калію в присутності тетраетил-етилендіаміну (TMEDA) з ізотіоціанатом 2 та подальшому гідролізі естеру 3 за відомою методикою [7]. Синтезований піперидин-1-карботіоамид 4 був введений в конденсацію з метиловим естером 3-хлор-2,4-діоксо-4-(α-фурил)масляної кислоти 7 в умовах класичної реакції Ганча [8]. Оскільки метиловий естер 3-хлор-2,4-діоксо-4-(α-фурил) масляної кислоти 7 є малостійким маслом, то він був одержаний однореакторно хлоруванням естеру 2,4діоксо-4-(α-фурил)масляної кислоти 6 хлористим сульфурилом. Метиловий естер 2-піперидин1-іл-5-(α-фуроїл)-тіазол-4-карбонової кислоти 8 був зациклізований у 2-піпіридин-7-(α-фуроїл)5Н-тіазоло[4,5-d]піридазин-4-он 9 кип'ятінням у спиртовому розчині гідразингідрату. Останній легко алкілується в ДМФА за наявності К2СО3 до 5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5Hтіазоло[4,5-d]піридазинону-4(DАМ0020930). Схема 1. Синтез 5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5H-тіазоло[4,5-d]піридазинону4(ВАМ0020930). O Cl EtO S N EtO 1 S O O O N N H EtO 4 3 2 O O N H2 N O O SO2Cl2 O O 4 O O Cl Me 5 6 O OMe 7 O OMe O N N S 8 COOMe N N2H4 N O S O 9 PhCH2Cl K2CO3 O N N N N S O DAM002930 2 NH N O UA 118861 U 5 10 15 20 25 30 35 40 45 50 55 Протипухлинна активність 5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5H-тіазоло[4,5d]піридазинону-4 (DAM0020930) вивчалась у Національному інституті раку США (National Cancer Institute of Health, USA) в рамках Development Therapeutic Program. Приклади конкретного виконання. Ізотіоціанатоестер (2) був одержаний із етилхлорформіату та сухого калію роданіду в присутності тетраметилетилендіаміну (TMEDA) як каталізатора за методом [6]. Піперидин-1карботіоамід (4) був одержаний за методикою [7]. Метил-2,4-діоксо-4-(α-фуроїл)-бутаноат (6) одержано за відомою конденсацією Клайзена на основі 2-ацетилфурану (2) та діетилоксалату в присутності натрій метилату за методом [9]. Приклад 1. Синтез метилового естеру 2-піперидин-1-іл-5-(α-фуроїл)-тіазол-4-карбонової кислоти (8). До розчину 9.8 г (0.05 моль) метил 2,4-діоксо-4-(α-фурил)-бутаноату (6) в 100 мл сухого хлороформу, нагрітого до 50 °C, при перемішуванні додавали по краплях 4.05 мл (0.05 моль) сульфурилхлориду. Реакційну суміш кип'ятили 2 години до повного припинення виділення газів. Після чого випарювали до сухого залишку. Вихід 7.26 г (63 %). Утворений метиловий естер 3-хлор-2,4-діоксо-4-(α-фурил)масляної кислоти (7) використовували без додаткової очистки. До розчину 2.306 г (0.01 моль) хлорпохідного (7) у 80 мл метанолу при перемішуванні додавали з 1.442 г (0.01 моль) тіоаміду (4). Кип'ятили зі зворотним холодильником 4 години. Суміш охолоджували та додавали 200 мл води. Підлужнювали 0.1 Н розчином NaOH до рН=8. Осад, що утворився, швидко відфільтровували, сушили. Кристалізували з метанолу. Вихід 2.496 г (78 %). Тпл= 145-147 °C. Знайдено, %: N=8.65 S=10.2. C15H16N2O4S. Вирахувано, %: N=8.74 S=10.0. Спектр ПМР (ДМСО-d6, ТМС): 1.68-1.72 (м, 6Н, піперидин), 3.56 (м, 4Н, піперидин), 3.85 (с, 3Н, ОСН3), 6.68 (т, 1Н, фурил), 6.95 (д, 1Н, фурил), 7.83 (д, 1Н, фурил). Приклад 2. Синтез 2-піперидин-1-іл-7-(α-фуроїл)- 5Н-тіазоло[4,5-d]піридазин-4-ону (9). До суспензії 1.60 г (0.005 моль) кетоестеру (8) в 100 мл етилового спирту додавали двократний надлишок гідразин-гідрату та кип'ятили зі зворотним холодильником 4 години. Суміш охолоджували. Осад, що утворився, відфільтровували. Кристалізували із суміші ДМФА: етанол (1:1). Вихід 1.32 г (87 %). Тпл=292-293 °C. Знайдено, %: N=18.4 S=10.7. C14H14N4O2S. Вирахувано, %: N=18.5 S=10.6. Спектр ПМР (ДМСО-d6, ТМС): 1.65-1.69 (м, 6Н, піперидин), 3.55 (м, 4Н, піперидин), 6.67 (т, 1Н, фурил), 6.96 (д, 1Н, фурил), 7.85 (д, 1Н, фурил), 13.0 (с, 1Н, NH). Приклад 3. 5-Бензил-7-(фуран-2-іл)-2-піпериди-1-іл-5H-тіазоло[4,5-d]піридазинон-4 (DAM0020930): До розчину 1.208 г (0.004 моль) 2-піперидин-1-іл-7-(α-фуроїл)- 5Н-тіазоло[4,5d]піридазин-4-ону (9) в 40 мл диметил-формаміду при перемішуванні додали еквімолярну кількість К2СО3 і поступово 0.004 моль бензилхлориду. Реакційну суміш перемішували при 80 °C протягом 40 хвилин, охолодили та додали 200 мл води. Осад, що утворився, відфільтровували та промивали водою. Кристалізували із суміші ДМФА: етанол (1:1). Вихід - 0.911 г (58 %). Тпл=173-175 °C. Знайдено, %: N=14.1 S=8.27. C21H20N4O2S. Вирахувано, %: N=14.3 S=8.17. Спектр ПМР (ДМСО-d6, ТМС):1.63 (м, 6Н, 3СН2 піперидин), 3.68 (м, 4Н, CH2NCH2), 5.19 (с, 2Н, СН2), 6.76 (дд, 1Н, фурил), 7.10 (д, 1Н, фурил), 7.26-7.56 (м, 5Н, Ph), 7.96 (д, 1Н, фурил). Приклад 4. Перший етап фармакологічного скринінгу (прескринінг) полягав у дослідженні протипухлинної активності сполук in vitro на лініях ракових клітин (лейкемії, меланоми, раку легень, товстого кишечнику, ЦНС, яєчників, нирок, простати, молочної залози) при дії речовини 5 в концентрації 10~ моль/л за стандартною процедурою [10] оцінки мітотичної активності нових потенційних біологічно активних сполук методом флуоресцентного зафарбування (барвник сульфородамін Б). Результат проведених досліджень виражали у відсотках росту клітин раку у порівнянні з контролем - 5-флуорурацилом. Наведені у таблиці значення показують на скільки досліджувані сполуки є більш ефективними у пригніченні росту ракових клітин у порівнянні з контролем. Визначення проводили флюорометричним методом, кількісно оцінюючи інтенсивність кольору флуоресцентного випромінювання (барвник - сульфородамін Б) через 48 год. опромінення клітини зі сполукою, що тестується. Використана система відбору та вивчення сполук з потенційною протипухлинною активністю in vitro базується на визначенні відсотку росту клітин пухлини (PG) під впливом сполуки, що тестується. -5 В умовах експерименту заявлена сполука (DAM0020930) у концентрації 10 моль/л виявила здатність пригнічувати ріст клітин раку, що охоплює практично весь спектр онкологічних захворювань людини (табл. 1). 3 UA 118861 U Таблиця 1 Протипухлинна активність 5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5Н-тіазоло[4,5-5 d]піридазинону-4 (DAM0020930) in vitro на лініях клітин раку при дії речовин в концентрації 10 -4 -8 моль/л та поглибленого in vitro скринінгу у градієнті концентрацій 10 -10 М. Тип раку Лейкемія Дрібноклітинний рак легенів Рак товстого кишечнику Рак кори головного мозку Меланома Рак яєчників Рак нирок Лінії ракових клітин CCRF-CEM HL-60(TB) K-562 MOLT-4 RPMI-8226 SR А549/АТСС НОР-62 НОР-92 NCI-H226 NCI-H23 NCI-H322M NCI-H522 COLO 205 НСС-2998 НСТ-116 НСТ-15 НТ29 КМ12 SW-620 SF-268 SF-295 SF-539 SNB-19 SNB-75 U251 LOX IMVI MALME-3M М14 MDA-MB-435 SK-MEL-2 SK-MEL-28 SK-MEL-5 UACC-257 UACC-62 IGROV1 OVCAR-3 OVCAR-4 OVCAR-5 OVCAR-8 NCI/ADR-RES SK-OV-3 786-0 A498 ACHN Параметри протипухлинної активності DAM00020930 Зміна оптичної щільності від Мітотична lgGI50 концентрації активність, % -8 -7 -6 -5 -4 10 10 10 10 10 99 99 87 37 43 39.81 -5.26 112 110 98 28 43 32.97 -5.31 97 111 88 31 34 38.70 -5.34 108 113 104 25 37 33.13 -5.31 99 98 97 35 45 57.13 -5.25 102 103 73 6 13 19.98 -5.65 92 93 85 36 44 64.39 -5.29 96 100 99 68 68 82.44 >-4.00 82 85 67 18 31 64.31 -5.66 85 96 83 43 59 68.87 >-4.00 100 103 98 81 78 105.81 >-4.00 107 104 92 68 80 99.40 -5.42 88 96 98 54 58 109.04 >-4.00 102 105 110 43 46 67.92 -5.10 101 101 99 70 81 88.66 >-4.00 104 104 92 29 31 36.09 -5.34 94 94 55 23 24 33.00 -5.83 109 107 115 43 46 63.84 -5.10 104 107 104 51 52 75.81 >-4.00 94 96 96 50 55 >-4.00 98 102 95 52 60 73.61 >-4.00 97 92 94 45 70 92 93 90 58 69 54.06 >-4.00 98 93 88 49 82 82 79 80 50 66 68.15 95 92 80 32 43 42.03 -5.38 100 102 95 33 46 45.57 -5.27 104 101 103 87 90 126.00 >-4.00 101 105 114 73 88 86.51 >-4.00 96 95 95 56 66 80.10 >-4.00 102 119 120 75 80 131.12 >-4.00 96 94 100 61 71 95.54 >-4.00 93 95 83 21 28 41.01 -5.47 92 90 87 69 69 105.34 >^.00 96 97 95 52 60 74.87 >-4.00 106 107 98 54 65 84.53 >-4.00 105 110 103 58 76 85.06 >-4.00 96 91 87 58 71 81.50 >-4.00 88 88 89 86 94 103.82 >-4.00 98 100 98 39 56 70.37 >-4.00 104 111 95 42 66 74.67 >-4.00 100 106 113 84 98 81.74 >-4.00 104 108 102 59 82 57.36 >-4.00 69 57 64 16 32 54.20 -5.70 97 102 96 55 69 81.40 >-4.00 4 UA 118861 U Рак простати Рак молочної залози 5 10 15 20 25 30 35 40 45 CAKI-1 RXF393 SN12C TK-10 UO-31 PC-3 DU-145 MCF7 MDA-MB231/ATCC HS 578T BT-549 T-47D MDA-MB-468 94 86 95 92 91 103 107 95 92 89 91 96 98 96 110 93 52 53 79 56 64 42 67 59 65.17 73.30 91.76 99.38 70.30 36.66 97.05 72.26 >-4.00 >-4.00 -5.42 >-4.00 102 104 90 48 60 66.47 95 100 91 79 61 53 54 47 84.85 58.16 74.53 91.67 >-4.00 >-4.00 >-4.00 92 98 96 91 88 72 88 89 85 71 105 94 88 96 96 81 33 30 53 48 49 35 61 49 66 58 71 61 Відповідно до табл. 1, сполука 5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5Н-тіазоло[4,5d]піридазинон-4 перевищує еталон на 54 лініях ракових клітин з 60, що досліджувалися. Найбільш ефективним (DAM0020930) виявився відносно лейкемії (перевищує дію 5фторурацилу на усі лінії клітин від 42,87 % для RPMI-8226 до 80,02 % для SR), клітин раку товстого кишечнику COLO 205, НТ-29, НСТ-116 та НСТ-15 (перевищує дію еталону на 32,08 %, 36,16 %, 63,91 % та 67,00 % відповідно), раку кори головного мозку U251 - на 57,97 %, меланоми LOX IMVI та SK-MEL-5 - на 54,43 % та 58,99 % відповідно та клітин раку простати РС3 перевищує дію 5-фторурацилу на 63,34 %. На другому етапі досліджень або поглибленому in vitro скринінгу, сполука (DAM0020930) тестувалась у п'яти концентраціях при 10-кратному розведенні (100 μМ, 10 μМ, 1 μМ, 0,1 μМ та 01 μМ) на перелічених лініях ракових клітин людини. У результаті експерименту розраховано три дозозалежні параметри, а саме: GI50 - концентрація сполуки, яка викликає пригнічення росту 50 % клітин лінії; TGI - концентрація, що створює повне пригнічення росту клітин; LC50 концентрація, яка викликає загибель 50 % пухлинних клітин. GI50 інтерпретовано як ефективний рівень інгібування, TGI - як цитостатичний ефект, a LC50 - летальна концентрація, що характеризує цитотоксичну дію. Якщо логарифмічні значення досліджуваних параметрів (lgGI50, lgTGI та lgLC50) є меншими, ніж -4,00, то сполука (DAM0002990) вважається активною [11]. Згідно з результатами ґрунтовного in vitro скринінгу тестована сполука проявила значний рівень протиракової активності. Так, щодо клітин лейкемії значення lgGI50 знаходиться в межах від -5.25 до 5.65, раку товстого кишечнику COLO 205 та НТ-29 lgLC50 становить -5.10, а для НСТ-116 і НСТ-15, складає -5.34 та -5.83 відповідно, раку кори головного мозку U251 lgLC50=5.38, меланоми LOX IMVI та SK-MEL-5 lgLC50=-5.27 та -5.47 відповідно та клітин раку простати РС-3 lgLC50=-5.42. Таким чином, запропонована нова біологічно активна сполука, яка може бути потенційним протипухлинним засобом для лікування лейкемії, клітин раку товстого кишечнику, меланоми та простати. Джерела інформації: 1. Протипухлинні (протибластомні) лікарські засоби. [Електронний ресурс]. Режим доступу: http://pidruchniki.com/68392/meditsina/protipuhlinni_protiblastomni_likarski_zasobi - Назва з екрану. 2. Препарати при онкології. [Електронний ресурс]. Режим доступу: http://fivobio.com/onkologija/2093-preparati-pri-onkologii.html - Назва з екрану. 3. 5-Фторурацил. [Електронний ресурс]. Режим доступу: https://ru.wikipedia.org/wiki/5 %D0 %A4 %D1 %82 %D0 %BE%D1 %80 %D1 %83 %D1 %80 %D0 % B0 %D1 %86 %D0 %B8 %D0 %BB - Назва з екрану. 4. Mifos (Имифос). [Електронний ресурс]. - Режим доступу: http://www.wiki-meds.ru/aktivnyeveshchestva/imifos-1632.htm - Назва з екрану. 5. Хіміотерапевтичні препарати. [Електронний ресурс]. Режим доступу: http://www.pharmencyclopedia.com.ua/article/188/ximioterapevtichni-preparat -Назва з екрану. 6. Gensler W. J. Synthesis of a triazole homo-C-nucleoside / Walter J. Gensler, Sum Chan, David B. Ball // Journal of Organic Chemistry.-1981. - Vol. 46, № 17.-P. 3407-3415. 7. Synthesis of mesoionic triazoline nucleosides / Masataka Yokoyama, Toshihiro Ikuma, Nobutoshi Obara, Hideo Togo // Journal of the Chemical Society, Perkin Transactions 1: Organic and Bio-Organic Chemistry (1972-1999).-1990. - № 12. - P. 3243-3247. 5 UA 118861 U 7 5 10 8. Патент 2011121137 WO, МПК A 61 К 31/495, A 61 P 25/00, A 61 P 29/00, С 07 D 487/04. Novel nk-3 receptor selective antagonist compounds, pharmaceutical composition and methods for use in nk-3 receptors mediated disorders / Hamid Hoveyda, Marie-Odile Roy, Graeme Lovat Fraser, Guillaume Dutheuil; Euroscreen S. A. - № 2011EP55218; заявл. 04.04.2011; опубл. 06.10.2011. 7 9. Пат. 2003/0212054 США, МПК А 61 К 31/553, А 61 К 31/47. Substituted amino methyl factor XA inhibitors / M. L. Quan, R. R. Wexler; Bristol-myers squibb company. -№ 10304810; заявл. 26.11.2002; опубл. 13.11.2003. 10. Teicher B.A. Anticancer drug development guide: preclinical screening, clinical / B.A. Teicher, P. A. Andrews. - Medical.-2004. - V. 1.-450 p. ll.Grever M.R. The National Cancer Institute: cancer drug discovery and development program / M.R. Grever, S.A. Schepartz, B.A. Chabner // Seminars in Oncol.-1992. - Vol. 19, № 6. - P. 622-638. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 15 5-Бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5Н-тіазоло [4,5-d]піридазинон-4 O N N S N N O , що має протипухлинні властивості. Комп’ютерна верстка Л. Бурлак Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 6
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61K 31/00, C07D 487/00
Мітки: 5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5н-тіазоло[4,5-d]піридазинон-4, властивості, протипухлинні, має
Код посилання
<a href="https://ua.patents.su/8-118861-5-benzil-7-furan-2-il-2-piperidin-1-il-5n-tiazolo45-dpiridazinon-4-shho-maeh-protipukhlinni-vlastivosti.html" target="_blank" rel="follow" title="База патентів України">5-бензил-7-(фуран-2-іл)-2-піперидин-1-іл-5н-тіазоло[4,5-d]піридазинон-4, що має протипухлинні властивості</a>
Попередній патент: Спосіб діагностики схильності до хронічного генералізованого катарального гінгівіту у дітей, хворих на муковісцидоз
Наступний патент: Спосіб лікування функціональних розладів жовчовивідних шляхів у дітей із застосуванням квіткового пилку
Випадковий патент: Спосіб виготовлення тонких електродів