Сполука включення b-циклодекстрину з тетраетилтіурамдисульфідом
Номер патенту: 30633
Опубліковано: 11.03.2008
Автори: Подолян Ілля Костянтинович, Ганін Едуард Вікторович, Юзюк Людмила Іванівна
Формула / Реферат
Сполука включення b-циклодекстрину з тетраетилтіурамдисульфідом, що має формулу
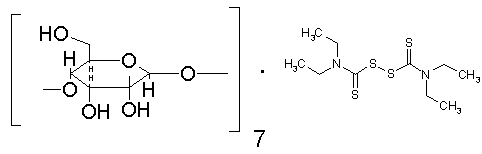 ,
,
проявляє фармакологічні властивості, аналогічні тетраетилтіурамдисульфіду, й здатна розчинятися у воді.
Текст
Сполука включення b-циклодекстрину з тетраетилтіурамдисульфідом, що має формулу 2 3 30633 Недоліком відомого тетурама є те, що він не розчинний у воді. Це не дозволяє його вводити в організм людини у вигляді розчину внутрівенно, або внутрім’язно у вигляді ін’єкцій. Тетурам використається у вигляді таблеток перорально. Або вшивається підшкірно. Це з’єднання обране як прототип. Завданням, на яке спрямоване описувана пропозиція, є створення хімічної сполуки, що має технічний результат - здатність створеного з’єднання розчинятися у дистильованій воді зі збереженням перерахованих фармацевтичних властивостей тетраетілті урамдісульфіду. Нове з’єднання включення одержують взаємодією вихідних компонентів bциклодекстрину і тетраетілтіурамдісульфіду у водно-органічному середовищі. Нове синтезоване з’єднання включення має аналогічні тетраетілтіурамдісульфіду фармацевтичні властивості (блокуючи ферментну биотрансформацию алкоголю збільшує концентрацію ацетальдегіду у крові). Структурна формула нового з’єднання включення наведена нижче. HO H O H3 C H H O H OH OH O . H3 C S N S S S N C H3 C H3 7 Це підтверджується проведеними дослідженнями створеного з’єднання включення різними способами. Структура перевірялася на приладах Derivatograph Q-1000D й 1Н NMR на приладі Varian WXP-300 (299.95 MHz) у D MSOd6 (99.9%), внутрішній стандарт - TMS. На Фіг. 1 зображена термограма bциклодекстрину при зміні температури від 20°С до 500°С і швидкості нагрівання 5 град у хв. На Фіг. 2 зображена термограмма з’єднання bциклодекстрин - тетраетілтіурамдісульфід при зміні температури від 20°С до 500°С і швидкості нагрівання 5 град у хв. На Фіг. 3 зображена термограма механічної суміші b-циклодекстрину (3 моль) й тетраетілтіурамдісульфіду (1 моль) при зміні температури від 20°С до 500°С і швидкості нагрівання 5 град у хв.. На Фіг. 4 зображено теоретичний 1Н NMR спектр - набір піків обумовлених сигналами метільних і метіленових протонів для тетраетілтіурамдісульфіду. На Фіг. 5 зображено теоретичний 1Н NMR спектр - набір піків обумовлених сигналами метільних і метиленових протонів для bциклодекстрину. На Фіг. 6 зображено реальний 1Н NMR спектр набір піків обумовлених сигналами метільних і метіленових протонів для b-циклодекстрину. На Фіг. 7 зображено реальний 1Н NMR спектр набір піків обумовлених сигналами метільних і 4 метіленових протонів для b-циклодекстрину висушеного при температурі 135°С. На Фіг. 8 зображено реальний 1Н NMR спектр набір піків обумовлених сигналами метільних і метіленових протонів для тетраетілтіурамдісульфіду. На Фіг. 9 зображено реальний 1Н NMR спектр набір піків обумовлених сигналами метільних і метіленових протонів для з’єднання bциклодекстрину й тетраетілтіурамдісульфіду висушеного при температурі 20-25°С. На Фіг. 10 зображено реальний 1Н NMR спектр - набір піків обумовлених сигналами метільних і метіленових протонів для з’єднання bциклодекстрину з тетраетілтіурамдісульфідом, перекристаллизованного і висушеного при температурі 20-25°С. На Фіг. 11 зображено реальний 1Н NMR спектр - набір піків обумовлених сигналами метільних і метіленових протонів для з’єднання bциклодекстрину з тетраетілтіурамдісульфідом, висушеного при температурі 135°С на протязі 4 годин. Одержання описуваного з’єднання ілюструється наступним прикладом. Приклад 1 1 ммоль b-циклодекстрину і 1 ммоль тетраетілтіурамдісульфіду розчиняли у 50мл 75% розчину метанолу при температурі 60-65°С. Тверде кристалічне з’єднання, що випало, відокремлювали декантацією, промивали 25мл етанолу і сушили на протязі 7 годин. Одержали кристали розміром 0,01-0,02мм. Вихід 96% відносно активного інгредієнту bциклодекстрину. Визначали температуру плавлення отриманого з’єднання включення; Грошев А.П. Технический анализ. -М.: Госхимиздат. 1953, с.426. Визначали зміст сірки в з’єднанні включення методом спалювання: Климова В.А. - Основные микрометоды анализа органических соединений. М.: Химия, с.23, 59. Проводили перекристалізацію нового з’єднання включення з 50% водно-спиртової суміші. Визначали розчинність і стабільність нового з’єднання включення у дистильованій воді. Записували термограми b-циклодекстрину, нового з’єднання включення, механічної суміші bциклодекстрину (3 моль) і тетраетілтіурамдісульфіду (1 моль) на деріватографі, прилад: Derivatograph Q-1000D. 1 Записували Н NMR спектри bциклодекстрину, нового з’єднання включення, тетраетілтіурамдісульфіду на приладі Varian WXP300 (299.95 MHz) в DMSOd6 (99.9%), внутрішній стандарт-TMS. Визначали на пацюках фармакологічні властивості з’єднання. Температура плавлення нового з’єднання включення становить 272-275°С. Температура плавлення b-циклодекстрину становить 298°С. 5 30633 Температура плавлення тетраетілтіурамдісульфіду становить 72°С. При перекристалізації нового з’єднання включення випали кристали білого кольору. Температура їхнього плавлення становить 272-275°С. Порівняння температур плавлення говорить про те, що отримано все те ж нове з’єднання включення. Розчинність нового з’єднання включення при 25°С у дистильованій воді становить 1мг/мл, при 65°С - 10мг/мл. Водяний розчин нового з’єднання включення 10мг/мл стерилізували при 100°С протягом 30хв. Потім розчин прохолоджували до 25°С. Протягом 12 годин осад не утворюється. Визначили кількість сірки в новому з’єднанні включення - S = 3,47% Обчислили по формулі С136Н230О 105 S 4 - S = 3,22%. Диференціальний термічний (крива ДТА) і термогравіметрічний (крива ТГ) аналіз проводили на приладі Derivatograph Q-1000D в одному зі стандартних інтервалів температур 20-500°С, що забезпечує одержання повної інформації про хімічне поводження органічних зразків (до їхнього згоряння), зі швидкістю нагрівання 5град/хв у керамічному тиглі, навішення 220-250мг, чутливість запису кривій ДТА - 250мВ. Інтервали температур для приладу Derivatograph Q-1000D можуть бути обрані в межах від 20°С (кімнатна) до 1000°С (максимум для приладу Derivatograph Q1000D) і виставляються в інтервалах: 20-250°С, 20-500°С, 20-1000°С. Інтервал 20-500°С дозволяє відстежити фазові перетворення органічних зразків перед їх повної не интерпретируемой термодеструкцией (горінням), що для органічних сполук звичайно починається при 400-500°С. Базова крива термічного аналізу - Т відбиває температуру досліджуваного зразка в тиглі, що обігріває трубчастою піччю із заданою швидкістю нагрівання 5град/хв. На записуваній термограмі крива Т починається в лівому нижньому куті (20°С) і закінчується в правому верхньому - (500°С). На осі абсцис відкладається час - у цьому випадку це 100 хвилин, на осі ординат - температура. Щохвилини температура підвищується на 5град., що й відбиває порівняно плавний підйом цієї кривої: ліворуч праворуч (так обертається барабан приладу). Ця крива не ідеально рівна, як можна було б припустити зі сталості динамічного підвищення температури в 5град/хв, оскільки термопара фіксує температуру зразка, а не пічі. При плавленні або випарі зразків (ендотермічні ефекти) відбувається поглинання зовнішнього тепла печі зразком і спостерігається деяке гальмування підйому температури зразка, а через нього й термопари. При сильних ендотермічних ефектах (характерних найчастіше для неорганічних зразків) на кривій - Т виникає "плато", при сильних екзотермічних ефекта х, навпроти, температура в зразку росте швидше, ніж у пічі. Крива ДТА, на якій заснований диференціальний термічний аналіз, описує результат порівняння (різницю температур) досліджуваного зразка й еталонного тигля з окисом алюмінію, що нагрівають тією же піччю. У 6 цьому випадку, проявляються навіть порівняно слабкі теплові ефекти. Під час відсутності е фектів крива паралельна осі абсцис. Реально, внаслідок зменшення обсягу зразка й оголенні термопари, у порівнянні з еталоном, до кінця процесів крива йде нагору. Ендотермічні ефекти (плавлення, випар зразків) на даній кривій являють собою піки спрямовані вниз. Горіння - екзотермічний процес, крива ДТА йде нагору. Плавлення з термічним розкладанням (окислюванням) - змішаний процес. Крива ТГ (термогравіметричний аналіз) описує зміна маси зразка в процесі нагрівання. Усе той же зразок зважується в процесі динамічного підйому температури. Під час відсутності змін маси крива паралельна осі абсцис. Найчастіше, включаючи наш випадок, спостерігають за зменшенням маси зразка, що носить східчастий характер і прив’язаний до конкретних інтервалів температур. У нашому випадку крива ТГ починається вгорі й східчасто йде вниз. Східчастий збиток описують у відсотках стосовно маси вихідного зразка. З урахуванням температур, може бути встановлений фізико-хімічний характер як, що йдуть у газову фазу речовин, так і що залишаються в тиглі. Цінністю методу є погодженість кривих, тому що всі вони записуються одночасно для того самого зразка. Так, з обліком дані фірми "Acros": bЦиклодекстрин - С42Н70О35 x H2 O; beta-Cyclodextrin hydrate; Т. пл.: 298-300°С; water < 14%, термограма b-циклодекстрину повинна являти собою двоступінчастий процес. На першому етапі убуває вода в районі 100°С і кількості 13.2%, (див.: water < 14%), на другому, у районі 300°С (див.: Т. пл.: 298-300°С) відбувається плавлення з термодеструкцією b-циклодекстрину, складається із цукорідних фрагментів. У нашому випадку деструкція не вимагає повної хімічної інтерпретації. У цілому, розкладається подібно цукрам або клітковині з обвуглюванням і приблизно 70-80% збитком ваги (до 500°С). Дійсно, термограма b-циклодекстрину (Фіг. 1) не суперечить такому припущенню. Крива ТГ описує 2-х східчастий збиток маси зразка. Реально (перший збиток маси), зразок містить 13.2%, ~ 8 моль Н2О на 1 моль b-циклодекстрину, причому процес супроводжується ендотермічним ефектом при 35-105°С (крива ДТА). Другий ефект описує плавлення в інтервалі 293-302°С (крива ДТА), щосупроводжується термодеструкцією зразка з майже повним збитком маси (крива ТГ). У тиглі залишається чорний склоподібний плав з пухирцями газів. Тетраетілтіурамдісульфід - с обліком дані фірми "Acros": Tetraethylthiuram disulfide; Т. пл.: 7074°С повинен мати ендотермічний ефект плавлення в районі 65-75°С (який буде перекриватися або збігатися з ендотермічним эффетом випару води з товарного bциклодекстрину). Другий ендотермічний ефект переходу в газову фазу тетраетілтіурамдісульфіду варто очікувати приблизно при 200-240°С, як для органічних сполук без водневих зв’язків приблизно такої ж молекулярної маси. 7 30633 Дійсно, термограмма однорідної механічної суміші b-циклодекстрину (3 моль) і тетраетілтіурамдісульфіду (1 моль) є результатом накладення ефектів, характерних окремо як для індивідуального b-циклодекстрину, так і для індивідуального тетраетілтіурамдісульфіду (Фіг. 3). Так, на кривій ДТА, на тлі убули ~ 8 моль Н 2О (55-125°С) b-циклодекстрину додатково з’являється ендотермічний ефект плавлення тетраетілтіурамдісульфіду (55-65°С). Потім, до плавлення й термодеструкції b-циклодекстрину (ДТА - 265-275°С) відбувається випар ~ 98% тетраетілтіурамдісульфіду, вкладеного в механічну суміш (ДТА - 200-235°С); при цьому, процес на кривій ТГ супроводжується вираженим щаблем. Процес завершується термодеструкцією b-циклодекстрину при 265-275°С, що тро хи нижче, ніж для чистого товарного 265-275°С bциклодекстрину (293-302°С, Фіг. 1), але цілком виправдано наявністю слідів низькоплавкого тетраетілтіурамдісульфіду. Примітка: домішки приводять до депресії т.пл. чисти х речовин. На відміну від механічної суміші bциклодекстрину і тетраетілтіурамдісульфіду з’єднання включення, що заявляється, (комплекс) (Фіг. 2), містить ~ 4 моль Н 2О (криві ТГ та ДТА), не має ефектів характерних для незв’язаного т тетраетілтіурамдісульфіду. Він стабільний до 250°С (крива ТГ), і плавиться з розкладанням при 250-290°С (криві ТГ і ДТА); візуально т. пл. комплексу 272-275°С (з розкладом). Відзначимо також складний характер кривої ДТА (наявність невеликого екзотермічного ефекту) в інтервалі 250-290°С для термограми з’єднання включення (комплексу) і загальна відмінність термограм отриманого комплексу (Фіг. 2) і вихідного компонента b-циклодекстрину (Фіг.1). Отже, по характері термічних кривих Т, ДТА, ТГ і максимумам температур фазових переходів (Таблиця 1) видно, що отримано нову тверду фазу - з’єднання включення Р-циклодекстрину з тетраетілтіурамдісульфідом. 8 Так, на відміну від механічної суміші, у комплексі відсутній ендотермічний ефект, що відповідає температурі плавлення тетраетілтіурамдісульфіду; комплекс стабільний при 200-235°С, тоді як для механічної суміші в цьому інтервалі температур відбувається перехід у газову фазу одного з компонентів тетраетілтіурамдісульфіду. Відзначимо, що в порівнянні з вихідним b-циклодекстрином комплекс менш обводнений (2-ий ефект і супровідний його процес убули маси зразка, Табл. 1) і піддається деструкції при більше низькій температурі (4-ої ефект і процес, Табл. 1) Таким чином, представлена сукупність даних: температура плавлення, результати диференціального термічного й термогравіметрічного аналізу дозволяє констатувати, що отримано нову стабільну тверду фазу: комплекс b-циклодекстрину з тетраетілтіурамдісульфідом. Склад комплексу (співвідношення в ньому компонент b-циклодекстрин: тетраетілтіурамдісульфід) визначають спектрометрією 1Н NMR. Метод дозволяє як якісно розрізняти протони функціональних гр уп по положенню їхніх сигналів щодо репера TMS (нижня шкала - s, м.д.), так і кількісно визначати їхнє взаємне співвідношення по інтегральній інтенсивності або "ваги" сигналів. Інтегральна інтенсивність записується або у вигляді кривої, або у відносних числови х одиницях. Теоретично (побудований у програмі 1 ACD/HNMR/v.6.12), спектр HNMR тетраетілтіурамдісульфіду являє собою набір піків, представлений на Фіг. 4. Піки в інтервалі 1.25-1.31м.д. обумовлені сигналами метільних протонів (СН3 - груп) тетраетілтіурамдісульфіду. Піки в інтервалі 3.714.04м.д. обумовлені сигналами метіленових протонів (СН2 - гр уп) те траетілтіурамдісульфіду. Інтегральна інтенсивність або "вага" протонів СН3 і СН2 груп (у даній програмі ACD/v.6.12 відбито червоною лінією) співвідноситься між собою як 12:8. Таблиця 1 Теоретичний спектр 1HNMR b-циклодекстрину являє собою набір сигналів, представлений Данітермічного аналізу b-циклодекстрину; нового з’єднання включення b-циклодекстрину з на Фіг. 5. Спектр більше складний. Сумарна кількість тетраетілтіурамдісульфідом; механічної суміші b-циклодекстрину ітетраетілтіурамдісульфіду, отримані на протонів всіх приладі Derivatograph Q-1000D. груп в b-циклодекстрині становить 70Н. Однак, цього досить щоб Ендотермічний ефект, °С [процес]визначати склад № З’єднання [навішення, мг] комплексу по співвідношенню інтенсивності піків 1-ий 2-ий 3-ий 4-ий 5-ий протонів тетраетілтіурамдісульфіду 293-302 ,500 (20Н) і b35-105 [збиток циклодекстрину (70Н), оскільки спектр комплексу [плавл. й 1 b-Циклодекстрин [240] немає 13.2%, ~ 8 моль немає буде накладенням двох вищенаведених спектрів, деструкція аН2О] положення піків протонів зразка] тетраетілтіурамдісульфіду й b-циклодекстрину 60-100 [збиток 250-290,500 З’єднання включення bістотно різні (нижня шкала - s, м.д.). [деструкція 5.5%, ~ 4 моль немає 2 циклодекстрину з немає У Н2О] реальному спектрі положення піків, як зразка] тетраетілтіурамдісульфідом [220] правило, [збиток 200-235 [збитокзалежить трохи інше, що від 55-125 265-275,500 Ме ханічна суміш b- 55-65 використаного ~ 8 100%, розчинника, взаємного впливу 12.5% маси, [плавл. й і (плавлення 3 циклодекстрину компонент, наявності води й ін. факторів. деструкція тетраетілтіурамдісульфіду - (3:1, тетраетілтіура моль Н2О, як тетраетілтіура Так реальні мдісульфіду] спектри (Фіг. мдісульфіду) у№1] зразка] 6-11) моль) [250] характеризуються наступними піками - s, м.д. для: 9 30633 1. тетраетілтіурамдісульфіду - 1.19т*), 1.39т, 3.97м *) (Фіг. 8) 2. b-циклодекстрину - 3.36м, 3.63м, 4.47м, 4.83м, 5.69м, 5.74м (Фіг. 6, Фіг. 7) где: *) т - триплет, м - мультиплет. Реальні спектри комплексів дійсно є як би накладенням спектрів тетраетілтіурамдісульфіду й b-циклодекстрину.(Фіг.9, Фіг. 10, Фіг. 11) Однак раніше було доведено, що отримано нову стабільну тверду фаз у - з’єднання включення bциклодекстрину з тетраетілтіурамдісульфідом. Сумарні інтегральні інтенсивності груп протонів тетраетілтіурамдісульфіду й b-циклодекстрину указують на співвідношення компонентів у комплексі = 1:3. (Фіг. 9, Фіг. 10, Фіг. 11). Контроль якості й складу комплексу здійснюють спектрометрією 1Н NMR на приладі Varian WXP-300 (299.95 MHz) в D MSO d6 (99.9%), внутрішній стандарт -TMS. (Таблиця 2). 10 утруднений подих, підвищене потовиділення й сечовипускання, підвищене каловиділення. Потім активність знизилася, тварини спали, відмовлялися від їжі протягом 20 годин. Стан пацюків помітно покращився тільки через 30 годин після введення розчину. Повторне введення ін’єкції розчину нового з’єднання включення (0,25мг/0,1мл), на тлі прийому алкоголю, викликало таку ж реакцію. Отримані дані підтверджують фармакологічні властивості нового з’єднання включення. Дія нового з’єднання включення засновано на його здатності специфічно впливати на обмін алкоголю в організмі. Алкоголь в організмі піддається окисним перетворенням, проходячи через фазу ацетальдегіду й оцтової кислоти. При участі ферменту ацетальдегідроксідази ацетальдегід звичайно швидко окисляється. Нове з’єднання включення блокує ферментну біотрансформацію алкоголю й сприяє накопиченню ацетальдегіду в організмі 2 Таблиця й приводить до зміни в його діяльності. Відбувається рясне потовиділення, підвищення температури, Дані спектрометрії 1Н NMR b-циклодекстрину; тетраетілті урамдісульфіду; нового з’єднання включення bциклодекстрину з тетраетілтіурамдісульфідом; а такожзбільшення серцебиття. Виробляється негативний нового з’єднання включення b-циклодекстрину з умовний рефлекс на Varian запах тетраетілтіурамдісульфідом перекристалізованого, виконані на приладі смак і WXP-300алкоголю. Фармакологічна активність нового з’єднання включення виявилася подібною 1 № З'єднання(число протонів) Н NMR -спектр, s, м.д. тетраетілтіурамдісульфіду. b-Циклодекстрин (70Н) 3,36м, 3,63м, 4,47м, 4,83м, 5,69м, 5,74м Приклад 2. Процес здійснювали аналогічно 2 Тетраетілтіурамдісульфід (20Н) прикладу 1, використовуючи (2 ммоль) 1,19т, 1,39т, 3,97м тетраетілтіурамдісульфіду. Вихід з’єднання включення становить 89%. 3 З'єднання включення bПриклад 3. Процес здійснювали аналогічно циклодекстрину з 1,19т, 1,39т, 3,36м, 3,63м, 4,48м, 4,83м, 5,69м, 5,74м 3,97м прикладу 1, використовуючи (3 ммоль) тетраетілтіурамдісульфідом тетраетілтіурамдісульфіду. Вихід з’єднання 4 З'єднання включення bвключення становить 82%. циклодекстрину з Приклад 4. Процес здійснювали аналогічно 1,18т, 1,38т, прикладу 3,35м, 3,63м, 4,47м, 4,83м, 5,69м, 5,74м 3,96м тетраетілтіурамдісульфідом 1, використовуючи 0,5 ммоль (перекристалізований)*) тетраетілтіурамдісульфіду. Вихід з’єднання включення становить 79%. Приклад 5. Процес здійснювали аналогічно *) - Інтегральна інтенсивність груп протонів bприкладу 1, використовуючи 0,3 ммоль циклодекстрину і тетраетілтіурамдісульфіду тетраетілтіурамдісульфіду. Вихід з’єднання відповідає складу комплексу 3:1. включення становить 72%. Таким чином, запропонований спосіб Приклад 6. Процес здійснювали аналогічно забезпечує простий і зручний шлях одержання прикладу 1, використовуючи як розчинник 75% водорозчинного з’єднання включення bрозчин етанолу. Вихід з’єднання включення циклодекстрину з тетраетілтіурамдісульфідом, становить 94%. який може бути використаний як проміжний Приклад 7. Процес здійснювали аналогічно продукт при синтезі нових фізіологічно активних прикладу 1, використовуючи як розчинник 75% з’єднань, так і самостійно в біохімічній або розчин пропанолу-2 (ізопропанол). Вихід з’єднання фармацевтичній промисловості. включення становить 85%. Фармакологічні властивості перевіряли на Приклад 8. Процес здійснювали аналогічно білих пацюках з вагою тіла 80гр. 10 особинам прикладу 1, використовуючи як розчинник 50мл пероральне протягом 14 доби через 5 годин води - 125мл метанолу і проводять нагрівання уводили розрахована кількість алкоголю (0,1мл вихідних компонентів при 50°С протягом 1,5год. до 30% розчину спирту). Реєстр ували їхній стан. повного їхнього розчинення. Вихід з’єднання Після введення алкоголю, на 10 добу активність включення становить 70%. трохи знизилася. Однак у цілому поводження й Приклад 9. Процес здійснювали аналогічно стан протягом 14 доби не змінилося. прикладу 1, проводячи нагрівання вихідних На 15 добу особинам перорально ввели компонентів при 35°С. Повного розчинення bрозраховану, фармакологічно активну, кількість циклодекстрину протягом 3год. не відбулося. нового з’єднання включення (0,25мг/0,1мл). Результати одержання нового з’єднання Через 2 години у тварин реєструвалося включення b-циклодекстрину з неспокійне поводження, сильна пульсація, тетраетілтіурамдісульфідом наведені в табл. 3. 11 30633 12 Перевірка способів одержання нового з’єднання включення при різних співвідношеннях вихідних компонентів показала, що отримано те саме з’єднання, зазначеної вище формули. Приклади 6 й 7 показали, що при заміні розчинника (метанолу) на етанол і пропанол-2 одержали те ж з’єднання включення із зазначеною вище формулою. Результати перевірки властивостей отриманого з’єднання включення в прикладах 1-8 такі ж, як і у прикладі 1. Таблиця 3 Результати одержання нового з’єднання включення b-циклодекстрину з тетраетілтіурамдісульфідом у різних розчинниках і різних молярних співвідношеннях Прикла д Розчинник b-Циклодекстрин Тетраетілтіурамдісу Співвіднош льфід (II) (І) ення І:II мг моль мг моль Вода 1 1285 1 ммоль 296 1 ммоль 1:1 метанол Вода 2 1285 1 ммоль 592 2 ммоль 1 :2 метанол Вода 3 1285 1 ммоль 888 3 ммоль 1 :3 метанол Вода 4 1285 1 ммоль 148 0,5 ммоль 1 :0.5 метанол Вода 5 1285 1 ммоль 99 0,3 ммоль 1 :0.3 метанол 6 Вода - этанол 1285 1 ммоль 296 1 ммоль 1:1 Вода 7 1285 1 ммоль 296 1 ммоль 1:1 пропанол-2 Вода 8 1285 1 ммоль 296 1 ммоль 1:1 метанол Вода 9 1285 1 ммоль 296 1 ммоль 1:1 метанол 1 *) - Склад комплексу встановлений на підставі Н NMR спектрів Вихід Склад комплексу *) мг % 1240 96 3 1 1160 89 3 1 1060 82 3 1 1030 79 3 1 940 72 3 1 1220 94 3 1 1110 85 3 1 910 70 3 1 Комплекс не отриманий 13 30633 14 15 30633 16
ДивитисяДодаткова інформація
Назва патенту англійськоюClathrate of b-cyclodextrin with tetraethyl thiuram disulphide
Автори англійськоюYuziuk Liudmyla Ivanivna, Podolayn Illay Kostayntynovich, Hanin Eduard Viktorovich
Назва патенту російськоюСоединение включения b-циклодекстрина с тетраэтилтиурамдисульфидом
Автори російськоюЮзюк Людмила Ивановна, Подолян Илья Константинович, Ганин Эдуард Викторович
МПК / Мітки
МПК: C08B 37/16, C07D 323/00
Мітки: тетраетилтіурамдисульфідом, сполука, b-циклодекстрину, включення
Код посилання
<a href="https://ua.patents.su/8-30633-spoluka-vklyuchennya-b-ciklodekstrinu-z-tetraetiltiuramdisulfidom.html" target="_blank" rel="follow" title="База патентів України">Сполука включення b-циклодекстрину з тетраетилтіурамдисульфідом</a>
Попередній патент: Спосіб експлуатації жалюзійного решета очистки зернового вороху
Наступний патент: Пристрій захисту мікрохвильових приймачів
Випадковий патент: Спосіб регулювання температури випромінюючого факела газового пальника та газовий пальник з регульованою температурою випромінюючого факела












