Спосіб одержання (1r, 2s, 4r)-(-)-2-[(2′-{n,n-диметиламіно}-етокси)]-2-[феніл]-1, 7, 7-три-[метил]-біцикло[2.2.1]гептану і його фармацевтично прийнятних кислотних адитивних солей
Номер патенту: 49974
Опубліковано: 15.10.2002
Автори: Мезеі Тібор, Суладьі Янош, НЕМЕТ Норберт, Надь Кальман, Порч-Маккаі Марта, ШІМІГ Дьюла, САБО Тібор, ДОНАТ ВЕРЕЦКЕІ Дьйордьі, Краснаі Дьйордь, Лукач Дьюла, Будаі Золтан
Формула / Реферат
1. Спосіб одержання (1R, 2S, 4R)-(-)-2-[(2'-{N,N-диметиламіно}-етокси)]-2-[феніл]-1,7,7-три-[метил]-біцикло[2.2.1]гептану формули
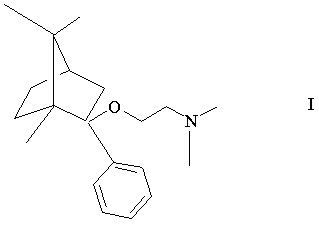
і його фармацевтично прийнятних кислотних адитивних солей, що включає перетворення (+)-1,7,7-три-[метил]-біцикло[2.2.1]гептан-2-ону {(+)-камфори} формули
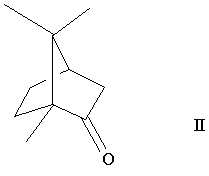
у (1R, 2S, 4R)-(-)-2-[феніл]-1,7,7-три-[метил]-біцикло[2.2.1]гептан-2-ол формули
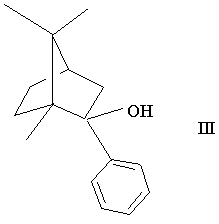
шляхом реакції сполуки формули II з металорганічною сполукою, зі здійсненням, якщо необхідно, руйнування продукту реакції, і реакцію одержаного в такий спосіб (1R,2S,4R)-(-)-2-[феніл]-1,7,7-три-[метил]-біцикло-[2.2.1]гептан-2-олу формули III з (2-{галогено}-етил)-диметиламіном у присутності агента, що утворює основну сіль, в органічному розчиннику, і, якщо потрібно, перетворення в такий спосіб одержаної основи (1R, 2S, 4R)-(-)-2-[(2'-{N,N-диметиламіно}-етокси)]-2-[феніл]-1,7,7-три-[метил]-біцикло[2.2.1]гептану формули І у сіль, який відрізняється тим, що реакцію (1R, 2S, 4R)-(-)-2-[феніл]-1,7,7-три-[метил]-біцикло[2.2.1]гептан-2-олу формули III з (2-{галогено}-етил)-диметиламіном проводять у середовищі, що містить 1 або більше сполуку(и), що має(ють) 5- або 6-членне насичене гетероциклічне кільце з 2 атомами кисню в кільці, узятому як розчинник(и).
2. Спосіб згідно з п.1, який відрізняється тим, що як розчинник використовують діоксан.
3. Спосіб згідно з пп.1 або 2, який відрізняється тим, що як металорганічну сполуку в реакції Гриньяра використовують фенілмагній галогенід.
4. Спосіб згідно з будь-яким з пп. від 1 до 3, який відрізняється тим, що використовують фенілмагній бромід.
5. Спосіб згідно з будь-яким з пп. від 1 до 3, який відрізняється тим, що використовують фенілмагній хлорид.
6. Спосіб згідно з будь-яким з пп. від 1 до 5, який відрізняється тим, що як 2-(2'-{галогено}-етил)-диметиламін використовують 2-(2'-{хлоро}-етил)-диметиламін.
7. Спосіб згідно з будь-яким з пп. від 1 до 6, який відрізняється тим, що як агент, що утворює основну сіль, використовують амід натрію.
8. Спосіб згідно з будь-яким з пп. від 1 до 7, який відрізняється тим, що реакцію алкілування (1R, 2S, 4R)-(-)-2-[феніл]-1,7,7-три-[метил]-біцикло[2.2.1]гептан-2-олу формули III з 2-(2'-{галогено}-етил)-диметиламіном здійснюють при нагріванні, зокрема при температурі кипіння реакційної суміші.
9. Спосіб згідно з будь-яким з пп. від 1 до 8, який відрізняється тим, що шляхом перетворення основи (1R, 2S, 4R)-(-)-2-[(2'-{N,N-диметиламіно}-етокси)]-2-[феніл]-1,7,7-три-[метил]-біцикло[2.2.1]гептану формули І у сіль одержують 2-(Е)-бутендіоатну (1:1) сіль (фумарат).
10. Спосіб згідно з будь-яким з пп. від 1 до 9, який відрізняється тим, що перетворення (1R, 2S, 4R)-(-)-2-[(2'-{N,N-диметиламіно}-етокси)]-2-[феніл]-1,7,7-три-[метил]-біцикло[2.2.1]гептану формули І у 2-(Е)-бутендіоатну (1:1) сіль (фумарат) здійснюють без виділення сполуки формули І.
Текст
1 Спосіб одержання (1R, 2S, 4R)-(-)-2-[(2'{г\І,г\І-диметиламіно}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло[2 2 1]гептану формули і його фармацевтично прийнятних кислотних адитивних солей, що включає перетворення (+)-1,7,7три-[метил]-біцикло[2 2 1]гептан-2-ону {(+)камфори} формули у (1R, 2S, 4Р)-(-)-2-[феніл]-1,7,7-три-[метил] біцикло[2 2 1]гептан-2-ол формули ОН III шляхом реакції сполуки формули II з металорганічною сполукою, зі здійсненням, якщо необхідно, руйнування продукту реакції, і реакцію одержаного в такий спосіб (1R,2S,4R)-(-)-2-[cpeHin]1,7,7-три-[метил]-біцикло-[2 2 1]гептан-2-олу формули III з (2-{галогено}-етил)-диметиламшом у присутності агента, що утворює основну сіль, в органічному розчиннику, і, якщо потрібно, перетворення в такий спосіб одержаної основи (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™iaMiHo}-eTOKCH)]-2[феніл]-1,7,7-три-[метил]-біцикло[2 2 1]гептану формули І у сіль, який відрізняється тим, що реакцію (1R, 2S, 4R)-(-)-2-[qbeHUT]-1,7,7-TpH-[Me™T]біцикло[2 21]гептан-2-олу формули III з (2{галогено}-етил)-диметиламшом проводять у середовищі, що містить 1 або більше сполуку(и), що має(ють) 5- або 6-членне насичене гетероциклічне кільце з 2 атомами кисню в КІЛЬЦІ, узятому як розчинники) 2 Спосіб згідно з п 1, який відрізняється тим, що як розчинник використовують діоксан 3 Спосіб згідно з пп 1 або 2, який відрізняється тим, що як металорганічну сполуку в реакції Гриньяра використовують фенілмагній галогенід 4 Спосіб згідно з будь-яким з пп від 1 до 3, який відрізняється тим, що використовують фенілмагній бромід 5 Спосіб згідно з будь-яким з пп від 1 до 3, який відрізняється тим, що використовують фенілмагній хлорид 6 Спосіб згідно з будь-яким з пп від 1 до 5, який відрізняється тим, що як 2-(2'-{галогено}-етил)диметиламш використовують 2-(2'-{хлоро}-етил) о 49974 диметиламін 7 Спосіб згідно з будь-яким з пп від 1 до 6, який відрізняється тим, що як агент, що утворює основну сіль, використовують амід натрію 8 Спосіб згідно з будь-яким з пп від 1 до 7, який відрізняється тим, що реакцію алкілування (1R, 2S, 4ї?)-(-)-2-[феніл]-1,7,7-три-[метил]біцикло[2 21]гептан-2-олу формули III з 2-(2'{галогено}-етил)-диметиламшом здійснюють при нагріванні, зокрема при температурі кипіння реакційної суміші 9 Спосіб згідно з будь-яким з пп від 1 до 8, який відрізняється тим, що шляхом перетворення основи (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiH0}етокси)]-2-[феніл]-1,7,7-три-[метил]біцикло[2 2 1]гептану формули І у сіль одержують 2-(Е)-бутендюатну (1 1) сіль (фумарат) 10 Спосіб згідно з будь-яким з пп від 1 до 9, який відрізняється тим, що перетворення (1R, 2S, 4R)(-)-2-[(2'-{г\І,г\І-диметиламіно}-етокси)]-2-[феніл]1,7,7-три-[метил]-біцикло[2 2 1]гептану формули І у 2-(Е)-бутендюатну (1 1) сіль (фумарат) здійснюють без виділення сполуки формули І Винахід стосується способу одержання (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiHo}-eTOKCH)]-2[феніл]-1,7,7-три-[метил]-біцикло[2,2,1]гептану і його фармацевтичне прийнятних кислотних адитивних солей 2-(Е)-бутендюатна (1 1) сіль (фумарат) (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiHo}-eTOKCH)]-2[феніл]-1,7,7-три-[метил]-біцикло[2,2,1]гептану згідно з формулою магнієм бромідом у діетиловому ефірі з одержанням (1R, 2S, 4^-(-)-2-[феніл]-1,7,7-три-[метил]біцикло[2,2,1]гептан-2-олу згідно з формулою є відомим седативним активним компонентом, що має МНН "дерамциклан фумарат" Сполука згідно з формулою 1 підпадає під загальну Формулу 1 Угорського патенту № 179, 164, але в описі винаходу до цього патенту вона фактично не була виразно розкрита, а також її одержання не було підтверджено в прикладах Згідно з Угорським патентом № 179, 164, циклоалкільні ефіри алканоламшу за загальною формулою 1 одержували шляхом реакції (+)-1,7,7-три-[метил]біцикло[2,2,1]гептан-2-ону, тобто (+)-камфори згідно з формулою з ВІДПОВІДНОЮ металоорганічною сполукою, з подальшим гідролізом одержаного адукту, і введенням у гідроксильну групу одержаного продукту основного бічного ланцюга шляхом етерифікації В якості металорганічної сполуки використовується реактив Гриньяра або органічна сполука лужного і/Ієталу, бажано, сполука ЛІТІЮ або натрію Одержання сполуки згідно з формулою 1 було фактично розкрите в Угорському патенті № 212, 574 Сутність цього способу така, що очищення продукту здійснюється на більш ПІЗНІЙ стадії синтезу Згідно З ЦИМ способом, (+)-камфора згідно з формулою II вступає в реакцію Гриньяра з феніл з 38%-им виходом (згідно З газовою хроматографію) Сполука (1R, 2S, 4^-(-)-2-[феніл]-1,7,7три-[метил]-біцикло[2,2,1]гептан-2-ол згідно з формулою III знаходиться в реакційній суміші і не виділяється з неї Далі комплекс руйнується, реакційна суміш переводиться без очищення в натрієву сіль шляхом реакції з амідом натрію або гідридом натрію, і одержана натрієва сіль вступає в реакцію з безводним (2-{хлоро}-етил)диметиламіном у середовищі толуолі Реакційна суміш містить крім основного (1R, 2S, 4R)-(-)-2-[(2'{N,Nдиметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло[2,2,1]гептану згідно з формулою І (що є присутнім у КІЛЬКОСТІ від 20 до 30%) значна КІЛЬКІСТЬ домішок і вихідних продуктів, тобто (+)камфори згідно з формулою II, (1R, 2S, 4R)-(-)-2[феніл]-1,7,7-три- [метил]-біцикло[2,2,1]гептан-2олу, 1,7,7-три-[метил]-біциклр[2,2,1]гептан-2-олу і біфенільних, трифенільних домішок і т д , що не прореагувли Основа (1R, 2S, 4R)-(-)-2- [(2'-{N,Nдиметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло-[2,2,1]гептан згідно з формулою І відокремлюється від цих домішкових речовин екстракцією у водний розчин винної кислоти, після чого основа звільняється й утворюється фумаратна сіль Загальна КІЛЬКІСТЬ (+)-камфори згідно, з формулою II і (1R, 2S, 4^-(-)-2-[фенил]-1,7,7-три[метил]- біцикло[2,2,1]гептан-2-ола згідно з формулою III, що не прореагували, залишається в органічній фазі після стадії екстракції винною кислотою, вона може бути використана повторно в реакції Гриньяра після видалення розчинника і води (тобто можлива його рециркуляція у виробництві) Таким чином, відпрацьована (+)-камфора може бути більш ефективно використана, без рециркуляції тільки 16% за вагою узятої (+)-камфори 49974 може бути використано, у той час як у випадку однократної і триразової рециркуляції ця КІЛЬКІСТЬ зростає до 22% і 25% за вагою ВІДПОВІДНО Таким чином, виходи занадто малі, особливо з погляду комерційної здійсненості Дуже важливим є той факт, і це варто особливо підкреслити, що значна частина (+)-камфори згідно з формулою II, використаної в реакції Гриньяра, не вступає в реакцію, і цей вихідний продукт технічно не може бути вилучений з одержуваного продукту через фізичні властивості (+)камфори і лабільності сполуки, що утворюється, (1R, 2S, 4R)-(-)-2-№eHin]-1,7,7-три-[метил]біцикло[2,2,1]гептан-2-ол згідно з формулою III, оскільки речовина (1R, 2S, 4Р)-(-)-2-[феніл]-1,7,7три-[метил]-біцикло[2,2,1]гептан-2-ол піддана розкладанню Тому згідно із способом, розкритим в Угорському патенті № 212, 574, стадія алкілювання завжди протікає в присутності (+)-камфори згідно з формулою II Усе вищесказане обумовлює недоліки способу, розкритого в Угорському патенті № 212, 574 Гідриди й аміди лужних металів, використані на першій стадії реакції алкілювання, утворюють солі не тільки зі спиртом (1R, 2S, 4Р)-(-)-2-[феніл]-1,7,7три-[метил]-біцикло[2,2,1]гептан-2-ол згідно з формулою 111, але також і (+)-камфорою згідно з формулою II і з іншими присутніми в реакційній суміші сполуками, що містять активний атом водню Тому, крім необхідної сполуки (1R, 2S, 4R)-(-)2-[(2'-{г\І,г\І-диметиламіно}-етокси)]-2-[феніл]-1,7,7три-[метил]-біцикло[2,2,1]гептану згідно з формулою І, утворюються ІНШІ алкільовані ПОХІДНІ, утворені, наприклад, з (+)-камфори, що не прореагувала, і необхідна сполука (1R, 2S, 4R)-(-)-2-[(2'-{N,Nдиметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло[2,2,1]гептан згідно з формулою І повинна бути виділена із суміші, що містить такі домішки і також (н-)-камфору, що не прореагувала, і (1R, 2S, 4R)-(-)-2-[cpeHUT]-1,7,7-TpH-[Me™T]біцикло[2,2,1]гептан-2-ол згідно з формулами II і III Неочищена речовина (1R, 2S, 4R)-(-)-2-[(2'-{N,Nдиметиламшо}-етокси)3-2-[феніл]-1,7,7-три[метил]-біцикло[2,2,1]-гептан згідно з формулою І може бути очищена, причому не повністю, тільки за допомогою перекристалізації з диметилформаміду Однак за допомогою перекристалізації цілком вилучені можуть бути тільки домішки неосновного характеру, що не утворюють солей Іншим недоліком перекристалізації з диметилформаміду є те, що СЛІДОВІ КІЛЬКОСТІ розчинника не можуть бути вилучені в потрібному ступені з необхідного фармацевтичного активного компонента Було виявлено, що у випадку проведення реакції алкілювання ( 1 R , 2S, 4R)-(-)-2-[cpeHU-|]-1,7,7три-[метил]-біцикло[2,2,1]гептан-2-олу згідно з формулою III із застосуванням (2-{хлоро}-етил)диметиламшу в присутності (+)-камфори згідно з формулою II завжди утворюються значні КІЛЬКОСТІ побічних продуктів, наприклад, (1R, 3S, 4R)-3-[(2'{г\І,г\І-диметиламіно}-етил)]-1,7,7-три-[метил]біцикло[2,2,1]гептан-2-он згідно з формулою Побічний продукт (1R, 3S, 4R)-3-[(2'-{N,Nдиметиламшо}-етил)]-1,7,7-три-[метил]біцикло[2,2,1]гептан-2-он згідно з формулою V утворюється за такою схемою в умовах, використовуваних для проведення реакції етерифікації, (+)-камфора згідно з формулою II утворює сіль лужного металу в позиції 3, що, у свою чергу, реагує з (2-[хлоро]-етил)-диметиламшом, використовуваним в якості алкілюючого агента, у результаті утворюється сполука згідно з формулою V КІЛЬКІСТЬ побічного продукту згідно з формулою V може складати від 1 до 10% Розчинність фумарату 2-(Е)-бутендюату (1 1) сполуки (1R, 3S, 4R)-3-[(2'г\І,г\І-диметиламіно}-етил)]-1,7,7-три-[метил]біцикло[2,2,1]гептан-2-ону згідно з формулою V приблизно ідентична з розчинністю фумарату необхідної речовини (1R, 2S, 4R)-(-)-2-[(2'-{N,Nдиметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло [2,2,1]гептану згідно з формулою І, і тому він кристалізується разом з фумаратом сполуки (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiH0}етокси)]-2-[феніл]-1,7,7-три-[метил]-біцикло[2,2,1]гептану згідно з формулою І і забруднює необхідний кінцевий продукт Якщо етерифікація виконується в толуолі, як описано в Угорському патенті № 212, 574, то продукт, одержаний після утворення солі в етанолі, містить значні КІЛЬКОСТІ ДОМІШКИ (1R, 3S, 4R)-3-[(2'-{N,N-flHMe™-iaMiH0}-e™-|)]-1,7,7три-[метил]-біцикло[2,2,1]гептан-2-ону згідно з формулою V Сіль Є дуже нерозчинною сполукою і може бути перекристалізована тільки з диметилформаміду Однак при проведенні перекристалізації з диметилформаміду неможливо одержати сполуку (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiHo}-eTOKCH)]2-[феніл]-1,7,7-три-[метил]-біцикло[2,2,1]гептан згідно з формулою І, що відповідає за чистотою вимогам Фармакопеї, за такими причинами а) Продукт, одержуваний після перекристалізації з диметилформаміду, усе-таки містить сполуку (1R, 3S, 4R)-3-[(2'-{N,N-flHMe™-iaMiH0}-e™-|)]1,7,7-три-[метил]-біцикло[2,2,1]гептан-2-он згідно з формулою V у КІЛЬКОСТІ, що перевищує гранично припустиму за Фармакопею (приблизно 0,5%), б) Диметилформамід характеризується дуже високою температурою кипіння і не може бути вилучений із продукту в потрібному ступені, тому що при високій температурі має місце руйнування продукту Очищення з одержанням продукту зі ступенем чистоти, що задовольняє вимогам Фармакопеї для лікарських засобів, не могла бути досягнута із застосуванням звичайних способів, таких, як перекристалізація з розчинника або фракційна перегонка З урахуванням твердих вимог Фармакопеї домішки, що присутні в занадто великих кількостях, можуть привести до заборони застосування активного компонента для фармацевтичних цілей Домішка (1R, 3S, 4R)-3-[(2'-{N,N-flHMe™iaMiHo} 49974 етил)]-1,7,7-три-[мегип]-біцикло[2,2,1]гептан-2-ону згідно з формулою V може тому створити проблеми в застосуванні сполуки (1R, 2S, 4R)-(-)-2-[(2'{г\І,г\І-диметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло[2,2,1]гептану згідно з формулою І в якості активного компонента В якості висновку можна припустити, що при очищенні (1R, 2S, 4R)-(-)-2-[(2'-{N,Nдиметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло[2,2,1]гептану згідно з формулою І, одержаного за допомогою відомого способу, диметилформамід, очевидно, є єдино можливим розчинником Однак цей спосіб перекристалізації не підходить для одержання фармацевтичного активного інгредієнта, що задовольняє вимогам Фармакопеї, тому що диметилформамід має таку високу температуру кипіння, що його СЛІДОВІ КІЛЬКОСТІ не можуть у достатньому ступені бути вилучені з продукту При необхідній високій температурі сполуки (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™iaMiHO }-етокси)]-2-[фенил]-1,7,7-три-[метил]біцикло[2,2,1]гептан згідно з формулою І піддається руйнуванню Як було показано раніше, (+)-камфора згідно з формулою II є присутньою у реакції алкілювання З (+)-камфори утворюється інший контамшант (1R, 4R)-2-[(2'-{N,N-flHMe™-iaMiHo}-eTOKCH)]- 1,7,7три-[метил]-біцикло[2,2,1]гептан згідно з формулою IV Якщо гідриди лужних металів або аміди лужних металів використовуються в якості агентів для одержання основних солей, КІЛЬКІСТЬ ДОМІШКИ (1R, 4R)-2-[(2'-{N,N-flHMeTHnaMiHo}-eTOKCH)]-1,7,7-Tpn[метил]-біцикло-[2,2,1]гептану згідно з формулою IV знаходиться в межах від 1 до 10% Речовина (1R, 4R)-2-[(2'-{N,N-flHMe™-iaMiHo}-eTOKCH)]-1,7,7три-[метил]-біцикло[2,2,1]гептан згідно з формулою IV була відома з існуючого рівня техніки [Yakugaku Zasshi, 75 1377, (1955), Chem Abstr 934U (1956)] Сполука (1R, 4R)-2-[(2'-{N,Nдиметиламшо}-етокси)]-1,7,7-три-[метил]біцикло[2,2,1]гептан згідно з формулою IV утворюється за такою схемою гідрид лужного металу або амід лужного металу, викооистовувані для утворення натрієвої солі на стадії етерифікації, відновлюють від 1 до 10% (+)-камфори згідно з формулою II у борнеол, що перетворюється у використовуваних умовах реакції в сіль лужного металу, і ця сіль лужного металу вступає в реакцію алкілювання з (2-{хлоро}-етил)-диметиламшом Однак ефір борнеолу (1R, 4R)-2-[(2'-{N,Nдиметиламшо}-етокси)]-1,7,7-три-[метил]біцикло[2,2,1]гептан згідно з формулою IV може бути відділений від необхідного продукту (1R, 2S, 4R)-(-)-2-[(2'-N,N-flHMeTHnaMiHo}-eTOKCH)]-2-[cpeHin]1,7,7-три-[метил]-біцикло[2,2,1]гептану згідно з формулою І у процесі обробки реакційної суміші Рішенням задачі, поставленої у винаході, повинний бути спосіб одержання (1R, 2S, 4R)-(-)-2[(2'-{г\І,г\І-диметиламіно}-етокси)]-2-[феніл]-1,7,7 8 три-[метил]-біцикло[2,2,1]гептану згідно з формулою І і його фармацевтичне прийнятних адитивних кислотних солей високого ступеня чистоти без необхідності проведення стадії очищення перекристалізацією, що так або інакше не забезпечила б потрібного ступеня чистоти препарату і зменшила б його вихід, більш того, мала б той недолік, що залишкові КІЛЬКОСТІ розчинника не могли б бути вилучені з кінцевого продукту в достатньому ступені навіть за допомогою складних способів очищення Несподівано ця задача була вирішена в даному винаході Даний винахід базується на дивному відкритті, що якщо реакція в реакційній суміші, що містить сполуки (1R, 2S, 4R)-(-)-2-[cpeHin]1,7,7-три-[метил]-біцикло[2,2,1]гептан-2-ол згідно з формулою III і (2-{хлоро}-етил)-диметиламш, здійснюється в присутності гідриду лужного металу або аміду лужного металу у середовищі, що складається з 1 або більше сполуки(ук), що мають 5або 6-членне насичене гетероциклічне кільце з 2 атомами кисню в КІЛЬЦІ, узятоі(их) в якості розчинника(ів), наприклад, діоксану, той напрямок реакції зміщається убік утворення необхідного (1R, 2S, 4R)-(-)-2-[(2'-{M,M-flHMe™-iaMiHo}-eTOKCH)]-2[феніл]-1,7,7-три-[метил]-біцикло-[2,2,1]гептану згідно з формулою І, а побічний продукт (1R, 3S, 4R)-3-[(2'-{N,N-flHMe™-iaMiHo}-e™-|)]-1,7,7-TpH[метил]-біцикло[2,2,1]гептан-2-он згідно з формулою V утворюється в мінімальних кількостях Вищеописане відкриття уможливлює одержання необхідної сполуки (1R, 2S, 4R)-(-)-2-[(2'-{N,Nдиметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло-[2,2,1]гептану згідно з формулою І з більш високим виходом і з більш високим ступенем чистоти, особливо по відношенню до домішки (1R, 3S, 4R)-3-[(2'-[N,N-flHMe™-iaMiH0}-e™-|)]-1,7,7три-[метил]-біцикло[2,2,1]гептан-2-он згідно з формулою V Таким чином, може бути одержана сполука (1R, 2S, 4R)-(-)-2-[(2'-{N,N- д и метилам і но}етокси)]-2-[феніл]-1,7,7-три-[метил]біцикло[2,2,1]гептан згідно з формулою І, що цілком задовольняє вимогам Фармакопеї по відношенню до чистоти і вмісту залишкових кількостей розчинника Скрізь по тексту процентні вираження, що показують вміст сполук за формулами І і V і інших речовин, є результатами газохроматографічного аналізу, причому вони обчислюються як відносини площі піка індивідуальної речовини до загальної площі всіх ПІКІВ Термін "фармацевтичне прийнятні кислотні адитивні солі", застосовуваний в описі даного патенту, означає солі, утворені з неорганічними кислотами, наприклад, соляною кислотою, бромистоводневою кислотою, сірчаною кислотою або фосфорною кислотою, або органічною кислотою, наприклад, оцтовою кислотою, винною кислотою, бурштиновою кислотою, яблучною кислотою, молочною кислотою, лимонною кислотою, малеїновою кислотою або фумаровою кислотою Сіль, утворена з фумаровою кислотою, має особливо корисні властивості (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiH0}етокси)]-2-[феніл]-1,7І7-три-[метил]біцикло[2,2,1]гептан згідно з формулою І має три асиметричних центри, а саме, у позиції 1, 2 і 4 49974 Таким чином, предметом винаходу є спосіб одержання (1R, 2S, 4R)-(-)-2-[(2'-{N,Nдиметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-бщикло-[2,2,1]гептану згідно з формулою І і його фармацевтично прийнятних кислотних адитивних солей шляхом перетворення (+)-1,7,7-три[метил]-біцикло[2,2,1]гептан-2-ону {(+)-камфори} згідно з формулою у (1R, 2S, 4^-(-)-2-[феніл]-1,7,7-7-три-[метил]біцікло[2,2,1]гепган-2-ол згідно з формулою QH за допомогою реакції сполуки згідно з формулою II з металоорганічною сполукою, зі здійсненням, при необхідності, руйнування продукту реакції, як правило, гідролізу, і реакції одержаного в такий спосіб (1R, 2S, 4Р)-(-)-2-[феніл]-1,7,7-три[метил]-біцикло[2,2,1]гептан-2-олу згідно з формулою III з (2-{галогено}-етил)-диметиламшом у присутності агента, що утворює основну сіль, в органічному розчиннику, і, якщо потрібно, перетворення в такий спосіб одержаної основи (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiHo}-eTOKCH)]2-[феніл]-1,7,7-три-[метил]-біцикло [2,2,1]гептану згідно з формулою І у сіль, який відрізняється тим, що реакцію (1R, 2S, 4R)-(-)-2-№eHin]-1,7,7-Tpn[метил]-біцикло[2,2,1]гептан-2-олу згідно з формулою III з (2-{галогено}-етил)-диметиламшом проводять у середовищі, що містить 1 або більше сполуку(и), що має(ють) 5- або 6-членне насичене гетероциклічне кільце з 2 атомами кисню в КІЛЬЦІ, узятого(их) як розчинник(и) Винахід не обмежується використанням 1 або більше сполуки(ук), що має(ють) 5- або 6-членне насичене гетероциклічне кільце з 2 атомами кисню в КІЛЬЦІ, таких, як діоксан, використовуваного(их) в якості розчинника(ів) солей, але також містить у собі використання розчинників, що містять, принаймні, 50% за вагою, переважно, 75% за вагою, однієї або більше сполуки(ук), що має(ють) 5- або б-членне насичене гетероциклічне кільце з 2 атомами кисню в КІЛЬЦІ, таких, як діоксан Істотною ознакою способу за винаходом є те, що алкілювання здійснюється в розчиннику, який не підходить для алкілювання в позиції 3 (+)камфори згідно з формулою II у присутності агента, що утворює основну сіль Було виявлено, що сполуки, які мають 5- або 6-членне насичене гетероциклічне кільце з 2 атомами кисню в КІЛЬЦІ, особливо діоксан, можуть бути переважно використані для цієї мети Як особливо кращий розчинник використову 10 ється діоксан Іншим прикладом є дюксолан Придатною металоорганічною сполукою для реакції Гриньяра є фенілмагній галогенід Іншими прикладами є феніллужні сполуки, такі, як феніл ЛІТІЙ Переважно використовується фенілмагній бромід Фенілмагній хлорид також може бути використаний Переважно, спосіб згідно з винаходом здійснюють у такий спосіб на першій стадії способу згідно з даним винаходом (+)-камфора згідно з формулою II піддається реакції Гриньяра, наприклад, з фенілмагній бромідом Реакція здійснюється способом, відомим per se Як реакційне середовище переважно може бути використаний тетрапдрофуран Фенілмагній бромід може бути використаний у КІЛЬКОСТІ ВІД 1 до Змоль, переважно, близько 1,5моль, по відношенню до 1моля (+)-камфори згідно з формулою II Краще здійснення може відбуватися при одержанні спочатку реактиву Гриньяра з магнію і бромбензолу у використовуваному розчиннику і далі додаванні розчину (+)-камфори згідно з формулою II в органічному розчиннику в реакційну суміш при температурі кипіння Краще використовувати той самий розчинник для одержання реактиву Гриньяра і розчину (+)-камфори згідно з формулою II Як розчинник переважно може бути використаний тетрапдрофуран Краще здійснювати реакцію при температурі кипіння реакційної суміші Реакційна суміш потім охолоджується, і одержаний адукт гідролізується Гідроліз здійснюється відомим способом, бажано, у кислому середовищі Переважно використовувати для цієї мети соляну кислоту (1R, 2S, 4R)-(-)-2-№eHin]-1,7,7-три-[метил]біцикло[2,2,1]гептан-2-ол згідно з формулою III, одержаний після руйнування комплексу Гриньяра, може бути підданий алкілюванню без очищення реакційної суміші Реакція може бути здійснена в присутності (+)-камфори згідно з формулою II, що не прореагувала У результаті утворюється невелика КІЛЬКІСТЬ алкільованих побічних продуктів, тому що згідно із способом за даним винаходом утворення (1R, 3S, 4R)-3-[(2'-{N,N-flHMe™iaMiHo}етил)]-1,7,7-три-[метил]-біцикло[2,2,1]гептан-2-ону згідно з формулою V подавлено Як уже було показано вище, алкілювання здійснюється в розчиннику, який не підходить для алкілювання в позиції 3 (+)-камфори згідно з формулою II, тобто в який (+)-камфора згідно з формулою II алкілюється тільки в дуже невеликій КІЛЬКОСТІ Особливо переважно використовувати діоксан як органічний розчинник, тому що в середовищі, що містить діоксан, алкілювання (+)камфори згідно з формулою II відбувається в невеликому ступені і, отже, вміст небажаної домішки (1R, 3S, 4R)-3-[(2'-{N,N-flHMeTHnaMiH0}-e™-|)]-1,7,7три-[метил]-біцикло[2,2,1]гептан-2-ону згідно з формулою V у кінцевому продукті (1R, 2S, 4R)-(-)-2[(2'-{г\І,І\І-диметиламіно}-етокси)]-2-[феніл]-1,7,7три-[метил]-біцикло- [2,2,1] гептан і згідно з формулою І мало Асиметричні центри (1R, 2S, 4R)-(-)-2-[(2'-{N,Nдиметиламшо}-етокси)]-2-[феніл]-1,7,7-три 12 11 49974 [метил]-біцикло [2,2,1]гептану згідно з формулою І гою неможливо видалити диметилформамід у неу позиції 1 і 4 утворюються з (+)-1,7,7-три-[метил]обхідному ступені через його високу температуру біцикло[2,2,1]гептан-2-ону {(+)-камфори} згідно з кипіння, при якій (1R, 2S, 4R)-(-)-2-[(2'-{N,Nформулою II диметиламшо}-етокси)]-2-[феніл]-1,7,7-три[метил]-біцикло[2,2,1]гептан згідно з формулою і Апелювання виконують у присутності агента, розкладається що утворює основну сіль Термін "агент, що утворює основну сіль" означає сполуки основного хаПеревагою способу даного винаходу є те, що рактеру, що перетворюють гідроксильну групу в він може здійснюватися зі значним виходом, і при сіль Для цієї мети можуть бути використані перецьому утворюється продукт високого ступеня чисважно аміди лужних металів, наприклад, амід натоти Вихід приблизно 46%, показаний у Приклатрію, або гідриди лужних металів, наприклад, гіддах, значно вище, ніж вихід, розкритий у докуменрид натрію Краще використання аміду натрію тах відомого рівня техніки, що не перевищує 25%, навіть якщо (+)-камфора рециркулюється кілька В якості (2-{галогено}-етил)-диметиламшу разів краще використовувати (2-{хлоро}-етил)диметиламш Винахід далі ілюструється Прикладами ТемОптимальним є використання агента, що утвоператури плавлення, представлені в Прикладах, є рює основну с ль, у КІЛЬКОСТІ від 1 до Змоль, перенеточними даними важно від 1,5 до 2моль, по відношенню до 1моля Приклад 1 (1R, 2S, 4R)-(-)-2-№eHin]-1,7,7-три-[метил](1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiH0}біцикло[2,2,1]гептан-2-олу згідно з формулою III етокси)]-2-[феніл]-1,7,7-три-[метил]КІЛЬКІСТЬ алкілюючого агента переважно складає біцикло[2,2,1]гептан фумарат (1 1) [Формула І] від 1,0 до 2,5моль, переважно від 1 до 1,1 моль по Реакція Гриньяра відношенню до агента, що утворює основну сіль До суспензії, що містить 48,6г (1,5г-атом) магПереважно реакцію алкілювання (1R, 2S, 4R)-(-)-2нієвої стружки і 600мл безводного тетрапдрофу[феніл]-1,7,7- три-[метил]-біцикло[2,2,1]гептан-2рану, додається порція 20мл суміші 236г (1,5моль) олу згідно з формулою III з (2-{хлоро}-етил)бромбензолу і 200мл безводного тетрапдрофурадиметиламіном проводять при нагріванні, зокрема, ну при температурі кипіння Після того, як реакція при температурі кипіння реакційної суміші Реакцію Гриньяра пішла, залишкова частина бромбензоварто проводити протягом від 3 до 5 годин, кралової суміші додається до суспензії по краплях щим часом реакції є приблизно 4 години протягом 1 години Реакційна суміш нагрівається до кипіння доти, поки магній цілком не розчинить(1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiH0}ся До реактиву Гриньяра додається розчин 183,2г етокси)]-2-[феніл]-1,7,7-три-[метил](1,0моль) (+)-камфори згідно з формулою II і біцикло[2,2,1]гептан згідно з формулою І може буЗООмл безводного тетрапдрофурану в умовах поти перетворений у фармацевтичне прийнятну сіль, стійного нагрівання до кипіння протягом приблизно переважно фумарат, без його виділення Це крапівгодини, і далі реакційна суміш нагрівається до щим образом можна зробити так з реакційної сукипіння протягом ще 5 годин міші, одержаної після алкілювання, неорганічні солі віддаляються фільтруванням при температурі Гідроліз від 0 до 30°С, переважно при 20°С, після чого відРеакційна суміш охолоджується до 25°С і влиповідна фармацевтичне прийнятна кислота, перевається в суміш 500мл гептану, 400г льоду, 30г важно фумарова кислота, хлориду натрію і 150мл концентрованої соляної кислоти при перемішуванні при температурі 0°С додається до фільтрату в еквімолярному КІЛЬОрганічна фаза відокремлюється і підлуговується КОСТІ (ВІД 1,0 до 1,5моль) Відфільтровується крисдо рНЮ шляхом додавання 25% за вагою/об'ємом талічний продукт, осаджений із середовища, наводного розчину гідроксиду амонію Після повторприклад, з діоксану ного відділення розчин висушується й упарюється Тому що (1R, 2S, 4R-)-2-[(2'-N,N- диметиламіу вакуумі У такий спосіб одержують 220г безбарвно}-етокси)]-2-[феніл]-1,7,7-три-[метил]ного масла біцикло[2,2,1]гептан згідно з формулою І або його фармацевтичне прийнятна кислотна адитивна Аналіз на основі газової хроматографії сіль, особливо (1R, 2S, 4R)-(-)-2-[(2'-{N,NДослідження виконувалося в газовому хромадиметиламшо}-етокси)]-2-[феніл]-1,7,7-тритографії Perkm Elmer Autosystem [метил]-біцикло[2,2,1]гептану фумарат (1 1), одерДовжина 10м (0,25мм) жані за способом згідно з винаходом, містять, гоВикористано капілярний стовпчик (CPSil-19CB, ловним чином, малі КІЛЬКОСТІ (1R,3S,4R)-3-[(2'Chrompack [Handelsprodukt]) з нерухомою фазою {г\І,г\І-диметиламіно}-етил)]-1,7,7-три-[метил]14% ціанопропіл 14% метил полісилокеан біцикло[2,2,1]гептан-2-олу згідно з формулою V Інжекція при 200°С або його фармацевтичне прийнятної кислотної Швидкість нагрівання 10°С/хв адитивної солі, ВІДПОВІДНО, ТО за способом згідно з Газ-носій гелій винаходом можна працювати без перекристалізаДетектор полуменево-юнізаційний, темперації з диметилформаміду, що використовується у тура інжекції 200°С, кінцева відомих способах і що, в будь-якому випадку, притемпература 250°С, тиск газу 40кРа водить до недостатнього очищення без видалення Вміст (1 R,2S,4R-)-2-№eHin]-1,7,7-три-[метил]слідових кількостей диметилформаміду з фармабіцикло [2,2,1]гептан-2-олу 66,5% Вміст (+)цевтичне активного - компонента Також спосіб камфори 25% , згідно з винаходом має значні переваги в порівЕтерифікація нянні з відомими способами, оскільки з їх допомоДо суспензії, що містить 45,5г (1,05моль) аміду 14 13 49974 натрію (вміст 90% вага/вага) і 500мл безводного ЛОЮ III, І діоксану додається суміш 220 г безбарвного мас2,2% інших домішок у менших кількостях ла, одержаного гідролізом і такого, що містить (1R, Етерифікація 2S, 4ї?)-(-)-2-[феніл]-1,7,7-три-[метил]До суспензії, що містить 3,4г (67МІЛІМОЛЬ) гідриду натрію і 50мл безводного толуолу, додавали біцикло[2,2,1]гептан-2-ол, ЮОмл безводного діокрозчин 40г масла, одержаного в реакції Гриньяра, сану при температурі кипіння протягом півгодини що містить (1R, 2S, 4^-(-)-2-[феніл]-1,7,7-триСуміш кип'ятиться протягом 2 годин, після чого [метил]-біцикло[2,2,1]-гептан-2-ол згідно з формудодається 113,0г (1,05моль) (2-{хлоро}-етил)лою III і ЗОмл безводного толуолу Реакційну суміш диметиламшу, і далі реакційна суміш нагрівається нагрівали до кипіння протягом 1 години, після чого до температури кипіння протягом 4 годин додавали розчин 6 85г (67МІЛІМОЛЬ) (2-{хлоро}Утворення фумаратной солі етил)-диметиламшу в Юмл толуолу при темпераСуспензія охолоджується до 20°С, фільтрутурі кипіння Далі реакційна суміш нагрівалася до ється, до чистого фільтрату додається 121,9г кипіння протягом 4 годин (1,05моль) фумарової кислоти при енергійному перемішуванні Реакційна суміш нагрівається до Розділення температури кипіння протягом Юхв, охолоджуєтьРеакційна суміш промивалася водою три рази ся до 15°С, перемішується далі протягом 1 години по 25мл Продукт екстрагували трьома рівними і фільтрується Залишок після фільтрації промивапорціями розчину з 10г (0,12моль) винної кислоти і ється діоксаном, водою і етанолом і висушується 40мл води Фази розділяли, водні шари збирали, при 80°С для видалення розчинника У такий спопідлуговували до рНЮ за допомогою концентросіб виходить 190,5г (0,456моль) білих кристалів, ваного розчину гідроксиду амонію, екстрагували вихід 45,6% (у розрахунку на (+)-камфору) Точка три рази дихлоретаном по 20мл, висушували над плавлення білих кристалів має значення від 214 сульфатом магнію і розчинник видаляли у вакуумі до216°С У такий спосіб одержували 14,5г безбарвного масла, що містило, згідно з газохроматографічним Аналіз для формули C20H31NO C4H4O4 аналізом (417,55) Розраховано С% = 69,03%, Н% = 8,45%, N% 74,2% (1R, 2S, 4R)-(-)-2-[(2'-{N,N=3,35% диметиламшо}-етокси)]-2-{феніл]-1,7,7-три[метил]-біцикло[2,2,1]гептан фумарату згідно з Виявлено С% = 69,06%, Н% = 8,42%, N% = формулою І, 3,39% 16,5% (1R, 4R)-2-[(2'-{N,N-flHMe™-iaMiH0}[а]22о = -92,5° (с = 0,4 диметилсульфоксид, етокси)]-2-{феніл]-1,7,7-три-[метил]435нм) біцикло[2,2,1]гептану згідно з формулою IV, Продукт містить менше, ніж 0,05% домішки 6,5% (1R, 3S, 4R)-3-[(21-{N,N-flHMeTHnaMiH0}(1R, 3S, 4R)-3-[(2'-{N,N-flHMe™-iaMiH0}-e™-|)]етил)]-1,7,7-три-[метил]-біцикло[2,2,1]-гептан-2-ону 1,7,7-три-[метил]-біцикло[2,2,1] гептан-2-ону фузгідно з формулою V, марату (1 1) деяка КІЛЬКІСТЬ інших неідентифікованих доміПриклад 2 (порівняльний приклад) шок, кожна в КІЛЬКОСТІ менше 1% (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiH0}Утворення фумаратної солі етокси)]-2-[феніль-1,7,7-три-[метил]До розчину 14,0г основного (1R, 2S, 4R)-(-)-2біцикло[2 2 1]гептан фумарат(1 1) [Формула І] [(2'-{г\І,г\І-диметиламіно}-етокси)]-2-[феніл]-1,7,7Відтворення способу, розкритого в Угорському три-{метил]-біІ4икло[2,2,1]гептану згідно з формупатенті № 212 574 Реакція Гриньяра лою І, виділеного зтартратної солі, і 150мл етаноДо реактиву Гриньяра, приготовленого з 5,52г лу, додають 9,07г (43,6МІЛІМОЛЬ) фумарової кисло(0,23г-атом) магнієвої стружки і 36,1г (0,23моль) ти при 70°С Продукт відфільтровують при 0°С і бромбензолу в 200 мл у безводному діетиловому перекристалізовують з 50мл диметилформаміду ефірі, додається розчин 30,4г (0,20моль) (+)камфори в 50мл безводного діетилового ефіру У такий спосіб одержують 13,5г необхідного Реакційна суміш нагрівається до кипіння протягом продукту (1R, 2S, 4R)-(-)-2-[(2'-{N,N-flHMe™-iaMiHo}5 годин Комплекс Гриньяра руйнується додаванетокси)]-2-[феніл]-1,7,7-три-[метил]-біцикло[2,2,1]ням охолодженого льодом водного розчину 20г гептану фумарату (1 1) згідно з формулою І у хлориду амонію, суміш промивається 3 рази вовигляді білих кристалів Вихід 16,2% (у розрахунку дою по ЗОмол, розділяється, висушується над безна (+)-камфору) Згідно з газохроматографічним водним сульфатом магнію, і розчинник віддаляаналізом в продукті можна знайти 0,5% (1R, 3S, ється випарюванням Таким чином, виходить 40,5г 4R)-3-[(2'-{N,N-flHMe™-iaMiHo}-e™i)]-1,7,7-TpHбезбарвного масла, що містить, згідно з газохро[метил]-біцикло[2,2,1]гептан-2-ону згідно з формуматографічним аналізом лою V Температура плавлення від 214 до 216°С Аналіз для формули C20H31NO 57,5% (+)- камфори згідно з формулою II, С4Н4О4(417,55) Розраховано С% = 69,03%, Н% = 5,8% 1,7,7-три-[метил]-біцикло[2,2,1]гептан-28,45%, N% = 3,35% Виявлено С% = 69,16%, Н% = олу (борнеолу), 8,52%, N% = 3,32% 34,5% (1R, 2S, 4R)-(-)- 2-[феніл]-1,7,7-три[метил]-біцикло[2,2,1]гептан-2-олу згідно з форму 15 49974 ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71 16
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for preparing (1r, 2s, 4r)-(-)-2-[(2'-(n,n-dimethylamino)-ethoxy)]-2-[phenyl]-1,7,7-tri-[methyl]-bicyclo[2.2.1]heptane and pharmaceutically acceptable acid addition salts thereof
Автори англійськоюLukacs Gyula, Nagy Kalman, Szabo, Tibor, Nemeth Norbert
Назва патенту російськоюСпособ получения (1r, 2s, 4r)-(-)-2-[(2'-{n,n-диметиламино}-этокси)]-2-[фенил]-1, 7, 7-три-[метил]-бицикло[2.2.1]гептана и его фaрмацевтически приемлемых кислотных адитивных солей
Автори російськоюЛукач Дьюла, Надь Калман, Немет Норберт
МПК / Мітки
МПК: C07B 53/00, A61K 31/135, C07C 217/02, A61P 25/22, C07C 213/00, C07C 217/12
Мітки: одержання, кислотних, прийнятних, спосіб, 4r)-(-)-2-[(2'-{n,n-диметиламіно}-етокси)]-2-[феніл]-1, адитивних, солей, фармацевтично, 7-три-[метил]-біцикло[2.2.1]гептану
Код посилання
<a href="https://ua.patents.su/8-49974-sposib-oderzhannya-1r-2s-4r-2-2-nn-dimetilamino-etoksi-2-fenil-1-7-7-tri-metil-biciklo221geptanu-i-jjogo-farmacevtichno-prijjnyatnikh-kislotnikh-aditivnikh-solejj.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання (1r, 2s, 4r)-(-)-2-[(2′-{n,n-диметиламіно}-етокси)]-2-[феніл]-1, 7, 7-три-[метил]-біцикло[2.2.1]гептану і його фармацевтично прийнятних кислотних адитивних солей</a>
Попередній патент: Датчик для вимірювання вологості газового середовища
Наступний патент: Вита дротова структура
Випадковий патент: Спосіб та пристрій для очищення продуктів нітрування












