(s)-(-)-амлодипіну камзилат або його гідрат і фармацевтична композиція, яка їх містить
Номер патенту: 93724
Опубліковано: 10.03.2011
Автори: Кім Хан Кіонг, Йоо Дзаєхо, Лі Моон Суб, Лі Гвансун, Лі Дзаєхеон, Чанг Янг-Кіл, Чоі Чанг-Дзу, Янг Веон Кі, Лі Дзає-Чул
Формула / Реферат
1. (S)-(-)-амлодипіну камзилат формули (І):
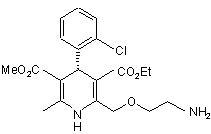
• Камфорсульфонова
кислота,
де камфорсульфонова кислота являє собою (1S)-(+)-10-камфорсульфонову кислоту або (±)-10-камфорсульфонову кислоту.
2. (S)-(-)-амлодипіну камзилат за п. 1, в якому камфорсульфонова кислота являє собою (1S)-(+)-10-камфорсульфонову кислоту, і його порошкова рентгенограма показує головні піки при куті 2![]() : 4,8±0,2, 10,0±0,2, 11,0±0,2, 13,8±0,2, 14,3±0,2, 16,4±0,2, 18,2±0,2, 18,8±0,2, 19,8±0,2, 20,0±0,2, 20,5±0,2 і 23,7±0,2.
: 4,8±0,2, 10,0±0,2, 11,0±0,2, 13,8±0,2, 14,3±0,2, 16,4±0,2, 18,2±0,2, 18,8±0,2, 19,8±0,2, 20,0±0,2, 20,5±0,2 і 23,7±0,2.
3. (S)-(-)-амлодипіну камзилат за п. 1, який являє собою аморфну форму.
4. (S)-(-)-амлодипіну камзилату гідрат формули (II):

• nH2O
Камфорсульфонова
кислота,
де камфорсульфонова кислота являє собою (1S)-(+)-10-камфорсульфонову кислоту або (±)-10-камфорсульфонову кислоту; і n дорівнює 1-2.
5. (S)-(-)-амлодипіну камзилату гідрат за п. 4, в якому камфорсульфонова кислота являє собою (1S)-(+)-10-камфорсульфонову кислоту, і його порошкова рентгенограма показує головні піки при куті 2![]() : 4,2±0,2, 7,8±0,2, 8,3±0,2, 11,3±0,2, 11,9±0,2, 12,5±0,2, 12,9±0,2, 16,7±0,2, 17,3±0,2, 17,6±0,2, 19,5±0,2, 20,2±0,2, 20,4±0,2, 20,7±0,2, 21,3±0,2, 24,4±0,2, 25,6±0,2 і 26,2±0,2.
: 4,2±0,2, 7,8±0,2, 8,3±0,2, 11,3±0,2, 11,9±0,2, 12,5±0,2, 12,9±0,2, 16,7±0,2, 17,3±0,2, 17,6±0,2, 19,5±0,2, 20,2±0,2, 20,4±0,2, 20,7±0,2, 21,3±0,2, 24,4±0,2, 25,6±0,2 і 26,2±0,2.
6. (S)-(-)-амлодипіну камзилату гідрат за п. 4, в якому камфорсульфонова кислота являє собою (±)-10-камфорсульфонову кислоту, і його порошкова рентгенограма показує головні піки при куті 2![]() : 3,1±0,2, 4,7±0,2, 5,5±0,2, 9,3±0,2, 11,4±0,2, 12,9±0,2, 13,0±0,2, 15,2±0,2, 15,7±0,2, 16,3±0,2, 17,4±0,2, 19,0±0,2, 20,0±0,2, 20,2±0,2, 21,0±0,2 і 25,8±0,2.
: 3,1±0,2, 4,7±0,2, 5,5±0,2, 9,3±0,2, 11,4±0,2, 12,9±0,2, 13,0±0,2, 15,2±0,2, 15,7±0,2, 16,3±0,2, 17,4±0,2, 19,0±0,2, 20,0±0,2, 20,2±0,2, 21,0±0,2 і 25,8±0,2.
7. Фармацевтична композиція для лікування серцево-судинних захворювань, яка містить (S)-(-)-амлодипіну камзилат за п. 1 або (S)-(-)-амлодипіну камзилату гідрат за п. 4 як активний інгредієнт.
8. Фармацевтична композиція за п. 7, де серцево-судинне захворювання являє собою стенокардію, гіпертензію або застійну кардіоплегію.
Текст
1. (S)-(-)-амлодипіну камзилат формули (І): 3 Даний винахід стосується (S)-(-)-амлодипіну камзилату або його гідрату, який має хорошу фотостабільність і високу розчинність, і фармацевтичної композиції, яка їх включає. Амлодипін, непатентована назва для 3-етил-5метил-2-(2-аміноетоксиметил)-4-(2-хлорфеніл)-6метил-1,4-дигідро-3,5-піридиндикарбоксилату, являє собою тривалодіючий блокатор кальцієвих каналів, застосовний для лікування серцевосудинних захворювань, таких як стенокардія, гіпертензія і застійна кардіоплегія. Як показано нижче, амлодипін існує у формі двох енантіомерів, що мають хіральний вуглець в 4-положенні. 93724 4 Публікація корейської патентної заявки №2005-61317 розкриває (S)-(-)-амлодипіну гентизат, який має більш високу фотостабільність, ніж (S)-(-)-амлодипіну безилат. Однак дана сіль має слабу розчинність у воді (її розчинність в дистильованій воді дорівнює приблизно 1мг/мл), яка не придатна для фармацевтичного застосування. Таким чином, існує потреба у створенні нової солі (S)-(-)-амлодипіну, яка має поліпшену фотостабільність і розчинність. Головна мета даного винаходу полягає в тому, щоб представити нову кислотно-адитивну сіль (S)(-)-амлодипіну, яка має підвищену стабільність і розчинність. Відповідно до одного аспекту даного винаходу представлений (S)-(-)-амлодипіну камзилат формули (І): де камфорсульфонова кислота являє собою (1S)-(+)-10-камфорсульфонову кислоту або ()-10камфорсульфонову кислоту. У даному винаході також пропонується (S)-(-)амлодипіну камзилату гідрат формули (II): (R)-(+)-амлодипш і (S)-(-)-амлодипін мають відмінні фармакологічні функції. Наприклад, (R)-(+)амлодипін, всупереч його недостатній активності по блокуванню кальцієвих каналів, є потужним інгібітором міграції гладком'язових клітин, який застосовується для попередження атеросклерозу і рестенозу. (S)-(-)-амлодипін має більш високу активність по зниженню кров'яного тиску в порівнянні з (R)-(+)-амлодипіном [див. РСТ публікацію WO 1995/05822]: його активність в 2 рази вище, ніж активність (R/S)-амлодипіну [див. J. Med. Chem. 1986, 29, 1696-1702]. Амлодипін у вигляді вільної основи показує низьку стійкість. Тому він переважно вводиться у формі фармацевтично прийнятної кислотноадитивної солі. Відносно цього були розроблені різні кислотно-адитивні солі (S)-(-)-амлодипіну. У РСТ публікації WO 2006/043148 описаний (S)-(-)-амлодипіну безилату геміпентагідрат і (S)-()-амлодипіну безилату дигідрат, але без зазначення їх специфічних фармакологічних, фізичних або хімічних властивостей. У публікації корейської патентної заявки №2005-37498 описано, що (S)-(-)-амлодипіну безилату дигідрат має підвищену розчинність у воді і високу біоактивність. Однак дана сіль має слабу фотостабільність при впливі сонячного світла. Корейський патент №515294 розкриває (S)-(-)амлодипіну нікотинату дигідрат, який має хорошу дію на зниження кров'яного тиску. Однак дана сіль також має слабу фотостабільність при впливі сонячного світла. де камфорсульфонова кислота являє собою (1S)-(+)-10-камфорсульфонову кислоту або ()-10камфорсульфонову кислоту; і n дорівнює 1-2. У даному винаході також пропонується фармацевтична композиція для лікування серцевосудинних захворювань, яка містить (S)-(-)амлодипіну камзилат або його гідрат як активний інгредієнт. Наведені вище і інші цілі і ознаки даного винаходу стануть очевидними з подальшого опису винаходу, представленого в поєднанні з наступними супроводжуючими кресленнями, які відповідно показують: Фіг.1 - рентгенограма (S)-(-)-амлодипіну (1S)(+)-10-камзилату гідрату; Фіг.2 - рентгенограма (S)-(-)-амлодипіну (1S)(+)-10-камзилату ангідриду; Фіг.3 - рентгенограма (S)-(-)-амлодипіну ()-10камзилату гідрату; і Фіг.4 - графік, що показує залежне від часу розкладання солей (S)-амлодипіну при впливі сонячного світла. (S)-(-)-амлодипіну камзилат може бути приготовлений: (а) перетворенням рацемату амлодипіну на вільну основу (S)-(-)-амлодипіну і (b) взаємодією вільної основи (S)-(-)-амлодипіну з 5 93724 6 камфорсульфоновою кислотою в розчиннику, як показано на схемі реакції 1. в якій камфорсульфонова кислота являє собою (1S)-(+)-10-камфорсульфонову кислоту або ()-10-камфорсульфонову кислоту; і n дорівнює 12. У схемі реакцій 1 стадію (а) можна проводити способом, описаним в РТС публікації WO 95/25722, для одержання вільної основи (S)-(-)амлодипіну, який має оптичну чистоту, що дорівнює 99% (ее) або вище. Стадію (b) можна проводити в суміші органічного розчинника і води або в суміші полярного розчинника і неполярного розчинника для одержання (S)-(-)-амлодипіну камзилату в гідратній або ангідридній формі залежно від використаного розчинника. Наприклад, коли розчинник для реакції являє собою суміш води і органічного розчинника, що змішується з водою, наприклад, метанол, етанол, ізопропанол, ацетонітрил або ацетон, переважно ізопропанол, (S)-(-)-амлодипіну камзилат одержується в гідратній формі, в якій одна молекула (S)-()-амлодипіну камзилату оточена однією-двома молекулами Н2О. Зокрема, (S)-(-)-амлодипіну (1S)(+)-10-камзилату гідрат має вміст вологи від 4 до 6%, і (S)-(-)-амлодипіну ()-10-камзилату гідрат має вміст вологи від 5 до 6%. Суміш органічного розчинника і води може мати сумішеве співвідношення від 1:1 до 1:30 (об./об.), переважно від 1:5 до 1:15 (об./об.). Коли розчинник для реакції являє собою суміш полярного розчинника (наприклад, метанол, етанол, ізопропанол, ацетонітрил, ацетон, діетиловий ефір, метил-трет-бутиловий ефір і їх суміш) і неполярного розчинника (наприклад, гексан, гептан і їх суміш), одержується (S)-(-)-амлодипіну (1S)-(+)10-камзилату ангідрид. Така ангідридна форма перетворюється на гідратну форму, коли вона абсорбує вологу з атмосфери. У даному винаході реакційний розчинник може застосовуватися в кількості від 5 до 50мл, переважно від 10 до 30мл, з розрахунку на 1,0г вільної основи (S)-(-)-амлодипіну. Крім того, стадію (b) можна виконувати при температурі від 0 до 50С, переважно від 10 до 30С, протягом 2-24 годин. (S)-(-)-амлодипіну камзилат або його гідрат, одержаний таким чином, має визначену рентгено граму, яка відрізняється від рентгенограм відомих солей (S)-(-)-амлодипіну, як показано на Фіг.1-3. (S8)-(-)-амлодипіну камзилат може бути перетворений на аморфну форму звичайним способом, таким як осадження розчинником, сушіння виморожуванням і розпилювальне сушіння. Крім того, з (S)-(-)-амлодипіну камзилату або його гідрату може бути виготовлена препаративна форма разом з традиційним антигіпертензивним засобом (наприклад, діуретиком, АСЕ інгібітором, блокатором кальцієвих каналів і блокатором рецептора ангіотензину), а також із звичайним антигіперліпідемічним засобом (наприклад, ловастатином, симвастатином, аторвастатином, росурвастатином і флувастатином). Відповідно до цього, в даному винаході пропонується фармацевтична композиція для лікування серцево-судинних захворювань, яка містить заявлений (S)-(-)-амлодипіну камзилат або його гідрат як активний інгредієнт. Фармацевтичну композицію можна вводити різними шляхами, які включають пероральне і парентеральне введення, і виготовляти препаративну форму з використанням звичайних фармацевтично прийнятних розріджувачів або наповнювачів, таких як наповнювач, сухий наповнювач, зв'язуюча речовина, змочувальні засоби, дезінтегруючі засоби і поверхнево-активні речовини. Тверді препаративні форми для перорального введення можуть бути у формі таблетки, пілюлі, порошку, гранули або капсули, які можуть містити щонайменше один наповнювач, такий як крохмаль, сахароза, лактоза або желатин, і мастильну речовину, таку як стеарат магнію і тальк. Рідка препаративна форма для перорального введення може бути у формі суспензії, розчину, емульсії або сиропу, що може містити розріджувач, такий як вода або парафінове масло, і щонайменше один наповнювач, такий як змочувальний засіб, підсолоджувач, смакова добавка і консерванти. Препаративна форма для парентерального введення може бути у формі стерильного водного розчину, неводного розчину, суспензії, емульсії, ліофілізованого продукту або супозиторія. Неводні розчини або суспензії можуть містити пропіленгліколь, поліетиленгліколь, рослинну олію, таку як 7 93724 8 оливкова олія, і ін'єктовний складний ефір, такий гексану для одержання осаду. До білої суспензії, як етилолеат. Супозиторій можна приготувати з що осіла, повільно додавали 9л гексану, і одержавикористанням основи, такої як вітепсол, макрону суміш потім перемішували при кімнатній темпегол, твін 61, масло какао, лауринове масло і гліцературі протягом 4 годин, фільтрували, промивали риновий желатин. гексаном, і сушили в теплому повітряному потоці Звичайна добова доза (S)-(-)-амлодипіну кампри 40С, одержуючи 525,8г (вихід: 93,9%) вказазилату або його гідрату може знаходитися в інтерної в заголовку сполуки у вигляді білої твердої валі від приблизно 1,0 до 5,0мг/кг маси тіла, переречовини. важно від 2,5 до 4,0мг/кг маси тіла, і може бути Оптична чистота: 99,9% ее. введена в разовій дозі або розділеними дозами. Приклад 1: Приготування (S)-(-)-амлодипіну Даний винахід буде описаний більш детально (1S)-(+)-10-камзилату гідрату з посиланням на приклади. Однак потрібно розумі300г вільної основи (S)-(-)-амлодипіну, одерти, що представлений опис не обмежується вижаної в приготуванні 2, додавали до суміші 900мл значеними прикладами. ізопропанолу і 900мл дистильованої води, і до Приклад даного вмісту додавали 170,4г (1S)-(+)-10Приготування 1: Приготування (S)-(-)камфорсульфонової кислоти, і одержану суміш амлодипін-гемі-D-тартратнагрівали для одержання гомогенного розчину. До монодиметилсульфоксиду сольвату даного розчину додавали 30,0г активованого ву1,5кг (R/S)-амлодипіну розчиняли в 7,5л димегілля і перемішували при кімнатній температурі тилсульфоксиду, до якого повільно по краплях протягом 1 години. Потім суміш фільтрували через додавали розчин 275,3г D-(-)винної кислоти в 7,5л целіт і промивали 300мл ізопропанолу і 300мл диметилсульфоксиду з перемішуванням при кімдистильованої води. До фільтрату повільно доданатній температурі. Одержану суспензію потім вали 6,3л дистильованої води, перемішували при перемішували при кімнатній температурі протягом 20С протягом 3 годин, і тверду речовину, що осі12 годин, і осаджену тверду речовину фільтрувала, фільтрували. Тверду речовину промивали ли, промивали 6,0л диметилсульфоксиду і 6,0л 600мл суміші ізопропанол-вода (1:5, об./об.), суацетону, і сушили в теплому повітряному потоці шили в теплому повітряному потоці при 40С, одепри 40С ніч, одержуючи 771г (вихід: 37,4%) вкаржуючи 414г (вихід: 88,0%) вказаної в заголовку заної в заголовку сполуки у вигляді білої твердої сполуки у вигляді білої твердої речовини. речовини. Оптична чистота: >99,9% ее, Оптична чистота: 98,2% ее (збагаченого енанвміст вологи: 4,4~4,6%, тіомера). т. пл.: 146,3~150,5С, 1 Приготування 2: Приготування вільної основи Н-ЯМР (300МГц, CDCl3) (м.ч.): 7,75 (с, 4Н), (S)-(-)-амлодипіну 7,45(6,09 (м, 4Н, АrН), 5,39 (с, 1H), 4,77 (кв, 2Н), 770г (S)-(-)-амлодипін-гемі-D-тартрат4,03 (м, 2Н), 3,85 (м, 2Н), 3,58 (с, 3Н), 3,35 (м, 2Н), монодиметилсульфоксиду сольвату, одержаного в 3,05 (кв, 2Н), 2,50~2,20 (м, 2Н), 2,38 (с, 3Н), приготуванні 1, додавали до 7,7л дихлорметану, 2,10~1,80 (м, 3Н), 1,75 (м, 1H), 1,38 (м, 1H), 1,15 (т, до цієї суміші повільно по краплях додавали 8,6л 2 3Н), 1,00 (с, 3Н), 0,80 (с, 3Н). Н розчину гідроксиду натрію, і одержану суміш Кристалічний стан одержаного (S)-(-)перемішували при кімнатній температурі протягом амлодипіну (1S)-(+)-10-камзилату гідрату аналізу40 хвилин. Органічний шар відділяли, промивали вали рентгенівською спектроскопією (Фіг.1). Спо7,7л води, сушили над безводним сульфатом настережувані основні піки при характеристичних трію і фільтрували. Дихлорметан видаляли при кутах дифракції перераховані в таблиці 1. зниженому тиску, і до маслянистого залишку додавали 1,5л гексану з подальшим випарюванням Таблиця 1 2 4,2 7,8 8,3 11,3 11,9 12,5 12,9 16,7 17,3 d 21,2 11,4 10,7 7,8 7,4 7,1 6,9 5,7 5,1 2: кут дифракції; d: міжплощинна відстань; І/І0 (%): відносна інтенсивність піка. І/І0 100 45,9 66,3 53,3 80,3 36,3 46,7 54,6 51,9 2 17,6 19,5 20,2 20,4 20,7 21,3 24,4 25,6 26,2 d 5,0 4,6 4,4 4,3 4,3 4,2 3,7 3,5 3,4 І/І0 31,4 87,1 62,7 55,2 57,2 44,9 48,0 53,5 46,9 9 93724 Приклад 2: Приготування (S)-(-)-амлодипіну (1S)-(+)-10-камзилату ангідриду 5г вільної основи (S)-амлодипіну, одержаної в приготуванні 2, додавали до 25мл ізопропанолу, в якому були розчинені 2,85г (1S)-(+)-10камфорсульфонової кислоти. До одержаного розчину додавали 99мл метил-трет-бутилового ефіру (МТВЕ) і 2мл гексану і суміші перемішували при кімнатній температурі протягом 2 годин. Тверду речовину, що утворилася, фільтрували в атмосфері азоту і сушили у вакуумі, одержуючи 6,4г (ви 10 хід: 81,5%) вказаної в заголовку сполуки у вигляді білої твердої речовини. Оптична чистота: >99,9% ее, вміст вологи: 0,3%, т. пл.: 145,5~149,4С, 1 H-ЯМР дані були однаковими з 1Н-ЯМР даними в прикладі 1. Кристалічний стан одержаного (S)-(-)амлодипіну (1S)-(+)-10-камзилату ангідриду аналізували рентгенівською спектроскопією (Фіг.2). Спостережувані основні піки при характеристичних кутах дифракції перераховані в таблиці 2. Таблиця 2 2 4,8 10,0 11,0 13,8 14,3 16,4 d 18,6 8,9 8,0 6,4 6,2 5,4 І/І0 28,0 35,5 27,3 30,0 25,8 26,9 2 18,2 18,8 19,8 20,0 20,5 23,7 d 4,9 4,7 4,5 4,5 4,3 3,8 І/І0 30,9 39,2 100 67,2 27,6 36,1 2: кут дифракції; d: міжплощинна відстань; І/І0 (%): відносна інтенсивність піка. Приклад 3: Приготування (S)-(-)-амлодипіну ()-10-камзилату гідрату 10г вільної основи (S)-амлодипіну, одержаної в приготуванні 2, додавали до 20мл ізопропанолу, в якому були повністю розчинені 5,68г ()камфорсульфонової кислоти. У цю суміш повільно по краплях додавали 200мл дистильованої води. Одержаний розчин перемішували при кімнатній температурі протягом 3 годин і потім при 15С протягом 2 годин і тверду речовину, що осіла, фільтрували. Тверду речовину промивали 25мл суміші ізопропанол-вода (1:10, об./об.), сушили в теплому повітряному потоці при 40С, одержуючи 13,7г (вихід: 87,4%) вказаної в заголовку сполуки у вигляді білої твердої речовини. Оптична чистота: >99,9% ее, вміст вологи: 5,4%, т. пл.: 140,2~142,6С, 1 Н-ЯМР дані були однаковими з 1Н-ЯМР даними в прикладі 1. Кристалічний стан одержаного гідрату (S)-(-)амлодипіну ()-10-камзилату аналізували рентгенівською спектроскопією (Фіг.3). Спостережувані основні піки при характеристичних кутах дифракції перераховані в таблиці 3. Таблиця 3 2 3,1 4,7 5,5 9,3 11,4 12,9 13,0 15,2 d 28,6 19,0 16,2 9,6 7,8 6,9 6,8 5,8 І/І0 100 32,5 76,6 79,7 61,0 68,1 46,1 44,6 2 15,7 16,3 17,4 19,0 20,0 20,2 21,0 25,8 d 5,6 5,5 5,1 4,7 4,4 4,4 4,2 3,5 І/І0 48,2 50,8 43,3 69,4 63,9 47,3 41,1 68,9 2: кут дифракції; d: міжплощинна відстань; І/І0 (%): відносна інтенсивність піка. Посилальний приклад 1: Приготування (S)-(-)амлодипіну (R)-камзилату 10г вільної основи (S)-амлодипіну, одержаної в приготуванні 2, і 5,68г (R)-камфорсульфонової кислоти розчиняли в 20мл ізопропанолу, до якого повільно додавали по краплях 200мл дистильованої води. Одержаний розчин перемішували при кімнатній температурі протягом ночі, охолоджували до 15С, і ще перемішували протягом 1 години. Тверду речовину, що осіла, фільтрували, промивали 25мл суміші ізопропанол-вода (1:10, об./об.), сушили в теплому повітряному потоці при 40С, одержуючи 9,77г (вихід: 62,3%) вказаної в заголовку сполуки у вигляді білої твердої речовини. 11 93724 12 Оптична чистота: >99,9% ее, )-амлодипіну нікотинату дигідрату [корейський павміст вологи: 3,2%. тент №515294]. Експериментальний приклад 1: Оцінка фотос100мг кожної з вищенаведених 6 солей помітабільності щали відповідно в 6 тест-пробірок для приготуванФармацевтична композиція, яка містить активня 36 зразків (6 зразків на сіль), і їх піддавали ний інгредієнт, повинна задовольняти необхідну впливу сонячного світла протягом 36 годин. Потім стабільність проти вологості, температури і світла. зразки кожної солі забирали з 6-годинними інтерУ випадку лікарського засобу для лікування серцевалами і зберігали в холодному і темному місці. во-судинних захворювань, таких як гіпертензія, Через 36 годин, кожний зразок розбавляли сумішзокрема, його фотостабільність є важливою, оскішю 20мМ буферний розчин ацетату амонію льки його звичайно призначають разом з іншими (рН=5,0) - ацетонітрил (1:1, об./об.) і аналізували лікарськими засобами для тривалого лікування в за допомогою ВЕРХ при наступних умовах: запечатаному в папері вигляді, що звичайно під- колонка: симетрія С8 (4,6мм 100мм, 3,5мкм, дається впливу світла протягом довгого періоду вода, US); часу. Відповідно, фотостабільність солей (S)-(-)- елюент: 1л розчину 7г моногідрату перхлорамлодипіну дуже важлива. ної кислоти і 1,74г моногідрофосфату калію в очиУ зв'язку з цим були визначені фотостабільнощеній воді, який встановлювали до рН 2,8 додасті солей (S)-(-)-амлодипіну, одержаних в приклаванням фосфорної кислоти. дах 1-3 і посилальному прикладі 1, і порівняні з Результати показані на Фіг.4 і в таблиці 4. фотостабільностями відомого (S)-(-)-амлодипіну безилату [РСТ публікація WO 2006/043148] і (S)-(Таблиця 4 Чистота (площа, %) Сіль (S)-(-)-амлодипіну Безилат Нікотинату дигідрат (R)-камзилат з посил. пр. 1 ()-10-Камзилату гідрат з пр. 3 (1S)-(+)-10-камзилату ангідрид з пр.2 (1S)-(+)-10-камзилату гідрат з пр. 1 Початкова 99,8 99,8 99,8 99,8 6 годин 12 годин 18годин 24 години 30 годин 36 годин 99,9 99,6 99,9 99,9 99,4 99,0 99,7 99,8 98,5 98,3 99,0 99,7 96,4 98,3 98,1 99,6 94,4 98,2 96,2 99,4 93,4 97,9 94,8 99,3 99,9 99,9 99,9 99,9 99,8 99,7 99,7 99,9 99,9 99,9 99,8 99,8 99,7 99,7 Як показано на Фіг.4 і в таблиці 4, (S)-(-)амлодипіну ()-10-камзилату гідрат, а також (S)-(-)амлодипіну (1S)-(+)-10-камзилату гідрат або ангідрид даного винаходу є високостійкими, навіть коли схильні до впливу сонячного світла протягом 36 годин. Зокрема, (1S)-(+)-10-камзилатна сіль виявляє більш високу фотостабільність в порівнянні з ()-10-камзилатною сіллю. Однак (S)-(-)амлодипіну (R)-камзилат зазнавав приблизно 5% розкладання, і відомий (S)-(-)-амлодипіну безилат і (S)-(-)-амлодипіну нікотинату дигідрат - приблизно 7% і 2% розкладання, відповідно, через 36 годин. Крім того, (S)-(-)-амлодипіну безилат і (S)-(-)амлодипіну (R)-камзилат зазнавали зміни в кольорі на їх поверхні від не зовсім білого до коричневого, і вони ставали частково розплавленими. Вищенаведені результати означають, що (S)(-)-амлодипіну камзилат або його гідрат має підвищену фотостабільність в порівнянні з відомими (S)-(-)-амлодипіну безилатом і (S)-(-)-амлодипіну нікотинату дигідратом. Експериментальний приклад 2: Оцінка розчинності Фармацевтично прийнятний активний інгредієнт має розчинність у воді не менше ніж 1мг/мл при рН 1 до 7,5, особливо при значенні рН крові, яке дорівнює приблизно 7,4. Відповідно до цього були виміряні розчинності і рН величина в точках насичення амлодипінкамзилатних солей, одержаних в прикладах 1 і 3 і посилальному прикладі 1, і порівняні з тими ж величинами амлодипіну безилату [Korean Patent Publication №1995-7228], амлодипіну гентизату [Korean Patent Publication №2005-61317] і кристалічного амлодипіну камзилату [WO 2002/079158 А1]. Вимірювання виконували згідно з процедурою, описаною в корейській фармакопеї, яка включає стадії розчинення кожної сполуки в дистильованій воді до насичення, аналіз насиченого розчину рідинною хроматографією і вимірювання розчиненої кількості кожної сполуки з розрахунку на кількість вільної основи амлодипіну. Результати показані в таблиці 5. 13 93724 14 Таблиця 5 Сіль (S)-(-)-амлодипіну Безилат Гентизат (1S)-(+)-10-камзилату гідрат з пр. 1 (R)-камзилат з посил. пр. 1 ()-10-Камзилату гідрат з пр. 3 Кристалічний (R/S)-амлодипіну (S)камзилат 12,5 мг/мл 2,63 1,03 2,72 3,93 3,42 25,0 мг/мл 2,63 1,03 2,73 3,93 3,51 50,0 мг/мл 2,61 1,02 2,73 3,94 3,67 Середнє 2,62 1,03 2,72 3,93 3,54 1,02 1,04 1,02 1,03 Як показано в таблиці 5, розчинність (S)-(-)амлодипіну камзилату вище, ніж розчинність амлодипіну безилату, і, зокрема, вона в 2,6 рази вище, ніж відомої гентизатної солі або кристалічного амлодипіну камзилату. Незважаючи на те, що даний винахід описаний відносно певних варіантів здійснення, потрібно визнати, що фахівцями в даній галузі можуть бути виконати різні модифікації і зміни у винаході, які також входять в об'єм винаходу, так само визначеного як прикладена формула винаходу. 15 Комп’ютерна верстка А. Крижанівський 93724 Підписне 16 Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською(s)-(-)-amlodipine camsylate or hydrate thereof and pharmaceutical composition comprising same
Автори англійськоюLee Jaeheon, Lee Moon Sub, Yang Weon Ki, Yoo Jaeho, Lee Jae-Chul, Choi Chang-Ju, Kim Han Kyong, Chang Young-Kil, Lee Gwansun
Назва патенту російською(s)-(-)-амлодипина камзилат или его гидрат и фармацевтическая композиция, которая их содержит
Автори російськоюЛи Дзаехеон, Ли Моон Суб, Янг Веон Ки, Йоо Дзаехо, Ли Дзае-Чул, Чои Чанг-Дзу, Ким Хан Кионг, Чанг Янг-Кил, Ли Гвансун
МПК / Мітки
МПК: C07D 211/90
Мітки: містить, камзилат, s)-(-)-амлодипіну, гідрат, фармацевтична, яка, композиція
Код посилання
<a href="https://ua.patents.su/8-93724-s-amlodipinu-kamzilat-abo-jjogo-gidrat-i-farmacevtichna-kompoziciya-yaka-kh-mistit.html" target="_blank" rel="follow" title="База патентів України">(s)-(-)-амлодипіну камзилат або його гідрат і фармацевтична композиція, яка їх містить</a>
Попередній патент: Спосіб лиття металу за одноразовими моделями в піщану форму під дією перепаду тиску
Наступний патент: Спосіб одержання композиційного матеріалу на основі заліза об’ємним боруванням
Випадковий патент: Спосіб здійснення реакції кляйзена-шмідта на гідрофобних субстратах












