Електроферментативний спосіб одержання 2,3-дигідроксифенільних похідних та спосіб електрохімічної регенерації nad(p)h з nad(p)+
Номер патенту: 75074
Опубліковано: 15.03.2006
Автори: Штекхан Еберхард (помер), Холльманн Франк, Хауер Бернхард, Целінскі Томас, Шмід Андреас
Формула / Реферат
1. Електроферментативний спосіб одержання 2,3-дигідроксифенільних похідних загальної формули І
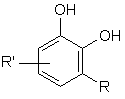 (І),
(І),
де
R означає незаміщену або від одного до декількох разів заміщену фенільну групу, алкільну групу з числом атомів вуглецю від одного до шести, атом галогену або нітрильну групу, а
R' означає атом водню або гідроксильну групу,
який відрізняється тим, що
моногідроксифенільну сполуку загальної формули II
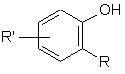 (ІІ),
(ІІ),
де
R та R' мають приведені вище значення,
піддають перетворенню під впливом 2-гідроксибіфеніл-3-монооксигенази (НbрА) (Е.С. 1.14.13.44) у присутності NADH та кисню і
NAD+, що утворився, електрохімічно відновлюють в присутності окисно-відновного гідридно-родієвого каталізатора до NADH.
2. Спосіб за п. 1, який відрізняється тим, що електрохімічне відновлення NAD+ проводять в присутності окисно-відновного гідридно-родієвого каталізатора, що утворюється та регенерується на катоді.
3. Спосіб за п. 2, який відрізняється тим, що як окисно-відновний каталізатор застосовують родієвий комплекс, що перетворюється електрохімічним шляхом у гідридно-родієвий комплекс при катодному потенціалі в межах від -650 до -800 мВ, який вимірюється відносно хлоросрібного електрода Аg/АgСl, при насиченні, рН = 6-9, температура 20-30° C.
4. Спосіб за п. 3, який відрізняється тим, що використовують родієвий комплекс загальної формули III
[Ср Rh(III) (bpy)Cl]Cl (III),
де
Ср означає циклопентадієнільний або пентаметилциклопентадієнільний залишок і
bру означає 2,2'-біпіридил, причому кожне з піридильних кілець може бути від одного до декількох разів заміщене донорною групою.
5. Спосіб за п. 4, який відрізняється тим, що родієвий комплекс формули III відновлюють на катоді з утворенням гідридно-родієвого комплексу формули ІІІа
[Ср Rh(І) (bpy)H]Cl (IІІa),
що може відновлювати NAD+.
6. Спосіб за одним з пп. 1-5, який відрізняється тим, що для його проведення використовують наступні умови: концентрація субстрату від 0,1 до 4 ммолей/л, концентрація NAD+ від 0,01 до 0,5 ммоля/л, концентрація родієвого комплексу від 5 мкмолей/л до 0,5 ммоля/л, концентрація НbрА від 10 до 1000 одиниць/л, концентрація FAD від 0 до 200 мкмолей/л, концентрація каталази від 0 до 1х107 одиниць/л, значення рН від 6 до 7,5, температура від 20 до 30° C, катодний потенціал від -650 до -800 мВ, подача кисню від 20 до 120 ![]() .
.
7. Спосіб електрохімічної регенерації NAD(P)H з NAD(P)+, що утворився в результаті ферментативного перетворення, який відрізняється тим, що окисну ферментативну взаємодію окиснюваного субстрату, яка проходить з витратою NAD(P)H, проводять в присутності NAD(P)H, a NAD(P)+, що утворився при окисненні субстрату, електрохімічним шляхом відновлюють до NAD(P)H, при цьому для ферментативного перетворення NАD(Р)Н-залежну монооксигеназу із класу Е.С.1.14.-.- інкубують з субстратом, що вступає в реакцію окиснення, у присутності NAD(P)H та в присутності кисню, a NAD(P)+, що утворився при відновному розщепленні кисню та при окисненні субстрату, електрохімічно відновлюють в присутності окисно-відновного гідридно-родієвого каталізатора до NAD(P)H.
8. Спосіб за п. 7, який відрізняється тим, що електрохімічне відновлення NAD(P)+ проводять в присутності гідридно-родієвого окисно-відновного каталізатора, що утворюється та регенерується на катоді.
9. Спосіб за п. 8, який відрізняється тим, що як окисно-відновний каталізатор застосовують родієвий каталізатор, і цей родієвий каталізатор може бути переведений у гідридно-родієвий комплекс при катодному потенціалі в межах від -650 до -800 мВ, що вимірюється відносно хлоросрібного електрода Аg/АgСl, при насиченні, рН = 6-9, температура від 20 до 35°С.
10. Спосіб за п. 9, який відрізняється тим, що використовують родієвий комплекс загальної формули III
[Ср Rh(ІІІ) (bpy)Cl]Cl (III),
де Ср означає циклопентадієнільний або пентаметилциклопентадієнільний залишок і
bру означає 2,2'-біпіридил, причому кожне з піридильних кілець може бути від одного до декількох разів заміщене донорною групою.
11. Спосіб за п. 10, який відрізняється тим, що родієвий комплекс формули III відновлюють на катоді в гідридно-родієвий комплекс формули ІІІа
[Ср Rh(І) (bpy)H]Cl (IІІa),
який може відновлювати NAD+.
12. Спосіб за одним з пп. 7-11, який відрізняється тим, що для його здійснення використовують наступні умови: концентрація NAD(P)+ від 10 мкмолей/л до 0,5 ммоля/л, концентрація родієвого комплексу від 5 ммолей/л до 0,5 ммоля /л, концентрація монооксигенази від 10 до 1000 одиниць/л, концентрація FAD від 0 до 200 мкмолей/л, концентрація каталази від 0 до 1х107 одиниць/л, значення рН від 5 до 9, температура від 20 до 35° C, катодний потенціал від -650 до -800 мВ, подача кисню від 20 до 120 ![]() .
.
13. Спосіб за одним з пп. 7-12, який відрізняється тим, що окисна ферментативна взаємодія включає одну з наступних реакцій: окиснення насичених або ненасичених аліфатичних або ароматичних атомів вуглецю, зокрема реакції гідроксилювання, епоксидування або окиснення за Байєром-Віллігером; окиснення сірки або селену; окиснення азоту або фосфору; окиснення галогенідів.
Текст
1. Електроферментативний спосіб одержання 2,3-дигідроксифенільних похідних загальної формули І OH 3 75074 4 6. Спосіб за одним з пп. 1-5, який відрізняється при катодному потенціалі в межах від -650 до -800 тим, що для його проведення використовують намВ, що вимірюється відносно хлоросрібного елекступні умови: концентрація субстрату від 0,1 до 4 трода Аg/АgСl, при насиченні, рН = 6-9, темпераммолей/л, концентрація NAD+ від 0,01 до 0,5 тура від 20 до 35°С. 10. Спосіб за п. 9, який відрізняється тим, що ммоля/л, концентрація родієвого комплексу від 5 мкмолей/л до 0,5 ммоля/л, концентрація НbрА від використовують родієвий комплекс загальної фо10 до 1000 одиниць/л, концентрація FAD від 0 до рмули III 200 мкмолей/л, концентрація каталази від 0 до [Ср Rh(ІІІ) (bpy)Cl]Cl (III), 1х107 одиниць/л, значення рН від 6 до 7,5, темпеде Ср означає циклопентадієнільний або пентамература від 20 до 30° C, катодний потенціал від тилциклопентадієнільний залишок і 650 до -800 мВ, подача кисню від 20 до 120 bру означає 2,2'-біпіридил, причому кожне з піри3 дильних кілець може бути від одного до декількох ñì / õâ ë . разів заміщене донорною групою. 7. Спосіб електрохімічної регенерації NAD(P)H з 11. Спосіб за п. 10, який відрізняється тим, що NAD(P)+, що утворився в результаті ферментатиродієвий комплекс формули III відновлюють на вного перетворення, який відрізняється тим, що катоді в гідридно-родієвий комплекс формули ІІІа окисну ферментативну взаємодію окиснюваного [Ср Rh(І) (bpy)H]Cl (IІІa), субстрату, яка проходить з витратою NAD(P)H, який може відновлювати NAD+. проводять в присутності NAD(P)H, a NAD(P)+, що 12. Спосіб за одним з пп. 7-11, який відрізняється утворився при окисненні субстрату, електрохімічтим, що для його здійснення використовують наним шляхом відновлюють до NAD(P)H, при цьому ступні умови: концентрація NAD(P)+ від 10 мкмодля ферментативного перетворення NАD(Р)Нлей/л до 0,5 ммоля/л, концентрація родієвого комзалежну монооксигеназу із класу Е.С.1.14.-.- інкуплексу від 5 ммолей/л до 0,5 ммоля /л, бують з субстратом, що вступає в реакцію окисконцентрація монооксигенази від 10 до 1000 одинення, у присутності NAD(P)H та в присутності ниць/л, концентрація FAD від 0 до 200 мкмолей/л, + кисню, a NAD(P) , що утворився при відновному концентрація каталази від 0 до 1х107 одиниць/л, розщепленні кисню та при окисненні субстрату, значення рН від 5 до 9, температура від 20 до 35° електрохімічно відновлюють в присутності окисноC, катодний потенціал від -650 до -800 мВ, подача відновного гідридно-родієвого каталізатора до кисню від 20 до 120 ñì 3 / õâ ë . NAD(P)H. 8. Спосіб за п. 7, який відрізняється тим, що еле13. Спосіб за одним з пп. 7-12, який відрізняється ктрохімічне відновлення NAD(P)+ проводять в притим, що окисна ферментативна взаємодія включає сутності гідридно-родієвого окисно-відновного каодну з наступних реакцій: окиснення насичених талізатора, що утворюється та регенерується на або ненасичених аліфатичних або ароматичних катоді. атомів вуглецю, зокрема реакції гідроксилювання, 9. Спосіб за п. 8, який відрізняється тим, що як епоксидування або окиснення за Байєромокисно-відновний каталізатор застосовують родієВіллігером; окиснення сірки або селену; окисненвий каталізатор, і цей родієвий каталізатор може ня азоту або фосфору; окиснення галогенідів. бути переведений у гідридно-родієвий комплекс Даний винахід відноситься до способу, що включає опосередковану електрохімічну регенерацію NAD(P)H з NAD(P)+, який, наприклад, утворюється при відновному розщепленні кисню, що каталізується ферментами. Відповідний винаходові спосіб електрохімічної регенерації може, зокрема, знайти застосування в рамках електроферментативних взаємодій, що проходять за участю NAD(P)H, зокрема, при окисних ферментативних перетвореннях субстратів при дії монооксигеназ. Зокрема, об'єктом винаходу є електроферментативний спосіб одержання 2,3-дигідроксифенільних похідних, який каталізується монооксигеназами. Біокаталітичні реакції набувають дедалі більшого значення в лабораторному органічному синтезі та в численних галузях промислового застосування. Зокрема, високі регіота стереоселективності, звичайні для ферментативних взаємодій, що протікають одночасно в м'яких умовах з високим виходом, роблять їх привабливими інструментами в плануванні синтезів. На відміну від гідролітичних ферментів, що вже знахо дять багатопланове застосування, використання окисно-відновних ферментів для енантіоселективного відновлення та для хемо-, регіо- та енантіоселективних окиснення, незважаючи на їх високий синтетичний потенціал, поширене ще не дуже широко. В основі цього лежить, насамперед, проблема ефективної регенерації кофактора, що не знайшла дотепер задовільного рішення. Поряд з усталеними способами регенерації кофакторів за участю спряжених ферментів [1а, б, в, г] були також розроблені та поширені на NAD(P)+- і NАО(Р)Н-залежн1 ферменти електрохімічні способи регенерації [2а, б, в]. Перевага опосередкованої електрохімічної регенерації кофактора полягає в тому, що для цього потрібний тільки фермент, який бере участь в утворенні продукту, і завдяки цьому стає зайвою оптимізація подвійної ферментної системи, яка часто досягається з великими труднощами. Крім того, при цьому можна відмовитися також від косубстрату. Монооксигенази мають важливе синтетичне значення, оскільки вони можуть регіо- та стерео 5 75074 6 селективно вбудовувати кисневі функціональні групи у відповідні субстрати. Для цього вони мають потребу в молекулярному кисні, О-О-зв'язок якого піддається відновному розщепленню з утворенням води [3а, б]. Нативні кофактори монооксигеназ NADH або NADPH дають необхідні для цього де відновні еквіваленти. Способи, які проводилися до R і R' мають приведені вище значення, піддасьогоднішнього дня in vitro за участю монооксигеють перетворенню під дією 2-гідроксибіфеніл-3наз як ферментів, що каталізують утворення промонооксигенази (HbpA) (E.C.1.14.13.44) в присутдукту, базуються на регенерації кофактора в ності NADH та кисню та спряженому ферментативному процесі з викорисб) NAD+, що утворився, електрохімічно відновтанням форміатдегідрогенази [4а, б] (для NADH люють до NADH. або, відповідно, NADPH) або глюкозо-6Крім того, ці задачі вирішуються завдяки розфосфатдегідрогенази [5] для (NADPH). робці способу регенерації NAD(P)H при окисному Reipa та ін. [10] описують спосіб електрохімічферментативному перетворенні субстрату, що ної регенерації путидаредоксину, природного парпроходить з витратою NAD(P)H, під час якого окитнера цитохром-CYP-101-монооксигенази сну ферментативну взаємодію, що проходить з (Е.С.1.14.15.1), в окисно-відновній реакції. Для витратою NAD(P)H, проводять у присутності цього запропоноване застосування спеціального NAD(P)H та бажано за участю кисню, a NAD(P)+, електрода з оксиду олова з доданням сурми, що який утворюється при окисненні субстрату, електпідходить тільки для відновлення путидаредоксирохімічно відновлюють до NAD(P)H. Так, наприну. клад, залежну від NAD(P)H монооксигеназу (із Held та ін. [8] описують біокаталітичне одеркласу Е.С 1.14.-.-) можна інкубувати разом із субжання 3-фенілпірокатехіну з використанням непостратом, що окиснюється, у присутності NAD(P)H шкоджених клітин Escherichia coli JM 101 (pHDT та в присутності кисню, а NAD(P)+, що утворюється 461). Цей рекомбінантний мікроорганізм призначепри відновному розщепленні кисню та окисненні ний для одержання ферменту 2-гідроксибіфеніл-3субстрату, електрохімічно відновлювати до монооксигенази. У цьому випадку немає необхідNAD(P)H. ності в електрохімічній регенерації використаного Даний винахід вперше дозволяє проводити не NADH, оскільки цей кофактор знову регенерується зв'язану з ферментом непряму електрохімічну реферментативною системою непошкоджених клітин генерацію NADH або, відповідно, NADPH, у рамках Escherichia coli. реакцій, що проходять з витратою кисню, наприЗадача даного винаходу полягала в тому, щоб клад реакцій, що каталізуються монооксигеназами. розробити безферментний, селективний та ефекЗавдяки непрямій електрохімічній регенерації котивний спосіб непрямої електрохімічної регенерафактора стає можливим перетворення субстрату ції NAD(P)H, що, наприклад, у сполученні з монооза безперервною схемою. ксигеназами може знайти використання для „Опосередкована” електрохімічної регенерації окисного перетворення субстратів при відновному NAD(P)H в рамках даного винаходу відбувається розщепленні кисню. Ще одна задача полягала в за умови регенерування кофактора через придатрозробці способу, що робить можливим ферменний для цього окисно-відновний каталізатор, що тативний синтез 2,3-дигідроксифенільних сполук, переносить необхідні для відновлення електрони який каталізується монооксигеназами, наприклад від катода на окиснений кофактор. 2,3-дигідроксибіфенілу, при непрямій електрохіміПершим об'єктом винаходу є електроферменчній регенерації NAD(P)H. тативний спосіб одержання 2,3Поставлені задачі вирішуються завдяки роздигідроксифенільних похідних загальної формули І робці електроферментативного способа одержання 2,3-дигідроксифенільних похідних загальної формули І де R означає незаміщену або заміщену від одного до декількох разів фенільну групу, алкільну групу з числом атомів вуглецю від одного до шести, атом галогену або нітрильну групу, а R' означає атом водню або гідроксильну групу, при цьому даний спосіб полягає в тому, що а) моногідроксифенільну сполуку загальної формули II де R означає незаміщену або від одного до декількох разів заміщену, наприклад атомами галогенів, наприклад, атомами фтору, хлору, брому або йоду, нітрильною або гідроксильною групою, зокрема, гідроксильною групою, фенільну групу, означає алкільну групу з числом атомів вуглецю від одного до шести, наприклад, це метильна, етильна, н-пропільна або ізопропільна група, нбутильная, ізобутильна або трет.-бутильна група, а також н-пентильна або н-гексильна група або у кожному окремому випадку їх розгалужені аналоги, 7 75074 8 означає атом галогену, наприклад атом фтору, II) від 0,01 до 50ммолей/л, зокрема, від 0,1 до хлору, брому або йоду, або ж означає нітрильну 4ммолей/л, групу, а б) концентрація NAD+ від 0,01 до 5ммолей/л, R' означає атом водню або гідроксильну групу, зокрема, від 0,01 до 0,5ммоля/л, причому R' знаходится в м- або в п-положенні, в) концентрація родієвого комплексу від переважно в п-положенні до 2-гідроксильної групи 1мкмоля/л до 5ммолей/л, зокрема, від 5мкмолей/л фенільного кільця, при цьому даний спосіб полядо 0,5ммоля /л, гає в тому, що г) концентрація НbрА від 1 до 5000одиниць/л, а) моногідроксифенільна сполука загальної зокрема, від 10 до 1000одиниць/л, формули II д) концентрація флавінаденіндинуклеотиду (FAD) від 0 до 200мкмолей/л, зокрема, від 0 до 20 або від 1 до 20мкмолей/л, e) концентрація каталази від 0 до 1x107 одиниць/л, ж) значення pH від 4 до 9, зокрема, від 6 до 7,5, де з) температура від 10 до 40°С, зокрема, від 20 R і R' мають приведені вище значення, піддадо 35°С або близько 30°С, ється перетворенню під дією 2-гідроксибіфеніл-3и) катодний потенціал від -600 до -900мВ, зокмонооксигенази (HbpA) (Е.С.1.14.13.44) у присутрема, від -650 до -800мВ, ності NADH та кисню і к) подача кисню від 20 до 120см3/(хв-л) шляб) NAD+, що утворився, електрохімічно відновхом барботування або, зокрема, без барботування люють до NADH. через проникні для кисню мембрани або шланги, Бажано, коли електрохімічне відновлення як це, наприклад, описане в [11]. + NAD проводять в присутності гідридно-родієвого Придатні для реалізації винаходу електродні окисно-відновного каталізатора, що утворюється системи описані в [12] та [13]. Як приклади прийнна катоді та регенерується. Окисно-відновний каятних анодно-катодних пар, що представляють талізатор при цьому бажано представлений розінтерес, але не обмежують об'єму правової охорочинним родієвим комплексом, який може бути елени, можна назвати пари вуглецевий кактрохімічно переведений у гідридно-родієвий тод/платиновий анод, в яких, зокрема, вуглецевий комплекс при катодному потенціалі в межах від катод виготовлений у формі циліндра (вугільний 650 до -800мВ, що вимірюється відносно хлорсріфетр, Sigraflex®), a анод виготовлений з платинобного електрода (Ag/AgCI, при насиченні) (pH = 6вого дроту. 9, температура 20-60°С, зокрема, від приблизно 20 Перетворювані відповідно до винаходу субдо 35°С, наприклад близько 30°С). Особлива пестрати формули II у загальному випадку предстаревага надається використанню при проведенні вляють собою доступні сполуки, і вони можуть реакції, що каталізується НbрА, родієвого комплебути придбані комерційним шляхом або отримані ксу загальної формули III звичайними для органічної хімії способами. Як [Ср Rh(lll) (bpy)CI]CI (III), приклади, що не можуть обмежувати обсяг праводе вої охорони, можна назвати: Ср означає циклопентадієнільний або пента2-гідрокси-алкілбензоли з числом атомів вугметилциклопентадієнільний залишок і bру означає лецю в алкільній групі від одного до шести, гало2,2'-біпіридил, причому кожне з піридильних кілець гензаміщені 2-гідроксибензоли, 2може бути від одного до декількох разів, зокрема, гідроксибензонітрил та 2,5-дигідроксизаміщені один раз, заміщене донорною групою, при цьому аналоги цих похідних бензолу; 2-гідроксибіфеніл донорна група вибрана з метильної групи, метокта заміщені декількома гідроксильними групами сигрупи та ацетамідогрупи. У бажаному варіанті біфеніли, наприклад 2,4-, 2,5або 2,6кожне піридильне кільце може нести ці замісники в дигідроксибіфеніл, 2,n'-дигідроксибіфеніли (тут n' 4- або в 5-положенні. В окремому випадку піридиозначає 2, 3 або 4) або ж 2,n',m'льні кільця заміщені однаковими донорними грутригідроксибіфеніли (при цьому n' і m' відрізняютьпами. ся один від одного та означають у кожному окреУ рамках відповідного винаходові способу при мому випадку 2, 3 або 4). каталізі за участю НbрА родієвий комплекс форВідповідно до винаходу перевага надається мули III відновлюється на катоді до здатного до використанню як окисно-відновних каталізаторів + відновлення NAD гідридно-родієвого комплексу [СрRh(bру)СІ]СІ-комплексів. Одержання цих комформули ІІІа плексів загальновідоме, і воно проводиться так, як [Ср Rh(l) (bpy)H]CI з Η у вигляді протона (ІІІа) це описано в [14] або [15]. Гідридно-родієві комабо плекси, що утворюються з них після електрохіміч[Ср Rh(lll) (bpy)H]CI з Η в вигляді гідридіона, ного відновлення при –700мВ (відносно Де Аg/АgСІнасич.) або після хімічного відновлення фоСр і bру мають приведені вище для формули рміатом, швидко та якісно переводять NAD(P)+ в III значення. 1,4-NАО(Р)Н-форму, активну по відношенню до Бажано, коли одержання дигідроксизаміщених ферментів [2, 6]. сполук, що відповідають винаходові, проводять в Як типовий приклад прийнятних ферментів умовах, що описані нижче: можна назвати 2-гідроксибіфеніл-3а) концентрація субстрату (сполука формули монооксигеназу, що є представником класу фла 9 75074 10 він-залежних монооксигеназ (HbpA, Е.С. Відповідний винаходові спосіб переважно ви1.14.13.44) P. azelaica, та має потребу в NADH як у користовує як окисно-відновний каталізатор для кофакторі [7]. Цей фермент знаходиться у вигляді регенерації NAD(P)H родієвий каталізатор, що при гомотетрамеру з загальною масою 256кДа, у відкатодному потенціалі в межах від -650 до -800мВ, повідності зі схемою 1 він каталізує селективне який вимірюється відносно хлорсрібного електрода (Ag/AgCI, при насиченні) (pH = 6-9, температура орто-гідроксилювання цілого ряду -заміщених 20-60°С, зокрема, від приблизно 20 до 35°С, нафенольних похідних. Хімічним шляхом цю реакцію приклад, близько 30°С) може бути переведений у не можна провести з порівняною селективністю. гідридно-родієвий комплекс. Схема 1: Принцип протікання реакції з НbрА Для регенерації NAD(P)H у відповідному винаходові способі перевага надається використанню родієвих комплексів загальної формули III' [Ср Rh(lll) (bpy)CI]CI (III'), де Ср означає циклопентадієнільний або пентаБажано, коли реакція, яка каталізується HbpA, метилциклопентадієнільний залишок, і bру ознапротікає у водному реакційному середовищі, значає 2,2'-біпіридил, причому кожне з піридильних чення pH якого встановлено за допомогою звикілець може бути від одного до декількох разів, чайних буферних сполук, що негативного не вплизокрема, один раз, заміщене донорною групою, вають на протікання реакції та на електрохімічний при цьому донорна група вибрана з метильної процес, таких як, наприклад, HEPES [N-(2групи, метоксигрупи та ацетамідогрупи. Крім того, гідроксиетил)-піперазин-N'-(2-етансульфонат)], як донорна група може виступати залишок, що PIPES [піперазин-1,4-біс(2-етансульфонат)] і, зокпредставляє собою похідне поліетиленгліколю, рема, буфер на основі фосфату калію та буфер на наприклад похідне поліетиленгліколю від 2000 до основі гідрохлориду ТРІС. Концентрація буфера 20000. У кращому варіанті кожне піридильне кільпри цьому лежить у межах від приблизно це може нести один такий замісник у 4- або в 520ммолей/л до 0,2моля/л, зокрема, від приблизно положенні. В окремому випадку піридильні групи 20ммолей/л до 50ммолей/л. Значення pH перевазаміщені однаковими донорними групами. жно встановлюють у межах від приблизно 6 до 8, Родієвий комплекс формули III відновлюється зокрема, близько 7,5. на катоді в гідридно-родієвий комплекс формули Реакційне середовище може містити також інІІІа' ші звичайні добавки, як, наприклад, солюбілізатор [Ср Rh(l) (bpy)H]CI з Η в вигляді протона, для субстрату, кофактори для ферменту, що викоабо ристовується, наприклад FAD або FMN, та інші [Ср Rh(lll) (bpy)H]CI з Η в вигляді гідридіона, подібні їм речовини. де Ср та bру мають приведені вище для форПри використанні чутливих до окиснення фермули III' значення, причому цей гідридно-родієвий ментних систем може мати сенс використовувати комплекс може відновлювати NAD+. антиоксиданти. Якщо, наприклад, за умовами проБажано, коли відповідний винаходові спосіб ведення процессу відбувається утворення перокрегенерації NAD(P)H реалізують у відповідності з сиду водню, який може справляти негативний наступними умовами: вплив на активність ферменту, то реакцію можна а) концентрація NAD(P)+ від 0,01 до проводити в присутності каталази, яка додається, 5 5ммолей/л, зокрема, від 0,01 до 0,5ммоля/л, наприклад, у концентрації 1 10 одиниць/л. б) концентрація родієвого комплексу від Ще один об'єкт винаходу відноситься до спо1мкмоля/л до 5ммолей/л, зокрема, від 5ммолей/л собу електрохімічної регенерації NAD(P)H, який до 0,5ммоля/л, використовується при окисному ферментативному в) концентрація монооксигенази від 1 до перетворенні субстрату, що проходить з витратою 5000одиниць/л, зокрема, від 10 до 1000одиниць/л, NAD(P)H, при цьому окисне ферментативне перег) концентрація кофактора (наприклад, FAD) творення окисного субстрату, яке проходить з вивід 0 до 200мкмолей/л, зокрема, від 0 до 20 або тратою NAD(P)H, проводять у присутності від 1 до 20мкмолей/л, NAD(P)H і переважно з витратою кисню, а утворе+ д) концентрація каталази від 0 до 1x107 одиний при окисненні субстрату NAD(P) електрохіміниць/л, чно відновлюють у NAD(P)H. Цей спосіб особливо e) значення pH від 4 до 9, зокрема, від 6 до прийнятний для застосування в рамках реакцій, 7,5, що каталізуються монооксигеназами. При цьому ж) температура від 10 до 40°С, зокрема, від 20 NAD(P)H-залежну монооксигеназу (із класу Е.С до 35°С або приблизно 30°С, 1.14.-.-) інкубують з субстратом, що вступає в реаз) катодний потенціал від -600 до -900мВ, зоккцію окиснення, у присутності NAD(P)H і в присут+ рема, від -650 до -800мВ, ності кисню, a NAD(P) , що утворився при віднові) подача кисню від 20 до 120см3/(хв-л) шляхом ному розщепленні кисню та при окисненні барботування або, зокрема, без барботування субстрату, електрохімічно відновлюють до через проникні для кисню мембрани або шланги, NAD(P)H. як це, наприклад, описане в [11]. Відповідно до кращого варіанта реалізації ви+ Реагуючі відповідно до винаходу субстрати находу електрохімічне відновлення NAD(P) пропредставляють собою в загальному випадку досводять в присутності переважно розчинного гідритупні сполуки, вони можуть бути придбані комердно-родієвого окисно-відновного каталізатора, що ційними шляхом або отримані звичайними для може утворюватися і регенеруватися на катоді. 11 75074 12 органічної хімії способами. на патент ФРН №19935115.5 (БАСФ АГ). Відповідно до винаходу перевага надається 3) гідроксилювання алільних або бензильних використанню як окисно-відновних каталізаторів атомів вуглецю [СрRh(bру)СІ]СІ-комплексів. Одержання цих комплексів загальновідоме і воно проводиться так, як це описано в [14] або [15]. Гідридно-родієві комплекси, що утворюються з них в результаті електрохімічного відновлення при -700мВ (по відношенню до Ag/АgСІнасич.) або ж після хімічного відновлення форміатом, швидко переводять H.Fretz, W.D.Woggon, R.Voges, Неl. Chim. Acta, NAD(P)+ в 1,4-NАО(Р)Н-форму, активну по відно1989, 72, 391-400. шенню до ферментів [2,6]. Бажано, коли реакція протікає у водному реакційному середовищі, значення pH якої встановлено на відповідну величину за допомогою звичайних буферних сполук, що не справляють негативного впливу на протікання реакції та на H.L.Holland, T.S.Manoharan, F.Schweizer, електрохімічний процес, таких, як, наприклад, Tetrahedron: Asymmetry, 1991, 2, 335-338. HEPES [N-(2-гідроксиетил)-піперазин-N'-(24) епоксидування: етансульфонат)], PIPES [піперазин-1,4-біс(2етансульфонат)] і, зокрема, буфер на основі фосфату калію і буфер на основі гідрохлориду ТРІС. Концентрація буфера при цьому лежить у межах S.W.May, B.J.Abbot, J. Biolog. Chem., 1973, від приблизно 20ммолей/л до 0,2моля/л, зокрема, 248, 1725-1730 від приблизно 20ммолей/л до 50ммолей/л. Зна5) окиснення за Байєром-Віллігером чення pH переважно встановлюють у межах від приблизно 6 до 8, зокрема, близько 7,5. Реакційне середовище може містити також інші звичайні добавки, як, наприклад, солюбілізатор для субстрату, кофактори для ферменту, що використовується, наприклад FAD або FMN, та інші подібні їм речовини. При використанні чутливих до окиснення ферRoberts та ін., J. Mol. Cat. В Enzymatic, 1998, 4, ментних систем може мати сенс застосовувати 111ст. антиоксиданти. Якщо, наприклад, за умовами про5) окиснення гетероароматичних сполук ведення процесу відбувається утворення пероксиду водню, який може негативно впливати на активність ферменту, то реакцію можна проводити в присутності каталази, яка додається, наприклад, у концентрації 1 105 одиниць/л. Відповідний спосіб регенерації NAD(P)H може переважно використовуватись для наступних типів реакцій, що включають окисне ферментативне перетворення: а) окиснення насичених або ненасичених аліфатичних або ароматичних атомів вуглецю, зокрема, це реакції гідроксилювання, епоксидування або окиснення за Байєром-Віллігером; б) окиснення сірки або селену; в) окиснення азоту або фосфору: г) окиснення галогенідів. Необмежуючими прикладами типу реакцій а) служать: 1) гідроксилювання аліфатичного вуглецю Прогестерон 11- -Гідроксипрогестерон Ця реакція описана, наприклад, у патенті Японії №75/54957 (Takeda). 2) -гідроксилювання довголанцюгових жирних кислот, що каталізується цитохром-Р450монооксигеназою. Це описане, наприклад, у заявці Каталіз у кожному випадку здійснюють за допомогою циклогексанон-монооксигенази, як це описано в роботах C.T.Walsh та ін., Angew. Chem., 1988, 100, 242, і Roberts та ін., J. Моl. Cat. В Enzymatic, 1998, 4, 111. Крім того, об'єктом винаходу є застосування окисно-відновного каталізатора відповідно до при 13 75074 14 веденого вище визначення для безперервного або Фіг.3 представляє передбачуваний механізм для періодичного процесу електрохімічної регенегідридокиснення. рації NAD(P)H, бажано для проведення реакцій, Фіг.4 представляє вплив вмісту кисню на утвощо протікають з поглинанням кисню, зокрема, для рення 2,3-дигідрокси-біфенілу при опосередковареакцій окиснення, які каталізуються монооксигеній електрохімічній регенерації кофактора (О без назами, зокрема, для реакцій окиснення зазначеподачі кисню в розчин, через 1 годину після поного вище типу. чатку постійної подачі кисню). І, нарешті, даний винахід стосується біореакФіг.5 представляє порівняння швидкості переторів для безперервного або періодичного проветворення при хімічному та опосередкованому еледення реакцій, які протікають з поглинанням кисктрохімічному утворенні гідридно-родієвого комню, зокрема, для електроферментативних реакцій, плексу (О окисно-відновна хімічна регенерація з що каталізуються монооксигеназами, та які вклюформіатом як розчинником, опосередкована чають в одному реакційному обсязі електродну електрохімічна регенерація). пару та рідке однофазне або двофазне реакційне Фіг.6 представляє схематичне зображення середовище, що містить у відповідності до привеприйнятного реактора для періодичного проведеного вище для кожного окремого випадку визнадення процесу, що включає об'єм для проведення чення фермент, зокрема, монооксигеназу, субреакції з мішалкою, кільцевий катод, розташовастрат, NAD(P)H як кофактор і окисно-відновний ний у центрі анод, електрод порівняння, підведенкаталізатор, причому на катоді створюється елекня стиснутого повітря в реакційне середовище. тродний потенціал, що достатній для переносу Приклад 1. Електроферментативне окиснення окисно-відновних еквівалентів (електронів) на оки2-гідроксибіфенілу до 2,3-дигідроксибіфенілу. сно-відновний каталізатор. У відповідності до Фіг.1 електроферментативДля ознайомлення з біореакторами відповідну взаємодію проводять у електролітичній комірці ного типу можна послатися, наприклад, на їх опис періодичної дії, що схематично представлена на у роботах [16] і [17]. Фіг.6. У ролі катода при цьому виступає циліндриФункціонування реактора та проведення прочний електрод з вуглецевого фетру (об'єм близько цесу можуть бути приведені спеціалістом у відпо27см3). Завдяки включенню платинового протиевідність з вимогами здійснюваної окисно-відновної лектрода в шланг для діалізу (маса від 10кДа череакції. Однофазні або двофазні реакційні серерез нього не проходить) досягаються умови роздідовища можуть використовуватись як і компартленої комірки. ментація реакційного простору. Двофазні реакційні За допомогою підключеного через шланг хлосистеми можуть бути, наприклад, бажаними при рсрібного електрода (Аg/АgСІнасич.) встановлюють взаємодії субстратів та/або при утворенні продуккатодний потенціал -750мВ. У 100мл фосфатнотів, що нерозчинні або погано розчинні у водному калієвого буфера (50ммолей/л, pH 7,5) розчиняреакційному середовищі. У цьому випадку, наприють кофактор окиснення NAD+ (0,2ммоля/л), клад, субстрат може знаходитися в органічному [Cp*Rh(bpy)CI]2+ (0,1ммоля/л), FAD (20мкмолей/л), середовищі. Він безперервно надходить у водну каталазу (250000 одиниць), HbpA (19 одиниць), а фазу, реагує в ній, а продукт, що утворився, може також субстрат (2ммоля). Реакція протікає при знову переходити в органічну фазу. Компартментемпературі 30°С протягом п'яти годин. тація дозволяє, наприклад, розділити в просторі та Протікання реакції контролюють за допомогою у часі ферментативну реакцію та реакцію на елекВЕРХ на колонці RP-18, використовуючи для тродах. Крім того, перевага надається введенню елюювання суміш метанолу з водою (0,1% фоскисню в газоподібному стані, зокрема, введенню форної кислоти) 60:40. газу без утворення бульбашок, для ознайомлення Приклад 2. Вплив розчиненого кисню на регез цим способом можна послатися, наприклад, на нерацію NADH. опис у роботі Rissom [46]. Оскільки кисень бере участь у здійсненні посВинахід більш детально ілюструється на приклідовності реакцій, вплив розчиненого кисню на ладах у прикладених схемах. компоненти системи повинен бути дослідженим. Фіг.1 є схематичним зображенням відповідного При цьому виявляється, що кисень інгібує утвовинаходові електроферментативного процесу, що рення NADH за участю гідридно-родієвого комплепротікає з утворенням 2,3-дигідро-оксибіфенілу з ксу як при його одержанні хімічним шляхом через одночасною електрохімічною регенерацієюNADH, форміат, так і при його одержанні відповідно до при цьому на катоді йдуть утворення та регенеравинаходу електрохімічним шляхом (Фіг.2). Як одція гідридно-родієвого (III) окисно-відновного катанозначно випливає з Фіг.2, при введенні кисню, лізатора. Після переносу гідридіона на NAD+ та наприклад зі швидкістю 10см3/хв, швидкість утвоутворення NADH він відновлює монооксигеназу, рення NADH знижується від 1,1ммолей/л год до наприклад, простетичну FAD-групу в 20,27ммолей/л год. При введенні 15см3/хв виявити гідроксибіфеніл-З-монооксигеназі з утворенням утворення NADH вже не вдається. Проте інгібуактивної РАОН2-функції. Ця відновлена форма вання носить зворотний характер, оскільки після ферменту каталізує потім у присутності кисню окприпинення подачі кисню швидкість утворення сигенування субстрату, наприклад, перетворення NADH знову швидко зростає до її оптимального 2-гідроксибіфенілу в 2,3-дигідроксибіфеніл. значення. Концентрація NADH також досягає макФіг.2 представляє вплив молекулярного кисню симального значення. Вдалося встановити, що на утворення NADH при непрямій електрохімічній продуктом реакції гідридно-родієвого комплексу з регенерації ( без продувки повітрям, О із продувмолекулярним киснем є пероксид водню, схему 3 кою повітрям 10см /хв). утворення якого можна уявити собі відповідно до 15 75074 16 Фіг.3. Крім того, при прикладеному потенціалі педозованого підведення субстрату in situ, що витіроксид водню утворюється також в результаті кає з цього, а також екстракції пірокатехінового прямого відновлення кисню на катоді. Тому доціпродукту з'являється можливість здійснення прольно додавати каталазу, оскільки вона розкладає цесу за ефективною безперервною схемою. пероксид водню при ферментативній взаємодії. Згідно з винаходом вперше вдалося успішно Приклад 3. Вплив подачі кисню на ступінь пепровести взаємодію з електрохімічною регенераретворення цією NADH, яка каталізується флавінзалежною Приведені на Фіг.3 результати показують, що монооксигеназою. ступінь перетворення при реакціях без зовнішньоДаний винахід створює основу для залучення го підведення кисню після закінчення короткого монооксигеназ в органічні синтези як у лабораторчасу перестає зростати, досягши значення близьному масштабі, так і у випадку промислового зако 20% (світлі кола або, відповідно, чорні квадрати стосування. Цей клас окиснюючих ферментів до приблизно 1 години). Після початку подачі киспредставляє великий інтерес у синтетичному відню через 1 годину (8см3/хв) швидкість перетвоношенні, оскільки вони, наприклад, можуть вводирення, а разом з нею й утворення продукту зрости гідроксильні функціональні групи в ароматичні системи, а також у неактивовані чисті вуглеводні. тають до величини 1,1ммоля/л год (202мг/л год). Крім того, вони можуть переносити кисень на гетеЗмінні значення для медіатора складають 11год-1. роатоми або на подвійні зв'язки з утворенням епоАналогічні значення одержують у тих випадках, ксидів. У доповнення до цього вони каталізують коли гідридно-родієвий комплекс утворюється хіреакції окиснення за Байєром-Віллігером. В усіх мічним шляхом з форміату натрію. На Фіг.5 покавипадках стають доступними чисті енантіомери зані швидкості перетворення для непрямої електпродуктів. рохімічної регенерації кофактора в названих Основна електрохімічна концепція регенерації умовах, але при постійному підведенні кисню зі NAD(P)H є ефективною альтернативою, що легко швидкістю 10см3/хв, а для окисно-відновного проздійснюється, використовуваним до сьогоднішньоцесу за участю форміату - це концентрація форміго дня процесам in vivo, або таким способам, що ату натрію 160ммоль/л при інших однакових умовключають ферментативні системи для регенеравах. Продуктивність складає близько 50% від ції. Вдалося довести загальну застосовуваність оптимізованого ферментативного способу або, залежних від кисню монооксигеназ, у тому числі у відповідно, способу in vitro зі спряженою фермензазначених умовах проведення взаємодії. тативною регенерацією NADH (390мг/л год) [8]. Список літератури Швидкість реакції лімітується не утворенням [1] a) Hummel, W., та ін., Eur. J. Biochem. 1989, гідридно-родієвого комплексу на катоді, а конкуре184, 1-13; б) Shaked, Ζ., та ін., J. Am. Chem. Soc. нтним інгібуванням окисно-відновного каталізато1980, 102, 7104-7108; в) Abril, О., та ін., Bioorg. ра паралельною реакцією з молекулярним киснем Chem. 1989, 17, 41-52; г) Seelbach, К., та ін., (Фіг.4). Tetrahedron Lett. 1996, 37, 1377-1380. У відповідному винаходові безперервному [2] a) Hilt, G., та ін., Liebigs Ann./Recueil 1997, електроферментативному процесі негативний 2289-2296; 6) Westerhausen, D., та ін., Angew. вплив розчиненого кисню на опосередковану елеChem. 1992, 104, 1496-1498; Angew. Chem. Int. Ed. ктрохімічну регенерацію NADH повинен бути легко Engl. 1992, 31, 1529-1531; в) Ruppert, R., та ін., виключений шляхом компартментації усієї системи Tetrahedron Lett. 1987, 52(28), 6583-6586. на окремі модулі. Завдяки розділенню в просторі [3] a) Walsh, С.Т., Асc. Chem. Res. 1980, 13, та дозованій подачі необхідного для протікання 148-155; б) Walsh, C.T. та ін., Angew. Chem. 1988, ферментативної реакції кисню, яка йде після елек100, 342-352; Angew. Chem.Int. Ed. Engl. 1988. трохімічного етапу, його інгібуючий ефект на реге[4] a) Hummel, W., та ін.; Appl. Microbiol нерацію NADH знижується до мінімуму. Biotechnol. 1986, 25, 175-185; б) Rissom, R. та ін., Стабільність у часі для проведених за періоTetrahedron Asymmetry 1997, 15(8), 2523-2526. дичною схемою електролізів може бути поліпшена [5] Wong, C.-H., та ін., J. Am. Chem. Soc. 1981, завдяки зниженню денатуруючого ефекту, що су103, 4890-4899. проводжує введення газу шляхом барботажу. На [6] a) Steckhan, Ε. та ін., Organometallics, 1991, границі розділення фаз рідина/газ виникають зсув10, 1568-1577; б) Ruppert, R. та ін., J. Chem. Soc, ні ефекти, що у порівняно короткий термін привоChem. Commun., 1988, 1150-1151. дять до денатурації ферменту. У дослідах порів[7] Suske, W. А. та ін., J. Biol. Chem., 1997, 272 няння вдалося показати, що HbpA при (39), 24257-242565. термостатуванні при 30°С та при перемішуванні [8] Held, M. та ін., Biotechnol. Bioeng., 1999, 62 (швидкість 250 обертів за хвилину) навіть через 12 (6), 641-648. годин зберігає більш 85% початкової активності. З [9] Wandrey, С, Chem. Ing. Tech. 1976, 48, 537. початком нагнітання повітря активність в залежно[10] Reipa, V. та ін., Proc. Natl. Acad. Sсi. USA, сті від швидкості подачі знижується протягом одні1997, 94, 13554-13558. єї години до 70%. Завдяки застосуванню обладна[11] Schneider та ін., Enzyme Microbiol. ного мембраною реактора для проведення Technol., 1995, 17, 839. ферментативних процесів [9] фермент може бути [12] Sawyer, D.T., Electrochemistry for Chemists, захищений від негативного впливу за допомогою 2-е вид, Уайлі-Інтерсайєнс; Нью Йорк. кисню, що вводиться гетерогенним шляхом, в ре[13] Kissinger, P. Т., Laboratory Techniques in зультаті чого досягається висока стабільність проElectroanalytical Chemistry, Марсель Деккер, Інк.; тікання процесу в часі. Зокрема, завдяки застосуНью Йорк/Базель. ванню двофазного способу ведення процесу та 17 75074 18 [14] Kölle, U. та ін., Angew. Chem. 1987, 99, [16] Kragl, U. та ін., Chem. Ing. Tech., 1992, 499 572. [17] Brielbeck, В. та ін., Biocatalysis, 1994, 10, [15] Kölle, U. та ін., Chem.Ber. 1989, 122, 1869. 49. Комп’ютерна верстка Л. Купенко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for the electroenzymatic production of 2,3-dihydroxyphenyl derivatives and method foe electrochemical regeneration of nad(p)h from nad(p)+
Назва патенту російськоюЭлектроферментативный способ получения 2,3-дигидроксифенильных производных и способ электрохимической регенерации nad(p)h из nad(p)+
МПК / Мітки
МПК: C12M 1/40, C12P 1/00, C12P 7/22
Мітки: похідних, 2,3-дигідроксифенільних, спосіб, електроферментативний, одержання, електрохімічної, nad(p)h, регенерації, nad(p)+
Код посилання
<a href="https://ua.patents.su/9-75074-elektrofermentativnijj-sposib-oderzhannya-23-digidroksifenilnikh-pokhidnikh-ta-sposib-elektrokhimichno-regeneraci-nadph-z-nadp.html" target="_blank" rel="follow" title="База патентів України">Електроферментативний спосіб одержання 2,3-дигідроксифенільних похідних та спосіб електрохімічної регенерації nad(p)h з nad(p)+</a>
Попередній патент: Спосіб одержання магнезитової добавки та спосіб модифікації аміачної селітри
Наступний патент: Спосіб виготовлення вибухової суміші та вибухова суміш
Випадковий патент: Спосіб одержання поверхнево-активних речовин












