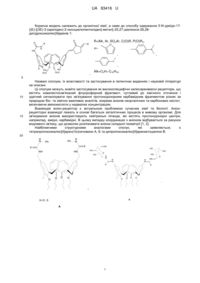
Спосіб одержання 5-n-уреїдо-17-{(е)-[(3e)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27-діалкокси-26,28-дигідроксикалікс[4]аренів
Номер патенту: 83416
Опубліковано: 10.09.2013
Автори: Шишкін Олег Валерійович, Пивоваренко Василь Георгійович, Матвєєв Юрій Іванович, Кальченко Віталій Іванович, Рябицький Олексій Борисович, Шишкіна Світлана Валентинівна, Духно Олексій Ігоревич
Формула / Реферат
Спосіб одержання 5-N-уреїдо-17-{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27-діалкокси-26,28-дигідроксикалікс[4]аренів загальної формули:

R=Alk, Ar, SO2Ar, C(O)R, P(O)R2
![]() ,
, ![]() ,
, ![]()
Alk=C3H7-C16H33
який відрізняється тим, що 5-нітро-17-форміл-25,27-дипропокси-26,28-дигідроксикалікс[4]арен конденсують з (2Е)-2-(ариліден)циклопентаноном в присутності диметиламонію диметилкарбамату (DIMCARB) в хлороформі при нагріванні в межах 20-60 °C з утворенням 5-нітро-17-{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27-діалкокси-26,28-дигідроксикалікс[4]аренів, відновлення яких гідразингідратом в присутності нікелю Ренея дає відповідні амінопохідні, які взаємодією з ізоціанатом при кімнатній температурі в етері перетворюються в цільові продукти, які виділяють звичайними методами.
Текст
Реферат: Спосіб одержання 5-N-уреїдо-17-{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27діалкокси-26,28-дигідроксикалікс[4]аренів полягає в тому, що 5-нітро-17-форміл-25,27дипропокси-26,28-дигідроксикалікс[4]арен конденсують з (2Е)-2-(ариліден)циклопентаноном в присутності диметиламонію диметилкарбамату (DIMCARB) в хлороформі при нагріванні в межах 20-60 °C з утворенням 5-нітро-17-{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]метил}25,27-діалкокси-26,28-дигідроксикалікс[4]аренів, відновлення яких гідразингідратом в присутності нікелю Ренея дає відповідні амінопохідні, які взаємодією з ізоціанатом при кімнатній температурі в етері перетворюються в цільові продукти, які виділяють звичайними методами. UA 83416 U (12) UA 83416 U UA 83416 U Корисна модель належить до органічної хімії, а саме до способу одержання 5-N-уреїдо-17{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]-метил}-25,27-діалкокси-26,28дигідроксикалікс[4]аренів 1: O O HN R R=Alk, Ar, SO2Ar, C(O)R, P(O)R2, R' O N H R'= N , , O O OH ALK O , HO ALK , Alk=C3H7-C16H33. 5 10 15 Названі сполуки, їх властивості та застосування в патентних виданнях і науковій літературі не описані. Ці сполуки можуть знайти застосування як високоспецифічні каліксаренвмісні рецептори, що містять ковалентнозв'язаний флуорофорний фрагмент, чутливий до хімічного оточення і здатний сигналізувати про зв'язування протонодонорним карбамідним фрагментом різних за природою біо- та хімічно важливих аналітів, зокрема аніонів неорганічних та карбонових кислот, включаючи амінокислоти у надмалих концентраціях. Взаємодія аніон-рецептор є актуальною проблемою сучасних хімії та біології. Аніонрецепторні взаємодії лежать в основі багатьох каталітичних процесів в живому організмі. Для зв'язування аніонів використовують нейтральні ліганди, які містять протонодонорні центри, наприклад, амідні, карбамідні. В цьому випадку координація з аніоном відбувається за рахунок водневого зв'язку, що дозволяє розпізнавати аніони складної геометрії [1, 2]. Найближчими структурними аналогами сполук, які заявляються, є тетрапропоксикалікс[4]арен(тіо)сечовини А, Б та дипропоксикалікс[4]аренкетоціаніни В: 20 H N Ph Ph H N X X NH OR HO HO HN HO OR O H N HO H N H N S O O O O HN O S O O O O , , Б X=O, S A 1 UA 83416 U O X R O OH Pr O , HO Pr X=H, CHO; R=OMe, NAlk2. B 5 Сполуки А, Б, отримані взаємодією відповідних каліксарендіамінів з ізо(тіо)ціанатами. Завдяки наявності карбамідних фрагментів на верхньому вінці макроциклу вони є селективними рецепторами бензилфосфонат-, дигідрофосфат-, хлорид-, ціанід- та ряду карбоксилат-аніонів [3]. Завдяки кооперативній дії зв'язуючих фрагментів на верхньому вінці макроциклу каліксаренкарбаміди А здатні утворювати стійкі комплекси з аніонами органічних кислот згідно нижченаведеної схеми: Ph Ph N H X H X O O N N H H CH3 N . 10 15 20 25 30 35 Каліксарени Б з фрагментами цукрів на верхньому вінці здатні до селективної взаємодії з білками Concanavalin А (Con А) та горіховим пектином (PNA) і специфічного зв'язування бензоат- та бензилфосфонат-іонів [4], які були зафіксовані методом ядерного магнітного резонансу. Разом з тим сполуки А, Б не містять хромо(флуоро)форних фрагментів, які б забезпечували відгук у спектрах флуоресценції на взаємодію рецептора з молекулами субстрату. Сполуки В, на відміну від А і Б містять на верхньому вінці макроциклу флуорофорний фрагмент на основі ариліденциклопентанону, чутливий до оточуючого середовища та здатний сигналізувати у видимому діапазоні про зв'язування різних за природою аналітів [5, 6]. Каліксаренкетоціаніни В виявляють дуже слабку сольватохромію та одночасно демонструють сильну позитивну сольватофлуорохромію. Однак, їх рецепторні можливості обмежені через відсутність координуючих груп, що забезпечували б утворення комплексів за принципом "гістьхазяїн" з біо- та хімічно важливими субстратами. Сполуки, які заявляються, 5-N-уреїдо-17-{(Е)-[(3Е)-3-(ариліден)-2оксоциклопентиліден]метил}-25,27-діалкокси-26,28-дигідроксикалікс[4]-арени 1 - відрізняються від тетрапропоксикалікс[4]арен(тіо)сечовин А, Б наявністю хромо(флуоро)фору на основі діариліденциклопентанону на верхньому вінці макроциклу, а від дипропоксикалікс[4]аренкетоціанінів В - наявністю карбамідних фрагментів. Тобто, ми маємо унікальний молекулярний контейнер з тривимірною порожниною, модифікованою аніонкоординуючими сечовинними групами та одночасно хромофорний фрагмент, надчутливий до оточуючого середовища. Завдяки такому унікальному поєднанню рецепторної та сигнальної частин, ковалентно зв'язаних в одній молекулі, каліксарени 1а, б є перспективними сполуками для створення нових високоспецифічних нанорозмірних молекулярних та аніонних хемосенсорів. Задачею корисної моделі є спосіб отримання 5-N-уреїдо-17-{(Е)-[(3Е)-3-(ариліден)-2оксоциклопентиліден]метил}-25,27-діалкокси-26,28-дигідроксикалікс[4]аренів 1 загальної формули: 2 UA 83416 U O O R R=Alk, Ar, SO2Ar, C(O)R, P(O)R2, R' O N H HN R'= N O , O O OH ALK 5 10 , , Alk=C3H7-C16H33. HO ALK , Спосіб отримання сполуки, яка заявляється, складається з трьох стадій, згідно наведеної нижче схеми. Взаємодією 5-нітро-17-форміл-26,28-дигідрокси-25,27-дипропоксикалікс[4]арену 2 [7] з (2Е)-2-(ариліден)циклопентаноном 3 в хлороформі в присутності іонної рідини диметиламонію диметилкарбамату (димкарб, англ. DIMCARB) як каталізатора та корозчинника [8, 9] при 20-60 °C отримуються 5-нітро-17-{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]метил}-26,28-дигідрокси-25,27-дипропоксикалікс[4]арени 4. Відновлення нітрокаліксаренів 4 гідразингідратом в присутності нікелю Ренея в метанолі дає відповідні амінопохідні 5, які без додаткового очищення при кімнатній температурі в етері реагують з ізоціанатом з утворенням цільових 5-N-уреїдо-17-{(E)-[(3E)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27-діалкокси26,28-дигідроксикалікс[4]аренів 1. O R' O2N CH=O O + DIMCARB R' O2N 45-50 C O O OH ALK HO ALK O 3 2 OH ALK O HO ALK 4 N2H4/NiRaney HN O R O R' O N H R' R O OH ALK O N O H2N HO ALK O 1 OH ALK O HO ALK 5 15 , R=Alk, Ar, SO2Ar, C(O)R, P(O)R2, O R'= N , O , , Alk=C3H7-C16H33. 20 Варто зазначити, що амінопохідні 5 не стійкі і легко окиснюються при спробі їх отримання в аналітично чистому вигляді. Тому одразу після відновлення їх перетворювали в кінцеві продукти 1 реакцією з ізоціанатом. 1 13 Індивідуальність та структура каліксаренів 1 та 4 доведені ІЧ-, H- та С-ЯМР спектрами, елементним аналізом, методом LCMS та рентгеноструктурним дослідженням (див. Фіг. 1, 2). 3 UA 83416 U 5 5 O 37 35 31 36 32 30 29 34 40 3 25 1 26 O 23 6 1 4 3 22 46 21 29 2 OH 28 15 25 26 O 23 47 14 48 22 46 21 8 15 20 25 30 35 40 2 8 9 O 13 OH 10 12 20 15 19 18 16 17 10 4 45 44 11 14 48 18 5 6 1 3 43 5 OH 27 24 11 7 1 N1 Me 4 45 10 12 20 19 40 3 9 O 13 39 34 6 44 8 38 41 33 2 43 5 OH 27 24 47 7 36 32 30 42 4 2 28 O Me 37 35 31 39 41 33 O 38 O N 16 17 O 7 7 O N 2 O 6 Схема 1. Нумерація атомів в молекулах 4 (R'=p-C6H4NMe2; Alk=n-Pr) та 4 (R'=p-C6H4OMe; Alk=n-Pr). Корисна модель ілюструється методами отримання і фізико-хімічними характеристиками всіх синтезованих сполук. Приклад 1 Спосіб одержання 5-нітро-17-{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]метил}-26,28дигідрокси-25,27-дипропоксикалікс[4]аренів 4. До розчину 290 мг (0,5 ммоля) нітроформілкаліксарену 2 в 3 мл хлороформу додають 1 мл (7,8 ммоля) DIMCARB та нагрівають до 45-50 °C (спостерігається виділення газу). Додають розчин 0,6 ммоля (2Е)-2-[4-диметиламіно(метокси)бензиліден]циклопентанону 3 в 3 мл хлороформу. Реакційну суміш перемішують при 45-50 °C впродовж 7 днів (хід реакції контролюють методом ТШХ). Після закінчення реакції розчинник упарюють, до залишку додають 12 мл хлороформу та 25 мл води. Органічний шар відокремлюють, промивають водою (3×20 мл) та насиченим розчином NaCl (2×20 мл), сушать над сульфатом натрію. Розчинник упарюють до об'єму 8-10 мл та додають 10-12 мл метанолу. Кристали, що утворились, очищують повторною кристалізацією з суміші хлороформ-метанол. 5-нітро-17-{(Е)-[(3Е)-3-(4-диметиламінобензиліден)-2-оксоциклопентиліден]метил}-26,28дигідрокси-25,27-дипропоксикалікс[4]арен 4а. 1 3 Вихід 87 %, Тпл. >300 °C (розкл.). Спектр ЯМР H (CDCl3) δ, м.ч.: 1,33 т (6Н, J H-H=7,3 Гц, ОСН2СН2СН3), 2,10 м (4Н, ОСН2СН2СН3), 3,04 с (6Н, N(CH3)2), 3,10 шир. с. (4Н, СН2СН2 2 циклопентанон), 3,46 та 3,49 два д, що перекриваються (4Н, J H-H=13,4, Ar-СН2-екв.), 4,02 м (4Н, 3 2 J H-H=6,3 Гц, ОСН2СН2СН3), 4,30 та 4,32 м 2 д, що перекриваються (4Н, J H-H=13,4, Ar-СН2-акс), 3 3 6,74 д (2Н, J H-H=8,7 Гц, ArН), 6,83 т (2Η, J H-H=7,75 Гц, ArН), 6,98 м (4Н, ArН), 7,36 с (2Н, ArН), 7,48 уш.с (1Н, -СН=), 7,52 та 7,55 два уш.с, що перекриваються (3Н, 2ArН+1-СН=), 8,04 с (2Н, 13 ArН), 8,73 та 9.52 два с (1Н кожен, ОН). Спектр ЯМР C (CDC13) , м.ч.: 195,72, 159.62, 151,55, 150,69, 134,88, 134,07, 132,99, 132,85, 132,81, 132,52, 131,60, 131,41, 129.50, 129.00, 128,40, 128,11, 125,60, 124,40, 112,10, 111,81, 78,62, 40,19, 31,62, 31,42, 26,79, 23,60, 11,05, LC-MS: + m/z=779.4 [М] . Обчислено, %: С 75,56; Η 6,47; Ν 3,60, C 49H50N2O7. Знайдено, %: С 77,32; Η 6,54; Ν 3,48. РСА: Кристали 4а моноклинні, C49H50N2O7·СНСl3, при -173 °C а=22,138(1), b=10,5509(5), 3 с=19.520(1) Å, =104,794(5)°, V=4408,3(4) Å , Мr=898,28, Ζ=4, просторова група P21/c, dобч=1,353 3 -1 г/см , (ΜοΚ)=0,264 мм , F(000)=1888. Параметри елементарної комірки та інтенсивності 33690 відбиттів (12849 незалежних, Rint=0,085) виміряні на дифрактометрі "Xcalibur-3" (ΜοΚ випромінення, CCD-детектор, графітовий монохроматор, -сканування, 2макс= 60°). Структура розшифрована прямим методом по комплексу програм SHELXTL [10]. Положення атомів Гідрогену виявлені з різницевого синтезу електронної густини та уточнені по моделі "вершника" з Uізо=nUeкв (n=1,5 для метильних груп и n=1,2 для інших атомів Гідрогену). Атоми Гідрогену, що приймають участь в утворенні водневих зв'язків О-Н…О, уточнені в ізотропному 2 наближенні. Структура уточнена по F повноматричними МНК в анізотропному наближенні для 4 Me 43 42 UA 83416 U 5 10 15 20 25 30 35 40 45 50 55 60 неводневих атомов до wR2=0,173 по 12811 відбиттям (R1=0,074 по 6897 відбиттям с F>4(F), S=0,987). 5-нітро-17-{(Е)-[(3Е)-3-(4-метоксибензиліден)-2-оксоциклопентиліден]метил}-26,28дигідрокси-25,27-дипропоксикалікс[4]арен 4б. 1 3 Вихід 69 %, Тпл. 303-306 °C. Спектр ЯМР H (CDCl3) , м.ч.: 1,32 т (6Η, J H-H=7,3 Гц, ОСН2СН2СН3), 2,08 м (4Н, ОСН2СН2СН3), 3,08 шир. с. (4Н, СН2СН2 циклопентанон), 3,47 та 3,50 2 3 2 д, що перекриваються (4Н, J H-H=13,2, Ar-СН2-екв.), 3,84 с (3Н, ОСН 3), 3,99 м (4Н, J H-H=6,3 Гц, 2 3 ОСН2СН2СН3), 4,31 та 4,32 м 2 д, що перекриваються (4Н, J H-H=13,2, Ar-СН2-акс), 6,83 т (2Н, J HH=7,6 Гц, ArH), 6,98 м (6Н, ArН), 7,37 с (2Н, ArН), 7,52 уш.с (1Н, -СН=), 7,55 уш.с та 7,57 д, що 3 перекриваються (3Н, 1-СН= + 2ArH, J H-H=7,6 Гц), 8,04 с (2Н, ArН), 8,79 та 9.52 два с (1Н кожен, 13 ОН). Спектр ЯМР C(CDCl3) , м.ч.: 195,78, 160,23, 159.58, 154,86, 151,54, 139.54, 135,32, 134,17, 133,81, 132,91, 132,76, 132,26, 131,61, 131,54, 129.44, 129.01, 128,73, 128,37, 128,19, 127,29, 125,57, 124,37, 114,17, 78,61, 55,38, 31,60, 31,40, 26,73, 26,64, 23,58, 11,03, LC-MS: + m/z=766,4 [M] . Обчислено, %: С 75,27; Η 6,19; Ν 1,83, C48H47NO8. Знайдено, %: С 76,02; Η 6,24; Ν 1,88. РСА: Кристали 4б моноклинні, C48H47NO8·0,5СН3ОН·Н2О, при -173 °C а=42,215(4), 3 b=10,2820(7), с=20,249(2) Å, =99,321(9)°, V=8673(1) Å , Мr=817,92, Ζ=4, просторова група С2/с, 3 -1 dобч=1,253 г/см , (ΜοΚ)=0,088 мм , F(000)=3480, Параметри елементарної комірки та інтенсивності 27822 відбиттів (7618 незалежних, Rint=0,125) виміряні на дифрактометрі "Xcalibur3" (ΜοΚ випромінення, CCD-детектор, графітовий монохроматор, -сканування, 2макс=50°). Структура розшифрована прямим методом по комплексу програм SHELXTL [10]. При уточненні структури застосовувались обмеження на довжину зв'язку С-O в сольватній молекулі метанолу (1,41 Å). Положення атомів Гідрогену виявлені з різницевого синтезу електронної густини та уточнені по моделі "вершника" з Uізо=nUeкв (n=1,5 для метильних груп и n=1,2 для інших атомів Гідрогену). Атоми Гідрогену, що приймають участь в утворенні водневих зв'язків ОН…О, уточнені в ізотропному наближенні. 2 Структура уточнена по F повноматричними МНК в анізотропному наближенні для неводневих атомов до wR2=0,210 по 7579 відбиттям (R1=0,080 по 3463 відбиттям с F>4(F), S=0,927). Приклад 2 Спосіб одержання 5-N-(2-метоксіетил)-N'-уреїдо-17-{(Е)-[(3Е)-3-(4-ариліден)-2оксоциклопентиліден]метил}-25,27-дипропокси-26,28-дигідроксикалікс[4]аренів 1. До суспензії 0,5 ммоля нітрокаліксарену 4 в 20 мл метанолу додають 1,5 мл 100 %-го гідразингідрату (30 ммоль). Реакційну суміш нагрівають до 70 °C і додають 0,1 мл 50 %-ї водної суспензії нікелю Ренея. Перемішують при 70 °C впродовж 5 годин. Охолоджують до кімнатної температури, додають 15 мл хлороформу, відфільтровують через фільтр Шота з силікагелем. Фільтрат випарюють досуха. Отримують амінокаліксарени 5 у вигляді лимонно-жовтого порошку. До розчину 0,4 ммоля амінокаліксарену 5 в 10 мл хлороформу додають 0,4 ммоля 2метоксіетилізоціанату в 2 мл хлороформу. Реакційну суміш перемішують при кімнатній температурі 12 годин. Розчинник упарюють, залишок - речовину 1 - очищують колонковою хроматографією (елюент-етилацетат). 5-N-(2-метоксіетил)-N'-уреїдо-17-{(Е)-[(3Е)-3-(4-диметиламінобензиліден)-2оксоциклопентиліден]метил}-25,27-дипропокси-26,28-дигідроксикалікс[4]аренів 1а. 1 3 Вихід 68 %, Тпл. >320 °C (розкл.). Спектр ЯМР H (CDCl3) , м.ч.: 1,32 т (6Н, J H-H=7,3 Гц, ОСН2СН2СН3), 2,08 м (4Н, ОСН2СН2СН3), 3,04 с (6Н, N(CH3)2), 3,09 шир. с. (4Н, СН2СН2 циклопентанон), 3,32 с (3Н, ОСН3), 3,38 та 3,43 два м, що перекриваються (8Н, СН2СН2 + Ar3 СН2-екв.), 3,99 т (4Η, J H-H=6,1 Гц, ОСН2СН2СН3), 4,31 та 4,32 м два д, що перекриваються (4Н, 2 3 3 J H-H=12,5, Ar-СН2-акс), 4,95 т (1Н, J H-H=5,4 Гц, NH), 6,14 с (1Н, NH), 6,73 д (2Н, J H-H=8,8 Гц, 3 ArН), 6,78 т (2Н, J H-H=7,6 Гц, ArН), 6,95 м (6Н, ArН), 7,35 с (2Н, ArН), 7,47 уш.с (1Н, -СН=), 7,52 уш.с та 7,54 д, що перекриваються (3Н, 1-СН= + 2ArН), 8,40 та 8,86 два с (1Н кожен, ОН). 13 Спектр ЯМР С (CDCl3) , м.ч.: 195,98, 156,84, 154,92, 151,77, 134,78, 134,10, 133,12, 132,97, 132,59, 131,50, 129.02, 128,93, 128,60, 128,42, 127,47, 125,45, 124,48, 111,85, 78,48, 71,95, 58,72, + 40,15, 31,59, 31,36, 30,96, 26,71, 23,52, 10,97, LC-MS: m/z=852,5 [M+H] . Обчислено, %: С 74,89; Η 7,00; Ν 4,94, C53H59N3O7. Знайдено, %: С 75,02; Η 6,94; Ν 4,88. 5-N-(2-мeтoкcіeтил)-N'-ypeїдo-17-{(E)-[(3E)-3-(4-мeтoкcибeнзилiдeн)-2оксоциклопентиліден]метил}-25,27-дипропокси-26,28-дигідроксикалікс[4]аренів 1б. 1 3 Вихід 88 %, Тпл. >260 °C (розкл.). Спектр ЯМР H (CDCl3) , м.ч.: 1,32 т (6Н, J H-H=7.3 Гц, ОСН2СН2СН3), 2,07 м (4Н, ОСН2СН2СН3), 3,11 шир. с. (4Н, СН2СН2 циклопентанон), 3,31 с (3Н, ОСН3), 3,36 та 3,42 два м, що перекриваються (8Н, СН2СН2 + Ar-СН2-екв.), 3,84 с (3Н, ОСН3), 5 UA 83416 U 3 5 10 15 20 25 30 2 3,99 т (4Η, J H-H=6-1 Гц, ОСН2СН2СН3), 4,29 та 4,32 м два д, що перекриваються (4Н, J H-H=13,2, 3 3 Ar-СН2-акс), 5,07 т (1Η, J H-H=5,5 Гц, NHCH2), 6,36 с (1Н, ArNH), 6,76 т (2H, J H-H=7,5 Гц, ArН), 6,95 м (8Н, ArН), 7,36 с (2Н, ArН), 7,52 уш.с (1Н, -СН=), 7,54 уш.с та 7,56 д, що перекриваються (3Н, 13 1-СН= + 2ArН), 8,36 та 8,91 два с (1Н кожен, ОН). Спектр ЯМР C (CDCl3) , м.ч.: 196,10, 160,34, 155,23, 151,76, 150,92, 135,47, 134,16, 134,07, 133,15, 132,86, 132,36, 131,67, 129,07, 128,94, 128,84, 128,81, 128,76, 128,52, 127,19, 125,43, 124,17, 114,23, 78,47, 71,97, 58,70, 55,37, 40,12, -1 31,58, 31,37, 26,64, 23,51, 10,96. ІЧ спектр (KBr, см ): ΝΗ=3260-3420, OH=2940, C=O=1655, 1595. Обчислено, %: С 74,62; Η 6,74; Ν 3,35. C52H56N2O8. Знайдено, %: С 75,08; Η 6,84; Ν 3,38. Джерела інформації: 1. Gale P.A. Anionand ion-pair receptor chemistry: highlights from 2000 and 2001 // Coord. Chem. Rev. - 2003. - Vol. 240, - P. 191-221. 2. Beer P.D., Gale P.A. Anion Recognition and Sensing: The State of the Art and Future Perspectives // Angew. Chem. Int. Ed.-2001. - Vol. 40, - P. 486-516. 3. Casnati A., Fochi M., Minari P., Pochini A., Reggiani M., Ungano R., Reinhoudt D.N. Upper-Rim Urea-Derivatized Calix[4]arenes as neutral Receptors for Monocarboxylate Anions. // Gazz. Chim. Ital. - 1996. - Vol. 126. - P. 99-106. 4. Sansone F., Chierici E., Casnati Α., Ungano R. Thiourea-linked upper rim calix[4]arene neoglycoconjugates: synthesis, conformations and binding properties. // Org. Biomol. Chem. - 2003. Vol.1. - P. 1802-1809. 5. Матвєєв Ю.І., Карпенко Ю.А., Кулінич А.В., Пивоваренко B.F., Кальченко Β.Θ. Спосіб одержання 5-форміл-17-{(Е)-[(3Е)-3-(4-метоксибензиліден)-2-оксоциклопентиліден]метил}-25,27дипропокси-26,28-дигідроксикалікс[4]арена. //Пат. Укр. № 57677, Бюл. № 5 від 10,03.2011. 6. Matvieiev Yu., Karpenko Iu., Kulinich Α., Ryabitskii Α., Pivovarenko V., Shishkina S., Shishkin O., Kalchenko V. Synthesis of Calixarene-Based Ketocyanine Fluorophores. // Tetrahedron Letters. 2011. - #52. - P. 3922-3925. 7. Arimura Т., Ide S., Nishioka Т., Sugihara H., Murata S., Yamato T. Synthesis of 5-formyl-17nitrocalix[4]arenes in the 1,3-alternate conformation // J. Chem. Research (S) - 2000, - P. 234-236. 8. Kreher, U.P.; Rosamilia, A.E.; Raston, C.L.; Scott, J.L. and Strauss, C.R. Direct Preparation of Monoarylidene Derivatives of Aldehydes and Enolizable Ketones with DIMCARB. // Org. Lett. - 2003 V.5. - P. 3107-3110, 9. Sridhar, G; Gunasundari, T. and Raghunathan, R. A greener approach for the synthesis of 1-Nmethyl-(spiro[2.3']oxindolespiro[3.2"]/spiro-[2.3']indan-1,3-dionespiro[2.2"]-cyclopentanone-4-aryl pyrrolidines. // Tetrahedron Lett. - 2007 - V. 48. - P. 319-322. 10. Sheldrick G.M. // Acta Crystallogr., Sect. A, 2008, A64, p. 112-122. 35 ФОРМУЛА КОРИСНОЇ МОДЕЛІ Спосіб одержання 5-N-уреїдо-17-{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27діалкокси-26,28-дигідроксикалікс[4]аренів загальної формули: 40 O O HN R R=Alk, Ar, SO2Ar, C(O)R, P(O)R2 O R' N H R'= N , O , Alk=C3H7-C16H33, O OH ALK 45 O HO ALK , який відрізняється тим, що 5-нітро-17-форміл-25,27-дипропокси-26,28-дигідроксикалікс[4]арен конденсують з (2Е)-2-(ариліден)циклопентаноном в присутності диметиламонію диметилкарбамату (DIMCARB) в хлороформі при нагріванні в межах 20-60 °C з утворенням 5нітро-17-{(Е)-[(3Е)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27-діалкокси-26,28дигідроксикалікс[4]аренів, відновлення яких гідразингідратом в присутності нікелю Ренея дає відповідні амінопохідні, які взаємодією з ізоціанатом при кімнатній температурі в етері перетворюються в цільові продукти, які виділяють звичайними методами. 6 , UA 83416 U Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 7
ДивитисяДодаткова інформація
Автори англійськоюMatvieev Yurii Ivanovych, Shyshkina Svitlana Valentynivna, Shyshkin Oleh Valeriiovych, Pyvovarenko Vasyl Heorhiiovych, Kalchenko Vitalii Ivanovych
Автори російськоюМатвеев Юрий Иванович, Шишкина Светлана Валентиновна, Шишкин Олег Валерьевич, Пивоваренко Василий Георгиевич, Кальченко Виталий Иванович
МПК / Мітки
МПК: C07C 37/00, C07C 47/52, C07C 39/12, C09B 23/00
Мітки: спосіб, одержання, 5-n-уреїдо-17-{(е)-[(3e)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27-діалкокси-26,28-дигідроксикалікс[4]аренів
Код посилання
<a href="https://ua.patents.su/9-83416-sposib-oderzhannya-5-n-uredo-17-e-3e-3-ariliden-2-oksociklopentilidenmetil-2527-dialkoksi-2628-digidroksikaliks4areniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 5-n-уреїдо-17-{(е)-[(3e)-3-(ариліден)-2-оксоциклопентиліден]метил}-25,27-діалкокси-26,28-дигідроксикалікс[4]аренів</a>
Попередній патент: Клеєний брус
Наступний патент: Прилад для визначення пружних деформацій плодів баштанних культур
Випадковий патент: Високоефективне стабілізоване силове джерело електроживлення дрьомова