Спосіб одержання екстракту з листя плюща, екстракт, його застосування та лікарський засіб
Номер патенту: 87114
Опубліковано: 25.06.2009
Автори: Шнайдер Вольфганг, Шмідт Олівер, Енгельхард Георг Максіміліан, Рункель Франк
Формула / Реферат
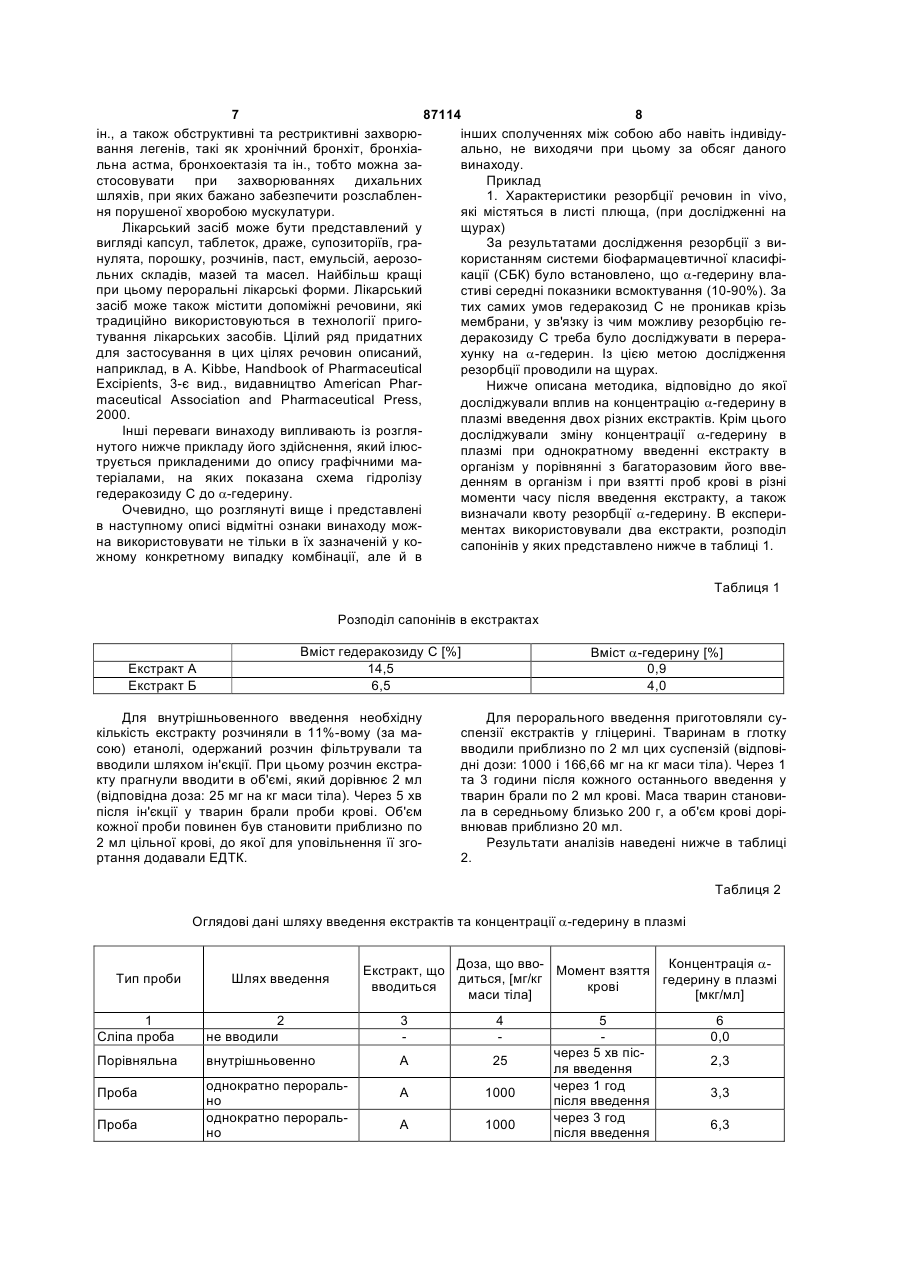
1. Спосіб одержання з листя плюща екстракту, який містить діючі речовини гедеракозид С та ![]() -гедерин, який полягає в тому, що
-гедерин, який полягає в тому, що
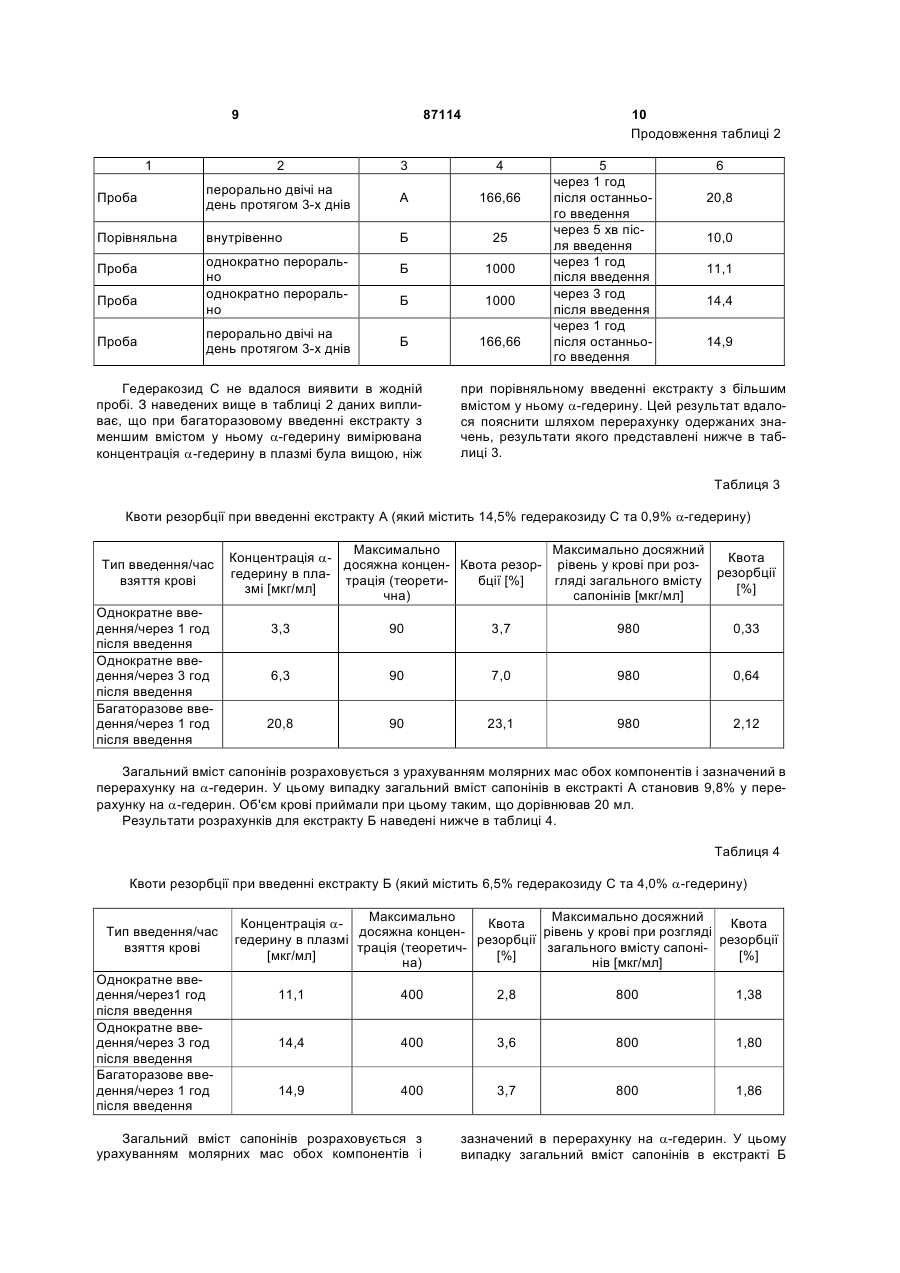
а) підготовляють перший, збагачений ![]() -гедерином екстракт, який містить принаймні 3 %
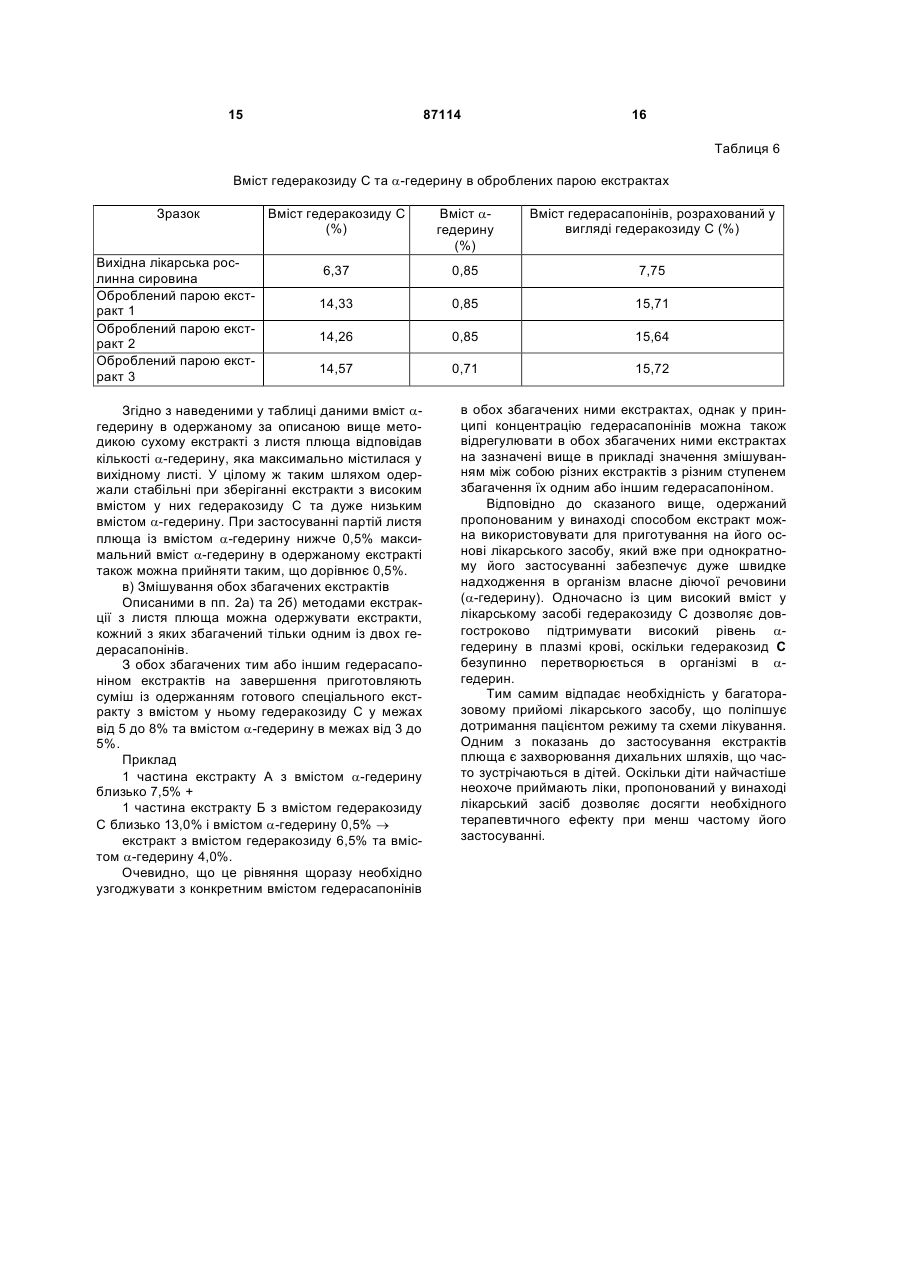
-гедерином екстракт, який містить принаймні 3 % ![]() -гедерину, причому перед екстракцією рослинної сировини здійснюють принаймні часткове ферментативне перетворення гедеракозиду С, що міститься у ній, на
-гедерину, причому перед екстракцією рослинної сировини здійснюють принаймні часткове ферментативне перетворення гедеракозиду С, що міститься у ній, на ![]() -гедерин,
-гедерин,
б) підготовляють другий, збагачений гедеракозидом С екстракт, який містить принаймні 5 % гедеракозиду С, причому перед екстракцією рослинну сировину обробляють гарячою водяною парою, та
в) перший та другий екстракти змішують між собою з одержанням екстракту з відрегульованим вмістом у ньому гедеракозиду С та відрегульованим вмістом ![]() -гедерину.
-гедерину.
2. Спосіб за п. 1, який відрізняється тим, що вміст ![]() -гедерину в збагаченому ним екстракті становить принаймні 5 %.
-гедерину в збагаченому ним екстракті становить принаймні 5 %.
3. Спосіб за п. 1 або 2, який відрізняється тим, що вміст гедеракозиду С у збагаченому ним екстракті становить принаймні 10 %, а вміст ![]() -гедерину становить менше 2 %.
-гедерину становить менше 2 %.
4. Спосіб за будь-яким з пп. 1-3, який відрізняється тим, що відрегульований вміст гедеракозиду С в одержуваному на стадії в) екстракті становить від приблизно 3 до приблизно 10 %, а вміст ![]() -гедерину - від приблизно 1 до приблизно 7 %.
-гедерину - від приблизно 1 до приблизно 7 %.
5. Спосіб за будь-яким з пп. 1-4, який відрізняється тим, що відрегульований вміст гедеракозиду С в одержуваному на стадії в) екстракті становить близько 6,5 %, а відрегульований вміст ![]() -гедерину - близько 4,0 %.
-гедерину - близько 4,0 %.
6. Екстракт, одержаний способом за будь-яким з пп. 1-5.
7. Екстракт за п. 6, який відрізняється тим, що вміст у ньому гедеракозиду С становить принаймні 4 %, а вміст ![]() -гедерину становить принаймні 2 %.
-гедерину становить принаймні 2 %.
8. Екстракт за п. 6 або 7, який відрізняється тим, що вміст у ньому гедеракозиду С становить 6,5 %, а вміст ![]() -гедерину - 4,0 %.
-гедерину - 4,0 %.
9. Застосування екстракту за будь-яким з пп. 6-8 для одержання лікарського засобу.
10. Застосування за п. 9, яке відрізняється тим, що лікарський засіб призначений для лікування захворювань дихальних шляхів.
11. Лікарський засіб, який містить екстракт за будь-яким з пп. 6-8.
Текст
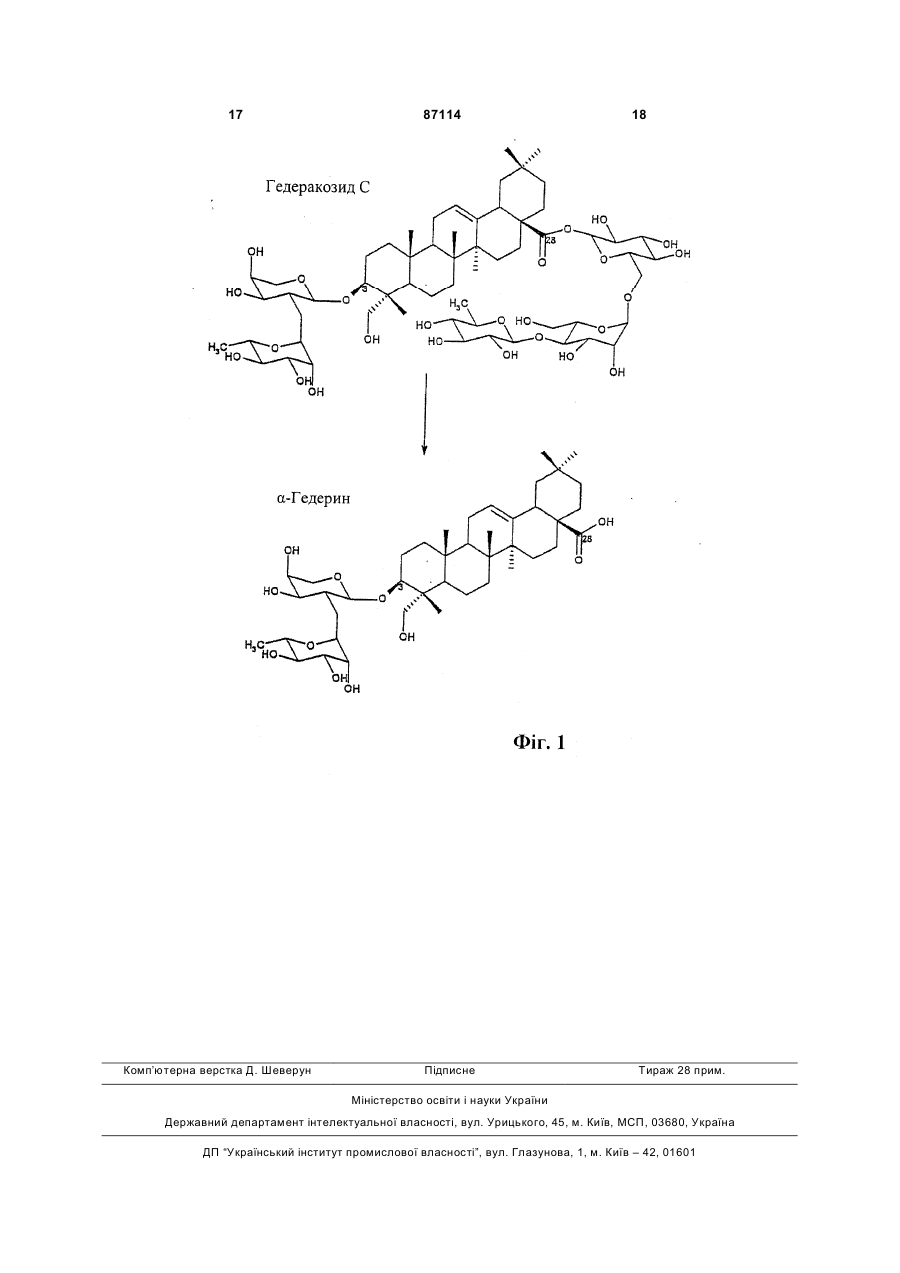
1. Спосіб одержання з листя плюща екстракту, який містить діючі речовини гедеракозид С та a гедерин, який полягає в тому, що а) підготовляють перший, збагачений aгедерином екстракт, який містить принаймні 3 % a -гедерину, причому перед екстракцією рослинної сировини здійснюють принаймні часткове ферментативне перетворення гедеракозиду С, що міститься у ній, на a -гедерин, б) підготовляють другий, збагачений гедеракозидом С екстракт, який містить принаймні 5 % гедеракозиду С, причому перед екстракцією рослинну сировину обробляють гарячою водяною парою, та C2 2 (19) 1 3 87114 4 листя плюща обумовлено головним чином вмістом терапевтичної дії доцільно мати екстракти з плюу таких екстрактах терапевтично важливих компоща із вмістом в них діючих речовин, яка задається. нентів, які відносяться до класу тритерпенових Недолік екстрактів, які застосовувалися дотесапонінів. Основними сапонінами при цьому є біспер, полягає далі в необхідності їх багаторазового введення в організм для забезпечення негайної й десмозидний гедеракозид C та a-гедерин, який довготривалої спазмолітичної дії на бронхи, яка утворюється з нього в результаті гідролізу складвикликається a-гедерином. Можлива причина цьоного ефіру. Іншим сапоніном, який можна виявити в екстрактах з листя плюща, є гедерагенін. го полягає в недостатній біодоступності aЕкстракти з листя плюща, які одержані різними гедерину, оскільки, наприклад, вже до моменту методами, часто мають з цієї причини ефективприйому екстрактів у них міститься мало aність, яка відрізняється між собою. Подібні розхогедерину. З іншого боку, і спочатку присутній в дження обумовлені тим, що вміст тих або інших екстракті a-гедерин порівняно швидко резорбуєтькомпонентів в екстракті залежить не тільки від ся in vivo, через що для досягнення терапевтичної природного складу вихідної сировини, але й від дії існує необхідність багаторазового введення в конкретного методу одержання екстракту. організм екстрактів, які його містять. За результатами останніх досліджень було Виходячи з вищесказаного, в основу даного встановлено, що a-гедерин являє собою власне винаходу була покладена задача розробити спосіб активну речовину, яка міститься в листі плюща, і одержання екстракту, а також запропонувати екстсприяє спазмолітичній дії на бронхи (бронхоспазракт, який забезпечував би швидку біодоступність молізу), оскільки ця речовина в результаті зв'язуa-гедерину та її збереження на незмінному рівні вання з b-адренорецепторами і тим самим запуску протягом більш тривалого періоду часу. відповідних каскадів викликає розслаблення гладПокладена в основу винаходу задача вирішукої мускулатури бронхіальної системи. ється за допомогою способу одержання екстракту Екстракти з рослинних матеріалів, насамперед з листя плюща з регульованим вмістом в екстракті сухі екстракти, а також різноманітні методи одергедеракозиду C та a-гедерину, який полягає в тожання таких екстрактів широко представлені в му, що літературі, яка присвячена фармації та насампеа) підготовляють перший, збагачений aред приготуванню лікарських засобів. гедерином екстракт, Один зі способів одержання сухих екстрактів з б) підготовляють другий, збагачений гедеракорослинних матеріалів відомий, наприклад, із заявзидом C екстракт та ки DE 10112168 Al. Описаний у цій заявці спосіб в) перший та другий екстракти змішують між повинен забезпечувати можливість регулювання собою з одержанням екстракту з відрегульованим вмісту в екстракті ліпофільних та гідрофільних вмістом у ньому гедеракозиду C та відрегульоваречовин. Для цього рослинний матеріал пропонуним вмістом a-гедерину. ється піддавати принаймні двом екстракційним Пропонований у винаході спосіб дозволяє обробкам розчинниками, які мають різну ліпофільодержувати екстракт, який містить, по-перше, aність, і окремо виділяти з них екстракти. Одержані гедерин як біологічно активну речовину з швидко екстракти сушать окремо один від одного й потім наступаючою дією та, по-друге, гедеракозид С, змішують між собою в необхідній пропорції. Таким який in vivo перетворюється в a-гедерин. При цьошляхом можна регулювати вміст в екстракті ліпому перший екстракт значно збагачений aфільних та гідрофільних речовин. Такий спосіб в гедерином, а другий екстракт - гедеракозидом C. принципі повинен бути придатний і для одержання Перший екстракт можна одержувати, наприсухих екстрактів із плюща (Hedera helix). Однак у клад, способом, при здійсненні якого вихідний мазазначеній публікації не описаний ні екстракт з теріал, наприклад, висушену лікарську рослинну цілеспрямовано відрегульованим у ньому вмістом сировину, спочатку подрібнюють, потім піддають a-гедерину і/або гедеракозиду С, ні спосіб, яким ферментації і після цього піддають попередньому можна було б одержувати подібний екстракт. набуханню, наприклад, у суміші спирту з водою, Крім цього із заявки DE 3025223 A1 відома зокрема у 30%-вому етанолі, та екстракційній обфармацевтична композиція на основі екстрактів робці. На завершення екстракт можна піддавати, плюща та спосіб їх одержання, при цьому до скланаприклад, випарюванню в плівковому випарному ду фармацевтичної композиції входить як діюча апараті та розпилювальному сушінню. Залежно від речовина екстракт, який містить 90% або 60% генеобхідного вмісту a-гедерину в екстракті фермедерасапоніну C або a-гедерин. Подібний екстракт нтації можна піддавати всю кількість висушеної одержують із застосуванням ацетону та метанолу. лікарської рослинної сировини й таким шляхом Для перетворення гедерасапоніну С, відповідно перетворювати весь присутній у ньому гедеракогедеракозиду C в a-гедерин і одержання тим сазид C в a-гедерин. В іншому варіанті ферментації мим екстракту, який містить тільки a-гедерин, 90%можна також піддавати тільки частину лікарської ий екстракт відповідно до зазначеної заявки підрослинної сировини, а іншу його частину домішудають омиленню гідроксидом натрію або гідроксивати тільки для попереднього набухання в етанолі, дом калію. одержуючи таким чином екстракт, який лише знаОднак і в цій публікації не описаний спосіб, чно збагачений a-гедерином. яким можна було б одержувати екстракт з відрегуПід "ферментацією" згідно із даним винаходом льованим на будь-яку величину вмістом у ньому aмається на увазі розкладання, відповідно перегедерину та гедеракозиду С. творення присутніх у вихідному матеріалі компоРазом з тим для забезпечення відтворюваної нентів в інші речовини при додаванні до вихідного 5 87114 6 матеріалу ферментаційного середовища, напривід приблизно 3 до приблизно 10%, насамперед, клад, води, з узгодженням при необхідності певних який становить приблизно 6,5%, та вмістом aпараметрів, наприклад, часу та температури, з гедерину, який становить від приблизно 1 до приособливостями процесу ферментації. Така нова близно 7%), насамперед, який становить приблизстадія ферментації надає можливість цілеспрямоно 4,0%. ваного одержання збагачених a-гедерином екстПеревага пропонованого у винаході екстракту рактів. завдяки відрегульованому вмісту в ньому обох Листя плюща можна при цьому використовувищевказаних діючих речовин полягає в тому, що вати, наприклад, у вигляді висушеної лікарської діюча речовина a-гедерин після введення екстракрослинної сировини. Перевага, пов'язана із застоту, у якому він спочатку присутній як такий, почисуванням при приготуванні лікарського засобу винає швидко надходити в організм. Поряд із цим сушеної лікарської рослинної сировини, полягає гедеракозид С, який міститься в екстракті окрім aзавдяки кращій її здатності до зберігання в більшій гедерину, резорбується in vivo із затримкою в часі, за певних умов зручності роботи з ним, ніж зі свівідповідно поступово перетворюється в a-гедерин, жозібраними лікарськими рослинами. Сказане, і тому після витрачання всього спочатку присутоднак, не виключає можливості застосування при нього в екстракті a-гедерину в організм продовжує одержанні пропонованого у винаході екстракту надходити перетворений з гедеракозиду C aсвіжого листя плюща. гедерин. Пов'язана із цим перевага полягає в збіВисушені лікарські рослини та їх частини нальшенні тривалості терапевтичної дії екстракту, зивають у фармації лікарською рослинною сировідповідно лікарського засобу, що його містить. виною. Подібні, представлені у вигляді лікарської Цей ефект був підтверджений експериментарослинної сировини лікарські рослини застосовульно. У цьому відношенні вдалося встановити, що ють або в незмінному, або в подрібненому вигляді. при застосуванні пропонованого у винаході екстДругий екстракт можна одержувати, наприракту, вміст у якому обох діючих речовин aклад, способом, при здійсненні якого висушену гедерину та гедеракозиду C - було відрегульовано лікарську рослинну сировину відразу ж після її на значення, яке перебуває в зазначеному вище подрібнювання змішують із екстрагентом, наприоптимальному інтервалі, концентрація a-гедерину клад, 30%-вим етанолом, і піддають екстракційній в плазмі крові швидко наростала та зберігалася на обробці традиційними методами. В іншому варіанпостійному рівні. Порівняльний же екстракт із ті подрібнену лікарську рослинну сировину можна більш високим вмістом гедеракозиду C і більш перед екстракційною обробкою етанолом обробнизьким вмістом a-гедерину на відміну від прополяти гарячою водяною парою. За результатами нованого у винаході екстракту для досягнення попроведених експериментів було встановлено, що рівнянних з ним значень концентрації a-гедерину в подібна обробка дозволяє підвищити в екстракті плазмі крові було потрібно вводити в організм знавміст гедеракозиду С, відповідно стабілізувати чно частіше. Відповідно до цього застосування його вміст щодо вихідного вмісту в лікарській роспропонованого у винаході нового екстракту дозволинній сировині та понизити вміст a-гедерину. Таляє вже після однократного його введення в оргаким шляхом одержують екстракти, які можна виконізм досягти такої концентрації a-гедерину в плазристовувати на стадії б) пропонованого у винаході мі крові, якої досить для забезпечення і тривалого способу як другого, збагаченого гедеракозидом C збереження спазмолітичної дії на бронхи. екстракту. Така нова стадія обробки парою надає При цьому найбільш краще застосовувати можливість цілеспрямованого одержання збагачеодержаний пропонованим у винаході способом них гедеракозидом C екстрактів. екстракт з вмістом гедеракозиду C близько 6,5% і На стадії а) пропонованого у винаході способу вмістом a-гедерину близько 4,0%і. найбільш краще використовувати збагачений aДаний винахід відноситься далі до застосугедерином екстракт з вмістом a-гедерину принайвання пропонованого в ньому екстракту для одермні 3%, насамперед 5%. жання лікарського засобу, призначеного насампеНа стадії б) пропонованого у винаході способу ред для лікування захворювань дихальних шляхів, краще далі використовувати збагачений гедеракоа також до лікарського засобу, який містить пропозидом C екстракт з вмістом гедеракозиду C принований у винаході екстракт. наймні 5%, насамперед принаймні 10%, та вмістом Пропоновані у винаході екстракти з відрегуa-гедерину менше 2%. льованим вмістом у них гедеракозиду C і aПри цьому на стадії в) пропонованого у винагедерину найбільш кращі для застосування як ліході способу краще одержувати екстракт з вмістом карські засоби, завдяки можливості досягнення з їх гедеракозиду С, який становить від приблизно 3 допомогою відтворюваної терапевтичної дії, а тадо приблизно 10%, насамперед, який становить кож завдяки негайному первинному, а потім поприблизно 6,5%, та вмістом a-гедерину, який стастійному, що зберігається протягом більш тривановить від приблизно 1 до приблизно 7%, насамлого періоду часу, надходженню в організм aперед, який становить приблизно 4,0%. гедерину, який являє собою біологічно активну Покладена в основу винаходу задача вирішуречовину, що має спазмолітичну дію. ється також за допомогою екстракту, одержаного Відповідно до цього пропонований у винаході пропонованим у винаході способом. Покладена в лікарський засіб можна використовувати для лікуоснову винаходу задача вирішується насамперед вання захворювань дихальних шляхів, таких як за допомогою одержаного пропонованим у винаінфекційно-запальні захворювання дихальних ході способом екстракту з листя плюща з відрегушляхів, наприклад, пневмонія, трахеїт, бронхіт та льованим вмістом гедеракозиду С, який становить 7 87114 8 ін., а також обструктивні та рестриктивні захворюінших сполученнях між собою або навіть індивідування легенів, такі як хронічний бронхіт, бронхіаально, не виходячи при цьому за обсяг даного льна астма, бронхоектазія та ін., тобто можна завинаходу. стосовувати при захворюваннях дихальних Приклад шляхів, при яких бажано забезпечити розслаблен1. Характеристики резорбції речовин in vivo, ня порушеної хворобою мускулатури. які містяться в листі плюща, (при дослідженні на Лікарський засіб може бути представлений у щурах) вигляді капсул, таблеток, драже, супозиторіїв, граЗа результатами дослідження резорбції з винулята, порошку, розчинів, паст, емульсій, аерозокористанням системи біофармацевтичної класифільних складів, мазей та масел. Найбільш кращі кації (СБК) було встановлено, що a-гедерину влапри цьому пероральні лікарські форми. Лікарський стиві середні показники всмоктування (10-90%). За засіб може також містити допоміжні речовини, які тих самих умов гедеракозид C не проникав крізь традиційно використовуються в технології пригомембрани, у зв'язку із чим можливу резорбцію гетування лікарських засобів. Цілий ряд придатних деракозиду C треба було досліджувати в перерадля застосування в цих цілях речовин описаний, хунку на a-гедерин. Із цією метою дослідження наприклад, в A. Kibbe, Handbook of Pharmaceutical резорбції проводили на щурах. Excipients, 3-є вид., видавництво American PharНижче описана методика, відповідно до якої maceutical Association and Pharmaceutical Press, досліджували вплив на концентрацію a-гедерину в 2000. плазмі введення двох різних екстрактів. Крім цього Інші переваги винаходу випливають із розглядосліджували зміну концентрації a-гедерину в нутого нижче прикладу його здійснення, який ілюсплазмі при однократному введенні екстракту в трується прикладеними до опису графічними маорганізм у порівнянні з багаторазовим його вветеріалами, на яких показана схема гідролізу денням в організм і при взятті проб крові в різні гедеракозиду C до a-гедерину. моменти часу після введення екстракту, а також Очевидно, що розглянуті вище і представлені визначали квоту резорбції a-гедерину. В експерив наступному описі відмітні ознаки винаходу можментах використовували два екстракти, розподіл на використовувати не тільки в їх зазначеній у косапонінів у яких представлено нижче в таблиці 1. жному конкретному випадку комбінації, але й в Таблиця 1 Розподіл сапонінів в екстрактах Вміст a-гедерину [%] 0,9 4,0 Вміст гедеракозиду C [%] 14,5 6,5 Екстракт А Екстракт Б Для внутрішньовенного введення необхідну кількість екстракту розчиняли в 11%-вому (за масою) етанолі, одержаний розчин фільтрували та вводили шляхом ін'єкції. При цьому розчин екстракту прагнули вводити в об'ємі, який дорівнює 2 мл (відповідна доза: 25 мг на кг маси тіла). Через 5 хв після ін'єкції у тварин брали проби крові. Об'єм кожної проби повинен був становити приблизно по 2 мл цільної крові, до якої для уповільнення її згортання додавали ЕДТК. Для перорального введення приготовляли суспензії екстрактів у гліцерині. Тваринам в глотку вводили приблизно по 2 мл цих суспензій (відповідні дози: 1000 і 166,66 мг на кг маси тіла). Через 1 та 3 години після кожного останнього введення у тварин брали по 2 мл крові. Маса тварин становила в середньому близько 200 г, а об'єм крові дорівнював приблизно 20 мл. Результати аналізів наведені нижче в таблиці 2. Таблиця 2 Оглядові дані шляху введення екстрактів та концентрації a-гедерину в плазмі Тип проби Шлях введення Доза, що ввоКонцентрація aЕкстракт, що Момент взяття диться, [мг/кг гедерину в плазмі вводиться крові маси тіла] [мкг/мл] 1 Сліпа проба 2 не вводили 3 4 Порівняльна внутрішньовенно А 25 А 1000 А 1000 Проба Проба однократно перорально однократно перорально 5 через 5 хв після введення через 1 год після введення через 3 год після введення 6 0,0 2,3 3,3 6,3 9 1 87114 10 Продовження таблиці 2 2 3 4 Проба перорально двічі на день протягом 3-х днів А 166,66 Порівняльна внутрівенно Б 25 Б 1000 Б 1000 Б 166,66 Проба Проба Проба однократно перорально однократно перорально перорально двічі на день протягом 3-х днів Гедеракозид C не вдалося виявити в жодній пробі. З наведених вище в таблиці 2 даних випливає, що при багаторазовому введенні екстракту з меншим вмістом у ньому a-гедерину вимірювана концентрація a-гедерину в плазмі була вищою, ніж 5 через 1 год після останнього введення через 5 хв після введення через 1 год після введення через 3 год після введення через 1 год після останнього введення 6 20,8 10,0 11,1 14,4 14,9 при порівняльному введенні екстракту з більшим вмістом у ньому a-гедерину. Цей результат вдалося пояснити шляхом перерахунку одержаних значень, результати якого представлені нижче в таблиці 3. Таблиця 3 Квоти резорбції при введенні екстракту А (який містить 14,5% гедеракозиду C та 0,9% a-гедерину) Тип введення/час взяття крові Однократне введення/через 1 год після введення Однократне введення/через 3 год після введення Багаторазове введення/через 1 год після введення Максимально Максимально досяжний Концентрація aКвота досяжна концен- Квота резор- рівень у крові при розрезорбції гедерину в платрація (теоретибції [%] гляді загального вмісту [%] змі [мкг/мл] чна) сапонінів [мкг/мл] 3,3 90 3,7 980 0,33 6,3 90 7,0 980 0,64 20,8 90 23,1 980 2,12 Загальний вміст сапонінів розраховується з урахуванням молярних мас обох компонентів і зазначений в перерахунку на a-гедерин. У цьому випадку загальний вміст сапонінів в екстракті А становив 9,8% у перерахунку на a-гедерин. Об'єм крові приймали при цьому таким, що дорівнював 20 мл. Результати розрахунків для екстракту Б наведені нижче в таблиці 4. Таблиця 4 Квоти резорбції при введенні екстракту Б (який містить 6,5% гедеракозиду C та 4,0% a-гедерину) Тип введення/час взяття крові Однократне введення/через1 год після введення Однократне введення/через 3 год після введення Багаторазове введення/через 1 год після введення Максимально Максимально досяжний Концентрація aКвота Квота досяжна конценрівень у крові при розгляді резорбції резорбції гедерину в плазмі трація (теоретичзагального вмісту сапоні[%] [%] [мкг/мл] на) нів [мкг/мл] 11,1 400 2,8 800 1,38 14,4 400 3,6 800 1,80 14,9 400 3,7 800 1,86 Загальний вміст сапонінів розраховується з урахуванням молярних мас обох компонентів і зазначений в перерахунку на a-гедерин. У цьому випадку загальний вміст сапонінів в екстракті Б 11 87114 12 одержуваних якими екстрактів з листя плюща відстановив 9,8% у перерахунку на a-гедерин. Об'єм різняється високим вмістом одного із двох гедерокрові приймали при цьому рівним 20 мл. сапонінів, відповідно інший з яких одночасно із Резюмуючи сказане вище, можна констатувацим міститься в екстракті лише у винятково малих ти, що при багаторазовому введенні збагачених aкількостях. гедерином і збіднених a-гедерином екстрактів кона) Одержання збагаченого a-гедерином екстцентрація a-гедерину в плазмі досягає порівнянракту них між собою рівнів. Однак з урахуванням вмісту При екстракційній обробці листя плюща цим гедеракозиду C в обох екстрактах і обчисленому методом необхідною передумовою для регулюзагальному вмісту обох сапонінів у перерахунку на вання співвідношення між гедеракозидом Ci aa-гедерин обидва екстракти лише незначно різгедерином є цілеспрямоване відщеплення в проняться між собою. Грунтуючись на цих результацесі екстракції залишку цукру, який знаходиться в тах, слід виходити з того, що in vivo відбувається положенні С28 від гедеракозиду С. Оскільки перевідщеплення залишку цукру, який знаходиться в творення гедеракозиду C в a-гедерин по суті відположенні С28, від гедеракозиду C з утворенням бувається кількісно, як вихідний матеріал для одеa-гедерину, що резорбується. Цей процес, тобто ржання збагаченого a-гедерином екстракту перетворення гедеракозиду C в a-гедерин, графіпридатна практично будь-яка партія листя плюща. чно проілюстрований на прикладеній до опису Після перевірки якості продукції відділом контсхемі. ролю якості й одержання від нього дозволу на виРезультати експериментів, які підтверджують пуск продукції частину лікарської рослинної сиронаявність у a-гедерину на відміну від гедеракозиду вини (листя плюща DAC) піддавали інтенсивному C спазмолітичної активності in vitro, і виявлення в подрібнюванню в млині й потім подрібнений матеплазмі a-гедерину, а не гедеракозиду С, дозволяріал просівали через сито для гарантованого відсіють виходити з того, що концентрація a-гедерину в вання тих шматочків, розмір яких перевищував крові значною мірою корелює з підтвердженою максимально припустимий розмір, що дорівнював багатьма клінічними дослідженнями терапевтич2´2 мм. Просіяний матеріал додатково перевіряли ною дією. візуально на наявність у ньому більших шматочків Тому при застосуванні оптимізованого відносі сторонніх домішок. но терапевтичної дії екстракту, концентрація aДо подрібненого зразка додавали водний комгедерину в плазмі в принципі завжди повинна понент у кількості, яка припадала на 6 частин ексшвидко досягати одного і того самого рівня, який трагенту (етанол у концентрації 30% (за масою)). зберігається й при багаторазовому введенні екстЦю суміш ферментували протягом 60 хв при 30°С, ракту в організм. Цій умові задовольняє екстракт періодично перемішуючи її. Б, вже через одну годину після введення якого в Після цього додавали 96%-ий етанол у кількоорганізм концентрація a-гедерину в плазмі на відсті, яка припадала на 6 частин екстрагенту, і суміш міну від екстракту А досягає рівня, порівнянного з гомогенізували шляхом її перемішування. концентрацією a-гедерину в плазмі після багатоПісля 6-годинної стадії попереднього набуханразового введення екстракту в організм. Екстракт ня елюат відокремлювали, а лікарську рослинну Б з вмістом гедеракозиду С, який дорівнює 6,5%, і сировину, що залишилася, перколювали іншими 6вмістом a-гедерину, який дорівнює 4,0%, відрізняа частинами екстрагенту. вся швидким настанням дії й відтворюваністю теОб'єднані елюати для видалення з них дрібних рапевтичної дії. часточок лікарської рослинної сировини ще раз З урахуванням сказаного вище оптимальні для фільтрували й гомогенізували, після чого сушили в терапевтичної дії межі вмісту гедеракозиду C і aплівковому випарному апараті при температурі гедерину в екстракті можна виходячи з екстракту Б 55°C і тиску 150 мбар до одержання згущеної маобмежити наступними значеннями; си. Цю масу гомогенізували й потім піддавали розгедеракозид С: 5-8%, пилювальному сушінню при температурі в інтерa-гедерин: 3-5%. валі від 45 до 60°С, одержуючи сухий екстракт із 2. Одержання оптимізованого екстракту з лислистя плюща. тя плюща Для перевірки цього способу одержання екстВідмітна риса оптимізованого екстракту з лисракту одержували наступні екстракти. З листя тя плюща полягає в тому, що він має у всіх партіях плюща з 3,91%-вим вмістом у них гедеракозиду C і однаковий у певних межах склад у перерахунку на 0,20%-вим вмістом a-гедерину одержували один його компоненти гедеракозид C і a-гедерин. При екстракт традиційним способом (подрібнювання цьому вміст гедеракозиду C у такому екстракті висушеного зразка з безпосереднім наступним повинен знаходитися в межах від 50 до 80 мг/г, а змішуванням з 30% (за масою) етанолу та екстравміст a-гедерину - у межах від 30 до 50 мг/г. Для кцією) і один екстракт новим способом. Результати дотримання зазначених специфікацій між собою хроматографічного аналізу цих екстрактів на вміст змішували декілька екстрактів. Однак екстракти, у них a-гедерину та гедеракозиду C наведені нижякі одержані традиційним способом, лише умовно че в таблиці 5. придатні для застосування в подібних процесах змішування через часто недостатньо високий вміст у них відповідної діючої речовини. Нижче описані методи екстракції, кожний з 13 87114 14 Таблиця 5 Вміст a-гедерину та гедеракозиду C в екстрактах a-гедерин (%) Традиційний спосіб Новий спосіб Гедеракозид C (%) 0,53 4,74 8,68 0 З наведених у таблиці даних випливає, що при екстракції новим способом гедеракозид С, який міститься в листках плюща вдалося повністю перетворити в a-гедерин. Оскільки й загальний вміст сапонінів, розрахований у вигляді гедеракозиду С, має той же порядок величин, знаючи відповідну концентрацію сапонінів у лікарській рослинній сировині й враховуючи коефіцієнт збагачення екстракту aгедерином, який дорівнює приблизно 2-3, можна оцінити кінцевий вміст a-гедерину в екстракті. Відповідно до цього для перетворення в aгедерин тільки деякої частини гедеракозиду С, який міститься в лікарській рослинній сировині, ферментації у воді можна піддавати ^тільки певну частину лікарської рослинної сировини, не змінюючи при цьому всі інші параметри процесу екстракції. Після 60-хвилинно'ї ферментації цієї деякої кількості лікарської рослинної сировини до неї потім для 6-годинного попереднього набухання додають іншу кількість лікарської рослинної сировини та етанол. Знаючи відповідну концентрацію сапонінів у лікарській рослинній сировині й враховуючи коефіцієнт збагачення екстракту aгедерином, який дорівнює приблизно 2-3, можна оцінити кінцевий вміст a-гедерину в екстракті. Таким чином, за допомогою пропонованого у винаході способу за рахунок передбаченої в ньому стадії ферментації можна цілеспрямовано варіювати склад сухого екстракту з листя плюща без значних витрат часу й засобів. Цілеспрямоване регулювання вмісту a-гедерину в сухому екстракті, відповідно, лікарському засобі позитивно позначається на ефективності екстракту, враховуючи крім іншого численні публікації про дієвість a-гедерину. б) Одержання з листя плюща сухих екстрактів з підвищеним вмістом у них гедеракозиду C В даному випадку при екстракційній обробці листя плюща необхідною передумовою для регулювання співвідношення між гедеракозидом C та a-гедерином є цілеспрямоване пригнічення в про Загальний вміст сапонінів, розрахований у вигляді гедеракозиду C (%) 9,54 7,71 цесі екстракції відщеплення залишку цукру, що знаходиться в положенні С28, від гедеракозиду C При виборі партії лікарської рослинної сировини необхідно стежити за тим, щоб на переробку потрапляло листя з низьким вмістом у них aгедерину. При цьому рекомендується використовувати листя із вмістом у них a-гедерину менше 0,5% у перерахунку на висушену лікарську рослинну сировину. Аналіз гомогенного зразка листя плюща показав наступний вміст у них обох сапонінів: гедеракозид С: 6,37%, a-гедерин: 0,85%. З такої лікарської рослинної сировини одержували по три екстракти проведенням екстракції відповідно з наступними методами. З г висушеної та подрібненої до шматочків розміром близько 3x3 мм лікарської рослинної сировини протягом декількох секунд обробляли гарячою водяною парою. Після цього оброблену таким шляхом лікарську рослинну сировину протягом приблизно 6 год піддавали попередньому набуханню в присутності 18 г екстрагенту (етанол у концентрації 30% (за масою)). Лікарську рослинну сировину, яка залишилася після зливу місцели, додатково перколювали 18 г екстрагенту. Цю місцелу сушилиу вакуумній сушильній шафі. В іншому варіанті сушіння можна проводити, наприклад, у плівковому випарному апараті, наприклад, при температурі 55°С та тиску 150 мбар з наступним розпилювальним сушінням при 45-60°С. Температуру в процесі екстракції бажано підтримувати в інтервалі від приблизно 20 до приблизно 40°С, насамперед на рівні приблизно 30°C. Співвідношення між лікарською рослинною сировиною та екстрагентом може при цьому становити, наприклад, 1:12. Результати аналізу одержаних таким шляхом екстрактів наведені нижче в таблиці 6. 15 87114 16 Таблиця 6 Вміст гедеракозиду C та a-гедерину в оброблених парою екстрактах Зразок Вихідна лікарська рослинна сировина Оброблений парою екстракт 1 Оброблений парою екстракт 2 Оброблений парою екстракт 3 Вміст гедеракозиду C (%) Вміст aгедерину (%) Вміст гедерасапонінів, розрахований у вигляді гедеракозиду C (%) 6,37 0,85 7,75 14,33 0,85 15,71 14,26 0,85 15,64 14,57 0,71 15,72 Згідно з наведеними у таблиці даними вміст aгедерину в одержаному за описаною вище методикою сухому екстракті з листя плюща відповідав кількості a-гедерину, яка максимально містилася у вихідному листі. У цілому ж таким шляхом одержали стабільні при зберіганні екстракти з високим вмістом у них гедеракозиду C та дуже низьким вмістом a-гедерину. При застосуванні партій листя плюща із вмістом a-гедерину нижче 0,5% максимальний вміст a-гедерину в одержаному екстракті також можна прийняти таким, що дорівнює 0,5%. в) Змішування обох збагачених екстрактів Описаними в пп. 2а) та 2б) методами екстракції з листя плюща можна одержувати екстракти, кожний з яких збагачений тільки одним із двох гедерасапонінів. З обох збагачених тим або іншим гедерасапоніном екстрактів на завершення приготовляють суміш із одержанням готового спеціального екстракту з вмістом у ньому гедеракозиду C у межах від 5 до 8% та вмістом a-гедерину в межах від 3 до 5%. Приклад 1 частина екстракту А з вмістом a-гедерину близько 7,5% + 1 частина екстракту Б з вмістом гедеракозиду C близько 13,0% і вмістом a-гедерину 0,5% ® екстракт з вмістом гедеракозиду 6,5% та вмістом a-гедерину 4,0%. Очевидно, що це рівняння щоразу необхідно узгоджувати з конкретним вмістом гедерасапонінів в обох збагачених ними екстрактах, однак у принципі концентрацію гедерасапонінів можна також відрегулювати в обох збагачених ними екстрактах на зазначені вище в прикладі значення змішуванням між собою різних екстрактів з різним ступенем збагачення їх одним або іншим гедерасапоніном. Відповідно до сказаного вище, одержаний пропонованим у винаході способом екстракт можна використовувати для приготування на його основі лікарського засобу, який вже при однократному його застосуванні забезпечує дуже швидке надходження в організм власне діючої речовини (a-гедерину). Одночасно із цим високий вміст у лікарському засобі гедеракозиду C дозволяє довгостроково підтримувати високий рівень aгедерину в плазмі крові, оскільки гедеракозид C безупинно перетворюється в організмі в aгедерин. Тим самим відпадає необхідність у багаторазовому прийомі лікарського засобу, що поліпшує дотримання пацієнтом режиму та схеми лікування. Одним з показань до застосування екстрактів плюща є захворювання дихальних шляхів, що часто зустрічаються в дітей. Оскільки діти найчастіше неохоче приймають ліки, пропонований у винаході лікарський засіб дозволяє досягти необхідного терапевтичного ефекту при менш частому його застосуванні. 17 Комп’ютерна верстка Д. Шеверун 87114 Підписне 18 Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for preparation of extraction of ivy leaves, extraction, use thereof and drug
Автори англійськоюRunkel Frank, Schneider Wolfgang, Schmidt, Oliver, Engelhard Georg MaximilLian
Назва патенту російськоюСпособ получения экстракта из листьев плюща, экстракт, его применение и лекарственное средство
Автори російськоюРункель Франк, Шнайдер Вольфганг, Шмидт Оливер, Энгельхард Георг Максимилиан
МПК / Мітки
МПК: A61P 11/00, A61K 36/25
Мітки: листя, застосування, лікарський, плюща, екстракту, засіб, спосіб, одержання, екстракт
Код посилання
<a href="https://ua.patents.su/9-87114-sposib-oderzhannya-ekstraktu-z-listya-plyushha-ekstrakt-jjogo-zastosuvannya-ta-likarskijj-zasib.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання екстракту з листя плюща, екстракт, його застосування та лікарський засіб</a>
Попередній патент: Спосіб одержання супозиторія на основі лікарського засобу із тканин плаценти
Наступний патент: Ацетоновий сольват диметоксидоцетакселу і спосіб його отримання
Випадковий патент: Спосіб здвоювання й устаткування здвоювання для виробництва багатошарових виробів