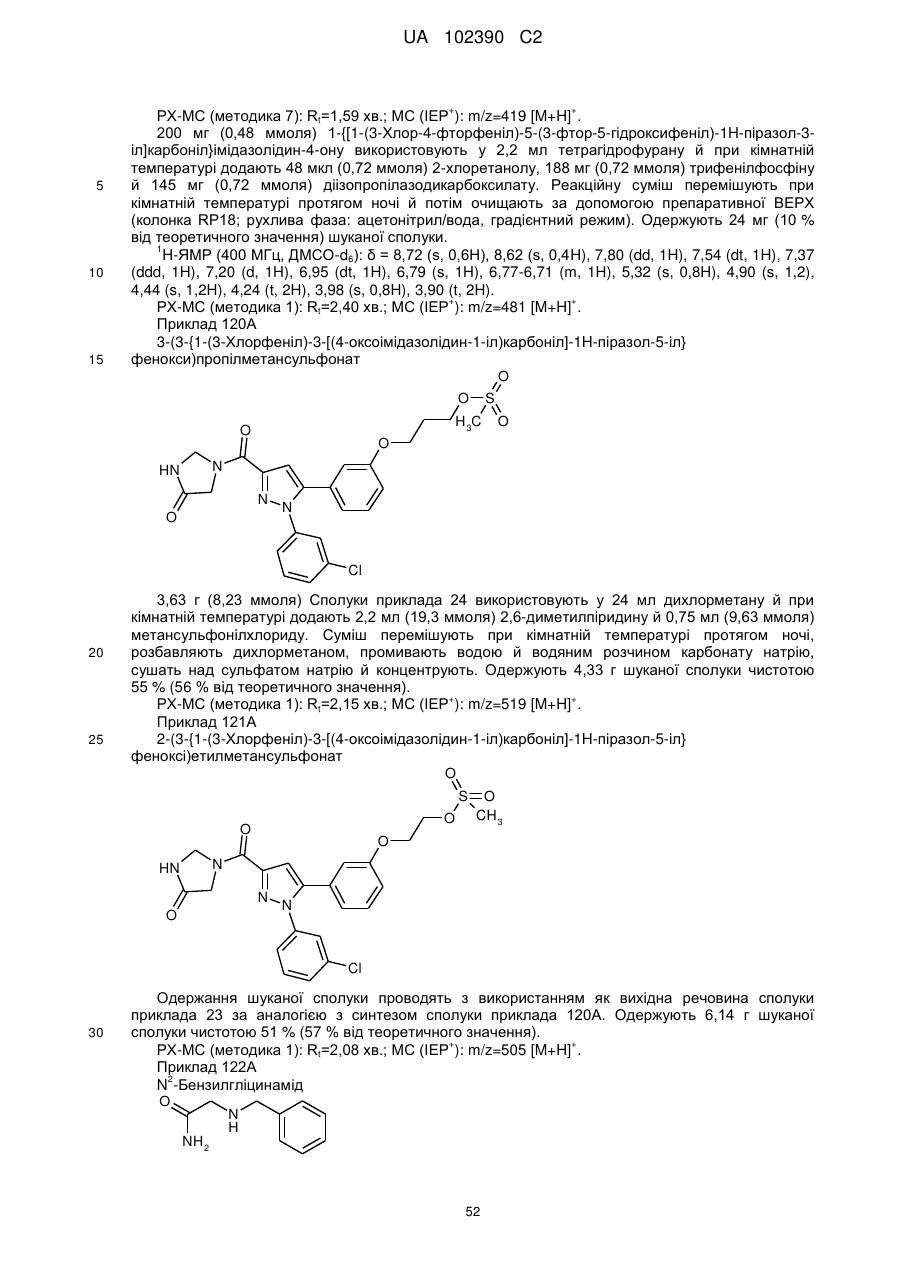
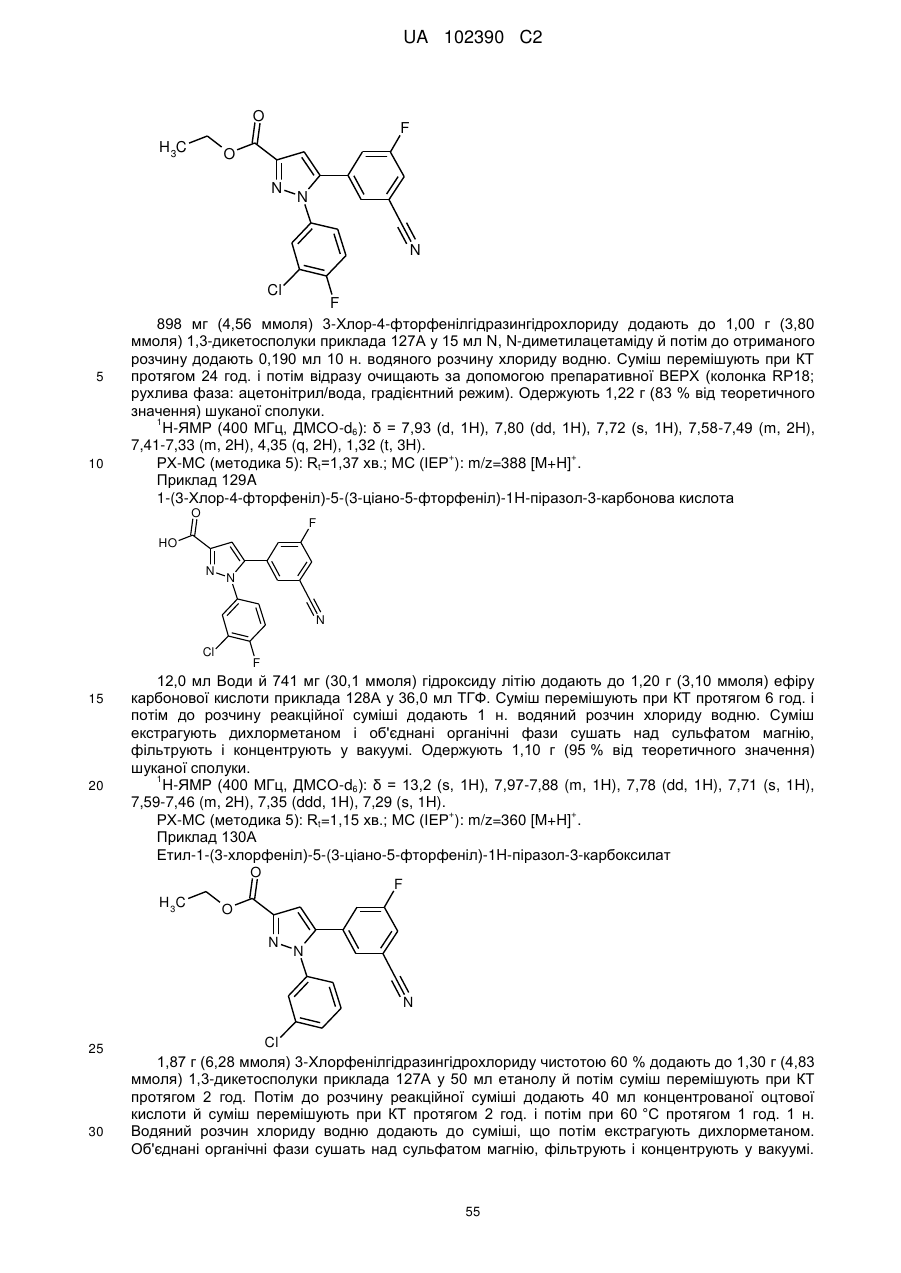
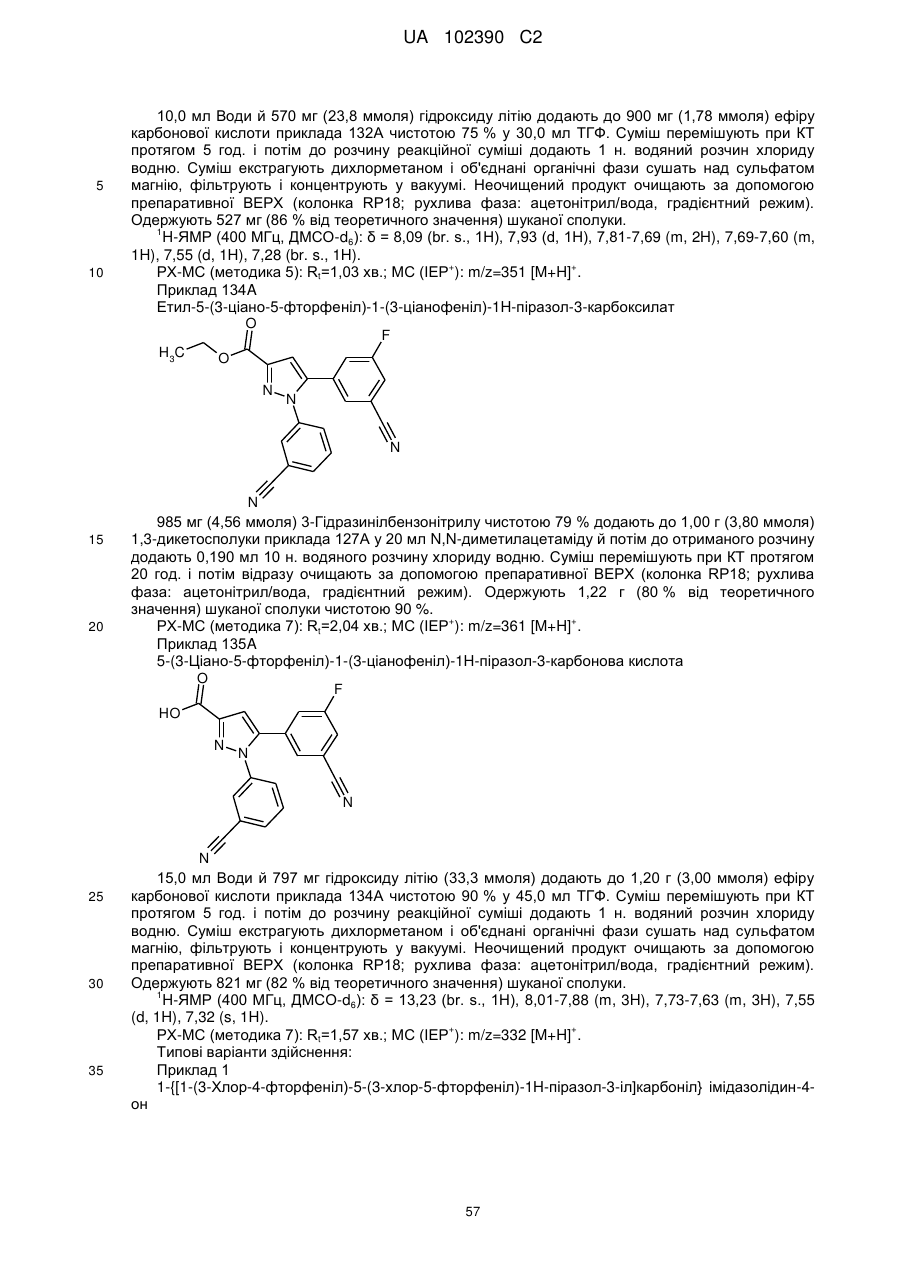
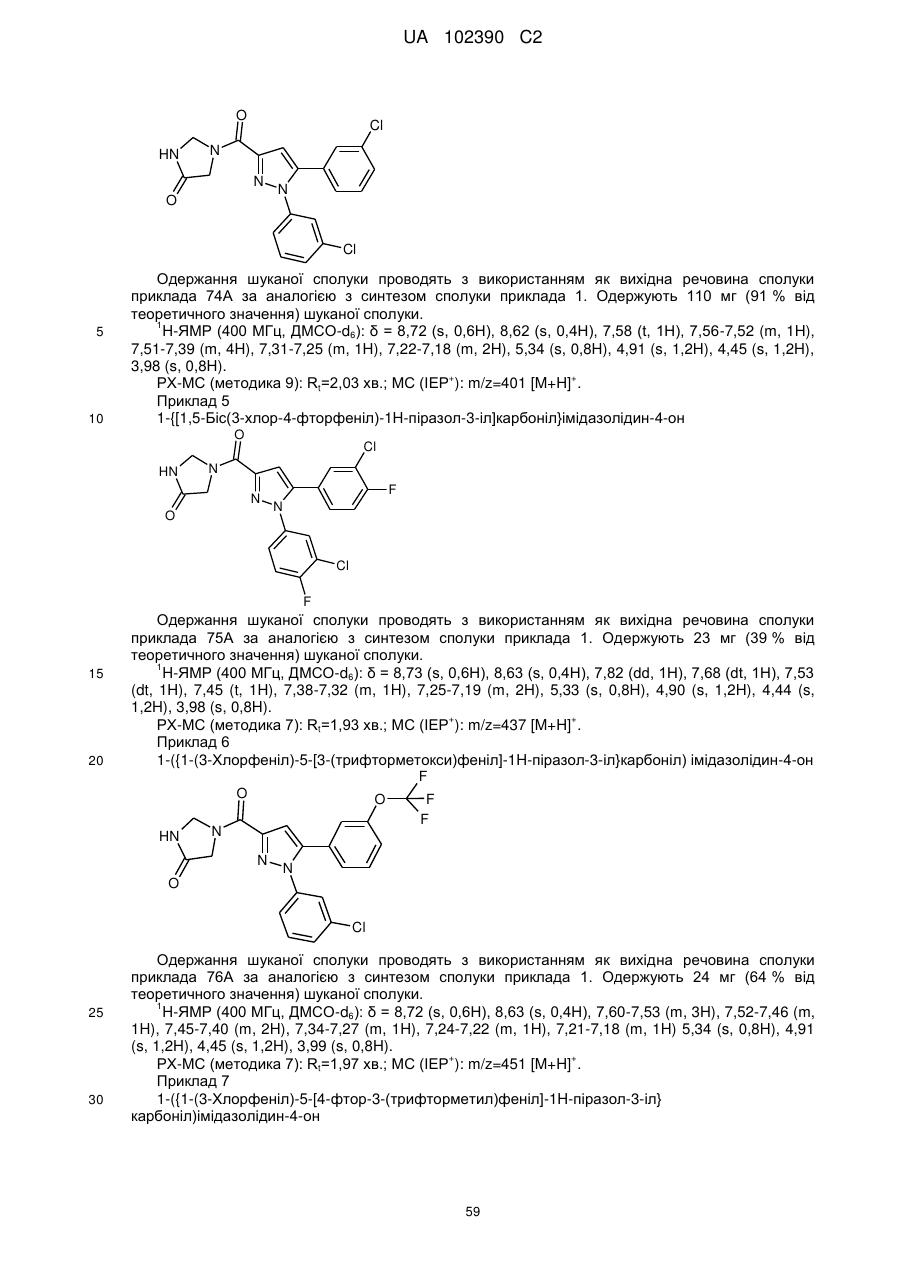
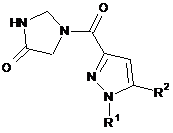
Похідні (піразолілкарбоніл)імідазолідинону, призначені для лікування ретровірусних захворювань
Номер патенту: 102390
Опубліковано: 10.07.2013
Автори: Грешат Сузанне, Вільдум Штеффен, Паульзен Даніела, Теде Кай
Формула / Реферат
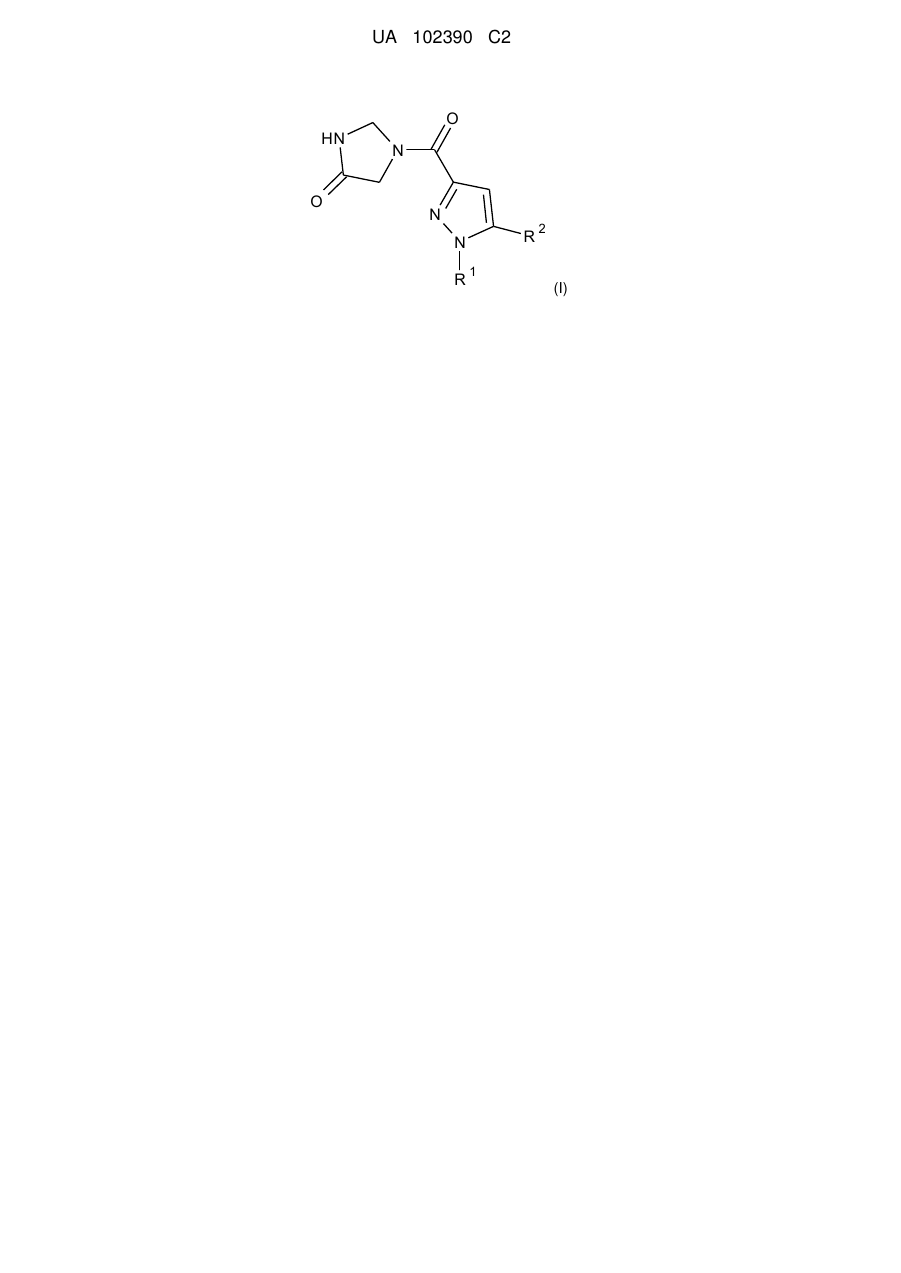
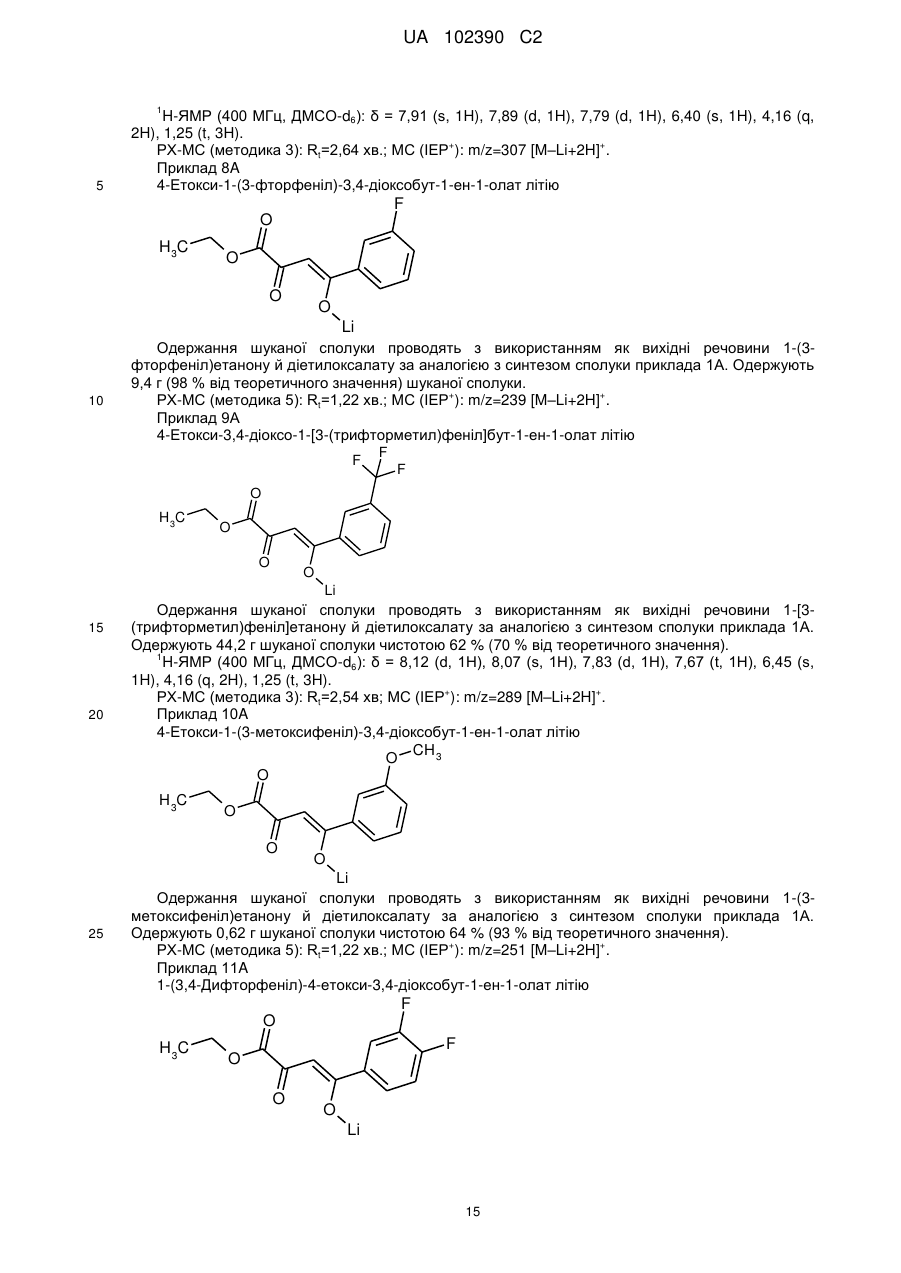
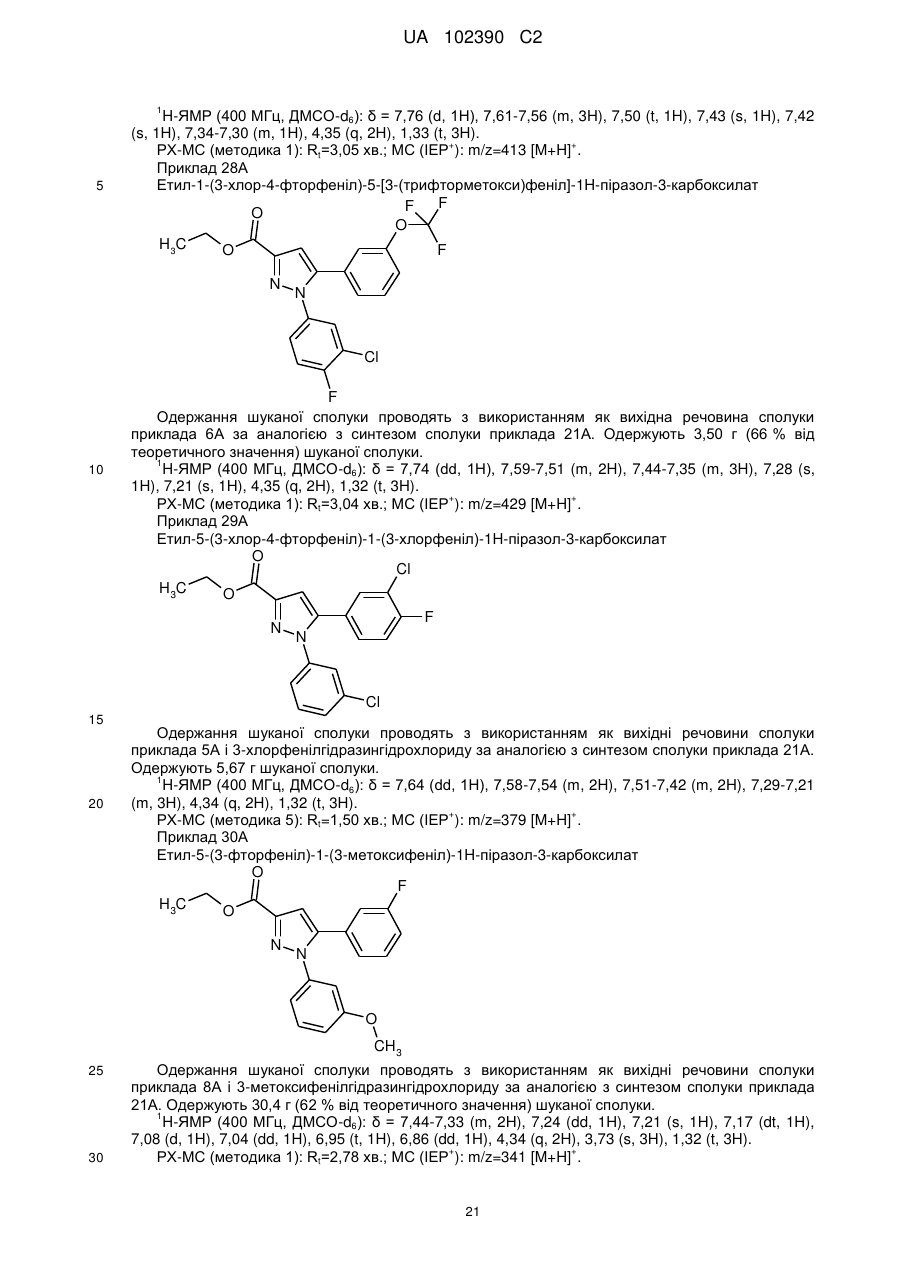
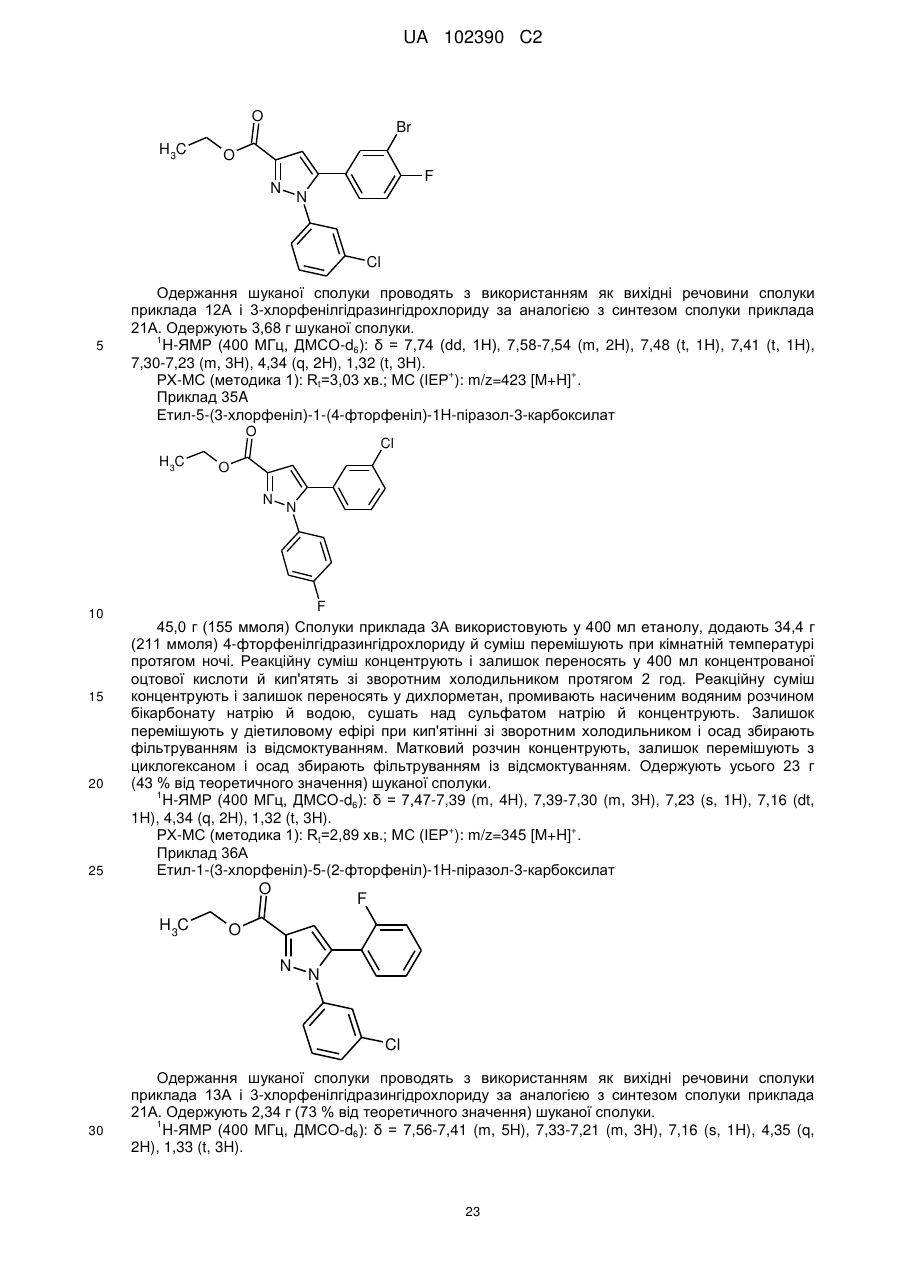
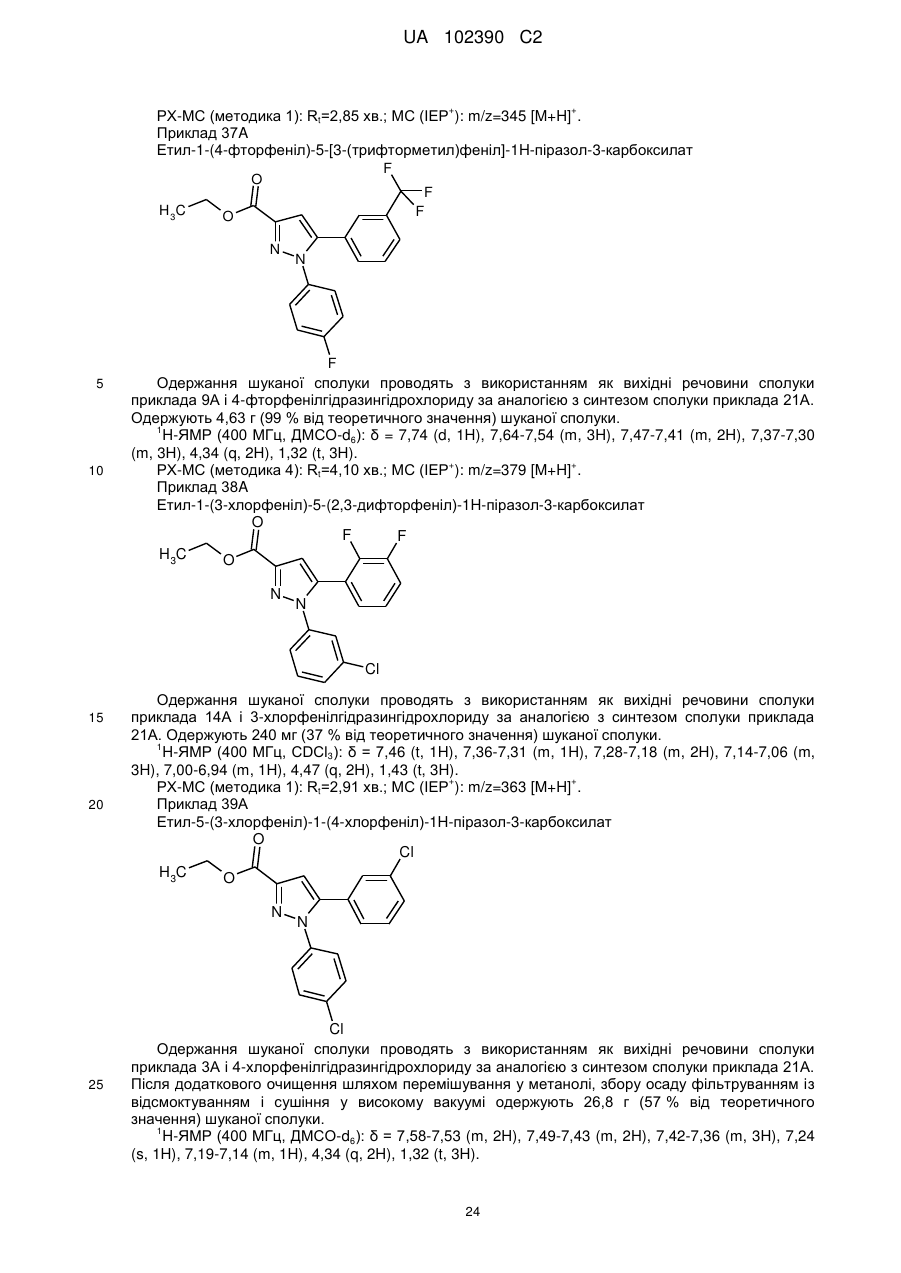
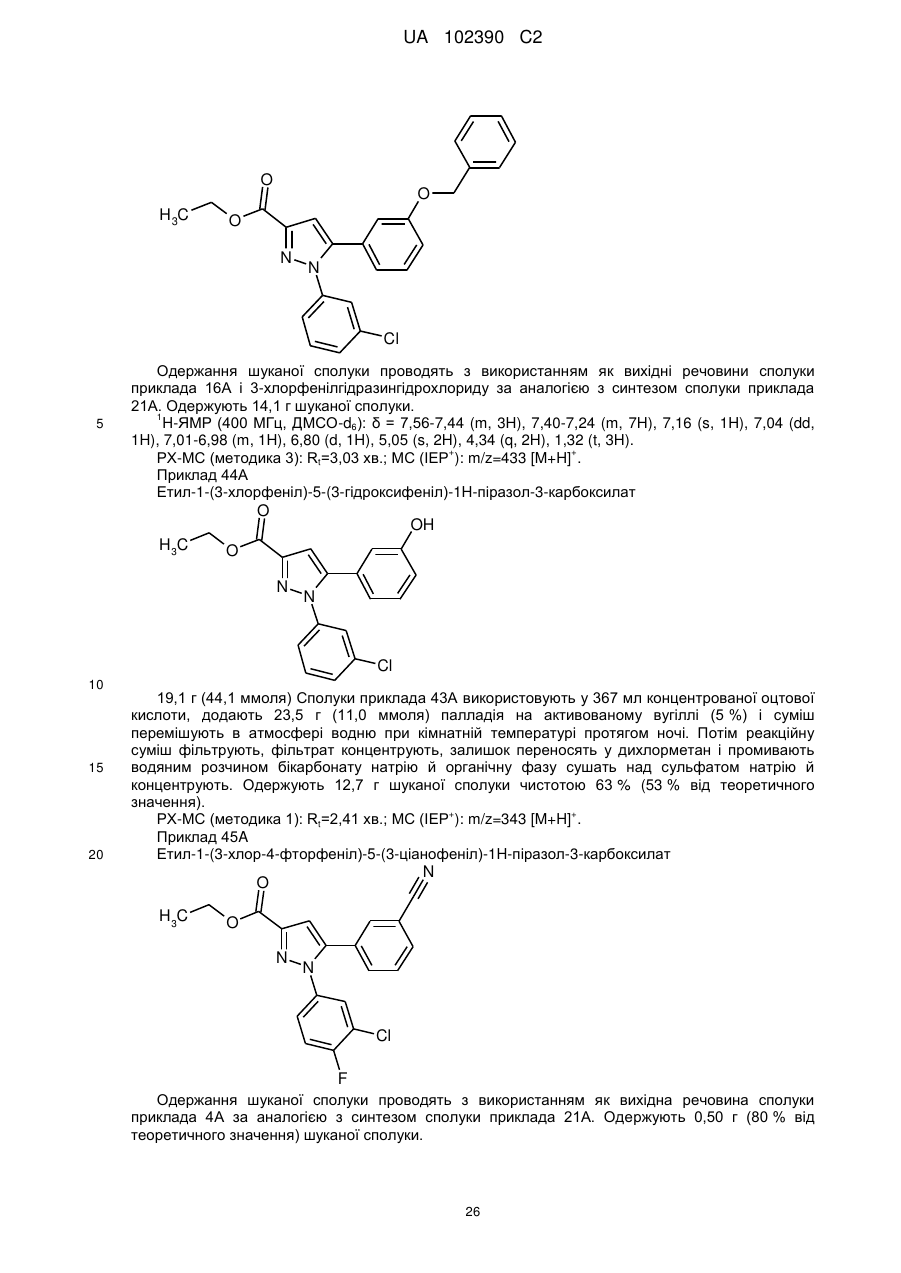
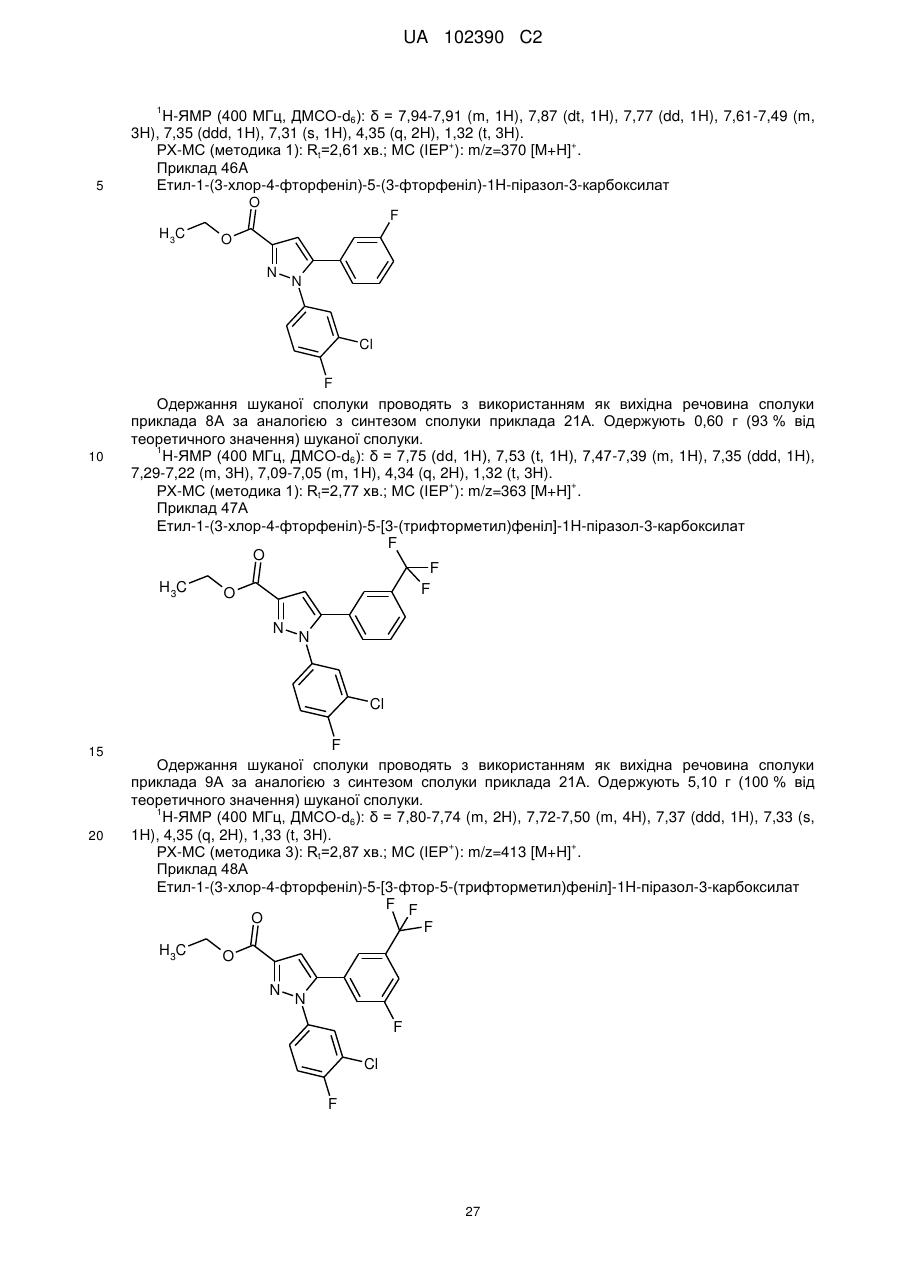
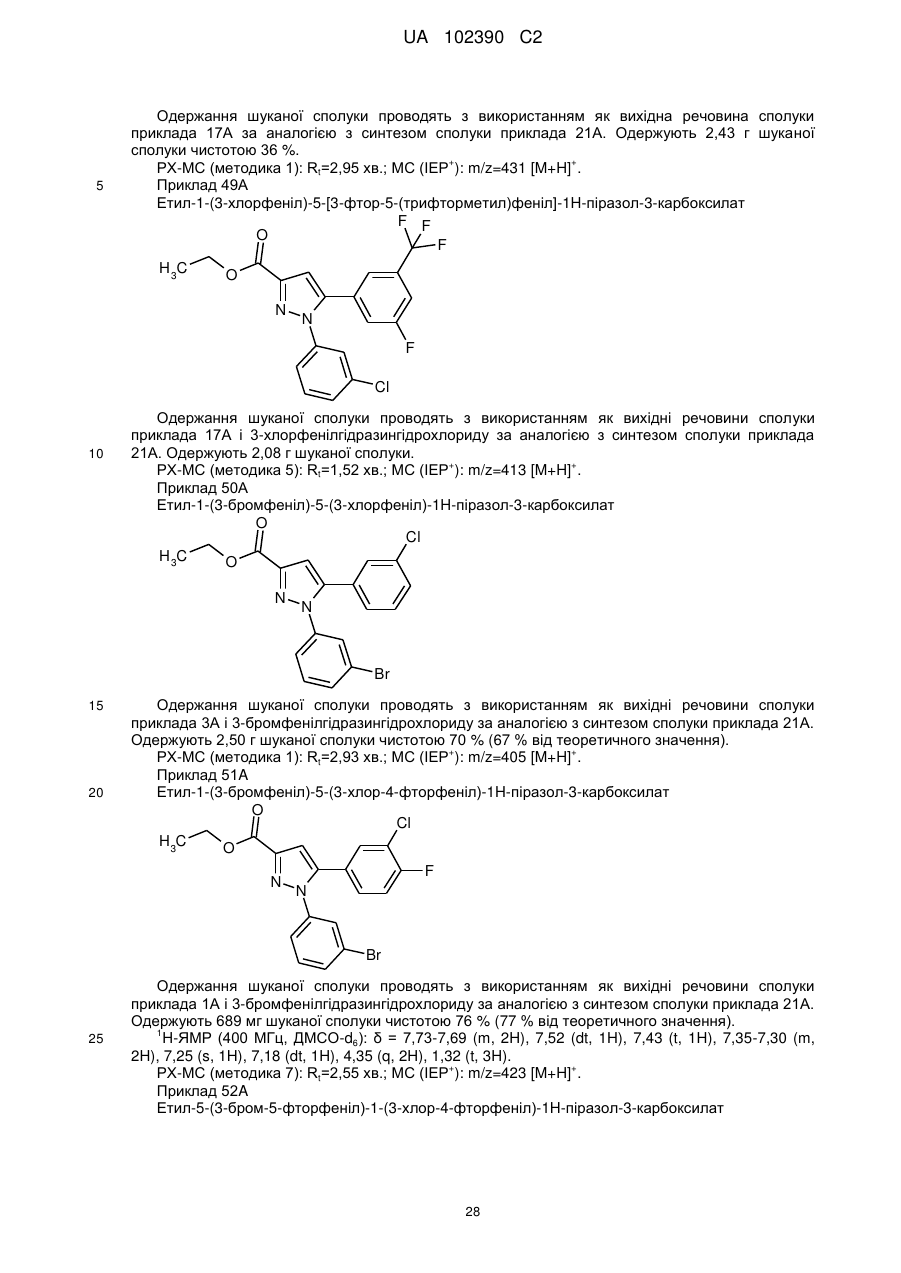
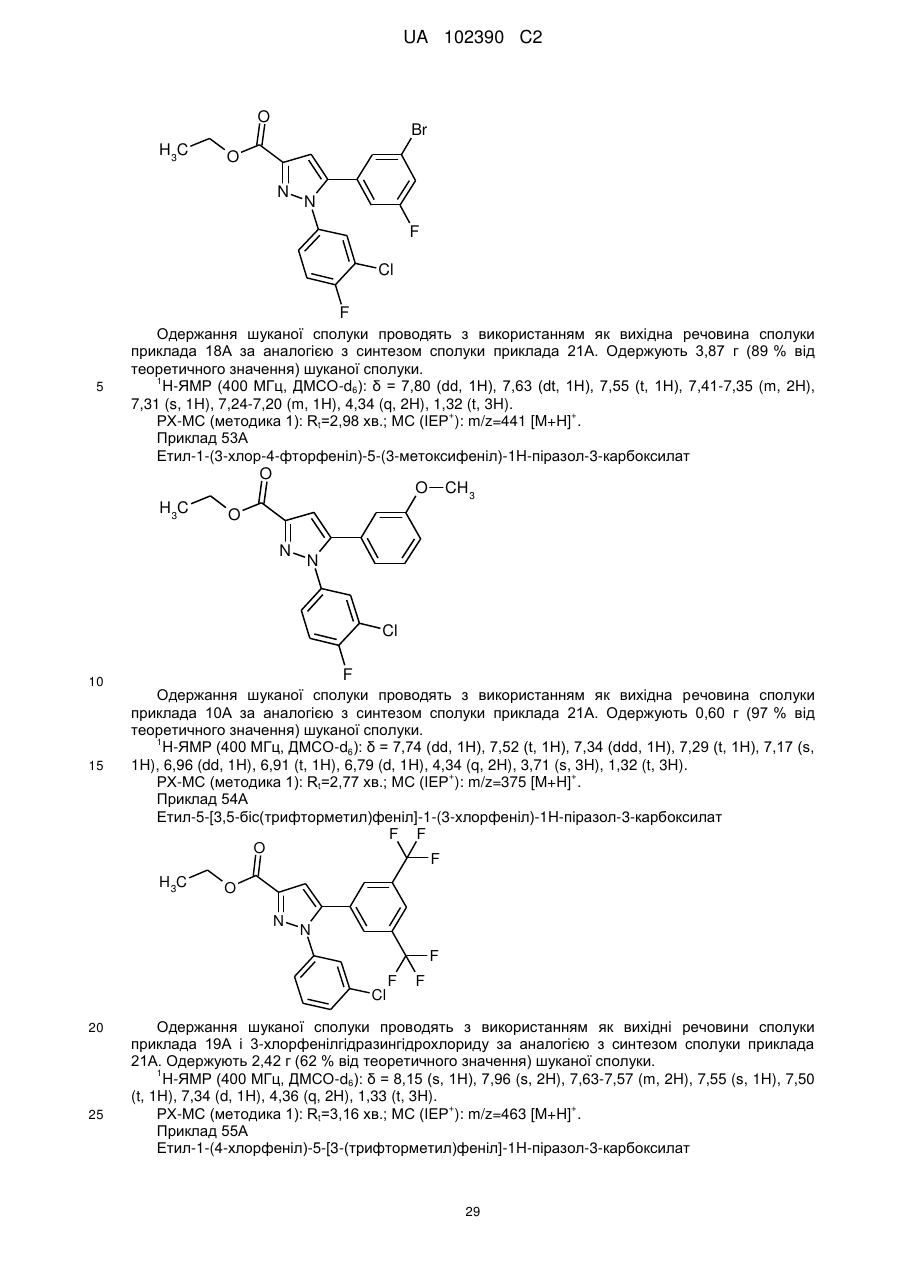
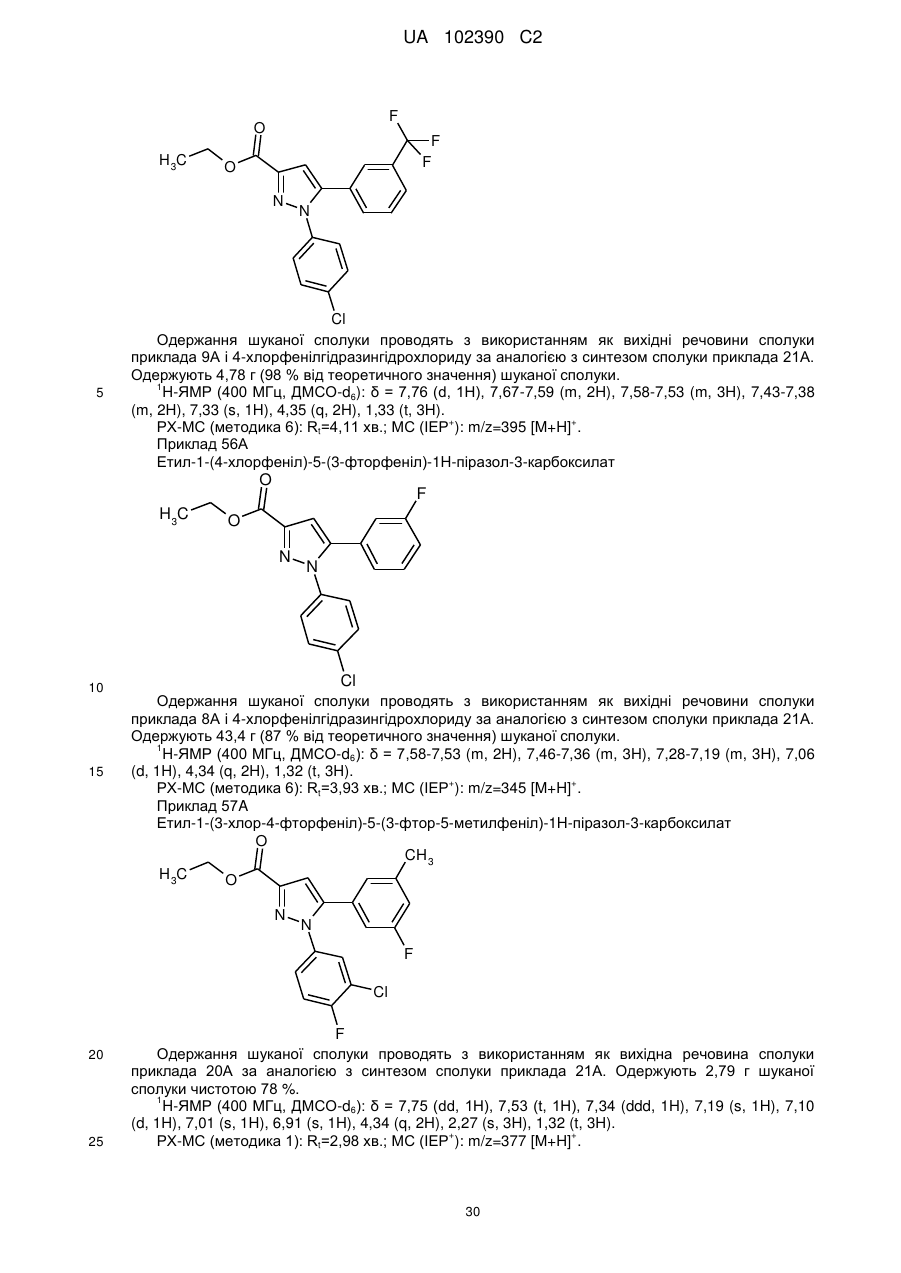
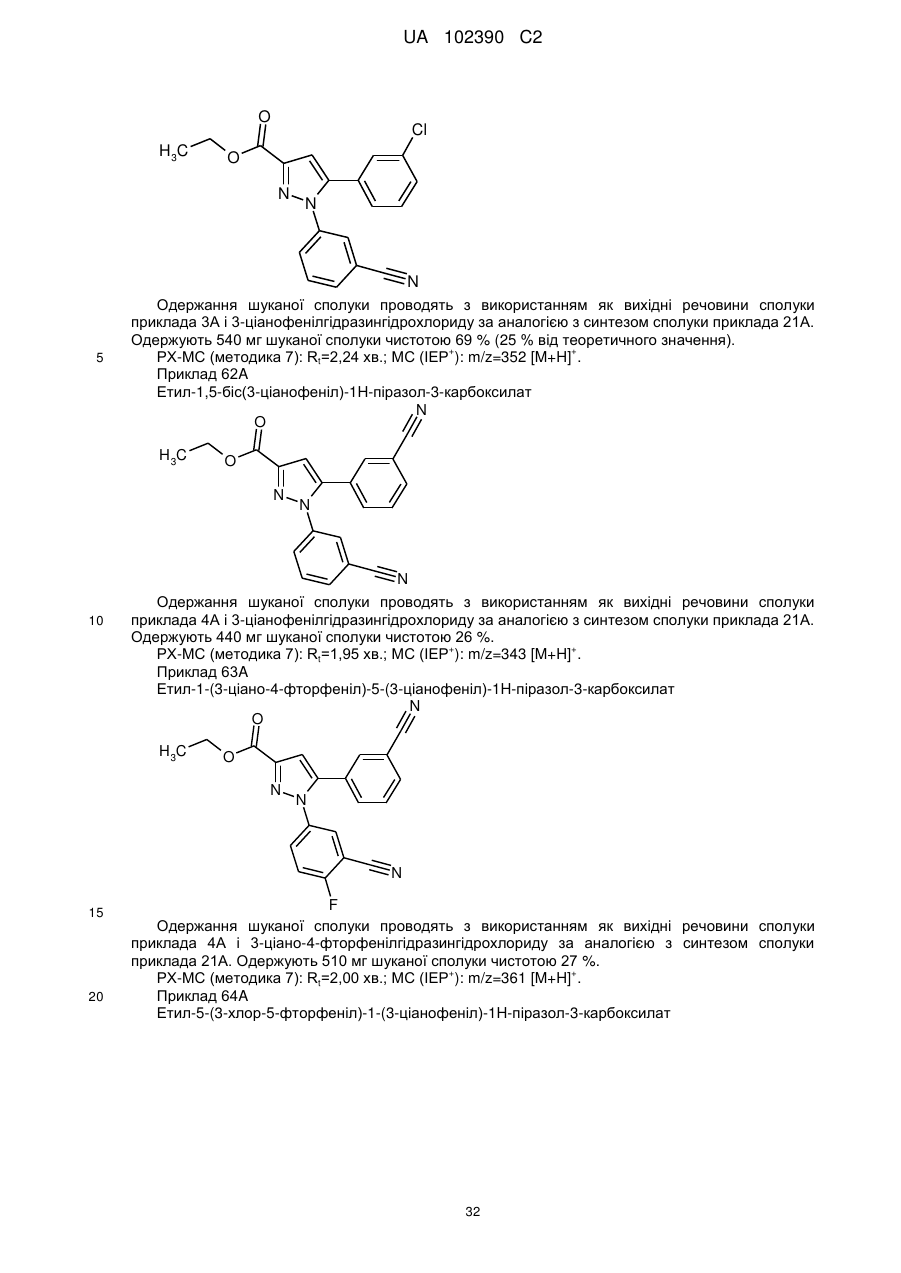
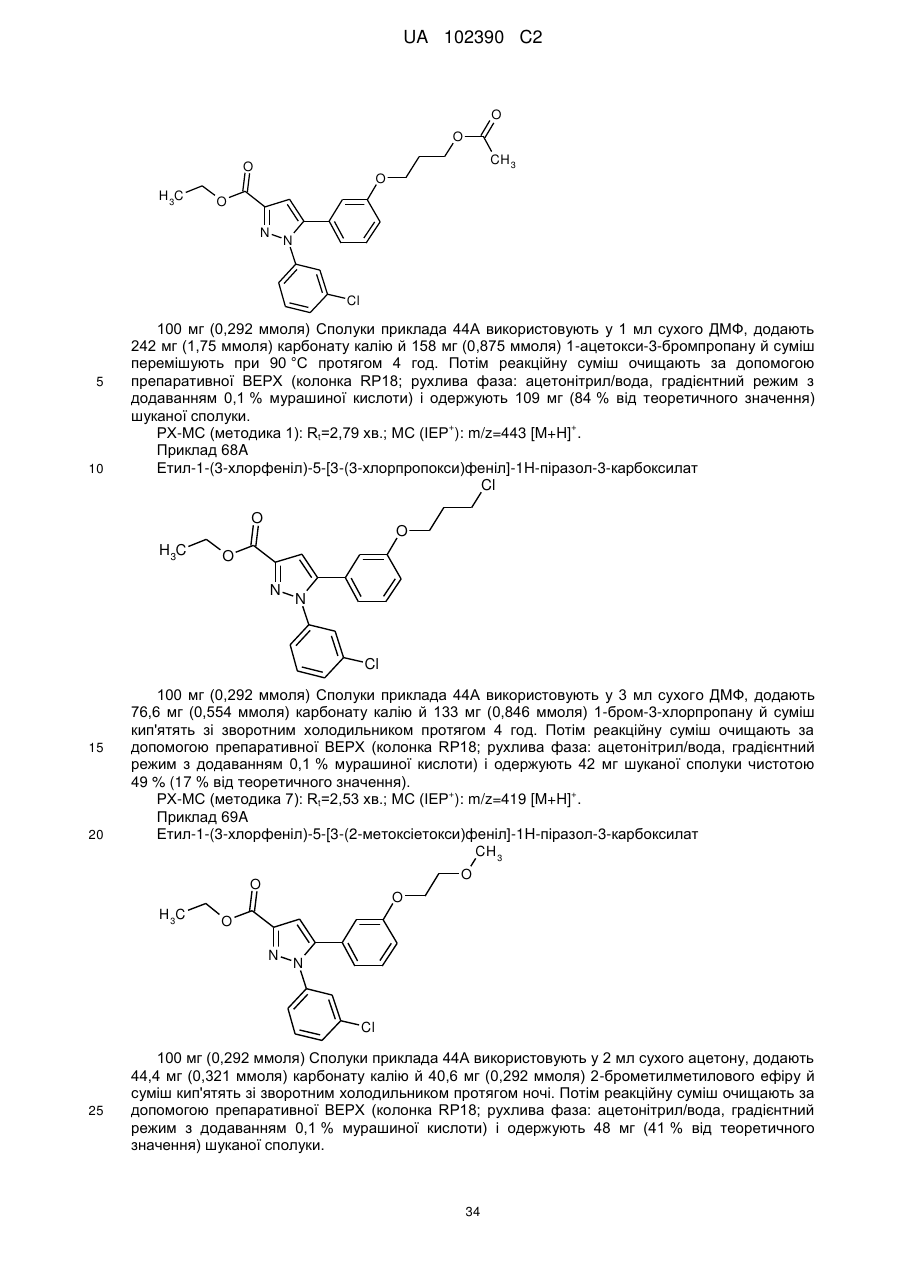
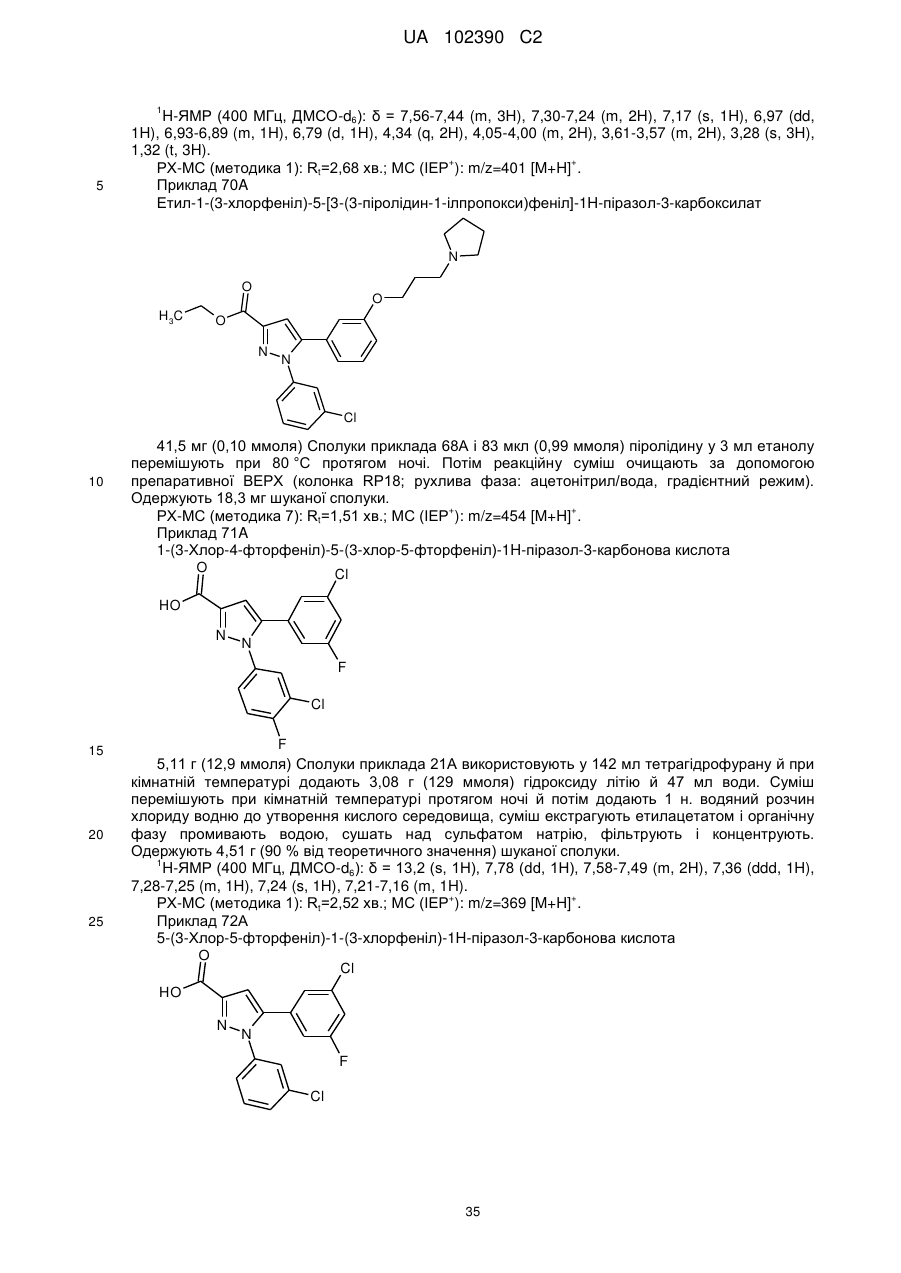
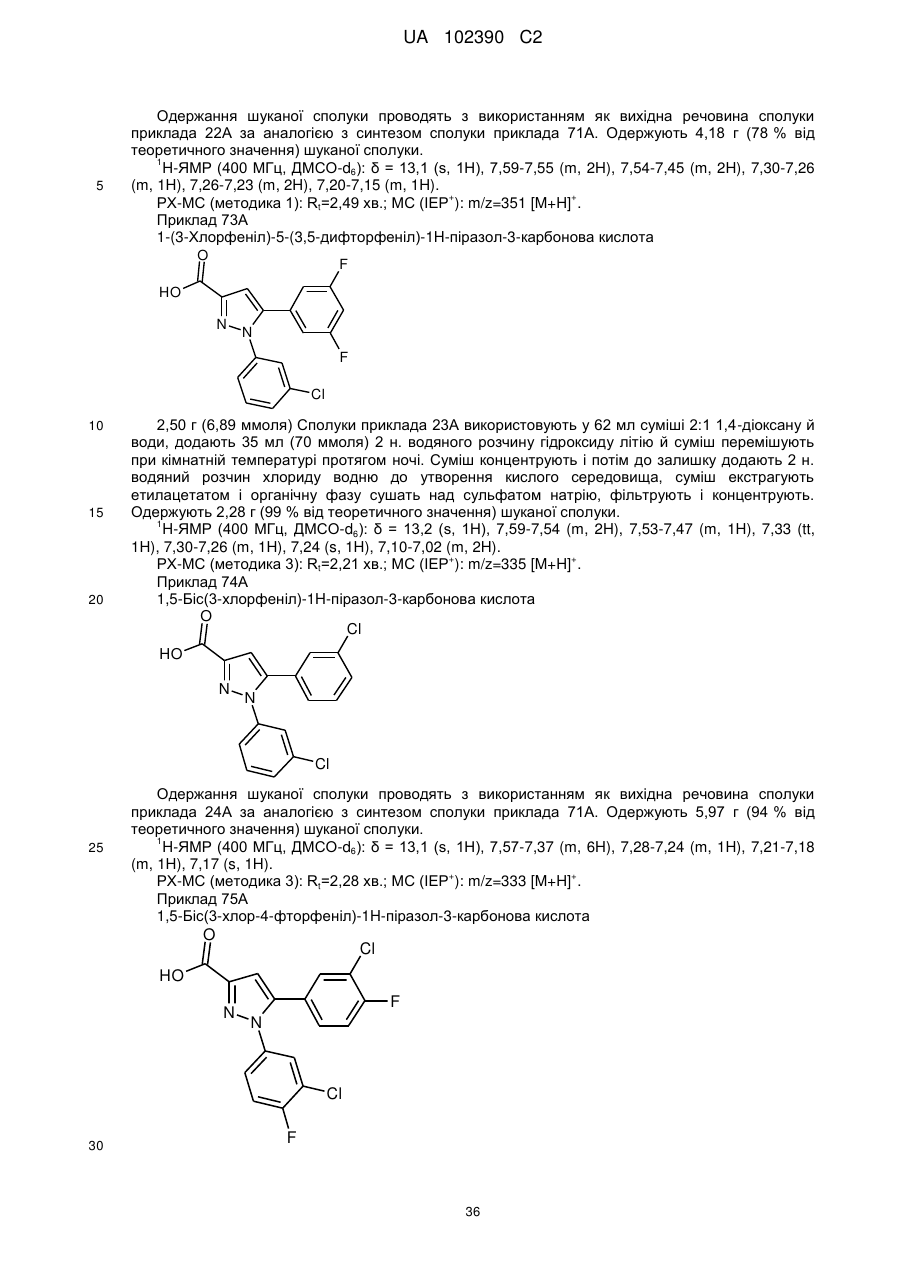
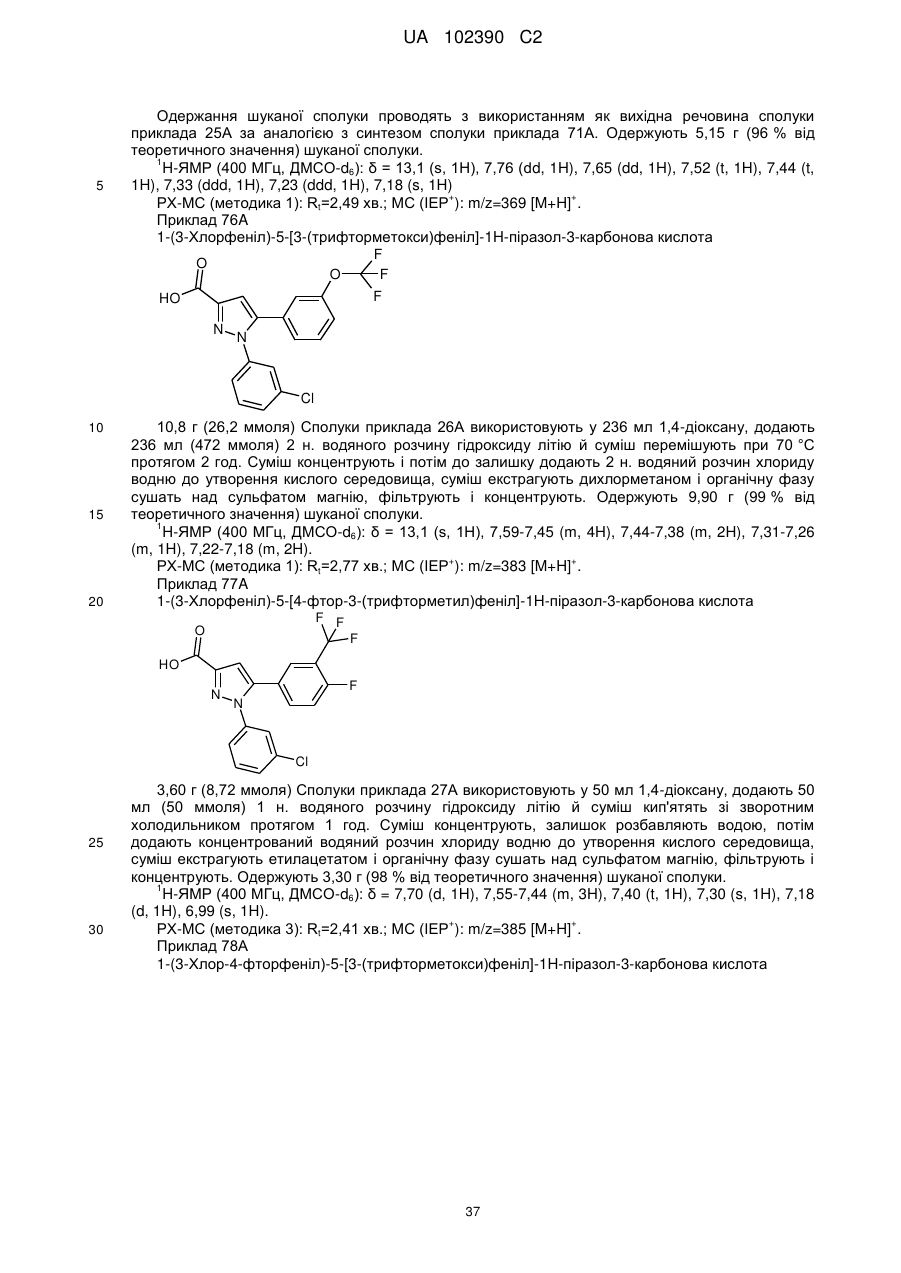
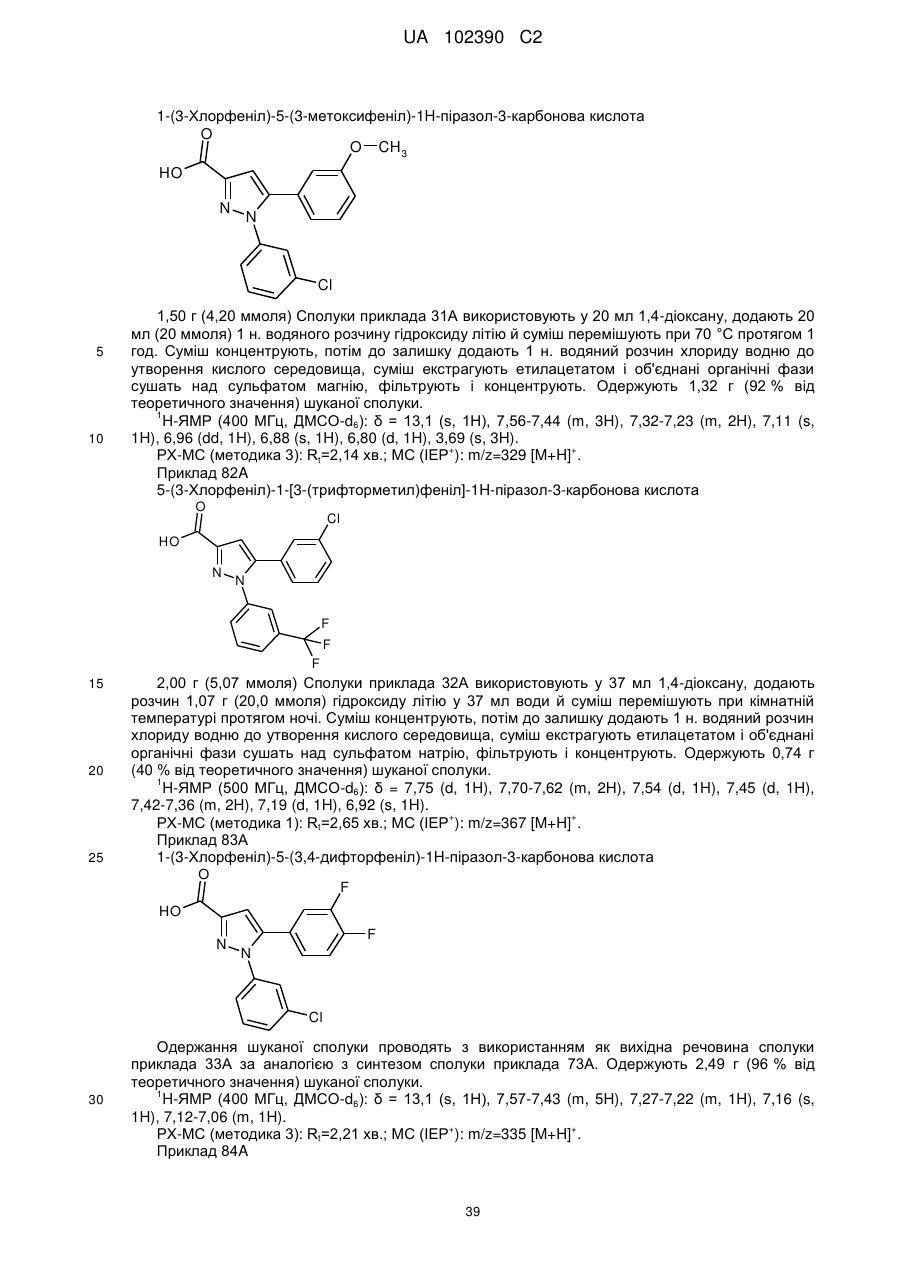
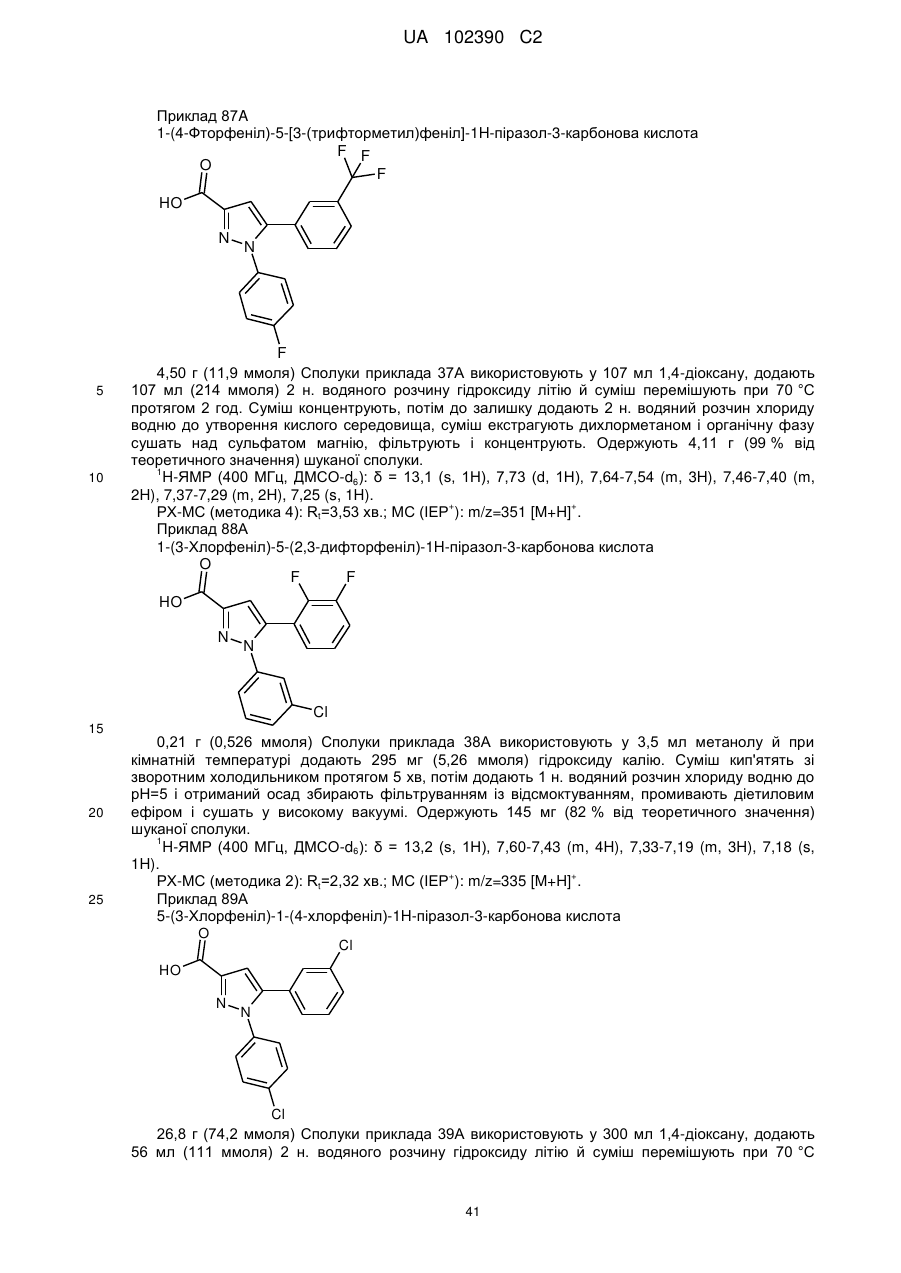
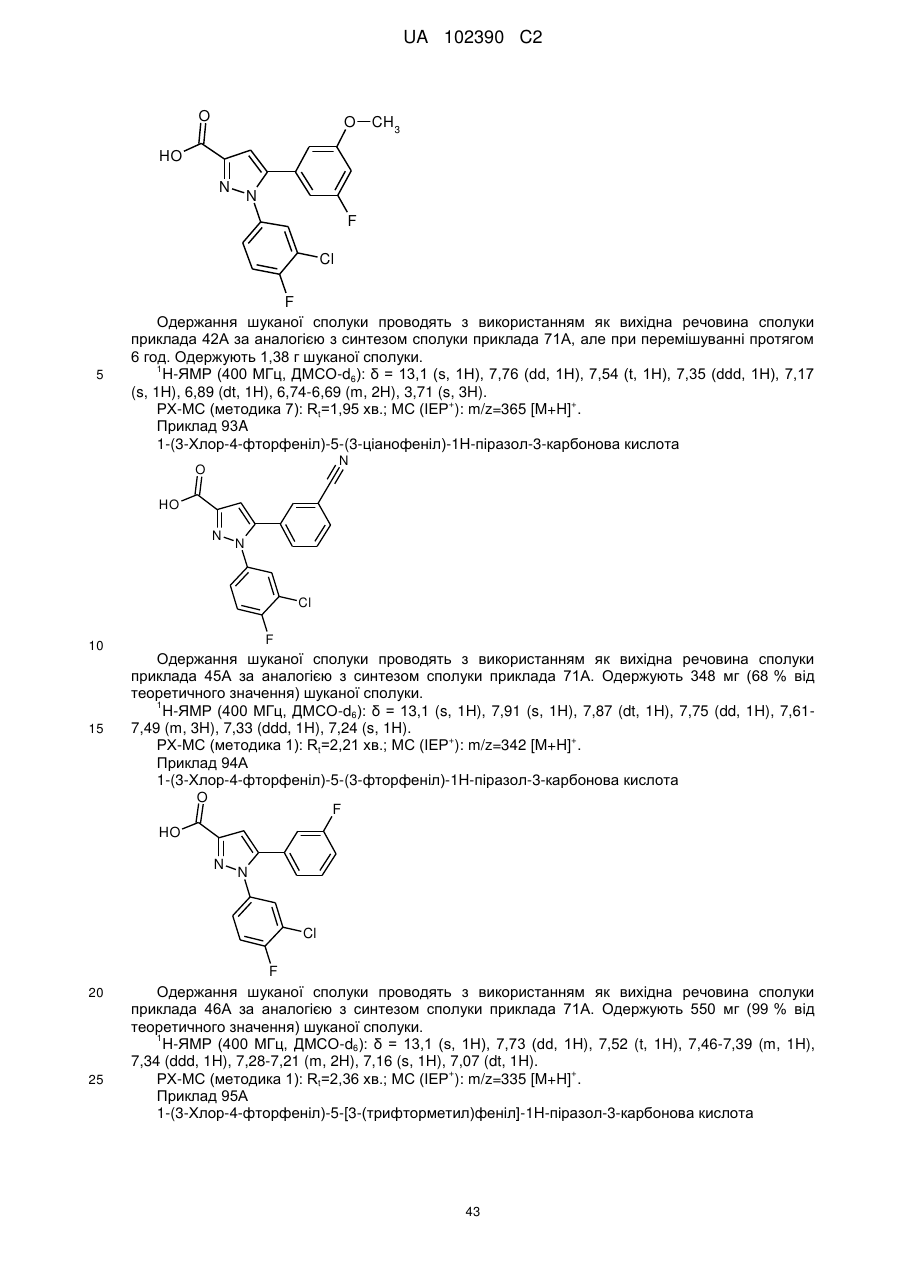
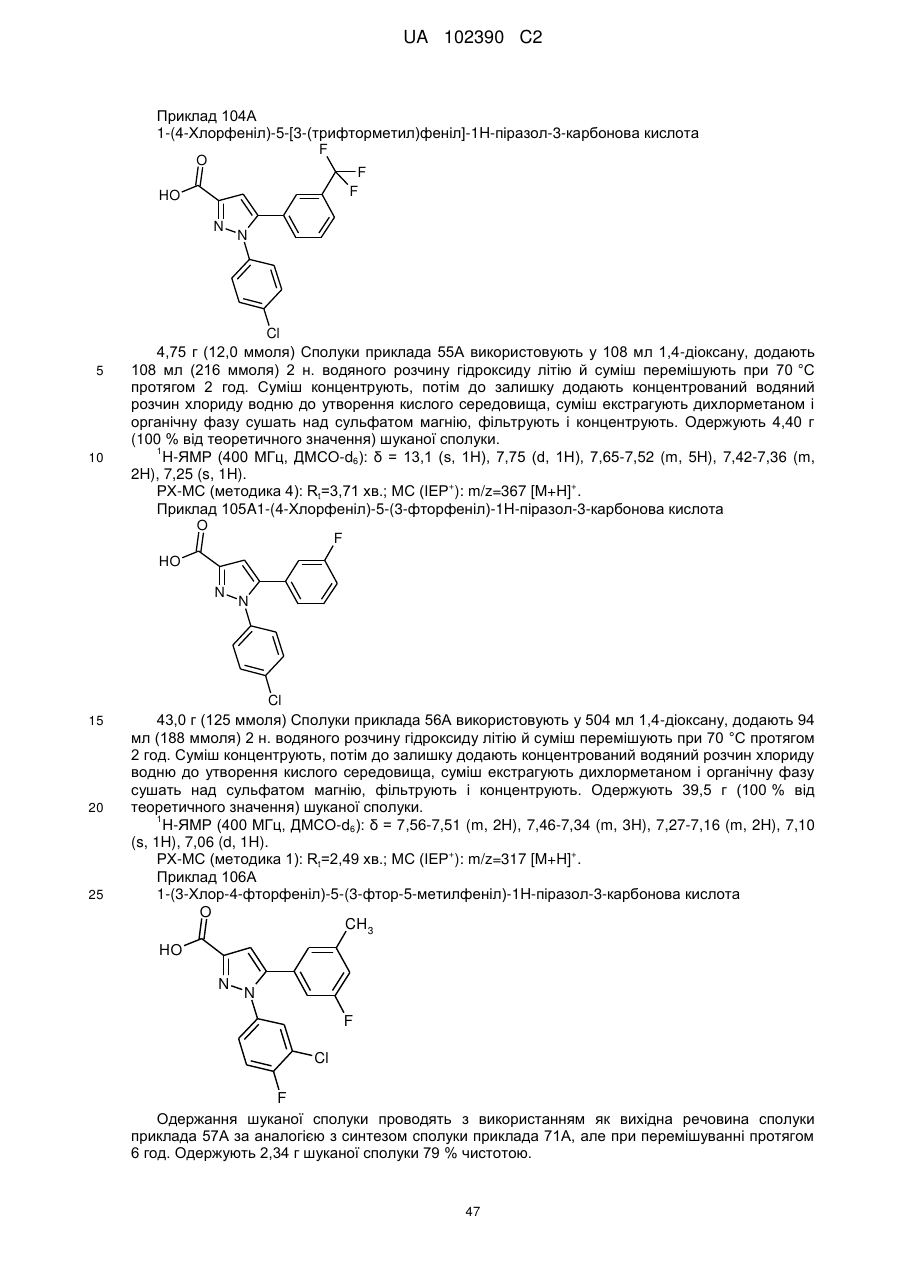
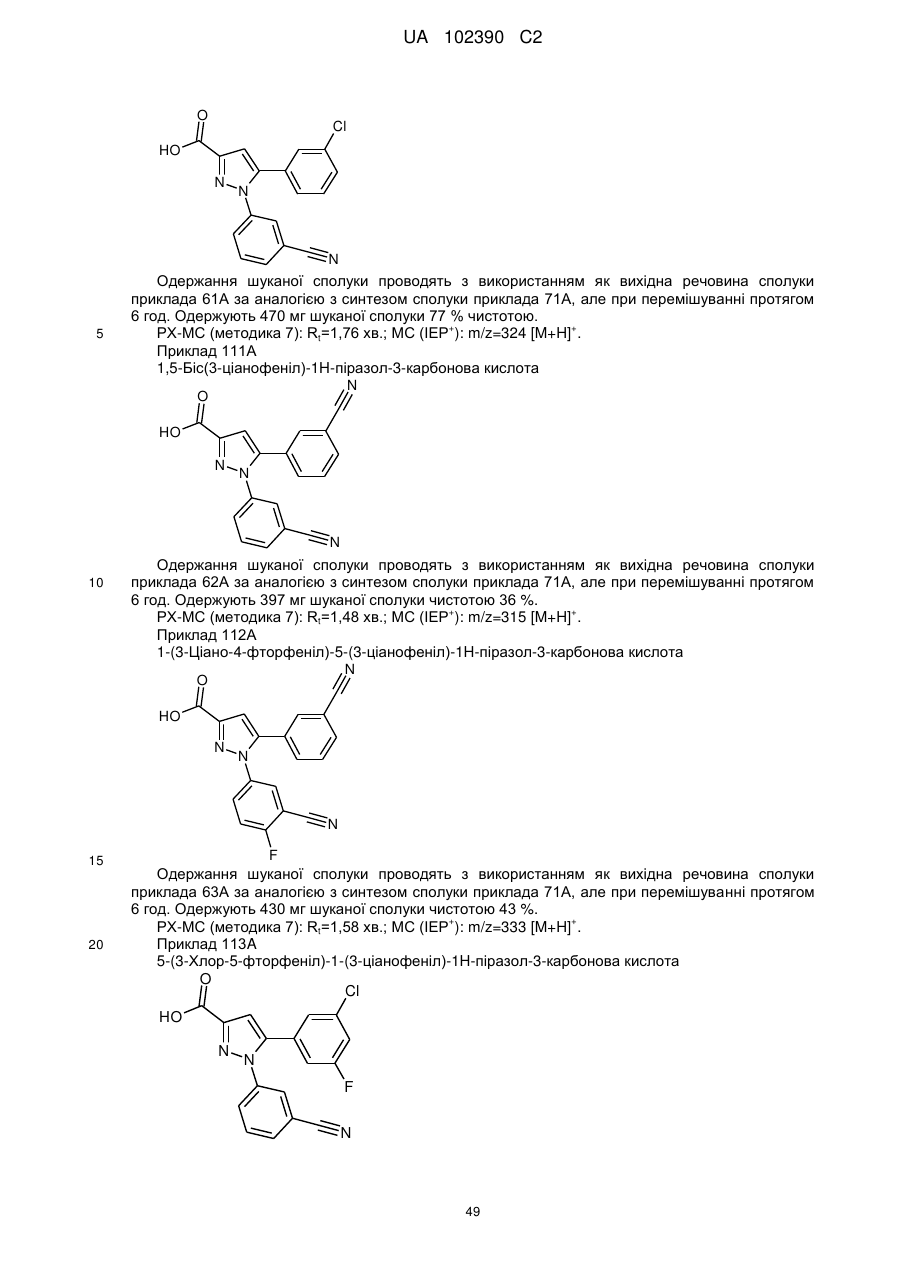
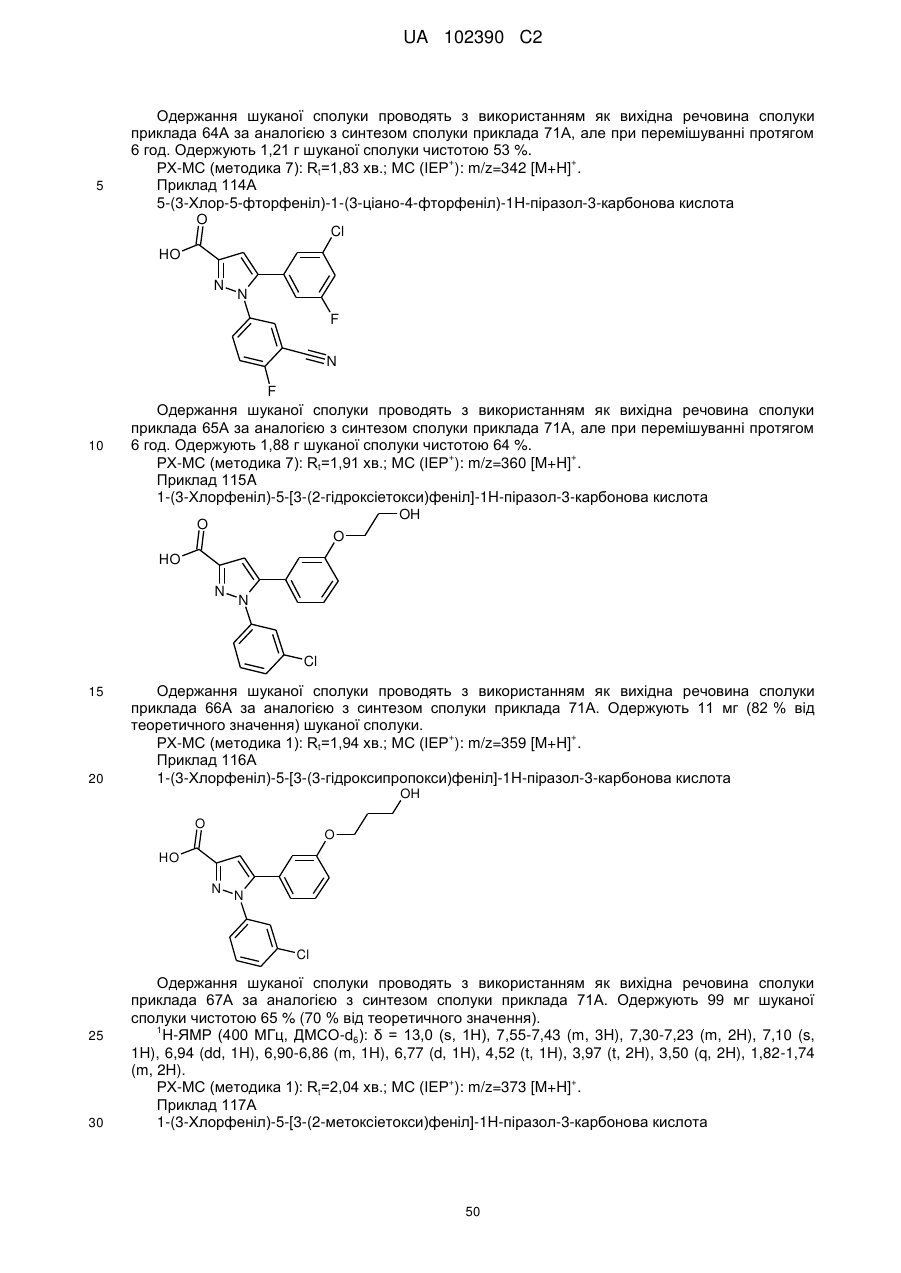
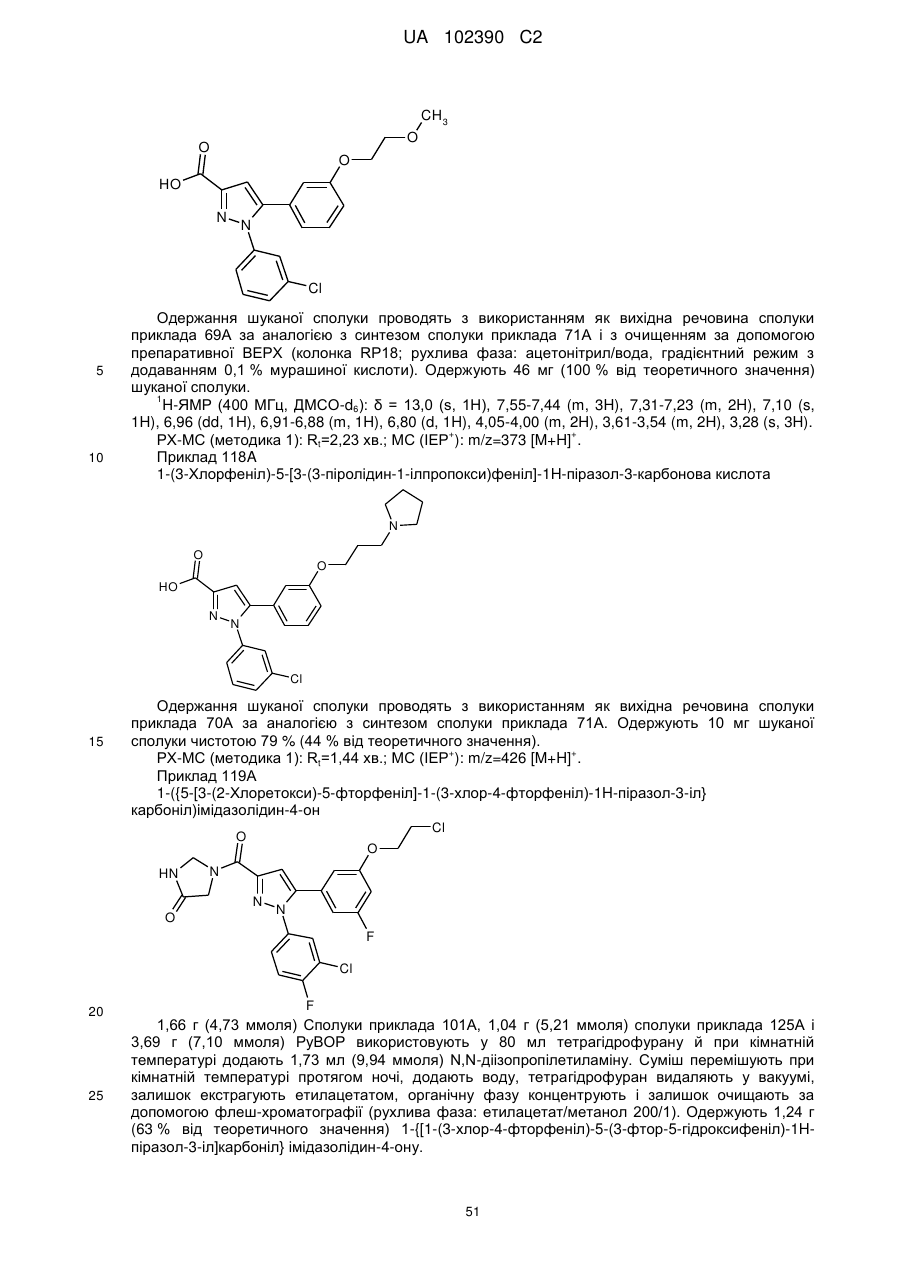
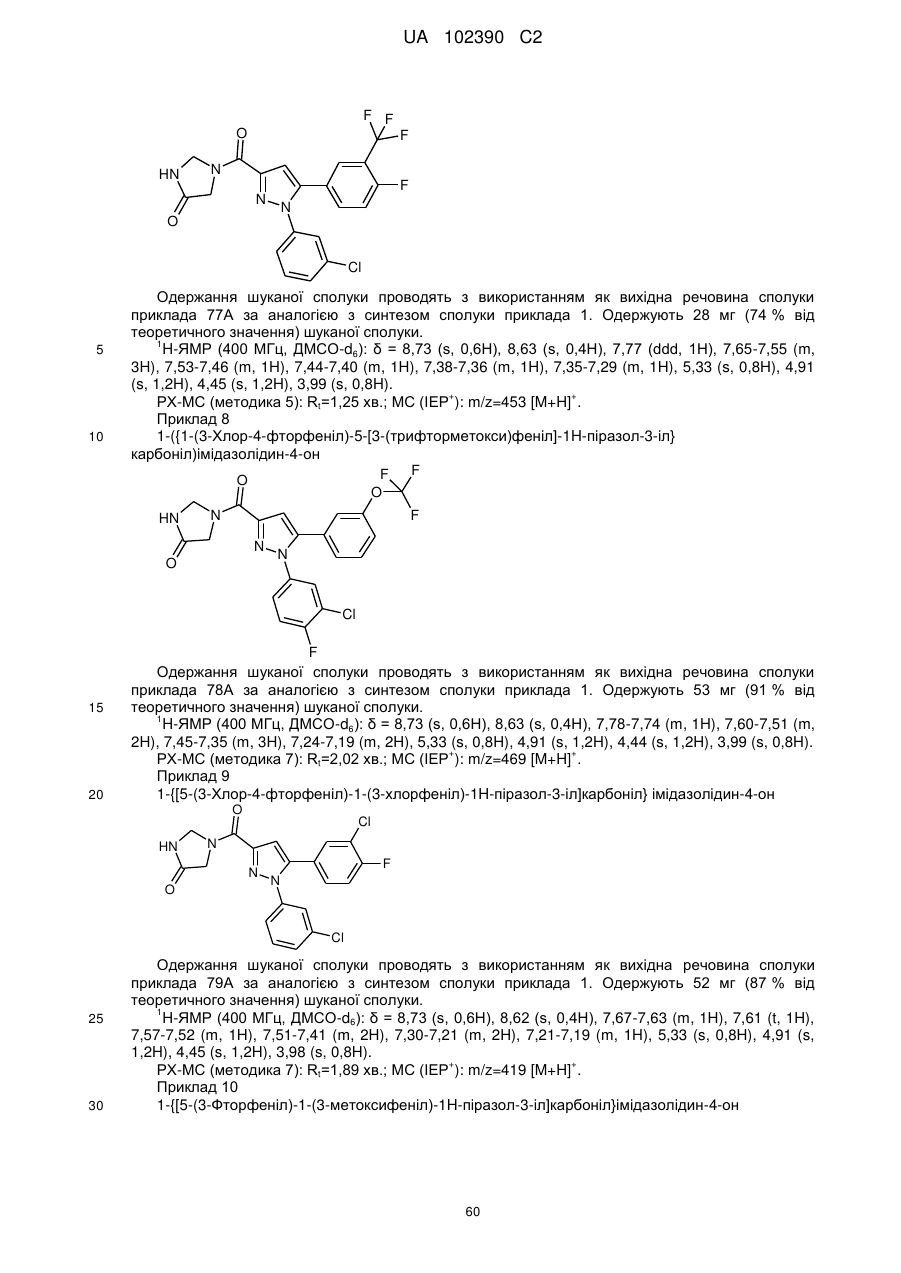
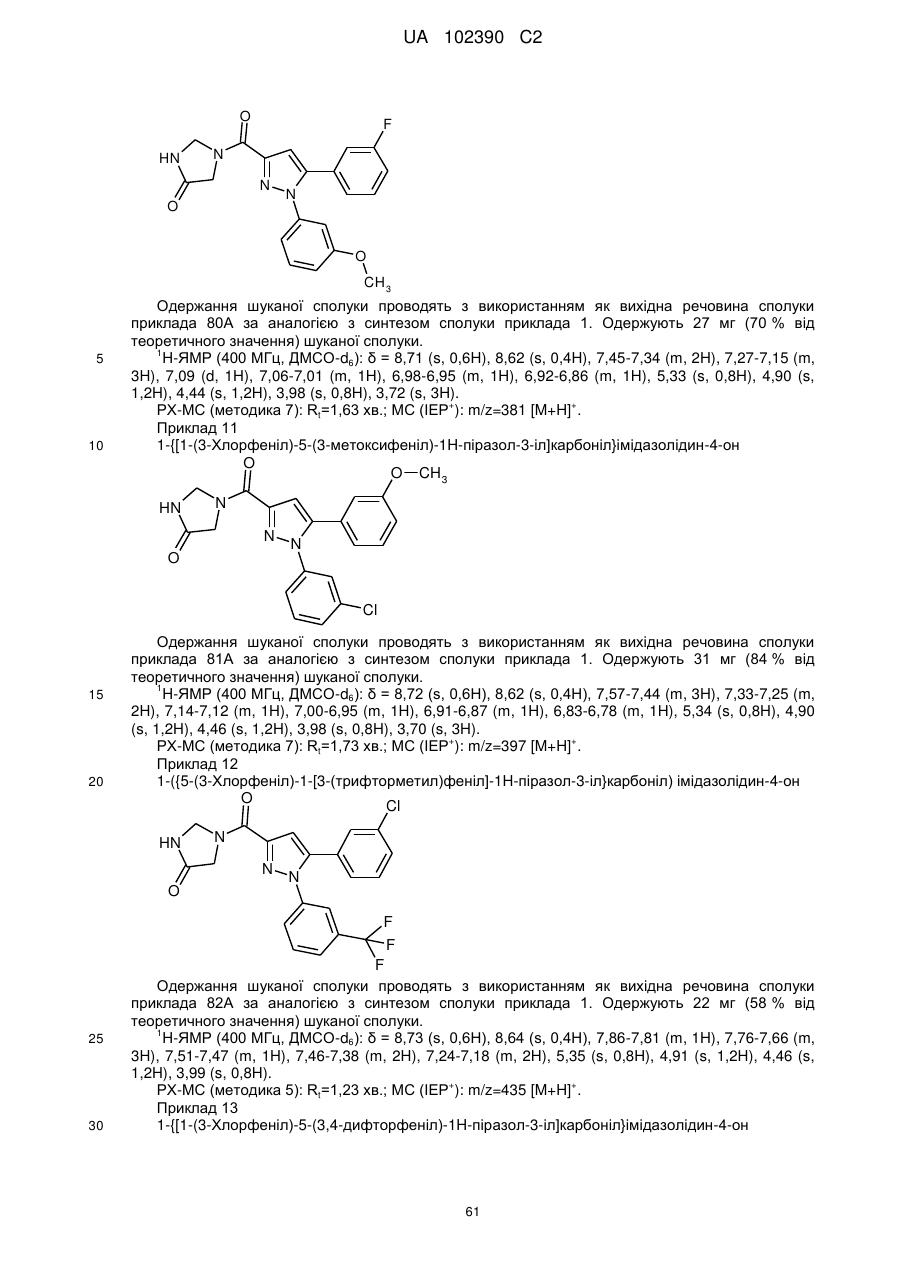
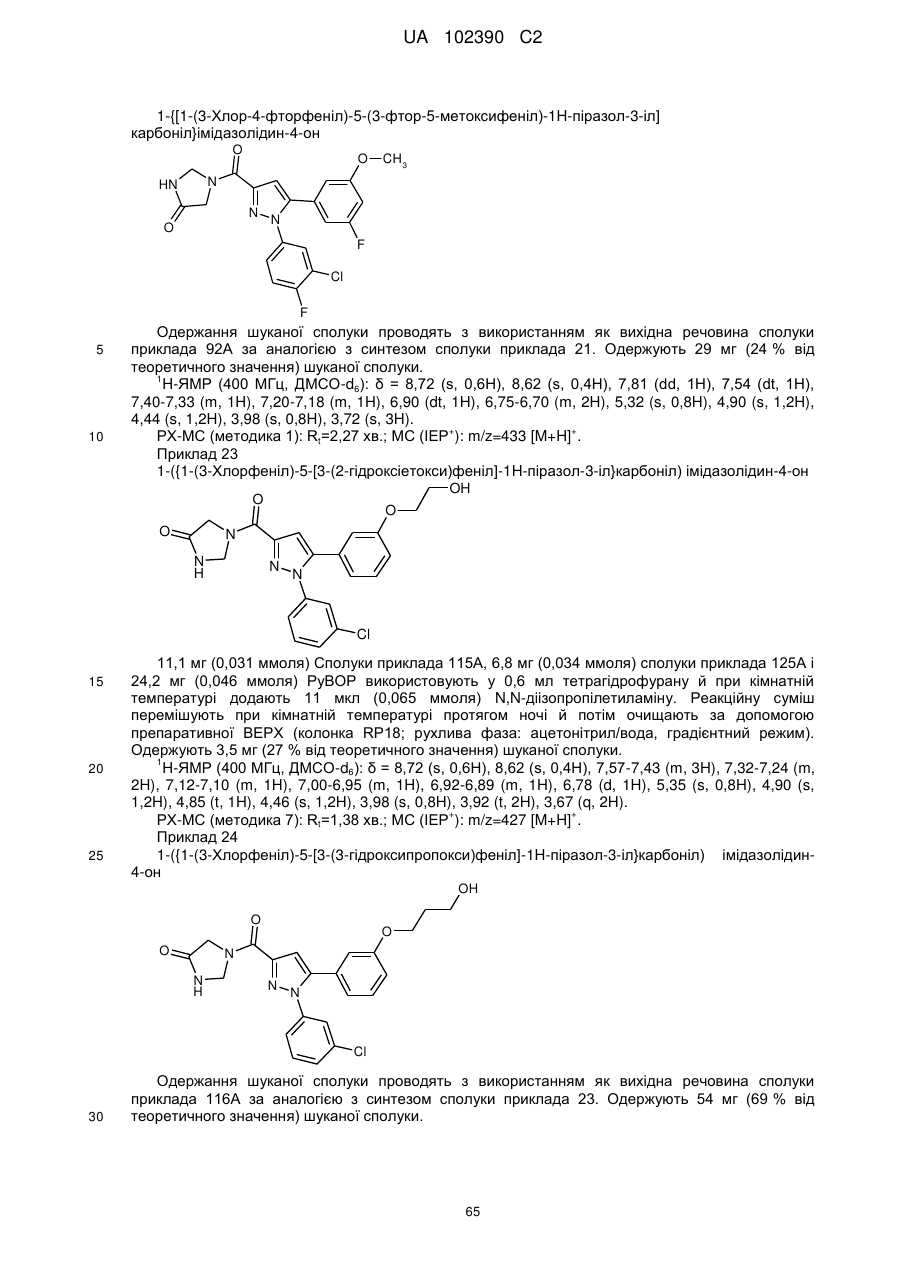
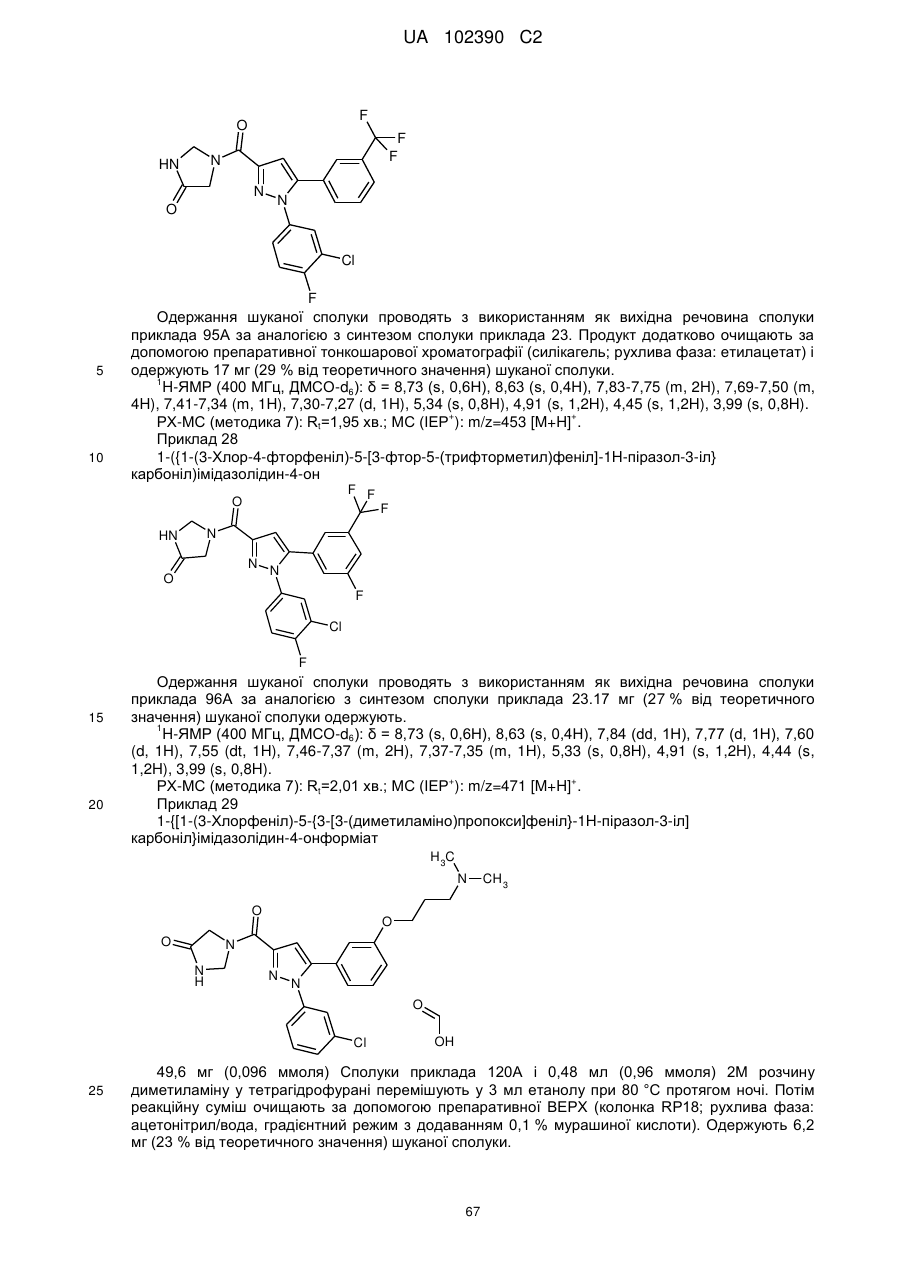
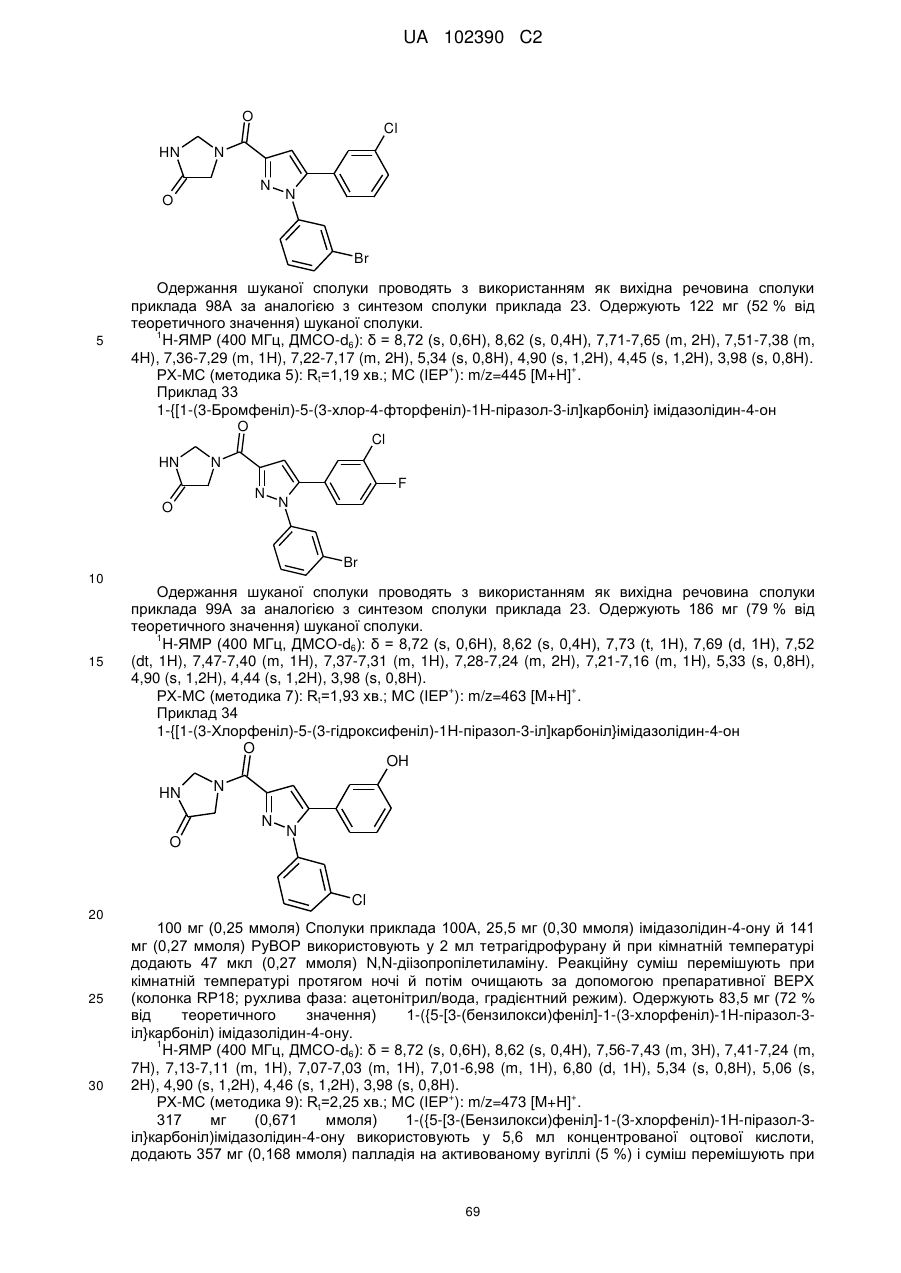
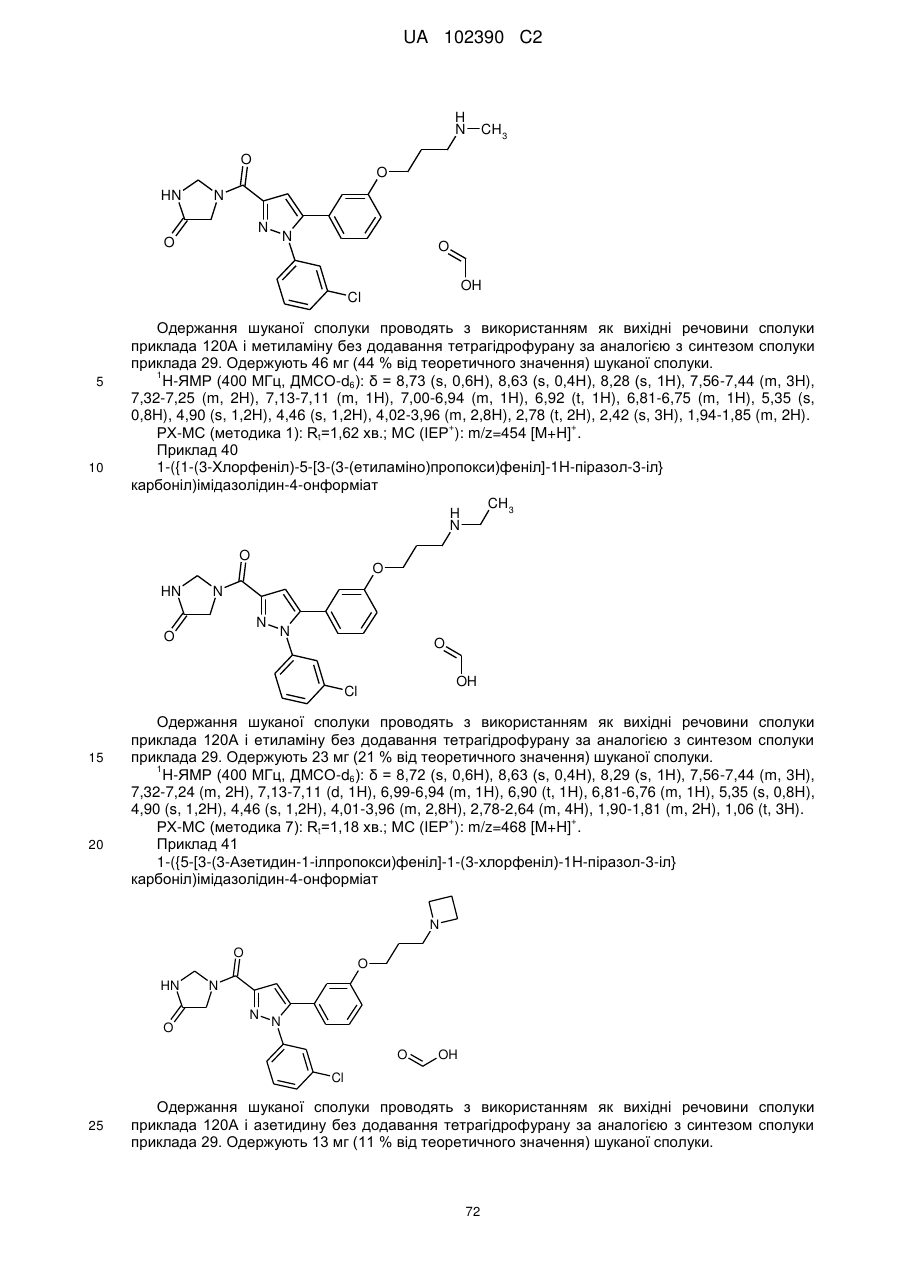
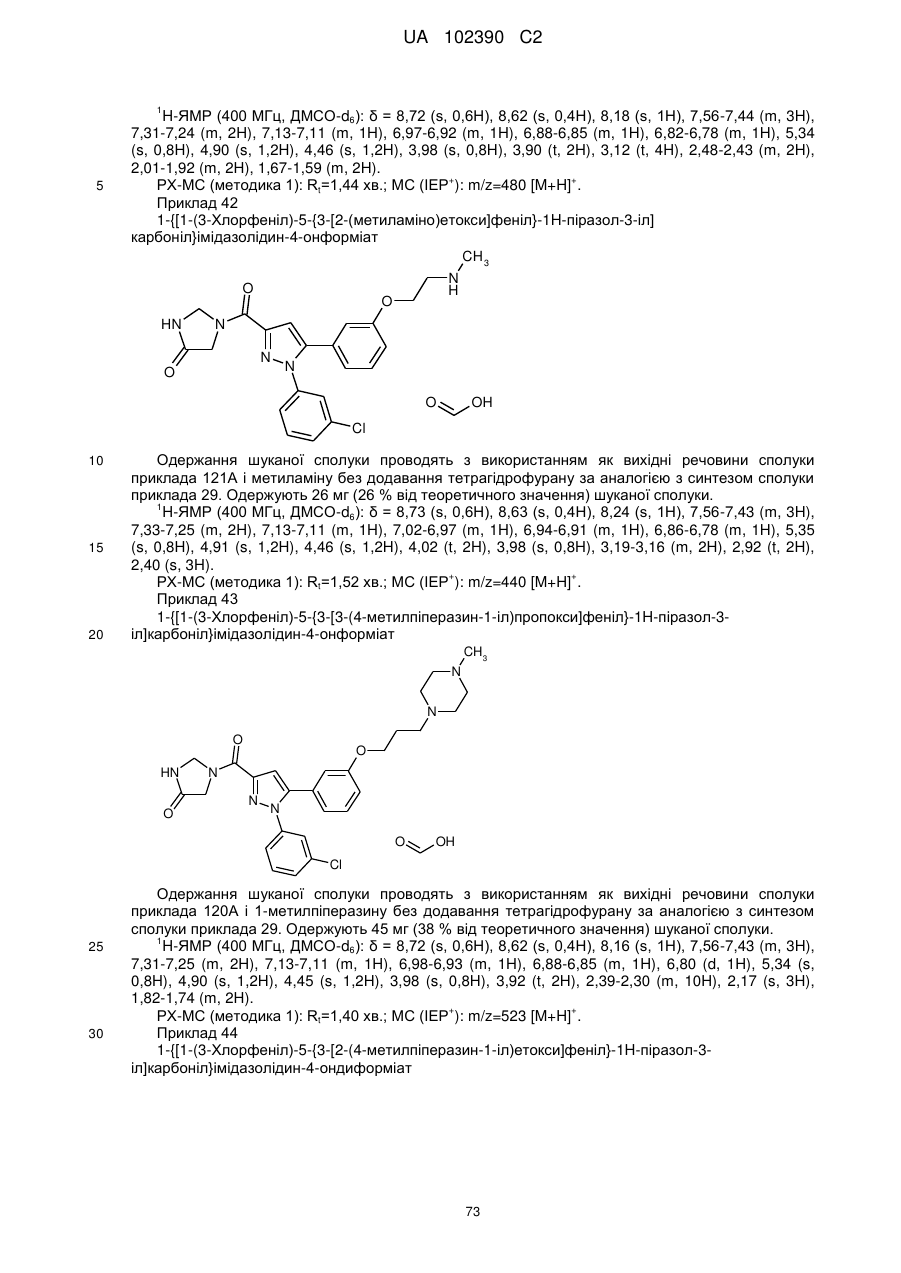
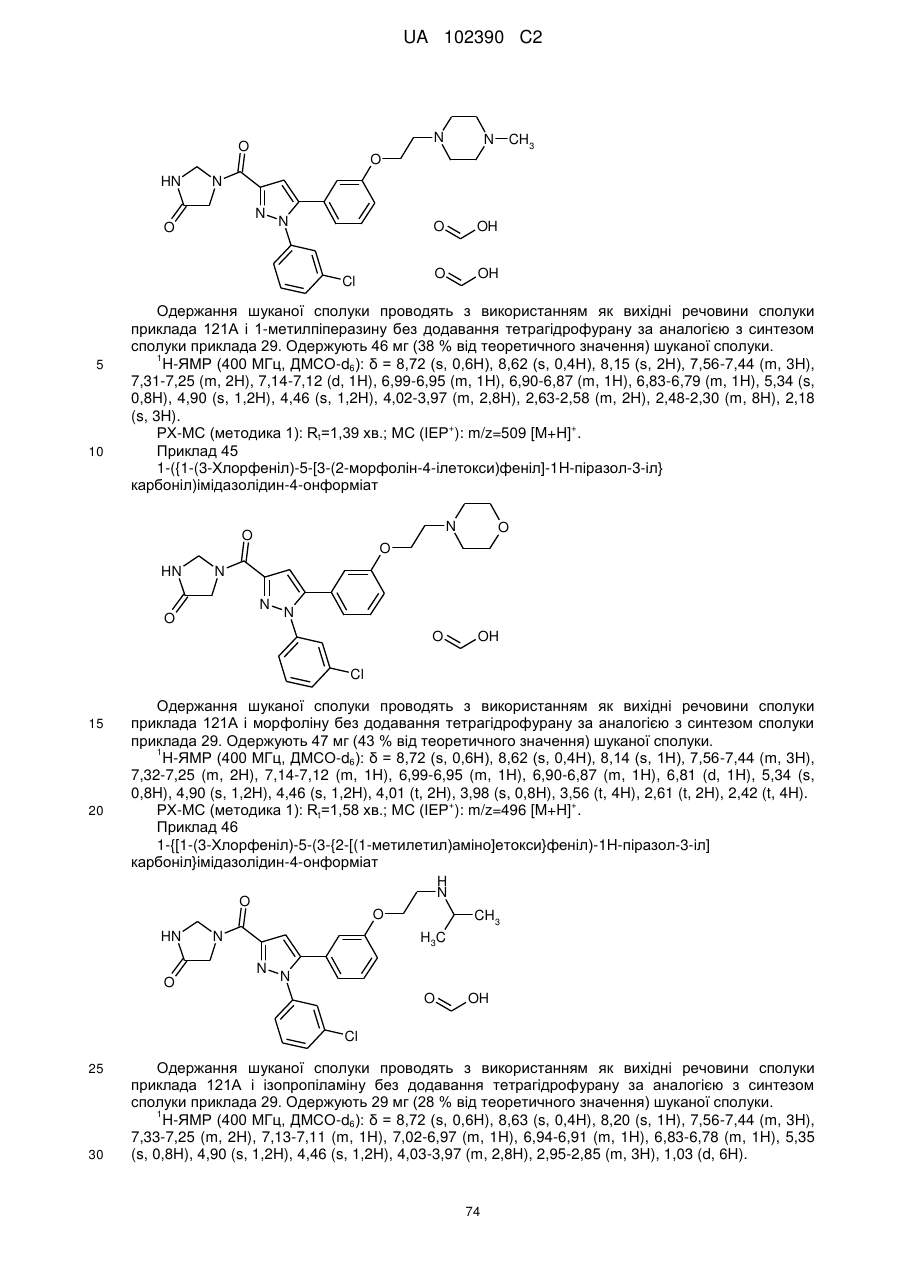
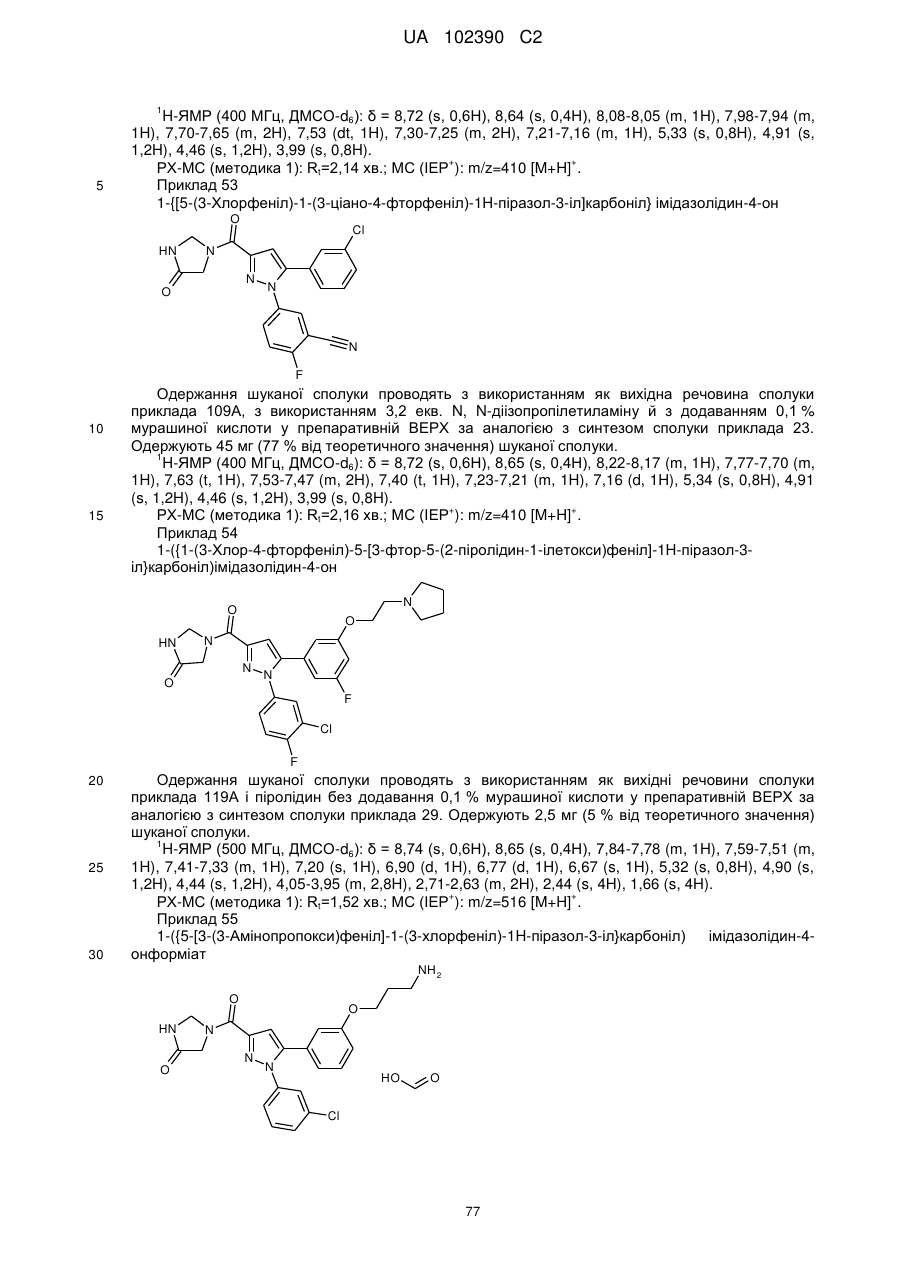
1. Сполука формули
 , (I)
, (I)
у якій
R1 означає феніл,
де феніл містить від 1 до 3 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (С1-С4)-алкіл і (С1-С4)-алкоксигрупу,
де
(С1-С4)-алкіл і (С1-С4)-алкоксигрупа, у свою чергу, можуть бути заміщені 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (С1-С4)-алкоксигрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу, ді-(С1-С4)-алкіламіногрупу, (С3-С7)-циклоалкіл і 4-7-членний гетероцикліл,
де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, всі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (С1-С4)-алкіл, трифторметил, гідроксигрупу, (С1-С4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу й ді-(С1-С4)-алкіламіногрупу,
R2 означає феніл,
де феніл містить від 1 до 3 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (С1-С4)-алкіл і (С1-С4)-алкоксигрупу,
де
(С1-С4)-алкіл і (С1-С4)-алкоксигрупа, у свою чергу, можуть бути заміщені 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (С1-С4)-алкоксигрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу, ді-(С1-С4)-алкіламіногрупу, (С3-С7)-циклоалкіл і 4-7-членний гетероцикліл,
де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, всі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (С1-С4)-алкіл, трифторметил, гідроксигрупу, (С1-С4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу й ді-(С1-С4)-алкіламіногрупу,
або одна з її солей, її сольватів або сольватів її солей.
2. Сполука за п. 1, яка відрізняється тим, що
R1 означає феніл,
де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (С1-С4)-алкіл і (С1-С4)-алкоксигрупу,
R2 означає феніл,
де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметоксигрупу, трифторметилтіогрупу, (С1-С4)-алкіл і (С1-С4)-алкоксигрупу,
де
(С1-С4)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (С1-С4)-алкоксигрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу, ді-(С1-С4)-алкіламіногрупу, (С3-С7)-циклоалкіл і 4-7-членний гетероцикліл,
де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, всі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (С1-С4)-алкіл, трифторметил, гідроксигрупу, (С1-С4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу й ді-(С1-С4)-алкіламіногрупу,
або одна з її солей, її сольватів або сольватів її солей.
3. Сполука за п. 1 або п. 2, яка відрізняється тим, що
R1 означає феніл,
де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, ціаногрупу, трифторметил і метоксигрупу,
R2 означає феніл,
де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, ціаногрупу, трифторметоксигрупу, метил і (С1-С3)-алкоксигрупу,
де
(С1-С3)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає гідроксигрупу, (С1-С4)-алкоксигрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу, ді(С1-С4)-алкіламіногрупу й 4-7-членний гетероцикліл,
де зазначені останніми гетероциклільні радикали, у свою чергу, всі можуть бути заміщені (С1-С4)-алкілом,
або одна з її солей, її сольватів або сольватів її солей.
4. Сполука за будь-яким із пп. 1-3, яка відрізняється тим, що
R1 означає феніл,
де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, ціаногрупу, трифторметил і метоксигрупу,
R2 означає феніл,
де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, ціаногрупу, трифторметоксигрупу, метил і метоксигрупу,
або одна з її солей, її сольватів або сольватів її солей.
5. Сполука за будь-яким із пп. 1-4, яка відрізняється тим, що
R1 означає феніл,
де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген і ціаногрупу,
R2 означає феніл,
де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген і ціаногрупу,
або одна з її солей, її сольватів або сольватів її солей.
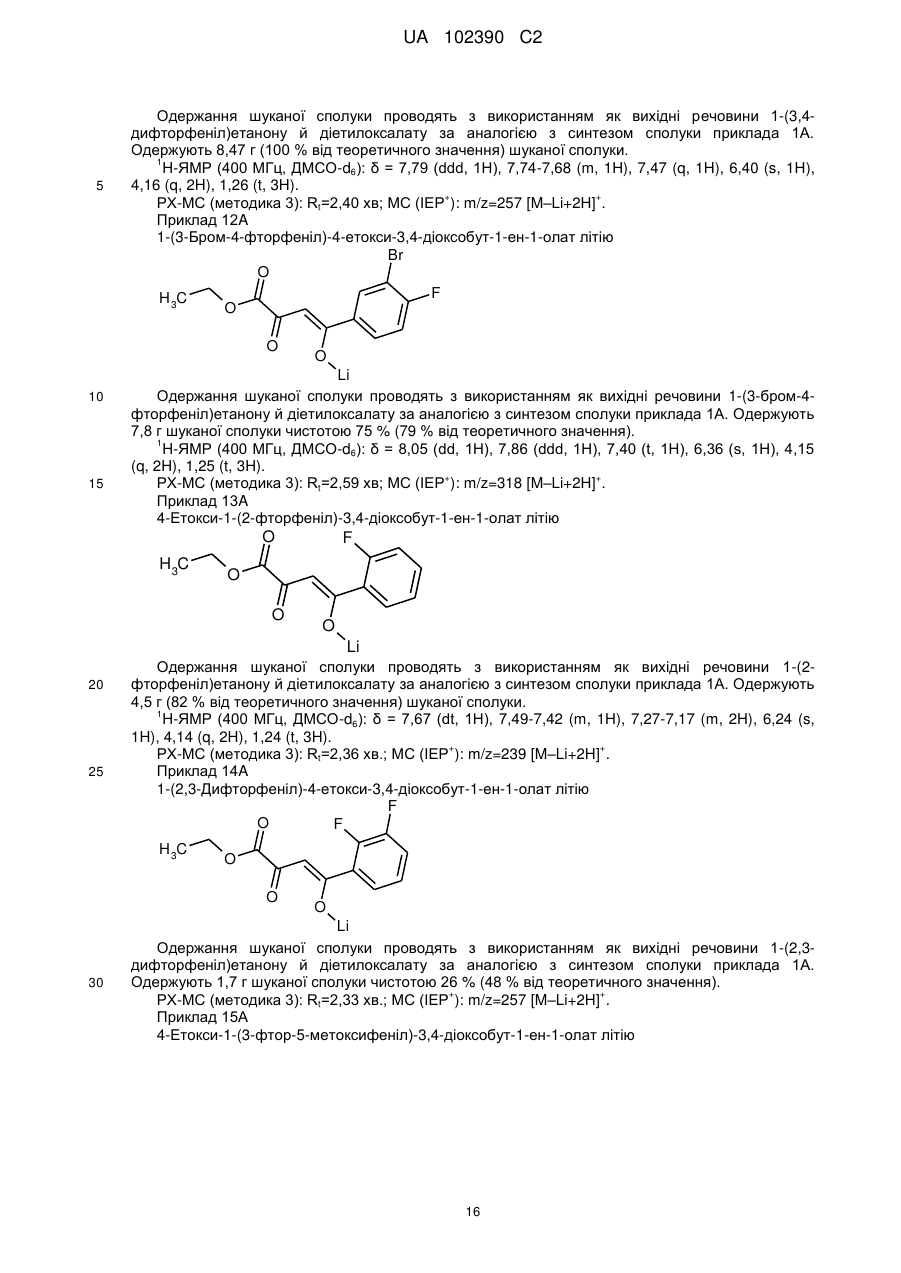
6. Сполука за п. 1, яка відрізняється тим, що вона описується формулою
 , (Ia)
, (Ia)
у якій
R3 означає водень, галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (С1-С4)-алкіл або (С1-С4)-алкоксигрупу,
R4 означає водень або галоген,
R5 означає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (С1-С4)-алкіл або (С1-С4)-алкоксигрупу,
де
(С1-С4)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (С1-С4)-алкоксигрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу, ді-(С1-С4)-алкіламіногрупу, (С3-С7)-циклоалкіл і 4-7-членний гетероцикліл,
де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, всі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (С1-С4)-алкіл, трифторметил, гідроксигрупу, (С1-С4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу й ді-(С1-С4)-алкіламіногрупу,
R6 означає водень або галоген,
або одна з її солей, її сольватів або сольватів її солей.
7. Сполука за п. 6, яка відрізняється тим, що
R3 означає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (С1-С4)-алкіл або (С1-С4)-алкоксигрупу,
R4 означає водень або галоген,
R5 означає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметоксигрупу, трифторметилтіогрупу, (С1-С4)-алкіл або (С1-С4)-алкоксигрупу,
де
(С1-С4)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (С1-С4)-алкоксигрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу, ді-(С1-С4)-алкіламіногрупу, (С3-С7)-циклоалкіл і 4-7-членний гетероцикліл,
де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, всі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (С1-С4)-алкіл, трифторметил, гідроксигрупу, (С1-С4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу й ді-(С1-С4)-алкіламіногрупу,
R6 означає водень або галоген,
або одна з її солей, її сольватів або сольватів її солей.
8. Сполука за п. 6 або п. 7, яка відрізняється тим, що
R3 означає галоген, ціаногрупу, трифторметил або метоксигрупу,
R4 означає водень або галоген,
R5 означає галоген, ціаногрупу, трифторметоксигрупу, метил або (С1-С3)-алкоксигрупу,
де
(С1-С3)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає гідроксигрупу, (C1-С4)-алкоксигрупу, аміногрупу, моно-(С1-С4)-алкіламіногрупу, ді-(С1-С4)-алкіламіногрупу й 4-7-членний гетероцикліл,
де зазначені останніми гетероциклільні радикали, у свою чергу, всі можуть бути заміщені (С1-С4)-алкілом,
R6 означає водень або галоген,
або одна з її солей, її сольватів або сольватів її солей.
9. Сполука за будь-яким із пп. 6-8, яка відрізняється тим, що
R3 означає галоген, ціаногрупу, трифторметил або метоксигрупу,
R4 означає водень, хлор або фтор,
R5 означає галоген, ціаногрупу, трифторметоксигрупу, метил або метоксигрупу,
R6 означає водень, хлор або фтор,
або одна з її солей, її сольватів або сольватів її солей.
10. Сполука за будь-яким із пп. 6-9, яка відрізняється тим, що
R3 означає галоген або ціаногрупу,
R4 означає водень або фтор,
R5 означає галоген або ціаногрупу,
R6 означає водень або фтор,
або одна з її солей, її сольватів або сольватів її солей.
11. Сполука за будь-яким із пп. 6-10, яка відрізняється тим, що
R3 означає хлор або ціаногрупу,
R4 означає фтор,
R5 означає хлор або ціаногрупу,
R6 означає фтор,
або одна з її солей, її сольватів або сольватів її солей.
12. Сполука за будь-яким із пп. 6-10, яка відрізняється тим, що
R3 означає хлор або ціаногрупу,
R4 означає фтор,
R5 означає хлор або ціаногрупу,
R6 означає водень,
або одна з її солей, її сольватів або сольватів її солей.
13. Сполука за будь-яким із пп. 6-10, яка відрізняється тим, що
R3 означає хлор або ціаногрупу,
R4 означає водень,
R5 означає хлор або ціаногрупу,
R6 означає водень,
або одна з її солей, її сольватів або сольватів її солей.
14. Сполука за будь-яким із пп. 6-10, яка відрізняється тим, що
R3 означає хлор або ціаногрупу,
R4 означає водень,
R5 означає хлор або ціаногрупу,
R6 означає фтор,
або одна з її солей, її сольватів або сольватів її солей.
15. Сполука за п. 6, яка відрізняється тим, що
R3 означає галоген, ціаногрупу, трифторметил або метоксигрупу,
R4 означає водень або галоген,
R5 означає трифторметил,
R6 означає фтор,
або одна з її солей, її сольватів або сольватів її солей.
16. Сполука за п. 6, яка відрізняється тим, що R3 означає водень,
R4 означає фтор або хлор,
R5 означає галоген, ціаногрупу, трифторметоксигрупу, метил або метоксигрупу,
R6 означає водень або галоген,
або одна з її солей, її сольватів або сольватів її солей.
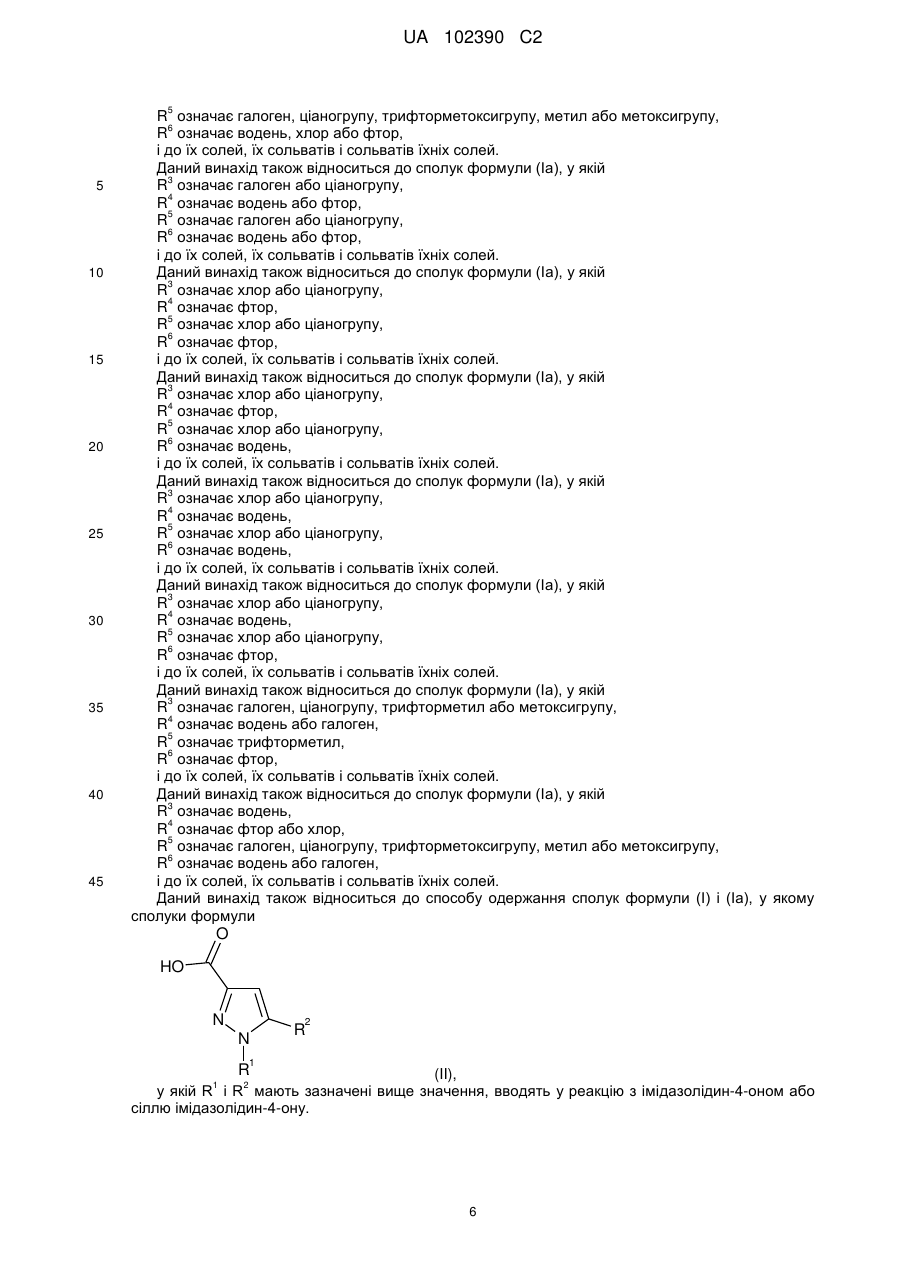
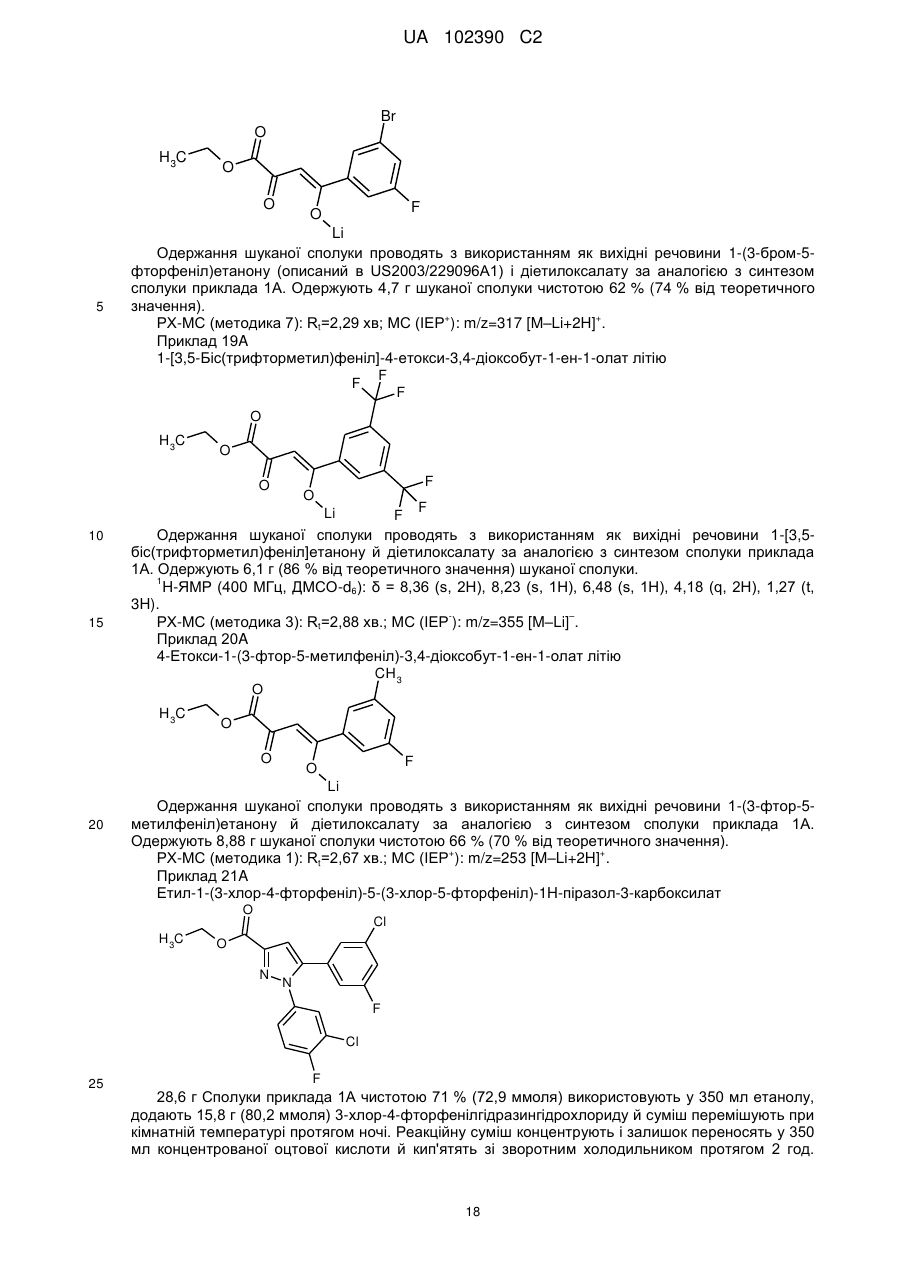
17. Спосіб одержання сполуки формули (І) за п. 1, у якому сполуку формули
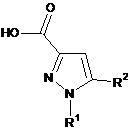 , (II)
, (II)
у якій R1 і R2 мають значення, зазначені у п. 1,
вводять у реакцію з імідазолідин-4-оном або сіллю імідазолідин-4-ону.
18. Сполука за будь-яким із пп. 1-16, призначена для лікування й/або профілактики захворювань.
19. Застосування сполуки за будь-яким із пп. 1-16 для готування лікарського засобу, призначеного для лікування й/або профілактики захворювань.
20. Застосування сполуки за будь-яким із пп. 1-6 для готування лікарського засобу, призначеного для лікування й/або профілактики ретровірусних захворювань.
21. Застосування за п. 20, яке відрізняється тим, що ретровірусне захворювання являє собою інфекцію вірусу НІ (імунодефіциту людини).
22. Лікарський засіб, що містить щонайменше одну сполуку за будь-яким із пп. 1-16 у комбінації щонайменше з одним іншим активним інгредієнтом.
23. Лікарський засіб, що містить щонайменше одну сполуку за будь-яким із пп. 1-16 у комбінації щонайменше з одним інертним, нетоксичним фармацевтично прийнятним наповнювачем.
24. Лікарський засіб за п. 22 або п. 23, призначений для лікування й/або профілактики ретровірусних захворювань.
25. Лікарський засіб за п. 24, який відрізняється тим, що ретровірусне захворювання являє собою інфекцію вірусу НІ (імунодефіциту людини).
26. Спосіб боротьби з вірусними захворюваннями у людей і тварин шляхом введення щонайменше однієї сполуки за будь-яким із пп. 1-16 або лікарського засобу за будь-яким із пп. 22-25 у противірусно ефективній кількості.
Текст
Реферат: Даний винахід стосується нових заміщених (піразолілкарбоніл)імідазолідинонів, способів їх одержання, їх застосування для лікування й/або профілактики захворювань, а також їх застосування для готування лікарських засобів, призначених для лікування й/або профілактики захворювань, переважно ретровірусних захворювань, у людей і/або тварин. O HN O N N R N R 2 1 (I) UA 102390 C2 (12) UA 102390 C2 O HN O N N R N R 2 1 (I) UA 102390 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід відноситься до нових заміщених (піразолілкарбоніл) імідазолідинонів, способів їх одержання, до їх застосування для лікування й/або профілактики захворювань, а також до їх застосування для готування лікарських засобів, призначених для лікування й/або профілактики захворювань, переважно ретровірусних захворювань у людей і/або тварин. HIV (ВІЛ - вірус імунодефіциту людини) приводить до хронічного стійкого прогресуючого інфекційного захворювання. Це захворювання протікає через різні стадії від безсимптомної інфекції до патологічного стану СНІД (синдром набутого імунодефіциту). СНІД є кінцевою стадією захворювання, викликаного інфекцією. Захворювання ВІЛ/СНІД характеризується тривалим клінічним латентним періодом зі стійкою вірусемією, яка на кінцевій стадії приводить до недостатнього імунного захисту. Розробка комбінованої анти-ВІЛ терапії уможливила у 1990-х рр. ефективне вповільнення прогресування захворювання й тим самим значне збільшення середньої тривалості життя ВІЛінфікованих пацієнтів (Palella et al., N. Engl. J. Med. 1998, 238, 853-860). Анти-ВІЛ речовини, наявні у цей час у продажу, придушують реплікацію ВІЛ шляхом інгібування головних ферментів вірусу - зворотної транскриптази (RT), протеази або інтегрази, або входу ВІЛ у клітину-мішень (див. огляд Flexner, Nature Reviews Drug Discovery 2007, 6, 959966). Існують два класи інгібіторів RT: нуклеозидні й нуклеотидні інгібітори RT (NRTI) діють за допомогою конкурентного інгібування або обриву ланцюга при полімеризації ДНК. Ненуклеозидні інгібітори RT (NNRTI) аллостерично зв'язуються з гідрофобною кишенею поблизу від активного центра RT і приводить до зміни конформації ферменту. Наявні у цей час інгібітори протеази (PI) блокують активні центри вірусної протеази й тим самим запобігають дозрівання часток, що знову утворилися, в інфікуючі віріони. Єдиний затверджений до застосування у цей час інгібітор інтегрази, ралтегравір, зв'язується з активним центром інтегрази ВІЛ і попереджає вбудовування провірусної ДНК у геном клітини-мішені. Інгібітори входу (інгібітори злиття й антагоністи співрецепторів) попереджають інфікування клітин за допомогою ВІЛ шляхом взаємодії з білком оболонки ВІЛ або шляхом блокування клітинних співрецепторів CCR5 або CXCR4. Оскільки монотерапія з використанням наявних у цей час анти-ВІЛ лікарських засобів через дуже нетривалий час стає неефективною внаслідок селекції резистентних вірусів, звичайно використовують комбіновану терапію зі застосуванням різних анти-ВІЛ речовин різних класів (високоактивна антиретровірусна терапія = HAART; Carpenter et al., J. Am. Med. Assoc. 2000, 283, 381-390). Незважаючи на успіхи антиретровірусної хіміотерапії недавні дослідження показали, що з використанням наявних лікарських засобів не слід очікувати знищення ВІЛ і пов'язаного з ним вилікування від інфікування за допомогою ВІЛ. Латентний вірус залишається у "дрімаючих" лімфоцитах і являє собою резервуар для реактивації й тим самим відновленого поширення вірусу (Finzi et al., Nature Med. 1999, 5, 512-517; Ramratnam et al., Nature Med. 2000, 6, 82-85). Тому ВІЛ-інфіковані пацієнти довічно залежать від ефективної противірусної терапії. Незважаючи на використання комбінованої терапії через якийсь час відбувається селекція резистентних вірусів. Оскільки резистентні мутації, характерні для кожного класу лікарських засобів, накопичуються, припинення дії одного лікарського засобу часто приводить до припинення дії всього класу речовин. Ця проблема перехресної резистентності найбільшою мірою проявляється для класу NNRTI, оскільки у цьому випадку одна точкова мутація у RT часто може бути достатньою для припинення дії всіх NNRTI (див. огляд Kavlick & Mitsuya, Antiretroviral Chemotherapy (editor De Clercq E.), 2001, ASM Press, 279-312). Розвитку резистентності звичайно сприяє погане дотримання режиму лікування пацієнтами, що обумовлено несприятливим профілем побічних ефектів і складним режимом прийому антиВІЛ лікарських засобів. Настійно необхідні нові терапевтичні засоби боротьби з інфекцією ВІЛ. Сучасним завданням досліджень в області боротьби з ВІЛ є виявлення нових основних хімічних структур, які або впливають на нові мішені реплікації ВІЛ і/або ефективні стосовно кількості, що збільшується, резистентних клінічних ізолятів ВІЛ. В US5624941 і EP576357 описані піразоли як антагоністи канабіноїдного рецептора, в EP418845, EP554829 і WO04/050632, зокрема, для лікування запальних і тромботичних захворювань, у WO03/037274 як інгібітори натрієвих іонних каналів для усунення болю, у WO06/015860 в якості лігандів аденозинового рецептора для лікування запальних і обструктивних респіраторних захворювань, в EP1762568 і EP1591443 як інгібітори агрегації тромбоцитів, у WO07/002559 як модулятори активності ядерних рецепторів, у WO07/020388 і WO05/080343 як модулятори канабіноїдного рецептора, зокрема, для лікування ожиріння й психічних і неврологічних порушень, у WO07/009701 і EP1743637 для усунення факторів ризику 1 UA 102390 C2 5 серцево-судинних захворювань, у WO2005/002576 як інгібітори різних кіназ і у DE102004054666 для боротьби зі шкідливими рослинами або для регулювання росту рослин. Тому одним об'єктом даного винаходу є розробка нових сполук, що мають таку же або поліпшену противірусну активність, призначену для лікування вірусних інфекційних захворювань у людей і тварин, які позбавлені описаних вище недоліків. Відповідно до винаходу зненацька було встановлено, що заміщені (піразолілкарбоніл)імідазолідинони, описані у даному винаході, мають противірусну активність. Даний винахід відноситься до сполук формули O HN O N N 2 N R 1 (I), у якій 1 R означає феніл, де феніл містить від 1 до 3 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (C1-C4)-алкіл і (C1-C4)-алкоксигрупу, де (C1-C4)-алкіл і (C1-C4)-алкоксигрупа, у свою чергу, можуть бути заміщені 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (C 1-C4)алкоксигрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу, ді-(C1-C4)-алкіламіногрупу, (C3-C7)циклоалкіл і 4-7-членний гетероцикліл, де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, усі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (C 1-C4)-алкіл, трифторметил, гідроксигрупу, (C1-C4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу й ді-(C1-C4)-алкіламіногрупу, 2 R означає феніл, де феніл містить від 1 до 3 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (C1-C4)-алкіл і (C1-C4)-алкоксигрупу, де (C1-C4)-алкіл і (C1-C4)-алкоксигрупа, у свою чергу, можуть бути заміщені 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (C 1-C4)алкоксигрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу, ді-(C1-C4)-алкіламіногрупу, (C3-C7)циклоалкіл і 4-7-членний гетероцикліл, де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, усі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (C 1-C4)-алкіл, трифторметил, гідроксигрупу, (C1-C4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу й ді-(C1-C4)-алкіламіногрупу, і до їх солей, їх сольватів і сольватів їхніх солей. Сполуки, запропоновані у даному винаході, являють собою сполуки формули (I) та їх солі, сольвати й сольвати їхніх солей, а також сполуки, які описуються формулою (I) і зазначені нижче у даному винаході, як типові варіанти здійснення, та їх солі, сольвати й сольвати їхніх солей, якщо тільки сполуки, які описуються формулою (I) і зазначені нижче, уже не є солями, сольватами й сольватами солей. Сполуки, запропоновані у даному винаході, залежно від своєї структури можуть існувати у стереоізомерних формах (енантіомери, діастереоізомери). Тому даний винахід також відноситься до енантіомерів або діастереоізомерів і відповідних їхніх сумішей. Стереоізомерно однорідні компоненти можна виділити з таких сумішей енантіомерів і/або діастереоізомерів за відомими методиками. Якщо сполуки, запропоновані у даному винаході, можуть існувати у таутомерних формах, то даний винахід відноситься до всіх таутомерних форм. Солями, кращими для завдань даного винаходу, є фізіологічно прийнятні солі сполук, запропонованих у даному винаході. Однак в обсяг даного винаходу також включені солі, які самі по собі непридатні для використання у фармацевтиці, але які можна використовувати, наприклад, для виділення або очищення сполук, запропонованих у даному винаході, або змішаних солей. R 10 15 20 25 30 35 40 45 50 2 UA 102390 C2 5 10 15 20 25 30 35 40 45 50 55 60 Фізіологічно прийнятні солі сполук, запропонованих у даному винаході, включають солі приєднання з неорганічними кислотами, карбоновими кислотами й сульфоновими кислотами, наприклад, солі хлористоводневої кислоти, бромистоводневої кислоти, сірчаної кислоти, фосфорної кислоти, метансульфонової кислоти, етансульфонової кислоти, толуолсульфонової кислоти, бензолсульфонової кислоти, нафталінсульфонової кислоти, оцтової кислоти, трифтороцтової кислоти, пропіонової кислоти, молочної кислоти, винної кислоти, яблучної кислоти, лимонної кислоти, фумарової кислоти, малеїнової кислоти й бензойної кислоти. Фізіологічно прийнятні солі сполук, запропонованих у даному винаході, також включають солі звичайних основ, такі як, наприклад і переважно, солі лужних металів (наприклад, солі натрію й калію), солі лужноземельних металів (наприклад, солі кальцію й магнію) і солі амонію, отримані з аміаку або органічних амінів, що містять від 1 до 16 атомів C, таких як, наприклад і переважно, етиламін, діетиламін, триетиламін, етилдіізопропіламін, моноетаноламін, діетаноламін, триетаноламін, дихлоргексиламін, диметиламіноетанол, прокаїн, дибензиламін, N-метилморфолін, аргінін, лізин, етилендіамін і N-метилпіперидин. Сольвати для завдань даного винаходу означають такі форми сполук, запропонованих у даному винаході, які у твердому або рідкому стані утворюють комплекс шляхом координації з молекулами розчинника. Гідрати є особливою формою сольватів, у яких координація відбувається з водою. У контексті даного винаходу замісники, якщо не зазначене інше, мають наступні значення: Алкіл і алкільні фрагменти в алкоксигрупі й алкоксикарбонілі означають алкіл, що має лінійний або розгалужений ланцюг, і включають, якщо не зазначене інше, (C1-C6)-алкіл, переважно (C1-C4)-алкіл, такий як, наприклад, метил, етил, пропіл, ізопропіл, бутил, ізобутил, трет-бутил. Алкоксигрупа для завдань даного винаходу переважно означає алкоксильний радикал, що має лінійний або розгалужений ланцюг, який переважно містить від 1 до 6, від 1 до 4 або від 1 до 3 атомів вуглецю. Алкоксильний радикал, що має лінійний або розгалужений ланцюг, який містить від 1 до 3 атомів вуглецю є кращим. Як приклад і переважно можна відзначити: метоксигрупу, етоксигрупу, н-пропоксигрупу, ізопропоксигрупу, трет-бутоксигрупу, нпентоксигрупу й н-гексоксигрупу. Алкоксикарбоніл наприклад і переважно означає метоксикарбоніл, етоксикарбоніл, нпропоксикарбоніл, ізопропоксикарбоніл, трет-бутоксикарбоніл, н-пентоксикарбоніл і нгексоксикарбоніл. Гетероцикліл означає моноциклічний гетероциклічний радикал, що містить від 4 до 7, переважно від 5 до 6 кільцевих атомів і до 3, переважно до 2 гетероатомів і/або гетероатомних груп, вибраних із групи, що включає N, O, S, SO, SO2, де атом азоту також може утворювати Nоксид. Гетероцикл може бути насиченим або частково ненасиченим. Перевага віддається 5-7членним моноциклічним насиченим гетероциклам, що містять до 2 гетероатомів, вибраних із групи, яка включає O, N і S, наприклад і переважно 1,4-оксазепаніл, піролідин-1-іл, піролідин-2іл, піролідин-3-іл, тетрагідрофураніл, тетрагідротієніл, піраніл, 1,3-тіазолідиніл, піперидин-1-іл, піперидин-2-іл, піперидин-3-іл, піперидин-4-іл, тіопіраніл, морфолін-2-іл, морфолін-3-іл, морфолін-4-іл, тіоморфолін-2-іл, тіоморфолін-3-іл, тіоморфолін-4-іл, пергідроазепініл, піперазин-1-іл, піперазин-2-іл. Галоген означає фтор, хлор, бром або йод, і переважно фтор або хлор, якщо не зазначене інше. Моно-(C1-C4)-алкіламіногрупа для завдань даного винаходу означає аміногрупу, що містить алкільний замісник, який має лінійний або розгалужений ланцюг, що містить від 1 до 4 атомів вуглецю. Як приклад і переважно можна відзначити метиламіногрупу, етиламіногрупу, нпропіламіногрупу, ізопропіламіногрупу, н-бутиламіногрупу, трет-бутиламіногрупу, нпентиламіногрупу й н-гексиламіногрупу. Ді-(C1-C4)-алкіламіногрупа для завдань даного винаходу означає аміногрупу, що містить 2 однакових або різних алкільних замісника, що мають лінійний або розгалужений ланцюг, кожний з яких містить від 1 до 4 атомів вуглецю. Як приклад і переважно можна відзначити: N,Nдиметиламіногрупу, N,N-діетиламіногрупу, N-етил-N-метиламіногрупу, N-метил-N-нпропіламіногрупу, N-ізопропіл-N-н-пропіламіногрупу, N, N-діізопропіламіногрупу, N-н-бутил-Nметиламіногрупу, N-трет-бутил-N-метиламіногрупу, N-метил-N-н-пентиламіногрупу і N-н-гексилN-метиламіногрупу. Для завдань даного винаходу (C3-C7)-циклоалкіл означає моноциклічний насичений карбоцикл, що містить від 3 до 7 або від 3 до 6 кільцевих атомів вуглецю. Як приклад і переважно можна відзначити: циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил. 3 UA 102390 C2 5 10 15 20 25 30 35 40 45 50 55 Наведені вище визначення радикалів і зазначені загальні або кращі діапазони відносяться й до кінцевих продуктів формули (I) і відповідно до вихідних речовин і проміжних продуктів, необхідних для їхнього одержання у кожному випадку. Визначення радикалів, спеціально зазначені у відповідних комбінаціях або кращих комбінаціях радикалів, незалежно від конкретних зазначених комбінацій радикалів при необхідності також заміняються на визначення радикалів інших комбінацій. Даний винахід також відноситься до сполук формули (I), у якій 1 R означає феніл, де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (C1-C4)-алкіл і (C1-C4)-алкоксигрупу, 2 R означає феніл, де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметоксигрупу, трифторметилтіогрупу, (C1-C4)-алкіл і (C1-C4)-алкоксигрупу, де (C1-C4)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (C 1-C4)алкоксигрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу, ді-(C1-C4)-алкіламіногрупу, (C3-C7)циклоалкіл і 4-7-членний гетероцикліл, де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, усі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (C 1-C4)-алкіл, трифторметил, гідроксигрупу, (C1-C4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу й ді-(C1-C4)-алкіламіногрупу, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (I), у якій 1 R означає феніл, де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, ціаногрупу, трифторметил і метоксигрупу, 2 R означає феніл, де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, ціаногрупу, трифторметоксигрупу, метил і (C 1-C3)-алкоксигрупу, де (C1-C3)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає гідроксигрупу, (C 1-C4)-алкоксигрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу, ді-(C1-C4)-алкіламіногрупу й 4-7-членний гетероцикліл, де зазначені останніми гетероциклільні радикали, у свою чергу, усі можуть бути заміщені (C1-C4)-алкілом, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (I), у якій 1 R означає феніл, де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, ціаногрупу, трифторметил і метоксигрупу, 2 R означає феніл, де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген, ціаногрупу, трифторметоксигрупу, метил і метоксигрупу, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (I), у якій 1 R означає феніл, де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген і ціаногрупу, 2 R означає феніл, де феніл містить від 1 до 2 замісників, де замісники незалежно один від іншого вибрані з групи, що включає галоген і ціаногрупу, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули 4 UA 102390 C2 O HN O N R 5 N N R R R 5 10 15 20 25 30 35 40 45 6 3 4 (Ia), у якій 3 R означає водень, галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (C1-C4)-алкіл або (C1-C4)-алкоксигрупу, 4 R означає водень або галоген, 5 R означає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (C1-C4)-алкіл або (C1-C4)-алкоксигрупу, де (C1-C4)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (C 1-C4)алкоксигрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу, ді-(C1-C4)-алкіламіногрупу, (C3-C7)циклоалкіл і 4-7-членний гетероцикліл, де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, усі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (C 1-C4)-алкіл, трифторметил, гідроксигрупу, (C1-C4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу й ді-(C1-C4)-алкіламіногрупу, 6 R означає водень або галоген, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметил, трифторметоксигрупу, трифторметилтіогрупу, (C1-C4)-алкіл або (C1-C4)-алкоксигрупу, 4 R означає водень або галоген, 5 R означає галоген, гідроксигрупу, ціаногрупу, нітрогрупу, трифторметоксигрупу, трифторметилтіогрупу, (C1-C4)-алкіл або (C1-C4)-алкоксигрупу, де (C1-C4)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає галоген, ціаногрупу, гідроксигрупу, (C 1-C4)алкоксигрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу, ді-(C1-C4)-алкіламіногрупу, (C3-C7)циклоалкіл і 4-7-членний гетероцикліл, де зазначені останніми циклоалкільні й гетероциклільні радикали, у свою чергу, усі можуть містити до 3 однакових або різних наступних замісників: галоген, ціаногрупу, (C 1-C4)-алкіл, трифторметил, гідроксигрупу, (C1-C4)-алкоксигрупу, трифторметоксигрупу, оксогрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу й ді-(C1-C4)-алкіламіногрупу, 6 R означає водень або галоген, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає галоген, ціаногрупу, трифторметил або метоксигрупу, 4 R означає водень або галоген, 5 R означає галоген, ціаногрупу, трифторметоксигрупу, метил або (C 1-C3)-алкоксигрупу, де (C1-C3)-алкоксигрупа, у свою чергу, може бути заміщена 1-3 однаковими або різними радикалами, вибраними із групи, що включає гідроксигрупу, (C 1-C4)-алкоксигрупу, аміногрупу, моно-(C1-C4)-алкіламіногрупу, ді-(C1-C4)-алкіламіногрупу й 4-7-членний гетероцикліл, де зазначені останніми гетероциклільні радикали, у свою чергу, усі можуть бути заміщені (C1-C4)-алкілом, 6 R означає водень або галоген, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає галоген, ціаногрупу, трифторметил або метоксигрупу, 4 R означає водень, хлор або фтор, 5 UA 102390 C2 5 5 10 15 20 25 30 35 40 45 R означає галоген, ціаногрупу, трифторметоксигрупу, метил або метоксигрупу, 6 R означає водень, хлор або фтор, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає галоген або ціаногрупу, 4 R означає водень або фтор, 5 R означає галоген або ціаногрупу, 6 R означає водень або фтор, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає хлор або ціаногрупу, 4 R означає фтор, 5 R означає хлор або ціаногрупу, 6 R означає фтор, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає хлор або ціаногрупу, 4 R означає фтор, 5 R означає хлор або ціаногрупу, 6 R означає водень, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає хлор або ціаногрупу, 4 R означає водень, 5 R означає хлор або ціаногрупу, 6 R означає водень, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає хлор або ціаногрупу, 4 R означає водень, 5 R означає хлор або ціаногрупу, 6 R означає фтор, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає галоген, ціаногрупу, трифторметил або метоксигрупу, 4 R означає водень або галоген, 5 R означає трифторметил, 6 R означає фтор, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до сполук формули (Ia), у якій 3 R означає водень, 4 R означає фтор або хлор, 5 R означає галоген, ціаногрупу, трифторметоксигрупу, метил або метоксигрупу, 6 R означає водень або галоген, і до їх солей, їх сольватів і сольватів їхніх солей. Даний винахід також відноситься до способу одержання сполук формули (I) і (Ia), у якому сполуки формули O HO N 2 N R 1 R (II), 1 2 у якій R і R мають зазначені вище значення, вводять у реакцію з імідазолідин-4-оном або сіллю імідазолідин-4-ону. 6 UA 102390 C2 5 10 15 20 25 30 Реакцію звичайно проводять в інертних розчинниках у присутності дегідратуючого реагенту, якщо це доцільно, то у присутності основи, переважно при температурі у діапазоні від -30 до 50 °C при атмосферному тиску. Прикладами інертних розчинників є галогеновані вуглеводні, такі як дихлорметан або трихлорметан, вуглеводні, такі як бензол або толуол, нітрометан, тетрагідрофуран, 1,4-діоксан, диметилформамід або ацетонітрил. Також можна використовувати суміші цих розчинників. Дихлорметан, диметилформамід, тетрагідрофуран або толуол є особливо кращими. Прикладами основ є карбонати лужних металів, такі як, наприклад, карбонат і бікарбонат натрію або калію, або органічні основи, такі як триалкіламіни, наприклад, триетиламін, Nметилморфолін, N-метилпіперидин, 4-диметиламінопіридин або діізопропілетиламін. Прикладами придатних дегідратуючих реагентів у цьому контексті є карбодііміди, такі як, наприклад, N,N'-діетил-, N,N'-дипропіл-, N,N'-діізопропіл-, N,N'-дициклогексилкарбодіімід, N-(3диметиламіноізопропіл)-N'-етилкарбодіімідгідрохлорид (ЕДХ), N-циклогексилкарбодіімід-N„пропілоксиметилполістирол (ПС-карбодіімід) або карбонільні сполуки, такі як карбонілдіімідазол, або 1,2-оксазолієві сполуки, такі як 2-етил-5-феніл-1,2-оксазолій-3-сульфат або 2-трет-бутил-5метилізоксазолійперхлорат, або ациламінові сполуки, такі як 2-етоксі-1-етоксикарбоніл-1,2дигідрохінолін, або пропанфосфоновий ангідрид, або ізобутилхлорформіат, або біс(2-оксо-3оксазолідиніл)фосфорилхлорид, або O-(бензотриазол-1-іл)-N, N,N',N'тетраметилуронійгексафторфосфат (HBTU), 2-(2-оксо-1-(2H)-піридил)-1,1,3,3тетраметилуронійтетрафторборат (TPTU) або O-(7-азабензотриазол-1-іл)-N, N,N',N'тетраметилуронійгексафторфосфат (HATU), або 1-гідроксибензотриазол (HOBt), або бензотриазол-1-ілокситрис(диметиламіно) фосфонійгексафторфосфат (BOP), або бензотриазол-1-ілокситрис(піролідино) фосфонійгексафторфосфат (PyBOP), або Nгідроксисукцинімід, або їх суміші з основами. Конденсацію переважно проводять з використанням PyBOP, TBTU або з ЕДХ у присутності HOBt. В альтернативному способі сполуки формули (II) можна спочатку ввести у реакцію з тіонілхлоридом і на другій стадії з імідазолідин-4-оном або сіллю імідазолідин-4-ону у присутності основи, такої як, наприклад, триетиламін. Сполуки формули (I) і (Ia), отримані зазначеними вище способами, якщо це доцільно, містять захисні групи, які можна видалити при умовах, відомих фахівцеві у даній області техніки, і одержати інші сполуки формули (I) і (Ia). Сполуки формули (II) є відомими або їх можна одержати шляхом гідролізу складноефірної групи у сполуках формули O H3C O N 2 N R 1 R 35 40 45 50 (III), у якій 1 2 R і R мають зазначені вище значення, з основою. Гідроліз складного ефіру основою звичайно проводять в інертних розчинниках, переважно при температурі у діапазоні від кімнатної температури до температури кипіння розчинника при атмосферному тиску. Прикладами основ є гідроксиди лужних металів, такі як гідроксид літію, натрію або калію, або карбонати лужних металів, такі як карбонат цезію, натрію або калію, і кращими є гідроксид літію, калію або натрію. Прикладами інертних розчинників є галогеновані вуглеводні, такі як метиленхлорид, трихлорметан, тетрахлорметан, трихлоретан, тетрахлоретан, 1,2-дихлоретан або трихлоретилен, прості ефіри, такі як діетиловий ефір, метил-трет-бутиловий ефір, 1,2диметоксіетан, 1,4-діоксан, тетрагідрофуран, диметиловий ефір гліколю або диметиловий ефір діетиленгліколю, спирти, такі як метанол, етанол, н-пропанол, ізопропанол, н-бутанол або третбутанол, вуглеводні, такі як бензол, ксилол, толуол, гексан, циклогексан або фракції нафти, або інші розчинники, такі як диметилформамід, диметилацетамід, диметилсульфоксид, ацетонітрил або піридин, або вода, або суміші розчинників. Кращими розчинниками є 1,4-діоксан, 7 UA 102390 C2 тетрагідрофуран і/або метанол. Гідроксид літію у тетрагідрофурані- або суміші 1,4-діоксан-вода, або гідроксид калію у метанолі є кращими. Сполуки формули (III) є відомими або їх можна одержати за реакцією на першій стадії сполук формули O 2 R O H3 C O 5 10 15 20 25 O Li (IV), у якій R має значення, зазначені вище, зі сполуками формули 1 R -NH-NH2(V), або сіллю сполук формули (V), 1 у якій R має значення, зазначені вище, і на другій стадії нагрівання в оцтовій кислоті. Реакцію на першій стадії звичайно проводять в інертних розчинниках, переважно при температурі у діапазоні від кімнатної температури до температури кипіння розчинника при атмосферному тиску. Прикладами інертних розчинників є спирти, такі як метанол, етанол, н-пропанол, ізопропанол, н-бутанол, трет-бутанол або 2-метоксіетанол, і кращим є етанол. Реакцію на другій стадії в оцтовій кислоті звичайно проводять при температурі у діапазоні від кімнатної температури до температури кипіння оцтової кислоти при атмосферному тиску. Реакцію також можна провести у метанолі, етанолі або діоксані при температурі у діапазоні від кімнатної температури до температури кипіння розчинників. Придатними є суміші метанолу, етанолу або діоксану з оцтовою кислотою в об'ємних співвідношеннях від 0,5/99,5 до 99,5/0,5. Також можна використовувати суміші метанолу, етанолу, діоксану або оцтової кислоти з іншими кислотами, такими як, наприклад, хлористоводнева кислота, метансульфонова кислота, птолуолсульфонова кислота, камфорсульфонова кислота або трифтороцтова кислота при зазначених умовах. Реакцію переважно проводять в оцтовій кислоті при кип'ятінні зі зворотним холодильником. Альтернативно, сполуки формули (III) можна одержати за реакцією сполук формули O 2 R H3 C 30 35 40 45 2 O O O (VI), 2 у якій R має значення, зазначені вище, зі сполуками формули (V). Реакцію звичайно проводять в інертних розчинниках, переважно при температурі у діапазоні від кімнатної температури до температури кипіння розчинника при атмосферному тиску, якщо це є придатним, то у присутності кислоти. Прикладами інертних розчинників є спирти, такі як метанол, етанол, н-пропанол, ізопропанол, н-бутанол, трет-бутанол або 2-метоксіетанол, або інші розчинники, такі як N,Nдиметилформамід, N,N-диметилацетамід або диметилсульфоксид. Якщо реакція протікає у присутності кислоти, то її можна додати до розчину реакційної суміші з самого початку або після спливу часу, рівного від 1 до 4 год., і в останньому випадку додавання кислоти розчин реакційної суміші, якщо це є придатним, нагрівають аж до температури кипіння розчинника. Кислотою є, наприклад, концентрована неорганічна кислота або концентрована карбонова кислота, така як, наприклад, концентрована хлористоводнева кислота, концентрована азотна кислота, концентрована сірчана кислота або концентрована оцтова кислота. Сполуки формул (IV), (V) і (VI) є відомими або їх можна синтезувати за відомими методиками з відповідних вихідних речовин. Одержання сполуки, запропоновані у даному винаході, як приклад можна проілюструвати наведеною нижче схемою синтезу. Схема синтезу: 8 UA 102390 C2 5 10 15 20 25 30 35 40 Сполуки, запропоновані у даному винаході, характеризуються сприятливим діапазоном фармакологічних характеристик, які було неможливо уявити. Тому вони придатні для застосування як лікарські засоби для лікування й/або профілактики захворювань у людей і тварин. Сполуки, запропоновані у даному винаході, зокрема, відрізняються сприятливим діапазоном антитеровірусних характеристик. Даний винахід також відноситься до застосування сполук, запропонованих у даному винаході, для лікування й/або профілактики захворювань, викликаних ретровірусами, переважно вірусами імунодефіциту людини. Даний винахід також відноситься до застосування сполук, запропонованих у даному винаході, для лікування й/або профілактики захворювань, переважно зазначених вище захворювань. Даний винахід також відноситься до застосування сполук, запропонованих у даному винаході, для готування лікарського засобу, призначеного для лікування й/або профілактики захворювань, переважно зазначених вище захворювань. Даний винахід також відноситься до способу лікування й/або профілактики захворювань, переважно зазначених вище захворювань, з використанням сполук, запропонованих у даному винаході, у терапевтично ефективній кількості. Прикладами випадків застосування у медицині, які можна відзначити, є: 1.) Лікування й профілактика ретровірусних інфекцій людини. 2.) Лікування й профілактика інфекцій і захворювань (СНІД), викликаних ВІЛ-1 (вірус імунодефіциту людини; раніше позначався, як HTLV III/LAV) і ВІЛ-2, і пов'язаних з ними стадій, таких як ARS (СНІД-асоційований комплекс) і LAS (лімфаденопатичний синдром), а також імунодефіциту й енцефалопатії, викликаної цим вірусом. 3.) Лікування інфекції ВІЛ, викликаної моно-, полі- або мультирезистентними вірусами імунодефіциту людини. Вираження "резистентні віруси імунодефіциту людини" означає, наприклад, віруси, що мають резистентність стосовно нуклеозидних інгібіторів (НІОТ), ненуклеозидних інгібіторів (NNRTI) або інгібіторів протеази (ІП) або віруси, що мають резистентність стосовно інших діючих речовин, наприклад, T20 (інгібітори злиття). 4.) Лікування або профілактика іншого стану носійності СНІД. 5.) Лікування або профілактика інфекції HTLV-I або HTLV-II. Прикладами випадків застосування у ветеринарії, які можна відзначити, є: Інфекції за допомогою a) вісна-Маеді (в овець і кіз) b) вірусу прогресивної пневмонії (PPV) (в овець і кіз) c) вірусу артроенцефаліту козлів (в овець і кіз) d) вірусу Zwoegerziekte (в овець) e) вірусу інфекційної анемії (коней) f) інфекції, викликані вірусом лейкозу кішок g) інфекції, викликані вірусом імунодефіциту кішок (FIV) h) інфекції, викликані вірусом імунодефіциту мавпи(SIV). 9 UA 102390 C2 5 10 15 20 25 30 35 40 45 50 55 Для випадків застосування у медицині перевага віддається розділам 2, 3 і 4, описаним вище. Ці речовини є особливо придатними для боротьби з вірусами імунодефіциту людини, що мають резистентність стосовно відомих ненуклеозидних інгібіторів зворотної транскриптази, таких як, наприклад, эфавіренц або невірапін. Даний винахід також відноситься до лікарських засобів, що включають щонайменше одну сполуку, запропоновану у даному винаході, і щонайменше один або більшу кількість інших активних інгредієнтів, переважно призначених для лікування й/або профілактики зазначених вище захворювань. Сполуки, запропоновані у даному винаході, особливо докладно описані вище у розділах 2, 3 і 4, також можна з успіхом використовувати як компоненти комбінованої терапії разом з одним або більшою кількістю інших сполук, які активні у цих випадках застосування. Ці сполуки, наприклад, можна використовувати у комбінації з ефективними дозами речовин, що мають противірусну активність, з урахуванням принципів дії, докладно описаних нижче: інгібітори протеази ВІЛ; прикладами, які можна відзначити, є: саквінавір, індинавір, ритонавір, нелфінавір, ампренавір, лопінавір, атазанавір, фосампренавір, типранавір, дарунавір; нуклеозидні, нуклеотидні й ненуклеозидні інгібітори зворотної транскриптази ВІЛ; прикладами, які можна відзначити, є: зидовудин, ламівудин, диданозин, залцитабін, ставудин, ламівудин, абакавір, тенофовір, адефовір, емтрицитабін, амдоксовір, априцитабін, рацивір, невірапін, делавірдин, ефавіренц, етравірин, рилпівірин, UK-453,061; інгібітори інтегрази ВІЛ, прикладами, які можна відзначити, є: ралтегравір, елвітегравір; інгібітори злиття ВІЛ; прикладом, який можна відзначити, є енфувіртид; інгібітори взаємодії CXCR4/CCR5/гp120; прикладами, які можна відзначити, є: маравирок, викривирок, INCB009471, AMD-070; інгібітори дозрівання поліпротеїнів; прикладом, який можна відзначити, є бевіримат. Цей вибір призначений для ілюстрації можливих комбінацій, але він не обмежується прикладами, докладно описаними у даному винаході. У принципі, будь-яку комбінацію сполук, запропонованих у даному винаході, з речовинами, що мають противірусну активність, варто вважати такою, що входить в обсяг даного винаходу. Сполуки, запропоновані у даному винаході, можуть діяти системно й/або місцево. Для забезпечення такого впливу їх можна вводити придатним шляхом, таким як, наприклад, пероральний, парентеральний, легеневий, назальний, сублінгвальний, лінгвальний, трансбуккальний, ректальний, шкірний, черезшкірний, кон'юнктивальний, вушний, або у вигляді імплантату або стента. При цих шляхах введення сполуки, запропоновані у даному винаході, можна вводити у придатних препаративних формах. Придатними для перорального введення є препаративні форми, які діють відповідно до попереднього рівня техніки й вивільняють сполуки, запропоновані у даному винаході, швидко й/або модифікованим чином і які містять сполуки, запропоновані у даному винаході, у кристалічній і/або аморфізованій і/або розчиненій формі, такі як, наприклад, таблетки (таблетки без покриття або з покриттям, наприклад, що мають покриття, стійкі до впливу шлункового соку, або які розчиняються з затримкою або нерозчинні й регулюють вивільнення сполук, запропонованих у даному винаході), таблетки або плівки/облатки, які швидко розпадаються у порожнині рота, плівки/ліофілізати, капсули (наприклад, капсули із твердого або м'якого желатину), таблетки, покриті цукром, гранули, пелети, порошки, емульсії, суспензії, аерозолі або розчини. Парентеральне ведення можна проводити з виключенням стадії усмоктування (наприклад, внутрішньовенно, внутрішньоартеріально, внутрішньокардіально, внутрішньохребтово або внутрішньопопереково) або з включенням стадії усмоктування (наприклад, внутрішньом'язово, підшкірно, внутрішньошкірно, нашкірно або внутрішньочеревинно). Препаративними формами, придатними для парентерального ведення, зокрема, є, препарати для ін'єкції й вливання у формі розчинів, суспензій, емульсій, ліофілізатів або стерильних порошків. Придатними для інших шляхів введення є, наприклад, фармацевтичні форми для інгаляції (зокрема, для порошкових інгаляторів, розпилювачів), краплі, розчини, спреї для носа; таблетки, плівки/облатки або капсули для лінгвального, сублінгвального або трансбуккального введення, супозиторії, препарати для очей і вух, вагінальні капсули, водні суспензії (лосьйони, колочені суміші), ліпофільні суспензії, мазі, креми, черезшкірні терапевтичні системи (такі як, наприклад пластирі), молочко, пасти, пінки, присипки, імплантати або стенти. 10 UA 102390 C2 5 10 15 20 25 30 35 Сполуки, запропоновані у даному винаході, можна перетворити у встановлені препаративні форми. Це можна виконати звичайним чином шляхом змішування з інертними, нетоксичними фармацевтично прийнятними інертними наповнювачами. Ці інертні наповнювачі, зокрема, включають носії (наприклад, мікрокристалічну целюлозу, лактозу, маніт), розчинники (наприклад, рідкі поліетиленгліколі), емульгатори й диспергуючі або змочувальні агенти (наприклад, додецилсульфат натрію, поліоксисорбітанолеат), сполучні (наприклад, полівінілпіролідон), синтетичні й натуральні полімери (наприклад, альбумін), стабілізатори (наприклад, антиоксиданти, такі як, наприклад аскорбінова кислота), барвники (наприклад, неорганічні пігменти, такі як, наприклад, оксиди заліза) і речовини, що виправляють смак і/або запах. Даний винахід також відноситься до лікарських засобів, які включають щонайменше одну сполуку, запропоновану у даному винаході, звичайно разом з одним або більшою кількістю інертних, нетоксичних фармацевтично прийнятних інертних наповнювачів, а також до їхнього застосування для зазначених вище потреб. Звичайно вважають, що у медицині й ветеринарії для забезпечення необхідного результату ефективно вводити активний інгредієнт(и), запропонований у даному винаході, у повних кількостях, рівних від 0,1 до 200 мг/кг, переважно від 1 до 100 мг/(кг маси тіла) кожні 24 год., якщо це є придатним, то у вигляді безлічі разових доз. Разова доза переважно містить активний інгредієнт(и), у кількостях, рівних від 1 до 80 мг/кг, переважно від 1 до 30 мг/(кг маси тіла). Проте, при відповідних показаннях може виявитися необхідним відхилення від зазначених кількостей, зокрема, залежно від маси тіла, шляху введення, індивідуальної реакції на активний інгредієнт, природи препарату й часу або інтервалу між введеннями. Таким чином, у деяких випадках буде досить використовувати кількість, меншу ніж зазначене мінімальне, а в інших випадках необхідно перевищити зазначену верхню межу. У випадку введення більше значних кількостей може виявитися доцільним їхній поділ на декілька окремих доз, що вводяться протягом доби. У наведених нижче дослідженнях і прикладах, якщо не зазначене інше, виражені у відсотках значення є масовими; виражені у частинах значення також є масовими. Співвідношення кількостей розчинників, співвідношення розведення й значення концентрації у розчинах рідина/рідина у всіх випадках є об'ємними. Вираження "мас./об." означає "маса/об'єм". Так, наприклад, "10 % мас./об." означає: 100 мл розчину або суспензії містить 10 г речовини. A) Приклади Абревіатури: ПХІ пряма хімічна іонізація (у МС) ДМА N,N-диметилацетамід ДМФ N,N-диметилформамід ДМСО диметилсульфоксид ЕДХ N'-(3-диметиламінопропіл)-N-етилкарбодіімід x HCl екв. еквівалент(и) ІЕР іонізація електророзпиленням (у МС) год. година(и) HATU O-(7-азабензотриазол-1-іл)-N,N,N',N'-тетраметилуронійгексафторфосфат ВЕРХ високоефективна рідинна хроматографія РХ-МС зв'язана рідинна хроматографія - мас-спектрометрія хв. хвилина (хвилини) МС мас-спектрометрія ЯМР спектроскопія ядерного магнітного резонансу PyBOP бензотриазол-1-ілокситрис(піролідино) фосфонійгексафторфосфат Rt час утримання (у ВЕРХ) КТ кімнатна температура TBTU O-(бензотриазол-1-іл)-N,N,N',N'-тетраметилуронійтетрафторборат ТФК трифтороцтова кислота ТГФ тетрагідрофуран ТМОФ триметилортоформіат Методики РХ-МС/ГХ-МС: Методика 1: Тип приладу МС: Micromass ZQ; тип приладу ВЕРХ: HP 1100 Series; УФ ДДМ (детектор на діодній матриці); колонка: Phenomenex Gemini 3 мкм 30 мм3,00 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 2,5 хв. 30 % A 3,0 хв. 5 % A 4,5 хв. 5 % A; швидкість 11 UA 102390 C2 5 10 15 20 25 30 35 40 45 50 55 потоку: 0,0 хв. 1 мл/хв., 2,5 хв./3,0 хв./4,5 хв. 2 мл/хв.; температура печі: 50 °C; детектування в УФ-області: 210 нм. Методика 2: Прилад: Micromass Quattro LCZ з HPLC Agilent Series 1100; колонка: Phenomenex Synergi 2 мкм Hydro-RP Mercury 20 мм4 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 2,5 хв. 30 % A 3,0 хв. 5 % A 4,5 хв. 5 % A; швидкість потоку: 0,0 хв. 1 мл/хв. 2,5 хв./3,0 хв./4,5 хв. 2 мл/хв.; температура печі: 50 °C; детектування в УФ-області: 208-400 нм. Методика 3: Тип приладу МС: Micromass ZQ; тип приладу ВЕРХ: Waters Alliance 2795; колонка: Phenomenex Synergi 2 мкм Hydro-RP Mercury 20 мм4 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 2,5 хв. 30 % A 3,0 хв. 5 % A 4,5 хв. 5 % A; швидкість потоку: 0,0 хв. 1 мл/хв. 2,5 хв./3,0 хв./4,5 хв. 2 мл/хв.; температура печі: 50 °C; детектування в УФ-області: 210 нм. Методика 4: Прилад: Micromass Quattro LCZ з HPLC Agilent Series 1100; колонка: Phenomenex Onyx Monolithic C18, 100 мм3 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 2 хв. 65 % A 4,5 хв. 5 % A 6 хв. 5 % A; швидкість потоку: 2 мл/хв.; температура печі: 40 °C; детектування в УФ-області: 208-400 нм. Методика 5: Прилад: Micromass QuattroPremier Waters UPLC Acquity; колонка: Thermo Hypersil GOLD 1,9 мкм 50 мм1 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 0,1 хв. 90 % A 1,5 хв. 10 % A 2,2 хв. 10 % A; температура печі: 50 °C; швидкість потоку: 0,33 мл/хв; детектування в УФ-області: 210 нм. Методика 6: Тип приладу МС: Waters ZQ; тип приладу ВЕРХ: Waters Alliance 2795; колонка: Phenomenex Onyx Monolithic C18, 100 мм3 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 2 хв. 65 % A 4,5 хв. 5 % A 6 хв. 5 % A; швидкість потоку: 2 мл/хв.; температура печі: 40 °C; детектування в УФ-області: 210 нм. Методика 7: Тип приладу МС: Micromass ZQ; тип приладу ВЕРХ: Waters Alliance 2795; колонка: Phenomenex Synergi 2,5 мкм MAX-RP 100A Mercury 20 мм4 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 0,1 хв. 90 % A 3,0 хв. 5 % A 4,0 хв. 5 % A 4,01 хв. 90 % A; швидкість потоку: 2 мл/хв.; температура печі: 50 °C; детектування в УФ-області: 210 нм. Методика 8: Прилад: Micromass Quattro LCZ з HPLC Agilent Series 1100; колонка: Phenomenex Gemini 3 мкм 30 мм3,00 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 2,5 хв. 30 % A 3,0 хв. 5 % A 4,5 хв. 5 % A; швидкість потоку: 0,0 хв. 1 мл/хв., 2,5 хв./3,0 хв./4,5 хв. 2 мл/хв.; температура печі: 50 °C; детектування в УФ-області: 208-400 нм. Методика 9: Прилад: Micromass Quattro LCZ з HPLC Agilent Series 1100; колонка: Phenomenex Synergi 2,5 мкм MAX-RP 100A Mercury 20 мм4 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 0,1 хв. 90 % A 3,0 хв. 5 % A 4,0 хв. 5 % A 4,1 хв. 90 % A; швидкість потоку: 2 мл/хв.; температура печі: 50 °C; детектування в УФ-області: 208-400 нм. Методика 10: Тип приладу МС: Waters (Micromass) Quattro Micro; тип приладу ВЕРХ: Agilent 1100 Series; колонка: Thermo Hypersil GOLD 3 мкм 20 мм4 мм; елюент A: 1 л води + 0,5 мл 50 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,5 мл 50 % мурашиної кислоти; градієнтний режим: 0,0 хв. 100 % A 3,0 хв. 10 % A 4,0 хв. 10 % A 4,01 хв. 100 % A (швидкість потоку 2,5 мл/хв.) 5,00 хв. 100 % A; температура печі: 50 °C; швидкість потоку: 2 мл/хв.; детектування в УФобласті: 210 нм. Методика 11: 12 UA 102390 C2 5 10 Прилад: Micromass GCT, GC6890; колонка: Restek RTX-35, 15 м200 мкм 0,33 мкм; постійна швидкість потоку гелію: 0,88 мл/хв.; температура печі: 70 °C; температура на вході: 250 °C; градієнтний режим: 70 °C, 30 °C/хв. 310 °C (витримування протягом 3 хв.). Методика 12: Прилад: Waters ACQUITY SQD UPLC system; колонка: Waters Acquity UPLC HSS T3 1,8 мкм 501 мм; елюент A: 1 л води + 0,25 мл 99 % мурашиної кислоти, елюент B: 1 л ацетонітрилу + 0,25 мл 99 % мурашиної кислоти; градієнтний режим: 0,0 хв. 90 % A 1,2 хв. 5 % A 2,0 хв. 5 % A; температура печі: 50 °C; швидкість потоку: 0,40 мл/хв.; детектування в УФ-області: 210400 нм. Вихідні сполуки й проміжні продукти: Приклад 1A 1-(3-Хлор-5-фторфеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію Cl O H 3C O O 15 20 25 O O 35 F Li Розчин 78 мл (78 ммоля) гексаметилдисилазиду літію (1 н. розчин у тетрагідрофурані) у 60 мл діетилового ефіру використовують при -78 °C в атмосфері аргону й додають розчин 12,5 г (72,4 ммоля) 1-(3-хлор-5-фторфеніл)етанону у 190 мл діетилового ефіру. Через 45 хв. при 78 °C по краплях додають 11,6 г (79,7 ммоля) діетилоксалату й суміш перемішують при кімнатній температурі протягом ночі. Реакційну суміш концентрують і одержують 28,6 г шуканої сполуки чистотою 71 % (100 % від теоретичного значення), що вводять у реакцію без додаткового очищення. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,63 (t, 1H), 7,55-7,50 (m, 2H), 6,33 (s, 1H), 4,14 (q, 2H), 1,24 (t, 3H). + РХ-МС (методика 1): Rt=2,65 хв.; МС (ІЕР (ІЕР - іонізація електророзпиленням)): m/z=273 + [M–Li+2H] . Приклад 2A 1-(3,5-Дифторфеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію F O H 3C 30 O O F Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3,5дифторфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 5,43 г (65 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,45 (d, 2H), 7,35 (t, 1H), 6,38 (s, 1H), 4,17 (q, 2H), 1,26 (t, 3H). + + РХ-МС (методика 3): Rt=2,43 хв.; МС (ІЕР ): m/z=257 [M–Li+2H] . Приклад 3A 1-(3-Хлорфеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію Cl O H 3C O O O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3хлорфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 40,4 г (92 % від теоретичного значення) шуканої сполуки. 13 UA 102390 C2 + + РХ-МС (методика 4): Rt=3,91 хв.; МС (ІЕР ): m/z=255 [M–Li+2H] . Приклад 4A 1-(3-Ціанофеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію N O H 3C O O O Li 5 10 Одержання шуканої сполуки проводять з використанням як вихідні речовини 3ацетилбензолкарбонітрилу й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 0,53 г шуканої сполуки чистотою 62 % (76 % від теоретичного значення). + + РХ-МС (методика 5): Rt=1,11 хв.; МС (ІЕР ): m/z=246 [M–Li+2H] . Приклад 5A 1-(3-Хлор-4-фторфеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію Cl O H 3C F O O O Li 15 Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3-хлор-4фторфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 9,7 г шуканої сполуки чистотою 66 % (79 % від теоретичного значення). + + РХ-МС (методика 1): Rt=2,69 хв.; МС (ІЕР ): m/z=273 [M–Li+2H] . Приклад 6A 4-Етокси-3,4-діоксо-1-[3-(трифторметокси)феніл]бут-1-ен-1-олат літію F F O F O H 3C O O 20 25 O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-[3(трифторметокси)феніл]етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 7,7 г шуканої сполуки чистотою 65 % (80 % від теоретичного значення). 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,84 (d, 1H), 7,70 (s, 1H), 7,56 (t, 1H), 7,45 (d, 1H), 6,41 (s, 1H), 4,15 (q, 2H), 1,25 (t, 3H). + + РХ-МС (методика 5): Rt=1,39 хв.; МС (ІЕР ): m/z=305 [M–Li+2H] . Приклад 7A 4-Етокси-1-[4-фтор-3-(трифторметил)феніл]-3,4-діоксобут-1-ен-1-олат літію F F F O H 3C F O O 30 O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-[4-фтор-3(трифторметил)феніл]етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 8,7 г шуканої сполуки чистотою 78 % (90 % від теоретичного значення). 14 UA 102390 C2 1 5 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,91 (s, 1H), 7,89 (d, 1H), 7,79 (d, 1H), 6,40 (s, 1H), 4,16 (q, 2H), 1,25 (t, 3H). + + РХ-МС (методика 3): Rt=2,64 хв.; МС (ІЕР ): m/z=307 [M–Li+2H] . Приклад 8A 4-Етокси-1-(3-фторфеніл)-3,4-діоксобут-1-ен-1-олат літію F O H 3C O O O Li 10 Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3фторфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 9,4 г (98 % від теоретичного значення) шуканої сполуки. + + РХ-МС (методика 5): Rt=1,22 хв.; МС (ІЕР ): m/z=239 [M–Li+2H] . Приклад 9A 4-Етокси-3,4-діоксо-1-[3-(трифторметил)феніл]бут-1-ен-1-олат літію F F F O H3C O O 15 20 O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-[3(трифторметил)феніл]етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 44,2 г шуканої сполуки чистотою 62 % (70 % від теоретичного значення). 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 8,12 (d, 1H), 8,07 (s, 1H), 7,83 (d, 1H), 7,67 (t, 1H), 6,45 (s, 1H), 4,16 (q, 2H), 1,25 (t, 3H). + + РХ-МС (методика 3): Rt=2,54 хв; МС (ІЕР ): m/z=289 [M–Li+2H] . Приклад 10A 4-Етокси-1-(3-метоксифеніл)-3,4-діоксобут-1-ен-1-олат літію CH 3 O O H 3C O O 25 O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3метоксифеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 0,62 г шуканої сполуки чистотою 64 % (93 % від теоретичного значення). + + РХ-МС (методика 5): Rt=1,22 хв.; МС (ІЕР ): m/z=251 [M–Li+2H] . Приклад 11A 1-(3,4-Дифторфеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію F O H 3C F O O O Li 15 UA 102390 C2 5 Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3,4дифторфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 8,47 г (100 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,79 (ddd, 1H), 7,74-7,68 (m, 1H), 7,47 (q, 1H), 6,40 (s, 1H), 4,16 (q, 2H), 1,26 (t, 3H). + + РХ-МС (методика 3): Rt=2,40 хв; МС (ІЕР ): m/z=257 [M–Li+2H] . Приклад 12A 1-(3-Бром-4-фторфеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію Br O F H 3C O O 10 15 O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3-бром-4фторфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 7,8 г шуканої сполуки чистотою 75 % (79 % від теоретичного значення). 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 8,05 (dd, 1H), 7,86 (ddd, 1H), 7,40 (t, 1H), 6,36 (s, 1H), 4,15 (q, 2H), 1,25 (t, 3H). + + РХ-МС (методика 3): Rt=2,59 хв; МС (ІЕР ): m/z=318 [M–Li+2H] . Приклад 13A 4-Етокси-1-(2-фторфеніл)-3,4-діоксобут-1-ен-1-олат літію O H3C F O O O Li 20 25 Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(2фторфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 4,5 г (82 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,67 (dt, 1H), 7,49-7,42 (m, 1H), 7,27-7,17 (m, 2H), 6,24 (s, 1H), 4,14 (q, 2H), 1,24 (t, 3H). + + РХ-МС (методика 3): Rt=2,36 хв.; МС (ІЕР ): m/z=239 [M–Li+2H] . Приклад 14A 1-(2,3-Дифторфеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію F O F H 3C O O 30 O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(2,3дифторфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 1,7 г шуканої сполуки чистотою 26 % (48 % від теоретичного значення). + + РХ-МС (методика 3): Rt=2,33 хв.; МС (ІЕР ): m/z=257 [M–Li+2H] . Приклад 15A 4-Етокси-1-(3-фтор-5-метоксифеніл)-3,4-діоксобут-1-ен-1-олат літію 16 UA 102390 C2 O CH 3 O H 3C O O 5 10 15 F O Li 5,00 г (29,4 ммоля) 3-Фтор-5-метоксибензойної кислоти використовують у 51 мл толуолу, додають 6,4 мл (88,2 ммоля) тіонілхлориду й суміш кип'ятять зі зворотним холодильником протягом 2 год. Потім реакційну суміш концентрують, залишок переносять у дихлорметан, додають 3,73 г (38,2 ммоля) N, O-диметилгідроксиламінгідрохлориду й при 0 °C додають 10,7 мл (76,4 ммоля) триетиламіну й суміш перемішують при кімнатній температурі протягом ночі. Додають воду, фази розділяють, проводять екстракцію дихлорметаном і об'єднані органічні фази сушать над сульфатом натрію, фільтрують і концентрують. Залишок розчиняють у 105 мл діетилового ефіру й додають до 9,6 мл (28,6 ммоля) 3M розчину метилмагнійброміду у діетиловому ефірі в атмосфері аргону при кімнатній температурі й суміш кип'ятять зі зворотним холодильником протягом 2 год. Потім додають насичений водяний розчин хлориду амонію, проводять екстракцію дихлорметаном і об'єднані органічні фази сушать над сульфатом натрію, фільтрують і концентрують. Неочищений продукт 1-(3-фтор-5-метоксифеніл)етанон уводять у реакцію з діетилоксалатом за аналогією з синтезом сполуки приклада 1A. Одержують 4,02 г шуканої сполуки 61 % чистотою (30 % від теоретичного значення). + + РХ-МС (методика 5): Rt=1,26 хв.; МС (ІЕР ): m/z=269 [M–Li+2H] . Приклад 16A 1-[3-(Бензилокси)феніл]-4-етокси-3,4-діоксобут-1-ен-1-олат літію O O H 3C O O 20 25 O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-[3(бензилокси)феніл]етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 8,1 г шуканої сполуки чистотою 74 % (82 % від теоретичного значення). 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,49-7,44 (m, 2H), 7,43-7,36 (m, 4H), 7,36-7,30 (m, 2H), 7,147,08 (m, 1H), 6,39 (s, 1H), 5,15 (s, 2H), 4,14 (q, 2H), 1,25 (t, 3H). + + РХ-МС (методика 2): Rt=2,96 хв.; МС (ІЕР ): m/z=327 [M–Li+2H] . Приклад 17A 4-Етокси-1-(3-фтор-5-трифторметилфеніл)-3,4-діоксобут-1-ен-1-олат літію F F F O H 3C O O 30 O F Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-[3-фтор-5(трифторметил)феніл]етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 1,5 г шуканої сполуки чистотою 62 % (62 % від теоретичного значення). + + РХ-МС (методика 5): Rt=1,37 хв; МС (ІЕР ): m/z=307 [M–Li+2H] . Приклад 18A 1-(3-Бром-5-фторфеніл)-4-етокси-3,4-діоксобут-1-ен-1-олат літію 17 UA 102390 C2 Br O H 3C O O 5 F O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3-бром-5фторфеніл)етанону (описаний в US2003/229096A1) і діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 4,7 г шуканої сполуки чистотою 62 % (74 % від теоретичного значення). + + РХ-МС (методика 7): Rt=2,29 хв; МС (ІЕР ): m/z=317 [M–Li+2H] . Приклад 19A 1-[3,5-Біс(трифторметил)феніл]-4-етокси-3,4-діоксобут-1-ен-1-олат літію F F F O H3C O F O 10 15 O Li F F Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-[3,5біс(трифторметил)феніл]етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 6,1 г (86 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 8,36 (s, 2H), 8,23 (s, 1H), 6,48 (s, 1H), 4,18 (q, 2H), 1,27 (t, 3H). – РХ-МС (методика 3): Rt=2,88 хв.; МС (ІЕР ): m/z=355 [M–Li] . Приклад 20A 4-Етокси-1-(3-фтор-5-метилфеніл)-3,4-діоксобут-1-ен-1-олат літію CH 3 O H 3C O O 20 F O Li Одержання шуканої сполуки проводять з використанням як вихідні речовини 1-(3-фтор-5метилфеніл)етанону й діетилоксалату за аналогією з синтезом сполуки приклада 1A. Одержують 8,88 г шуканої сполуки чистотою 66 % (70 % від теоретичного значення). + + РХ-МС (методика 1): Rt=2,67 хв.; МС (ІЕР ): m/z=253 [M–Li+2H] . Приклад 21A Етил-1-(3-хлор-4-фторфеніл)-5-(3-хлор-5-фторфеніл)-1H-піразол-3-карбоксилат O H3C Cl O N N F Cl 25 F 28,6 г Сполуки приклада 1A чистотою 71 % (72,9 ммоля) використовують у 350 мл етанолу, додають 15,8 г (80,2 ммоля) 3-хлор-4-фторфенілгідразингідрохлориду й суміш перемішують при кімнатній температурі протягом ночі. Реакційну суміш концентрують і залишок переносять у 350 мл концентрованої оцтової кислоти й кип'ятять зі зворотним холодильником протягом 2 год. 18 UA 102390 C2 5 Реакційну суміш додають до етилацетату й промивають водою й насиченим водяним розчином бікарбонату натрію. Органічну фазу концентрують і очищають за допомогою флешхроматографії (рухлива фаза: циклогексан/етилацетат 20:1). Одержують 22,6 г (76 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,80 (dd, 1H), 7,58-7,50 (m, 2H), 7,38 (ddd, 1H), 7,31 (s, 1H), 7,27 (s, 1H), 7,19 (dt, 1H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 5): Rt=1,52 хв.; МС (ІЕР ): m/z=397 [M+H] . Приклад 22A Етил-5-(3-хлор-5-фторфеніл)-1-(3-хлорфеніл)-1H-піразол-3-карбоксилат O ClH 3C O N N F Cl 10 15 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 1A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 5,82 г шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,61-7,56 (m, 2H), 7,54-7,47 (m, 2H), 7,32 (s, 1H), 7,30 (d, 1H), 7,25 (d, 1H), 7,18 (dt, 1H), 4,35 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 5): Rt=1,51 хв.; МС (ІЕР ): m/z=379 [M+H] . Приклад 23A Етил-1-(3-хлорфеніл)-5-(3,5-дифторфеніл)-1H-піразол-3-карбоксилат O F H 3C O N N F Cl 20 25 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 2A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Після очищення за допомогою флеш-хроматографії (рухлива фаза: циклогексан/етилацетат 3:1) одержують 2,58 г (68 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,60-7,56 (m, 2H), 7,53-7,47 (m, 1H), 7,37-7,27 (m, 3H), 7,107,03 (m, 2H), 4,35 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 3): Rt=2,74 хв.; МС (ІЕР ): m/z=363 [M+H] . Приклад 24A Етил-1,5-біс(3-хлорфеніл)-1H-піразол-3-карбоксилат O Cl H3C O N N Cl 30 112 г (413 ммоля) Сполуки приклада 3A використовують у 1120 мл етанолу, додають 101 г (561 ммоля) 3-хлорфенілгідразингідрохлориду й суміш перемішують при кімнатній температурі протягом ночі. Реакційну суміш концентрують і залишок переносять у 1120 мл концентрованої оцтової кислоти й кип'ятять зі зворотним холодильником протягом 2 год. Суміш витримують при 19 UA 102390 C2 5 кімнатній температурі протягом ночі, отриманий осад збирають фільтруванням із відсмоктуванням і перемішують з циклогексаном і осад збирають фільтруванням із відсмоктуванням, промивають циклогексаном і сушать у високому вакуумі. Одержують 126 г (80 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,58-7,54 (m, 2H), 7,51-7,43 (m, 3H), 7,40 (t, 1H), 7,30-7,26 (m, 1H), 7,25 (s, 1H), 7,19 (d, 1H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 2): Rt=3,00 хв.; МС (ІЕР ): m/z=361 [M+H] . Приклад 25A Етил-1,5-біс(3-хлор-4-фторфеніл)-1H-піразол-3-карбоксилат O Cl H 3C O N F N Cl 10 15 F Одержання шуканої сполуки проводять з використанням як вихідна речовина сполуки приклада 5A за аналогією з синтезом сполуки приклада 21A. Одержують 5,78 г шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,78 (dd, 1H), 7,67 (dd, 1H), 7,53 (t, 1H), 7,44 (t, 1H), 7,35 (ddd, 1H), 7,25 (s, 1H), 7,22 (ddd, 1H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 5): Rt=1,51 хв.; МС (ІЕР ): m/z=397 [M+H] . Приклад 26A Етил-1-(3-хлорфеніл)-5-[3-(трифторметокси)феніл]-1H-піразол-3-карбоксилат F F O O H 3C O F N N Cl 20 25 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 6A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 4,56 г (95 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,59-7,46 (m, 4H), 7,46-7,38 (m, 2H), 7,32-7,27 (m, 2H), 7,227,19 (m, 1H), 4,35 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 3): Rt=2,92 хв.; МС (ІЕР ): m/z=411 [M+H] . Приклад 27A Етил-1-(3-хлорфеніл)-5-[4-фтор-3-(трифторметил)феніл]-1H-піразол-3-карбоксилат F O F F H 3C O N F N Cl 30 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 7A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 3,60 г шуканої сполуки. 20 UA 102390 C2 1 5 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,76 (d, 1H), 7,61-7,56 (m, 3H), 7,50 (t, 1H), 7,43 (s, 1H), 7,42 (s, 1H), 7,34-7,30 (m, 1H), 4,35 (q, 2H), 1,33 (t, 3H). + + РХ-МС (методика 1): Rt=3,05 хв.; МС (ІЕР ): m/z=413 [M+H] . Приклад 28A Етил-1-(3-хлор-4-фторфеніл)-5-[3-(трифторметокси)феніл]-1H-піразол-3-карбоксилат F F O O H 3C O F N N Cl 10 F Одержання шуканої сполуки проводять з використанням як вихідна речовина сполуки приклада 6A за аналогією з синтезом сполуки приклада 21A. Одержують 3,50 г (66 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,74 (dd, 1H), 7,59-7,51 (m, 2H), 7,44-7,35 (m, 3H), 7,28 (s, 1H), 7,21 (s, 1H), 4,35 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=3,04 хв.; МС (ІЕР ): m/z=429 [M+H] . Приклад 29A Етил-5-(3-хлор-4-фторфеніл)-1-(3-хлорфеніл)-1H-піразол-3-карбоксилат O Cl H 3C O N F N Cl 15 20 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 5A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 5,67 г шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,64 (dd, 1H), 7,58-7,54 (m, 2H), 7,51-7,42 (m, 2H), 7,29-7,21 (m, 3H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 5): Rt=1,50 хв.; МС (ІЕР ): m/z=379 [M+H] . Приклад 30A Етил-5-(3-фторфеніл)-1-(3-метоксифеніл)-1H-піразол-3-карбоксилат O F H 3C O N N O CH 3 25 30 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 8A і 3-метоксифенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 30,4 г (62 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,44-7,33 (m, 2H), 7,24 (dd, 1H), 7,21 (s, 1H), 7,17 (dt, 1H), 7,08 (d, 1H), 7,04 (dd, 1H), 6,95 (t, 1H), 6,86 (dd, 1H), 4,34 (q, 2H), 3,73 (s, 3H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=2,78 хв.; МС (ІЕР ): m/z=341 [M+H] . 21 UA 102390 C2 Приклад 31A Етил-1-(3-хлорфеніл)-5-(3-метоксифеніл)-1H-піразол-3-карбоксилат O O CH3 H 3C O N N Cl5 10 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 10A і 3-хлорфенілгідразингідрохлориду з очищенням за допомогою препаративної ВЕРХ (колонка RP18; рухлива фаза: ацетонітрил/вода, градієнтний режим) за аналогією з синтезом сполуки приклада 21A. Одержують 1,60 г шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,57-7,51 (m, 2H), 7,47 (t, 1H), 7,31-7,25 (m, 2H), 7,17 (s, 1H), 6,96 (dd, 1H), 6,89 (s, 1H), 6,80 (d, 1H), 4,34 (q, 2H), 3,69 (s, 3H), 1,32 (t, 3H). + + РХ-МС (методика 3): Rt=2,68 хв.; МС (ІЕР ): m/z=357 [M+H] . Приклад 32A Етил-5-(3-хлорфеніл)-1-[3-(трифторметил)феніл]-1H-піразол-3-карбоксилат O H 3C Cl O N N F F F 15 20 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 3A і 3-(трифторметил)фенілгідразингідрохлориду з очищенням за допомогою препаративної ВЕРХ (колонка RP18; рухлива фаза: ацетонітрил/вода, градієнтний режим) за аналогією з синтезом сполуки приклада 21A. Одержують 2,00 г (42 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,85 (d, 1H), 7,75 (s, 1H), 7,71 (t, 1H), 7,64 (d, 1H), 7,50-7,43 (m, 2H), 7,40 (t, 1H), 7,27 (s, 1H), 7,20 (d, 1H), 4,35 (q, 2H), 1,33 (t, 3H). + + РХ-МС (методика 1): Rt=3,09 хв; МС (ІЕР ): m/z=395 [M+H] . Приклад 33A Етил-1-(3-хлорфеніл)-5-(3,4-дифторфеніл)-1H-піразол-3-карбоксилат O F H3C O F N N Cl 25 30 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 11A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 2,83 г (49 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,58-7,43 (m, 5H), 7,28-7,24 (m, 1H), 7,22 (s, 1H), 7,11-7,06 (m, 1H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 3): Rt=2,72 хв.; МС (ІЕР ): m/z=363 [M+H] . Приклад 34A Етил-5-(3-бром-4-фторфеніл)-1-(3-хлорфеніл)-1H-піразол-3-карбоксилат 22 UA 102390 C2 O H 3C Br O F N N Cl 5 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 12A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 3,68 г шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,74 (dd, 1H), 7,58-7,54 (m, 2H), 7,48 (t, 1H), 7,41 (t, 1H), 7,30-7,23 (m, 3H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=3,03 хв.; МС (ІЕР ): m/z=423 [M+H] . Приклад 35A Етил-5-(3-хлорфеніл)-1-(4-фторфеніл)-1H-піразол-3-карбоксилат O Cl H3C O N 10 15 20 25 N F 45,0 г (155 ммоля) Сполуки приклада 3A використовують у 400 мл етанолу, додають 34,4 г (211 ммоля) 4-фторфенілгідразингідрохлориду й суміш перемішують при кімнатній температурі протягом ночі. Реакційну суміш концентрують і залишок переносять у 400 мл концентрованої оцтової кислоти й кип'ятять зі зворотним холодильником протягом 2 год. Реакційну суміш концентрують і залишок переносять у дихлорметан, промивають насиченим водяним розчином бікарбонату натрію й водою, сушать над сульфатом натрію й концентрують. Залишок перемішують у діетиловому ефірі при кип'ятінні зі зворотним холодильником і осад збирають фільтруванням із відсмоктуванням. Матковий розчин концентрують, залишок перемішують з циклогексаном і осад збирають фільтруванням із відсмоктуванням. Одержують усього 23 г (43 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,47-7,39 (m, 4H), 7,39-7,30 (m, 3H), 7,23 (s, 1H), 7,16 (dt, 1H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=2,89 хв.; МС (ІЕР ): m/z=345 [M+H] . Приклад 36A Етил-1-(3-хлорфеніл)-5-(2-фторфеніл)-1H-піразол-3-карбоксилат O H 3C F O N N Cl 30 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 13A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 2,34 г (73 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,56-7,41 (m, 5H), 7,33-7,21 (m, 3H), 7,16 (s, 1H), 4,35 (q, 2H), 1,33 (t, 3H). 23 UA 102390 C2 + + РХ-МС (методика 1): Rt=2,85 хв.; МС (ІЕР ): m/z=345 [M+H] . Приклад 37A Етил-1-(4-фторфеніл)-5-[3-(трифторметил)феніл]-1H-піразол-3-карбоксилат F O F H3C F O N 5 10 N F Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 9A і 4-фторфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 4,63 г (99 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,74 (d, 1H), 7,64-7,54 (m, 3H), 7,47-7,41 (m, 2H), 7,37-7,30 (m, 3H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 4): Rt=4,10 хв.; МС (ІЕР ): m/z=379 [M+H] . Приклад 38A Етил-1-(3-хлорфеніл)-5-(2,3-дифторфеніл)-1H-піразол-3-карбоксилат O F F H3C O N N Cl 15 20 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 14A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 240 мг (37 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, CDCl3): δ = 7,46 (t, 1H), 7,36-7,31 (m, 1H), 7,28-7,18 (m, 2H), 7,14-7,06 (m, 3H), 7,00-6,94 (m, 1H), 4,47 (q, 2H), 1,43 (t, 3H). + + РХ-МС (методика 1): Rt=2,91 хв.; МС (ІЕР ): m/z=363 [M+H] . Приклад 39A Етил-5-(3-хлорфеніл)-1-(4-хлорфеніл)-1H-піразол-3-карбоксилат O Cl H3C O N 25 N Cl Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 3A і 4-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Після додаткового очищення шляхом перемішування у метанолі, збору осаду фільтруванням із відсмоктуванням і сушіння у високому вакуумі одержують 26,8 г (57 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,58-7,53 (m, 2H), 7,49-7,43 (m, 2H), 7,42-7,36 (m, 3H), 7,24 (s, 1H), 7,19-7,14 (m, 1H), 4,34 (q, 2H), 1,32 (t, 3H). 24 UA 102390 C2 + + РХ-МС (методика 1): Rt=3,07 хв.; МС (ІЕР ): m/z=361 [M+H] . Приклад 40A Етил-5-(3-фторфеніл)-1-(4-фторфеніл)-1H-піразол-3-карбоксилат O F H 3C O N 5 10 N F Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 8A і 4-фторфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 23,0 г (44 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,46-7,37 (m, 3H), 7,37-7,29 (m, 2H), 7,26-7,16 (m, 3H), 7,05 (d, 1H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=2,76 хв.; МС (ІЕР ): m/z=329 [M+H] . Приклад 41A Етил-1-(3-хлорфеніл)-5-(3-фтор-5-метоксифеніл)-1H-піразол-3-карбоксилат O O CH3 H3C O N N F Cl 15 20 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 15A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 2,20 г шуканої сполуки 68 % чистотою. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,59-7,55 (m, 2H), 7,50 (t, 1H), 7,31-7,27 (m, 1H), 7,24 (s, 1H), 6,89 (dt, 1H), 6,74-6,69 (m, 2H), 4,34 (q, 2H), 3,70 (s, 3H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=2,80 хв.; МС (ІЕР ): m/z=375 [M+H] . Приклад 42A Етил-1-(3-хлор-4-фторфеніл)-5-(3-фтор-5-метоксифеніл)-1H-піразол-3-карбоксилат O O CH 3 H 3C O N N F Cl 25 30 F Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 15A і 3-хлор-4-фторфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 2,36 г шуканої сполуки 82 % чистотою. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,77 (dd, 1H), 7,54 (t, 1H), 7,36 (ddd, 1H), 7,24 (s, 1H), 6,89 (dt, 1H), 6,75-6,70 (m, 2H), 4,34 (q, 2H), 3,71 (s, 3H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=2,82 хв.; МС (ІЕР ): m/z=393 [M+H] . Приклад 43A Етил-5-[3-(бензилокси)феніл]-1-(3-хлорфеніл)-1H-піразол-3-карбоксилат 25 UA 102390 C2 O H 3C O O N N Cl 5 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 16A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 14,1 г шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,56-7,44 (m, 3H), 7,40-7,24 (m, 7H), 7,16 (s, 1H), 7,04 (dd, 1H), 7,01-6,98 (m, 1H), 6,80 (d, 1H), 5,05 (s, 2H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 3): Rt=3,03 хв.; МС (ІЕР ): m/z=433 [M+H] . Приклад 44A Етил-1-(3-хлорфеніл)-5-(3-гідроксифеніл)-1H-піразол-3-карбоксилат O H 3C OH O N N Cl 10 15 20 19,1 г (44,1 ммоля) Сполуки приклада 43A використовують у 367 мл концентрованої оцтової кислоти, додають 23,5 г (11,0 ммоля) палладія на активованому вугіллі (5 %) і суміш перемішують в атмосфері водню при кімнатній температурі протягом ночі. Потім реакційну суміш фільтрують, фільтрат концентрують, залишок переносять у дихлорметан і промивають водяним розчином бікарбонату натрію й органічну фазу сушать над сульфатом натрію й концентрують. Одержують 12,7 г шуканої сполуки чистотою 63 % (53 % від теоретичного значення). + + РХ-МС (методика 1): Rt=2,41 хв.; МС (ІЕР ): m/z=343 [M+H] . Приклад 45A Етил-1-(3-хлор-4-фторфеніл)-5-(3-ціанофеніл)-1H-піразол-3-карбоксилат N O H 3C O N N Cl F Одержання шуканої сполуки проводять з використанням як вихідна речовина сполуки приклада 4A за аналогією з синтезом сполуки приклада 21A. Одержують 0,50 г (80 % від теоретичного значення) шуканої сполуки. 26 UA 102390 C2 1 5 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,94-7,91 (m, 1H), 7,87 (dt, 1H), 7,77 (dd, 1H), 7,61-7,49 (m, 3H), 7,35 (ddd, 1H), 7,31 (s, 1H), 4,35 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=2,61 хв.; МС (ІЕР ): m/z=370 [M+H] . Приклад 46A Етил-1-(3-хлор-4-фторфеніл)-5-(3-фторфеніл)-1H-піразол-3-карбоксилат O F H3C O N N Cl 10 F Одержання шуканої сполуки проводять з використанням як вихідна речовина сполуки приклада 8A за аналогією з синтезом сполуки приклада 21A. Одержують 0,60 г (93 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,75 (dd, 1H), 7,53 (t, 1H), 7,47-7,39 (m, 1H), 7,35 (ddd, 1H), 7,29-7,22 (m, 3H), 7,09-7,05 (m, 1H), 4,34 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 1): Rt=2,77 хв.; МС (ІЕР ): m/z=363 [M+H] . Приклад 47A Етил-1-(3-хлор-4-фторфеніл)-5-[3-(трифторметил)феніл]-1H-піразол-3-карбоксилат F O F H3C F O N N Cl 15 20 F Одержання шуканої сполуки проводять з використанням як вихідна речовина сполуки приклада 9A за аналогією з синтезом сполуки приклада 21A. Одержують 5,10 г (100 % від теоретичного значення) шуканої сполуки. 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,80-7,74 (m, 2H), 7,72-7,50 (m, 4H), 7,37 (ddd, 1H), 7,33 (s, 1H), 4,35 (q, 2H), 1,33 (t, 3H). + + РХ-МС (методика 3): Rt=2,87 хв.; МС (ІЕР ): m/z=413 [M+H] . Приклад 48A Етил-1-(3-хлор-4-фторфеніл)-5-[3-фтор-5-(трифторметил)феніл]-1H-піразол-3-карбоксилат F F O F H 3C O N N F Cl F 27 UA 102390 C2 5 Одержання шуканої сполуки проводять з використанням як вихідна речовина сполуки приклада 17A за аналогією з синтезом сполуки приклада 21A. Одержують 2,43 г шуканої сполуки чистотою 36 %. + + РХ-МС (методика 1): Rt=2,95 хв.; МС (ІЕР ): m/z=431 [M+H] . Приклад 49A Етил-1-(3-хлорфеніл)-5-[3-фтор-5-(трифторметил)феніл]-1H-піразол-3-карбоксилат F F O H 3C F O N N F Cl 10 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 17A і 3-хлорфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 2,08 г шуканої сполуки. + + РХ-МС (методика 5): Rt=1,52 хв.; МС (ІЕР ): m/z=413 [M+H] . Приклад 50A Етил-1-(3-бромфеніл)-5-(3-хлорфеніл)-1H-піразол-3-карбоксилат O Cl H 3C O N N Br 15 20 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 3A і 3-бромфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 2,50 г шуканої сполуки чистотою 70 % (67 % від теоретичного значення). + + РХ-МС (методика 1): Rt=2,93 хв.; МС (ІЕР ): m/z=405 [M+H] . Приклад 51A Етил-1-(3-бромфеніл)-5-(3-хлор-4-фторфеніл)-1H-піразол-3-карбоксилат O Cl H 3C O N F N Br 25 Одержання шуканої сполуки проводять з використанням як вихідні речовини сполуки приклада 1A і 3-бромфенілгідразингідрохлориду за аналогією з синтезом сполуки приклада 21A. Одержують 689 мг шуканої сполуки чистотою 76 % (77 % від теоретичного значення). 1 H-ЯМР (400 МГц, ДМСО-d6): δ = 7,73-7,69 (m, 2H), 7,52 (dt, 1H), 7,43 (t, 1H), 7,35-7,30 (m, 2H), 7,25 (s, 1H), 7,18 (dt, 1H), 4,35 (q, 2H), 1,32 (t, 3H). + + РХ-МС (методика 7): Rt=2,55 хв.; МС (ІЕР ): m/z=423 [M+H] . Приклад 52A Етил-5-(3-бром-5-фторфеніл)-1-(3-хлор-4-фторфеніл)-1H-піразол-3-карбоксилат 28
ДивитисяДодаткова інформація
Назва патенту англійською(pyrazolyl carbonyl)imidazolidinone derivatives for the treatment of retroviral diseases
Автори англійськоюThede Kai, Grischat, Susanne, Wildum, Steffen, Paulsen, Daniela
Назва патенту російськоюПроизводные (пирразолилкарбонил)имидазолидинона, предназначенные для лечения ретровирусных заболеваний
Автори російськоюТеде Кай, Грешат Сузанне, Вильдум Штеффен, Паульзен Даниэла
МПК / Мітки
МПК: C07D 403/06, C07D 403/14, A61K 31/4166, A61P 35/00
Мітки: захворювань, ретровірусних, похідні, призначені, лікування, піразолілкарбоніл)імідазолідинону
Код посилання
<a href="https://ua.patents.su/92-102390-pokhidni-pirazolilkarbonilimidazolidinonu-priznacheni-dlya-likuvannya-retrovirusnikh-zakhvoryuvan.html" target="_blank" rel="follow" title="База патентів України">Похідні (піразолілкарбоніл)імідазолідинону, призначені для лікування ретровірусних захворювань</a>
Попередній патент: Пристрій для детектування аналіту та спосіб детектування аналіту
Наступний патент: Гербіцидні композиції, що містять піроксасульфон
Випадковий патент: Склад добрива, який містить поживні мікроелементи, і спосіб його отримання