Похідні (тіо)морфоліну як модулятори s1p
Номер патенту: 106994
Опубліковано: 10.11.2014
Автори: Коолен Гейн К.А.К., Кам ван дер Елізабет, Стойт Аксель, Франкена Юр'єн, Івема Баккер Воутер І., Монс Гармен, Ронкен Ерік
Формула / Реферат
1. Похідне (тіо)морфоліну формули (І)

де
R1 вибраний з-поміж:
ціано,
(2-4С)алкініл,
(1-4С)алкіл,
(3-6С)циклоалкіл,
(4-6С)циклоалкеніл,
(6-8С)біциклоалкіл,
(8-10С)біциклічна група, кожна вибірково заміщена (1-4С)алкілом,
феніл, біфеніл, нафтил, кожний вибірково заміщений одним або більше замісниками, незалежно вибраними з-поміж галогену, (1-4С)алкілу, вибірково заміщеного одним або більше атомами фтору, (2-4С)алкінілу, (1-4С)алкокси, вибірково заміщений одним або більше атомами фтору, аміно, ді(1-4С)алкіламіно, -SО2-(1-4С)алкіл, -СО-(1-4С)алкіл, -СО-О-(1-4С)алкіл, -NН-СО-(1-4С)алкіл та (3-6С)циклоалкіл, феніл, заміщений фенокси, бензилом, бензилокси, фенілетилом або моноциклічним гетероциклом, кожний вибірково заміщений (1-4С)алкілом, моноциклічний гетероцикл, вибірково заміщений галогеном, (1-4С)алкіл або феніл, вибірково заміщений (1-4С)алкілом,
та
біциклічний гетероцикл, вибірково заміщений (1-4С)алкілом; А вибраний з-поміж -СО-О-, -О-СО-, -NH-CO-, -CO-NH, -С=С-, -ССН3-О- та зв'язуючої групи -Y-(CH2)n-X-, де
Υ приєднаний до R1 та вибраний з-поміж зв'язку, -О-, -S-, -SO-, -SO2-, -CH2-O-, -CO-, -О-СО-, -СО-О-, -CO-NH-, -NH-CO-, -С=С- та -СºС-;
n - ціле від 1 до 10; та
X приєднаний до фенілен/піридильної групи та вибраний з-поміж зв'язку, -О-, -S-, -SO-, -SO2-, -NH, -CO-, -C=C- та -СºС-; кільцева структура В вибірково містить один атом азоту;
R2 - це Н, (1-4С)алкіл, вибірково заміщений одним або більше атомами фтору, (1-4С)алкокси, вибірково заміщений одним або більше атомами фтору, або галоген; та
R3 - це (1-4С)алкілен-R5, де алкіленова група може бути заміщена (СН2)2 з утворенням циклопропілової частини або одного або двох атомів галогену, або
R3 - це (3-6С)циклоалкілен-R5 або -CO-CH2-R5, де R5 - це -ОН, -РО3Н2, -ОРО3Н2, -СООН, -СОО(1-4С)алкіл або тетразол-5-іл;
R4 - це Η або (1-4С)алкіл;
R6 - це один або більше замісників, незалежно вибраних з-поміж: Н, (1-4С)алкіл або оксо;
W - це -О-, -S-, -SO- або -SO2-;
або його фармацевтично прийнятна сіль, сольват або гідрат;
за умови, що похідне формули (І) - це не 2-(4-етилфеніл)-4-морфолінетанол або 4-[4-(2-гідроксіетил)-2-морфолініл]бензолацетонітрил, або 3-метил-2-[4-(фенілметокси)феніл]-4-морфоліноетанолгідрохлорид.
2. Сполука за пунктом 1, де кільцева структура В - це фенілен.
3. Сполука за пунктом 1 або 2, що має структуру (II)
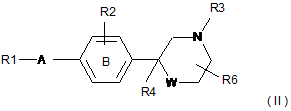 .
.
4. Сполука за будь-яким з пунктів 1-3, де R3 вибраний з-поміж: -(СН2)2-ОН, -СН2-СООН, -(СН2)2-СООН, -(СН2)3-СООН, -СН2-СНСН3-СООН, -СН2-С(СН3)2-СООН, -СНСН3-СН2-СООН, -CH2-CF2-COOH, -СО-СН2-СООН, 1,3-циклобутилен-СООН, -(СН2)2-РО3Н2, -(СН2)3-РО3Н2, -(СН2)2-ОРО3Н2, -(СН2)3-ОРО3Н2, -СН2-тетразол-5-іл, -(СН2)2-тетразол-5-іл та -(СН2)3-тетразол-5-іл;
a W - це -О- або -S-.
5. Сполука за будь-яким з пунктів 1-4, де R2 - це Н, метил, метокси, трифторметил, дифторметил, трифторметокси, дифторметокси, Сl або F;
a R4 - це Η або метил.
6. Сполука за будь-яким з пунктів 1-5, де А вибраний з-поміж -СО-О-, -NH-CO-, -СО-ΝΗ, -С=С-, -ССН3-О- та зв'язуючої групи -Y-(CH2)n-X-, де
Υ приєднаний до R1 та вибраний з-поміж зв'язку, -О-, -SO2-, -СН2-О-, -CO-, -СО-О-, -NH-CO-, -С=С- та -СºС-; n - ціле від 1 до 7; та X приєднаний до фенілен/піридилової групи та вибраний з-поміж зв'язку, -О-, -S- та -ΝΗ.
7. Сполука за будь-яким з пунктів 1-6, де R1 вибраний з-поміж ціано, етинілу, (1-4С)алкілу, циклопентилу, циклогексилу, циклогексенілу, 6,6-диметилбіцикло[3.1.1]гепт-2-илу, інданілу, вибірково заміщеного метилом, біфенілом, нафтилом, фенілу, вибірково заміщеного одним, двома або трьома замісниками, незалежно вибраними з-поміж хлору, фтору, брому, (1-4С)алкілу, (2-4С)алкінілу, (1-4С)алкокси, диметиламіно, трифторметилу, трифторметокси та (3-6С)циклоалкілу, фенілу, монозаміщеного фенокси, бензилом, бензилокси, фенілетилом, піразолілом або триазолілом, піразолілу, тіазолілу, оксадіазолілу, тієнілу, тетрагідрофуранілу, піридинілу, тетрагідропіранілу, кожний вибірково заміщений хлором, (1-4С)алкілу або фенілу, заміщеного (1-4С)алкілом, та індолілу, імідазопіридинілу, дигідробензофуранілу та бенздіоксанілу, кожний вибірково заміщений (1-4С)алкілом.
8. Сполука за пунктом 7, де R1 вибраний з-поміж (1-4С)алкілу, циклопентилу, циклогексилу, піридинілу та фенілу, де останні дві групи вибірково заміщені одним або двома замісниками, незалежно вибраними з-поміж хлору, фтору, брому, (1-4С)алкілу, (1-4С)алкокси та трифторметилу.
9. Сполука за пунктом 8, де R1 вибраний з-поміж (1-4С)алкілу та дихлорфенілу.
10. Сполука за пунктом 1, що має структуру (II), де R1 є 2,6-дихлорфеніл; А - це зв'язуюча група -Y-(CH2)n-X-, де Υ приєднаний до R1 та є зв'язком, n - це ціле, вибране з-поміж 1-6, а X приєднаний до феніленової групи та є -О-; кільцева структура В - це фенілен; R2 - це Н; R3 - це -(СН2)2-СООН та R4 - це Н.
11. Сполука за пунктом 1, що має структуру (II), де R1 - це (1-4С)алкіл; А- це зв'язуюча група -Y-(CH2)n-X-, де Υ приєднаний до R1 та є зв'язок, n - це ціле, вибране з-поміж 1-6, та X приєднаний до феніленової групи та є -О- або зв'язок; кільцева структура В - це фенілен; R2 - це Н; R3 вибраний з-поміж -(СН2)2-СООН, -(СН2)3-СООН, -СH2-СНСН3-СООН, -СН2-С(СН3)2-СООН, -СНСН3-СН3-СООН, -(СН2)2-РО3Н2, -(СН2)3-РО3Н2 та -(СН2)2-ОРО3Н2; та R4 - це Η.
12. Сполука за пунктом 11, де R1 та -(СН2)n- разом є лінійна октильна група, Χ - це -О- та R3 - це -(СН2)2-РО3Н2.
13. Сполука за пунктом 1, вибрана з-поміж
3-{2-[4-(бензилокси)феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(6-метилімідазо[1,2-а]-піридин-2-ілметокси)-феніл]морфолін-4-іл}пропіонової кислоти,
3-(2-{4-[3-(2-пропілтіазол-5-ілокси)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-{2-[4-(2-бензилоксіетокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-феноксіетокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-гекс-5-инілоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(4-ацетоксибутокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-(2-{4-[3-(4-фторфенокси)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-(2-{4-[2-(нафтален-2-ілоксі)-етокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-[2-(4-фенілкарбамоїлметоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(4-піразол-1-ілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(1-метил-1Н-піразол-3-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-хлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(6-ціаногексилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-фенетилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(3-фенілпропокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-бензилоксипропокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(7-метоксигептилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-(2-{4-[3-(4-трет-бутилфеніл)-[1,2,4]оксадіазол-5-ілметокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-{2-[4-(5-оксогексилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-фенілбутокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-метоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-циклогексилметоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(2-бензолсульфонілетокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-феноксипропокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-[1,2,4]триазол-1-ілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,3-дигідробензофуран-2-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-біфеніл-4-іл-2-оксоетокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-феноксибутокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-оксо-2-фенілетокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-хлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-(2-{4-[2-(1Н-індол-3-іл)-етокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
(+)-3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
(-)-3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-(2-(4-октилфеніл)-морфолін-4-іл)-пропіонової кислоти,
4-[2-(4-октилфеніл)-морфолін-4-іл]-масляної кислоти,
3-[2-(4-гексилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
4-[2-(4-гексилоксифеніл)-морфолін-4-іл]-масляної кислоти,
3-[2-(4-гептилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
4-[2-(4-гептилоксифеніл)-морфолін-4-іл]-масляної кислоти,
3-(2-(4-октилоксифеніл)-морфолін-4-іл)-пропіонової кислоти,
(+)-3-[2-(4-октилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
(-)-3-[2-(4-октилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
4-[2-(4-октилоксифеніл)-морфолін-4-іл]-масляної кислоти,
2,2-диметил-3-(2-(4-октилоксифеніл)-морфолін-4-іл)-пропіонової кислоти,
3-[2-(4-октилоксифеніл)-морфолін-4-іл]-масляної кислоти,
2-метил-3-[2-(4-октилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(2-хлор-6-фторбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дифторбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-диметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3,5-дихлорпіридин-4-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,4-дихлорпіридин-3-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорфенілкарбамоїл)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорфеноксиметил)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-(2-{4-[2-(2,6-дихлорфеніл)-вініл]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-[2-(4-фенетилфеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензиламіно)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензоїламіно)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-2-метилморфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-фторбензилокси)-феніл]-2-метилморфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-трифторметилбензилокси)-феніл]-2-метилморфолін-4-іл}-пропіонової кислоти,
3-[2-метил-2-(4-октилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
4-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-масляної кислоти,
3-(2-{4-[1-(2,6-дихлорфеніл)-етокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-(2-{4-[2-(2,6-дихлорфеніл)-етил]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-{2-[3-метокси-4-(2-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-фторбензилокси)-3-метоксифеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-3-метоксифеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-метоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(5-бром-2-метоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,4-дихлорбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,3-диметоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-циклопентилметокси-2-метилфеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(2,5-дихлорбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(піридин-3-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(нафтален-2-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(бензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-метоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(6-метилпіридин-2-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлорбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,5-диметоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-бромбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(2-метилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(6,6-диметилбіцикло[3.1.1]гепт-2-илметокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-фторбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(біфеніл-2-ілметокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(2-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3,5-дихлорбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(3-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-хлорбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-ізопропілбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(3-феноксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-метоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(2-фенетилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3,4-диметоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3,5-диметилбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-бензилоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(тіофен-2-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-фторбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-бензилоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-фторбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(біфеніл-4-ілметокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,3-дигідробензо[1,4]диоксін-2-ілметокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(піридин-2-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-бутоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-циклогексилметокси-2-метилфеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[2-метил-4-(тетрагідрофуран-2-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(3-метилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,3-дифторбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(4-трифторметоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-хлорбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(тетрагідропіран-2-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(4-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3,4-дифторбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(2,3,4-триметоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(циклогекс-3-енілметокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-бутилбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(4-метилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-диметиламінобензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(піридин-4-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-йодбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3,5-диметоксибензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,4-дифторбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(2,4,5-триметоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-бромбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-бромбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(4-трет-бутилбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,5-дифторбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-метил-4-(тетрагідрофуран-3-ілметокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-2-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-3-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-оцтова кислота,
3-[2-(4-октилоксифеніл)-морфолін-4-іл]-3-оксопропіонової кислоти,
2,2-дифтор-3-[2-(4-октилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
2-[2-(4-октилоксифеніл)-морфолін-4-іл]-етанол,
2-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-етанол,
{3-[2-(4-октилоксифеніл)-морфолін-4-іл]-пропіл}-фосфонієвої кислоти,
{2-[2-(4-октилоксифеніл)-морфолін-4-іл]-етил}-фосфонієвої кислоти,
моно-{2-[2-(4-октилоксифеніл)-морфолін-4-іл]-етил}ефір фосфорної кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-2-метилпропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-масляної кислоти,
фосфорної кислоти моно-(2-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-етил)ефір,
3-{2-[3-метил-4-(2-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-фторбензилокси)-3-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-3-метилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,3-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-5-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-3-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,3,6-трихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-метилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-5-метилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-5-етилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-5-пропілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-5-ізопропілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,4,6-трихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлор-4-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлор-4-йодбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-(2-{4-[3-(2-фторфеніл)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-{2-[4-(2,6-дихлор-4-етилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлор-4-метилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-бензилоксифеніл)-5-оксоморфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-5-оксоморфолін-4-іл}-пропіонової кислоти,
3-[2-(4-октилоксифеніл)-5-оксоморфолін-4-іл]-пропіонової кислоти,
3-(2-{4-[3-(2-трифторметилфеніл)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-(2-{4-[3-(2-хлор-6-фторфеніл)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-(2-{4-[3-(2,6-дихлорфеніл)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-(2-{4-[3-(4-хлорфеніл)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-(2-{4-[3-(2-хлорфеніл)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-(2-{4-[3-(2,3-дифторфеніл)-пропокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-{2-[3-хлор-4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[3-хлор-4-(2-хлор-6-фторбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[3-хлор-4-(2-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-фторбензилокси)-2-фторфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-2-фторфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-фтор-4-(2-трифторметилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлор-3-етилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-етилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-ізопропілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-циклопропілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-ізобутилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-5,5-диметилморфолін-4-іл}-пропіонової кислоти,
3-[5,5-диметил-2-(4-октилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-октилокси-2-трифторметилфеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{6-[4-(2,6-дихлорбензилокси)-феніл]-2,2-диметилморфолін-4-іл}-пропіонової кислоти,
3-[2,2-диметил-6-(4-октилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(2,6-дихлор-4-пропілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлор-4-ізопропілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлор-4-проп-1-інілбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-б-трифторметоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-4-метилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-3-метилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,4-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
4-[4-(2-карбоксіетил)-морфолін-2-іл]-фенілефір 2,6-дихлорбензойної кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-циклобутанкарбоксильної кислоти,
3-{2-[4-(2,6-дихлорбензилсульфаніл)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлорбензилсульфаніл)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-фторбензилсульфаніл)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-октилсульфанілфеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(4,4-диметилциклогексилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-дифторметоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(3-трифторметилбензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-етилбензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-трифторметоксибензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-ізопропілбензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-фторбензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-трифторметилбензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-циклопропілбензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-діетилбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[2-хлор-4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензил)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-дифторметоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-хлор-6-дифторметоксибензилокси)-2-трифторметилфеніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(3-бензилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-[2-(3-октилоксифеніл)-морфолін-4-іл]-пропіонової кислоти,
3-{2-[3-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[3-(2-хлорбензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-[2-(4-бензилоксифеніл)-тіоморфолін-4-іл]-пропіонової кислоти,
3-{2-[4-(2-хлорбензилокси)-феніл]-тіоморфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-тіоморфолін-4-іл}-пропіонової кислоти,
3-[2-(4-октилоксифеніл)-тіоморфолін-4-іл]-пропіонової кислоти,
3-{2-[5-(2,6-дихлорбензилокси)-піридин-2-іл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(індан-1-ілокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(7-метиліндан-1-ілокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,3-дигідробензофуран-3-ілокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-(2-{4-[3-(4-хлорфеніл)-алілокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-{2-[4-(3-фенілпроп-2-інілокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-(2-{4-[3-фенілалілокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-(2-{4-[3-(4-хлорфеніл)-проп-2-інілокси]-феніл}-морфолін-4-іл)-пропіонової кислоти,
3-{2-[4-(4-метоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2-метоксибензилокси)-феніл]-морфолін-4-іл}-пропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-3-оксопропіонової кислоти,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-2,2-дифторпропіонової кислоти,
(3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіл)-фосфонієвої кислоти,
2-[4-(2,6-дихлорбензилокси)-феніл]-4-(1(2)Н-тетразол-5-ілметил)-морфоліну,
3-{2-[4-(2-оксо-2-фенілетил)-феніл]-морфолін-4-іл}-пропіонової кислоти,
2-[4-(2,6-дихлорбензилокси)-феніл]-4-[2-(2Н-тетразол-5-іл)-етил]-морфоліну,
3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-2,2-диметилпропіонової кислоти,
або її фармацевтично прийнятна сіль, сольват або гідрат.
14. Сполука за пунктом 1, яка є
(-)-3-{2-[4-(2,6-дихлорбензилокси)-феніл]-морфолін-4-іл}-пропіоновою кислотою.
15. Сполука за будь-яким з пунктів 1-14 для застосування у терапії.
16. Фармацевтична композиція, що містить сполуку за будь-яким з пунктів 1-14 та принаймні одну фармацевтично прийнятну допоміжну речовину.
17. Застосування сполуки за будь-яким з пунктів 1-14 для виготовлення медикаменту для лікування, полегшення або запобігання захворюванням та умовам, у яких задіяний будь-який рецептор S1P або у яких задіяна модуляція ендогенної сигнальної системи S1P за допомогою рецептора S1P.
18. Застосування за пунктом 17, де захворювання - це розлади ЦНС, як-от нейродегенеративні розлади, зокрема вибрані з-поміж когнітивних розладів, хвороби Альцгеймера, (судинної) деменції, хвороби Ньюмена-Піка та когнітивних дефіцитів при шизофренії, обсесивно-компульсивної поведінки, великої депресії, аутизму, множинного склерозу та болю, та, зокрема, захворювання - це когнітивні розлади, як-от старече зниження когнітивних функцій.
19. Застосування агоніста S1P5 для виготовлення медикаменту для лікування, полегшення або запобігання нейродегенеративним розладам, вибраним з-поміж когнітивних розладів, хвороби Альцгеймера, (судинної) деменції, хвороби Ньюмена-Піка та когнітивних дефіцитів при шизофренії, обсесивно-компульсивної поведінки, великої депресії, аутизму, множинного склерозу та болю, та, зокрема, розлади - це когнітивні розлади, як-от старече зниження когнітивних функцій.
Текст
Реферат: Даний винахід стосується похідних (тіо)морфоліну формули (І) UA 106994 C2 ДЕРЖАВНА СЛУЖБА ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ УКРАЇНИ UA 106994 C2 R3 R2 R1 N A B R4 W R6 , (I) де R1 вибраний з-поміж: ціано, (2-4С)алкініл, (1-4С)алкіл, (3-6С)циклоалкіл, (4-6С)циклоалкеніл, (6-8С)біциклоалкіл, (8-10С)біциклічна група, кожна вибірково заміщена (1-4С)алкілом, феніл, біфеніл, нафтил, кожний вибірково заміщений одним або більше замісниками, незалежно вибраними з-поміж галогену, (1-4С)алкілу, вибірково заміщеного одним або більше атомами фтору, (2-4С)алкініл, (1-4С)алкокси, вибірково заміщений одним або більше атомами фтору, аміно, ді(1-4С)алкіламіно, -SО2-(1-4С)алкіл, -СО-(1-4С)алкіл, -СО-О-(1-4С)алкіл, -NН-СО-(14С)алкіл та (3-6С)циклоалкіл, феніл, заміщений фенокси, бензилом, бензилокси, фенілетилом або моноциклічним гетероциклом, кожний вибірково заміщений (1-4С)алкілом, моноциклічний гетероцикл, вибірково заміщений галогеном, (1-4С)алкіл або фенілом, вибірково заміщеним (14С)алкілом, та біциклічний гетероцикл, вибірково заміщений (1-4С)алкілом; А вибраний з-поміж: -СО-О-, -ОСО-, -NH-CO-, -CO-NH, -С=С-, -ССН3-О- та зв'язуюча група -Y-(CH2)n-X-, де Υ приєднаний до R1 та вибраний з-поміж зв'язку, -О-, -S-, -SO-, -SO2-, -СН2-О-, -CO-, -О-СО-, СО-О-, -CO-NH-, -NH-CO-, -С=С- та -СС- ; n - ціле від 1 до 10; та X приєднаний до фенілен/піридильної групи та вибраний з-поміж зв'язку, -О-, -S-, -SO-, -SO2-, NH, -CO-, -C=C- та -CC-; кільцева структура В вибірково містить один атом азоту; R2 - це Н, (1-4С)алкіл, вибірково заміщений одним або більше атомами фтору, (1-4С)алкокси, вибірково заміщений одним або більше атомами фтору, або галоген; та R3 - це (1-4С)алкілен-R5, де алкіленова група може бути заміщена (СН2)2 з утворенням циклопропільної частини або одного або двох атомів галогену, або R3 - це (3-6С)циклоалкілен-R5 або -CO-CH2-R5, де R5 - це -ОН, -РО3Н2, -ОРО3Н2, -СООН, СОО(1-4С)алкіл або тетразол-5-іл; R4 - це Η або (1-4С)алкіл; R6 - це один або більше замісників, незалежно вибраних з-поміж Н, (1-4С)алкілу або оксо; W - це -О-, -S-, -SO- або -SO2-; або його фармацевтично прийнятної солі, сольвату або гідрату; за умови, що похідне формули (І) це не 2-(4-етилфеніл)-4-морфоліноетанол або 4-[4-(2-гідроксіетил)-2морфолініл]бензолацетонітрил або його фармацевтично прийнятна сіль, сольват або гідрат. Сполуки за винаходом мають спорідненість до рецепторів S1P та можуть бути застосовані для лікування, полегшення або запобігання захворюванням та станам, медійованим рецепторами S1P. R3 R2 N R1 A B R4 W R6 UA 106994 C2 5 10 15 20 25 30 35 40 Галузь техніки Винахід стосується нових похідних (тіо)морфоліну, що мають спорідненість до рецепторів S1P, фармацевтичної композиції, що містить зазначені сполуки, а також застосування зазначених сполук для приготування лікарського засобу для лікування, полегшення або запобігання захворювань та станів, при яких задіяний будь-який рецептор S1P або при яких задіяна модуляція ендогенної сигнальної системи S1P через будь-який рецептор S1P. Передумови створення винаходу Сфінгосин-1-фосфат (S1P) – це біоактивний сфінголіпід, який медиює широкий ряд клітинних відгуків, як от проліферація, організація цитоскелету та міграція, збирання прилипання та щільного контакту, та морфогенез. S1P можуть зв'язуватися з членами сімейства генів діференцуючої ендотеліальної клітини (EDG рецептори) плазми локалізованих в мембранах G протеїн зв'язаних рецепторів. На сьогоднішній день, п'ять членів цього сімейства ідентифіковані як рецептори S1P у різних типах клітин, S1P1 (EDG-1), S1P2 (EDG-5), S1P3 (EDG-3), S1P4 (EDG-6) та S1P5 (EDG-8). S1P можуть викликати цитоскелетні реаранжування у багатьох типах клітин, щоб регулювати направлену міграцію імунних клітин, васкулярний гомеостаз та клітинний зв'язок у центральній нервовій системі (ЦНС) та у системі периферійних органів. Відомо, що S1P секретується судинним ендотелієм та є присутній у крові у концентрації 200900 наномоль та зв'язується альбуміном та іншими протеїнами плазми. Це забезпечує стабільне сховище у зовнішньо клітинних рідинах та ефективну доставку до високо-споріднених рецепторів клітинної поверхні. S1P зв'язується із низькою наномолярною спорідненістю з п'ятьма рецепторами S1P1-5. Додатково, тромбоцити також містять S1P та можуть бути локально вивільнені, спричиняючи, наприклад, ангіоспазм. Підтипи рецепторів S1P1, S1P2 та S1P3 широко експресуються та представляють домінантні рецептори у серцево-судиній системі. Далі, S1P1 – це також рецептор до лімфоцитів. Рецептори S1P4 майже винятково знаходяться у гематопоетичній та лімфоїдній системах. S1P5 переважно (але не винятково) експресуються у центральній нервовій системі. Експресія S1P5 вважається обмеженою до олігодендрогліоцитів у мишей, мієлінізуючі клітини мозку, тоді як у щурів та людей виявлена експресія на рівні астроцитів та ендотеоліальних клітин, але не на рівні олігодендроцитів. Модулятори рецепторів S1P - це сполуки які сигналізують як (атн)агоністи одного або більше рецепторів S1P. Даний винахід стосується модуляторів рецепторів S1P5, зокрема агоністів, та переважно агоністів з селективністю щодо рецепторів S1P1 та/або S1P3, з точки зору небажаного серцево-судинного та/або імуномодулюючого ефектів. Встановлено, що S1P5 агоністи можуть застосовуватися у лікуванні когнітивних розладів, зокрема при старечому зниженню когнітивних функцій. Хоча дослідженя по розробці терапевтичного засобу, який може бути застосований для лікування старечого зниження когнітивних функцій та деменції продовжуються, успішних результатів досі не всановлено. Тому, є необхідність у новому терапевтичному засобі з бажаними властивостями. Опис винаходу Встановлено, що (тіо)морфолін похідні формули (I) R3 R2 R1 N A B R4 W 45 50 55 R6 (I) де R1 обраний з-поміж ціано, (2-4C)алкініл, (1-4C)алкіл, (3-6C)циклоалкіл, (4-6C)циклоалкеніл, (6-8C)біциклоалкіл, (8-10C)біциклічна група, кожна вибірково заміщена (1-4C)алкілом, феніл, біфеніл, нафтил, кожна вибірково заміщена одним або більше замісниками, незалежно обраними з-поміж галоген, (1-4C)алкіл вибірково заміщений одним або більше атомами фтору, (2-4C)алкініл, (1-4C)алкокси, вибірково заміщений одним або більше атомами 1 UA 106994 C2 5 10 15 20 25 30 35 40 45 50 55 фтору, аміно, ди(1-4C)алкіламіно, -SO2-(1-4C)алкіл, -CO-(1-4C)алкіл, -CO-O-(1-4C)алкіл, -NHCO-(1-4C)алкіл та (3-6C)циклоалкіл, феніл, заміщений фенокси, бензил, бензилокси, фенілетил або моноциклічним гетероциклом, кожна вибірково заміщена (1-4C)алкіл, моноциклічний гетероцикл, вибірково заміщений галоген, (1-4C)алкіл або феніл, вибірково заміщений (1-4C)алкіл, та біциклічний гетероцикл вибірково заміщений (1-4C)алкіл; A обраний з-поміж -CO-O-, -O-CO-, -NH-CO-, -CO-NH, -C=C-, -CCH3-O- та зв'язуюча група –Y(CH2)n-X- де Y приєднаний до R1 та обраний з-поміж зв'язку, -O-, -S-, -SO-, -SO2-, -CH2-O-, -CO-, -O-CO-, -CO-O-, -CO-NH-, -NH-CO-, -C=C- та -C≡C-; n - ціле від 1 до 10; та X приєднаний до фенілен / піридильної групи та обраний з-поміж зв'язку, -O-, -S-, -SO-, -SO2-, -NH, -CO-, -C=C- та -C≡C-; кільцева структура B вибірково містить один атом азоту; R2 - це H, (1-4C)алкіл, вибірково заміщений одним або більше атомами фтору, (1-4C)алкокси, вибірково заміщений одним або більше атомами фтору, або галоген; та R3 - це (1-4C)алкілен-R5 де алкіленова група може бути заміщена (CH2)2 з утворенням циклопропилової частки, або одного або двох атомів галогену, або R3 - це (3-6C)циклоалкіленR5 або -CO-CH2-R5, де R5 – це -OH, -PO3H2, -OPO3H2, -COOH, -COO(1-4C)алкіл або тетразол-5іл; R4 - це H або (1-4C)алкіл; R6 - це один або більше замісників, незалежно обраних з-поміж H, (1-4C)алкіл або оксо; W це -O-, -S-, -SO- або -SO2-; або його фармацевтично прийнятна сіль, сольват або гідрат; за умови, що похідне формули (I) не є 2-(4-етилфеніл)-4-морфоліноетанол, 4-[4-(2-гідроксиетил)-2-морфолініл]бензолацетонітрил або або 3-метил-2-[4(фенілметокси)феніл]-4-морфоліноетанол гідрохлорид. виявляють спорідненість щодо рецепторів S1P. Зокрема, сполуки за винаходом показують вибіркову спорідненість щодо рецепторів S1P5 над рецептор(ами) S1P1 та/або S1P3. Застосування сполуки 2-(4-етилфеніл)-4-морфоліноетанолу у якості реагента у виготовленні 2-(2-арилморфоліно)етил ефірів напроксену описано у Database CA [Online] Chemical Abstracts Service, Columbus, OHIO, US; 2008, Hu, Ai-Xi et al, XP002558960, що знаходиться у базі даних STN, номер доступу 2008:1527686; & Huaxue Xuebao, 66(22), 2553-2557 Coden: HHHPA4; ISSN: 0567-7351, 2008. No описується фармакологічна активність сполук. Подібно, у Farmatsiya (Sofia), Vol.45, no.1, 1998, pages 3-11, XP009126794 Yordanova, K. et al. описується застосування 4-[4-(2-гідроксиетил)-2-морфолініл]-бензолацетонітрилу у якості реагента у виготовленні антидепресантних похідних фенілморфоліну. Не описано жодних фармакологічно активних сполук. Крім того у Database CA [Online] Chemical Abstracts Service, Columbus, OHIO, US; 2005, Hu, Ai-Xi et al, XP002602146 STN database accession No.2005:1091431; & Hu, Ai-Xi et al.: "Synthesis and characterization of 2-arylmorpholine hydrochloride" Hunan Daxue Xuebao, Ziran Kexueban, vol.32, no.4, 2005, pages 72-76, вказані, тільки синтез та характеристики 3-метил-2-[4(фенілметокси)феніл]-4-морфоліноетанол гідрохлориду. Про фармакологічну активність сполук не доповідалось. Сполуки за винаходом - це модулятори рецепторів S1P, зокрема рецепторів S1P5. Більш докладно, сполуки за винаходом - це агоністи рецепторів S1P5. Сполуки за винаходом є корисними для лікування, полегшення та запобігання захворювань та станів, при яких задіяні (будь-які) рецептор(и) S1P - зокрема S1P5 або при яких модуляція ендогенної S1P signaling система via any S1P рецептор is involved. Зокрема, сполуки за даним винаходом можуть бути застосовані для лікування, полегшення або запобігання розладів ЦНС (центральної нервової системи), як от нейродегенеративні розлади, зокрема -але не обмежуючись когнітивні розлади (зокрема старече зниження когнітивних функцій) та споріднені стани, хвороба Альцгеймера, (судинна) деменція, хвороба Ньюмена-Піка, та когнітивні дефіцити при шизофренії, обсесивнокомпульсивна поведінка, велика депресія, аутизм, множинний склероз, біль, тощо. Переважно, сполуки за даним винаходом можуть бути застосовані для лікування, полегшення або запобігання когнітивним розладам (зокрема старече зниження когнітивних функцій) та споріднені стани. У варіантах здійснення винаходу, кільцева структура B - це фенілен. У одному з варіантів за винаходом, сполуки мають структуру (II) 2 UA 106994 C2 R3 R2 N R1 A B R4 W R6 (II). У іншому варіанті за винаходом, сполуки мають формулу (I), де R3 обраний з-поміж -(CH2)2OH, -CH2-COOH, -(CH2)2-COOH, -(CH2)3-COOH, -CH2-CHCH3-COOH, -CH2-C(CH3)2-COOH, COOH 5 10 15 20 25 30 35 40 45 50 -CHCH3-CH2-COOH, , -CH2-CF2-COOH, -CO-CH2-COOH, 1,3-циклобутиленCOOH, -(CH2)2-PO3H2, -(CH2)3-PO3H2, -(CH2)2-OPO3H2, -(CH2)3-OPO3H2, -CH2-тетразол-5-іл, (CH2)2-тетразол-5-іл та -(CH2)3-тетразол-5-іл. Переважні групи R3 обрані з-поміж -CH2-COOH, -(CH2)2-COOH, -(CH2)3-COOH, -CH2-CHCH3-COOH, -CH2-C(CH3)2-COOH, -CHCH3-CH2-COOH, (CH2)2-PO3H2, -(CH2)3-PO3H2 та -(CH2)2-OPO3H2 і зокрема -(CH2)2-COOH and -(CH2)2-PO3H2. Більш переважними є -(CH2)2-COOH. У іншому варіанті, W is-O-or -S-. У переважних варіантах, W – це -O-. У іще одному варіанті за винаходом, R4 - це H або метил і зокрема, R4 - це H. У іншому варіанті, сполуки мають формулу (I) де R2 - це H, метил, метокси, трифторметил, діфторметил, трифторметокси, діфторметокси, Cl або F. У інших переважних варіантах, R2 - це H або трифторметил. Далі, у варіанті за винаходом, A обраний з-поміж -CO-O-, -NH-CO-, -CO-NH, -C=C-, -CCH3-Oта зв'язуюча група –Y-(CH2)n-X- де Y приєднаний до R1 та обраний з-поміж зв'язку, -O-, -SO2-, CH2-O-, -CO-, -CO-O-, -NH-CO-, -C=C- та -C≡C-; n - ціле від 1 до 7; а X приєднаний до фенілен / піридильної групи та обраний з-поміж зв'язку, -O-, -S- та -NH. Переважно, A обраний з-поміж CO-NH, -C=C-, -CCH3-O- та зв'язуючої групи -(CH2)n-X- та -O-(CH2)n-X-. У переважних варіантах A - це CH2-O-. У інших варіантах за винаходом, R1 обраний з-поміж ціано, етиніл, (1-4C)алкіл, циклопентил, циклогексил, циклогексеніл, 6,6-диметил-біцикло[3.1.1]гепт-2-іл, інданіл вибірково заміщений метилом, біфенілом, нафтилом, фенілом, вибірково заміщеним одним, двома або трьома замісниками, незалежно обраними з-поміж хлор, фтор, бром, (1-4C)алкіл, (2-4C)алкініл, (1-4C)алкокси, диметиламіно, трифторметил, трифторметокси та (3-6C)циклоалкіл, та R1 далі обраний з-поміж фенілу, монозаміщеного фенокси, бензилу, бензилокси, фенілетилу, піразолілу або триазолілу, та R1 далі обраний з-поміж піразолілу, тіазолілу, оксадіазолілу, тієнілу, тетрагідрофуранілу, піридинілу, тетрагідропіранілу, кожне вибірково заміщене хлором, (14C)алкілом або фенілом, заміщеним (1-4C)алкілом, та R1 далі обраний з-поміж індолілу, імідазопіридинілу, дигідробензофуранілу та бенздиоксанілу, кожний вибірково заміщений (1-4C)алкілом. У переважних варіантах, R1 обраний з-поміж етинілу, (1-4C)алкілу, циклопентилу, циклогексилу, циклогексенілу, біфенілу, нафтилу, феніл вибірково заміщений одним, двома або трьома замісниками, незалежно обраними з-поміж хлору, фтору, брому, (1-4C)алкілу, (1-4C)алкокси, диметиламіно, трифторметилу та трифторметокси, та далі обраний з-поміж фенілу, монозаміщеного фенокси, бензилом, бензилокси, фенілетилом, піразолілом або триазоліл, та далі обраний з-поміж тіазолілу, тієнілу, тетрагідрофуранілу, піридинілу, тетрагідропіранілу, кожний вибірково заміщений хлором або (1-4C)алкілом, та бенздиоксанілу. Зокрема, R1 обраний з-поміж (1-4C)алкілу, циклопентилу, циклогексилу, піридинілу та фенілу, де останні дві групи вибірково заміщені одним або двома замісниками, незалежно обраними зпоміж хлору, фтору, брому, (1-4C)алкілу, (1-4C)алкокси та трифторметилу. У переважних варіантах, R1 - це (1-4C)алкіл або дихлорфеніл. У більш переважному варіанті за винаходом, R1 - це 2,6-дихлорфеніл; A - це зв'язуюча група -Y-(CH2)n-X-, де Y приєднаний до R1 та є зв'язком, n - це 1, а X приєднаний до феніленової групи та є -O-; R2 - це H; R3 - це -(CH2)2-COOH; а R4 - це H. У інших переважних варіантах за винаходом, R1 - це (1-4C)алкіл; A - це зв'язуюча група -Y(CH2)n-X-, де Y приєднаний до R1 та є зв'язком, n - це ціле, обране з-поміж 1-6 та X приєднаний до фенілен / піридильної групи та є -O- або зв'язком; R2 - це H; R3 обраний з-поміж -(CH2)2COOH, -(CH2)3-COOH, -CH2-CHCH3-COOH, -CH2-C(CH3)2-COOH, -CHCH3-CH2-COOH, -(CH2)2PO3H2, -(CH2)3-PO3H2 та -(CH2)2-OPO3H2; а R4 - це H. Переважно, R1 та -(CH2)n- разом являють лінійну октильну групу. Переважним є R3 -(CH2)2-PO3H2. У іншому переважному варіанті, X - це -O-. Термін галоген стосується фтору, хлору, брому, або йоду. Переважні галогени - це фтор та 3 UA 106994 C2 5 10 хлор, зокрема хлор. Термін (1-4C)алкіл означає розгалужена або нерозгалужена алкільна група, що має 1-4 атоми вуглецю, наприклад метил, етил, пропил, ізопропил та бутил. Переважна алкільна група це метил. Термін (1-4C)алкокси означає алкокси група, що має 1-4 атоми вуглецю, де алкільна частина є як визначено вище. Переважна алкокси група - це метокси. Термін (1-4C)алкілен означає розгалужена або нерозгалужена алкіленова група, що має 1-4 атоми вуглецю, наприклад метилен, -CCH3CH2-, та подібні. У визначенні R3, який є (14C)алкілен-R5, один або більше атомів вуглецю у алкіленовій групі можуть (серед інших) незалежно бути заміщений (CH2)2 з утворенням циклопропильної частини, з утворенням групи R3 як от R5 15 20 25 30 35 40 45 50 55 . Термін (2-4C)алкініл означає розгалужена або нерозгалужена алкінільна група, що має 2-4 атоми вуглецю, де потрійний зв'язок може бути присутній у різних позиціях у групі, наприклад етиніл, протаргіл, 1-бутиніл, 2-бутиніл, тощо. Термін (3-6C)циклоалкіл означає циклічну алкільну групу, що має 3-6 атоми вуглецю, як от циклопропил, циклобутил, циклопентил або циклогексил. Переважними є циклопентил та циклогексил. Термін (4-6C)циклоалкеніл означає циклічну алкенільну групу, що має 4-6 атоми вуглецю та містить один або два подвійні зв'язки, наприклад циклогексеніл. Термін (3-6C)циклоалкілен означає циклічну алкільну групу, що має дві точки приєднання. Переважним є 1,3-циклобутилен, що має структуру . Термін (6-8C)біциклоалкіл означає конденсована кільцева система із двох циклоалкільних груп, що має разом 6-8 атомів вуглецю, наприклад група біцикло[3.1.1]гепт-2-іл. Термін (810C)біциклічна група означає конденсована кільцева система ароматичної та неароматичної кільцевої структури, що має разом 8-10 атомів вуглецю, наприклад інданова група. Термін моноциклічний гетероцикл охоплює моноциклічні гетероарильні групи та неароматичні гетеромоноциклічні групи, наприклад фураніл, тієніл, пірроліл, оксазоліл, тіазоліл, імідазоліл, піразоліл, ізоксазоліл, ізотіазоліл, триазоліл, оксадіазоліл, піридил, піридазиніл, піримідиніл, піразиніл, триазиніл, тетрагідрофураніл, тетрагідропіраніл, диоксаніл, морфолініл, та подібні. Термін біциклічний гетероцикл охоплює біциклічні гетероарильні групи та не-ароматичні гетеробіциклічні групи, наприклад індоліл, індазоліл, ізоіндоліл, індолізиніл, бензімідазоліл, імідазотіазоліл, імідазопіридиніл, бензфураніл, дигідробензофураніл, бенздиоксаніл, хінолініл, ізохінолініл, хінолізиніл, тетрагідроізохінолініл, та подібні. З огляду на замісники, термін "незалежно" означає, що замісники можуть бути однакові або різні один від одного у одній самій молекулі. Сполуки за винаходом можуть бути зручно одержані відомими способами, як показано у експериментальному розділі опису. Сполуки за даним винаходом можуть містити один або більше асиметричних центрів і тому можуть виступати у якості рацематів та рацемічних сумішей, одиничних енантіомерів, діастереомерних сумішей та індивідуальних діастереомерів. В залежності від природи різних замісників, молекули можуть мати додатковий асиметричний центр. Кожний такий асиметричний центр буде незалежно виробляти два оптичні ізомери. Всі можливі оптичні ізомери та діастереомери, у сумішах та як чисті або частково очищені сполуки, включені в обсяг цього винаходу. Даний винахід охоплює усі такі ізомерні форми таких сполук. Незалежний синтез цих діастереомерів або їх хроматографічне розділення, можуть проводитись способом, відомим з рівня техніки шляхом відповідної модифікації описаної тут методології. Їх абсолютна стереохімія може бути визначена шляхом рентгенівської кристалографії кристалічних продуктів або кристалічних проміжних сполук, які за бажанням дериватизують з реагентом, що містить асиметричний центр відомої абсолютної конфігурації. За бажанням, або їх хроматографічне розділення, можуть проводитись способом, відомим з рівня техніки шляхом відповідної модифікації описаної тут методології. Їх абсолютна стереохімія може бути визначена шляхом рентгенівської кристалографії кристалічних продуктів або кристалічних проміжних сполук, які за 4 UA 106994 C2 5 10 15 20 25 30 35 40 45 50 55 60 бажанням дериватизують з реагентом, що містить асиметричний центр відомої абсолютної конфігурації. Рацемічні суміші сполук можуть бути розділені у індивідуальні енантіомери способами, відомими з рівня техніки, як от сполучення рацемічної суміші сполук у енантіомерно чисту сполуку, утворюючи діастереомерну суміш, з подальшим розділенням індивідуальних діастереомерів стандартними способами, як от фракціонована кристалізація або хроматографія. Сполуки можуть існувати як поліморфи та по суті також належать до обсягу даного винаходу. Додатково, сполуки можуть утворювати сольвати з водою (тобто, гідрати) або звичайними органічними розчинниками, і такі сольвати також належать до обсягу даного винаходу. Мічені ізотопами сполуки формули (I) або їх фармацевтично прийнятні солі, включаючи сполуки формули (I) які розпізнаються методами PET або SPECT, також належать до обсягу даного винаходу. Це ж стосується сполук формули стосується тих солей, які є, з точки зору здорового медичного глузду, підходящими для застосування у контакті з тканинами людини або нижчої тварини без впливу токсичності, подразнення, алергічної реакції, тощо, та є відповідними при обґрунтованому співвідношенні користь ризик. Фармацевтично прийнятні солі є добре відомі з рівня техніки. Вони можуть бути одержані in situ при кінцевому виділенні та очищенні сполук за винаходом, або самі по собі шляхом їх реакції з фармацевтично прийнятними не токсичними основами або кислотами, включаючи неорганічні або органічні основи та неорганічні або органічні кислоти. Сполуки за винаходом можуть бути введені ентерально або парентерально. Точна доза та шлях затосування сполуки та їх композицій залежить від біологічної активності сполуки per se, віку, ваги та статі пацієнта, потреб індивідувального пацієнта, якому вводять лікарський засіб, ступеню хвороби або потреби та розсуду медичного фахівця. Взагалі, парентеральне введення потребує нижчих доз, ніж інші способи введення, які більш залежать від абсорбції. Але, дози для людей є переважно 0.001 – 10 мг на кг ваги тіла. Взагалі, ентеральні та парентеральні дози знаходяться в межах від 0.1 до 1,000 мг на день усієї кількості активних інгредієнтів. У суміші з фармацевтично придатними допоміжними речовимнами, наприклад, як описано у st стандартному посиланні "Remington, The Science and Practice of Pharmacy" (21 edition, Lippincott Williams & Wilkins, 2005, див. зокрема Part 5: Pharmaceutical Manufacturinг) сполуки можуть бути сформовані у тверді дозувальні одиниці, як от пілюлі або таблетки, або бути сформовані у капсули або суппозиторії. За допомогою фармацевтично придатних рідин сполуки можуть такою бути у формі розчинів, суспензій або емульсій. Для утворення дозувальних одиниць, наприклад, таблеток, передбачається застосування звичайних допоміжних речовин, як от наповнювачів, барвників, полімерних зв'язувачів та подібних. Взагалі, можуть застосовуватись будь-які фармацевтично придатні домішки, які не впливають на функцію діючої сполуки. Відповідні носії, з якими можуть застосовуватися сполуки за винаходом, включають, наприклад, лактозу, крохмаль, похідні целюлози та подібні, або їх суміші, узяті у відповідних кількостях. Композиції для внутрішньовенного введення можуть, наприклад, бути розчини сполук за винаходом у стерильному ізотонічному буферному розчині. За необхідності, композиції для внутрішньовенного введення можуть включати, наприклад, розчинники, стабілізатори та/або місцеві анестетики для полегшення болі у місці ін'єкції. Фармацевтичні композиції за винаходом можуть бути складені для будь-якого шляху введення та містити принаймні одну сполуку за даним винаходом та її фармацевтично прийнятні солі, з будь-яким фармацевтично придатним інгредієнтом, наповнювачем, носієм, допоміжним або транспортним засобом. "Фармацевтично придатний" означає, що носій, розчинник або наповнювач має бути сумісним з іншими інгредієнтами композиції та не завдавати шкоди особі, що приймає цей засіб. У варіанті за винаходом, передбачений фармацевтичний комплект або набор, що містить один або більше контейнерів, наповнених однією або більше фармацевтичних композицій за винаходом. До цього контейнеру (ів) можуть додаватися різні письмові матеріали, як от інструкція із застосування, або повідомлення у формі, передбаченій державним закладом, що регулює виробництво, застосування або продаж фармацевтичних продуктів. Це повідомлення може містити узгодження щодо виробництва, застосування, або продажу для застосування для людей або тварин. Якщо не зазначено інше, усі застосовані тут технічні та наукові термінимають значення, звичайно зрозумілі для фахівця у галузі, до якої стосується даний винахід. Хоча на практиці або при випробуваннях за даним винаходом можуть застосовуватися способи та матеріали, подібні або еквівалентні до описаних, відповідні методи та матеріали описані у цьому документі. 5 UA 106994 C2 5 10 15 20 25 30 35 40 45 50 ОПИС КРЕСЛЕНЬ Фіг. 1 Процентне відношення чередування молодих та старих самців мишей C57BL/6J у Tлабіринті або з носієм (контрольні групи) або зі сполукою 34b (10мг/кг; p.o.) Наступні приклади наведені лише для подальшого більш детального освітлення винаходу. ПРИКЛАДИ §1. МАТЕРІАЛИ ТА СПОСОБИ 1 Спектр ядерного магнітного резонансу ( H ЯМР) визначають у визначеному розчиннику 1 13 використовуючи апарат Bruker Avance-I 400 з магнітом 9.4T ( H: 400 MHz, C: 100 MHz), обладниний інверсивним широкополосним зондом BBI із Z-градієнтом та ATM, або апарат Bruker Avance-DRX 600 з магнітом 14.1T, обладнаний TXI інверсивним кріозондом з потрійним резонансом із Z-градієнтом та ATM, при 300 K, якщо не зазначено інше. Спектр визначають у дейтерованому хлороформі (CDCl3) з 99.8 атом% D; або у диметилсульфоксиді-d6 (DMSO-d6) що містить 0.03 v/v% тетраметилсилан; обидва виробництва Aldrich. Хімічні зсуви наводяться у ч. на млн. (шкала δ), починаючи від тетраметилсилану. Константи взаємодії J наведені у Гц. Максимальні рівні ЯМР спектру показані символами "q" (квартет), "dq" (подвійний квартет), "t" (триплет), "dt" (подвійний триплет), "d" (дуплет), "dd" (подвійний дуплет), "ddd" (подвійний подвійний дуплет), "s" (синглет), "bs" (широкий синглет) та "m" (мультиплет). Сигнали NH та OH визначають після змішування зразка з краплиною D2O. Точки топлення записують на апараті для визначення точок топлення Büchi B-545. Усі реакції, у яких задіяні чутливі до вологи сполуки або умови, виконують у атмосфері безводного азоту. Реакції контролюють з використанням тонкошарової хроматографії (TLC) на пластикових листах з кварцевим покриттям (покритий силікагелем Merck 60 F254) із зазначеним елюентом. Плями визначають УФ світлом (254 нм) або I2. Рідинна хроматографія – масс-спектрометрія (LC-MS) Система A: Колонка: Acquity UPLC BEH C18 1,7 мкм, 50 × 2.1 мм з частками 1.7 мкм. Колонка є термостабільною у печі для колонок при 45 °C. Визначення: Масив диодів між 210 та 260 нм. етап загальний час витрата (мкл/хвил) A(%) B(%) 0 0 800 95 5 1 0.1 800 95 5 2 4.5 800 10 90 3 5 800 10 90 4 5.01 800 95 5 A=99.9 % води з 0.1 % CH3COOH B=99.9 % CH3CN з 0.1 % CH3COOH Система B: Колонка: Waters Sunfire C18, 30 × 4.6 мм з частками 2.5 мкм. Колонка є термостабільною у печі для колонок при 23 °C. Визначення: Вимірювач UV/VIS з довжиною хвилі від 254 нм + випарювальний детектор розсіювання світла, що працює при 70° цельсію та тиску 1.7 bar N2. етап загальний час витрата (мкл/хвил) A(%) B(%) 0 0 1800 95 5 1 1.8 1800 0 100 2 2.6 1800 0 100 3 2.8 1800 95 5 4 3.0 1800 95 5 A=99.9 % води з 0.1 % HCOOH B=99.9 % CH3CN з 0.1 % HCOOH Час затримки (Rt), для Система B, для піків у хроматографі загального іонного потоку (TIC) яки показує масу для [M+H]+ без 0.5 amu точності вирахуваної точної MW та має відповідний пік у хроматографі випарювального розсіювання світла (ELS) з відповідною площею % (чистота) >85 %. §2. ЗАГАЛЬНІ АСПЕКТИ СИНТЕЗУ Відповідний синтез заявлених сполук та проміжних, що містять 2-арил-морфолін частки, проходить шляхом, як вказано у Схемі 1, як описано нижче. Схема 1 6 UA 106994 C2 R2 R2 Q1 NH2 N Q1 OH OH R2 R2 R2 Br Q1 OH Q1 O Q1 O (II) (III) (IV) R2 R2 R2 Q1 Q1 Q1 O R4 O O O R4 N R4 N (V) R4 (VII) 20 25 30 35 O A Q1 15 (VI) R1 O 10 N H R2 R2 5 H N R4 R4 N Q2 (I) N R3 Q1 - це група, еквівалентна R1-A, або група, яка може бути перетворена на R1-A. Q2 - це група, еквівалентна R3, або група, яка може бути перетворена на R3. Детальніше, дивитися наведене нижче. Синтез починається з відповідно заміщеним ацетофеноном (II). Відповідно заміщені ацетофенони є доступними на ринку або можуть бути одержані із доступних на ринку ацетофенонів. Наприклад шляхом O-алкіляцї (не)заміщених 4-гідроксиацетофенонів. Ця Oалкіляція може бути виконана з відповідним алкілюючим засобом, як от 1-бромоктан або бензил бромід, у розчинниках, як от диметилсульфоксид (DMSO), ацетон, або ацетонітрил, у присутності основи як от гідроксид калію або карбонат калію, при температурі між 0 °C та 60 °C. У іншому прикладі, 1-(4-бензилокси-3-трифторметил-феніл)-етанон одержують із 4'-фтор-3'(трифторметил)ацетофенону шляхом реакції з бензиловим спритом у присутності сильної основи, як от калій трет-бутоксид, у розчиннику як от тетрагідрофуран, при температурі біля 70 °C. Відповідно заміщений ацетофенон (II) бромінують щоб одержати 2’-бром-ацетофенони (III). Бромінація може бути виконана із бромідом міді(II) у відповідному розчиннику як от етил ацетат при нагріванні зі зворотнім холодильником; шляхом реакції відповідного етеру силіл енолу, обробленим з DIPEA та TMSOTf, при 0 °C, з NBS у розчиннику як от дихлорметан, при кімнатній температурі; або з тетра-N-бутиламоній трибромід, у розчиннику як от метанол, при кімнатній температурі. Реакція 2’-бромацетофенону (III) з бензил аміном, у розчиннику як от етанол та хлороформ, при температурі між 0 °C та кімнатною температурою, дає амінокетони (R4=H), які безпосередньо відновлюють з відновлюючим засобом як от борогідрид натрію у розчиннику як от етанол та хлороформ, при температурі між 0 °C та кімнатною температурою, даючи аміно спирти (IV, R4=H). Альтернативно, 2’-бромацетофенон (III) може бути відновлений з відповідним відновлюючим засобом, як от NaBH4, у розчиннику як от 1,4-диоксан, при кімнатній температурі, з подальшою обробкою з основою, як от KOH, у суміші води та відповідного розчинника, як от Et2O, даючи 2-арилоксирани, що при обробці з бензил аміном при температурі 80 °C, дає аміно спирти (IV, R4=H). Інший спосіб синтезу аміноспиртів (IV, R4=Me) - це реакція відповідно заміщеного ацетофенону з триметилсиліл цианідом у присутності кислоти Льюїса, як от йодид цинку, при кімнатній температурі, без домішок. Подальше відновлення проміжного ціаногідрину з відновлюючим засобом, як от алюмогідрид літію, у розчиннику як от тетрагідрофуран, та подальше утворення іміну з бензальдегідом у присутності кислотного каталізатора, як от pтолуолсульфонова кислота, у розчиннику як от толуол, та кінцеве відновлення проміжного іміну з борогідридом натрію, у розчиннику як от метанол, при температурі між -15 °C та кімнатною температурою. 7 UA 106994 C2 5 10 15 20 25 Аміно спирти (IV) можуть реагувати з активованою хлороцтовою кислотою або бромоцтовою кислотою у розчиннику як от дихлорметан з основою, як от триетиламін, та в подальшому циклізують у розчиннику як от 2-пропанол з основою, як от гідроксид калію даючи морфолін-3они. Ці морфолін-3-они можуть потім бути відновлені з відновлюючим засобом, як от боран, у розчиннику як от тетрагідрофуран, при температурі між 0 °C та кімнатною температурою, даючи N-бензил морфоліни (V). Деякі з N-бензил морфолінів (V) можуть бути перетворені на інші Nбензил морфоліни (V), див. Схему 2. Наприклад N-бензил-2-(4-бромфеніл)-морфолін (V-Br) застосовують як вихідний матеріал у наступних послідовностях: Таким чином, обробка V-Br з n-бутилом літію при -75 °C, у розчиннику як от тетрагідрофуран або диетил етер, з подальшим гасінням з формамідом, як от N, N-диметилформамід або Nформилморфолін, приводить до утворення V-CHO. Якщо проміжні види літію гасять з відповідним ізоціанатом, потім утворюються відповідні аміди V-CONHG. Відновлення V-CHO, з відновлюючим засобом як от борогідрид натрію, у розчиннику як от метанол, при температурі між 0 °C та кімнатною температурою, дає бензилові спирти V-CH2OH. Сполуки типу V-CH2OH можуть бути сполучені за умов реакції Міцунобу з фенолами, у розчиннику як от тетрагідрофуран або дихлорметан, при кімнатній температурі. Сполуки типу V-CHO можуть також бути сполучені з відповідним ілідом фосфонію, у розчиннику як от тетрагідрофуран при температурі біля 70 °C, даючи сполуки типу V-CHCHG. The ілід може бути утвоерний із відповідної солі фосфонію із сильною основою, як от гідрид натрію у розчиннику як от тетрагідрофуран, при температурі біля 0 °C. V-Br також може бути перетворений на V-OH, з відповідним каталізатором паладію, у розчиннику як от 1,4-диоксан (Anderson K.W.; Ikawa T., Tundel R.E., Buchwald S.L. J. Am. Chem. Soc. 2006 128(33), 10694-10695). Сполуки V-OH можуть бути алкільовані, наприклад за умов міжфазного переносу у розчиннику як от вода та 1,4-диоксан, з основою, як гідроксид калію та каталізатора міжфазного переносу, як от тетрабутиламоній бромід, при температурі біля точки кипіння розчинника. Схема 2 8 UA 106994 C2 R2 G N N R2 G O N R4 O R4 O (V-CONHG) (V-CHCHG) R2 R2 G N R2 N N Br R4 O OHC R4 O (V-CH2G) R4 O (V-Br) R2 (V-CHO) R2 N N N HO Ph R2 R4 O R4 O Ph N (V-OH) G HO R4 O (V-CH2OH) R2 R2 N N O H2 N R4 O R4 O (V-OCH2G) R2 (V-NH2) N G O R4 O R2 G N N H R4 O (V-NHCH2G) O R2 G N N H R4 O (V-NHCOG) 5 10 15 20 25 G - це група, яка є частиною R1-A у кінцевій сполуці I. За умови каталізатора паладію IV-Br може також бути перетворений на V-CH2G з відповідним органометалевим реагентом, як от реагент бору (реакція Сузукі), або реагент цинку (реакція Негіші), у розчиннику як от толуол або тетрагідрофуран, при температурі біля точки кипіння розчинника. Також V-Br можуть бути сполучені з відповідним донором аміну, як от бензофенон імін, за умов каталізу паладію у присутності основи, як от натрій трет-бутоксид, у розчиннику як от толуол при температурі біля 100 °C. Подальша обробка з водною кислотою, як от соляна кислота, при кімнатній температурі, дає проміжні V-NH2. V-NH2 можуть реагувати з відповідним алкілюючим засобом та основою як от N-етилдиізопропиламін, у розчиннику як от метанол при кімнатній температурі даючи вторинні аміни V-NHCH2G. V-NH2 також можуть реагувати з відповідним ацилюючим реагентом, як от ацил хлорид, з відповідною основою, як от N-етилдиізопропиламін, у розчиннику як от ацетонітрил, при температурі між 0 °C та кімнатною температурою даючи аміди V-NHCOG. Видалення N-бензильної групи у N-бензил морфолінах (V), може бути виконане шляхом гідрогенації у розчиннику, як от етанол та каталізатора, як от гідроксид паладію, або альтернативно шляхом реакції з ACE-Clу розчиннику, як от 1,2-дихлоретан, з подальшою реакцією проміжного карбамату з метанолом. Одержані морфоліни (VI) можуть бути перетворені на інші морфоліни (VI) послідовністю етапів. Див. Схема 3. Наприклад, (VI-OH) може бути захищена при азоті з відповідною захисною групою (P.G.M. Wuts, T.W. Greene Protective groups in organic synthesis, 4th ed., John Wiley & Sons, 2006), як от третбутилоксикарбоніл (BOC), шляхом реакції з ди-трет-бутил дикарбонатом у розчиннику, як от ацетонітрил при кімнатній температурі. В подальшому, фенольна група може реагувати з відповідним алкілюючим реагентом у розчиннику, як от ацетонітрил, у присутності основи як от карбонат калію, при кімнатній температурі. Після чого група трет-бутилоксикарбонілу (BOC) 9 UA 106994 C2 може бути видалена шляхом обробки кислотою, як от гідроген хлорид, у розчиннику як от етанол, при температурі між кімнатною температурою та 60 °C, даючи модифікований морфолін (VI-OГ). Схема 3 5 R2 R2 R2 HO HO R4 (VI-OH) R4 N H O O R4 35 R4 N G O (VI-OG) O O N H E O R4 N (VIIa-SAc) 30 O R2 R2 S 25 R2 G O (VIIa-OG) E O 20 O O R4 N (VIIa-OH) 15 N O R2 G O HO 10 R4 N O O R4 O O R2 O G O O O O O E (VIIa-SG) N O O E Морфоліни (VI) можуть реагувати з естером (мет)акрилової кислоти, у так названій реакції Майкла, у розчиннику як от ацетонітрил, метанол, або N, N-диметил-формамід, при температурі між кімнатною температурою та 85 °C, та потім з додаванням деякої основи, як от триетиламін або 1,8-диазабіцикло[5.4.0]ундец-7-ен, даючи ефіри морфолін-4-іл-пропіонової кислоти (VIIa, Q2=CH2CH2COOR"). Якщо ці ефіри морфолін-4-іл-пропіонової кислоти (VIIa, Q2=CH2CH2COOR") містять фенольну групу (VIIa-OH), ці сполуки можуть бути перетворені наступним чином: Шляхом реакції з відповідним алкілюючим реагентом, як от алкіл бромід або алкіл хлорид, у присутності основи, як от карбонат калію або карбонат цезію, у розчиннику як от ацетонітрил та / або тетрагідрофуран, при кімнатній температурі, даючи сполуки типу VIIa-OG. Альтернативно, VIIa-OH можуть бути перетворені на VIIa-OG, шляхом реакції з відповідним спиртом, у присутності трифенілфосфіну, та відповідного азо-реагента, як от диізопропил азодикарбоксилат, у розчиннику як от тетрагідрофуран або дихлорметан. Далі, VII-OH можуть бути перетворені на відповідний ефір трифторметансульфонової кислоти шляхом реакції з Nфенілбіс(трифторметан-сульфонімід) у присутності основи, як от Et3N, у розчиннику, як от CHCl3, при температурі між кімнатною температурою 60 °C. Ці ефіри трифторметансульфонової кислоти можуть реагувати з тіоацетатом при каталізі паладію, у розчиннику як от толуол, при 110 °C, даючи тіоефіри VIIa-SAc. Основний гідроліз тіоефіру, з основою як от NaOH, у розчиннику як от EtOH та воді, при 0 °C, що безпосередньо супроводжуеться алкіляцією з відповідним алкілюючим засобом, при кімнатній температурі, дає тіоетери VIIa-SG. Сполуки типу VIIa-OG та VIIa-SG можуть бути перетворені у кінцеві сполуки I шляхом основного або кислотного гідролізу ефіру, в залежності від природи групи E. Наприклад, третбутил ефіри (E=C(CH3)3) можуть бути оброблены кислотою, як от трифтороцтова кислота або хлоридом водню, у розчиннику як от CH2Cl2 або 1,4-диоксан, при кімнатній температурі. Як подальший приклад, етил ефіри (E=CH 2CH3) можуть бути оброблені з основою, як от гідроксид натрію або гідроксид літію, у розчинниках, як от етанол, THF, та/або вода, при температурі між кімнатною температурою та 70 °C. Сполуки типу VI можуть також бути заміщені при азоті шляхом реакції з відповідним алкілюючим реагентом, як от an алкіл бромід або алкіл хлорид, у присутності основи, як от карбонат калію, триетиламін, або 1,8-диазабіцикло[5.4.0]ундец-7-ен, вибірково у присутності йодид натріюу, у розчиннику як от ацетонітрил або DMF, при температурі між кімнатною температурою та 100 °C. Далі, сполуки типу VI можуть також бути ацмльовані при азоті, з хлорид кислоти або іншим активуючим ациляцію реагентом, у присутності основи, як от 10 UA 106994 C2 5 10 N-етилдиізопропиламін, у розчиннику, як от ацетонітрил, при кімнатній температурі. Сполуки типу VI можуть також бути перетворені на азот з ефірною групою 2,2-діфторпропіонової кислоти, шляхом наступної послідовності етапів (Cheguillaume A., Lacroix S., Marchand-Brynaert J. Тетраhedron Letters 2003, 44, 2375): Перша реакція з 1H-бензотриазол-1метанолом у розчиннику як от етанол, при температурі біля 50 °C; з подальшою реакцією з реагентом цинку, одержаного із цинкового пилу, триметилсилілхлоридом та бромдіфторацетатом, у розчиннику як от тетрагідрофуран, при температурі біля 70 °C. Морфоліни типу VI можуть також бути перетворені на азот шляхом реакції з диефір вінілфосфонату, у розчиннику як от ацетонітрил при температурі біля 85 °C. Сполуки типу I де R3 = (CH2)2OPO3H2 можуть бути синтезовані, як показано на схемі 4. Схема 4 R2 R2 R1 O R2 R1 A O R1 A R4 N H R4 N O R2 R1 O A O N R4 O E O P O O E 30 OH A R4 25 N R2 R1 20 R4 O VI 15 O A N OH O P OH O Таким чином відповідний заміщений морфолін VI реагує з 2-(2-хлор-етокси)тетрагідро-2Hпіраном, у присутності основи, як от карбонат калію, та йодид натрію, у розчиннику як от DMF, при температурі біля 100 °C. Групу тетрагідро-2H-пірану видаляють шляхом обробки з кислотою, як от p-толуолсульфонова кислота, у розчиннику як от метанол, при кімнатній температурі. Утворений спирт потім обробляють реагентом фосфорамідиту, як от ди-трет-бутил N, N-диізопропилфосфорамідит, у присутності тетразолу, у суміші розчинників, як от THF, CH2Cl2, та CH3CN, при кімнатній температурі, та в подальшому окислюють з окислюючим реагентом як от пероксид водню або трет-бутилгідропероксид у таких же розчинниках, при кімнатній температурі. Частковий гідроліз ефірів фосфату може бути виконаний при умовах, що залежать від природи групи E. Наприклад ди-трет-бутил ефіри можуть бути гідролізовані шляхом обробки кислотою, як от TFA, у розчиннику, як от CH2Cl2, при кімнатній температурі. Як інший приклад, ди-етил ефіри можуть реагувати з бромтриметилсиланом у розчиннику, як от CH2Cl2, при кімнатній температурі, з подальшою обробкою з метанолом щоб впливати на гідроліз. Сполуки, де W - це -S-, -SO- або -SO2- можуть бути одержані, як описано нижче та показано на схемі 5. Схема 5 11 UA 106994 C2 R2 O R2 O Br (VIII) S S Q1 Q1 Q1 N N H R2 O O S (XII) 35 N H O R2 R1 O O S A Q1 (XIII) O (XI) O Q1 30 N O R2 O O S 25 R2 O O S R2 R2 20 W N R3 (I, W = S, SO) N Q2 (X) (IX) N H A Q1 15 (IX) R2 R1 S Q1 N H O R2 10 S Q1 Q1 5 R2 S N Q2 (I, W = SO2) N R3 Q1 - це група, еквівалентна R1-A, або група, яка може бути перетворена на R1-A. Q2 - це група, еквівалентна R3, або група, яка може бути перетворена на R3. Детальніше, див. наведене нижче. Синтез починається з відповідно заміщеного ефіру бром-феніл-оцтової кислоти. Відповідно заміщені ефіри бром-феніл-оцтової кислоти є доступними на ринку або можуть бути одержані згідно зі способами, відомими з літератури. Ефір бром-феніл-оцтової кислоти реагує з 2аміноетантіолом, у присутності основи, як от карбонат калію, у розчиннику як от етанол, при кімнатній температурі, одержуючи 2-арил-тіоморфолін-3-они (VIII). Ці тіоморфолін-3-они можуть потім бути відновлені з відновлюючим засобом, як от боран, у розчиннику, як от тетрагідрофуран, при температурі між 0 °C та кімнатною температурою, даючи 2-арилтіоморфоліни (IX). Тіоморфоліни (IX) можуть реагувати з ефіром (мет)акрилової кислоти, у так названій реакції Майкла, у розчиннику, як от ацетонітрил, метанол, або N, N-диметил-формамід, при температурі між кімнатною температурою та 85 °C, та потім з додаванням деякої основи, як от триетиламін або 1,8-диазабіцикло[5.4.0]ундец-7-ен, даючи ефіри морфолін-4-іл-пропіонової кислоти (X, Q2=CH2CH2COOR"). Якщо ці ефіри тіоморфолін-4-іл-пропіонової кислоти (X, Q2=CH2CH2COOR") є заміщені бромом (X, Q1=Br), бром може бути заміщений йодом (X, Q1=I) у реакції з йодидом натрію, каталізований йодидом міді(I), у присутності N, Nдиметилетилендиаміну, у розчиннику, як от 1,4-диоксан, при температурі біля 130 °C, у закритій посудині. В подальшому, йод (X, Q1=I), може бути заміщений відповідним спиртом, у присутності основи, як от карбонат цезію, та каталізований йодидом міді(I) та 1,10фенантроліном, у розчиннику, як от толуол, при температурі біля 110 °C, одержуючи сполуки, у яких Q1 еквівалентний R1-A, а Q2=CH2CH2COOR". У випадку, якщо R" - це трет-бутил, ефір може бути гідролізований кислотою, як от соляна кислота, у розчиннику, як от 1,4-диоксан, при температурі між кімнатною температурою та 80 °C, даючи сполуки (I, W=S). Тіоморфоліни (X, W=S, Q1=R1-A, Q2=CH2CH2COOR"), можуть бути окислені з окислюючим реагентом, як от калій ® пероксимоносульфат (Оксоne ), у розчиннику, як от метанол/вода, при температурі між 0 °C та кімнатною температурою, даючи тіоморфолін 1-оксиди (X, W=SO, Q1=R1-A, Q2=CH2CH2COOR"). У випадку, коли R" - це трет-бутилова кислота, гідроліз, описаний для тіоморфолінів, дає сполуки (I, W=SO). Тіоморфоліни (IX) можуть бути захищені при азоті з відповідною захисною групою (P.G.M. Wuts, T.W. Greene Protective groups in organic synthesis, 4th ed., John Wiley & Sons, 2006), як от трет-бутилоксикарбоніл (BOC), шляхом реакції з ди-трет-бутил дикарбонатом у розчиннику, як от ацетонітрил, при кімнатній температурі. В подальшому, тіоморфоліни можуть бути окислені з окислюючим реагентом, як от 3-хлорпероксибензойна кислота, у розчиннику як от дихлорметан, 12 UA 106994 C2 5 10 15 20 25 30 35 40 45 50 55 60 при температурі між 0 °C та кімнатною температурою, одержуючи тіоморфолін 1,1-диоксиди (XI). Після чого група трет-бутилоксикарбонілу (BOC) може бути видалена шляхом обробки з кислотою, як от хлорид водню, у розчиннику, як от етанол, при температурі між кімнатною температурою та 60 °C, даючи модифікованиі 1,1-диоксиди тіоморфоліну (XII). 1,1-Диоксиди тіоморфоліну можуть потім реагувати у так названій реакції Майкла, як описано вище для тіоморфолінів, одержуючи сполуки XIII (Q2=CH2CH2COOR"). Якщо сполуки XIII заміщені бромом (Q1=Br), вони можуть бути заміщені відповідним спиртом, у присутності основи, як от карбонат цезію, та каталізовані каталізатором паладію, як от Pd(AcO) 2, та відповідним лігандом фосфіну, у розчиннику, як от толуол, при температурі біля 100 °C, одержуючи сполуки XIII (W=SO2, Q1=R1-A, Q2=CH2CH2COOR"). Якщо R" - це трет-бутилова кислота, гідроліз, описаний для тіоморфолінів, дає сполуки (I, W=SO2). Скорочення ACE-Cl 1-Хлоретил хлороформат AcCl Ацетил хлорид AlCl3 Алюміній хлорид 9-BBN 9-борабіцикло[3.3.1]нонан димер BH3∙THF Комплекс боран тетрагідрофуран n-BuLi n-Бутил літій nBu4NBr Тетрабутиламоній хлорид CHCl3 Хлороформ CH2Cl2 Дихлорметан CH3CN Ацетонітрил Cs2CO3 Карбонат цезію CuBr2 Бромід міді(II) CuI Йодид міді(I) DBU 1,8-Диазабіцикло[5.4.0]ундец-7-ен DIAD Диізопропил азодикарбоксилат DIPEA N, N-Диізопропилетиламін DMF N, N-диметилформамід DMSO Диметил сульфоксид Et3N Триетиламін Et2O Диетил етер EtOH Етанол EtOAc Етил ацетат HCl Хлорид водню H2SO4 Сірчана кислота K2CO3 Карбонат калію KHCO3 Бікарбонат калію KI Йодид калію KOH Гідроксид калію KOtBu трет-бутоксид калію LiAlH4 Алюмогідрид літію LiHMDS Літій біс(триметилсиліл)амід LiOH Гідроксид літію MeI Метил йодид MeMgBr Бромід метилмагнію MeOH Метанол min. хвилини NaBH4 Борогідрид натрію NaHCO3 Бікарбонат натрію NaI Йодид натрію NaN3 Азид натрію NaOH Гідроксид натрію NaOtBu трет-бутоксид натрію Na2SO4 Сульфат натрію NBS N-Бромсукцинімід PBr3 Трибромід фосфору Pd2dba3 Трис(дибензиліденацетон)дипаладій(0) Pd(dppf)Cl2 [1,1’-біс(дифенілфосфін)ферроцен]дихлорпаладій(II) PdCl2(PPh3)2 Біс(трифенілфосфін)паладій(II) дихлорид Pd(PPh3)4 Тетракіс(трифенілфосфін)паладій(0) iPr2O Диізопропил етер 13 UA 106994 C2 5 10 RT Кімнатна температура SiO2 Силікагель TFA Трифтороцтова кислота THF Тетрагідрофуран TMSCl Хлортриметилсилан TMSOTf Триметилсиліл трифторметансульфонат p-TsOH Моногідрат p-толуолсульфонової кислоти ZrCl4 Тетрахлорид цирконію §3. СИНТЕЗ ПРОМПКНИХ СПОЛУК Арил(ТІО)морфолінИ O O 15 20 1-(4-Октилокси-феніл)-етанон: До розчину 4'-гідроксиацетофенону (25.0 г; 183.6 ммоль) у DMSO (300. мл) додають KOH (11.3 г; 201.9 ммоль.) та реакційну суміш перемішують 1 годину при RT. Після 1 години реакційну суміш охолоджують (0 °C) та додають 1-бромоктан (34.9 мл; 201.9 ммоль). Льодову баню видаляють та реакційну суміш перемішують усю ніч при RT. Реакційну суміш екстрагують з EtOAc/ 5 % водний NaHCO3 розчин. Органічний шар висушують з Na2SO4 та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O: гексан 1:3) даючи 1-(4-октилокси-феніл)-етанон (43.08 г) O O 25 1-(4-бензилокси-2-метилфеніл)-етанон: Суміш 4'-гідрокси-2’-метилацетофенону (24.88 г; 165.7 ммоль)), KI (5.50 г; 33.1 ммоль), K2CO3 (34.3 г; 248.5 ммоль) та бензил броміду (21.7 мл; 182.2 ммоль) у ацетоні (200 мл) перемішують усю ніч при RT. В подальшому одержану суміш фільтрують та розділяють між EtOAc та 5 % водним NaHCO3. Органічний шар висушують (Na2SO4), фільтрують та концентрують у вакуумі, даючи 1-(4-бензилокси-2-метилфеніл)-етанон, який використовують як є. 30 O O 35 40 1-(4-бензилокси-3-метилфеніл)-етанон: Суміш 4'-гідрокси-3’-метилацетофенону (10.00 г; 66.6 ммоль) та K2CO3 (13.80 г; 99.9 ммоль) у ацетоні (100 мл) перемішують, при RT 40 хвилин. В подальшому, додають бензил бромід (7.9 мл; 66.6 ммоль) та одержану суміш нагрівають зі зворотнім холодильником 2,5 год. Після охолодження до RT суміш концентрують у вакуумі. Осад розчиняють у EtOAc, промивають з 5 % водним амонієм, водою, та розсолом, висушують (MgSO4), фільтрують та концентрують у вакуумі, даючи 1-(4-бензилокси-3-метилфеніл)-етанон (15.86 г). Наступні сполуки одержують відповідно подібним чином: 1-(4-Бензилокси-3-метокси-феніл)-етанон 14 UA 106994 C2 F F F O O 5 1-(4-Бензилокси-3-трифторметил-феніл)-етанон: Суміш бензилового спирту (10.9 мл; 104.98 ммоль) та KOtBu (12.96 г; 115.5 ммоль) у THF (500 мл) нагрівають зі зворотнім холодильником 10 хвилин. В подальшому, додають 4'-фтор-3'-(трифторметил)ацетофенон (21.64 г; 105 ммоль) та суміш нагрівають зі зворотнім холодильником іще 2 години. Після охолодження до RT, суміш розділяють між EtOAc та 5 % водним розчином NaHCO3. Органічний шар відділяють, висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O: гексан 1:2.5) даючи 1-(4-Бензилокси-3-трифторметил-феніл)-етанон (22.37 г). 10 F F F O O 15 20 O S O Метансульфонова кислота 4-ацетил-3-трифторметил-феніл ефір: До розчину 1-(4-гідрокси2-трифторметил-феніл)-етанону (29.74 г; 145.7 ммоль) у CH2Cl2 (300 мл) та THF (120 мл) додають Et3N (24.4 мл; 174.8 ммоль), при 0 °C. До одержаної суміші додають по краплинах розчин метансульфоніл хлориду (12. 5 мл; 160.3 ммоль) у CH 2Cl2 (60 мл), при 0 °C. В подальшому суміш перемішують усю ніч при RT, та виливають у крижану воду. Шари відділяють та органічний шар промивають з 1 M водним HCl та водою; висушують (MgSO 4), фільтрують та концентрують у вакуумі, даючи 4-ацетил-3-трифторметил-феніл ефір метансульфонової кислоти (40.47 г), який використовують як є. Наступні сполуки одержують аналогічним чином: 4-Ацетил-2-хлор-феніл ефір метансульфонової кислоти 4-Ацетил-3-фтор-феніл ефір метансульфонової кислоти O Cl 25 30 O 1-(2-Хлор-4-метокси-феніл)-етанон До суміші AlCl3 (42.08 г; 315.60 ммоль) у CH2Cl2 (300 мл) додають по краплинах 3-хлоранізол (22.50 г; 157.80 ммоль), при -30 °C. До одержаної суміші додають по краплинах розчин AcCl (10.50 мл; 147.63 ммоль) у CH2Cl2 (100 мл) у такому співвідношенні, щоб тримати температуру нижче -15 °C. Одержану суміш перемішують 4 години при -10 °C. В подальшому, суміш виливають на кригу та екстрагують з CH2Cl2. Поєднані органічні шари, висушують (MgSO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O/гексан 1:9) даючи 1-(2-хлор-4-метокси-феніл)-етанон (17.68 г). 35 O O 40 Br 2-Бром-1-(4-октилокси-феніл)-етанон: До розчину 1-(4-октилокси-феніл)-етанону (43.0 г; 173.1 ммоль) у EtOAc (200 мл) додають CuBr2 (77.3 г; 346.2 ммоль) та нагрівають до температури зворотнього холодильника 2 години. Реакційну суміш фільтрують крізь Кизельгуром. Реакційну суміш промивають з 10 % водним розчином натрій тіосульфату та 15 UA 106994 C2 розсолу. Органічний шар висушують над Na2SO4, концентрують у вакуумі та очищують колонковою хроматографією (SiO2, Et2O: гексан 1:7)) даючи 2-бром-1-(4-октилокси-феніл)етанон (36.3 г) O Br O 5 10 15 1-(4-Бензилокси-2-метил-феніл)-2-бром-етанон: До розчину 1-(4-бензилокси-2-метилфеніл)етанону (42.00 г; 174.8 ммоль) у MeOH (300 мл) додають тетра-N-бутиламоній трибромід (84.28 г; 174.8 ммоль) та суміш перемішують усю ніч при RT. В подальшому, MeOH випарюють у вакуумі, та осад розділяють між EtOAc (300 мл) та 5 % водним NaHCO3. Органічний шар висушують (Na2SO4), фільтрують, концентрують у вакуумі та очищують колонковою хроматографією (SiO2, Et2O: гексан 1:1) даючи 1-(4-бензилокси-2-метил-феніл)-2-бром-етанон (49.93 г). Наступну сполуку одержують згідно з подібним шляхом: 1-(4-Бензилокси-3-трифторметилфеніл)-2-бром-етанон O Br O 20 25 30 1-(4-Бензилокси-3-метил-феніл)-2-бром-етанон: До розчину 1-(4-бензилокси-3-метил-феніл)етанону (12.89 г; 53.1 ммоль) у CH2Cl2 додають, по краплинах, при 0 °C, DIPEA (10.9 мл; 63.7 ммоль) та триметилсиліл трифторметансульфонат (11.1 мл; 61.1 ммоль). Одержану суміш перемішують при 0 °C 1 годину, та в подальшому, NBS (10.87 г; 61.1 ммоль) додають однією порцією. Суміші дають нагрітися до RT, перемішуючи усю ніч. Потім суміш концентрують у вакуумі, осад розчиняють у EtOAc, промивають з водою двічі, та розсолом, висушують (MgSO 4), фільтрують, та концентрують у вакуумі, даючи 1-(4-бензилокси-3-метил-феніл)-2-бром-етанон (11.90 г). Наступну сполуку одержують згідно з подібним шляхом: 1-(4-Бензилокси-3-метокси-феніл)-2-бром-етанон 4-(2-Бром-ацетил)-3-трифторметил-феніл ефір метансульфонової кислоти 4-(2-Бром-ацетил)-2-хлор-феніл ефір метансульфонової кислоти 4-(2-Бром-ацетил)-3-фтор-феніл ефір метансульфонової кислоти 1-(3-Бензилокси-феніл)-2-бром-етанон 2-Бром-1-(2-хлор-4-метокси-феніл)-етанон 2-Бром-1-(5-бром-pyriдиn-2-іл)-етанон 35 +N O N N O 40 2-азидо-1-(4-бензилокси-феніл)-етанон До суміші 1-(4-бензилокси-феніл)-2-бром-етанону (28.55 г; 93.6 ммоль) у CH2Cl2 (300 мл) та воді (30 мл) додають nBu4NBr (1.51 г; 4.7 ммоль) та NaN3 (6.69 г; 102.9 ммоль) однією порцією. Після 4 год. при RT, шари відділяють. Органічний шар промивають з водою, висушують (Na2SO4), фільтрують та концентрують у вакуумі, даючи 2-азидо-1-(4-бензилокси-феніл)-етанон (23.64 г). 16 UA 106994 C2 F F F O O 5 10 15 O S O 4-Оксираніл-3-трифторметил-феніл ефір метансульфонової кислоти: До розчину 4-(2-бромацетил)-3-трифторметил-феніл ефіру метансульфонової кислоти (33.95 г; 89.3 ммоль) у 1,4диоксані (150 мл) додають по краплинах розчин NaBH 4 (2.37 г; 62.5 ммоль) у воді (47 мл). Одержану суміш перемішують при RT 2.5 години, в подальшому, гасять з 0.5M водної HCl (125 мл), та екстрагують зEtOAc. Поєднані органічні шари промивають з водою, висушують (MgSO4), фільтрують та концентрують у вакуумі. Осад розчиняють у Et 2O (500 мл) та обробляють з розчином KOH (4.19 г; 74.7 ммоль) у воді (100 мл). Одержану суміш нагрівають зі зворотнім холодильником 4 години. Після охолодження до RT, літучі компоненти видаляють у вакуумі та осад розділяють між EtOAc та водою. Органічний шар промивають з водою, висушують (MgSO4), фільтрують та концентрують у вакуумі. Осад очищують колонковою хроматографією (CH2Cl2), даючи 4-оксираніл-3-трифторметил-феніл ефір метансульфонової кислоти (23.54 г). Наступні сполуки одержують аналогічним чином: 4-Оксираніл-3-фтор-феніл ефір метансульфонової кислоти 4-Оксираніл-2-хлор-феніл ефір метансульфонової кислоти 2-(2-Хлор-4-метокси-феніл)-оксиран OH NH2 O 20 25 2-Аміно-1-(4-бензилокси-феніл)-етанол: До суспензії LiAlH4 (8.18 г; 215.6 ммоль) у THF (100 мл), додають по краплинах розчин 2-азидо-1-(4-бензилокси-феніл)-етанону (23.05 г; 86.2 ммоль) у THF (200 мл), при 0 °C. Суміш перемішують при 0 °C 20 хвил. та в подальшому 2 години при RT. Після цього, послідовно додають воду (50 мл), та 2M водний розчин NaOH (150 мл). Утворений осад видаляють фільтрацією над кизельгуром, та промивають з MeOH. Фільтрат концентрують у вакуумі та водний шар, що лишився, екстрагують з CH 2Cl2. Поєднані органічні шари висушують (Na2SO4), фільтрують та концентрують у вакуумі, даючи 2-аміно-1-(4бензилокси-феніл)-етанол (20.10 г). 30 OH H N O 35 40 45 2-Бензиламіно-1-(4-октилокси-феніл)-етанол: До охолодженої (0 °C) суспензії 2-Бром-1-(4октилокси-феніл)-етанону (36.1 г; 110.3 ммоль) у EtOH (500 мл) та CHCl 3 (100 мл) додають бензиламін (48.2 мл; 441.2 ммоль). Після 30 хвилин водяну баню видаляють та суміш перемішуючи іще 2 години при RT. В подальшому реакційну суміш охолоджують знову до 0 °C та додають NaBH4 (6.26 г; 165.5 ммоль) малими порціями. Одержану суміш перемішують при 0 °C 1 годину, а після цього іще 4 години при RT. Реакційну суміш гасять з 1M водним HCl (750 мл) при 0 °C та перемішуючи при RT 1 годину. Реакційну суміш концентрують у вакуумі та осад розділяють між EtOAc та 2 N водного NaOH. Органічний шар висушують (Na 2SO4), фільтрують, концентрують у вакуумі, та очищують колонковою хроматографією (SiO 2, EtOAc), даючи 2бензиламіно-1-(4-октилокси-феніл)-етанол (22.58 г) Наступні сполуки одержують згідно з подібним шляхом: 2-Бензиламіно-1-(4-бром-феніл)-етанол 2-Бензиламіно-1-(4-бензилокси-феніл)-етанол 17 UA 106994 C2 5 2-Бензиламіно-1-(4-бензилокси-2-метил-феніл)-етанол 2-Бензиламіно-1-(4-бензилокси-3-метил-феніл)-етанол 2-Бензиламіно-1-(4-бензилокси-3-трифторметил-феніл)-етанол 2-Бензиламіно-1-(4-бензилокси-3-метокси-феніл)-етанол 2-Бензиламіно-1-(3-бензилокси-феніл)-етанол 2-(Бензгідрил-аміно)-1-(5-бром-піридин-2-іл)-етанол F F F OH O 10 15 20 H N O S O 4-(2-Бензиламіно-1-гідрокси-етил)-3-трифторметил-феніл ефір метансульфонової кислоти: 4-оксираніл-3-трифторметил-феніл ефір метансульфонової кислоти (23.54 г; 79.2 ммоль) розчиняють у бензиламіні (26 мл). Одержану суміш перемішують при 80 °C 4 год. Після охолодження до RT, додають Et2O та суміш охолоджують до 0 °C. Утворений осад збирають фільтрацією, промивають з Et2O, and висушують під вакуумом, при 40 °C, даючи на виході 4-(2бензиламіно-1-гідрокси-етил)-3-трифторметил-феніл ефір метансульфонової кислоти у якості білої твердої речовини (26.87 г) який використовують як є. Наступні сполуки одержують подібним шляхом: 4-(2-Бензиламіно-1-гідрокси-етил)-3-фтор-феніл ефір метансульфонової кислоти 4-(2-Бензиламіно-1-гідрокси-етил)-2-хлор-феніл ефір метансульфонової кислоти 2-Бензиламіно-1-(2-хлор-4-метокси-феніл)-етанол OH NH2 O 25 30 1-Аміно-2-(4-бензилокси-феніл)-пропан-2-ол: Суміш 1-(4-бензилокси-феніл)-етанон (18.50 г; 81.8 ммоль), йодид цинку (0.52 г; 1.6 ммоль), та триметилсиліл цианід (33.8 мл; 269.8 ммоль) перемішують усю ніч при RT. В подальшому, надлишок триметилсиліл цианіду видаляють у вакуумі, а осад розчиняють у THF (100 мл). Одержаний розчин додають, по краплинах, до суміші алюмогідриду літію (12.7 г; 335.2 ммоль) у THF (200 мл). Одержану суміш нагрівають зі зворотнім холодильником 2 год. Далі, суміш охолоджують до 0 °C та ретельно перемішують з водою (13 мл), 2M водниого NaOH (26 мл), та водою (13 мл). Після цього суміш нагрівають зі зворотнім холодильником 15 хвилин, охолоджують знову до RT, фільтрують над кизельгуром, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, MeOH) даючи 1Аміно-2-(4-бензилокси-феніл)-пропан-2-ол (18.15 г). OH H N O 35 40 1-Бензиламіно-2-(4-бензилокси-феніл)-пропан-2-ол: Суміш 1-аміно-2-(4-бензилокси-феніл)пропан-2-олу (1.26 г; 4.9 ммоль), бензальдегіду (0.55 мл; 5.4 ммоль), та p-толуолсульфонової кислоти (0.04 г; 0.24 ммоль) у толуолі (30 мл) нагрівають зі зворотнім холодильником у апараті Діна-Старка, усю ніч. В подальшому, суміш охолоджують до RT та розчинник видаляють у вакуумі. Осад суспендують у MeOH (30 мл), охолоджують до -15 °C, та обробляють з NaBH4 (0.74 г; 19.6 ммоль), порціонно. Після завершення додавання суміш нагрівають до RT, перемішуючи одну годину. В подальшому, MeOH видаляють у вакуумі. Осад розділяють між 18 UA 106994 C2 Et2O та 5 % водним NaHCO3. Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O: гексан 2:1), одержуючи 1-бензиламіно-2-(4-бензилокси-феніл)-пропан-2-ол (1.07 г). O O N 5 10 15 20 25 30 O 4-Бензил-6-(4-октилокси-феніл)-морфолін-3-он: До розчину 2-бензиламіно-1-(4-октилоксифеніл)-етанолу (22.50 г; 63.3 ммоль) та Et3N (9.7 мл; 69.6 ммоль) у CH2Cl2 (500 мл) додають по краплинах розчин хлориду хлорацетилу (5.5 мл; 69.6 ммоль) у CH 2Cl2 (25 мл), при 0 °C. Після 1 години при 0 °C реакційну суміш гасять з 1M водним HCl (200 мл). Шари відділяють та органічний шар промивають з 5 % водним розчином NaHCO3, висушують (Na2SO4) та концентрують у вакуумі. Осад розчиняють у 2-пропанолі (250 мл) та додають KOH (4.26 г; 76 ммоль). Одержану суміш перемішують при RT 1 годину та в подальшому концентрують у вакуумі. Сирий продукт розділяють між EtOAc та 0.5 M водного HCl. Шари відділяють та органічний шар промивають з 5 % водним розчином NaHCO3, висушують (Na2SO4) та випарюють у вакуумі, даючи 4-бензил-6-(4-октилокси-феніл)-морфолін-3-он (22.30 г) який використовують як є на наступному етапі. Наступні сполуки одержують згідно з подібним шляхом: 4-Бензил-6-(4-бром-феніл)-морфолін-3-он 4-Бензил-6-(4-бензилокси-феніл)-морфолін-3-он 4-Бензил-6-(4-бензилокси-2-метил-феніл)-морфолін-3-он 4-Бензил-6-(4-бензилокси-3-метил-феніл)-морфолін-3-он 4-Бензил-6-(4-бензилокси-3-метокси-феніл)-морфолін-3-он 4-Бензил-6-(4-бензилокси-3-трифторметил-феніл)-морфолін-3-он 4-Бензил-6-(4-бензилокси-феніл)-6-метил-морфолін-3-он 4-Бензил-6-(3-бензилокси-феніл)-морфолін-3-он 4-Бензил-6-(2-хлор-4-метокси-феніл)-морфолін-3-он 4-Бензгідрил-6-(5-бром-піридин-2-іл)-морфолін-3-он Наступні сполуки одержують згідно з подібним шляхом із феніл ефірів метансульфонової кислоти використовуючи 2.5 еквівалентів KOH замість 1.25 еквівалентів. 4-Бензил-6-(4-гідрокси-2-трифторметил-феніл)-морфолін-3-он 4-Бензил-6-(2-фтор-4-гідрокси-феніл)-морфолін-3-он 4-Бензил-6-(3-хлор-4-гідрокси-феніл)-морфолін-3-он Cl OH O NH O 35 40 N-[2-(4-Бензилокси-феніл)-2-гідрокси-етил]-2-хлор-ацетамід: До суміші 2-аміно-1-(4бензилокси-феніл)-етанолу (20.10 г; 82.6 ммоль), Et3N (13.82 мл; 99.1 ммоль), CH2Cl2 (200 мл) та MeOH (20 мл) додають по краплинах хлорацетил хлорид (7.24 мл; 90.9 ммоль) при -10 °C. Одержаній суміші дають нагрітися до RT, перемішуючи усю ніч, і в подальшому концентрують у вакуумі. Осад очищують випарювальною хроматографією (SiO 2, EtOAc) даючи N-[2-(4бензилокси-феніл)-2-гідрокси-етил]-2-хлор-ацетамід (17.45 г). 19 UA 106994 C2 O O NH O 5 6-(4-Бензилокси-феніл)-морфолін-3-он: До розчину KOtBu (6.68 г; 59.5 ммоль) у 2-метил-2бутанолі (100 мл) додають по краплинах розчин N-[2-(4-бензилокси-феніл)-2-гідрокси-етил]-2хлор-ацетаміду (17.30 г; 54.1 ммоль) у THF (100 мл). Одержану суміш перемішують 1 годину при RT та потім концентрують у вакуумі. Осад розчиняють у CH2Cl2 та обробляють з 1M водного розчину HCl, при 0 °C. Шари відділяють та водний шар екстрагують зCH 2Cl2. Поєднані органічні шари висушують (Na2SO4), фільтрують та концентрують у вакуумі, даючи 6-(4-бензилоксифеніл)-морфолін-3-он (14.10 г). 10 O O N N O 15 20 O O O 4-Бензил-6-(4-бензилокси-феніл)-2,2-диметил-морфолін-3-он та 4-Бензил-6-(4-бензилоксифеніл)-2-метил-морфолін-3-он: До розчину 4-бензил-6-(4-бензилокси-феніл)-морфолін-3-ону (6.90 г; 18.5 ммоль) у THF (100 мл) додають по краплинах розчин LiHMDS у THF (18.5 мл; 1.00 моль/л; 18.5 ммоль), при -78 °C. Одержану суміш перемішують при -78 °C 15 хвилин, в подальшому, MeI (1.15 мл; 18.5 ммоль) додають, а одержану суміш перемішують 1 годину при 78 °C. Послідовність додавання LiHMDS та MeI, повторюють тричі. Після останнього додавання MeI суміші дають нагрітися до RT та перемішують усю ніч. Потім додають 5 % водний розчин NaHCO3 та суміш екстрагують зEtOAc. Поєднані органічні шари висушують (Na2SO4), фільтрують та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O/гексан 1:1) даючи дві сполуки. Найменш полярна сполука - це 4-бензил-6-(4-бензилоксифеніл)-2,2-диметил-морфолін-3-он (1.90 г), а найбільш полярна сполука - це 4-бензил-6-(4бензилокси-феніл)-2-метил-морфолін-3-он (3.81 г). 25 S NH O Br 30 2-(4-Бром-феніл)-тіоморфолін-3-он: До розчину гідрохлориду 2-аміноетанттіолу (6.93 г; 61 ммоль) у EtOH (400 мл) додають K2CO3 (16.86 г; 122 ммоль), при RT, а через 15 хвилин додають етил ефір бром-(4-бром-феніл)-оцтової кислоти (12 мл; 61 ммоль). Одержану суміш перемішують при RT два дні, в подальшому, додають воду та одержану суміш екстрагують з EtOAc. Поєднані органічні шари висушують (MgSO4), фільтрують, та концентрують у вакуумі. Осад рекристалізують із EtOH, одержуючи 2-(4-бром-феніл)-тіоморфолін-3-он (12.8 г). O N 35 O 4-Бензил-2-(4-октилокси-феніл)-морфолін: До 20 розчину 4-бензил-6-(4-октилокси-феніл) UA 106994 C2 5 10 15 морфолін-3-ону (22.22 г; 56.2 ммоль) у THF (400 мл) додають комплекс боран-THF (1M, 140.4 мл; 140.4 ммоль) по краплинах, при 0 °C. Через 1 годину суміші дають нагрітися до RT та перемішують іще 2 години. До реакційної суміші додають MeOH (30 мл), при 0 °C, та одержану суміш перемішують при RT 30 хвилин, та в подальшому концентрують у вакуумі. Осад суспендують у MeOH (300 мл.) та додають 1 M водного NaOH (112 мл) і нагрівають зі зворотнім холодильником 1 годину. Одержану суміш концентрують у вакуумі, а осад розділяють між EtOAc та 5 % водним розчином NaHCO3. Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі, одержуючи 4-бензил-2-(4-октилокси-феніл)-морфолін (20.33 г), який використовують як є на наступному етапі. Наступні сполуки одержують згідно з подібним шляхом: 4-Бензил-6-(4-бром-феніл)-морфолін 4-Бензил-2-(4-бензилокси-феніл)-морфолін 4-Бензил-2-(4-бензилокси-2-метил-феніл)-морфолін 4-Бензил-2-(4-бензилокси-3-метил-феніл)-морфолін 4-Бензил-2-(4-бензилокси-3-метокси-феніл)-морфолін 4-Бензил-2-(4-бензилокси-3-трифторметил-феніл)-морфолін 4-Бензил-2-(4-бензилокси-феніл)-2-метил-морфолін 4-Бензил-6-(4-бензилокси-феніл)-2,2-диметил-морфолін 4-Бензгідрил-2-(5-бром-піридин-2-іл)-морфолін 20 F F F O N HO 25 30 35 4-(4-Бензил-морфолін-2-іл)-3-трифторметил-фенол: До розчину 4-бензил-6-(4-гідрокси-2трифторметил-феніл)-морфолін-3-ону (26.18 г; 67.3 ммоль) у THF (600 мл) додають по краплинах BH3∙THF у THF (235.4 мл; 1.00 моль/лl; 235.4 ммоль), при 0 °C. Одержану суміш перемішують 1 годину при 0 °C та після цього 18 години при RT. В подальшому, 1M водний HCl (550 мл) додають та суміш перемішують усю ніч при RT. Одержану суміш розділяють між EtOAc та 2M водного NaOH (350 мл), органічні шари висушують (MgSO 4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, CH2Cl2/MeOH 98:2), одержуючи 4(4-бензил-морфолін-2-іл)-3-трифторметил-фенол Наступні сполуки одержують згідно з подібним шляхом: 4-(4-Бензил-морфолін-2-іл)-3-фтор-фенол 4-Бензил-2-(3-бензилокси-феніл)-морфолін 4-Бензил-2-(2-хлор-4-метокси-феніл)-морфолін 2-(4-Бром-феніл)-тіоморфолін O Cl N HO 40 45 4-(4-Бензил-морфолін-2-іл)-2-хлор-фенол: До розчину 4-бензил-6-(3-хлор-4-гідрокси-феніл)морфолін-3-ону (13.05 г; 39.0 ммоль) у THF (600 мл) додають порціонно LiAlH4 (4.44 г; 117.04 ммоль) при 0 °C. Одержаній суміші дають нагрітися до RT та перемішують усю ніч. В подальшому, суміш охолоджують до 0 °C, та додають послідовно воду (4.5 мл), 2M водний розчин NaOH (9.0 мл) та воду (9.0 мл).Після цього суміш перемішують 1 год. Утворений осад видаляють фільтрацією над кизельгуром, та промивають з EtOAc. Органічний розчин концентрують у вакуумі, та осад очищують колонковою хроматографією (SiO 2, CH2Cl2/MeOH 98:2) одержуючи 4-(4-бензил-морфолін-2-іл)-2-хлор-фенол (9.10 г) 21 UA 106994 C2 Cl O N HO 5 10 4-(4-Бензил-морфолін-2-іл)-3-хлор-фенол: До розчину 1 додекантіолу (12.7 мл; 52.86 ммоль) у сухому DMF (50 мл), додають KOtBu (5.93 г; 52.86 ммоль) при 0 °C. Після завершення додавання суміші дають повільно дійти до RT (~30 хвил), та потім додають 4-бензил-2-(2-хлор4-метокси-феніл)-морфолін (5.60 г; 17.62 ммоль). Одержану суміш перемішують при 110 °C 6 годин. Після охолодження до RT, додають EtOAc та одержану суміш промивають з 5 % водним NaHCO3, водою та розсолом; висушують (MgSO4), фільтрують та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, CH2CL2/MeOH 99:1) одержуючи 4-(4-бензилморфолін-2-іл)-3-хлор-фенол (4.56 г). O N O 15 20 4-Бензил-2-(4-бензилокси-феніл)-5,5-диметил-морфолін До розчину 4-бензил-6-(4-бензилокси-феніл)-морфолін-3-ону (7.14 г; 19.1 ммоль) у THF (100 мл) додають ZrCl4 (4.46 г; 19.1 ммоль), при -10 °C. Одержану суміш перемішують 30 хвил. при 10 °C, в подальшому, розчин MeMgBr у Et2O (38.2 мл; 3.00 моль/л; 114.6 ммоль) додають по краплинах, тримаючи температуру нижче 10 °C. Після завершення додавання одержану суміш перемішують при RT 1 годину. Після охолодження суміші до 0 °C додають по краплинах 2M водного розчину NaOH. Одержану суспензію фільтрують та фільтрат екстрагують тричі з CH2Cl2. Поєднані органічні шари висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O/гексан 1:3), одержуючи 4-бензил-2-(4бензилокси-феніл)-5,5-диметил-морфолін (3.6 г). O N 25 30 35 HO 4-(4-Бензил-морфолін-2-іл)-фенол: До суспензії 4-бензил-6-(4-бром-феніл)-морфоліну (8.70 г; 26.19 ммоль) у воді (25 мл) та 1,4-диоксані (25 мл) додають KOH (3.23 г; 57.61 ммоль), трис(дибензиліденацетон)дипаладій(0) (479.6 мг; 0.52 ммоль) та ди-трет-бутил-(2',4',6'триізопропил-біфеніл-2-іл)-фосфан (444.8 мг; 1.05 ммоль). Одержану суміш нагрівають зі зворотнім холодильником дві години. Після охолодження до RT реакційну суміш концентрують у вакуумі. Осад розділяють між EtOAc та 5 % водним розчином NaHCO3. Органічний шар висушують (Na2SO4), фільтрують та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O: гексан 1:1) одержуючи 4-(4-бензил-морфолін-2-іл)-фенол (3.67 г). 6-(4-Бензгідрил-морфолін-2-іл)-піридин-3-ol одержують подібним способом. O N O 40 4-Бензил-2-(4-гексилокси-феніл)-морфолін: До суміші 4-(4-бензил-морфолін-2-іл)-фенолу (1.33 г; 4.94 ммоль) у воді (10 мл) та 1,4-диоксані (10 мл) додають KOH (0.55 г; 9.88 ммоль), 1 22 UA 106994 C2 5 бромгексан (1.04 мл; 7.41 ммоль) та тетрабутиламоній бромід (0.16 г; 0.49 ммоль), одержану суміш нагрівають зі зворотнім холодильником усю ніч. Після охолодження до RT суміш концентрують у вакуумі, та розділяють між EtOAc та 5 % водним розчином NaHCO3. Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O: гексан 1:1) одержуючи 4-бензил-2-(4-гексилокси-феніл)-морфолін (1.31 г). 4-Бензил-2-(4-гептилокси-феніл)-морфолін одержують згідно з подібним шляхом. O Cl N Cl O Cl 10 15 20 4-Бензил-2-[3-хлор-4-(2,6-дихлор-бензилокси)-феніл]-морфолін: Суміш 4-(4-бензилморфолін-2-іл)-2-хлор-фенолу (0.50 г; 1.56 ммоль), 2,6-дихлорбензил броміду (0.39 г; 1.64 ммоль) та Cs2CO3 (2.55 г; 7.82 ммоль) у CH3CN (20 мл) нагрівають зі зворотнім холодильником усю ніч. Після охолодження до RT одержану суміш розділяють між EtOAc та водою. Шари відділяють та органічний шар, висушують (MgSO 4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, CH2Cl2:MeOH 98:2) одержуючи 4-бензил-2[3-хлор-4-(2,6-дихлор-бензилокси)-феніл]-морфолін (0.74 г). Наступні сполуки одержують згідно з подібним шляхом: 4-Бензил-2-[3-хлор-4-(2-хлор-6фтор-бензилокси)-феніл]-морфолін 4-Бензил-2-[3-хлор-4-(2-трифторметил-бензилокси)-феніл]морфолін O N 25 30 4-Бензил-2-(4-октил-феніл)-морфолін: До розчину 1-октену (2.12 мл, 13.5 ммоль) у THF (50 мл) додають 9-BBN (4.3g, 17,6 ммоль), при 0 °C. Реакційній суміші дають нагрітися до RT та перемішують усю ніч. В подальшому, додають K3PO4 (7.6 g, 35.8 ммоль), потім, після 45 хвилин, додають 4-бензил-6-(4-бром-феніл)-морфолін (3.0 g, 9 ммоль), паладій(II) ацетат (80мг; 4моль%), та дициклогексил-(2',6'-диметокси-біфеніл-2-іл)-фосфан (296мг; 8моль%). Одержану суміш нагрівають зі зворотнім холодильником 2 години. Після охолодження до RT суміш концентрують у вакуумі, осад розчиняють у EtOAc, та промивають з 5 % водним розчином NaHCO3. Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O: гексан, 1:1) одержуючи 4-бензил-2-(4-октилфеніл)-морфолін (2.58г). O N H 35 40 O 4-(4-Бензил-морфолін-2-іл)-бензальдегід: До розчину 4-бензил-6-(4-бром-феніл)-морфоліну (1.73 г; 5.21 ммоль) у THF (25 мл) додають по краплинах n-BuLi (2.08 мл; 2.50 моль/л; 5.21 ммоль), при -78 °C. Одержану суміш перемішують одну годину, та в подальшому додають по краплинах розчин N-формилморфоліну (0.90 г; 7.81 ммоль) у THF (5 мл), при -78 °C. Реакцію гасять додаванням 5 % водного розчину NaHCO3, при -70 °C. Одержану суміш екстрагують з Et2O. Поєднані органічні шари висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O: гексан 1:1) одержуючи 4-(4-бензилморфолін-2-іл)-бензальдегід (1.21 г). 23 UA 106994 C2 O N HO 5 10 [4-(4-Бензил-морфолін-2-іл)-феніл]-метанол: До розчину 4-(4-бензил-морфолін-2-іл)бензальдегіду (1.19 г; 4.23 ммоль) у MeOH (25 мл) додають NaBH 4 (0.16 г; 4.23 ммоль), малими порціями, при 0 °C. Після завершення додавання суміші дають нагрітися до RT та перемішують одну годину. В подальшому, суміш охолоджують до 0 °C, додають воду, та випарюють у вакуумі MeOH. До водного розчину додають 5 % водний розчин NaHCO3 та EtOAc. Шари відділяють та органічний шар висушують (Na2SO4), фільтрують та концентрують у вакуумі, одержуючи [4-(4бензил-морфолін-2-іл)-феніл]-метанол (1.16 г), який використовують як є. O N Cl O Cl 15 20 4-Бензил-2-[4-(2,6-дихлор-феноксиметил)-феніл]-морфолін: До розчину 2,6-дихлорфенол (0.68 г; 4.19 ммоль) у THF (20 мл) додають DIAD (1.13 мл; 5.72 ммоль), та трифенілфосфін (1.50 г; 5.72 ммоль), при RT, потім, через 30 хвилин, [4-(4-бензил-морфолін-2-іл)-феніл]-метанол (1.08 г; 3.81 ммоль). В подальшому, одержану суміш перемішують при RT 1 годину, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O: гексан 1:1) одержуючи 4бензил-2-[4-(2,6-дихлор-феноксиметил)-феніл]-морфолін (2.35 г), який використовують як є на наступному етапі. Наступну сполуку одержують згідно з подібним шляхом: 4-Бензил-2-[2-хлор-4-(2,6-дихлор-бензилокси)-феніл]-морфолін O Cl N H N Cl O 25 30 4-(4-Бензил-морфолін-2-іл)-N-(2,6-дихлор-феніл)-бензамід: До розчину 4-бензил-6-(4-бромфеніл)-морфоліну (1.01 г; 3.04 ммоль) у THF (25 мл) додають по краплинах n-BuLi (1.2 мл; 2.5 моль/л у гексані; 3.04 ммоль), при -78 °C. Через 1 годину при -78 °C, додають по краплинах розчин 2,6-дихлорфеніл ізоціанату (0.63 г; 3.34 ммоль) у THF (5 мл). Суміші дають нагрітися до RT та потім додають 5 % водний NaHCO3. В подальшому, суміш екстрагують з Et2O. Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (Et2O:гексан 1:1) одержуючи 4-(4-бензил-морфолін-2-іл)-N-(2,6-дихлор-феніл)бензамід (0.68 г). O N Cl 35 Cl 24 UA 106994 C2 5 10 4-Бензил-2-{4-[2-(2,6-дихлор-феніл)-вініл]-феніл}-морфолін: До суспензії (2,6-дихлорбензил)-трифеніл-фосфоній броміду (2.06 г; 4.1 ммоль) (Див.: A. Schmidpeter, H. Noeth, G. Jochem, H.-P. Schroedel, K. Karaghiosoff; Chem. Ber., 1995, 128, 379) у THF (25 мл) додають гідрид натрію (60 % дисперсія у мінеральнії олії) (215 мг; 4.5 ммоль), при 0 °C. Після перемішування 1 годину, додають 4-(4-бензил-морфолін-2-іл)-бензальдегід (1.05 г; 3.7 ммоль), при 0 °C. В подальшому, одержану суміш нагрівають зі зворотнім холодильником 1 годину. Після охолодження до RT, 5 % додають водний NaHCO3 та суміш екстрагують з Et2O. Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O: гексан 1:1), одержуючи 4-бензил-2-{4-[2-(2,6-дихлорфеніл)-вініл]-феніл}-морфолін (1.15 г). O N Cl Cl 15 20 4-Бензил-2-[4-(2,6-дихлор-бензил)-феніл]-морфолін: До суміші хлориду 2,6дихлорбензилцинку (7.95 мл; 0.50 моль/л у THF; 3.97 ммоль) та тетракіс(трифенілфосфін)паладію(0) (83.48 мг; 0.07 ммоль) у THF (25 мл) додають 4-бензил-6(4-бром-феніл)-морфолін (1.20 г; 3.61 ммоль). Одержану суміш перемішують при RT 2 години, та в подальшому нагрівають зі зворотнім холодильником, 2 год. Після охолодження до RT суміш концентрують у вакуумі. Осад розділяють між 5 % водним NaHCO3 та EtOAc.Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O: гексан 1:1), одержуючи 4-бензил-2-[4-(2,6-дихлор-бензил)-феніл]морфолін (1.40 г). O N O 25 30 2-[4-(4-Бензил-морфолін-2-іл)-феніл]-1-феніл-етанон: До дегазованого розчину 4-бензил-2(4-бром-феніл)-морфоліну (205 мг; 0.62 ммоль) та ацетофенону (87 µL; 0.74 ммоль) у толуолі (4 мл) додають NaOtBu (148.3 мг; 1.54 ммоль), 2,2'-біс(дифенілфосфін)-1,1'-бінафтил (38.4 мг; 0.06 ммоль) та трис(дибензиліденацетон)дипаладій(0) (28.3 мг; 0.03 ммоль). Одержану суміш нагрівають до 110 °C 30 хвил. у мікрохвилях. Після охолодження до кімнатної температури додають 5 % водний NaHCO3 та суміш екстрагують зEtOAc. Поєднані органічні шари висушують (Na2SO4), фільтрують та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O / гексан 1:1) одержуючи 2-[4-(4-Бензил-морфолін-2-іл)-феніл]-1-феніл-етанон (110.00 мг). 35 O N N 40 Бензгідриліден-[4-(4-бензил-морфолін-2-іл)-феніл]-амін: До дегазованого розчину 4-бензил6-(4-бром-феніл)-морфоліну (4.00 г; 12.04 ммоль) у толуолі (50 мл) додають бензофенон імін (2.42 мл; 14.45 ммоль), 2,2'-біс(дифенілфосфін)-1,1'-бінафтил (0.60 г; 0.96 ммоль), трис(дибензиліденацетон)-дипаладій(0) (0.22 г; 0.24 ммоль) та NaOtBu (1.62 г; 16.86 ммоль). Одержану суміш нагрівають до 100 °C 16 годин. Після охолодження до RT додають 5 % водний 25 UA 106994 C2 NaHCO3 розчин, та продукт екстрагують з EtOAc. Поєднані органічні шари висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O: гексан 1:1) одержуючи бензгідриліден-[4-(4-бензил-морфолін-2-іл)-феніл]-амін (3.30 г). O N 5 10 H2 N 4-(4-Бензил-морфолін-2-іл)-феніламін: До розчину бензгідриліден-[4-(4-бензил-морфолін-2іл)-феніл]-аміну (3.30 г; 7.63 ммоль) у THF (50 мл) додають соляну кислоту (30.5 мл; 1.00 моль/л у воді; 30.5 ммоль). Одержану суміш перемішують усю ніч при RT. Реакційну суміш розділяють між 1M водним HCl та EtOAc. Водний шар одержують основним з 1M водного NaOH (pH > 10) та екстрагують зEtOAc. Органічний шар висушують (Na2SO4), фільтрують та концентрують у вакуумі одержуючи 4-(4-бензил-морфолін-2-іл)-феніламін (1.85 г). O N Cl N H Cl 15 20 [4-(4-Бензил-морфолін-2-іл)-феніл]-(2,6-дихлор-бензил)-амін: Суміш 4-(4-бензил-морфолін2-іл)-феніламіну (0.82 г; 3.06 ммоль), DIPEA (1.57 мл; 9.17 ммоль) та 2,6-дихлорбензил бромід (0.88 г; 3.67 ммоль) у MeOH (25 мл). перемішують при RT, усю ніч. Одержану суміш розділяють між 5 % водним NaHCO3 та EtOAc. Органічний шар висушують (Na2SO4), фільтрують та концентрують у вакуумі, одержуючи [4-(4-бензил-морфолін-2-іл)-феніл]-(2,6-дихлор-бензил)амін (1.25 г). O Cl N O N H Cl 25 30 N-[4-(4-Бензил-морфолін-2-іл)-феніл]-2,6-дихлор-бензамід: До суміші 4-(4-бензил-морфолін2-іл)-феніламіну (0.48 г; 1.8 ммоль), та N-етилдиізопропиламіну (0.92 мл; 5.4 ммоль) у CH3CN (10 мл) додають 2,6-дихлорбензоїл хлорид (0.31 мл; 2.2 ммоль), при 0 °C. Одержаній суміші дають нагрітися до RT, перемішують 1 год., та розділяють між Et 2O та 5 % водним NaHCO3. Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O) одержуючи N-[4-(4-бензил-морфолін-2-іл)-феніл]-2,6дихлор-бензамід (0.61 г). O N Cl Cl 35 4-Бензил-2-{4-[2-(2,6-дихлор-феніл)-етил]-феніл}-морфолін: До дегазованого розчину калій [2-(2,6-дихлорфеніл)етил]трифторборату (0.28 г; 1 ммоль) та триосновного калій фосфату (0.58 26 UA 106994 C2 5 10 15 20 г; 2.7 ммоль) у толуолі (20 мл) та воді (4 мл) додають 4-бензил-6-(4-бром-феніл)-морфолін (0.30 г; 0.90 ммоль), паладій(II) ацетат (6.1 мг; 0.03 ммоль), та 2-дициклогексилфосфін-2',6'диізопропокси-1,1'-біфеніл (25.3 мг; 0.05 ммоль). Одержану суміш нагрівають зі зворотнім холодильником, усю ніч. Після охолодження до RT, суміш концентрують у вакуумі та розділяють між EtOAc та 5 % водний NaHCO3. Органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO 2, Et2O:гексан 1:1) одержуючи 4-бензил-2-{4-[2-(2,6-дихлор-феніл)-етил]-феніл}-морфолін (0.21 г). Бажаний калій [2-(2,6-дихлорфеніл)етил]трифторборат одержують наступним чином: До розчину 2,6-дихлорстиролу (1.58 мл; 11.6 ммоль) у THF (15 мл) додають хлор(1,5циклооктадієн)Іридій(I) димер (38.8 мг; 0.06 ммоль), 1,2-біс(дифенілфосфін)етан (46.1 мг; 0.12 ммоль) та пінаколборан (11.6 мл; 1M у THF; 11.6 ммоль). Одержану суміш перемішують при RT, усю ніч, в подальшому, концентрують у вакуумі та очищують колонковою хроматографією (SiO2, Et2O:гексан 1:3). Одержаний продукт обробляють з MeOH (56 мл), водою (14 мл), та калій біфторидом (3.43 г; 43.9 ммоль), та перемішують при RT, усю ніч. В подальшому, розчинники видаляють у вакуумі та осад обробляють з толуолом та концентрують у вакуумі. Останні етапи повторюють тричі щоб видалити усю воду. Одержану тверду частину обробляють з CH 3CN, та нагрівають при 50 °C. Осад видаляють фільтрацією та промивають з CH 3CN. Поєднані CH3CN шари концентрують у вакуумі та осад обробляють з Et2O. Утворений осад збирають фільтрацією та висушують у вакуумі, одержуючи калій [2-(2,6-дихлорфеніл)етил]трифторборат (1.12 г), який використовують як є. O O O N O O 25 Трет-бутил ефір 3-[2-(4-Бензилокси-феніл)-5-оксо-морфолін-4-іл]-пропіонової кислоти: До суміші 6-(4-бензилокси-феніл)-морфолін-3-ону (13.40 г; 47.3 ммоль) та порошкоподібного NaOH (3.78 г; 94.6 ммоль) у THF (250 мл) додають трет-бутил акрилат (13.7 мл; 94.6 ммоль). Одержану суміш перемішують при RT 2 години та в подальшому концентрують у вакуумі. Осад очищують колонковою хроматографією (SiO2, Et2O) одержуючи трет-бутил ефір 3-[2-(4бензилокси-феніл)-5-оксо-морфолін-4-іл]-пропіонової кислоти (14.20 г). 30 O NH O 35 40 45 2-(4-октилокси-феніл)-морфолін: До розчину 4-бензил-2-(4-октилокси-феніл)-морфоліну (20.22 г; 53 ммоль) у MeOH (400 мл) додають паладій гідроксид (0.74 г; 5.30 ммоль). Суміш обробляють з H2, при нормальному тиску, усю ніч. Реакційну суміш фільтрують над кизельгуром. Фільтрат промивають з розчином амонію у MeOH. Випарювання розчинника дає 2(4-октилокси-феніл)-морфолін (14.80 г), який використовують як є на наступному етапі. Наступні сполуки одержують згідно з подібним шляхом: 3-Метил-4-морфолін-2-іл-фенол 4-Морфолін-2-іл-фенол 2-(4-Октил-феніл)-морфолін 2-(4-Гексилокси-феніл)-морфолін 2-(4-Гептилокси-феніл)-морфолін 4-Морфолін-2-іл-2-трифторметил-фенол 4-(2-Метил-морфолін-2-іл)-фенол 2-Метил-4-морфолін-2-іл-фенол 2-Метокси-4-морфолін-2-іл-фенол 4-(5,5-Диметил-морфолін-2-іл)-фенол 4-Морфолін-2-іл-3-трифторметил-фенол 27 UA 106994 C2 5 3-Фтор-4-морфолін-2-іл-фенол трет-бутил ефір 3-[2-(4-гідрокси-феніл)-5-оксо-морфолін-4-іл]-пропіонової кислоти: 4-(6,6-Диметил-морфолін-2-іл)-фенол 3-Морфолін-2-іл-фенол 6-Морфолін-2-іл-піридин-3-ol O NH 10 15 20 25 30 35 40 2-(4-фенетил-феніл)-морфолін: Суміш 4-бензил-2-{4-[2-(2,6-дихлор-феніл)-вініл]-феніл}морфоліну (0.54 г; 1.27 ммоль) та паладій гідроксиду (0.04 г; 0.25 ммоль) у MeOH (25 мл) обробляють з H2, при нормальному тиску, усю ніч. Одержану суміш фільтрують над кизельгуром та розчинники випарюють, одержуючи 2-(4-фенетил-феніл)-морфолін (0.34 г). (+)-2-(4-октилокси-феніл)-морфолін та (-)-2-(4-октилокси-феніл)-морфолін: Рацемічний 2-(4-октилокси-феніл)-морфолін розділяють на обидва оптичні ізомери ® препаративною хіральною HPLC, при RT на обладнанні CHIRALPAK IA 20 μm-250 × 76 мм колонна, з мобільною фазою 99.9 % CH3CN / 0.1 % диетиламін (v/v) при рівні потоку 270 мл/хвил., та з UV-визначенням при 240 нм. Це дає після випарювання розчинників (+)-2-(425 октилокси-феніл)-морфолін (e.e. 98.3 %; [α]D = +24 (c 1.0, MeOH)) та (-)-2-(4-октилокси-феніл)25 морфолін (e.e. 99.0 %, [α]D = -28 (c 1.0, MeOH)). 2-[4-(2,6-Дихлор-феноксиметил)-феніл]-морфолін: До розчину 4-бензил-2-[4-(2,6-дихлорфеноксиметил)-феніл]-морфоліну (2.25 г; 3.7 ммоль) у 1,2-дихлоретані (10 мл), додають по краплинах 1-хлоретил хлороформат (0.44 мл; 4.0 ммоль), при 0 °C. Через 15 хвилин, охолодження зупиняють та в подальшому суміш нагрівають зі зворотнім холодильником усю ніч. Після охолодження до RT суміш концентрують у вакуумі. До осаду додають толуол та суміш концентрують у вакуумі. Цей останній етап повторюють двічі. До фінального осаду додають MeOH (10 мл), та цю суміш перемішують усю ніч при RT. Іще раз суміш концентрують у вакуумі. Осад розділяють між EtOAc та 2 M водним NaOH. Шари відділяють, та органічний шар висушують (Na2SO4), фільтрують, та концентрують у вакуумі, одержуючи 2-[4-(2,6-Дихлорфеноксиметил)-феніл]-морфолін (0.98 г), який використовують як є на наступному етапі. Наступні сполуки одержують згідно з подібним шляхом: N-(2,6-Дихлор-феніл)-4-морфолін-2-іл-бензамід 2-{4-[2-(2,6-Дихлор-феніл)-вініл]-феніл}-морфолін (2,6-Дихлор-бензил)-(4-морфолін-2-іл-феніл)-амін 2,6-Дихлор-N-(4-морфолін-2-іл-феніл)-бензамід 2-{4-[2-(2,6-Дихлор-феніл)-етил]-феніл}-морфолін 2-[4-(2,6-дихлор-бензил)-феніл]-морфолін 2-[3-Хлор-4-(2,6-дихлор-бензилокси)-феніл]-морфолін 2-[3-Хлор-4-(2-хлор-6-фтор-бензилокси)-феніл]-морфолін 2-[3-Хлор-4-(2-трифторметил-бензилокси)-феніл]-морфолін 2-[2-Хлор-4-(2,6-дихлор-бензилокси)-феніл]-морфолін 2-(4-Морфолін-2-іл-феніл)-1-феніл-етанон O N O HO 45 O Трет-бутил ефір 2-(4-гідрокси-феніл)-морфолін-4-карбоксильної кислоти: Суміш 4-морфолін2-іл-фенолу (0.99 г; 5.41 ммоль) та ди-трет-бутил дикарбонату (1.18 г; 5.41 ммоль) у CH3CN (50 мл) перемішують при RT 3 дні. В подальшому, одержану суміш концентрують у вакуумі та осад очищують колонковою хроматографією (SiO2, CH2Cl2:CH3OH 97:3), одержуючи трет-бутил ефір 2-(4-гідрокси-феніл)-морфолін-4-карбоксильної кислоти (1.15 г). 28
ДивитисяДодаткова інформація
Назва патенту англійською(thio)morpholine derivatives as s1p modulators
Автори англійськоюIwema Bakker, Wouter I., Coolen, Hein K.A.C., Mons, Harmen, Stoit, Axel, Ronken, Eric, Kam, van der Elizabeth, Frankena, Jurjen
Автори російськоюИвема Баккер Воутер И., Коолен Гэйн К.А.К., Монс Гармен, Стойт Аксель, Ронкен Эрик, Кам ван дер Элизабет, Фрапкена Юрьен
МПК / Мітки
МПК: A61P 25/18, C07D 279/12, A61P 25/06, A61P 25/28, C07D 265/32, C07D 417/12, A61P 25/16, A61P 25/04, A61K 31/5377, C07D 413/12, C07D 419/00, A61P 25/24, C07D 471/04, C07D 265/30, C07D 487/04
Мітки: модулятори, тіоморфоліну, похідні
Код посилання
<a href="https://ua.patents.su/92-106994-pokhidni-tiomorfolinu-yak-modulyatori-s1p.html" target="_blank" rel="follow" title="База патентів України">Похідні (тіо)морфоліну як модулятори s1p</a>












