Сполуки, що сприяють росту гематопоетичних стовбурових клітин
Номер патенту: 103206
Опубліковано: 25.09.2013
Автори: Теллью Джон, Ванг Ксінг, Шульц Пітер Г., Бойтено Ентоні, Пан Шіфенг, Кук Майкл, Ван Йонгцін
Формула / Реферат
1. Сполука Формули Іа:
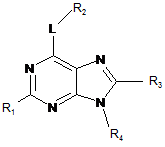 , Іa
, Іa
у якій:
L вибирають з таких як: -NR5a(CH2)2-3-, -NR5aCH(C(O)OCH3)CH2-, -NR5a(CH2)2NR5b-, -NR5a(CH2)2S-, -NR5aCH2CH(CH3)CH2-, -NR5aCH2CH(OH)- або -NR5aCH(CH3)CH2-; де R5a та R5b незалежно вибирають з таких як: водень або С1-4алкіл;
R1 вибирають з таких як: тіофеніл, фураніл, 1H-бензоімідазоліл, ізохінолініл, 1H-імідазопіридиніл, бензотіофеніл, піримідиніл, піридиніл, 1Н-імідазоліл, піразиніл, піридазиніл, 1Н-піроліл або тіазоліл; де зазначені тіофеніл, фураніл, 1Н-бензоiмідазоліл, ізохінолініл, 1Н-імідазопіридиніл, бензотіофеніл, піримідиніл, піридиніл, 1Н-імідазоліл, піразиніл, піридазиніл, 1Н-піроліл або тіазоліл радикала R1 можуть бути необов'язково заміщені за допомогою 1-3 радикалів, що незалежно вибирають з таких як: ціаногрупа, гідроксигрупа, С1-4алкіл, С1-4алкоксигрупа, галоген, галогензаміщений С1-4алкіл, галогензаміщена-С1-4алкоксигрупа, аміногрупа, -C(O)R8a, -S(O)0-2R8a, -C(O)OR8a або -C(O)NR8aR8b; де R8a та R8b незалежно вибирають з таких як: водень або С1-4алкіл;
R2 вибирають з таких як: -S(O)2NR6aR6b, -NR6aC(O)R6b, -NR6aC(O)NR6bR6c, феніл, 1Н-піролопіридин-3-іл, 1Н-піролопіридин-5-іл, 1Н-індоліл, тіофеніл, піридиніл, 1Н-1,2,4-триазоліл, 2-оксоімідазолідиніл, 1Н-піразоліл, 2-оксо-2,3-дигідро-1H-бензоімідазоліл або 1Н-індазоліл; де
R6a, R6b та R6c незалежно вибирають з таких як: водень або С1-4алкіл;
зазначені феніл, 1Н-піролопіридин-3-іл, 1Н-піролопіридин-5-іл, 1-H-індоліл, тіофеніл, піридиніл, 1Н-1,2,4-триазоліл, 2-оксоімідазолідиніл, 1Н-піразоліл, 2-оксо-2,3-дигідро-1Н-бензоімідазоліл або 1Н-індазоліл радикала R2 необов'язково заміщені за допомогою 1-3 радикалів, що незалежно вибирають з таких як: гідроксигрупа, галоген, метил, метоксигрупа, аміногрупа, -O(CH2)2NR7aR7b, -S(O)2NR7aR7b, -OS(O)2NR7aR7b або -NR7aS(O)2R7b; де R7a та R7b незалежно вибирають з таких як: водень або С1-4алкіл;
R3 вибирають з таких як: водень, С1-4алкіл або біфеніл;
R4 вибирають з таких як: С1-10алкіл, проп-1-ен-2-іл, циклогексил, циклопропіл, 2-(2-оксопіролідин-1-iл)етил, оксетан-2-іл, оксетан-3-іл, бензгідрил, тетрагідро-2Н-піран-3-іл, тетрагідро-2Н-піран-2-іл, феніл, тетрагiдрофуран-3-іл або бензил; де
зазначені алкіл, циклопропіл, циклогексил, 2-(2-оксопіролідин-1-іл)етил, оксетан-3-іл, оксетан-2-іл, бензгідрил, тетрагідро-2Н-піран-2-іл, тетрагідро-2Н-піран-3-іл, феніл, тетрагідрофуран-3-іл або бензил можуть бути необов'язково заміщені за допомогою 1-3 радикалів, що незалежно вибирають з таких як: гідроксигрупа, С1-4алкіл або галогензаміщений С1-4алкіл;
або її сіль.
2. Сполука за п. 1, у якій
R1 вибирають з таких як: тіофен-2-іл, тіофен-3-іл, фуран-3-іл, 1Н-бензо[d]імідазол-1-іл, ізохінолін-4-іл, 1Н-імідазо[4,5-b]піридин-1-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, піридин-2-іл, піридин-4-іл, 1H-імідазол-1-іл, піразин-2-іл, піридин-3-іл, піридазин-4-іл, 1Н-пірол-2-іл або тіазол-5-іл; де
зазначені тіофен-2-іл, тіофен-3-іл, фуран-3-іл, 1Н-бензо[d]імідазол-1-іл, ізохінолін-4-іл, 1Н-імідазо[4,5-b]піридин-1-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, піридин-2-іл, піридин-4-іл, 1Н-імідазол-1-іл, піразин-2-іл, піридин-3-іл, піридазин-4-іл, 1Н-пірол-2-іл або тіазол-5-іл радикала R1 можуть бути необов'язково заміщені за допомогою 1-3 радикалів, що незалежно вибирають з таких як: ціаногрупа, С1-4алкіл, С1-4алкоксигрупа, галоген, галогензаміщений С1-4алкіл, -S(O)0-2R8a або -C(O)OR8a; де R8a вибирають з таких як: водень або С1-4алкіл;
R2 вибирають з таких як: -NR6aC(O)NR6bR6c, феніл, 1Н-піроло[2,3-b]піридин-3-іл, 1Н-піроло[2,3-b]піридин-5-іл, 1Н-індол-3-іл, тіофен-3-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1Н-1,2,4-триазол-5-іл, 1Н-1,2,4-триазол-3-іл, 2-оксоімідазолідин-1-іл, 1Н-піразол-3-іл, 1Н-піразол-4-іл, 2-оксо-2,3-дигідро-1Н-бензо[d]імідазол-5-іл або 1Н-індазол-3-іл; де
R6a, R6b та R6c незалежно вибирають з таких як: водень або С1-4алкіл;
зазначені феніл, 1H-піроло[2,3-b]піридин-3-іл, 1Н-піроло[2,3-b]піридин-5-іл, 1Н-індол-3-іл, тіофен-3-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1Н-1,2,4-триазол-5-іл, 1Н-1,2,4-триазол-3-іл, 2-оксоімідазолідин-1-іл, 1Н-піразол-3-іл, 1Н-піразол-4-іл, 2-оксо-2,3-дигідро-1Н-бензо[d]імідазол-5-іл або 1Н-індазол-3-іл радикала R2 необов'язково заміщені за допомогою 1-3 радикалів, що незалежно вибирають з таких як: гідроксигрупа, галоген, метил, метоксигрупа, аміногрупа, -OS(O)2NR7aR7b або -NR7aS(O)2R7b;
де R7a та R7b незалежно вибирають з таких як: водень або С1-4алкіл;
R3 являє собою водень;
R4 вибирають з таких як: ізопропіл, метил, етил, проп-1-ен-2-іл, ізобутил, циклогексил, втор-бутил, (S)-втор-бутил, (R)-втор-бутил, 1-гідроксипропан-2-іл, (S)-1-гідроксипропан-2-іл, (R)-1-гідроксипропан-2-іл, нонан-2-іл, 2-(2-оксопіролідин-1-іл)етил, оксетан-3-іл, оксетан-2-іл, бензгідрил, феніл, тетрагідрофуран-3-іл або бензил; де
зазначені циклогексил, 2-(2-оксопіролідин-1-іл)етил, оксетан-3-іл, оксетан-2-іл, бензгідрил, феніл, тетрагідрофуран-3-іл або бензил можуть бути необов'язково заміщені за допомогою 1-3 радикалів, що незалежно вибирають з таких як: С1-4алкіл або галогензаміщений С1-4алкіл.
3. Сполука за п. 1 або п. 2, у якій
L вибирають з таких як: -NHCH2)2-3-, -NH(CH2)2NH-, -NH(CH2)2S-, -NHCH(CH3)CH2- або -NHCH2CH(OH)-.
4. Сполука за п. 1 або п. 2, у якій
L являє собою -NH(CH2)2-.
5. Сполука за будь-яким з пп. 1-4, у якій
R2 вибирають з таких як: феніл, 1Н-індол-3-іл, тіофен-3-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1Н-1,2,4-триазол-3-іл, 1Н-1,2,4-триазол-5-іл, 2-оксоімідазолідин-1-іл, 1Н-піразол-3-іл, 1Н-піразол-4-іл або 2-оксо-2,3-дигідро-1Н-бензо[d]імідазол-5-іл; де
зазначені феніл, 1H-індол-3-іл, тіофен-3-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H-1,2,4-триазол-3-іл, 1H-1,2,4-триазол-5-іл, 2-оксоімідазолідин-1-іл, 1H-піразол-3-іл, 1Н-піразол-4-іл або 2-оксо-2,3-дигідро-1H-бензо[d]імідазол-5-іл радикала R2 є необов'язково заміщеними за допомогою гідроксигрупи, метоксигрупи, метилу, галогену або аміногрупи.
6. Сполука за будь-яким з пп. 1-5, у якій
R4 вибирають з таких як: ізопропіл, метил, етил, проп-1-ен-2-іл, ізобутил, циклогексил, втор-бутил, (S)-втор-бутил, (R)-втор-бутил, 1-гідроксипропан-2-іл, (S)-1-гідроксипропан-2-іл, (R)-1-гідроксипропан-2-іл, нонан-2-іл.
7. Сполука за п. 1, що має формулу Ia:
 , Ia
, Ia
у якій
L являє собою -NН(CН2)2-;
R1 вибирають з таких як: тіофен-2-іл, тіофен-3-іл, фуран-3-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, піридин-2-іл, піридин-4-іл, 1Н-імідазол-1-іл, піразин-2-іл, піридин-3-іл, піридазин-4-іл, 1Н-пірол-2-іл або тіазол-5-іл; де
зазначені тіофен-2-іл, тіофен-3-іл, фуран-3-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, піридин-2-іл, піридин-4-іл, 1Н-імідазол-1-іл, піразин-2-іл, піридин-3-іл, піридазин-4-іл, 1H-пірол-2-іл або тіазол-5-іл радикала R1 можуть бути необов'язково заміщені за допомогою 1-3 радикалів, що незалежно вибирають з таких як: ціаногрупа, гідроксигрупа, С1-4алкіл, С1-4алкоксигрупа, галоген, галогензаміщений С1-4алкіл, -S(O)0-2R8a або -C(O)OR8a; де R8a вибирають з таких як: водень або С1-4алкіл;
R2 вибирають з таких як: феніл, 1Н-індол-3-іл, тіофен-3-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1Н-1,2,4-триазол-5-іл, 2-оксоімідазолідин-1-іл, 1Н-піразол-3-іл, 1H-піразол-4-іл або 2-оксо-2,3-дигідро-1Н-бензо[d]імідазол-5-іл; де
зазначені феніл, 1Н-індол-3-іл, тіофен-3-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1Н-1,2,4-триазол-5-іл, 2-оксоімідазолідин-1-іл, 1Н-піразол-3-іл, 1Н-піразол-4-іл або 2-оксо-2,3-дигідро-1Н-бензо[d]імідазол-5-іл радикала R2 є необов'язково заміщеними за допомогою 1-3 радикалів, що незалежно вибирають з таких як: гідроксигрупи, галоген, метоксигрупи, аміногрупа, -OS(O)2NR7aR7b або -NR7aS(O)2R7b, де R7a та R7b вибирають з таких як: водень або С1-4алкіл;
R3 являє собою водень;
R4 вибирають з таких як: ізопропіл, ізобутил, втор-бутил, 1-гідроксипропан-2-іл, оксетан-3-іл, оксетан-2-іл, бензгідрил, тетрагідро-2Н-піран-2-іл, феніл, тетрагідрофуран-3-іл або бензил; де
зазначені оксетан-3-іл, оксетан-2-іл, бензгідрил, тетрагідро-2Н-піран-2-іл, феніл, тетрагідрофуран-3-іл або бензил можуть бути необов'язково заміщені за допомогою 1-3 радикалів, що незалежно вибирають з таких як: С1-4алкіл або галогензаміщений С1-4алкіл.
8. Сполука за п. 1, яку вибирають з групи, яка складається з таких як:
4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-втор-бутил-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-бензгідрил-2-(бензо[b]тіофен-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-(тетрагідро-2Н-піран-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(тіофен-2-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-(4-(трифторметил)бензил)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізобутил-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-метил-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-(4-метилбензил)-9Н-пурин-6-іламіно)етил)фенол;
N-(2-(1Н-індол-3-іл)етил)-2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9Н-пурин-6-амін;
2-(бензо[b]тіофен-3-іл)-9-ізопропіл-N-(2-(тіофен-3-іл)етил)-9Н-пурин-6-амін;
3-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
2-(бензо[b]тіофен-3-іл)-N-(4-фторфенетил)-9-ізопропіл-9Н-пурин-6-амін;
N-(4-амінофенетил)-2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9Н-пурин-6-амін;
4-(2-(9-ізопропіл-2-(піримідин-5-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(тіофен-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(фуран-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
2-(бензо[b]тіофен-3-іл)-N-(4-фторфенетил)-9-феніл-9Н-пурин-6-амін;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-(нонан-2-іл)-9Н-пурин-6-іламіно)етил)фенол;
N-(2-(1Н-індол-3-іл)етил)-2-(бензо[b]тіофен-3-іл)-9-втор-бутил-9Н-пурин-6-амін;
4-(2-(9-ізопропіл-2-(піридин-4-іл)-9Н-пурин-6-іламіно)етил)фенол;
етил-5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9Н-пурин-2-іл)нікотинат;
4-(2-((9-ізопропіл-2-(5-метоксипіридин-3-іл)-9Н-пурин-6-іл)аміно)етил)фенол;
4-(2-(2-(6-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(4-метилпіридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9Н-пурин-2-іл)нікотинонітрил;
4-(2-(2-(1Н-імідазол-1-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(піридазин-4-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(піразин-2-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(піридин-2-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(5-(метилсульфоніл)піридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(5-метилпіридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(4-хлорпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-((9-ізопропіл-2-(4-метилтіофен-3-іл)-9Н-пурин-6-іл)аміно)етил)фенол;
4-(2-(9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)-2-метоксифенол;
N-[2-(6-метоксі-1Н-індол-3-іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)-9Н-пурин-6-амін;
N-[2-(5-метил-1Н-індол-3-іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)-9Н-пурин-6-амін;
1-(2-{[9-(пропан-2-іл)-2-(піридин-3-іл)-9Н-пурин-6-іл]аміно}етил)імідазолідин-2-он;
N-(2-{[9-(пропан-2-іл)-2-(піридин-3-іл)-9Н-пурин-6-іл]аміно}етил)піридин-2-амін;
9-(пропан-2-іл)-N-[3-(1Н-піразол-4-іл)пропіл]-2-(піридин-3-іл)-9Н-пурин-6-амін;
N-{2-[(3-метил-1Н-1,2,4-триазол-5-іл)сульфаніл]етил}-9-(пропан-2-іл)-2-(піридин-3-іл)-9Н-пурин-6-амін;
1-(2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9Н-пурин-6-іл]аміно}етил)імідазолідин-2-он;
N-[2-(5-аміно-1Н-1,2,4-триазол-3-іл)етил]-2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9Н-пурин-6-амін;
N-(2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9Н-пурин-6-іл]аміно}етил)піридин-2-амін;
2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-N-[3-(1Н-піразол-4-іл)пропіл]-9Н-пурин-6-амін;
2-(1-бензотіофен-3-іл)-N-[3-(3,5-диметил-1Н-піразол-4-іл)пропіл]-9-(пропан-2-іл)-9Н-пурин-6-амін;
(2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9Н-пурин-6-іл]аміно}етил)сечовина;
N-[2-(1Н-індол-3-іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)-9Н-пурин-6-амін;
N-(4-(2-(9-iзoпpoпiл-2-(пipидин-3-іл)-9H-пypин-6-iлaмінo)eтил)фeнiл)мeтaнcyльфoнaмiд;
4-(2-(2-(піридин-3-іл)-9-(тетрагідрофуран-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іламіно)пропіл)фенол;
4-(2-(9-(оксетан-3-іл)-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
N-(2-(1H-iндaзoл-3-iл)eтил)-9-iзoпpoпiл-2-(пipидин-3-iл)-9H-пypин-6-aмiн;
4-(2-((9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іл)(метил)аміно)етил)фенол;
4-(2-(9-(1-гідроксипропан-2-іл)-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)фенілсульфамат;
4-(2-(2-(2-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(1-метил-1Н-пірол-2-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(тіазол-5-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(1Н-бензо[d]імідазол-1-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(2,4-диметил-1Н-імідазол-1-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(2-метил-1Н-імідазол-1-іл)-9Н-пурин-6-іламіно)етил)фенол;
5-(9-втор-бутил-6-(4-гідрокси-3-метилфенетиламіно)-9Н-пурин-2-іл)нікотинонітрил;
N-(2-(1Н-піроло[2,3-b]піридин-5-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-амін;
9-ізопропіл-N-(2-(5-метил-1Н-піразол-3-іл)етил)-2-(піридин-3-іл)-9Н-пурин-6-амін;
4-(2-(2-(5-фторпіридин-3-іл)-9-(оксетан-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(5-хлорпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(5-(трифторметил)-піридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
5-(6-(2-(1Н-індол-3-іл)етиламіно)-9-втор-бутил-9Н-пурин-2-іл)нікотинонітрил;
N-(2-(1Н-індол-3-іл)етил)-9-втор-бутил-2-(5-метилпіридин-3-іл)-9Н-пурин-6-амін;
(R)-N-(2-(1Н-індол-3-іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9Н-пурин-6-амін;
(S)-N-(2-(1Н-індол-3-іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9Н-пурин-6-амін;
N-(2-(1Н-індол-3-іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9Н-пурин-6-амін;
(R)-N-(2-(1Н-індол-3-іл)етил)-9-втор-бутил-2-(5-метилпіридин-3-іл)-9Н-пурин-6-амін;
(S)-N-(2-(1Н-індол-3-іл)етил)-9-втор-бутил-2-(5-метилпіридин-3-іл)-9Н-пурин-6-амін;
5-(6-(4-гідроксифенетиламіно)-9-(оксетан-3-іл)-9Н-пурин-2-іл)нікотинонітрил;
(R)-4-(2-(2-(5-фторпіридин-3-іл)-9-(тетрагідрофуран-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)-3-метилфенол;
5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9Н-пурин-2-іл)піколінонітрил;
3-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9Н-пурин-2-іл)ізонікотинонітрил;
3-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9Н-пурин-2-іл)піколінонітрил;
4-(2-(9-ізопропіл-2-(6-метилпіридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(ізохінолін-4-іл)-9Н-пурин-6-іламіно)етил)фенол;
2-хлор-4-(2-(9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
3-фтор-4-(2-(9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
N-(2-(5-хлор-1H-індол-3-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-амін;
N-(2-(5-фтор-1H-індол-3-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-амін;
4-(2-(9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-іламіно)етил)-2-метилфенол;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-(оксетан-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
(S)-4-(2-(2-(бензо[b]тіофен-3-іл)-9-(тетрагідрофуран-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
(R)-4-(2-(2-(бензо[b]тіофен-3-іл)-9-(тетрагідрофуран-3-іл)-9Н-пурин-6-іламіно)етил)фенол;
2-(6-(2-(1Н-індол-3-іл)етиламіно)-2-(5-фторпіридин-3-іл)-9Н-пурин-9-іл)пропан-1-ол;
(R)-2-(6-(2-(1Н-індол-3-іл)етиламіно)-2-(5-фторпіридин-3-іл)-9Н-пурин-9-іл)пропан-1-ол;
(S)-2-(6-(2-(1Н-індол-3-іл)етиламіно)-2-(5-фторпіридин-3-іл)-9Н-пурин-9-іл)пропан-1-ол;
(R)-N-(2-(1Н-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-(тетрагідрофуран-3-іл)-9Н-пурин-6-амін;
4-(2-(2-(3Н-імідазо[4,5-b]піридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(1Н-імідазо[4,5-b]піридин-1-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(2-(4,5-диметил-1Н-імідазол-1-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(піридин-3-іл)етил)-9Н-пурин-6-амін;
4-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)-1-гідроксіетил)фенол;
2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(6-метоксі-1Н-індол-3-іл)етил)-9Н-пурин-6-амін;
N-(2-(1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-амін;
2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(5-метоксі-1H-індол-3-іл)етил)-9Н-пурин-6-амін;
N-(2-(1Н-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-(проп-1-ен-2-іл)-9Н-пурин-6-амін;
5-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)піридин-2-ол;
N-(2-(1Н-піроло[2,3-b]піридин-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-амін;
N-(2-(6-(2-(дieтилaмiнo)eтoкcі)-1H-iндoл-3-iл)eтил)-2-(5-фтopпipидин-3-iл)-9-iзoпpoпiл-9H-пурин-6-амін;
N-(2-(1Н-індол-3-іл)етил)-9-втор-бутил-2-(2-метил-1Н-імідазол-1-іл)-9Н-пурин-6-амін;
4-(2-(2-(2-етил-1Н-імідазол-1-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(2-пропіл-1Н-імідазол-1-іл)-9Н-пурин-6-іламіно)етил)фенол;
3-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-іламіно)етил)-1Н-індол-6-ол;
N-(2-(1Н-індол-3-іл)етил)-9-ізопропіл-2-(5-метилпіридин-3-іл)-9Н-пурин-6-амін;
N-(2-(1Н-індол-3-іл)етил)-9-ізопропіл-2-(2-метил-1Н-імідазол-1-іл)-9Н-пурин-6-амін;
2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(7-метил-1Н-індол-3-іл)етил)-9Н-пурин-6-амін;
N-(2-(1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-(оксетан-3-іл)-9Н-пурин-6-амін;
N-(2-(1Н-індол-3-іл)етил)-2-(5-метилпіридин-3-іл)-9-(оксетан-3-іл)-9Н-пурин-6-амін;
N-(2-(6-фтор-1Н-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-амін;
2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(6-метил-1Н-індол-3-іл)етил)-9Н-пурин-6-амін;
2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(2-метил-1Н-індол-3-іл)етил)-9Н-пурин-6-амін;
N-(2-(4-фтор-1Н-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-амін;
N-(2-(7-фтор-1Н-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9Н-пурин-6-амін;
2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(4-метил-1Н-індол-3-іл)етил)-9Н-пурин-6-амін;
N-(2-(1H-піроло[2,3-b]піридин-5-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9Н-пурин-6-амін;
4-(2-(2-(5-фторпіридин-3-іл)-9-(1-гідроксипропан-2-іл)-9Н-пурин-6-іламіно)етил)-2-метилфенол;
4-(2-(2-(бензо[b]тіофен-3-іл)-9-циклогексил-9Н-пурин-6-іламіно)етил)фенол;
4-(2-(9-ізопропіл-2-(тіофен-3-іл)-9Н-пурин-6-іламіно)етил)фенол та
1-(2-(2-(бензо[b]тіофен-3-іл)-6-(4-гідроксифенетиламіно)-9Н-пурин-9-іл)етил)піролідин-2-он;
або її сіль.
9. Сполука формули:
 ,
,
або її сіль.
10. Сполука формули:
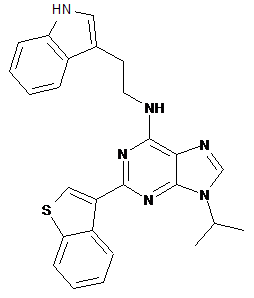 ,
,
або її сіль.
11. Сполука формули:
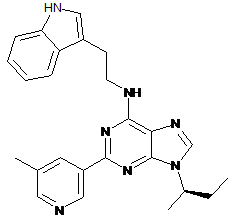 ,
,
або її сіль.
12. Сполука формули:
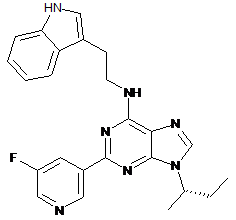 ,
,
або її сіль.
13. Сполука формули:
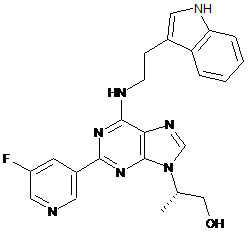 ,
,
або її сіль.
14. Застосування сполуки за будь-яким з пп. 1-13 у виготовленні композиції для підвищення кількості стовбурових клітин та клітин-попередників, де сполука являє собою агент, здатний антагонізувати активність та/або експресію арилвуглеводневого рецептора та/або нижчерозташованого ефектора шляху арилвуглеводневого рецептора.
15. Застосування за п. 14, у якому стовбурові клітини отримані від людини.
16. Застосування за п. 15, у якому стовбурові клітини отримані з кісткового мозку.
17. Застосування за п. 15, у якому стовбурові клітини отримані з пуповинної крові.
18. Застосування за будь-яким з пп. 14-17, у якому стовбурові клітини являють собою гематопоетичні стовбурові клітини.
19. Спосіб розмноження гематопоетичних стовбурових клітин, у якому
(а) беруть вихідну клітинну популяцію, що включає гематопоетичні стовбурові клітини, отримані з клітин пуповинної крові або з клітин мобілізованої периферичної крові, збагачених CD34+ клітинами, та
(b) культивують зазначену вихідну клітинну популяцію гематопоетичних стовбурових клітин ex vivo у присутності агенту, здатного антагонізувати активність та/або експресію арилвуглеводневого рецептора та/або нижчерозташованого ефектора шляху арилвуглеводневого рецептора, за прийнятних умов для розмноження гематопоетичних стовбурових клітин, де агент являє собою сполуку за будь-яким з пп. 1-13.
20. Спосіб за п. 19, у якому нижчерозташований ефектор шляху арилвуглеводневого рецептора вибирають з таких як: Сур1В1, Сур1А1, бета-катенін, АНRR, STAT5 або STAT1.
21. Спосіб за п. 19, у якому зазначену вихідну клітинну популяцію отримують з однієї або двох одиниць пуповинної крові.
22. Спосіб за п. 19, у якому клітини мобілізованої периферичної крові отримують з одного суб'єкта-ссавця.
23. Спосіб за п. 19, у якому зазначена вихідна клітинна популяція в основному складається з CD34+ клітин, очищених з однієї або двох одиниць пуповинної крові, переважно однієї одиниці пуповинної крові.
24. Спосіб за п. 19, у якому зазначена вихідна клітинна популяція в основному складається з CD34+ клітин, очищених з однієї або двох одиниць пуповинної крові, використовуючи колонки для афінної хроматографії або магнітні мікроносії, що включають фрагменти CD34 антиген зв'язуючого антитіла.
25. Спосіб за п. 19, у якому зазначені умови для розмноження гематопоетичних стовбурових клітин включають культивування зазначеної вихідної клітинної популяції у присутності достатньої кількості IL6, Flt3-L, ТРО та SCF.
26. Спосіб за п. 19, у якому сполуку за будь-яким з пп. 1-13 вводять у середовище клітинної культури при концентрації від 1 пМ до 10 мкМ.
27. Спосіб за п. 19, у якому зазначена вихідна клітинна популяція в основному складається з CD34+ клітин, очищених з однієї або двох одиниць пуповинної крові, та зазначену вихідну клітинну популяцію культивують у присутності сполуки за будь-яким з пп. 1-13 від приблизно 3 днів до приблизно 90 днів.
28. Спосіб за п. 19, у якому зазначену вихідну клітинну популяцію культивують у присутності сполуки за будь-яким з пп. 1-13 впродовж часу, достатнього для 10-50000-разового збільшення кількості CD34+ клітин.
29. Набір для розмноження гематопоетичних стовбурових клітин, що включає сполуку за будь-яким з пп. 1-13 та інструкції для застосування, та, необов'язково, один або більше з наступних: цитокіни, фактори росту або середовище росту клітин.
30. Набір за п. 29, у якому зазначений один або більшу кількість цитокінів або факторів росту вибирають з групи, що складається з IL6, Flt3-L, SCF та TРО.
31. Композиція, що містить клітинну популяцію гематопоетичних стовбурових клітин, отриману відповідно до способу за п. 19, причому композиція додатково містить сполуку за будь-яким з пп. 1-13.
32. Композиція за п. 31, яка є ресуспендованою у фармацевтично прийнятному середовищі.
33. Композиція, що містить клітинну популяцію з гематопоетичних стовбурових клітин та сполуку за будь-яким з пп. 1-13.
34. Композиція за п. 33, у якій клітинна популяція отримана з однієї або двох одиниць пуповинної крові, де зазначена композиція містить загальну кількість клітин, що становить щонайменше 105 клітин, 107 клітин, 108 клітин або 109 клітин, та де від 20-100 % від загальної кількості клітин являють собою CD34+ клітини.
35. Композиція за п. 34, де зазначена композиція містить у межах 0,1-40 % від загальної кількості клітин, що експресують CD34 та Thy1 маркери; 20-80 % від загальної кількості клітин, що експресують CD34 та СD45RA маркери; 10-95 % клітин являють собою CD38+ та 5-70 % клітин являють собою CD133+.
36. Композиція за будь-яким з пп. 31-35 для застосування у алогенній трансплантації гематопоетичних стовбурових клітин у суб'єкта-ссавця.
37. Композиція за п. 36 для лікування порушення кровотворення.
38. Композиція за п. 37, де порушення кровотворення являє собою спадковий імунодефіцит, аутоімунну хворобу або розлад кровотворення.
39. Композиція за п. 38, де зазначений розлад кровотворення вибирають з таких як: гострий мієлолейкоз, гострий лімфобластний лейкоз, хронічна мієлоїдна лейкемія, хронічна лімфоцитарна лейкемія, мієлопроліферативні розлади, мієлодиспластичні синдроми, мієломна хвороба, неходжкінська лімфома, ходжкінська хвороба, апластична анемія, істинна еритроцитарна аплазія, нічна пароксизмальна гемоглобінурія, анемія Фанконі, велика таласемія, серповидноклітинна анемія, важкий комбінований імунодефіцит, синдром Віскота-Олдрича, гемофагоцитарний лімфогістіоцитоз або вроджені порушення обміну речовин.
40. Застосування сполуки за будь-яким з пп. 1-13 для розмноження гематопоетичних стовбурових клітин, корисних для лікування спадкового імунодефіциту, аутоімунної хвороби та/або розладу кровотворення, де сполука являє собою агент, здатний регулювати у бік зменшення активність та/або експресію арилвуглеводневого рецептора.
41. Застосування за п. 40, у якому гематопоетичний розлад вибраний з таких як: мієломна хвороба, неходжкінська лімфома, ходжкінська хвороба, гострий мієлолейкоз, нейробластома, герміногенні пухлини, аутоімунні розлади та амілоїдоз.
42. Застосування за п. 41, у якому аутоімунні розлади вибирають з системного червоного вовчака та системного склерозу.
43. Застосування за п. 42, у якому гематопоетичний розлад вибраний з таких як: гострий мієлолейкоз, гострий лімфобластний лейкоз, хронічна мієлоїдна лейкемія, хронічна лімфоцитарна лейкемія, мієлопроліферативні розлади, мієлодиспластичні синдроми, мієломна хвороба, неходжкінська лімфома, ходжкінська хвороба, апластична анемія, істинна еритроцитарна аплазія, нічна пароксизмальна гемоглобінурія, анемія Фанконі, велика таласемія, серповидноклітинна анемія, важкий комбінований імунодефіцит, синдром Віскота-Олдрича, гемофагоцитарний лімфогістіоцитоз або вроджені порушення обміну речовин.
44. Застосування за п. 43, у якому вроджені порушення обміну речовин вибирають з мукополісахаридозу, хвороби Гоше, метахроматичних лейкодистрофій або адренолейкодистрофій.
Текст
Реферат: Даний винахід стосується сполук та композицій для розмноження кількості CD34+ клітин для трансплантації. Даний винахід додатково стосується клітинної популяції, що включає розмножені гематопоетичні стовбурові клітини (HSC), та її застосування у аутоімунній або алогенній UA 103206 C2 (12) UA 103206 C2 трансплантації для лікування пацієнтів із вродженим імунодефіцитом та аутоімунними хворобами та різними розладами кровотворення для відновлення послідовностей гематопоетичних клітинних поколінь та захисту імунної системи. UA 103206 C2 5 10 15 20 25 ПЕРЕХРЕСНІ ПОСИЛАННЯ ДО ЗВ'ЯЗАНИХ ЗАЯВОК Дана заявка заявляє пріоритет до Попередньої Патентної Заявки США Номер 61/109,821, поданої 30 жовтня 2008 року, та до Попередньої Патентної Заявки США Номер 61/242,765, поданої 15 вересня 2009 року. Повне розкриття цих заявок включене у даний опис шляхом посилання у їх повноті та для всіх цілей. ПЕРЕДУМОВИ СТВОРЕННЯ ВИНАХОДУ Галузь винаходу Даний винахід відноситься до сполук та композицій для розмноження CD34+ клітин для трансплантації. Даний винахід додатково відноситься до клітинної популяції, що включає розмноження гематопоетичних стовбурових клітин (HSC) та її застосування у аутологічній або алогенній трансплантації для лікування пацієнтів з вродженим імунодефіцитом та аутоімунними хворобами та різними гематопоетичними розладами для відновлення послідовностей гематопоетичних клітинних поколінь та захисту імунної системи. Попередній рівень техніки Гематопоетичні стовбурові клітини (HSC) здатні відновлювати всі продукти крові за життя індивіда, урівноважуючи їх самооновлення з диференціюванням потомства. Гематопоетичні стовбурові клітини мають терапевтичний потенціал як результат їх здатності відновлювати кров та імунні клітини у реципієнтів трансплантатів. Більше того, HSC мають потенціал створювати клітини для інших тканин, таких як мозок, м'язи та печінка. Способи аутологічної та алогенної трансплантації кісткового мозку у людини наразі використовують як терапії для лейкемії, лімфоми та інших хвороб, що загрожують життю. Для цих процедур, велика кількість стовбурових клітин повинна бути виділена для забезпечення того, що клітин HSC буде достатньо для приживлення трансплантату. Кількість HSC клітин, доступна для лікування, є клінічним обмеженням. Даний винахід відноситься до сполук та композицій для розмноження популяцій гематопоетичних стовбурових клітин та їх застосувань. КОРОТКИЙ ОПИС ВИНАХОДУ У одному аспекті, даний винахід забезпечує сполуку Формули I: R2 L G2 G3 R1 G1 G4 N R4 I 30 35 40 45 50 у якій: G1 вибирають з N та CR3; G2, G3 та G4 незалежно вибирають з CH та N; за умови, що щонайменше 1 з G3 та G4 являє собою N; за умови, що G1 та G2 обидва не являють собою N; L вибирають з таких як: –NR5a(CH2)0-3– (0-3 у цьому описі означає 0, 1, 2 або 3), –NR5aCH(C(O)OCH3)CH2–, –NR5a(CH2)2NR5b–, –NR5a(CH2)2S–, –NR5aCH2CH(CH3)CH2–, –NR5aCH2CH(OH)– та –NR5aCH(CH3)CH2–; де R5a та R5b незалежно вибирають з таких як: водень та C1-4алкіл; R1 вибирають з таких як: водень, феніл, тіофеніл, фураніл, 1H-бензоімідазоліл, ізохінолініл, 1H-імідазопіридиніл, бензотіофеніл, піримідиніл, 1H-піразоліл, піридиніл, 1H-імідазоліл, піролідиніл, піразиніл, піридазиніл, 1H-піроліл та тіазоліл; де зазначений феніл, тіофеніл, фураніл, 1H-бензоімідазоліл, ізохінолініл, 1H-імідазопіридиніл, бензотіофеніл, піримідиніл, 1Hпіразоліл, піридиніл, 1H-імідазоліл, піролідиніл, піразиніл, піридазиніл, 1H-піроліл або тіазоліл радикалу R1 може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: ціано група, гідрокси група, C 1-4алкіл, C1-4алкокси група, гало група, галозаміщений-C1-4алкіл, гало-заміщена-C1-4алкокси група, гідрокси група, аміно група, –C(O)R8a, –S(O)0-2R8a, –C(O)OR8a та –C(O)NR8aR8b; де R8a та R8b незалежно вибирають з таких як: водень та C1-4алкіл; за умови, що R1 та R3 обидва не являють собою водень; R2 вибирають з таких як: –S(O)2NR6aR6b, –NR9aC(O)R9b, –NR6aC(O)NR6bR6c, феніл, 1Hпіролопіридин-3-іл, 1H-індоліл, тіофеніл, піридиніл, 1H-1,2,4-триазоліл, 2-оксоімідазолідиніл, 1Hпіразоліл, 2-оксо-2,3-дигідро-1H-бензоімідазоліл та 1H-індазоліл; де R6a, R6b та R6c незалежно вибирають з таких як: водень та C1-4алкіл; де зазначений феніл, 1H-піролопіридин-3-іл, 1Hіндоліл, тіофеніл, піридиніл, 1H-1,2,4-триазоліл, 2-оксоімідазолідиніл, 1H-піразоліл, 2-оксо-2,3дигідро-1H-бензоімідазоліл або 1H-індазоліл радикалу R2 необов'язково заміщений за 1 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 допомогою 1-3 радикалів, що незалежно вибирають з таких як: гідрокси група, гало група, метил, метокси група, аміно група, -O(CH2)nNR7aR7b, –S(O)2NR7aR7b, –OS(O)2NR7aR7b та –NR7aS(O)2R7b; де R7a та R7b незалежно вибирають з таких як: водень та C1-4алкіл; R3 вибирають з таких як: водень, C1-4алкіл та біфеніл; та R4 вибирають з таких як: C1-10алкіл, проп-1-ен-2-іл, циклогексил, циклопропіл, 2-(2оксопіролідин-1-іл)етил, оксетан-3-іл, бензгідрил, тетрагідро-2H-піран-3-іл, тетрагідро-2H-піран4-іл, феніл, тетрагідрофуран-3-іл, бензил, (4-пентилфеніл)(феніл)метил та 1-(1-(2-оксо-6,9,12триокса-3-азатетрадекан-14-іл)-1H-1,2,3-триазол-4-іл)етил; де зазначений алкіл, циклопропіл, циклогексил, 2-(2-оксопіролідин-1-іл)етил, оксетан-3-іл, оксетан-2-іл, бензгідрил, тетрагідро-2Hпіран-2-іл, тетрагідро-2H-піран-3-іл, тетрагідро-2H-піран-4-іл, феніл, тетрагідрофуран-3-іл, тетрагідрофуран-2-іл, бензил, (4-пентилфеніл)(феніл)метил або 1-(1-(2-оксо-6,9,12-триокса-3азатетрадекан-14-іл)-1H-1,2,3-триазол-4-іл)етил може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: гідрокси група, C 1-4алкіл та галозаміщений-C1-4алкіл; або їх N-оксидні похідні, пролікарські похідні, захищені похідні, окремі ізомери та суміш ізомерів; або солі (переважно фармацевтично прийнятні солі) та сольвати (наприклад, гідрати) таких сполук. КОРОТКИЙ ОПИС МАЛЮНКІВ На Фігурі 1 показана PXRD діаграма твердотільної модифікації A 4-(2-(2-(бензо[b]тіофен-3іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенолу. На Фігурах 2-12 показані PXRD діаграми твердих форм солей 4-(2-(2-(бензо[b]тіофен-3-іл)-9ізопропіл-9H-пурин-6-іламіно)етил)фенолу, відповідно нітратна, мезилатна, тозилатна, гідрохлоридна, сульфатна, безилатна, езилатна, гідробромідна, оротатна, фумаратна та нападизилатна солі. На Фігурі 13 показана DSC діаграма аморфної форми 4-(2-(2-(бензо[b]тіофен-3-іл)-9ізопропіл-9H-пурин-6-іламіно)етил)фенолу. ДЕТАЛЬНИЙ ОПИС ВИНАХОДУ Визначення "Алкіл", як група або як структурний елемент інших груп, наприклад, таких як галозаміщений-алкіл та алкокси група, може бути або лінійно-ланцюговим або розгалуженим. Наприклад, алкіл включає метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил, третбутил, тощо. C1-4алкокси група включає метокси групу, етокси групу та подібні. Гало-заміщений алкіл включає трифторметил, пентафторетил та подібні. "Арил" являє собою моноциклічний або сконденсований біциклічний ароматичний кільцевий комплекс, що включає від шести до десяти кільцевих атомів вуглецю. Наприклад, арил може являти собою феніл або нафтил, переважно феніл. "Арилен" являє собою двовалентний радикал, одержаний з арильної групи. "Гетероарил" приймає такі значення ж що і для арилу, у якому один або більша кількість кільцевих членів являють собою гетероатом або залишок, вибраний з –O-, -N=, -NR-, -C(O) -, -S-, -S(O) - або -S(O)2-, де R являє собою водень, C1-4алкіл або азот-захисну групу. Наприклад, гетероарил включає піридил, індоліл, індазоліл, хіноксалініл, хінолініл, бензофураніл, бензопіраніл, бензотіопіраніл, бензо[1,3]діоксол, імідазоліл, бензо-імідазоліл, піримідиніл, фураніл, оксазоліл, ізоксазоліл, триaзоліл, тетразоліл, піразоліл, тієніл, тощо. "Циклоалкіл" являє собою насичений або частково ненасичений, моноциклічний, сконденсований біциклічний або містковий поліциклічний кільцевий комплекс, що містить зазначену кількість кільцевих атомів. Наприклад, C3-10циклоалкіл включає циклопропіл, циклобутил, циклопентил, циклогексил, тощо. "Гетероциклоалкіл" являє собою циклоалкіл, як визначено у даній заявці, за умови, що один або більше з зазначених кільцевих атомів вуглецю замінені залишком, вибраним з таких як: -O-, -N=, -NR-, -C(O) -, -S-, -S(O) - або -S(О)2-, де R являє собою водень, C1-4алкіл або азот-захисну групу. Наприклад, C3-8гетероциклоалкіл, як використано у даній заявці для опису сполук даного винаходу, включає морфоліно групу, піролідиніл, піперазиніл, піперидиніл, піперидинілон, 2-оксо-піролідин-1-іл, 1,4-діокса-8-азаспіро[4.5]дец-8-іл, тощо. "Галоген" (або гало) переважно являє собою хлор або фтор, але також може являти собою бром або йод. “Гематопоетичні стовбурові клітини” (HSC), як використано у цьому описі, відносяться до незрілих клітин крові, що мають здатність самооновлюватися та диференціюватися у більш зрілі клітини крові, що включають гранулоцити (наприклад, промієлоцити, нейтрофіли, еозинофіли, базофіли), еритроцити (наприклад, ретикулоцити, еритроцити), тромбоцити (наприклад, мегакаріобласти, тромбоцит-виробляючі мегакаріобласти, тромбоцити), та моноцити (наприклад, моноцити, макрофаги). У цьому описі HSC взаємозамінно називаються 2 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 стовбуровими клітинами. У даній галузі техніки відомо, що такі клітини можуть включати або не + + включати CD34 клітин. CD34 клітини являють собою незрілі клітини, які експресують CD34 клітинний поверхневий маркер. Вважають, що CD34+ клітини включають субпопуляцію клітин із властивостями стовбурових клітин, визначену вище. У даній галузі техніки добре відомо, що HSC клітини включають плюрипотентні стовбурові клітини, мультипотентні стовбурові клітини (наприклад, стовбурова лімфоїдна клітина), та/або стовбурові клітини, комітовані до специфічних послідовностей гематопоетичних клітинних поколінь. Стовбурові клітини, комітовані до специфічних послідовностей гематопоетичних клітинних поколінь, можуть бути з послідовностей T клітинних поколінь, послідовностей B клітинних поколінь, послідовностей дендритних клітинних поколінь, послідовностей клітинних поколінь Лангерганса та/або послідовностей лімфоїдних ткане-специфічних макрофагальних клітинних поколінь. Крім того, HSC клітини також відносяться до довгострокової HSC (LT-HSC) та короткострокової HSC (STHSC). ST-HSC клітини є більш активними та більш проліферативними, ніж LT-HSC. Однак, LTHSC мають необмежене самооновлення (тобто вони існують у періоді зрілості), в той час як STHSC мають обмежене самооновлення (тобто вони існують тільки впродовж обмеженого періоду часу). Будь-які з цих HSC клітин можуть бути використані у будь-якому зі способів, розкритих у цьому описі. Необов'язково, ST-HSC є корисними, тому що вони є високо проліферативними, і таким чином, швидко розмножують HSC клітини та їх нащадків. Гематопоетичні стовбурові клітини необов'язково одержують з продуктів крові. Продукт крові включає продукт, отриманий з тіла або органу тіла, що містить клітини гематопоетичного походження. Такі джерела включають нефракціонований кістковий мозок, пуповину, периферичну кров, печінку, тимус, лімфу та селезінку. Всі з зазначених вище сирих або нефракціонованих продуктів крові можуть бути збагачені клітинами, що мають характеристики гематопоетичних стовбурових клітин, шляхами, відомими спеціалістам, кваліфікованим у даній галузі техніки. "Лікувати", "що лікують" та "лікування" відноситься до способу полегшення симптомів або ослаблення хвороби та/або її супутніх симптомів. "Розмноження" у контексті клітин відноситься до збільшення кількості характеристичного клітинного типу, або клітинних типів, з початкової клітинної популяції, які можуть бути ідентифіковані або ні. Початкові клітини, що використовують для розмноження, можуть не бути однаковими з клітинами, які створюються після розмноження. "Клітинна популяція" відноситься до клітин еукаріотичного ссавця, переважно людини, що виділяють з біологічних джерел, наприклад, продуктів крові або тканин та отримують з більше ніж однієї клітини. "Збагачений" при використанні у контексті клітинної популяції відноситься до клітинної популяції, що вибирають, базуючись на присутності одного або більшої кількості маркерів, наприклад, CD34+. Термін "CD34+ клітини" відноситься до клітин, які експресують на їх поверхні CD34 маркер. CD34+ клітини можуть бути визначені та обраховані, використовуючи, наприклад, цитометрію у потоці та флуоресцентно мічені анти-CD34 антитіла. "Збагачений CD34+ клітинами" означає, що клітинну популяцію вибирають, базуючись на присутності CD34 маркеру. Відповідно, відсоток CD34+ клітин у клітинній популяції після методу відбору є більшим, ніж відсоток CD34+ клітин у початковій клітинній популяції до стадії відбору, базуючись на CD34 маркерах. Наприклад, CD34+ клітини можуть представляти щонайменше 50 %, 60 %, 70 %, 80 % або щонайменше 90 % клітин у клітинній популяції, збагаченій CD34+ клітинами. "Одиниця пуповинної крові" відноситься до крові, що збирають з пуповини одних пологів. Опис кращих варіантів втілення Даний винахід відноситься до способів та композицій для розмноження HSC клітин, використовуючи агент, здатний регулювати у бік зменшення активність та/або експресію арилвуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору. У одному варіанті втілення, зазначений агент, здатний регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору, являє собою сполуку Формули I. У одному варіанті втілення, з посиланням на сполуки Формули I, сполуки вибирають з Формул Ia, Ib, Ic, Id та Ie: 3 UA 103206 C2 R2 R2 L L N N N N R3 N N R1 R1 R4 Ib R4 Ia N N R2 R2 L L N N N R3 R3 N R1 R1 R4 Ic N N R4 Id R2 L N R1 R3 N N Ie 5 10 15 20 25 30 R4 у яких: L вибирають з таких як: –NR5a(CH2)0-3–, –NR5aCH(C(O)OCH3)CH2–, –NR5a(CH2)2NR5b–, –NR5a(CH2)2S–, –NR5aCH2CH(CH3)CH2–, –NR5aCH2CH(OH)– та –NR5aCH(CH3)CH2–; де R5a та R5b незалежно вибирають з таких як: водень та C 1-4алкіл; де правий бік L залишку, як показано, прикріплений до R2, наприклад: –NR5a(CH2)0-3–R2, –NR5aCH(C(O)OCH3)CH2–R2, –NR5a(CH2)2NR5b–R2, –NR5a(CH2)2S–R2, –NR5aCH2CH(CH3)CH2–R2, –NR5aCH2CH(OH)–R2 та –NR5aCH(CH3)CH2–R2. R1 вибирають з таких як: водень, феніл, тіофен-2-іл, тіофен-3-іл, фуран-3-іл, 1Hбензо[d]імідазол-1-іл, ізохінолін-4-іл, 1H-імідазо[4,5-b]піридин-1-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, 1H-піразол-4-іл, піридин-2-іл, піридин-4-іл, 1H-імідазол-1-іл, піролідин-1-іл, піразин-2-іл, піридин-3-іл, піридазин-4-іл, 1H-пірол-2-іл та тіазол-5-іл; де зазначений феніл, тіофен-2-іл, тіофен-3-іл, фуран-3-іл, 1H-бензо[d]імідазол-1-іл, ізохінолін-4-іл, 1H-імідазо[4,5-b]піридин-1-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, піридин-2-іл, піридин-4-іл, 1H-імідазол-1-іл, піролідин-1-іл, піразин-2-іл, піридин-3-іл, піридазин-4-іл, 1H-пірол2-іл або тіазол-5-іл радикалу R1 може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: ціано група, гідрокси група, C 1-4алкіл, C1-4алкокси група, гало група, гало-заміщений-C1-4алкіл, –S(O)0-2R8a та –C(O)OR8a; де R8a та R8b незалежно вибирають з таких як: водень та C1-4алкіл; за умови, що R1 та R3 обидва не являють собою водень; R2 вибирають з таких як: –NR6aC(O)NR6bR6c, феніл, 1H-піроло[2,3-b]піридин-3-іл, 1Hпіроло[2,3-b]піридин-5-іл, 1H-індол-3-іл, тіофен-3-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H1,2,4-триазол-5-іл, 2-оксоімідазолідин-1-іл, 1H-піразол-3-іл, 1H-піразол-4-іл, 2-оксо-2,3-дигідро1H-бензо[d]імідазол-5-іл та 1H-індазол-3-іл; де R6a, R6b та R6c незалежно вибирають з таких як: водень та C1-4алкіл; де зазначений феніл, 1H-піроло[2,3-b]піридин-3-іл, 1H-піроло[2,3-b]піридин5-іл, 1H-індол-3-іл, тіофен-3-іл піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H-1,2,4-триазол-5-іл, 2оксоімідазолідин-1-іл, 1H-піразол-3-іл, 1H-піразол-4-іл, 2-оксо-2,3-дигідро-1H-бензо[d]імідазол-5іл або 1H-індазол-3-іл радикалу R2 необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: гідрокси група, гало група, метокси група, аміно група, –OS(O)2NR7aR7b та –NR7aS(O)2R7b; де R7a та R7b незалежно вибирають з таких як: водень та C1-4алкіл; 4 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 R3 вибирають з таких як: водень, C1-4алкіл та біфеніл; та R4 вибирають з таких як: ізопропіл, метил, етил, проп-1-ен-2-іл, ізобутил, циклогексил, вторбутил, (S)-втор-бутил, (R)-втор-бутил, 1-гідроксипропан-2-іл, (S)-1-гідроксипропан-2-іл, (R)-1гідроксипропан-2-іл, нонан-2-іл, 2-(2-оксопіролідин-1-іл)етил, оксетан-3-іл, оксетан-2-іл, бензгідрил, тетрагідро-2H-піран-2-іл, феніл, тетрагідрофуран-3-іл та бензил; де зазначений циклогексил, 2-(2-оксопіролідин-1-іл)етил, оксетан-3-іл, оксетан-2-іл, бензгідрил, тетрагідро-2Hпіран-4-іл, феніл, тетрагідрофуран-3-іл або бензил може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: C 1-4алкіл та гало-заміщений-C1-4алкіл. У іншому варіанті втілення, L вибирають з таких як: –NR5a(CH2)0-3–, -NR5aCH(C(O)OCH3)CH2-, –NR5a(CH2)2NR5b–, -NR5a(CH2)2S-, -NR5aCH2CH(CH3)CH2-, -NR5aCH(CH3)CH2- та -NR5aCH2CH(OH)–; де R5a та R5b незалежно вибирають з таких як: водень та метил; та R 1 вибирають з таких як: водень, феніл, тіофен-2-іл, тіофен-3-іл, фуран-3-іл, 1H-бензо[d]імідазол-1іл, ізохінолін-4-іл, 1H-імідазо[4,5-b]піридин-1-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, 1H-піразол-4іл, піридин-2-іл, піридин-4-іл, 1H-імідазол-1-іл, піролідин-1-іл, піразин-2-іл, піридин-3-іл, піридазин-4-іл, 1H-пірол-2-іл та тіазол-5-іл; де зазначений феніл, тіофен-2-іл, тіофен-3-іл, фуран-3-іл, 1H-бензо[d]імідазол-1-іл, ізохінолін-4-іл, 1H-імідазо[4,5-b]піридин-1-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, піридин-2-іл, піридин-4-іл, 1H-імідазол-1-іл, піролідин-1-іл, піразин-2-іл, піридині-3-іл, піридазин-4-іл, 1H-пірол-2-іл або тіазол-5-іл радикалу R1 може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: ціано група, гідрокси група, C1-4алкіл, C1-4алкокси група, гало група, гало-заміщений-C1-4алкіл, –S(O)0-2R8a та –C(O)OR8a; де R8a та R8b незалежно вибирають з таких як: водень та C 1-4алкіл; за умови, що R1 та R3 обидва не являють собою водень. У іншому варіанті втілення, коли L являє собою –NR5a(CH2)0-3, кращим є –NR5a(CH2)1-3 (де 1-3 у цьому описі позначає 1, 2 або 3). У іншому варіанті втілення, R2 вибирають з таких як: сечовина, феніл, 1H-індол-2-іл, 1Hіндол-3-іл, тіофен-3-іл, піперидин-1-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H-1,2,4-триазол3-іл, 1H-1,2,4-триазол-5-іл, 2-оксоімідазолідин-1-іл, 1H-піразол-3-іл, 1H-піразол-4-іл, 2-оксо-2,3дигідро-1H-бензо[d]імідазол-5-іл, 1H-бензо[d]імідазол-5-іл та 1H-імідазол-4-іл; де зазначений феніл, 1H-індол-2-іл, 1H-індол-3-іл, тіофен-3-іл, піперидин-1-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H-1,2,4-триазол-3-іл, 1H-1,2,4-триазол-5-іл, 2-оксоімідазолідин-1-іл, 1H-піразол-3іл, 1H-піразол-4-іл, 2-оксо-2,3-дигідро-1H-бензо[d]імідазол-5-іл або 1H-бензо[d]імідазол-5-іл радикалу R2 є необов'язково заміщеним за допомогою гідрокси групи, метокси групи, метилу, гало групи, аміно групи та аміно-сульфонілу. У іншому варіанті втілення, R3 вибирають з таких як: водень, метил та біфеніл; та R 4 вибирають з таких як: ізопропіл, метил, етил, проп-1-ен-2-іл, ізобутил, циклогексил, втор-бутил, (S)-втор-бутил, (R)-втор-бутил, 1-гідроксипропан-2-іл, (S)-1-гідроксипропан-2-іл, (R)-1гідроксипропан-2-іл, нонан-2-іл, 2-(2-оксопіролідин-1-іл)етил, оксетан-3-іл, оксетан-2-іл, бензгідрил, тетрагідро-2H-піран-2-іл, феніл, тетрагідрофуран-3-іл та бензил; де зазначений циклогексил, 2-(2-оксопіролідин-1-іл)етил, оксетан-3-іл, оксетан-2-іл, бензгідрил, тетрагідро-2Hпіран-4-іл, феніл, тетрагідрофуран-3-іл або бензил може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: метил та трифторметил. У іншому варіанті втілення сполуки вибирають з таких як: 4-(2-(2-(бензо[b]тіофен-3-іл)-9ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-втор-бутил-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-бензгідрил-2-(бензо[b]тіофен-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-(тетрагідро-2H-піран-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9ізопропіл-2-(тіофен-2-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-(4(трифторметил)бензил)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9ізобутил-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-метил-9H-пурин-6іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-(4-метилбензил)-9H-пурин-6іламіно)етил)фенол; N-(2-(1H-індол-3-іл)етил)-2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6амін; 2-(бензо[b]тіофен-3-іл)-9-ізопропіл-N-(2-(тіофен-3-іл)етил)-9H-пурин-6-амін; 3-(2-(2(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 2-(бензо[b]тіофен-3-іл)-N-(4фторфенетил)-9-ізопропіл-9H-пурин-6-амін; N-(4-амінофенетил)-2-(бензо[b]тіофен-3-іл)-9ізопропіл-9H-пурин-6-амін; 4-(2-(9-ізопропіл-2-(піримідин-5-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-феніл-9Hпурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(тіофен-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4(2-(2-(фуран-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 2-(бензо[b]тіофен-3-іл)-N-(4фторфенетил)-9-феніл-9H-пурин-6-амін; N-бензил-8-(біфеніл-4-іл)-9-ізопропіл-9H-пурин-6-амін; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-(нонан-2-іл)-9H-пурин-6-іламіно)етил)фенол; N-(2-(1H-індол-3 5 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 іл)етил)-2-(бензо[b]тіофен-3-іл)-9-втор-бутил-9H-пурин-6-амін; 3-(2-(2-(бензо[b]тіофен-3-іл)-9ізопропіл-9H-пурин-6-іламіно)етил)-1H-індол-5-іл 5-((3aS, 4S, 6aR)-2-оксогексагідро-1H-тієно[3,4d]імідазол-4-іл)пентаноат; N-(2-(2-(2-(2-(4-(1-(2-(бензо[b]тіофен-3-іл)-6-(4гідроксифенетиламіно)-9H-пурин-9-іл)етил)-1H-1,2,3-триазол-1іл)етокси)етокси)етокси)етил)ацетамід; 4-(2-(9-ізопропіл-2-(піридин-4-іл)-9H-пурин-6іламіно)етил)фенол; етил 5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)нікотинат; етил 5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)нікотинат; 4-(2-(2-(6-фторпіридин3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(4-метилпіридин-3-іл)-9Hпурин-6-іламіно)етил)фенол; 5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2іл)нікотинонітрил; 4-(2-(9-ізопропіл-2-(піролідин-1-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2(1H-імідазол-1-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридазин-4іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піразин-2-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-2-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9ізопропіл-2-(5-(метилсульфоніл)піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл2-(5-метилпіридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(4-хлорпіридин-3-іл)-9-ізопропіл9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(1-метил-1H-піразол-4-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)-2метоксифенол; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)-2-метоксифенол; N[2-(6-метокси-1H-індол-3-іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-амін; N-[2-(5-метил1H-індол-3-іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-амін; 1-(2-{[9-(пропан-2-іл)-2(піридин-3-іл)-9H-пурин-6-іл]аміно}етил)імідазолідин-2-он; N-(2-{[9-(пропан-2-іл)-2-(піридин-3-іл)9H-пурин-6-іл]аміно}етил)піридин-2-амін; 9-(пропан-2-іл)-N-[3-(1H-піразол-4-іл)пропіл]-2(піридин-3-іл)-9H-пурин-6-амін; N-{2-[(3-метил-1H-1,2,4-триазол-5-іл)сульфаніл]етил}-9-(пропан2-іл)-2-(піридин-3-іл)-9H-пурин-6-амін; 1-(2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6іл]аміно}етил)імідазолідин-2-он; N-[2-(5-аміно-1H-1,2,4-триазол-3-іл)етил]-2-(1-бензотіофен-3-іл)9-(пропан-2-іл)-9H-пурин-6-амін; N-(2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6іл]аміно}етил)-піридин-2-амін; 2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-N-[3-(1H-піразол-4іл)пропіл]-9H-пурин-6-амін; 2-(1-бензотіофен-3-іл)-N-[3-(3,5-диметил-1H-піразол-4-іл)пропіл]-9(пропан-2-іл)-9H-пурин-6-амін; (2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6іл]аміно}етил)сечовина; 5-({[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6-іл]аміно}метил)2,3-дигідро-1H-1,3-бензодіазол-2-он; N-[2-(1H-індол-3-іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)9H-пурин-6-амін; N-(4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)феніл)метансульфонамід; 4-(2-(2-(піридин-3-іл)-9-(тетрагідрофуран-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)пропіл)фенол; 4-(2-(9-(оксетан-3-іл)-2(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9Hпурин-2-іл)-N-метилнікотинамід; 4-(2-(9-(1-гідроксипропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)феніл сульфамат; 4-(2-(2-(2-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9ізопропіл-2-(1-метил-1H-пірол-2-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(тіазол-5іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(1H-бензо[d]імідазол-1-іл)-9-ізопропіл-9H-пурин-6іламіно)етил)фенол; 4-(2-(2-(2,4-диметил-1H-імідазол-1-іл)-9-ізопропіл-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(2-метил-1H-імідазол-1-іл)-9H-пурин-6іламіно)етил)фенол; 5-(9-втор-бутил-6-(4-гідрокси-3-метилфенетиламіно)-9H-пурин-2іл)нікотинонітрил; N-(2-(1H-піроло[2,3-b]піридин-5-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9H-пурин6-амін; 9-ізопропіл-N-(2-(5-метил-1H-піразол-3-іл)етил)-2-(піридин-3-іл)-9H-пурин-6-амін; 4-(2-(2(5-фторпіридин-3-іл)-9-(оксетан-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(5-хлорпіридин-3іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(5-(трифторметил)піридин-3іл)-9H-пурин-6-іламіно)етил)фенол; 5-(6-(2-(1H-індол-3-іл)етиламіно)-9-втор-бутил-9H-пурин-2іл)нікотинонітрил; N-(2-(1H-індол-3-іл)етил)-9-втор-бутил-2-(5-метилпіридин-3-іл)-9H-пурин-6амін; (R)-N-(2-(1H-індол-3-іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9H-пурин-6-амін; (S)-N(2-(1H-індол-3-іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9H-пурин-6-амін; N-(2-(1H-індол-3іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9H-пурин-6-амін; (R)-N-(2-(1H-індол-3-іл)етил)-9втор-бутил-2-(5-метилпіридин-3-іл)-9H-пурин-6-амін; (S)-N-(2-(1H-індол-3-іл)етил)-9-втор-бутил2-(5-метилпіридин-3-іл)-9H-пурин-6-амін; 5-(6-(4-гідроксифенетиламіно)-9-(оксетан-3-іл)-9Hпурин-2-іл)нікотинонітрил; 4-(2-(6-(5-фторпіридин-3-іл)-1-ізопропіл-1H-піразоло[3,4-d]піримідин4-іламіно)етил)фенол; 4-(2-(6-(бензо[b]тіофен-3-іл)-1-ізопропіл-1H-піразоло[3,4-d]піримідин-4іламіно)етил)фенол; (R)-4-(2-(2-(5-фторпіридин-3-іл)-9-(тетрагідрофуран-3-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)-3-метилфенол; 5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)піколінонітрил; 3-(6-(4 6 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)ізонікотинонітрил; 4-(2-(2-(5-фторпіридин-3-іл)7-ізопропіл-7H-піроло[2,3-d]піримідин-4-іламіно)етил)фенол; 3-(6-(4-гідроксифенетиламіно)-9ізопропіл-9H-пурин-2-іл)піколінонітрил; 4-(2-(9-ізопропіл-2-(6-метилпіридин-3-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(ізохінолін-4-іл)-9H-пурин-6-іламіно)етил)фенол; 2-хлор4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 3-фтор-4-(2-(9-ізопропіл-2(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; N-(2-(5-хлор-1H-індол-3-іл)етил)-9-ізопропіл-2(піридин-3-іл)-9H-пурин-6-амін; N-(2-(5-фтор-1H-індол-3-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9Hпурин-6-амін; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)-2-метилфенол; 4-(2-(2(бензо[b]тіофен-3-іл)-9-(оксетан-3-іл)-9H-пурин-6-іламіно)етил)фенол; (S)-4-(2-(2(бензо[b]тіофен-3-іл)-9-(тетрагідрофуран-3-іл)-9H-пурин-6-іламіно)етил)фенол; (R)-4-(2-(2(бензо[b]тіофен-3-іл)-9-(тетрагідрофуран-3-іл)-9H-пурин-6-іламіно)етил)фенол; 2-(6-(2-(1Hіндол-3-іл)етиламіно)-2-(5-фторпіридин-3-іл)-9H-пурин-9-іл)пропан-1-ол; (R)-2-(6-(2-(1H-індол-3іл)етиламіно)-2-(5-фторпіридин-3-іл)-9H-пурин-9-іл)пропан-1-ол; (S)-2-(6-(2-(1H-індол-3іл)етиламіно)-2-(5-фторпіридин-3-іл)-9H-пурин-9-іл)пропан-1-ол; (R)-N-(2-(1H-індол-3-іл)етил)-2(5-фторпіридин-3-іл)-9-(тетрагідрофуран-3-іл)-9H-пурин-6-амін; 4-(2-(2-(3H-імідазо[4,5-b]піридин3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(1H-імідазо[4,5-b]піридин-1-іл)-9ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(6-(5-фторпіридин-3-іл)-1-ізопропіл-1Hімідазо[4,5-c]піридин-4-іламіно)етил)фенол; 4-(2-(2-(4,5-диметил-1H-імідазол-1-іл)-9-ізопропіл9H-пурин-6-іламіно)етил)фенол; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(піридин-3-іл)етил)-9Hпурин-6-амін; 4-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)-1гідроксиетил)фенол; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(6-метокси-1H-індол-3-іл)етил)-9Hпурин-6-амін; N-(2-(1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-амін; 2-(5фторпіридин-3-іл)-9-ізопропіл-N-(2-(5-метокси-1H-індол-3-іл)етил)-9H-пурин-6-амін; N-(2-(1Hіндол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-(проп-1-ен-2-іл)-9H-пурин-6-амін; 5-(2-(2-(5фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)піридин-2-ол; N-(2-(1H-піроло[2,3b]піридин-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-амін; N-(2-(6-(2(діетиламіно)етокси)-1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-амін; 4(2-(5-(5-фторпіридин-3-іл)-3-ізопропіл-3H-імідазо[4,5-b]піридин-7-іламіно)етил)фенол; N-(2-(1Hіндол-3-іл)етил)-9-втор-бутил-2-(2-метил-1H-імідазол-1-іл)-9H-пурин-6-амін; 4-(2-(2-(2-етил-1Hімідазол-1-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(2-пропіл-1Hімідазол-1-іл)-9H-пурин-6-іламіно)етил)фенол; 3-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9Hпурин-6-іламіно)етил)-1H-індол-6-ол; N-(2-(1H-індол-3-іл)етил)-9-ізопропіл-2-(5-метилпіридин-3іл)-9H-пурин-6-амін; N-(2-(1H-індол-3-іл)етил)-9-ізопропіл-2-(2-метил-1H-імідазол-1-іл)-9H-пурин6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(7-метил-1H-індол-3-іл)етил)-9H-пурин-6-амін; N(2-(1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-(оксетан-3-іл)-9H-пурин-6-амін; N-(2-(1H-індол-3іл)етил)-2-(5-метилпіридин-3-іл)-9-(оксетан-3-іл)-9H-пурин-6-амін; N-(2-(6-фтор-1H-індол-3іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропілN-(2-(6-метил-1H-індол-3-іл)етил)-9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(2метил-1H-індол-3-іл)етил)-9H-пурин-6-амін; N-(2-(4-фтор-1H-індол-3-іл)етил)-2-(5-фторпіридин3-іл)-9-ізопропіл-9H-пурин-6-амін; N-(2-(7-фтор-1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9ізопропіл-9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(4-метил-1H-індол-3-іл)етил)9H-пурин-6-амін; 4-(2-(2-(бензо[b]тіофен-3-іл)-7-ізопропіл-7H-піроло[2,3-d]піримідин-4іламіно)етил)фенол; 9-ізопропіл-2-(піридин-3-іл)-N-(2-(піридин-4-іл)етил)-9H-пурин-6-амін; N-(2(1H-піроло[2,3-b]піридин-5-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-амін; 4-(2-(2-(5фторпіридин-3-іл)-9-(1-гідроксипропан-2-іл)-9H-пурин-6-іламіно)етил)-2-метилфенол; 4-(2-(2(бензо[b]тіофен-3-іл)-9-циклогексил-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(тіофен3-іл)-9H-пурин-6-іламіно)етил)фенол; та 1-(2-(2-(бензо[b]тіофен-3-іл)-6-(4гідроксифенетиламіно)-9H-пурин-9-іл)етил)піролідин-2-он. Сполуки Формули I детально описані у Прикладах та Таблиці 1 нижче. У іншому варіанті втілення представлені сполуки Формули Ia: R2 L N N R1 R3 N N R4 у якій: L вибирають з таких як: –NR5a(CH2)0-3–, –NR5aCH(C(O)OCH3)CH2–, –NR5a(CH2)2NR5b–, –NR5a(CH2)2S–, –NR5aCH2CH(CH3)CH2–, –NR5aCH(CH3)CH2–, –(CH2)3–, –CH2OCH2–, 7 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 –CH2NR5aCH2–, –NR5aC(O)CH2– та –NR5aY–; де R5a та R5b незалежно вибирають з таких як: водень та C1-4алкіл; та Y являє собою 5-членне гетероарильне кільце, що містить до 3 гетероатомів, вибраних з O, N та S; R1 вибирають з таких як: водень, феніл, тіофен-2-іл, тіофен-3-іл, фуран-2-іл, фуран-3-іл, бензо[b]тіофен-2-іл, бензо[b]тіофен-3-іл, бензофуран-2-іл, бензофуран-3-іл, піримідин-4-іл, піримідин-5-іл, 1H-піразол-4-іл, 1H-піразол-3-іл, піридин-2-іл, піридазин-3-іл, піридин-4-іл, 1Hімідазол-1-іл, піролідин-1-іл, піразин-2-іл, піридин-3-іл, 1H-піразол-1-іл, піридазин-4-іл, 1H-індол2-іл, тіазол-4-іл, 1H-індол-3-іл, 1H-пірол-2-іл та тіазол-5-іл; де зазначений феніл, тіофен-2-іл, тіофен-3-іл, фуран-2-іл, фуран-3-іл, бензо[b]тіофен-2-іл, бензо[b]тіофен-3-іл, бензофуран-2-іл, бензофуран-3-іл, піримідин-4-іл, піримідин-5-іл, 1H-піразол-4-іл, 1H-піразол-3-іл, піридин-2-іл, піридазин-3-іл, піридин-4-іл, 1H-імідазол-1-іл, піролідин-1-іл, піразин-2-іл, піридин-3-іл, 1Hпіразол-1-іл, піридазин-4-іл, 1H-індол-2-іл, тіазол-4-іл, 1H-індол-3-іл, 1H-пірол-2-іл або тіазол-5іл радикалу R1 може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: ціано група, гідрокси група, C1-4алкіл, C1-4алкокси група, гало група, галозаміщений-C1-4алкіл, гало-заміщена-C1-4алкокси група, гідрокси група, аміно група, –C(O)R8a, –S(O)0-2R8a, –C(O)OR8a та –C(O)NR8aR8b; де R8a та R8b незалежно вибирають з таких як: водень та C1-4алкіл; за умови, що R1 та R3 обидва не являють собою водень; R2 вибирають з таких як: –S(O)2NR6aR6b, –NR9aC(O)R9b, –NR6aC(O)NR6bR6c, феніл, 1H-індол-2іл, 1H-індол-3-іл, бензо[b]тіофен-2-іл, бензо[b]тіофен-3-іл, бензофуран-2-іл, бензофуран-3-іл, тіофен-2-іл, тіофен-3-іл, фуран-2-іл, фуран-3-іл, піперидин-4-іл, піперидин-3-іл, піперидин-2-іл, піперидин-1-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H-1,2,4-триазол-3-іл, 1H-1,2,4-триазол5-іл, 2-оксоімідазолідин-1-іл, 1H-піразол-3-іл, 1H-піразол-4-іл, 3-оксопіперазин-1-іл, 2-оксо-2,3дигідро-1H-бензо[d]імідазол-5-іл, 1,2,3,4-тетрагідронафталін-2-іл, індолін-5-іл, 2-оксоіндолін-5-іл, 1H-бензо[d]імідазол-5-іл, 1H-індазол-5-іл та 1H-імідазол-4-іл; де R6a, R6b та R6c незалежно вибирають з таких як: водень та C1-4алкіл; де зазначений феніл, 1H-індол-2-іл, 1H-індол-3-іл, бензо[b]тіофен-2-іл, бензо[b]тіофен-3-іл, бензофуран-2-іл, бензофуран-3-іл, тіофен-2-іл, тіофен3-іл або фуран-2-іл, фуран-3-іл, піперидин-4-іл, піперидин-3-іл, піперидин-2-іл, піперидин-1-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H-1,2,4-триазол-3-іл, 1H-1,2,4-триазол-5-іл, 2оксоімідазолідин-1-іл, 1H-піразол-3-іл, 3-оксопіперазин-1-іл, 2-оксо-2,3-дигідро-1Hбензо[d]імідазол-5-іл, 1,2,3,4-тетрагідронафталін-2-іл, індолін-5-іл, 2-оксоіндолін-5-іл, 1Hбензо[d]імідазол-5-іл, 1H-індазол-5-іл або 1H-імідазол-4-іл радикалу R2 необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: гідрокси група, гало група, метил, метокси група, аміно група, –S(O)2NR7aR7b, –OS(O)2NR7aR7b та –NR7aS(O)2R7b; де R7a та R7b незалежно вибирають з таких як: водень та C1-4алкіл; або один радикал, вибраний з таких як: 5-((3aS, 4S, 6aR)-2-оксогексагідро-1H-тієно[3,4-d]імідазол-4-іл)пентаноїлокси група, 2(2-(5-((3aS, 4S, 6aR)-2-оксогексагідро-1H-тієно[3,4-d]імідазол-4-іл)пентанамідо)етокси)етокси група та 2-(4-(4-гекс-5-инамідобензоїл)феніламіно)-2-оксоетокси група; R3 вибирають з таких як: водень, C1-4алкіл та біфеніл; та R4 вибирають з таких як: ізопропіл, ізобутил, втор-бутил, 1-гідроксипропан-2-іл, циклопропіл, оксетан-3-іл, оксетан-2-іл, бензгідрил, піперидин-4-іл, піперидин-3-іл, піперидин-2-іл, тетрагідро2H-піран-2-іл, тетрагідро-2H-піран-3-іл, тетрагідро-2H-піран-4-іл, феніл, тетрагідрофуран-3-іл, тетрагідрофуран-2-іл, бензил, (4-пентилфеніл)(феніл)метил та 1-(1-(2-оксо-6,9,12-триокса-3азатетрадекан-14-іл)-1H-1,2,3-триазол-4-іл)етил; де зазначений циклопропіл, оксетан-3-іл, оксетан-2-іл, бензгідрил, піперидин-4-іл, піперидин-3-іл, піперидин-2-іл, тетрагідро-2H-піран-2-іл, тетрагідро-2H-піран-3-іл, тетрагідро-2H-піран-4-іл, феніл, тетрагідрофуран-3-іл, тетрагідрофуран-2-іл, бензил, (4-пентилфеніл)(феніл)метил або 1-(1-(2-оксо-6,9,12-триокса-3азатетрадекан-14-іл)-1H-1,2,3-триазол-4-іл)етил може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: C 1-4алкіл та гало-заміщений-C1-4алкіл; або їх N-оксидні похідні, пролікарські похідні, захищені похідні, окремі ізомери та суміш ізомерів; або фармацевтично прийнятні солі та сольвати (наприклад, гідрати) таких сполук. У додатковому варіанті втілення, з посиланням на сполуки Формули Ia, L вибирають з таких як: –NR5a(CH2)0-3–, –NR5aCH(C(O)OCH3)CH2–, –NR5a(CH2)2NR5b–, –NR5a(CH2)2S–, –NR5aCH2CH(CH3)CH2–, –NR5aCH(CH3)CH2–, –(CH2)3–, –CH2OCH2–, –CH2NR5aCH2–, –NR5aC(O)CH2– та –NR5aY–; де R5a та R5b незалежно вибирають з таких як: водень та метил; Y вибирають з таких як: ізоксазол та 1,3,4-оксадіазол. У іншому варіанті втілення, коли L являє собою –NR5a(CH2)0-3, кращим є –NR5a(CH2)1-3 (де 1-3 у цьому описі позначає 1, 2 або 3). У іншому варіанті втілення, R1 вибирають з таких як: водень, феніл, тіофен-3-іл, тіофен-2-іл, фуран-3-іл, фуран-2-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, піридин-4-іл, піридин-2-іл, піролідин 8 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 1-іл, 1H-піразол-4-іл, піразин-2-іл, піридазин-3-іл, піридазин-4-іл, 1H-піразол-1-іл, 1H-піразол-3іл, 1H-імідазол-1-іл, тіазол-4-іл, 1H-пірол-2-іл, тіазол-5-іл, та піридин-3-іл; де зазначений феніл, тіофен-3-іл, тіофен-2-іл, фуран-3-іл, фуран-2-іл, бензо[b]тіофен-3-іл, піримідин-5-іл, піридин-4-іл, піридин-2-іл, піролідин-1-іл, 1H-піразол-4-іл, піразин-2-іл, піридазин-3-іл, піридазин-4-іл, 1Hпіразол-1-іл, 1H-піразол-3-іл, 1H-імідазол-1-іл, тіазол-4-іл, 1H-пірол-2-іл, тіазол-5-іл або піридин3-іл радикалу R1 необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: ціано група, метил, метил-сульфоніл, метокси група, гало група, гідрокси група, карбоксил, етокси-карбоніл, метил-аміно-карбоніл та аміно група; за умови, що R1 та R3 обидва не являють собою водень. У іншому варіанті втілення, R2 вибирають з таких як: аміно-сульфоніл, метил-карбоніл-аміно група, метил-сульфоніл-аміно група, аміно-сульфоніл-окси група, сечовина, феніл, 1H-індол-2іл, 1H-індол-3-іл, бензо[b]тіофен-2-іл, бензо[b]тіофен-3-іл, бензофуран-2-іл, бензофуран-3-іл, тіофен-2-іл, тіофен-3-іл, фуран-2-іл, фуран-3-іл, піперидин-4-іл, піперидин-3-іл, піперидин-2-іл, піперидин-1-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H-1,2,4-триазол-3-іл, 1H-1,2,4-триазол5-іл, 2-оксоімідазолідин-1-іл, 1H-піразол-3-іл, 1H-піразол-4-іл, 3-оксопіперазин-1-іл, 2-оксо-2,3дигідро-1H-бензо[d]імідазол-5-іл, 1,2,3,4-тетрагідронафталін-2-іл, індолін-5-іл, 2-оксоіндолін-5-іл, 1H-бензо[d]імідазол-5-іл, 1H-індазол-5-іл та 1H-імідазол-4-іл; де зазначений феніл, 1H-індол-2іл, 1H-індол-3-іл, бензо[b]тіофен-2-іл, бензо[b]тіофен-3-іл, бензофуран-2-іл, бензофуран-3-іл, тіофен-2-іл, тіофен-3-іл, фуран-2-іл, фуран-3-іл, піперидин-4-іл, піперидин-3-іл, піперидин-2-іл, піперидин-1-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл, 1H-1,2,4-триазол-3-іл, 1H-1,2,4-триазол5-іл, 2-оксоімідазолідин-1-іл, 1H-піразол-3-іл, 1H-піразол-4-іл, 3-оксопіперазин-1-іл, 2-оксо-2,3дигідро-1H-бензо[d]імідазол-5-іл, 1,2,3,4-тетрагідронафталін-2-іл, індолін-5-іл, 2-оксоіндолін-5-іл, 1H-бензо[d]імідазол-5-іл, 1H-індазол-5-іл та 1H-імідазол-4-іл радикалу R2 необов'язково заміщений за допомогою таких як: гідрокси група, метокси група, метил, гало група, аміно група, аміно-сульфоніл, 5-((3aS, 4S, 6aR)-2-оксогексагідро-1H-тієно[3,4-d]імідазол-4-іл)пентаноїлокси група, 2-(2-(5-((3aS, 4S, 6aR)-2-оксогексагідро-1H-тієно[3,4-d]імідазол-4іл)пентанамідо)етокси)етокси група та 2-(4-(4-гекс-5-инамідобензоїл)феніламіно)-2-оксоетокси група. У іншому варіанті втілення, R3 вибирають з таких як: водень, метил, та біфеніл; та R4 вибирають з таких як: ізопропіл, ізобутил, втор-бутил, 1-гідроксипропан-2-іл, циклопропіл, оксетан-3-іл, оксетан-2-іл, бензгідрил, піперидин-4-іл, піперидин-3-іл, піперидин-2-іл, тетрагідро2H-піран-2-іл, тетрагідро-2H-піран-3-іл, тетрагідро-2H-піран-4-іл, феніл, тетрагідрофуран-3-іл, тетрагідрофуран-2-іл, бензил, (4-пентилфеніл)(феніл)метил та 1-(1-(2-оксо-6,9,12-триокса-3азатетрадекан-14-іл)-1H-1,2,3-триазол-4-іл)етил; де зазначений циклопропіл, оксетан-3-іл, оксетан-2-іл, бензгідрил, піперидин-4-іл, піперидин-3-іл, піперидин-2-іл, тетрагідро-2H-піран-2-іл, тетрагідро-2H-піран-3-іл, тетрагідро-2H-піран-4-іл, феніл, тетрагідрофуран-3-іл, тетрагідрофуран-2-іл, бензил, (4-пентилфеніл)(феніл)метил або 1-(1-(2-оксо-6,9,12-триокса-3азатетрадекан-14-іл)-1H-1,2,3-триазол-4-іл)етил може бути необов'язково заміщений за допомогою 1-3 радикалів, що незалежно вибирають з таких як: метил та трифторметил. У іншому варіанті втілення сполуки вибирають з таких як: 4-(2-(2-(бензо[b]тіофен-3-іл)-9ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-втор-бутил-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-бензгідрил-2-(бензо[b]тіофен-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-(тетрагідро-2H-піран-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2(бензо[b]тіофен-3-іл)-9-(4-(трифторметил)-бензил)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2(бензо[b]тіофен-3-іл)-9-ізобутил-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9метил-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-(4-метилбензил)-9Hпурин-6-іламіно)етил)фенол; N-(2-(1H-індол-3-іл)етил)-2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9Hпурин-6-амін; 2-(бензо[b]тіофен-3-іл)-9-ізопропіл-N-(2-(тіофен-3-іл)етил)-9H-пурин-6-амін; 3-(2(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 2-(бензо[b]тіофен-3-іл)-N(4-фторфенетил)-9-ізопропіл-9H-пурин-6-амін; N-(4-амінофенетил)-2-(бензо[b]тіофен-3-іл)-9ізопропіл-9H-пурин-6-амін; 4-(2-(9-ізопропіл-2-(піримідин-5-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-феніл-9Hпурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(тіофен-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4(2-(2-(фуран-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 2-(бензо[b]тіофен-3-іл)-N-(4фторфенетил)-9-феніл-9H-пурин-6-амін; N-бензил-8-(біфеніл-4-іл)-9-ізопропіл-9H-пурин-6-амін; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-(нонан-2-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2(бензо[b]тіофен-3-іл)-9-((4-пентилфеніл)(феніл)метил)-9H-пурин-6-іламіно)етил)фенол; N-(2(1H-індол-3-іл)етил)-2-(бензо[b]тіофен-3-іл)-9-втор-бутил-9H-пурин-6-амін; 4-(2-(2(бензо[b]тіофен-3-іл)-9-втор-бутил-9H-пурин-6-іламіно)етил)фенол; 3-(2-(2-(бензо[b]тіофен-3-іл)9-ізопропіл-9H-пурин-6-іламіно)етил)-1H-індол-5-ол; 3-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H 9 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 пурин-6-іламіно)етил)-1H-індол-5-іл 5-((3aS, 4S, 6aR)-2-оксогексагідро-1H-тієно[3,4-d]імідазол-4іл)пентаноат; N-(2-(2-(3-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)-1Hіндол-5-ілокси)етокси)етил)-5-((3aS, 4S, 6aR)-2-оксогексагідро-1H-тієно[3,4-d]імідазол-4іл)пентанамід; N-(4-(4-(2-(3-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)-1Hіндол-5-ілокси)ацетамідо)бензоїл)феніл)гекс-5-инамід; N-(2-(2-(2-(2-(4-(1-(2-(бензо[b]тіофен-3іл)-6-(4-гідроксифенетиламіно)-9H-пурин-9-іл)етил)-1H-1,2,3-триазол-1-іл)етокси)етокси)етокси)етил)ацетамід; 4-(2-(9-ізопропіл-2-(піридин-4-іл)-9H-пурин-6-іламіно)етил)фенол; етил 5(6-(4-гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)нікотинат; етил 5-(6-(4гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)нікотинат; 4-(2-(2-(6-фторпіридин-3-іл)-9ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(4-метилпіридин-3-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(2-метоксипіридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 5-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)нікотинонітрил; 4-(2-(9-ізопропіл-2(піролідин-1-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(1H-піразол-1-іл)-9H-пурин6-іламіно)етил)фенол; 4-(2-(2-(1H-імідазол-1-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4(2-(9-ізопропіл-2-(піридазин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридазин4-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піразин-2-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-2-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9ізопропіл-2-(5-(метилсульфоніл)піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл2-(5-метилпіридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(2-хлорпіридин-3-іл)-6-ізопропіл2,6-дигідроімідазо[4,5-c]піразол-3-іламіно)етил)фенол; 4-(2-(2-(4-хлорпіридин-3-іл)-9-ізопропіл9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(4-метоксипіридин-3-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4(2-(9-ізопропіл-2-(тіазол-4-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(1-метил-1Hпіразол-4-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(1H-піразол-3-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(1H-піразол-4-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2(9-ізопропіл-2-(тіофен-2-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(6-(4-гідроксифенетиламіно)-9ізопропіл-9H-пурин-2-іл)тіофен-2-карбонова кислота; 4-(2-(2-(фуран-2-іл)-9-ізопропіл-9H-пурин6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(4-метилтіофен-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)-2-метоксифенол; 4-(2-(9-ізопропіл-2(піридин-3-іл)-9H-пурин-6-іламіно)етил)-2-метоксифенол; N-[2-(6-метокси-1H-індол-3-іл)етил]-9(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-амін; N-[2-(5-метил-1H-індол-3-іл)етил]-9-(пропан-2-іл)2-(піридин-3-іл)-9H-пурин-6-амін; N-[2-(піперидин-4-іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)-9Hпурин-6-амін; 1-(2-{[9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-іл]аміно}етил)піперидин-4-ол; метил (2S)-3-(4-гідроксифеніл)-2-{[9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6іл]аміно}пропаноат; 4-(2-{[9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-іл]аміно}етил)бензол-1сульфонамід; 2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6-іл]аміно}етан-1сульфонамід; 4-(2-{[9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-іл]аміно}етил)бензол-1,2-діол; N[2-(1H-імідазол-4-іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-амін; 1-(2-{[9-(пропан-2-іл)2-(піридин-3-іл)-9H-пурин-6-іл]аміно}етил)імідазолідин-2-он; N-[2-(5-аміно-1H-1,2,4-триазол-3іл)етил]-9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-амін; N-(2-{[9-(пропан-2-іл)-2-(піридин-3-іл)9H-пурин-6-іл]аміно}етил)піридин-2-амін; 9-(пропан-2-іл)-N-[3-(1H-піразол-4-іл)пропіл]-2(піридин-3-іл)-9H-пурин-6-амін; N-[2-({[9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6іл]аміно}метил)пропіл]ацетамід; 4-(2-{[9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6іл]аміно}етил)піперазин-2-он; N-{2-[(3-метил-1H-1,2,4-триазол-5-іл)сульфаніл]етил}-9-(пропан-2іл)-2-(піридин-3-іл)-9H-пурин-6-амін; N-[3-(3,5-диметил-1H-піразол-4-іл)пропіл]-9-(пропан-2-іл)-2(піридин-3-іл)-9H-пурин-6-амін; (2-{[9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6іл]аміно}етил)сечовина; 5-({[9-(пропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-іл]аміно}метил)-2,3дигідро-1H-1,3-бензодіазол-2-он; 2-(1-бензотіофен-3-іл)-N-[2-(1H-імідазол-4-іл)етил]-9-(пропан-2іл)-9H-пурин-6-амін; 1-(2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6іл]аміно}етил)імідазолідин-2-он; N-[2-(5-аміно-1H-1,2,4-триазол-3-іл)етил]-2-(1-бензотіофен-3-іл)9-(пропан-2-іл)-9H-пурин-6-амін; N-(2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6іл]аміно}етил)піридин-2-амін; 2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-N-[3-(1H-піразол-4іл)пропіл]-9H-пурин-6-амін; N-[2-({[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6іл]аміно}метил)-пропіл]ацетамід; 4-(2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6іл]аміно}етил)піперазин-2-он; 2-(1-бензотіофен-3-іл)-N-{2-[(3-метил-1H-1,2,4-триазол-5іл)сульфаніл]етил}-9-(пропан-2-іл)-9H-пурин-6-амін; 2-(1-бензотіофен-3-іл)-N-[3-(3,5-диметил1H-піразол-4-іл)пропіл]-9-(пропан-2-іл)-9H-пурин-6-амін; (2-{[2-(1-бензотіофен-3-іл)-9-(пропан-2іл)-9H-пурин-6-іл]аміно}етил)сечовина; 5-({[2-(1-бензотіофен-3-іл)-9-(пропан-2-іл)-9H-пурин-6іл]аміно}метил)-2,3-дигідро-1H-1,3-бензодіазол-2-он; N-[2-(1H-індол-3-іл)етил]-9-(пропан-2-іл)-2(піридин-3-іл)-9H-пурин-6-амін; N-(4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6 10 UA 103206 C2 5 10 15 20 25 іламіно)етил)феніл)-метансульфонамід; 4-(2-(2-(піридин-3-іл)-9-(тетрагідрофуран-3-іл)-9Hпурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)пропіл)фенол; 4-(2-(9-(оксетан-3-іл)-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 5-(6-(4гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)-N-метилнікотинамід; 6-(9-ізопропіл-2(піридин-3-іл)-9H-пурин-6-іламіно)-5,6,7,8-тетрагідронафталін-2-ол; N-(2-(1H-індазол-3-іл)етил)9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-амін; 4-(2-((9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6іл)(метил)аміно)-етил)фенол; 4-(2-(9-ізопропіл-8-метил-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 1-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)-1H-бензо[d]імідазол2(3H)-он; 4-(3-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іл)пропіл)фенол; 4-((((9-ізопропіл-2(піридин-3-іл)-9H-пурин-6-іл)метил)(метил)аміно)метил)фенол; 4-(((9-ізопропіл-2-(піридин-3-іл)9H-пурин-6-іл)метиламіно)метил)фенол; 4-(((9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6іл)метокси)метил)фенол; N-(2-(індолін-5-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-амін; 4(2-(9-(1-метилпіперидин-4-іл)-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9(піперидин-4-іл)-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; N-(2-(1H-індазол-5-іл)етил)-9ізопропіл-2-(піридин-3-іл)-9H-пурин-6-амін; N-(2-(1H-бензо[d]імідазол-5-іл)етил)-9-ізопропіл-2(піридин-3-іл)-9H-пурин-6-амін; 5-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6іламіно)етил)індолін-2-он; 4-(2-(9-циклопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-(1-гідроксипропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)феніл сульфамат; 2-(4-гідроксифеніл)-N-(9-ізопропіл-2(піридин-3-іл)-9H-пурин-6-іл)ацетамід; 4-(5-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6іламіно)ізоксазол-3-іл)фенол; 4-(5-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)-1,3,4оксадіазол-2-іл)фенол; 4-(2-(2-(2-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(1-метил-1H-пірол-2-іл)-9H-пурин-6-іламіно)етил)фенол; та 4-(2-(9-ізопропіл2-(тіазол-5-іл)-9H-пурин-6-іламіно)етил)фенол. У іншому варіанті втілення представлена сполука Формули 1f: R2 HN N N S N N R4 If 30 35 у якій: R2 вибирають з таких як: 1H-індол-3-іл та феніл необов'язково заміщений за допомогою гідрокси групи; та R4 вибирають з таких як: ізопропіл, втор-бутил, бензгідрил, нонан2-іл, оксетан-3-іл та тетрагідрофуран-3-іл. У додатковому варіанті втілення сполуки вибирають з таких як: 4-(2-(2-(бензо[b]тіофен-3-іл)9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-втор-бутил-9H-пурин6-іламіно)етил)фенол; 4-(2-(9-бензгідрил-2-(бензо[b]тіофен-3-іл)-9H-пурин-6іламіно)етил)фенол; N-(2-(1H-індол-3-іл)етил)-2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6амін; 4-(2-(2-(бензо[b]тіофен-3-іл)-9-(нонан-2-іл)-9H-пурин-6-іламіно)етил)фенол; N-(2-(1H-індол3-іл)етил)-2-(бензо[b]тіофен-3-іл)-9-втор-бутил-9H-пурин-6-амін; 4-(2-(2-(бензо[b]тіофен-3-іл)-9(оксетан-3-іл)-9H-пурин-6-іламіно)етил)фенол; (S)-4-(2-(2-(бензо[b]тіофен-3-іл)-9(тетрагідрофуран-3-іл)-9H-пурин-6-іламіно)етил)фенол; та (R)-4-(2-(2-(бензо[b]тіофен-3-іл)-9(тетрагідрофуран-3-іл)-9H-пурин-6-іламіно)етил)фенол. У іншому варіанті втілення представлена сполука Формули 1g: 11 UA 103206 C2 R2 HN N N Rc N N R4 Rb N Ra Ig 5 10 15 20 25 30 35 40 45 у якій: R2 вибирають з таких як: 1H-піроло[2,3-b]піридин-3-іл; 1H-індол-3-іл, необов'язково заміщений за допомогою 1-2 радикалів, що незалежно вибирають з таких як: гало група, метил та метокси група; та феніл, необов'язково заміщений за допомогою 1-2 радикалів, що незалежно вибирають з таких як: метил, гало група та гідрокси група; R4 вибирають з таких як: ізопропіл, втор-бутил, 1-гідроксипропан-2-іл, проп-1-ен-2-іл, бензгідрил, нонан-2-іл, оксетан-3-іл та тетрагідрофуран-3-іл; та Ra, Rb та Rc незалежно вибирають з таких як: водень, ціано група, метил, гало група, -SO2CH3 та трифторметил. У додатковому варіанті втілення сполуки вибирають з таких як: 4-(2-(9-ізопропіл-2-(піридин3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(6-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(4-метилпіридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 5(6-(4-гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2-іл)нікотинонітрил; 4-(2-(9-ізопропіл-2-(5метилпіридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(5(метилсульфоніл)піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(4-хлорпіридин-3-іл)-9ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6іламіно)етил)фенол; 9-ізопропіл-N-(2-(6-метокси-1H-індол-3-іл)етил)-2-(піридин-3-іл)-9H-пурин-6амін; 9-ізопропіл-N-(2-(5-метил-1H-індол-3-іл)етил)-2-(піридин-3-іл)-9H-пурин-6-амін; N-(2-(1Hіндол-3-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-амін; 4-(2-(9-(оксетан-3-іл)-2-(піридин-3іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-(1-гідроксипропан-2-іл)-2-(піридин-3-іл)-9H-пурин-6іламіно)етил)фенол; 4-(2-(2-(2-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 5(9-втор-бутил-6-(4-гідрокси-3-метилфенетиламіно)-9H-пурин-2-іл)нікотинонітрил; 4-(2-(2-(5фторпіридин-3-іл)-9-(оксетан-3-іл)-9H-пурин-6-іламіно)етил)фенол; 4-(2-(2-(5-хлорпіридин-3-іл)9-ізопропіл-9H-пурин-6-іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(5-(трифторметил)піридин-3-іл)9H-пурин-6-іламіно)етил)фенол; 5-(6-(2-(1H-індол-3-іл)етиламіно)-9-втор-бутил-9H-пурин-2іл)нікотинонітрил; N-(2-(1H-індол-3-іл)етил)-9-втор-бутил-2-(5-метилпіридин-3-іл)-9H-пурин-6амін; (R)-N-(2-(1H-індол-3-іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9H-пурин-6-амін; (S)-N(2-(1H-індол-3-іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9H-пурин-6-амін; N-(2-(1H-індол-3іл)етил)-9-втор-бутил-2-(5-фторпіридин-3-іл)-9H-пурин-6-амін; (R)-N-(2-(1H-індол-3-іл)етил)-9втор-бутил-2-(5-метилпіридин-3-іл)-9H-пурин-6-амін; (S)-N-(2-(1H-індол-3-іл)етил)-9-втор-бутил2-(5-метилпіридин-3-іл)-9H-пурин-6-амін; 5-(6-(4-гідроксифенетиламіно)-9-(оксетан-3-іл)-9Hпурин-2-іл)нікотинонітрил; 4-(2-(6-(5-фторпіридин-3-іл)-1-ізопропіл-1H-піразоло[3,4-d]піримідин4-іламіно)етил)фенол; 3-(6-(4-гідроксифенетиламіно)-9-ізопропіл-9H-пурин-2іл)ізонікотинонітрил; 4-(2-(2-(5-фторпіридин-3-іл)-7-ізопропіл-7H-піроло[2,3-d]піримідин-4іламіно)етил)фенол; 4-(2-(9-ізопропіл-2-(6-метилпіридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 2хлор-4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; 3-фтор-4-(2-(9-ізопропіл2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)фенол; N-(2-(5-фтор-1H-індол-3-іл)етил)-9-ізопропіл-2(піридин-3-іл)-9H-пурин-6-амін; N-(2-(5-хлор-1H-індол-3-іл)етил)-9-ізопропіл-2-(піридин-3-іл)-9Hпурин-6-амін; 4-(2-(9-ізопропіл-2-(піридин-3-іл)-9H-пурин-6-іламіно)етил)-2-метилфенол; 2-(6-(2(1H-індол-3-іл)етиламіно)-2-(5-фторпіридин-3-іл)-9H-пурин-9-іл)пропан-1-ол; (R)-2-(6-(2-(1Hіндол-3-іл)етиламіно)-2-(5-фторпіридин-3-іл)-9H-пурин-9-іл)пропан-1-ол; (S)-2-(6-(2-(1H-індол-3іл)етиламіно)-2-(5-фторпіридин-3-іл)-9H-пурин-9-іл)пропан-1-ол; (R)-N-(2-(1H-індол-3-іл)етил)-2(5-фторпіридин-3-іл)-9-(тетрагідрофуран-3-іл)-9H-пурин-6-амін; 4-(2-(6-(5-фторпіридин-3-іл)-1ізопропіл-1H-імідазо[4,5-c]піридин-4-іламіно)етил)фенол; N-(2-(1H-індол-3-іл)етил)-2-(5фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(6метокси-1H-індол-3-іл)етил)-9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(5метокси-1H-індол-3-іл)етил)-9H-пурин-6-амін; N-(2-(1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9(проп-1-ен-2-іл)-9H-пурин-6-амін; N-(2-(1H-піроло[2,3-b]піридин-3-іл)етил)-2-(5-фторпіридин-3іл)-9-ізопропіл-9H-пурин-6-амін; 4-(2-(5-(5-фторпіридин-3-іл)-3-ізопропіл-3H-імідазо[4,5 12 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 b]піридин-7-іламіно)етил)фенол; N-(2-(1H-індол-3-іл)етил)-9-ізопропіл-2-(5-метилпіридин-3-іл)9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(7-метил-1H-індол-3-іл)етил)-9H-пурин6-амін; N-(2-(1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-(оксетан-3-іл)-9H-пурин-6-амін; N-(2(1H-індол-3-іл)етил)-2-(5-метилпіридин-3-іл)-9-(оксетан-3-іл)-9H-пурин-6-амін; N-(2-(6-фтор-1Hіндол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9ізопропіл-N-(2-(2-метил-1H-індол-3-іл)етил)-9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропілN-(2-(6-метил-1H-індол-3-іл)етил)-9H-пурин-6-амін; N-(2-(4-фтор-1H-індол-3-іл)етил)-2-(5фторпіридин-3-іл)-9-ізопропіл-9H-пурин-6-амін; 2-(5-фторпіридин-3-іл)-9-ізопропіл-N-(2-(4-метил1H-індол-3-іл)етил)-9H-пурин-6-амін; N-(2-(7-фтор-1H-індол-3-іл)етил)-2-(5-фторпіридин-3-іл)-9ізопропіл-9H-пурин-6-амін; та 4-(2-(2-(5-фторпіридин-3-іл)-9-(1-гідроксипропан-2-іл)-9H-пурин-6іламіно)етил)-2-метилфенол. У іншому варіанті втілення представлений спосіб застосування сполуки Формули I для стимулювання розмноження стовбурових клітин шляхом збільшення кількості ділень; зазначений спосіб включає контактування стовбурових клітин зі сполукою Формули I. У іншому варіанті втілення представлений спосіб, у якому розмноження стовбурових клітин відбувається in vivo, in vitro, або ex vivo. У іншому варіанті втілення представлений спосіб, у якому стовбурові клітини являють собою гематопоетичні стовбурові клітини людини. У іншому варіанті втілення представлена клітинна популяція із розмноженими гематопоетичними стовбуровими клітинами, як одержують або може бути одержано за способом даного винаходу. У додатковому варіанті втілення представлена композиція, що включає клітинну популяцію із розмноженими клітинами HSC, отриманими з однієї або двох одиниць пуповинної крові, переважно однієї одиниці пуповинної крові, де зазначена композиція містить загальну кількість 5 7 8 9 клітин щонайменше 10 клітин, 10 клітин, 10 клітин або 10 клітин, та де у межах 20-100 % загальної кількості клітин становлять CD34+ клітини, наприклад, у межах 40-80 % загальної кількості клітин становлять CD34+. У іншому варіанті втілення представлений спосіб лікування хвороби або розладу, для якого терапія стовбуровими клітинами буде приводити до попередження, лікування або усунення зазначеного розладу. Передбачається, що так як застосування стовбурових клітин має успіх, перелік хвороб, які можуть лікуватися трансплантацією стовбурових клітин, буде розширюватися. Необмежуючий перелік прикладів представлений нижче. У іншому варіанті втілення представлене застосування сполуки Формули I, як визначено у Короткому описі даного винаходу, або її солі, у одержанні композиції для лікування вродженої імунодефіцитної хвороби, аутоімунної хвороби та/або гематопоетичного розладу. У додатковому варіанті втілення, введення являє собою аутологічну трансплантацію та гематопоетичний розлад вибирають з таких як: мієломна хвороба, неходжкінівська лімфома, ходжкінівська хвороба, гострий мієлолейкоз, нейробластома, герміногенні пухлини, аутоімунні розлади та амілоїдоз. У додатковому варіанті втілення, аутоімунні розлади вибирають з системного червоного вовчаку (SLE) та системного склерозу. У додатковому варіанті втілення, введення являє собою алогенну трансплантацію та гематопоетичний розлад вибирають з таких як: гострий мієлолейкоз, гострий лімфобластний лейкоз, хронічна мієлоїдна лейкемія, хронічна лімфоцитарна лейкемія, мієлопроліферативні розлади, мієлодиспластичні синдроми, мієломна хвороба, неходжкінівська лімфома, ходжкінівська хвороба, апластична анемія, справжня еритроцитарна аплазія, нічна пароксизмальна гемоглобінурія, анемія Фанконі, велика талассемія, серповидно-клітинна анемія, важкий комбінований імунодефіцит (SCID), синдром Віскота-Олдрича, гемофагоцитарний лімфогістіоцитоз (HLH) та вроджені пороки метаболізму. У додатковому варіанті втілення, вроджені пороки метаболізму вибирають з мукополісахаридозу, хвороби Гоше, метахроматичних лейкодистрофій та адренолейкодистрофій. У іншому варіанті втілення представлений спосіб лікування вродженої імунодефіцитної хвороби, аутоімунної хвороби та/або гематопоетичного розладу, що включає введення пацієнту, якому необхідне таке лікування, гематопоетичних стовбурових клітин, кількість яких була збільшена за допомогою сполуки, як описано у Короткому описі даного винаходу. У додатковому варіанті втілення, введення являє собою аутологічну трансплантацію та гематопоетичний розлад, що вибирають з таких як: мієломна хвороба, неходжкінівська 13 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 лімфома, ходжкінівська хвороба, гострий мієлолейкоз, нейробластома, герміногенні пухлини, аутоімунні розлади та амілоїдоз. У додатковому варіанті втілення, аутоімунні розлади вибирають з системного червоного вовчаку (SLE) та системного склерозу. У додатковому варіанті втілення, введення являє собою алогенну трансплантацію та гематопоетичний розлад вибирають з таких як: гострий мієлолейкоз, гострий лімфобластний лейкоз, хронічна мієлоїдна лейкемія, хронічна лімфоцитарна лейкемія, мієлопроліферативні розлади, мієлодиспластичні синдроми, мієломна хвороба, неходжкінівська лімфома, ходжкінівська хвороба, апластична анемія, справжня еритроцитарна аплазія, нічна пароксизмальна гемоглобінурія, анемія Фанконі, велика талассемія, серповидно-клітинна анемія, важкий комбінований імунодефіцит (SCID), синдром Віскота-Олдрича, гемофагоцитарний лімфогістіоцитоз (HLH) та вроджені пороки метаболізму. У додатковому варіанті втілення, вроджені пороки метаболізму вибирають з мукополісахаридозу, хвороби Гоше, метахроматичних лейкодистрофій та адренолейкодистрофій. Застосування HSC клітини являють собою ембріональні клітини, здатні регенерувати всі кров'яні клітини. У процесі розвитку, кровотворення переходить від ембріональної печінки до кісткового мозку, який далі залишається місцем кровотворення впродовж дорослого життя. Коли кровотворення встановлюється у кістковому мозку, HSC клітини не розповсюджуються довільно по кістковій порожнині. Замість цього, вони знайдені у тісній близькості до ендостальних поверхонь. Більш зрілі стовбурові клітини збільшуються у кількості при збільшенні відстані від поверхні кістки. Нарешті, коли наближаються до центральної подовжньої вісі кістки, відбувається кінцева диференціація зрілих клітин. Розмноження кількості стовбурових клітин, чи з дорослого, пуповинної крові, фетального чи з ембріонального джерел, буде мати великий вплив на трансплантацію та інші терапії для гематологічних та онкологічних хвороб та розладів, найменшим з яких буде збільшена безпека та знижена ціна. Як описано у способах у цьому описі, кількості HSC збільшують ex vivo. Спосіб збільшення кількостей стовбурових клітин є важливим, так як у даний час приблизно 25 % аутологічних донорних трансплантатів заборонені через відсутність достатньої кількості стовбурових клітин. Крім того, менше, ніж 25 % пацієнтів, яким необхідна алогенна трансплантація, можуть знайти гістосумісного донора. Наразі існують банки пуповинної крові та вони покривають широкий расовий склад загального населення, але ці банки зараз заборонені для застосування у дітей через невідповідні кількості стовбурових клітин у зразках для дорослих реципієнтів. Спосіб для збільшення кількостей стовбурових клітин дозволяє зробити пуповину корисною для дорослих пацієнтів, таким чином, розширюючи застосування алогенної трансплантації. Сполуки даного винаходу також можуть бути використані для збільшення кількостей клітин-попередників, які є клінічно корисними, наприклад, прискорити приживлення трансплантату та зменшити тривалість нейтропенії. Відповідно, забезпечується спосіб підвищення кількості клітин HSC. Як використано у цьому описі, збільшення у HSC клітинах означає, що суб'єкт має щонайменше на одну більше HSC, 10 % збільшення, 20 % збільшення, 30 % збільшення або більше. HSC клітини можуть складатися з підгрупи CD34+ клітин, збільшення HSC клітин може бути визначене непрямо шляхом обрахування кількості CD34+ клітин у клітинній популяції та, необов'язково, шляхом оцінювання диференціаційних властивостей CD34+ клітин шляхом аналізування колонієутворюючих одиниць (CFU) як описано у експериментальній частині нижче: збільшення кількості CD34+ клітинної культури щонайменше на 10 %, переважно 20 % збільшення або 30 % збільшення або більше у порівнянні з контролем без розмноження є показником розмноження HSC клітин. Розмножену популяцію HSC клітин збирають, наприклад, із зразку кісткового мозку суб'єкта або з культури. Збір HSC клітин проводять як вилучення або відділення клітин. Це здійснюють, використовуючи декілька способів, таких як ферментативний, неферментативний, центрифужний, електричний способи або спосіб, оснований на різниці розмірів, або переважно, шляхом змивання клітин, використовуючи культуральне середовище (наприклад, середовище, у якому інкубують клітини) або забуферений розчин. Ці клітини необов'язково збирають, розділяють та додатково розмножують, створюючи навіть більші популяції HSC клітин та потомство диференційованих клітин. Спосіб одержання розмноженої популяції HSC клітин включає контактування агенту, знатного регулювати у бік зменшення активність та/або експресію AHR та/або нижчележачого ефектору AHR, наприклад, сполуки даного винаходу, з вихідною клітинною популяцією (тобто не розмноженою популяцією клітин), що включає суміш HSC клітин та необов'язково HSC 14 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 підтримуючих клітин. Стадія введення відбувається ex vivo, in vivo та/або in vitro. Як розкрито у цьому описі, розмножену популяцію HSC клітин необов'язково вводять суб'єкту. Для ex vivo розмноження, такий агент для HSC розмноження, наприклад сполука даного винаходу, може бути сформульований у ДМСО або деякому іншому підходящому носії, "відмитий" від клітин та клітин можуть бути перенесені, наприклад, у інфузійний буфер. ДМСО композиція, наприклад, може містити 0,3 мг/мл сполуки даного винаходу у розчині 60 % ДМСО/40 % води. Таким чином, пропонуються способи забезпечення розмноженої популяції HSC клітин суб'єкту, що включають введення суб'єкту розмноженої популяції HSC клітин, розкритої у цьому описі, або отриманої за способами, розкритими у цьому описі. Розмножену популяцію HSC клітин необов'язково використовують для одержання клітин крові. Клітини крові необов'язково вводять суб'єкту, якому це необхідно. Необов'язково, суб'єкт являє собою того самого суб'єкта, від якого отримано нерозмножену популяцію HSC клітин або суміш HSC клітин та HSC підтримуючих клітин. Як використано у цьому описі, термін HSC підтримуюча клітина відноситься до клітин, що природно знайдені поблизу однієї або більше HSC клітин, таким чином, що фактори, вивільнені HSC підтримуючими клітинами, досягають HSC клітини, наприклад, шляхом дифузії. HSC підтримуючі клітини включають, не обмежуючись наведеними, лімфоретикулярні стромальні клітини. Лімфоретикулярні стромальні клітини, як використано у цьому описі, включають, не обмежуючись наведеними, всі типи клітин, присутні у лімфоїдній тканині, які не являють собою лімфоцити або прекурсори або попередники лімфоцитів. Таким чином, лімфоретикулярні стромальні клітини включають остеобласти, епітеліальні клітини, ендотеліальні клітини, мезотеліальні клітини, дендритні клітини, спленоцити та макрофаги. Лімфоретикулярні стромальні клітини також включають клітини, які не будуть звичайно функціонувати як лімфоретикулярні стромальні клітини, такі як фібробласти, які були генетично змінені для секретування або експресії на їх клітинній поверхні факторів, необхідних для підтримання, росту або диференціації HSC клітин, включаючи їх потомство. Лімфоретикулярні стромальні клітини необов'язково отримують з дезагрегації частини лімфоїдної тканини. Такі клітини здатні підтримувати in vitro або in vivo збереження, ріст або диференціацію HSC клітин, включаючи їх потомство. Під лімфоїдною тканиною розуміють кістковий мозок, периферичну кров (включаючи мобілізовану периферичну кров), пуповинну кров, плацентарну кров, плідну печінку, ембріональні клітини (включаючи ембріональні стовбурові клітини), клітини, отримані з аортально-гонадно-мезонефросу, та лімфоїдну м'яку тканину. Лімфоїдна м'яка тканина, як використано у цьому описі, включає, не обмежуючись наведеними, тканини, такі як тимус, селезінка, печінка, лімфовузли, шкіра, мигдалеподібна залоза, аденоїди та пейєрові бляшки, та їх комбінації. Лімфоретикулярні стромальні клітини забезпечують підтримку мікрооточення у інтактній лімфоїдній тканині для збереження, росту або диференціації HSC клітин, включаючи їх потомство. Мікрооточення включає розчинні та клітино-поверхневі фактори, що експресуються різними типами клітин, які включають лімфоретикулярну строму. В основному, підтримка, яку забезпечують лімфоретикулярні стромальні клітини, характеризується і як контакт-залежна, і як не-контакт-залежна. Лімфоретикулярні стромальні клітини, наприклад, є аутологічними (власними) або неаутологічними (не-власними, наприклад, гетерологічними, алогенними, сингенними або ксеногенними) по відношенню до HSC клітин. Аутологічні, як використано у цьому описі, відноситься до клітин з того самого суб'єкта. Алогенні, як використано у цьому описі, відноситься до клітин того самого виду, але які відрізняються генетично. Сингенні, як використано у цьому описі, відноситься до клітин іншого суб'єкта, які єгенетично ідентичними з порівнюваною клітиною. Ксеногенні, як використано у цьому описі, відноситься до клітин іншого виду. Лімфоретикулярні стромальні клітини отримують, наприклад, з лімфоїдної тканини людського або нелюдського суб'єкта у будь-який час після розвинення органу/тканини до стадії (тобто стадії розвитку), при якій вона може підтримувати збереження, ріст або диференціацію HSC клітин. Лімфоїдна тканина, з якої отримують лімфоретикулярні стромальні клітини, звичайно визначає комітування клітинної лінії, що беруть на себе HSC клітини, що приводить до одержання специфічності клітинної лінії диференційованого потомства. Спів-культивування HSC клітин (та їх потомства) з лімфоретикулярними стромальними клітинами, звичайно відбувається за умов, відомих у даній галузі техніки (наприклад, таких як температура, вміст CO2 та O2, поживне середовище, тривалість, тощо). Час, достатній для збільшення кількості клітин, являє собою час, який може бути легко визначений спеціалістом, кваліфікованим у даній галузі техніки, та змінюється в залежності від вихідної кількості посіяних клітин. Кількості HSC клітин та лімфоретикулярних стромальних клітин, що спочатку вводять (та 15 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 далі сіють), змінюються в залежності від потреб експерименту. Ідеальні кількості легко визначаються спеціалістом, кваліфікованим у даній галузі техніки, у відповідності з потребами. Як використано у цьому описі, під суб'єктом розуміють індивіда. Таким чином, суб'єкти включають, наприклад, домашніх тварин, таких як кішки та собаки, поголів'я худоби (наприклад, велика рогата худоба, коні, свині, вівці, та кози), лабораторних тварин (наприклад, миші, кролики, щури та морські свинки), ссавців, нелюдських ссавців, приматів, нелюдських приматів, гризунів, птахів, рептилій, амфібій, риб та будь-яких інших тварин. Суб'єкт необов'язково являє собою ссавця, такого як примат або людина. Способи розмноження гематопоетичних стовбурових клітин Отже, даний винахід відноситься до способу розмноження гематопоетичних стовбурових клітин, що включає (a) забезпечення вихідної клітинної популяції, що містить гематопоетичні стовбурові клітини, та (b) культивування зазначеної вихідної клітинної популяції ex vivo у присутності агенту, здатного регулювати у бік зменшення активність та/або експресію арилвуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору, за прийнятних умов для розмноження гематопоетичних стовбурових клітин. Арил-вуглеводневий (діоксин) рецептор (AHR) являє собою цитозольний ліганд-активований транскрипційний фактор, що, як відомо, опосередковує велику кількість токсичних та канцерогенних ефектів у тварин та можливо у людини (Safe S 2001 Toxicol Lett 120: 1-7). Як наслідок AHR активації його лігандами, багато генів детоксифікації є транскрипційно індукованими, включаючи ті, що кодують ксенобіотик-метаболізуючі ферменти фази I, такі як цитохроми P450 CYP1A1, CYP1A2, CYP1B1 та CYP2S1, та ферменти фази II, такі як UDPглюкуронозилтрансфеза UGT1A6, NAD(P)H-залежна хінон оксидоредуктаза-1 (NQO1), альдегід дегідрогеназа ALDH3A1, та декілька глутатіон-S-трансфез. У одному варіанті втілення, агент, здатний регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору та/або нижчележачого ефектору шляху арилвуглеводневого рецептору, вибирають з групи, що включає такі як: (i) органічна сполука; (ii) молекула короткої інтерферуючої РНК (кіРНК), здатна регулювати у бік зменшення експресію AHR; та (iii) антисмисловий олігонуклеотид, здатний регулювати у бік зменшення експресію AHR. У одному специфічному варіанті втілення, зазначений спосіб для розмноження гематопоетичних стовбурових клітин, включає (a) забезпечення вихідної клітинної популяції, що включає гематопоетичні стовбурові клітини, та (b) культивування зазначеної вихідної клітинної популяції ex vivo в присутності агенту, здатного регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору та/або нижчележачого ефектору шляху арилвуглеводневого рецептору, за прийнятних умов для розмноження гематопоетичних стовбурових клітин, де зазначений агент, здатний регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору, не являє собою альфа-нафтофлавон або 3'-метокси-4'-нітрофлавон. Органічна сполука, яка інгібує AHR активність (що також називають як AHR антагоніст), описана у даній галузі техніки, наприклад, така як: 2-метил-2H-піразол-3-карбонової кислоти (2метил-4-о-толілазофеніл)амід (CH223191), альфа-нафтофлавон, ресвератрол (Nutr. Metab. Cardiovasc. Dis., 2003 Apr; 13(2):104-13), 3’-метокси-4'-нітрофлавон (Biochem. Pharmacol., 2007 May 15; 73(10):1622-34, Epub 2007 Jan 30), та 6-метил-1,3,8-трихлордибензофуран (Cancer Res., 2004, Apr 15;64(8):2889-97). Інгібітор AHR активності відноситься до сполуки, яка знижує AHR активність до щонайменше 10 %, 20 %, 30 %, 50 %, 60 %, 70 %, 80 % або щонайменше 90 % транскрипційної активності AHR, що спостерігається за активованих умов. Дослідження для визначення AHR інгібуючої активності являє собою, наприклад, діоксин-викликане AHR залежне дослідження репортерного гену люциферази, як описано у Прикладах. У одному варіанті втілення, інгібітор AHR активності являє собою сполуку, яка має EC 50 менше, ніж 10 мкM, переважно менше, ніж 5 мкM, як виміряно у діоксин-викликаному AHR залежному дослідженні репортерного гену люциферази. AHR являє собою транскрипційний фактор, що регулює транскрипцію різних генів у людини. У одному варіанті втілення, нижчележачий ефектор AHR шляху являє собою ген, який безпосередньо регулюється на транскрипційному рівні за допомогою AHR. Приклади таких генів вибирають з Cyp1B1, Cyp1A1, та AHRR. AHR також функціонує у шляхах поза його добре охарактеризованої ролі у ксенобіотичній ферментативній індукції. Ксенобіотичні ліганди AHR, як показано, регулюють бета катенін, STAT5, STAT1, HES-1, c-Myc, C/EBP, PU.1, β-катенін, p21, P27, pRb, деоксинуклеотидил трансферазу, CXCR4, та її хемокіновий ліганд CXCL12 (SDF-1). 16 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 У одному специфічному варіанті втілення, агент, здатний регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору, являє собою сполуку, визначену у Короткому описі даного винаходу. У іншому варіанті втілення, агент, здатний регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору, являє собою антисмисловий олігонуклеотид або молекулу короткої інтерферуючої РНК (кіРНК), що здатні регулювати у бік зменшення AHR білкову експресію або білкову експресію одного або більшої кількості нижчележачих ефекторів AHR. На конструкцію антисмислових олігонуклеотидів, які можуть бути використані для ефективного інгібування AHR білкової експресії, мають впливати таким чином, щоб такі олігонуклеотиди специфічно зв'язували визначену мРНК у клітинах таким шляхом, що інгібує їх трансляцію. Послідовність, прийнятна для застосування у побудові та синтезі антисмислових олігонуклеотидів, які специфічно зв'язують AHR мРНК, геномна ДНК та/або її промотер або інші контрольні послідовності є доступними у опублікованій послідовності AHR, зокрема AHR людини. Крім того, також є доступними алгоритми для визначення послідовностей з найвищою передбачуваною зв'язуючою афінністю до їх цільової мРНК, що базуються на термодинамічному циклі, який вираховує енергетики структурних змін як у цільовій мРНК, так і у олігонуклеотидах. На синтез РНКі молекул, що підходять для застосування з даним винаходом, можна впливати наступним чином: Спочатку, AHR мРНК послідовність (або один або більшу кількість нижчележачих ефекторів) сканують нижче AUG вихідного кодону для AA-динуклеотидних послідовностей. Появу кожної AA та 19 3’-суміжної записують як потенційний кіРНК цільовий сайт. Потім, потенційні цільові сайти порівнюють до відповідної геномної бази даних (наприклад, людини, миші, щура, тощо), використовуючи будь-яке програмне забезпечення для вирівнювання послідовності. Припустимий цільовий сайт, який показує значну гомологію до інших кодуючих послідовностей, відкидають. Тоді кращі послідовності являють собою ті, що мають низький G/C вміст, зокрема послідовності з G/C вмістом, нижче ніж 55 %. Декілька цільових сайтів потім вибирають вздовж цільового гену. Способи або алгоритми для визначення припустимого цільового сайту кіРНК описані, наприклад, у (Tilesi, et al., Curr. Opin. Mol. Ther. 11:156, 2009). Приклади кіРНК молекул, які здатні регулювати у бік зменшення експресію AHR, включають такі як: AHR 111S, 5' GCG GCA TAG AGA CCG ACT TAA TTT CAA GAG AAT TAA GTC GGT CTC TAT GCC GCT TTT TTG G 3'; AHR 111AS, 5' CGC GCC AAA AAA GCG GCA TAG AGA CCG ACT TAA TTC TCT TGA AAT TAA GTC GGT CTC TAT GCC GC 3'; AHR 242S, 5' GGC TTC TTT GAT GTT GCA TTA ATT CAA GAG ATT AAT GCA ACA TCA AAG AAG CCT TTT TTG G 3'; AHR 242AS, 5' CGC GCC AAA AAA GGC TTC TTT GAT GTT GCA TTA ATC TCT TGA ATT AAT GCA ACA TCA AAG AAG CC 3'. Вихідна клітинна популяція, що включає гематопоетичні стовбурові клітини, буде вибрана спеціалістом, кваліфікованим у даній галузі техніки, в залежності від передбачуваного застосування. Різні джерела клітин, що включають гематопоетичні стовбурові клітини, були описані у даній галузі техніки, включаючи кістковий мозок, периферичну кров, неонатальну пуповинну кров, плаценту або інші джерела, такі як печінка, особливо плідна печінка. Клітинна популяція спочатку може бути піддана стадіям збагачення або очищення, включаючи негативний та/або позитивний відбір клітин на основі специфічних клітинних маркерів для того, щоб забезпечити вихідну клітинну популяцію. Способи виділення зазначеної вихідної клітинної популяції на основі специфічних клітинних маркерів можуть застосовувати технологію сортування флюоресцентно-активованих клітин (FACS), що також називають цитометрією у потоці, або твердий або нерозчинний субстрат, до якого прикріплені антитіла або ліганди, які взаємодіють із специфічними клітинними поверхневими маркерами. Наприклад, клітини можуть бути приведені у контакт із твердим субстратом (наприклад, колонка гранул, колби, магнітні частинки), що містить антитіла, та будь-які незв'язані клітини видаляють. Коли використовують твердий субстрат, що містить магнітні або парамагнітні гранули, клітини, зв'язані з цими гранулами, можуть бути легко виділені за допомогою магнітного сепаратору. У одному варіанті втілення, зазначену вихідну клітинну популяцію збагачують на бажаний фенотип клітинного маркеру (наприклад, CD34+, CD133+, CD90+) або базуючись на відтоку барвників, таких як родамін, хьохст (Hoechst) або активності альдегід дегідрогенази. У одному специфічному варіанті втілення, зазначену вихідну клітинну популяцію збагачують на CD34+ клітини. Способи збагачення клітинної популяції крові на CD34+ клітини включають набори, комерціалізовані Miltenyi Biotec (набір прямого виділення CD34+, Miltenyi Biotec, Bergisch, Gladbach, Germany) або Baxter (Isolex 3000). 17 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 Кількість пуповинної крові з одних пологів є часто недостатньою для лікування дорослого або підлітка. Одна перевага способів розмноження, використовуючи сполуки даного винаходу або агент, здатний регулювати у бік зменшення активність та/або експресію арилвуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору, полягає у тому, що вони дають можливість виробляти достатню кількість гематопоетичних стовбурових клітин тільки від однієї одиниці пуповинної крові. Відповідно, у одному варіанті втілення, вихідну клітинну популяцію отримують з клітин неонатальної пуповинної крові, яку збагачують CD34+ клітинами. У одному зв'язаному варіанті втілення, зазначену вихідну клітинну популяцію отримують з однієї або двох одиниць пуповинної крові. У іншому варіанті втілення, вихідну клітинну популяцію отримують з клітин мобілізованої периферичної крові людини, які збагачують CD34+ клітинами. У одному зв'язаному варіанті втілення, зазначену вихідну клітинну популяцію отримують з клітин мобілізованої периферичної крові людини, виділених тільки від одного пацієнта. Зазначена вихідна клітинна популяція може переважно містити щонайменше 50 % CD34+ 5 клітин, у деяких варіантах втілення, більше ніж 90 % CD34+ клітин, та може включати від 10 до 9 10 ядровмісних клітин. Вихідна клітинна популяція може бути використана безпосередньо для розмноження або заморожена та зберігатися до застосування пізніше. Умови культивування вихідної клітинної популяції для розмноження гематопоетичних стовбурових клітин буде змінюватися в залежності, серед інших, від вихідної клітинної популяції, бажаної кінцевої кількості клітин, та бажаної кінцевої пропорції HSC клітин. У одному специфічному варіанті втілення, зокрема, використовуючи вихідну клітинну популяцію з клітин пуповинної крові, збагачених CD34+ клітинами, умови культивування включають застосування інших цитокінів та факторів росту, в основному відомих у даній галузі техніки для розмноження гематопоетичних стовбурових клітин. Такі цитокіни та фактори росту включають без обмеження IL-1, IL-3, IL-6, IL-11, G-CSF, GM-CSF, SCF, FlT3-L, тромбопоетин (TPO), еритропоетин, та їх аналоги. Як використано у цьому описі, "аналоги" включають будь-які структурні варіанти цитокінів та факторів росту, що мають біологічну активність як форми природного походження, включаючи без обмеження, варіанти із посиленою або зменшеною біологічною активністю у порівнянні з формами природного походження, або агоністи цитокінового рецептору, такі як агоніст антитіла проти TPO рецептору (наприклад, VB22B sc(Fv)2, як детально описано у патентній публікації WO 2007/145227, та подібній). Комбінації цитокіну та фактору росту вибирають для розмноження HSC та клітин-попередників, при цьому обмежуючи вироблення остаточно диференційованих клітин. У одному специфічному варіанті втілення, один або більшу кількість цитокінів та факторів росту вибирають з групи, що складається з SCF, Flt3-L та TPO. У одному специфічному варіанті втілення, щонайменше TPO використовують у вільному від сироватки середовищі за прийнятних умов для розмноження HSC клітин. У одному зв'язаному варіанті втілення, суміш IL6, SCF, Flt3-L та TPO використовують у способі для розмноження HSC клітин у комбінації зі сполукою даного винаходу або агентом, здатним регулювати у бік зменшення активність та/або експресію арилвуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору. Людський IL6 або інтерлейкін-6, також відомий як B-клітинний стимулюючий фактор 2 описаний у (Kishimoto, Ann. review of Imm. 23:1 2005) та є комерційно доступним. Людський SCF або фактор стовбурових клітин, також відомий як c-kit ліганд, фактор росту мастоцитів або стальний фактор описані у (Smith, MA et al., ACTA Haematologica, 105, 3:143, 2001) та є комерційно доступними. Flt3-L або FLT-3 ліганд, що також називається як FL, являє собою фактор, який зв'язує flt3-рецептор. Він описаний у (Hannum C, Nature 368 (6472): 643-8) та є комерційно доступним. TPO або тромбопоетин, також відомий як фактор росту мегакаріоцитів (MGDF) або c-Mpl ліганд описаний у (Kaushansky K (2006). N. Engl. J. Med. 354 (19): 2034-45) та є комерційно доступним. Розмноження HSC клітин може бути проведене у базальному середовищі, яке доповнене сумішами цитокінів та факторів росту, розкритими вище. Базальне середовище, як правило, включає амінокислоти, джерела вуглецю, вітаміни, сироваткові білки (наприклад, альбумін), неорганічні солі, двовалентні катіони, буфери та будь-який інший елемент, що підходить для застосування у розмноженні HSC клітин. Приклади такого базального середовища, що ® підходить для способу розмноження HSC клітин, включають, без обмеження, StemSpan SFEM – безсироваткове середовище для розмноження (StemCell Technologies, Vancouver, Canada), 18 UA 103206 C2 ® 5 10 15 20 25 30 35 40 45 50 55 60 StemSpan H3000 – Середовище певного складу (StemCell Technologies, Vancouver, Canada), ® CellGro SCGM (CellGenix, Freiburg Germany), StemPro®-34 SFM (Invitrogen). У одному варіанті втілення, сполуку даного винаходу або агент, здатний регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору, вводять у процесі способу розмноження зазначеної вихідної клітинної популяції при концентрації, що придатна для розмноження HSC клітин. У одному специфічному варіанті втілення, зазначену сполуку або AhR модулюючий агент вводять при концентрації, що становить від 1 пM до 100 мкM, наприклад, від 10 пM до 10 мкM, або від 100 пM до 1 мкM. У одному специфічному варіанті втілення, коли вихідна клітинна популяція головним чином складається із CD34+ збагачених клітин від однієї або двох одиниць пуповинної крові, ці клітини вирощують за умов для розмноження HSC клітин від приблизно 3 днів до приблизно 90 днів, наприклад, від 7 до 2 днів та/або до одержання зазначеної кратності розмноження та характеристичних клітинних популяцій. У одному специфічному варіанті втілення, клітини вирощують за умов для розмноження HSC клітин не більше, ніж 21 день, 14 днів або 7 днів. У одному варіанті втілення, вихідну клітинну популяцію культивують впродовж часу, 5 6 7 8 достатнього для досягнення абсолютної кількості CD34+ клітин щонайменше 10 , 10 , 10 , 10 9 або 10 клітин. У іншому варіанті втілення, зазначену вихідну клітинну популяцію культивують впродовж часу, достатнього для 10-50000 разового розмноження CD34+ клітин, наприклад, від 100 до 10000 разового розмноження. Клітинна популяція, отримана після способу розмноження, може бути використана без додаткового очищення або може бути піддана стадіям додаткового очищення або відбору. Ця клітинна популяція далі може бути промита для видалення сполуки даного винаходу або будь-якого іншого агенту, здатного регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору, та/або будь-яких інших компонентів клітинної культури та знову суспендована у відповідному середовищі для клітинної суспензії для застосування у короткі терміни або у середовищі для тривалого зберігання, наприклад, середовищі, прийнятному для кріоконсервації. Клітинна популяція з розмноженими HSC клітинами, отримана за допомогою способу розмноження, та терапевтичні композиції Даний винахід додатково забезпечує клітинну популяцію з розмноженими HSC клітинами, що може бути отримана або яка отримана за допомогою способу розмноження, розкритого вище. У одному специфічному варіанті втілення, таку клітинну популяцію знову суспендують у фармацевтично прийнятному середовищі, що підходить для введення хазяїну-ссавцю, таким чином, забезпечуючи одержання терапевтичної композиції. Сполука, як описано у Короткому описі даного винаходу, або агент, здатний регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору, дозволяють розмножувати HSC клітини, наприклад, тільки від однієї або двох одиниць пуповинної крові, для забезпечення одержання клітинної популяції, кількісно та якісно придатної для ефективного короткострокового та тривалого приживлення трансплантату у пацієнта-людини, якій це необхідно. Зокрема, даний винахід відноситься до композиції, що включає клітинну популяцію з розмноженими HSC клітинами, отриману не більше, ніж з однієї або двох одиниць пуповинної крові, де зазначена 5 6 7 8 9 терапевтична композиція містить загальну кількість клітин щонайменше 10 , 10 , 10 , 10 або 10 клітин, при цьому 20-100 %, наприклад, 40-80 % від загальної кількості клітин є CD34+ клітинами. У одному зв'язаному варіанті втілення, зазначена композиція містить 0,1-40 %, наприклад, 0,1-10 % від загальної кількості клітин, що є CD34+Thy1+, та 20-80 % клітин є CD34+CD45RA+. У деяких специфічних варіантах втілення, зазначена композиція містить 1095 % клітин, що є CD38+, та 5-70 % клітин, що є CD133+. Застосування терапевтичних композицій Даний винахід додатково забезпечує клітинну популяцію з розмноженими HSC клітинами або її композицію для застосування у алогенній або аутологічній трансплантації стовбурових клітин у суб'єкта-ссавця. Суб'єкт, на який посилаються у даному описі, являє собою, наприклад, донора кісткового мозку або індивіда з виснаженими або обмеженими рівнями клітин крові або підвищеним ризиком їх мати. Необов'язково, суб'єкт являє собою донора кісткового мозку до відбирання кісткового мозку або донора кісткового мозку після відбирання кісткового мозку. Суб'єкт необов'язково являє собою реципієнта трансплантату кісткового мозку. Способи, розкриті у цьому описі, є особливо корисними у суб'єктів, які мають обмежений запас кісткового мозку, 19 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 таких як суб'єкти похилого віку або суб'єкти, які попередньо піддавалися лікуванню, що виснажує імунну систему, або мієлоаблятивному лікуванню, такому як хіміотерапія, наприклад, для лікування лейкемії або лімфом. Цей суб'єкт, необов'язково, має знижений рівень клітин крові або ризик появи зниженого рівня клітин крові у порівнянні з контрольним рівнем клітин крові. Як використано у цьому описі термін контрольний рівень клітин крові відноситься до середнього рівня клітин крові у суб'єкта до або по суті за відсутності явища, яке змінює рівні клітин крові у суб'єкта. Явище, яке змінює рівні клітин крові у суб'єкта, включає, наприклад, анемію, травму, хіміотерапію, трансплантацію кісткового мозку та променеву терапію. Наприклад, суб'єкт має анемію або втрату крові, наприклад, через травму. Розмножену HSC популяцію або композицію, що містить клітинну популяцію з розмноженими HSC клітинами, вводять суб'єкту, наприклад, до, у той же час або після хіміотерапії, променевої терапії або трансплантації кісткового мозку. Суб'єкт необов'язково має виснажений кістковий мозок, що пов'язане, наприклад, з вродженим, генетичним або набутим синдромом, що характеризується втратою кісткового мозку або виснаженим кістковим мозком. Таким чином, суб'єкт необов'язково являє собою суб'єкт, якому необхідне кровотворення. Необов'язково, суб'єкт являє собою донора кісткового мозку або являє собою суб'єкт з виснаженим кістковим мозком або має ризик ним стати. Маніпуляція з гематопоетичними стовбуровими клітинами є корисною як додаткове лікування до хіміотерапії або променевої терапії. Наприклад, HSC клітини збирають у периферичній крові та потім виділяють з суб'єкта, якого будуть піддавати хіміотерапії, та після цієї терапії, клітин повертають. Таким чином, суб'єкт являє собою суб'єкта, якого піддають або, як очікується, піддадуть лікуванню, що виснажує імунні клітини, такому як хіміотерапія, променева терапія, або який виступає як донор для трансплантації кісткового мозку. Кістковий мозок являє собою одну з найбільш продуктивних тканин у організмі та тому часто являє собою орган, який першочергово уражується хіміотерапевтичними лікарськими засобами та опромінюванням. Результатом є те, що вироблення клітин крові швидко руйнується у процесі хіміотерапії або променевого лікування, та хіміотерапія або опромінювання повинні бути обмежені для того, щоб дозволити кровотворній системі відновити запаси клітин крові до повторного лікування пацієнта хіміотерапією. Тому, як розкрито у цьому описі, HSC клітини або клітини крові, отримані за способами, описаними у цьому описі, необов'язково вводять таким суб'єктам, яким необхідні додаткові клітини крові. Забезпечуються HSC клітини, розмножені за допомогою сполуки даного винаходу або агенту, здатного регулювати у бік зменшення активність та/або експресію арил-вуглеводневого рецептору та/або нижчележачого ефектору шляху арил-вуглеводневого рецептору, або композицій з розмноженими HSC клітинами, як описано вище, у комбінації з терапевтичним засобом, здатним посилювати проліферацію HSC клітин in vivo, in vitro, або ex vivo (наприклад, невелика молекула, антитіло, або подібні), та необов'язково щонайменше одним фармацевтично прийнятним наповнювачем або носієм. Під терапевтичним засобом, здатним посилювати проліферацію HSC клітин розуміють такі як: агоніст антитіла проти TPO рецептору (наприклад, VB22B sc(Fv)2, як детально описано у патентній публікації WO 2007/145227, та подібній); цитокін, такий як SCF, IL-6, Flt-3 ліганд, TPO або TPO міметик (наприклад, такий як описаний у WO/2007/022269; WO/2007/009120; WO/2004/054515; WO/2003/103686; WO/2002/085343; WO/2002/049413; WO/2001/089457; WO/2001/039773; WO/2001/034585; WO/2001/021180; WO/2001/021180; WO/2001/017349; WO/2000/066112; WO/2000/035446; WO/2000/028987; WO/2008/028645; та подібних); гранулоцитарний колонієстимулюючий фактор (G-CSF); гранулоцитарно-моноцитарний колонієстимулюючий фактор (GM-CSF); простагландин або агоніст простагландинового рецептору (наприклад, агоніст простагландинового E2 рецептору-1 (EP-I), агоніст простагландинового E2 рецептору-2 (EP-2), агоніст простагландинового E2 рецептору -3 (EP-3) та агоністи простагландинового E2 рецептору-4 (EP-4), як детально описано у патентній публікації WO/2008/073748); тетраетиленпентамін (TEPA); Notch-ліганди (Дельта-1); та/або WNT агоніст. Крім того, культивування стовбурових клітин з мезенхімальними стовбуровими клітинами (MSC) запобігає появі хвороби трансплантат-проти-хазяїна (GVHD) та може допомогти розмноженню стовбурових клітин. MSC та стовбурові клітини можуть бути трансплантовані як цільна культура. Під фармацевтично прийнятним розуміють матеріал, який не є біологічно або іншим чином небажаним, тобто матеріал може бути введений суб'єкту або у клітину, не викликаючи небажаних біологічних ефектів або не взаємодіючи шкідливим чином з іншими компонентами фармацевтичної композиції, у якій він міститься. Носій або наповнювач вибирають таким чином, щоб мінімізувати розкладання активного інгредієнту та мінімізувати шкідливі побічні ефекти у суб'єкта або клітини. 20 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 Композиції формулюють будь-яким підходящим способом для застосування у способах, розкритих у цьому описі. Введення відбувається будь-яким шляхом, що, як відомо ординарно кваліфікованому спеціалісту, є ефективним. Наприклад, композиції вводять перорально, парентерально (наприклад, внутрішньовенно), шляхом внутрішньом'язової ін'єкції, шляхом внутрішньочеревної ін'єкції, крізьшкірно, екстракорпорально, інтраназально або місцево. Кращим способом введення є внутрішньовенна інфузія. Кількість влитих клітин буде залежати від факторів, таких як стать, вік, маса, типи хвороби або розладу, стадія розладу, відсоток бажаних клітин у клітинній популяції та кількість клітин, необхідна для одержання терапевтичної користі. У одному особливому варіанті втілення, композицію вводять 4 5 7 внутрішньовенною інфузією та вона включає щонайменше 10 клітин/кг, від 10 до 5.10 клітин/кг або більше, якщо необхідно. У одному специфічному варіанті втілення, всі влиті клітини є розмноженими клітинами пуповинної крові від одних пологів. Фармацевтично прийнятний носій для інфузії композиції, що містить клітини, у пацієнта, як правило, включає забуферений сольовий розчин з 5 % HSA або не доповнене базальне середовище або середовище, відоме у даній галузі техніки. Для перорального введення, композиції приймають форму, наприклад, таблеток або капсул, отриманих звичайними засобами з фармацевтично прийнятними наповнювачами, такими як зв'язуючі агенти (наприклад, пептизований кукурудзяний крохмаль, полівінілпіролідон або гідроксипропіл-метилцелюлоза); наповнювачі (наприклад, лактоза, мікрокристалічна целюлоза або гідрофосфат кальцію); любриканти (наприклад, стеарат магнію, тальк або кремнезем); дезінтегранти (наприклад, картопляний крохмаль або натрію гліколят крохмалю); або зволожуючі агенти (наприклад, лаурилсульфат натрію). Таблетки покривають за способами, добре відомими у даній галузі техніки. Рідкі препарати для перорального введення приймають форму, наприклад, розчинів, сиропів або суспензій, або вони можуть бути представлені у вигляді сухого продукту для розведення водою або іншим підходящим носієм перед застосуванням. Такі рідкі препарати одержують звичайними засобами з фармацевтично прийнятними добавками, такими як суспендуючи агенти (наприклад, сорбітовий сироп, похідні целюлози або гідрогеновані харчові жири); емульгуючи агенти (наприклад, лецитин або гумміарабік); не-водні носії (наприклад, мигдальне масло, масляні складні ефіри, етиловий спирт або фракціоновані рослинні масла); та консерванти (наприклад, метил або пропіл-пгідроксибензоати або сорбінова кислота). Препарати необов'язково містять буферні солі, ароматизатори, барвники та підсолоджувачі, якщо прийнятно. Композиції формулюють для парентерального введення за допомогою ін'єкції, наприклад, за допомогою болюсного вливання або безперервної інфузії. Склади для ін'єкції представляють у одиничній лікарській формі, наприклад, у ампулах або у багатодозних контейнерах, з доданим консервантом або без нього. Композиції приймають такі форми як суспензії, розчини або емульсії у масляних або водних носіях, та можуть містити складові агенти, такі як суспендуючі, стабілізуючі та/або диспергуючі агенти. Альтернативно, активний інгредієнт знаходиться у порошковій формі для розведення підходящим носієм, наприклад, таким як стерильна апірогенна вода, перед застосуванням. В основному, вода, підходяще масло, сольовий розчин, водний розчин декстрози (глюкоза), та зв'язані розчини цукру та гліколі, такі як пропіленгліколь або поліетиленгліколі, є підходящими носіями для парентеральних розчинів. Розчини для парентерального введення містять, наприклад, водорозчинну сіль активного інгредієнту, підходящі стабілізуючі агенти та, якщо необхідно, буферні речовини. Антиоксиданти, такі як бісульфат натрію, сульфіт натрію або аскорбінова кислота, або окремо або комбіновано, являють собою підходящі стабілізуючі агенти. Також необов'язково використовують лимонну кислоту та її солі та натрію етилендіамінтетраоцтову кислоту (EDTA). Крім того, парентеральні розчини необов'язково містять консерванти, такі як бензалконіум хлорид, метил- або пропілпарабен та хлорбутанол. Підходящі фармацевтичні носії описані у Remington: The Science and Practice of Pharmacy, 21st Edition, David B. Troy, ed., Lippicott Williams & Wilkins (2005), який включений шляхом посилання у його повноті щонайменше стосовно матеріалу, що пов'язаний з фармацевтичними носіями та композиціями. Композиції необов'язково формулюють у вигляді препарату депо. Такі склади тривалої дії необов'язково вводять шляхом імплантації. Таким чином, наприклад, композиції формулюють з підходящими полімерними або гідрофобними матеріалами (наприклад, у вигляді емульсій у прийнятному маслі) або іонообмінними смолами, або як важкорозчинні похідні, наприклад, у вигляді важкорозчинної солі. Композиції застосовують або вводять з імплантатами одночасно з або після хірургічного імплантату. Крім того, стандартні фармацевтичні способи використовують для контролю тривалості дії. Вони включають препарати контрольованого вивільнення та відповідні макромолекули, 21 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, полімери, поліскладні ефіри, поліамінокислоти, полівініл, піролідон, етиленвінілацетат, метилцелюлоза, карбоксиметилцелюлоза або протаміну сульфат. Концентрацію макромолекул, також як і способи включення підбирають для того, щоб контролювати вивільнення. Необов'язково, агент включають у частинки полімерних матеріалів, такі як поліскладні ефіри, поліамінокислоти, гідрогелі, співполімери полі(молочної кислоти) або етиленвінілацетату. Окрім включення, ці агенти необов'язково використовують для утримання сполуки у мікрокапсулах. Композицію для застосування у способах, описаних у цьому описі, необов'язково формулюють у вигляді складу з уповільненим та/або відстроченим вивільнення. Такі склади з уповільненим та/або відстроченим вивільнення одержують за допомогою засобів уповільненого вивільнення або пристроїв доставки, які добре відомі спеціалістам, ординарно кваліфікованим у даній галузі техніки. Ці композиції використовують для забезпечення повільного або уповільненого вивільнення одного або більшої кількості активних інгредієнтів, використовуючи, наприклад, гідропропілметилцелюлозу, інші полімерні матриці, гелі, проникні мембрани, осмотичні системи, багатошарові покриття, мікрочастинки, ліпосоми, мікросфери або їх комбінацію для забезпечення бажаного профілю вивільнення у змінних співвідношеннях. Підходящі склади з уповільненим вивільнення вибирають для застосування з композиціями, розкритими у цьому описі. Таким чином, використовують одиничні стандартні лікарські форми, що підходять для перорального введення, такі як, не обмежуючись наведеними, таблетки, капсули, гелеві капсули, каплети, порошки, які адаптовані для уповільненого вивільнення. Композиції необов'язково доставляють за допомогою системи контрольованого вивільнення. Наприклад, композицію вводять, використовуючи внутрішньовенну інфузію, імплантуємий осмотичний насос, ліпосоми, або інші способи введення. Системи контрольованого вивільнення поміщають у близькості до цілі. Необов'язково, бажано вводити композицію місцево, тобто у область, яка потребує лікування. Наприклад, композицію вводять шляхом ін'єкції, наприклад, у кістковий мозок довгої кістки. Місцеве застосування проводять, наприклад, шляхом місцевої інфузії впродовж хірургічної операції, місцевого введення (наприклад, у поєднанні з перев'язуванням рани після хірургічної операції), ін'єкції, катетеру, супозиторії або імплантату. Імплантат складається з пористого, непористого або желатинового матеріалу, включаючи мембрани, такі як силастикові мембрани, або волокон. Фармацевтичні композиції, розкриті у цьому описі, вводять будь-якими звичайними засобами, доступними для застосування у поєднанні з фармацевтичними препаратами, або як окремі терапевтичні активні інгредієнти або у комбінації терапевтичних активних інгредієнтів. Їх необов'язково вводять окремо, але в основному вводять з фармацевтичним носієм, вибраним на основі вибраного шляху введення та стандартної фармацевтичної практики. Сполуки, розкриті у цьому описі, забезпечують у фармацевтично прийнятній формі, включаючи їх фармацевтично прийнятні солі та похідні. Термін фармацевтично прийнятна форма відноситься до композицій, що включають сполуки, розкриті у цьому описі, які є в основному безпечними, відносно нетоксичними та не є ні біологічно ні іншим чином небажаними. Ці композиції необов'язково включають фармацевтично прийнятні носії або стабілізатори, які є нетоксичними для клітин або суб'єкта, що піддається їх дії, у використовуваних дозах та концентраціях. Приклади фізіологічно прийнятних носіїв включають буфери, такі як фосфат, цитрат та інші органічні кислоти; антиоксиданти, включаючи аскорбінову кислоту; поліпептиди з низькою молекулярною масою (менше, ніж приблизно 10 залишків); білки, такі як сироватковий альбумін, желатин, або імуноглобуліни; гідрофільні полімери, такі як полівінілпіролідон; амінокислоти, такі як гліцин, глутамін, аспарагін, аргінін або лізин; моносахариди, дисахариди, та інші карбогідрати, включаючи глюкозу, манозу або декстрини; хелатуючі агенти, такі як ЕДТА; цукрові спирти, такі як маніт або сорбіт; солеутворюючі протиіони, такі як натрій; та/або неіонні поверхнево-активні речовини, такі як TWEEN™ (Uniqema, United Kingdom), поліетиленгліколь (PEG), та PLURONICS™ (BASF, Germany). Термін фармацевтично прийнятні кислі солі та похідні відноситься до солей та похідних сполук Формули I, розкритих у цьому описі, які зберігають біологічну ефективність та властивості, як описано, та які не є біологічно або іншим чином небажаними. Фармацевтично прийнятні солі утворюють, наприклад, з неорганічними кислотами, такими як соляна кислота, бромистоводнева кислота, сірчана кислота, азотна кислота, фосфорна кислота та подібні, та органічними кислотами, такими як оцтова кислота, пропіонова кислота, гліколева кислота, піровиноградна кислота, щавлева кислота, малеїнова кислота, малонова кислота, бурштинова кислота, фумарова кислота, винна кислота, лимонна кислота, бензойна кислота, корична 22 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 кислота, мигдальна кислота, метансульфонова кислота, етансульфонова кислота, птолуолсульфонова кислота, саліцилова кислота, та подібні. Хімічну стабільність композиції, що включає сполуку Формули I або її фармацевтично прийнятну сіль або складний ефір, посилюють за допомогою способів, відомих спеціалісту, кваліфікованому у даній галузі техніки. Наприклад, складний ефір алканової кислоти та поліетоксильованого сорбіту (полісорбат) додають до композиції, що містить сполуку Формули I, у кількості, ефективній для посилення хімічної стабільності зазначеної сполуки. Дані, отримані з досліджень клітинної культури та досліджень на тваринах, необов'язково використовують у створенні інтервалу доз для застосування у людей. Доза таких сполук переважно лежить у інтервалі циркулюючих концентрацій, що мають невелику токсичність або не мають токсичності. Доза варіюється у цьому інтервалі в залежності від використовуваної лікарської форми та використовуваного шляху введення. Для будь-якої сполуки, що використовують у забезпечених способах, терапевтично ефективну дозу спочатку оцінюють з досліджень клітинної культури. У даному описі також забезпечується пакет або набір, що містить один або більшу кількість контейнерів, заповнених одним або більшою кількістю інгредієнтів, розкритих у цьому описі. Такі набори необов'язково включають розчини та буфери, якщо необхідно або бажано. Набір необов'язково включає розмножену популяцію стовбурових клітин, отриману за способами, розкритими вище, або може містити контейнери або композиції для одержання розмноженої популяції HSC клітин. Зокрема, даний винахід забезпечує набір для розмноження ex vivo гематопоетичних стовбурових клітин, що включає сполуку, як визначено у Короткому описі даного винаходу, та інструкції для застосування такої сполуки у способі для розмноження HSC клітин та, необов'язково, один або більшу кількість цитокінів або факторів росту, або середовище для росту клітин, зокрема середовище для росту гематопоетичних стовбурових клітин, як описано вище. Цей набір може додатково включати антитіла для контролювання вироблення клітин, такі як анти-CD34, анти-CD133, анти-CD38, анти-CD45RA та/або анти-Thy1 антитіла. У одному специфічному варіанті втілення, такий набір додатково включає один або більшу кількість цитокінів або факторів росту, що вибирають з групи, яка складається з IL6, FLT3-L, SCF та TPO. Необов'язково зв'язаними з таким(и) пакетом(ами) або набором(ами) є інструкції для застосування. Також забезпечується набір для забезпечення ефективної кількості сполуки даного винаходу для збільшення кількості HSC клітин у суб'єкта, що включає одну або більшу кількість доз сполуки для застосування впродовж періоду часу, де загальна кількість доз сполуки даного винаходу у наборі дорівнює ефективній кількості, достатній для збільшення кількості HSC клітин у суб'єкта. Період часу становить від приблизно одного до декількох днів або тижнів або місяців. Таким чином, період часу становить від щонайменше приблизно 5, 6, 7, 8, 10, 12, 14, 20, 21, 30 або 60 днів або більше або будь-яку кількість днів від одного до 90. Способи одержання сполук даного винаходу Даний винахід також включає способи одержання сполук даного винаходу. У описаних реакціях, може бути необхідно захистити реакційноздатні функціональні групи, наприклад, гідрокси, аміно, іміно, тіо або карбокси групи, де вони є бажаними у кінцевому продукті, для уникнення їх небажаного приймання участі у реакціях. Звичайні захисні групи можуть бути використані у відповідності зі стандартною практикою, наприклад, дивись T.W. Greene та P. G. M. Wuts у "Protective Groups in Organic Chemistry", John Wiley and Sons, 1991. Наступні схеми реакцій 1-5 детально описують одержання сполук даного винаходу. Спеціаліст, кваліфікований у даній галузі техніки, визнає, що наступне введення за допомогою способів, деталізованих нижче, будь-якої з груп R1, R2, R3, R4, та L1 необов'язково може бути додатково удосконалене за відомими трансформаціями для одержання бажаних кінцевих сполук Формули I. Сполуки Формули I можуть бути одержані відповідно до наступної Схеми реакції 1: Схема реакції 1 23 UA 103206 C2 Cl Cl G3 Cl G4 R4 -X1 (7) G2 G1 N H G3 Cl G4 (6) G2 G1 N R4 (4) R1 R2 H2 N R2 L1 L1 (5) HN R2 OH G4 G3 G2 G1 N R4 R1 (2) 5 10 15 20 25 HN (3) G3 Cl HO B G4 L1 G2 G1 N R4 (I) у якій G1, G2, G3, G4, R1, R2 та R4 приймають значення, визначені для Формули I у Короткому описі даного винаходу та L Формули I визначений у схемі реакції як –NH-L1-, який являє собою еквівалент, наприклад, –NR5a(CH2)0-3–, де R5a являє собою водень та –(CH2)0-3– являє собою L1. Сполуки Формули I можуть бути одержані шляхом введення у реакцію сполуки Формули 2 зі сполукою Формули 3 в присутності прийнятного каталізатору (наприклад, Pd2(dba)3, або подібні) в присутності відповідного ліганду (наприклад, 1,3-біс(2,4,6-триметилфеніл)імідазоліум хлорид), прийнятної основи (наприклад, Cs2CO3, або подібної) та прийнятного розчиннику (наприклад, 1,4-діоксану) при температурі від приблизно 80 до 100 °C впродовж 2 до приблизно 48 годин. Сполуки Формули 2 у свою чергу можуть бути одержані шляхом введення у реакцію сполуки Формули 4 з невеликим надлишком амінної сполуки Формули 5 у прийнятному розчиннику (наприклад, ізопропанолі) при температурі від приблизно кімнатної температури до приблизно 80 °C. Сполуки Формули 4 можуть бути одержані шляхом алкілування сполуки Формули 6 з придатним алкілуючим агентом 7, у якому X1 являє собою хлор, бром, йод або сульфонатний складний ефір, в присутності прийнятної основи (наприклад, гідриду натрію або карбонату калію), у прийнятному розчиннику (наприклад, ДМФА), при температурі від приблизно 0 °C до приблизно 80 °C. Альтернативно, реакція може бути проведена за умов Мітсунобу, використовуючи придатний спирт R4-OH в присутності підходящого фосфіну (наприклад, трифенілфосфіну) та азодикарбоксилату (наприклад, діетилазодикарбоксилату), у інертному розчиннику, такому як ТГФ або толуол, при температурі від приблизно 0 °C до приблизно кімнатної температури. Сполуки Формули Ia, у яких G1 являє собою CR3 та у яких всі інші G групи являють собою N, також можуть бути одержані шляхом проведення процесу як у наступній Схемі реакції 2: Схема реакції 2 у якій R1, R2, R3 та R4 приймають значення, визначені для Формули I у Короткому описі даного винаходу, та L Формули I визначений у схемі реакції як –NH-L1-, який являє собою 24 UA 103206 C2 5 10 15 20 25 30 35 40 45 еквівалент, наприклад, до –NR5a(CH2)0-3–, де R5a являє собою водень та –(CH2)0-3– являє собою L1. Сполуки Формули I можуть бути одержані шляхом введення у реакцію сполуки Формули 8 з амінною сполукою Формули 5 у прийнятному розчиннику (наприклад, ізопропанолі) при o температурі від приблизно кімнатної температури до приблизно 100 C. Сполуки Формули 8 у свою чергу можуть бути одержані шляхом введення у реакцію сполуки Формули 9 зі сполукою Формули 3 в присутності прийнятного каталізатору (наприклад, Pd(Ph 3P)4, Pd2(dba)3 або подібного), необов'язково в присутності прийнятного ліганду (наприклад, 1,3-біс(2,4,6триметилфеніл)імідазолiум хлорид), підходящої основи (наприклад, Cs2CO3, або подібної) та придатного розчиннику (наприклад, 1,4-діоксану) при температурі від приблизно 80 до 100 °C впродовж від 2 до приблизно 48 годин. Сполуки Формули 9 у свою чергу можуть бути одержані шляхом введення у реакцію сполуки Формули 10 з сумішшю ді-йодметану, йодиду міді(I), та алкіл-нітриту (наприклад, ізоамілнітриту), необов'язково в присутності інертного розчиннику, при температурі від приблизно 50 до 100 °C. Сполуки Формули 10 можуть бути одержані шляхом алкілування сполуки Формули 11 з прийнятним алкілуючим агентом 7, у якому X 1 являє собою хлор, бром, йод або сульфонатний складний ефір, в присутності прийнятної основи (наприклад, гідриду натрію або карбонату натрію), у придатному розчиннику (наприклад, ДМФА), при температурі від приблизно 0 °C до приблизно 80 °C. Альтернативно, реакція може бути проведена за умов Мітсунобу, використовуючи придатний спирт R 4-OH в присутності прийнятного фосфіну (наприклад, трифенілфосфіну) та азодикарбоксилату (наприклад, діетилазодикарбоксилату), у інертному розчиннику, такому як ТГФ або толуол, при температурі o від приблизно 0 C до приблизно кімнатної температури. Сполуки Формули II, які є підмножиною сполук Формули I, у яких R 1 являє собою N-зв'язаний гетероцикліл або N-зв'язаний гетероарил, можуть бути одержані як детально описано у наступній Схемі реакцій 3: Схема реакції 3 R2 H R2 L1 R1 HN L1 HN (20) G2 G3 G2 G1 G3 G1 N G4 R1 R4 G4 N Cl R4 (2) (II) G1, G2, G3, G4, R1, R2 та R4 приймають значення, визначені для Формули I у Короткому описі даного винаходу та L Формули I визначений у схемі реакції як –NH-L1-, який являє собою еквівалент, наприклад, до –NR5a(CH2)0-3–, де R5a являє собою водень та –(CH2)0-3– являє собою L1. Сполуки Формули II можуть бути одержані шляхом введення у реакцію сполуки Формули 2 зі сполукою Формули 20 в присутності надлишку циклічного аміну або NH-несучого гетероциклу (наприклад, заміщеного піразолу, заміщеного імідазолу та подібного), при температурі від приблизно 50 °C до приблизно 250 °C, впродовж від приблизно 1 до приблизно 24 годин, необов'язково в присутності основи, такої як гідрид натрію або DBU. Сполуки Формули 10, у яких G1 являє собою CR3, та у яких всі інші G групи являють собою N, також можуть бути одержані шляхом проведення процесу як у наступній Схемі реакції 4: Схема реакції 4 де R3 та R4 приймають значення, визначені для Формули I у Короткому описі даного винаходу. Сполуки Формули 10 можуть бути одержані відповідно до процедур, описаних у J. Med. Chem, 1972, 456, та J. Med. Chem., 1992, 4180. Ортоскладноефірну сполуку Формули 21 вводять у реакцію зі сполукою Формули 22, необов'язково в присутності кислоти, такої як оцтова кислота, при температурі від приблизно кімнатної температури до приблизно 150 °C, впродовж від приблизно 1 до приблизно 24 годин. Сполука Формули 22 у свою чергу може бути одержана 25 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 шляхом введення у реакцію сполуки Формули 23 зі сполукою первинного аміну Формули 24, необов'язково в присутності кислоти, такої як pTSA, або основи, такої як триетиламін або DBU, при температурі від приблизно 50 до приблизно 200 °C. Сполуки Формули IV можуть бути одержані як детально описано у наступній Схемі реакції 5: Схема реакції 5 R2 R2 L1 L1 HN HN G2 G3 G2 G1 G3 G1 N R1 G4 OH R1 G4 N O R20 R21 R20 R 21 O (IV) (III) де G1, G2, G3, G4, R1 та R2 приймають значення, визначені для Формули I у Короткому описі даного винаходу, та L Формули I визначений у схемі реакції як –NH-L1-, який являє собою еквівалент, наприклад, до –NR5a(CH2)0-3–, де R5a являє собою водень та –(CH2)0-3– являє собою L1. R20 та R21 незалежно вибирають з таких як: водень та C1-4алкіл. Сполука Формули IV, у якій R21 являє собою водень, може бути одержана зі сполуки Формули III шляхом обробки з придатним відновлюючим агентом, таким як алюмогідрид літію або діізобутил-алюмогідрид, у придатному розчиннику, такому як ТГФ або толуол, при температурі від приблизно -78 °C до приблизно 50 °C. Реакція до закінчення займає від 0,5 до приблизно 16 годин. Сполука Формули IV, у якій R21 являє собою нижчий алкіл, може бути одержана шляхом обробки сполуки Формули III з алкіл-літієм або реагентом Гріньяра, у придатному розчиннику, такому як ефір або тетрагідрофуран, при температурі від приблизно -78 °C до приблизно 50 °C. Реакція до закінчення займає від 0,5 до приблизно 16 годин. Детальні приклади синтезу сполуки Формули I можуть бути знайдені у Прикладах, представлених нижче. Додаткові способи одержання сполук даного винаходу Сполука даного винаходу може бути одержана у вигляді солі приєднання фармацевтично прийнятної кислоти шляхом введення у реакцію вільно-основної форми зазначеної сполуки з фармацевтично прийнятною неорганічною або органічною кислотою. Альтернативно, сіль приєднання фармацевтично прийнятної основи зазначеної сполуки даного винаходу може бути одержана шляхом введення у реакцію вільно-кислотної форми зазначеної сполуки з фармацевтично прийнятною неорганічною або органічною основою. Альтернативно, сольові форми сполук даного винаходу можуть бути одержані, використовуючи солі вихідних матеріалів або проміжних сполук. Наприклад, сольові форми 4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6іламіно)етил)фенолу (Приклад 1, нижче) синтезовані наступним чином: Мезилатна сіль: 4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)-фенольну вільну основу (0,60 г; 1,40 ммоль) розчиняють у 12 мл ацетону при 50 °C. Метансульфонову кислоту (0,137 г; 1,40 ммоль) додають краплинним способом. Кристалізація проходить швидко. Білу суспензію залишають охолодитися впродовж приблизно 30 хвилин з охолодженням до кімнатної температури. Цю суспензію перемішують впродовж 18 годин при кімнатній температурі та фільтрують. Тверду речовину промивають ацетоном (6 мл) трьома частинами та сушать спочатку впродовж приблизно 3 годин при 50 °C / приблизно 10 мбар та потім впродовж приблизно 16 годин при 80 °C / приблизно 10 мбар. Цей матеріал має температуру плавлення при приблизно 233 °C з ентальпією плавлення 98 г/Дж. Отриманий матеріал показав втрату при сушінні 0,2 %. Поглинання води оцінюють за термогравіметрією після піддавання відносній вологості (80 %вв) впродовж 24 годин. Спостерігають 0,4 % поглинання води. У іншому варіанті втілення, даний винахід забезпечує мезилатну сіль сполуки Прикладу 1. У додатковому варіанті втілення, даний винахід забезпечує мезилатну сіль сполуки Прикладу 1, що включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 6,4, 6,7, 18,3, 18,6, 26,9; та що у додатковому варіанті втілення включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 6,4, 6,7, 10,3, 12,9, 16,4, 18,3, 25,8, 26,5, 26,9. У ще одному додатковому варіанті втілення, даний винахід забезпечує мезилатну сіль сполуки Прикладу 1, що має модель порошкової рентгенівської дифракції, показану на Фігурі 3 у цьому описі. 26 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 60 Тозилатна сіль: 4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенольну вільну основу (0,60 г; 1,40 ммоль) розчиняють у 12 мл при 50 °C. Розчин паратолуолсульфонової кислоти моно-гідрату (0,271 г; 1,40 ммоль) у ацетоні (1,2 мл) додають краплинним способом. У цей розчин вводять зародки кристалізації при 50 °C та кристалізація відбувається швидко. Цю суспензію залишають охолодитися впродовж приблизно 30 хвилин до кімнатної температури та перемішують впродовж приблизно 18 годин. Після фільтрування тверду речовину промивають ацетоном (6 мл) трьома частинами та сушать спочатку впродовж приблизно 3 годин при 50 °C / приблизно 10 мбар та потім впродовж приблизно 16 годин при 80 °C /приблизно 10 мбар. Цей матеріал має температуру плавлення при приблизно 233 °C з ентальпією плавлення 88 г/Дж. Отриманий матеріал показав втрату при сушінні 0,2 %. Поглинання води оцінюють за термогравіметрією після піддавання відносній вологості (80 %вв) впродовж 24 годин. Спостерігають 0,4 % поглинання води. У іншому варіанті втілення, даний винахід забезпечує тозилатну сіль сполуки Прикладу 1. У додатковому варіанті втілення, даний винахід забезпечує тозилатну сіль сполуки Прикладу 1, що включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 6,2, 13,3, 16,7, 19,5, 25,4; та що у додатковому варіанті втілення включає наступні піки порошкової рентгенівської дифракції: 6,2, 7,6, 12,4, 13,3, 15,1, 16,7, 17,7, 19,5, 20,2, 24,6, 24,9, 25,4, 25,6. У ще одному додатковому варіанті втілення, даний винахід забезпечує тозилатну сіль сполуки Прикладу 1, що має модель порошкової рентгенівської дифракції, показану на Фігурі 4 у цьому описі. Сульфатна сіль: 4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)-фенольну вільну основу (0,60 г; 1,40 ммоль) розчиняють у 10 мл ацетону та 1 мл води при приблизно 55 °C. Розчин сірчаної кислоти (0,280 г; 2,79 ммоль) у 1 мл води додають краплинним способом. Кристалізація проходить швидко. Цю суспензію залишають охолодитися впродовж приблизно 30 хвилин з охолодженням до кімнатної температури, перемішують впродовж приблизно 18 годин та фільтрують. Осад на фільтрі промивають за допомогою 6 мл ацетону трьома частинами та сушать спочатку впродовж приблизно 3 годин при 50 °C /приблизно 10 мбар та потім впродовж приблизно 16 годин при 80 °C /приблизно 10 мбар. Цей матеріал має температуру плавлення при приблизно 224 °C з ентальпією плавлення 91 г/Дж. Отриманий матеріал показав втрату при сушінні 0,05 %. Поглинання води оцінюють за термогравіметрією після піддавання відносній вологості (80 %вв) впродовж 24 годин. Спостерігають 0,2 % поглинання води. У іншому варіанті втілення, даний винахід забезпечує сульфатну сіль сполуки Прикладу 1. У додатковому варіанті втілення, даний винахід забезпечує сульфатну сіль сполуки Прикладу 1, що включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 6,5, 6,8, 10,7, 13,5, 26,4, 27,6; та що у додатковому варіанті втілення включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 6,5, 6,8, 10,7, 13,1, 13,5, 18,6, 18,8, 20,8, 26,4, 27,1, 27,6. У ще одному додатковому варіанті втілення, даний винахід забезпечує сульфатну сіль сполуки Прикладу 1, що має модель порошкової рентгенівської дифракції, показану на Фігурі 6 у цьому описі. Езилатна сіль: 4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)-фенольну вільну основу (0,60 г; 1,40 ммоль) розчиняють у 12 мл ацетону при 50 °C. Етансульфонову кислоту (0,155 г; 1,40 ммоль) додають краплинним способом. Кристалізація відбувається швидко. Отриману білу суспензію залишають охолодитися впродовж приблизно 30 хвилин до кімнатної температури. Цю суспензію перемішують впродовж приблизно 18 годин при кімнатній температурі та фільтрують. Тверду речовину промивають за допомогою 6 мл ацетону трьома частинами та сушать спочатку впродовж приблизно 3 годин при 50 °C /приблизно 10 мбар та потім впродовж приблизно 16 годин при 80 °C /приблизно 10 мбар. Цей матеріал має температуру плавлення при приблизно 231 °C з ентальпією плавлення 76 г/Дж. Отриманий матеріал показав втрату при сушінні 0,6 %. Поглинання води оцінюють за термогравіметрією після піддавання відносній вологості (80 %вв) впродовж 24 годин. Спостерігають 0,05 % поглинання води. У іншому варіанті втілення, даний винахід забезпечує езилатну сіль сполуки Прикладу 1. У додатковому варіанті втілення, даний винахід забезпечує езилатну сіль сполуки Прикладу 1, що включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 6,3, 9,9, 18,4, 25,3, 26,1; та що у додатковому варіанті втілення включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 6,3, 9,9, 17,1, 17,9, 18,4, 19,0, 22,0, 25,3, 26,1, 27,1. У ще одному додатковому варіанті втілення, даний винахід забезпечує езилатну сіль сполуки Прикладу 1, що має модель порошкової рентгенівської дифракції, показану на Фігурі 8 у цьому описі. 27 UA 103206 C2 5 10 15 20 25 30 35 40 45 50 55 Гідробромідна сіль: 4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенольну вільну основу (0,60 г; 1,40 ммоль) розчиняють у 6 мл ДМФА при 65 °C. Гідробромну кислоту 48 % (0,235 г; 1,40 ммоль) додають краплинним способом. Цей розчин залишають охолодитися впродовж приблизно 30 хвилин до кімнатної температури. Зародки кристалізації додають при 55 °C та кристалізація відбувається повільно. Цю суспензію перемішують впродовж приблизно 18 годин при кімнатній температурі та фільтрують. Тверду речовину промивають за допомогою 4 мл суміші ДМФА/вода 1:1 та 6 мл води. Сіль сушать спочатку впродовж приблизно 3 годин при 50 °C / приблизно 10 мбар та потім впродовж приблизно 16 годин при 80 °C /приблизно 10 мбар. Цей матеріал має температуру плавлення при приблизно 285 °C з ентальпією плавлення 119 г/Дж. Отриманий матеріал показав втрату при сушінні 1,0 %. Поглинання води оцінюють за термогравіметрією після піддавання відносній вологості (80 %вв) впродовж 24 годин. Ніякого поглинання води не спостерігається. У іншому варіанті втілення, даний винахід забезпечує гідробромідну сіль сполуки Прикладу 1. У додатковому варіанті втілення, даний винахід забезпечує гідробромідну сіль сполуки Прикладу 1, що включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 7,0, 25,9, 26,8, 27,9; та що у додатковому варіанті втілення включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 7,0, 11,4, 13,3, 21,4, 23,4, 25,9, 26,4, 26,8, 27,9. У ще одному додатковому варіанті втілення, даний винахід забезпечує гідробромідну сіль сполуки Прикладу 1, що має модель порошкової рентгенівської дифракції, показану на Фігурі 9 у цьому описі. Оротатна сіль: 4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)-фенольну вільну основу (0,60 г; 1,40 ммоль) та оротову кислоту (0,222 г; 1,40 ммоль) розчиняють у 7,8 мл NMP (1-Метил-2-піролідон) при 85 °C. Цей розчин охолоджують до 60 °C та 6 мл води додають краплинним способом впродовж приблизно 5 хвилин. Отриману білу суспензію залишають охолодитися впродовж приблизно 30 хвилин до кімнатної температури та перемішують впродовж 18 годин. Після фільтрування осад на фільтрі промивають за допомогою 4 мл суміші NMP/вода 1:1 двома частинами та 6 мл води трьома частинами. Тверду речовину сушать спочатку впродовж приблизно 3 годин при 50 °C /приблизно 10 мбар та потім впродовж приблизно 16 годин при 80 °C /приблизно 10 мбар. Цей матеріал має температуру плавлення при приблизно 240 °C з ентальпією плавлення 130 г/Дж. Отриманий матеріал показав втрату при сушінні 0,05 %. Поглинання води оцінюють за термогравіметрією після піддавання відносній вологості (80 %вв) впродовж 24 годин. Спостерігається поглинання води 1,7 %. У іншому варіанті втілення, даний винахід забезпечує оротатну сіль сполуки Прикладу 1. У додатковому варіанті втілення, даний винахід забезпечує оротатну сіль сполуки Прикладу 1, що включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 7,1, 16,3, 19,2, 23,5, 25,6, 26,9; та що у додатковому варіанті втілення включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 7,1, 14,4, 16,3, 18,6, 19,2, 21,7, 23,0, 23,5, 25,6, 26,9, 28,7. У ще одному додатковому варіанті втілення, даний винахід забезпечує оротатну сіль сполуки Прикладу 1, що має модель порошкової рентгенівської дифракції, показану на Фігурі 10 у цьому описі. Гемі-фумаратна сіль: 4-(2-(2-(бензо[b]тіофен-3-іл)-9-ізопропіл-9H-пурин-6-іламіно)етил)фенольну вільну основу (0,60 г; 1,40 ммоль) розчиняють у 18 мл метанолу при 65 °C. Додають фумарову кислоту (0,164 г; 1,40 ммоль) та 6 мл метанолу. Цей розчин залишають охолодитися впродовж приблизно 30 хвилин до кімнатної температури. Декілька зародків кристалізації додають при 60 °C та кристалізація відбувається повільно. Цю суспензію перемішують впродовж 18 годин при кімнатній температурі та фільтрують. Тверду речовину промивають за допомогою 6 мл метанолу трьома частинами та сушать спочатку впродовж приблизно 3 годин при 50 °C /приблизно 10 мбар та потім впродовж приблизно 16 годин при 80 °C /приблизно 10 мбар. Цей матеріал має температуру плавлення при приблизно 232 °C з ентальпією плавлення 83 г/Дж. Отриманий матеріал показав втрату при сушінні 0,05 %. Поглинання води оцінюють за термогравіметрією після піддавання відносній вологості (80 %вв) впродовж 24 годин. Спостерігається поглинання води 0,3 %. У іншому варіанті втілення, даний винахід забезпечує гемі-фумаратну сіль сполуки Прикладу 1. У додатковому варіанті втілення, даний винахід забезпечує гемі-фумаратну сіль сполуки Прикладу 1, що включає наступні піки порошкової рентгенівської дифракції (Кут 2тета°): 7,2, 8,7, 14,4, 15,8, 17,4, 19,0, 23,7; та що у додатковому варіанті втілення включає наступні піки порошкової рентгенівської дифракції (Кут 2-тета°): 7,2, 8,7, 10,8, 14,4, 15,8, 17,4, 17,8, 19,0, 20,1, 23,7, 27,5. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюCompounds that expand hematopoietic stem cells
Автори російськоюBoitano, Anthony, Cooke, Michael, Pan, Shifeng, Schultz, Peter G., Tellew, John, Wan, Yongqin, Wang, Xing
МПК / Мітки
МПК: A61K 31/52, C07D 473/34, A61K 31/519, A61P 37/00, C07D 487/04
Мітки: сприяють, гематопоетичних, стовбурових, росту, клітин, сполуки
Код посилання
<a href="https://ua.patents.su/96-103206-spoluki-shho-spriyayut-rostu-gematopoetichnikh-stovburovikh-klitin.html" target="_blank" rel="follow" title="База патентів України">Сполуки, що сприяють росту гематопоетичних стовбурових клітин</a>
Попередній патент: Спосіб одержання ліпідів з біомаси
Наступний патент: Гідравлічна система із середовищем під тиском (варіанти) та спосіб її застосування
Випадковий патент: Поршень для двигуна внутрішнього згорання












