Спосіб отримання похідних 1-(2-галогенбіфеніл-4-іл)-циклопропанкарбонової кислоти
Номер патенту: 101835
Опубліковано: 13.05.2013
Автори: Ботте Губерт, Піветті Фаусто, Фоллеас Беноі, Делакруа Томас
Формула / Реферат
1. Спосіб отримання сполуки загальної формули (І)
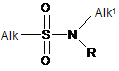 , (І)
, (І)
де
X - флуор;
R - один або більше атомів галогену,
вказаний спосіб включає нижченаведені стадії, за якими:
(і) сполуку формули (II)
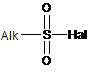 , (II)
, (II)
де X визначено вище, X' вибрано з групи: хлор, бром, йод або трифлат (CF3SO2), піддають реагуванню зі сполукою формули (III)
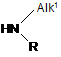 , (IIІ)
, (IIІ)
де R визначено вище, з утворенням сполуки формули (IV)
 ; (IV)
; (IV)
(іі) сполуку формули (IV) піддають радикальному бромуванню з утворенням сполуки формули (V)
 ; (V)
; (V)
ііі) сполуку формули (V) перетворюють у відповідну нітрильну похідну формули (VI)
 ; (VI)
; (VI)
iv) сполуку формули (VI) піддають реагуванню з 1,2-дибромметаном з утворенням сполуки формули (VII)
 ; (VII)
; (VII)
v) сполуку формули (VII) гідролізують з утворенням сполуки формули (І).
2. Спосіб за п. 1, що додатково включає стадії виділення та кристалізації сполуки формули (І).
3. Спосіб за п. 2, де кристалізацію проводять із застосуванням суміші н-гептану та ізопропанолу.
4. Спосіб за будь-яким з пп. 1-3, де етап (і) проводять при наявності паладієвого каталізатора, вибраного з групи, що складається з: тетракис(трифенілфосфін)паладію, паладію на активованому вугіллі та паладію на алюмінію оксиді.
5. Спосіб за п. 4, де паладієвим каталізатором є паладій на активованому вугіллі.
6. Спосіб за будь-яким з попередніх пунктів, де стадію (іі) проводять з N-бромсукцинімідом при наявності каталітичної кількості бензоїлпероксиду, застосовуючи ацетонітрил як розчинник.
7. Спосіб за п. 1, де атомом галогену є хлор.
8. Спосіб за п. 7, де сполукою формули (І) є 1-(3',4'-дихлор-2-флуор[1,1'-біфеніл]-4-іл)циклопропанкарбонова кислота.
9. Спосіб за п. 8, що включає нижченаведені стадії, за якими:
(і) 4-бром-3-флуортолуєн піддають реагуванню з 3,4-дихлорфенілбороновою кислотою з утворенням 3',4'-дихлор-2-флуор-4-метилбіфенілу;
(іі) 3',4'-дихлор-2-флуор-4-метилбіфеніл піддають радикальному бромуванню з утворенням 3',4'-дихлор-2-флуор-4-бромметилбіфенілу;
ііі) 3',4'-дихлор-2-флуор-4-бромметилбіфеніл перетворюють у відповідний 3',4'-дихлор-2-флуор-4-ціанометилбіфеніл;
iv) 3',4'-дихлор-2-флуор-4-ціанометилбіфеніл піддають реагуванню з 1,2-диброметаном з утворенням 1-(3',4'-дихлор-2-флуор[1,1'-біфеніл]-4-іл)циклопропаннітрилу;
v) 1-(3',4'-дихлор-2-флуор[1,1'-біфеніл]-4-іл)циклопропаннітрил гідролізують з утворенням 1-(3',4'-дихлор-2-флуор[1,1'-біфеніл]-4-іл)циклопропанкарбонової кислоти.
10. Спосіб отримання фармацевтичної композиції, що включає стадії (і)-(v) за п. 1 та додаткову стадію (vi), за якою додають один або більше фармацевтично прийнятних наповнювачів.
Текст
Реферат: Винахід стосується способу отримання сполуки формули (І) COOH X R , (І) а також прийнятних проміжних сполук способу. UA 101835 C2 (12) UA 101835 C2 UA 101835 C2 Винахід стосується способу отримання сполуки формули (І): COOH (І) 5 10 X R Винахід також стосується корисних інтермедіатів. Хвороба Альцгеймера є нейродегенеративним розладом, що характеризується розсіяною наявністю зовнішньоклітинних та периваскулярних нейритних бляшок та внутрішньоклітинних нейрофібрилярних сплетінь у церебральній паренхімі пацієнтів з хворобою Альцгеймера. Нейритні бляшки головним чином складаються з агрегатів білку з 39-43 амінокислотних залишків, відомого як β-амілоїд (βА), та, залежно від числа амінокислот, Аβ39, Аβ40, Аβ42 та Аβ43. У рівні техніки повідомлено про сполуки, що можуть зменшувати вироблення найбільш нейротоксичної ізоформи β-амілоїду, що містить 42 амінокислоти (Аβ42), їх взаємодією з макромолекулярним/багатобілковим ферментним комплексом з аспартил-протеазною активністю, відомим як γ-секретаза. Зокрема WО 2004/074232 розкриває похідні 1-(2-галогенбіфеніл-4-іл)циклопропанкарбонової кислоти загальної формули (І) COOH (І) X R 15 20 25 30 35 40 де Х та R визначені нижче, здатні модулювати активність γ-секретази без впливу на інші важливі метаболічні процеси, як-то активність ферментів циклооксигеназ. Ключовим етапом отримання вказаних сполук є реакція Сузукі між придатною фенілбороновою кислотою або її естером з 3,4-дигалогенциклопропанкарбоновою кислотою. У WО 2004/074232, 3,4-дигалогенциклопропанкарбонову кислоту отримують, починаючи з 3,4-дигалогентолуєну, котрий перетворюють у відповідний бензилбромід бромуванням радикалу у карбон тетрахлориді (ССl4); утворений бромід перетворюють у 3,4дигалогенфенілацетонітрил; останній реагує з 1,2 диброметаном, утворюючи відповідний 3,4дигалогенфенілциклопропаннітрил, що далі гідролізують до потрібної 3,4дигалогенциклопропанкарбонової. Однак, спосіб, описаний у WО 2004/074232, дає низький загальний вихід (12-14 %) та потерпає від суворих обмежень для промислового застосування. Наприклад, етап бромування радикалу дає значну кількість біс-галогенованого побічного продукту та задіює застосування ССl4, що є дуже токсичним, озон-виснажливим газом. На додаток, кінцева реакція сполучення Сузукі дає поганий вихід та утворений продукт важко очищати кристалізацією без втрати виходу. Наприклад, хроматографію на силікагелі застосовано для такої очистки, але хроматографія на силікагелі у збільшеному масштабі є трудомісткою та потребує великих об'ємів розчинників. Тому об'єктом цього винаходу забезпечити спосіб отримання похідних 1-(2-галогенбіфеніл4-іл)-циклопропанкарбонової кислоти формули (І), альтернативний розкритому у WО 2004/074232, що не має усіх вищезгаданих вад. Об'єктом цього винаходу є проведення реакції Сузукі на першому етапі. Більш того, впроваджені відмінні умови для поліпшення виходу з інших етапів, зокрема етапу бромування радикалу. Спосіб винаходу є більш ефективним, особливо для вироблення у великому масштабі, забезпечуючи вищий вихід сполуки формули (І) з високою хімічною чистотою без потреби хроматографічної очистки. Предметом цього винаходу є спосіб отримання сполуки загальної формули (І) або її солі 1 UA 101835 C2 COOH (І) X R 5 10 15 20 25 30 35 40 45 де Х - атом галогену, переважно флуор; R - одна або більше з груп, незалежно вибраних з нижченаведеного: - атоми галогену, переважно хлор; - СF3; - СН=СН2; - СN; - СН2ОН; - NО2; - метилендіокси; - етилендіокси; - циклоалкіл, переважно С3-С6 циклоалкіл; - феніл; - ОR1 або NНСОR1 де R1 вибрано з групи: СF3, алкеніл, алкініл; бензил; та феніл; - SR2, SОR2 або СОR2 де R2 – алкіл; вказаний спосіб має нижченаведені етапи згідно зі схемою 1: (і) реагування сполуки формули (ІІ), де Х визначено вище, та Х" – хлор, бром, йод або трифлат (СF3SО3) зі сполукою формули (ІІІ), де R визначено вище, з утворенням сполуки формули (ІV); (іі) піддавання сполуки формули (ІV) бромуванню радикалу з утворенням сполуки формули (V); ііі) перетворення сполуки формули (V) у відповідне нітрил-похідне формули (VІ); іv) реагування сполуки формули (VІ) з 1,2-диброметаном з утворенням сполуки формули (VІІ); та v) гідроліз сполук формули (VІІ) з утворенням сполуки формули (І). Переважно, бромування радикалу проводять з N-бромсукцинимідом (NВS) при наявності каталітичної кількості бензоїлпероксиду [РhСОО)2] та ацетонітрилу як розчиннику. Винахід також стосується сполуки (VІІ), котру отримано як стабільний інтермедіат реакції, описаної вище. Винахід крім того стосується способу отримання фармацевтичної композиції, вказаний спосіб має етапи (і) – (v) та додатковий етап (vі), що полягає у змішуванні одного або більше фармацевтично прийнятних наповнювачів. Терміни в описі мають нижченаведені значення: "Атоми галогену" охоплюють флуор, хлор, бром, та йод. "Алкіл" означає С1-С4 алкіл з нерозгалуженим або розгалуженим ланцюгом, як-то метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, "Алкеніл" означає С2-С6 алкеніл з нерозгалуженим або розгалуженим ланцюгом, як-то вініл, 1-пропеніл, 2-пропеніл, 1-бутеніл, ізобутеніл, або нерозгалужений-або розгалужений-пентеніл та гексеніл. Термін "алкініл" застосовувано аналогічно. "Циклоалкіл" означає циклічну неароматичну вуглеводневу групу, що містить 3-8 атомів карбону. Приклади охоплюють циклопропіл, циклобутил, циклопентил, циклогексил та циклогептил. "Насичена гетероциклічна" означає насичену гетероциклічну групу, що має принаймні 4 атоми карбону та принаймні один гетероатом, переважно один – чотири гетероатоми, вибрані з нітрогену, оксигену та сульфуру. Приклади охоплюють піперидил або тетрагідрофурил. Цей винахід стосується способу отримання сполуки загальної формули (І) згідно зі схемою 1 2 UA 101835 C2 COOH (І) X 5 10 R де Х та R визначені вище. Коли R – циклоалкіл, вказане кільце є необов'язково заміщеним одною або більше групами, незалежно вибраними з нижченаведеного: алкіл, СF3, ОН та оксогрупа. Переважно циклоалкілом є С3-С6 циклоалкіл. Коли R – феніл, вказане кільце є необов'язково заміщеним одною або більше групами, незалежно вибраними з нижченаведеного: атоми галогену, СF 3, ОСF3, ОН, алкіл та насичений гетероцикл. Насичена гетероциклічна група є переважно моноциклічним кільцем, що має 5 або 6 атомів та один або два атоми нітрогену або один атом нітрогену та один атом оксигену, як-то піролідин, імідазолідин та ізоксазолідин. СХЕМА 1 15 20 25 30 35 На першому етапі (етап і) сполука, що має формулу (ІІ), де Х – атом галогену, переважно флуор, а Х" вибрано з групи: хлор, бром, йод та СF 3SО3 (трифлат), реагує з фенілбороновою кислотою формули (ІІІ), де R – одна або більше груп, незалежно вибраних з нижченаведеного: атоми галогену, переважно хлор; СF3; СН=СН2; СN; СН2ОН; NО2; метилендіокси; етилендіокси; циклоалкіл; феніл; ОR1 або NНСОR1, де R1 вибрано з групи: СF3, алкеніл, алкініл; бензил; феніл; SR2, SОR2 та СОR2, де R2 – алкіл. Сполуки формули (ІІ) та (ІІІ) є комерційно доступними або їх можна отримувати способами, добре відомими спеціалісту. Переважно реакцію, відому як реакція Сузукі або реакція Міяура-Сузукі, проводять, застосовуючи 4-бром-3-флуор-толуєн як сполуку формули (ІІ) та 3,4-дихлор-фенілборонову кислоту як сполуку формули (ІІІ). Вказану реакцію, що відбувається на паладієвому каталізаторі, можна також проводити з алкілбороновими естерами замість боронових кислот. Переважно, будь-який паладієвий каталізатор, як-то тетракіс(трифенілфосфін)паладій [Рd(РРh)3], паладій на активованому вугіллі, також відомий, як паладій на вугіллі (Рd на С), паладій на алюмінію оксиді, можна застосовувати, як каталізатор. Переважно Рd на С застосовують, оскільки він є менш дорогим та легшим для поводження. Загалом, етап (і) проводять при наявності органічного розчиннику. Органічні розчинники, що можна переважно застосовувати, охоплюють етанол, ацетон, тетрагідрофуран (ТГФ), ізопропанол, N-метилпіролідон (NМП), діоксан та їх суміші з водою. Комбінацію органічних розчинників можна застосовувати також. 3 UA 101835 C2 5 10 15 20 25 30 35 40 45 50 55 60 Переважно, реакцію проводять при температурі кипіння розчиннику. Коли застосовують Рd(РРh)3, кращим розчинником є суміш діоксан/вода 2:1 за об'ємом, тоді як, коли застосовують Рd/С, кращим розчинником є етанол. Переважно, етап (і) проводять при наявності основи. Основи, що можна переважно застосовувати охоплюють Nа2СО3, К2СО3, К3РО4, Сs2СО3, NаОН, та КОН. Кращою основою є Nа2СО3. Необов'язково адитиви, як-то трифенілфосфін (Р(Рh3)), поліметилгідросилоксан (РМНS), тетрабутиламонію бромід (ТВАВ), 1,4-діазабіцикло[2,2,2]октан (DАВСО), або NаІ, можна додавати до реакційного середовища. Переважно, етап (і) проводять з невеликим молярним надлишком сполуки (ІІІ) відносно сполуки (ІІ). Кращі умови для проведення реакції з етапу (і) є повідомленими, як нижченаведені: - розчинник: 20 об'ємів етанолу; - основа: 2 еквіваленти Nа2СО3; - каталізатор: 13 мас% Рd на С 10 %. - температура: при кипінні під зворотним холодильником. Звичайно, сполуку формули (ІV) отримують з виходом вище, ніж 70 %, переважно вище, ніж 80 %. Сполукою формули (ІV) є переважно 3’,4’-дихлор-2-флуор-4-метил-біфеніл. На другому етапі (етап іі), сполуку формули (ІV) піддають бромуванню радикалу з утворенням сполуки формули (V), де Х та R визначені вище. Сполука (ІV) може бути, як сирий продукт або може бути заздалегідь кристалізованою стандартними способами. Переважно бромування радикалу проводять з N-бромсукцинимідом (NВS) при наявності каталітичної кількості бензоїлпероксиду [РhСОО)2] та ацетонітрилу, як розчиннику. Загалом, реакцію проводять при температурі кипіння розчиннику. Переважно, для мінімізації утворення дибромованого продукту, етап (іі) проводять з невеликим надлишком NВS, переважно 1,05 моль відносно 1 моль сполуки (ІV), та при наявності 0,04 еквівалента РhСООО2. Загалом сполуку формули (V), котрою є переважно 3",4’-дихлор-2-флуор-4-бромметилбіфеніл, отримують з виходом вище, ніж 85 %, переважно вище, ніж 90 %. Необов'язково, сполуку формули (V) можна крім того очищати кристалізацією стандартними способами. На третьому етапі (етап ііі) сполуку формули (V) перетворюють у відповідне нітрил-похідне формули (VІ), де Х та R визначені вище. Натрію ціанід або інші придатні солі можна застосовувати. Переважно етап (ііі) проводять в органічному розчиннику, як-то етанол або ацетонітрил, переважно етанол. Температура на етапі (ііі) є переважно приблизно від 20 °C до 60 °C, більш переважно між приблизно 40 °C та приблизно 50 °C. Переважно, етап (ііі) проводять з молярним надлишком натрію ціаніду. Переважно між 1,2 моль та 1,0 моль натрію ціаніду, та переважно застосовують 1,05 моль – 1 моль сполуки (V). Загалом сполуку формули (VІ), котрою є переважно 3’,4’-дихлор-2-флуор-4-ціанометилбіфеніл, отримують з виходом вище, ніж 50 %, переважно приблизно 55-60 %. Необов'язково, вказану сполуку можна крім того очищати кристалізацією стандартними способами, переважно суспендуванням в етанолі. На четвертому етапі (іv), сполука формули (VІ) реагує з 1,2-диброметаном з утворенням сполуки формули (VІІ), де Х та R визначені вище. Переважно етап (іv) проводять в органічному розчиннику, як-то етанол або ацетонітрил або їх суміші з водою. Переважно вказаний етап циклопропанування проводять, як реакцією з каталізом фазопереносом при наявності 30 % NаОН та тетрабутиламонію хлориду (ТВАС) або тетрабутиламонію броміду (ТВАВ). Температура на етапі (іv) є переважно приблизно від 20 °C до 50 °C. Загалом сполуку формули (VІІ), котрою є переважно 1-(3’,4’-дихлор-2-флуор[1,1’-біфеніл]-4іл)-циклопропаннітрил, отримують з виходом вище, ніж 60 %, переважно приблизно 65-70 %. Необов'язково, вказану сполуку можна крім того очищати кристалізацією стандартними способами, переважно, застосовуючи н-гептан, як кристалізаційний розчинник. На п'ятому етапі (етап v), сполуку формули (VІІ) гідролізують для отримання потрібної сполуки формули (І) способами, добре відомими спеціалісту. 4 UA 101835 C2 5 10 15 Переважно гідроліз проводять у суміші метанолу та води при наявності сильної основи, переважно КОН при кипінні під зворотним холодильником. Загалом сполуку формули (І), котрою є переважно 1-(3’,4’-дихлор-2-флуор[1,1’-біфеніл]-4іл)-циклопропанкарбонова кислота, отримують з виходом вище, ніж 65 %. Сполуку формули (І) можна промивати, фільтрувати та виділяти різними способами, відомими у рівні техніки. Вказану сполуку можна крім того очищати кристалізацією стандартними способами та отримувати з високою хімічною чистотою, наприклад, вище, ніж 95 %, без застосування кінцевої очистки хроматографією. Кристалізація з суміші н-гептану та ізопропанолу є особливо кращою. Загальний вихід є звичайно принаймні 20 %, переважно рівним або вище, ніж 25 %, більш переважно вище, ніж 30 %. У кращому втіленні винахід стосується способу отримання сполуки формули (І), де Х – флуор та R – хлор. У ще кращому втіленні винахід стосується способу отримання 1-(3’,4’-дихлор-2-флуор[1,1’біфеніл]-4-іл)-циклопропан-карбонової кислоти, що має формулу (Іа) COOH (Іа) F Cl Cl 20 25 30 35 40 45 50 Отриману сполуку (І) можна також перетворювати у відповідні фармацевтично прийнятні солі різними способами, відомими у рівні техніки. Фармацевтично прийнятні солі охоплюють солі, у котрих кислотна функціональна група реагує з прийнятною основою з утворенням, наприклад, солей натрію, калію, кальцію, магнію та амонію. Сполуки формули (І), отримані способом винаходу, можна застосовувати при отриманні фармацевтичних композицій для лікування та/або відвернення нейродегенеративної хвороби, як-то хвороба Альцгеймера. Вказані фармацевтичні композиції, переважно для перорального застосування, містять принаймні одну сполуку формули (І) у суміші із фармацевтично прийнятними наповнювачами та/або носіями, наприклад, описаними у Rеmіngtоn's Рhаrmасеutісаl Sсіеnсеs Наndbооk, ХVІІ Еd., Масk Рub., N.Y., U.S.А. Винахід ілюстровано детальніше нижченаведеними прикладами. Приклад 1 Отримання 3’,4’-дихлор-2-флуор-4-метил-біфенілу 3-Флуор-4-бромтолуєн (50 г, 0,265 моль) та 3,4-дихлорфенілборонову кислоту (53 г, 0,278 моль) розчиняють в етанолі (970 мл) та додають натрію карбонат (56,1 г, 0,529 моль). Паладій 10 % на вугіллі (6,6 г) додають, та суміш гріють при кипінні під зворотним холодильником протягом 4 годин під азотом. Реакційну суміш охолоджують, фільтрують та концентрують, додають ізопропілацетат (250 мл), та тоді розчин концентрують знов. Залишок розчиняють в ізопропілацетаті (250 мл) та 1М натрію гідроксиді (250 мл). Органічну фазу відокремлюють, промивають водою (125 мл), нейтралізують гідрогенхлорид 3 М, промивають розсолом (250 мл) та концентрують. Залишок додають з сумішшю ацетонітрил/вода 1/1 за об'ємом (150 мл), гріють до 40ºС до розчинення та тоді охолоджують до 0-5ºС, та перемішують протягом 30 хвил при цій температурі. Сполука 3’,4’-дихлор-2-флуор-4-метил-біфеніл кристалізується, як порошок, що фільтрують, промивають сумішшю ацетонітрил/вода 1/1 за об'ємом (25 мл) та сушать при 40ºС (56 г, 86 % виходу). ВЕРХ-УФ-чистота (210 нм): 95,0 % 1 Н ЯМР (ДМСО-d6, 300 МГц): 7,73 (m, 2Н); 7,49 (m, 2Н); 7,14 (m, 2Н); 2,36 (s, 3Н) Приклад 2 Отримання 3’,4’-дихлор-2-флуор-4-бромметил-біфенілу 3",4’-Дихлор-2-флуор-4-метил-біфеніл (29 г, 0,114 моль), N-бромсукцинимід (21,2 г, 0,119 моль), бензоїлпероксид (1,4 г, 0,004 моль) розчиняють в ацетонітрилі (190 мл). Суміш гріють при кипінні під зворотним холодильником протягом 3 годин, тоді охолоджують, 5 UA 101835 C2 5 10 15 20 25 30 35 40 45 50 55 60 додають у розчин натрію сульфіту (2,2 г) у воді (54 мл), перемішують протягом 30 хвил та тоді залишають фази розділятися. Нижчу водну фазу відокремлюють та екстрагують дихлорметаном (29 мл). Вищу фазу концентрують під вакуумом, додають у воду (10 мл) та дихлорметан (58 мл) та перемішують. Органічні фази відокремлюють та комбінують, промивають двічі водою (29 мл), та концентрують під вакуумом. Сполуку 3’,4’-дихлор-2-флуор-4-бромметил-біфеніл виділяють, як оранжеве масло (35,7 г, 94 % виходу). ВЕРХ-УФ-чистота (250 нм): 77,1 % 1 Н ЯМР (ДМСО-d6, 300 МГц): 7,87-7,12 (m, 6Н); 4,76 (s, 2Н) Приклад 3 Отримання 3’,4’-дихлор-2-флуор-4-ціанометил-біфенілу 3",4’-Дихлор-2-флуор-4-бромметил-біфеніл (35,0 г, 0,105 моль) та натрію ціанід (5,4 г, 0,110 моль) розчиняють у суміші етанолу (228 мл) та води (25 мл), тоді гріють при 50ºС протягом 3 годин. Розчин концентрують під вакуумом та залишок суспендують в етанолі/воді 1/1 за об'ємом (35 мл) та охолоджують при 0-5ºС протягом 30 хвил. Отриманий твердий матеріал фільтрують та сушать при 40ºС під вакуумом. Сирий продукт суспендують в етанолі (56 мл) при 20-25ºС протягом 30 хвил, фільтрують та сушать при 40ºС під вакуумом. Сполуку 3’,4’-дихлор-2-флуор-4-ціанометил-біфеніл отримують, як світло-коричневий порошок (16,8 г, 57 % виходу). ВЕРХ-УФ-чистота (250 нм): 92,3 %. 1 Н ЯМР (ДМСО-d6, 300 МГц): 7,78 (m, 2Н); 7,60 (m, 2Н); 7,34 (m, 2Н); 4,14 (s, 1Н). Приклад 4 Отримання 1-(3’,4’-дихлор-2-флуор[1,1’-біфеніл]-4-іл)-циклопропан-нітрилу 3’,4’-Дихлор-2-флуор-4-ціанометил-біфеніл (9,0 г, 0,032 моль), 1,2-дибромметан (9,0 г, 0,048 моль), тетрабутиламонію хлорид (1,2 г, 0,043 моль), толуєн (60 мл) та воду (9 мл) завантажують у реактор. Натрію гідроксид 30 % водн. (60 г, 0,45 моль) додають краплями протягом 30 хвил при 2025ºС та реакційну суміш перемішують протягом 6 годин. Органічну фазу відокремлюють, та промивають послідовно водою (12 мл), гідрогенхлоридом 3 М водн. (36 мл) та зрештою водою (12 мл). Розчин концентрують, тоді н-гептан (18 мл) додають при 80ºС. Розчин охолоджують до 0-5ºС та перемішують протягом 30 хвил. Продукт, кристалізований з розчину, фільтрують, промивають холодним н-гептаном (5 мл) та сушать при 40ºС під вакуумом. Сполуку 1-(3’,4’-дихлор-2-флуор[1,1’-біфеніл]-4-іл)-циклопропаннітрил отримують, як жовтий порошок (6,4 г, 65 % виходу). ВЕРХ-УФ-чистота (250 нм): 98,2 %. 1 Н ЯМР (ДМСО-d6, 300 МГц): 7,78 (m, 2Н); 7,60 (m, 2Н); 7,30 (m, 2Н); 1,84 (m, 2Н); 1,63 (m, 2Н). Приклад 5 Отримання 1-(3’,4’-дихлор-2-флуор[1,1’-біфеніл]-4-іл)-циклопропан-карбонової кислоти 1-(3’,4’-Дихлор-2-флуор[1,1’-біфеніл]-4-іл)-циклопропаннітрил (14,3 г, 0,047 моль) розчиняють у суміші метанолу (143 мл) та води (71,5 мл), додають порціями калію гідроксид (35,1 г, 0,563 моль), та суміш гріють при кипінні під зворотним холодильником протягом 48 годин. Реакційну суміш охолоджують та виливають у розчин водного гідрогенхлориду 36 % (57 мл) у воді (57 мл) при 20-25ºС. Суспензію перемішують та фільтрують; твердий матеріал неодноразово промивають водою та сушать при 40ºС під вакуумом. Сирий продукт розчиняють у киплячому 2-пропанолі (178 мл), у розчин додають активоване вугілля (0,3 г), перемішують при кипінні під зворотним холодильником та фільтрують, концентрують та додають н-гептан (116 мл). Гарячий розчин охолоджують до 0-5ºС та кристалізований твердий матеріал фільтрують, промивають 2-пропанолом та сушать при 40ºС під вакуумом. Сполуку 1-(3’,4’-дихлор-2-флуор[1,1’-біфеніл]-4-іл)-циклопропанкарбонову кислоту отримують, як білий порошок (10,3 г, 68 % виходу). ВЕРХ-УФ-чистота (255 нм): 99,8 % 1 Н ЯМР (ДМСО-d6, 300 МГц): 12,51 (bs, 1Н); 7,78 (m, 2Н); 7,54 (m, 2Н); 7,30 (m, 2Н); 1,48 (m, 2Н); 1,22 (m, 2Н). МС (ІЕР , 40 V): 323 (М ); 279. 6 UA 101835 C2 Межі плавлення: 199-200ºС. ФОРМУЛА ВИНАХОДУ 5 1. Спосіб отримання сполуки загальної формули (І) COOH X R 10 , (І) де X - флуор; R - один або більше атомів галогену, вказаний спосіб включає нижченаведені стадії, за якими: (і) сполуку формули (II) X' X , (II) де X визначено вище, X' вибрано з групи: хлор, бром, йод або трифлат (CF3SO2), піддають реагуванню зі сполукою формули (III) OH B 15 OH R , (IIІ) де R визначено вище, з утворенням сполуки формули (IV) X R ; (IV) (іі) сполуку формули (IV) піддають радикальному бромуванню з утворенням сполуки формули (V) Br X 20 R ; (V) ііі) сполуку формули (V) перетворюють у відповідну нітрильну похідну формули (VI) 7 UA 101835 C2 CN X R ; (VI) iv) сполуку формули (VI) піддають реагуванню з 1,2-дибромметаном з утворенням сполуки формули (VII) CN X R 5 10 15 20 25 ; (VII) v) сполуку формули (VII) гідролізують з утворенням сполуки формули (І). 2. Спосіб за п. 1, що додатково включає стадії виділення та кристалізації сполуки формули (І). 3. Спосіб за п. 2, де кристалізацію проводять із застосуванням суміші н-гептану та ізопропанолу. 4. Спосіб за будь-яким з пп. 1-3, де етап (і) проводять при наявності паладієвого каталізатора, вибраного з групи, що складається з: тетракис(трифенілфосфін)паладію, паладію на активованому вугіллі та паладію на алюмінію оксиді. 5. Спосіб за п. 4, де паладієвим каталізатором є паладій на активованому вугіллі. 6. Спосіб за будь-яким з попередніх пунктів, де стадію (іі) проводять з N-бромсукцинімідом при наявності каталітичної кількості бензоїлпероксиду, застосовуючи ацетонітрил як розчинник. 7. Спосіб за п. 1, де атомом галогену є хлор. 8. Спосіб за п. 7, де сполукою формули (І) є 1-(3',4'-дихлор-2-флуор[1,1'-біфеніл]-4іл)циклопропанкарбонова кислота. 9. Спосіб за п. 8, що включає нижченаведені стадії, за якими: (і) 4-бром-3-флуортолуєн піддають реагуванню з 3,4-дихлорфенілбороновою кислотою з утворенням 3',4'-дихлор-2-флуор-4-метилбіфенілу; (іі) 3',4'-дихлор-2-флуор-4-метилбіфеніл піддають радикальному бромуванню з утворенням 3',4'дихлор-2-флуор-4-бромметилбіфенілу; ііі) 3',4'-дихлор-2-флуор-4-бромметилбіфеніл перетворюють у відповідний 3',4'-дихлор-2-флуор4-ціанометилбіфеніл; iv) 3',4'-дихлор-2-флуор-4-ціанометилбіфеніл піддають реагуванню з 1,2-диброметаном з утворенням 1-(3',4'-дихлор-2-флуор[1,1'-біфеніл]-4-іл)циклопропаннітрилу; v) 1-(3',4'-дихлор-2-флуор[1,1'-біфеніл]-4-іл)циклопропаннітрил гідролізують з утворенням 1(3',4'-дихлор-2-флуор[1,1'-біфеніл]-4-іл)циклопропанкарбонової кислоти. 10. Спосіб отримання фармацевтичної композиції, що включає стадії (і)-(v) за п. 1 та додаткову стадію (vi), за якою додають один або більше фармацевтично прийнятних наповнювачів. 30 Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 8
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess of preparing derivatives of 1-(2-halobiphenyl-4-yl)-cyclopropanecarboxylic acid
Автори англійськоюFolleas, Benoit, Botte, Hubert, Delacroix, Thomas, Pivetti, Fausto
Назва патенту російськоюСпособ получения производных 1-(2-галогенбифенил-4-ил)-циклопропанкарбоновой кислоты
Автори російськоюФоллеас Бенои, Ботте Губерт, Делакруа Томас, Пиветти Фаусто
МПК / Мітки
МПК: C07C 17/26, C07C 255/35, C07C 51/09, C07C 25/00, C07C 57/46, C07C 253/14, C07C 17/14
Мітки: кислоти, 1-(2-галогенбіфеніл-4-іл)-циклопропанкарбонової, спосіб, отримання, похідних
Код посилання
<a href="https://ua.patents.su/10-101835-sposib-otrimannya-pokhidnikh-1-2-galogenbifenil-4-il-ciklopropankarbonovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання похідних 1-(2-галогенбіфеніл-4-іл)-циклопропанкарбонової кислоти</a>
Попередній патент: Детермінативна сегментація, повторна сегментація і доповнення в блоках (sdu) даних служби підрівня керування (rlc) лінією радіозв’язку
Наступний патент: Сполука 3-фенілпіразол[5,1-b]тіазолу
Випадковий патент: Маятниковий гаситель поперечних коливань












