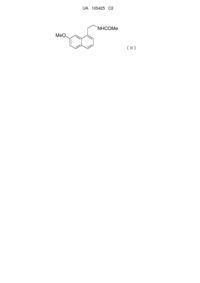
Кристалічна форма агомелатину гідрохлориду гідрату і спосіб її отримання
Номер патенту: 105425
Опубліковано: 12.05.2014
Автори: Йу Ксіонг, Шан Ханбін, Жу Ксуеян, Жанг Пенг, Пан Хонгджуан, Йуан Жедонг
Формула / Реферат
1. Кристалічна форма агомелатину гідрохлориду гідрату формули І:
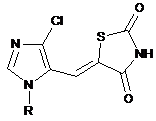 , (І)
, (І)
де X являє собою Сl,
яка характеризується наступними показниками кута Брегга 2θ, міжплощинного інтервалу d і відносної інтенсивності (І %):
2-Тета
d (Å)
Відносна інтенсивність (І %)
9,076
9,7360
11,24
13,635
6,4887
27,62
14,427
6,1345
16,38
16,872
5,2507
34,17
18,176
4,8767
100,00
21,610
4,1089
62,25
22,259
3,9905
7,94
22,794
3,8981
19,22
23,878
3,7235
31,32
24,214
3,6726
82,40
25,457
3,4960
41,45
25,714
3,4617
37,06
27,430
3,2488
31,69
29,207
3,0551
13,75
і в якій пік кутів дифракції кристалів знаходиться в межах похибки, яка становить ±0,2°.
2. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату, вказаної у п. 1, який відрізняється тим, що агомелатин піддають взаємодії з водним розчином НСl для одержання агомелатину гідрохлориду гідрату.
3. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 2, який відрізняється тим, що агомелатин піддають взаємодії з НСl у водному органічному розчиннику для одержання агомелатину гідрохлориду гідрату.
4. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 3, який відрізняється тим, що агомелатин розчиняють в органічних розчинниках перед додаванням водного розчину НСl для осадження кристала продукту.
5. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 4, який відрізняється тим, що вказаний водний розчин НСl додають краплями.
6. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 3, який відрізняється тим, що агомелатин додають у водний органічний розчинник, що містить НСl, для осадження кристала продукту.
7. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 4 або 6, який відрізняється тим, що додатково здійснюють промивання і висушування твердої речовини після кристалізації.
8. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 4 або 6, який відрізняється тим, що температуру реакції підтримують 0-20 °C.
9. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 4 або 6, який відрізняється тим, що вказаний органічний розчинник є етилацетатом, метилацетатом, n-бутилацетатом, ацетоном або ацетонітрилом.
10. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 9, який відрізняється тим, що вказаний органічний розчинник є етилацетатом.
11. Фармацевтична композиція, що містить кристалічну форму агомелатину гідрохлориду гідрату, вказану у п. 1, в поєднанні з фармацевтично прийнятними допоміжними речовинами або наповнювачами.
12. Застосування кристалічної форми агомелатину гідрохлориду гідрату, вказаної у п. 1, для лікування розладів мелатонінергічної системи, розладів сну, стресу, тривоги, сезонних афективних розладів, значної депресії, серцево-судинних захворювань, захворювань травної системи, безсоння і втоми, викликаних порушенням добового ритму організму через зміну часових поясів, шизофренії, фобії або депресивних розладів.
Текст
Реферат: Даний винахід стосується агомелатину гідрохлориду гідрату формули І, його приготування і застосування, а також фармацевтичної композиції, що його містить. Агомелатину гідрохлориду гідрат, одержаний за допомогою даного способу, має значно підвищену розчинність у порівнянні з агомелатином і тому більше придатний для виготовлення фармацевтичних лікарських засобів. Крім того, продукт має більш високу стабільністю і чистоту. Використовуючи даний спосіб, продукт високої чистоти може бути одержаний за допомогою простого процесу, без будь-яких складних кроків NHCOMe MeO .HX.H2O , (І) де X являє собою Сl. UA 105425 C2 (12) UA 105425 C2 NHCOMe MeO (Ⅱ) UA 105425 C2 5 Галузь техніки Даний винахід стосується агомелатин гідрохлорид гідрату, його приготування і застосування, а також фармацевтичної композиції, що його містить. Рівень техніки Агомелатин, або N-[2-(7-метокси-1-нафтил)етил]ацетамід, має структуру формули II. Він є комерційно доступним під торговою назвою Валдоксан від французької компанії Серв'є як агоніст мелатоніну та антагоніст рецептора 5HT 2C. Це перший антидепресант мелатонінового типу, показаний для лікування депресії, покращення сну і сексуальної функції. NHCOMe MeO 10 15 20 25 30 35 40 45 50 (Ⅱ) З погляду на його фармацевтичне значення, важливо виробити його комплекс або сполуку з кращою чистотою, розчинністю та відтворюваністю. Сутність винаходу Об'єктом даного винаходу є надання агомелатин гідрохлорид гідрату, який забезпечує відмінну розчинність, стабільність і чистоту, що робить його придатним для використання у виробництві фармацевтичних лікарських засобів, які містять агомелатин. Коли дані винахідники намагалися очистити продукт агомелатину, ми несподівано виявили, що агомелатин може утворювати фізично і хімічно стабільний агомелатин гідрохлорид гідрат при змішуванні з хлористоводневою кислотою (HCl). Вищезгаданий агомелатин гідрохлорид гідрат придатний для виготовлення фармацевтичних лікарських засобів. При використанні інших звичайних неорганічних кислот (наприклад, сірчаної кислоти, фосфорної кислоти, перхлорної кислоти) або органічних кислот (наприклад, оцтової кислоти, щавлевої кислоти, винної кислоти, фумарової кислоти) виробляти гідрат було нелегко або були отримані гідрати з нестабільними фізичними і хімічними властивостями. Даний винахід надає агомелатин гідрохлорид гідрат з наступною структурою формули I: (I), де X являє собою Cl. Даний винахід також стосується способу приготування вищезгаданого агомелатин гідрохлорид гідрату, в якому агомелатин взаємодіє з HCl в будь-якій формі для одержання агомелатин гідрохлорид гідрату. Може бути два процеси: агомелатин може бути розчинений у водному органічному розчиннику перед тим, як HCl газ пропускають через нього, а осаджений кристал промивають і висушують, або агомелатин може бути доданим у розчин, що містить HCl, а потім осаджений кристал промивають і висушують. Результати повторних експериментів демонструють, що в першому способі надлишок HCl приводить тільки до зниження виходу, в той час як у другому способі легше контролювати кількість HCl у розчиннику. Таким чином, другий спосіб є переважнішим. Зокрема, агомелатин також може бути доданий до водного органічного розчинника перед тим, як додають краплями розчинник, що містить HCl, і осаджений кристал промивають і висушують. Альтернативно агомелатин розчиняють в органічному розчиннику перед тим, як додають краплями водний розчин HCl, і осаджений кристал промивають і висушують. Температура реакції в даному винаході може бути звичайною температурою для таких реакцій в даній галузі техніки до того часу, поки вона є нижчою ніж точка кипіння розчинника. Для підвищення виходу кращою є кімнатна температура або нижче, більш кращою є температура нижче кімнатної температури, і найкращою є температура 0-20°C. У вищезгаданому способі приготування вказаного агомелатин гідрохлорид гідрату органічний розчинник спеціально не обмежується, до того часу, поки він може розчиняти початкові матеріали агомелатину і HCl, і одночасно дозволяє вказаному агомелатин гідрохлорид гідрату бути осадженим. Придатний розчинник, що може бути використаним, включає етилацетат, метилацетат, n-бутилацетат, ацетон, ацетонітрил і т.п., і етилацетат є переважним. Органічні розчинники з більш високою полярністю, такі як спирти (етанол і метанол, та ін), ДМФ, ДМСО є менш бажаними. Даний винахід має перевагу в тому, що винахідники виявили, що серед великої кількості 1 UA 105425 C2 5 10 15 20 25 30 35 40 45 50 55 60 звичайних кислот агомелатин може реагувати з HCl з утворенням стабільного агомелатин гідрохлорид гідрату, фізичні властивості якого, такі як стабільність, розчинність і гігроскопічність, є кращими у порівнянні з продуктами агомелатину з будь-якою іншою звичайною кислотою. Цей процес також є менш складним, ніж при використанні іншої кислоти. Агомелатин гідрохлорид гідрат, виготовлений відповідно до цього способу, має суттєво підвищену розчинність у порівнянні з агомелатином per se і тому більше підходить для виготовлення фармацевтичних лікарських засобів. Продукт має більш високу стабільність, чистоту і розчинність. Крім того, продукт з високою чистотою можна одержати за допомогою простого процесу, без будь-яких складних кроків. Фармакологічні випробування агомелатин гідрохлорид гідрату продемонстрували, що він може бути застосований для лікування розладів мелатонінергічної системи, розладів сну, стресу, тривоги, сезонних афективних розладів, значної депресії, серцево-судинних захворювань, захворювань травної системи, безсоння і втоми, викликаних порушенням добового ритму організму через зміну часових поясів, шизофренії, фобії або депресивних розладів. Даний винахід додатково надає фармацевтичну композицію, що містить агомелатин гідрохлорид гідрат, згідно з винаходом, у поєднанні з фармацевтично прийнятними допоміжними речовинами або наповнювачами. Фармацевтична композиція може бути сформульована для різних шляхів введення, зокрема, для перорального введення або для ін'єкцій. Придатне дозування може бути скориговане в залежності від характеру і тяжкості захворювання, що підлягає лікуванню, способу введення, віку та маси пацієнта. Добова доза варіює від 0,1 мг до 1 г, і може бути введена як єдина доза або як декілька розділених доз. Короткий опис фігур Типові приклади даного винаходу проілюстровані фігурами для того, щоб краще передати об'єкти, характерні особливості та переваги даного винаходу. Фіг. 1 демонструє ТГА термограму продукту Прикладу 1 в даному винаході. Фіг. 2 демонструє зразок рентгенівської порошкової дифракції продукту Прикладу 7 в даному винаході. Приклади Приклад 1 1 г агомелатину додають до 20 мл EtOAc, 0,5 г водного розчину HCl (36%) додають о краплями при температурі 10 С. Суміш перемішують протягом 1 год, а потім фільтрують і тверду речовину двічі промивають 2 мл EtOAc, і висушують при температурі 40°С з одержанням 1 г білої твердої речовини (чистота: 99,9%; вихід: 81,7%). Елементний аналіз для Cl: Розраховано: Cl% (11,91 мас. %) Знайдено: Cl% (11,88% мас. %) Температура плавлення: 88-90°С Приклад 2 10 г агомелатину додають до 100 мл EtOAc, і 4,6 г водного розчину HCl (36%) додають краплями при температурі 10°C. Суміш перемішують протягом 1 год, а потім фільтрують і тверду речовину двічі промивають 10 мл EtOAc, і висушують при температурі 40°C з одержанням 10,2 г білої твердої речовини (чистота: 99,8%; вихід: 88,7%). Елементний аналіз для Cl: Розраховано: Cl% (11,91 мас. %) Знайдено: Cl% (11,86% мас. %) Температура плавлення: 88-90°С Приклад 3 1 г агомелатину розчиняють в 10 мл EtOAc при перемішуванні і додають краплями концентровану H2SO4 при кімнатній температурі. Протягом всього процесу тверда речовина не осаджується. Приклад 4 1 г агомелатину розчиняють в 10 мл EtOAc при перемішуванні і додають краплями концентровану H2SO4 при температурі -10°C. Протягом всього процесу тверда речовина не осаджується. Приклад 5 1 г агомелатину розчиняють в 10 мл EtOAc при перемішуванні і крижану оцтову кислоту додають краплями при температурі -10°C. Протягом всього процесу тверда речовина не осаджується. 2 UA 105425 C2 5 10 15 20 25 Приклад 6 1 г агомелатину розчиняють в 10 мл EtOAc при перемішуванні і фумарову кислоту додають краплями при температурі -10°C. Протягом всього процесу тверда речовина не осаджується. Приклад 7 100 г агомелатину додають до 1 л EtOAc і 50 г водного розчину HCl (36%) додають краплями при температурі 10°C. Суміш перемішують протягом 1 год, а потім фільтрують і тверду речовину двічі промивають 100 мл EtOAc, і висушують при температурі 40°C з одержанням 101 г білої твердої речовини (чистота: 99,7%; вихід: 82,5%). Елементний аналіз для Cl: Розраховано: Cl% (11,91 мас. %) Знайдено: Cl% (11,86 мас. %) Температура плавлення: 87-89°С Агомелатин, використаний у наведених вище прикладах, є комерційно доступним або може бути одержаним відповідно до способів, відомих в даній галузі техніки. Приклад 8: Фармацевтична композиція Рецептура для приготування 1000 капсул, кожна з яких містить дозу 25 мг (агомелатин) Сполука Прикладу 7 30,5 г Лактоза (Сферолак 100) 85,2 г Крохмаль 1500 25,5 г CMS-Na 8,5 г Ac-Di-Sol® (FMC) 17 г Стеаринова кислота 3,4 г Способи виявлення та результати 1. Чистота зразків Хроматографічні умови: колонка C18; мобільна фаза: 10 ммоль/л фосфатного буфера (доводять до рН 7,0 за допомогою NaOH): ацетонітрил=2:7 (об’єм/об’єм); температура колонки: 40°С; довжина хвилі виявлення: 220 нм, внутрішній стандартний спосіб використовують на продуктах з Прикладів 1 і 2. Розчини продуктів в концентрації 1 мг/мл одержують за допомогою мобільної фази. 10 мкл кожного розчину вводять в систему рідинного хроматографа та реєструють хроматограми. Результати чистоти продемонстровані в прикладах 1 і 2. 2. Тест на стабільність Деяку кількість продукту Прикладу 1 вміщують в інкубатор при температурі 40°C на 30 днів, щоб визначити його стабільність за допомогою ВЕРХ. Результати представлені у наступній таблиці 1. 30 Таблиця 1 Продукт Прикладу 1 AG·HCl·H2O День 0 99,6% День 5 99,5% День 10 99,5% День 30 99,5% AG = агомелатин C15H17NO2 35 3. Розчинність у воді Використовуючи спосіб зовнішнього стандарту, продукт Прикладу 1 тестують за допомогою ВЕРХ, порівнюють з агомелатином кристалічної форми II. Результати представлені в наступній таблиці 2: Таблиця 2 Зразок AG кристалічної форми II AG·HCl·H2O 40 У воді 0,26 0,30 Вміст агомелатину (мг/мл) У 0,1 Н HCl У буфері з рівнем pH 7,0 0,30 0,25 0,40 0,30 Як можна побачити, агомелатин гідрохлорид гідрат, згідно з цим винаходом, має кращу розчинність, ніж агомелатин per se у воді, у 0,1 Н HCl, який схожий на людський шлунковий сік, або у буфері з рівнем рН 7,0. Це означає, що перший має потенціал більш високої біодоступності, ніж останній. 4. Аналіз кристалізаційної води 3 UA 105425 C2 5 10 15 Розрахований вміст води в C15H17NO2·HCl·H2O дорівнює 6,06 мас. %. 4.1. Спосіб Фішера (Додаток VIII M, Китайська фармакопея, 2010) Продукт Прикладу 1 проаналізували згідно із зазначеним способом Фішера і виявили, що вміст води дорівнює 6,15 мас. %. Продукт Прикладу 7 проаналізували згідно із зазначеним способом Фішера і виявили, що вміст води дорівнює 6,10 мас %. 4.2. Термогравіметричний аналіз (Додаток VIII Q, Китайська фармакопея, 2010) Продукт Прикладу 1 проаналізували згідно із зазначеним способом ТГА і виявили, що втрати води дорівнювали 6,67 мас. %, тобто вміст кристалізаційної води у продукті становив 6,67 мас. %. Фіг. 1 демонструє ТГА-термограму. Умови вимірювання для способу ТГА є наступними: Тип інструмента: NETZSCH TG 209F1 Тип тиглю: Al2O3 Продувний газ: N2 20 мл/хв. Захисний газ: N2 10 мл/хв. Діапазон Кімнатна температур: температура ~300°С Швидкість нагріву: 10°С /хв. 5. Аналіз кристалічної структури Умови вимірювання для порошкової дифракції рентгенівських променів продукту Прикладу 7 даного винаходу є наступними: Параметри XRD (дифракції рентгенівських променів) Інструмент: Дифрактометр рентгенівських променів Bruker D8 ADVANCE Детектор: LynxEye детектор Рентгенівські промені: CuK 40 кВ/40 мА Режим сканування: Тета/Тета Монохроматор: Ni-фільтр Щілина розходження: 1 градус Приймальна щілина: 1,0 мм Сканування: Безперервне сканування від 3° до 45° з 0,02 °/крок Час сканування: 5 хв. Швидкість сканування: 8,0°/хв. Температура сканування: Кімнатна температура Зразок порошкової дифракції рентгенівських променів агомелатин гідрохлорид гідрату характеризується наступними показниками кута Брегга 2θ, міжплощинного інтервалу d і відносної інтенсивності (I%): 4 UA 105425 C2 Таблиця 3 2-Тета 9,076 13,635 14,427 16,872 18,176 21,610 22,259 22,794 23,878 24,214 25,457 25,714 27,430 29,207 5 10 15 d(Å) 9,7360 6,4887 6,1345 5,2507 4,8767 4,1089 3,9905 3,8981 3,7235 3,6726 3,4960 3,4617 3,2488 3,0551 I% 11,24 27,62 16,38 34,17 100,00 62,25 7,94 19,22 31,32 82,40 41,45 37,06 31,69 13,75 Коли кристал даного винаходу вимірюється за допомогою дифракції рентгенівських променів, можуть бути похибки вимірювання для зареєстрованих піків, іноді, через устаткування або через умови застосування. Зокрема, наприклад, значення 2θ іноді має похибку, що приблизно становить ±0,2, а іноді має похибку, що приблизно становить ±0,1, навіть якщо використовується дуже точне технічне обладнання. Таким чином, похибку вимірювання необхідно брати до уваги при визначенні структури кожного кристалу. 6. Тестування стабільності агомелатин гідрохлорид гідрату Спосіб тестування стабільності, який описаний в Китайській фармакопеї, використовували для цього тесту. 1. Тестування впливаючих факторів (у відкритому контейнері протягом 10 днів): висока температура (60°C), фотостабільность під впливом сильного світла (4500 лк), висока вологість (92,5% ВВ - відносної вологості - при температурі 25°C). 2. Прискорений тест (у закритому контейнері протягом 6 місяців): при температурі 40°C, вологість: 75% ВВ. 3. Довготривалий тест (у закритому контейнері протягом 9 місяців): при температурі 25°C, вологість: 60% ВВ. Результати представлені в наступній таблиці 4. 20 Таблиця 4 Зразок Висока температура Діючі фактори Сильне світло Висока вологість Прискорений тест Довготривалий тест 25 Вода (6,10%) Cl (11,86%) 1,00 5,95 6,03 6,02 6,00 1,75 11,48 11,63 11,65 11,53 Агомелатин гідрохлорид гідрат Прикладу 7 (початкова чистота: 99,72%) 99,51 99,67 99,73 99,64 99,74 Таким чином, за винятком того, що вміст води і вміст Cl агомелатин гідрохлорид гідрату зменшуються під впливом дуже суворих умов, агомелатин гідрохлорид гідрат є стабільним в інших умовах, зокрема, у прискореному тестуванні і довготривалому тестуванні, що є сприятливим для використання у фармацевтичних лікарських засобах. 5 UA 105425 C2 ФОРМУЛА ВИНАХОДУ 1. Кристалічна форма агомелатину гідрохлориду гідрату формули І: NHCOMe MeO .HX.H2O 5 , (І) де X являє собою Сl, яка характеризується наступними показниками кута Брегга 2θ, міжплощинного інтервалу d і відносної інтенсивності (І %): 2-Тета 9,076 13,635 14,427 16,872 18,176 21,610 22,259 22,794 23,878 24,214 25,457 25,714 27,430 29,207 10 15 20 25 30 d (Å) 9,7360 6,4887 6,1345 5,2507 4,8767 4,1089 3,9905 3,8981 3,7235 3,6726 3,4960 3,4617 3,2488 3,0551 Відносна інтенсивність (І %) 11,24 27,62 16,38 34,17 100,00 62,25 7,94 19,22 31,32 82,40 41,45 37,06 31,69 13,75 і в якій пік кутів дифракції кристалів знаходиться в межах похибки, яка становить ±0,2°. 2. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату, вказаної у п. 1, який відрізняється тим, що агомелатин піддають взаємодії з водним розчином НСl для одержання агомелатину гідрохлориду гідрату. 3. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 2, який відрізняється тим, що агомелатин піддають взаємодії з НСl у водному органічному розчиннику для одержання агомелатину гідрохлориду гідрату. 4. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 3, який відрізняється тим, що агомелатин розчиняють в органічних розчинниках перед додаванням водного розчину НСl для осадження кристала продукту. 5. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 4, який відрізняється тим, що вказаний водний розчин НСl додають краплями. 6. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 3, який відрізняється тим, що агомелатин додають у водний органічний розчинник, що містить НСl, для осадження кристала продукту. 7. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 4 або 6, який відрізняється тим, що додатково здійснюють промивання і висушування твердої речовини після кристалізації. 8. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 4 або 6, який відрізняється тим, що температуру реакції підтримують 0-20 °C. 9. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 4 або 6, який відрізняється тим, що вказаний органічний розчинник є етилацетатом, метилацетатом, nбутилацетатом, ацетоном або ацетонітрилом. 10. Спосіб отримання кристалічної форми агомелатину гідрохлориду гідрату за п. 9, який відрізняється тим, що вказаний органічний розчинник є етилацетатом. 6 UA 105425 C2 5 11. Фармацевтична композиція, що містить кристалічну форму агомелатину гідрохлориду гідрату, вказану у п. 1, в поєднанні з фармацевтично прийнятними допоміжними речовинами або наповнювачами. 12. Застосування кристалічної форми агомелатину гідрохлориду гідрату, вказаної у п. 1, для лікування розладів мелатонінергічної системи, розладів сну, стресу, тривоги, сезонних афективних розладів, значної депресії, серцево-судинних захворювань, захворювань травної системи, безсоння і втоми, викликаних порушенням добового ритму організму через зміну часових поясів, шизофренії, фобії або депресивних розладів. 7 UA 105425 C2 Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 8
ДивитисяДодаткова інформація
Назва патенту англійськоюAgomelatine hydrochloride hydrate and preparation thereof
Автори англійськоюShan, Hanbin, Yuan, Zhedong, Xhu, Xueyan, Zhang, Peng, Pan, Hongjuan, Yu, Xiong
Автори російськоюШан Ханбин, Йуан Жедонг, Жу Ксуеян, Жанг Пенг, Пан Хонгджуан, Йу Ксионг
МПК / Мітки
МПК: C07C 231/12, C07C 233/18, A61K 31/165, A61P 25/24
Мітки: кристалічна, форма, гідрохлориду, агомелатину, гідрату, отримання, спосіб
Код посилання
<a href="https://ua.patents.su/10-105425-kristalichna-forma-agomelatinu-gidrokhloridu-gidratu-i-sposib-otrimannya.html" target="_blank" rel="follow" title="База патентів України">Кристалічна форма агомелатину гідрохлориду гідрату і спосіб її отримання</a>
Попередній патент: Агомелатину гідроброміду гідрат і його отримання
Наступний патент: Спосіб безперервної термомеханічної обробки катанки
Випадковий патент: Композиція тривалого вивільнення і спосіб її одержання