Поліморфні форми фуразидину
Номер патенту: 115290
Опубліковано: 10.10.2017
Автори: Лукянова Ніна, Матіушенков Євгєній, Лієпінс Вілніс, Скоморохов Міхаіл, Ревюка Єкатеріна
Формула / Реферат
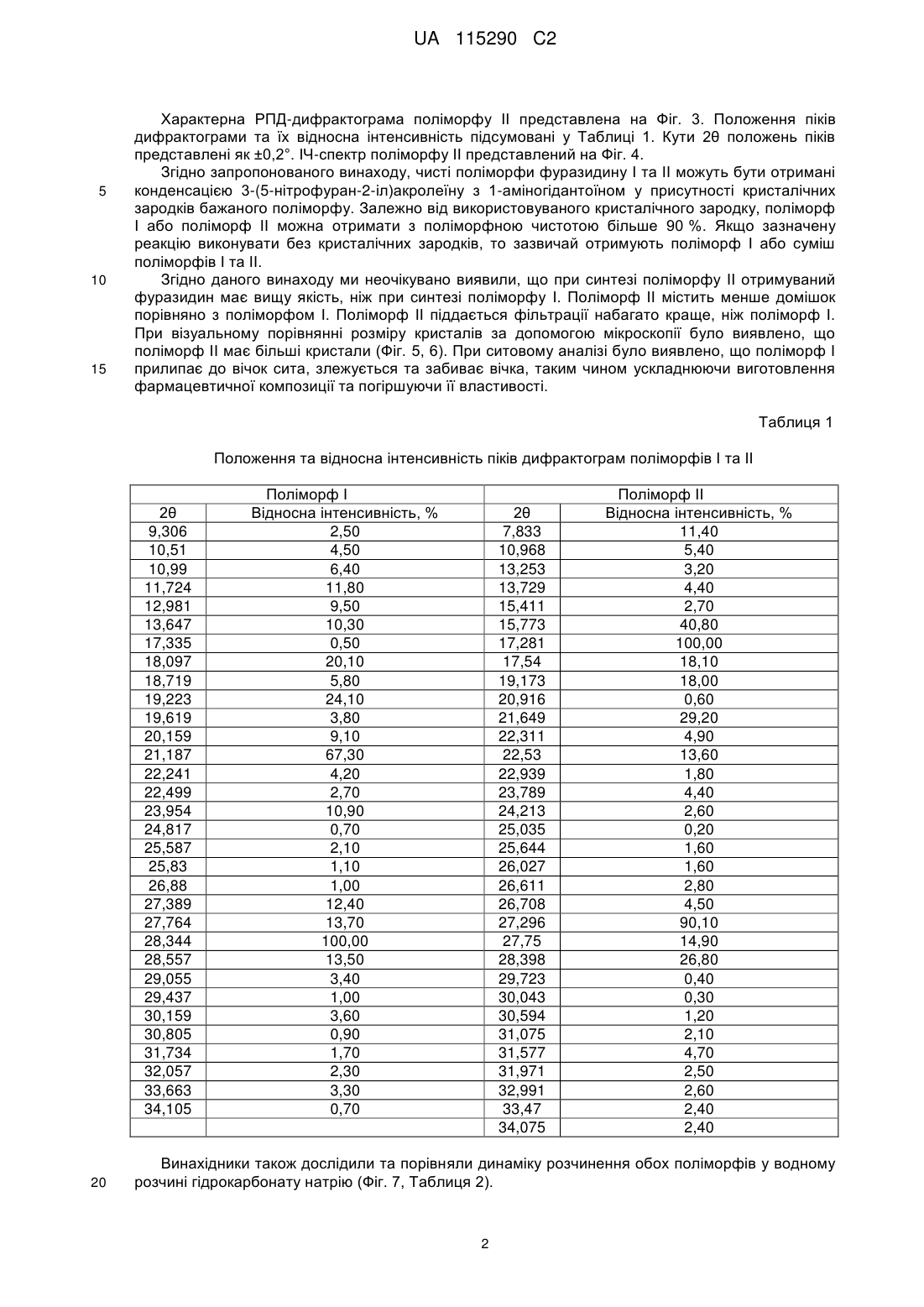
1. Кристалічна форма І фуразидину, яка відрізняється тим, що її РПД-дифрактограма має піки при кутах дифракції 2θ 10,5±0,2; 11,0±0,2; 11,7±0,2; 13,0±0,2; 13,7±0,2; 18,1±0,2; 18,7±0,2; 19,2±0,2; 20,2±0,2; 21,2±0,2; 22,2±0,2; 24,0±0,2; 27,4±0,2; 27,8±0,2; 28,3±0,2.
2. Кристалічна форма І фуразидину за п. 1, що характеризується РПД-дифрактограмою, як показано на Фіг. 1.
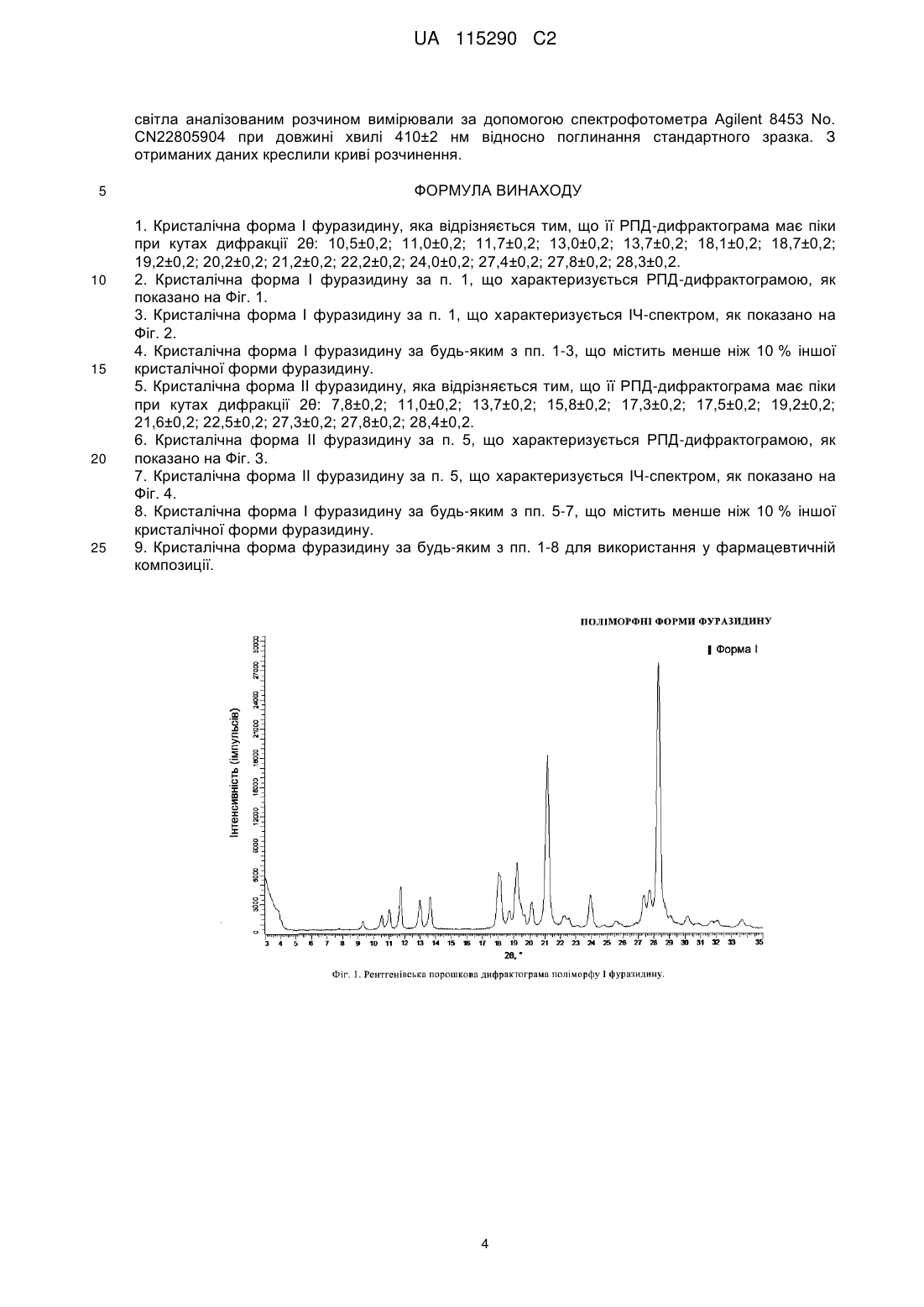
3. Кристалічна форма І фуразидину за п. 1, що характеризується ІЧ-спектром, як показано на Фіг. 2.
4. Кристалічна форма І фуразидину за будь-яким з пп. 1-3, що містить менше ніж 10 % іншої кристалічної форми фуразидину.
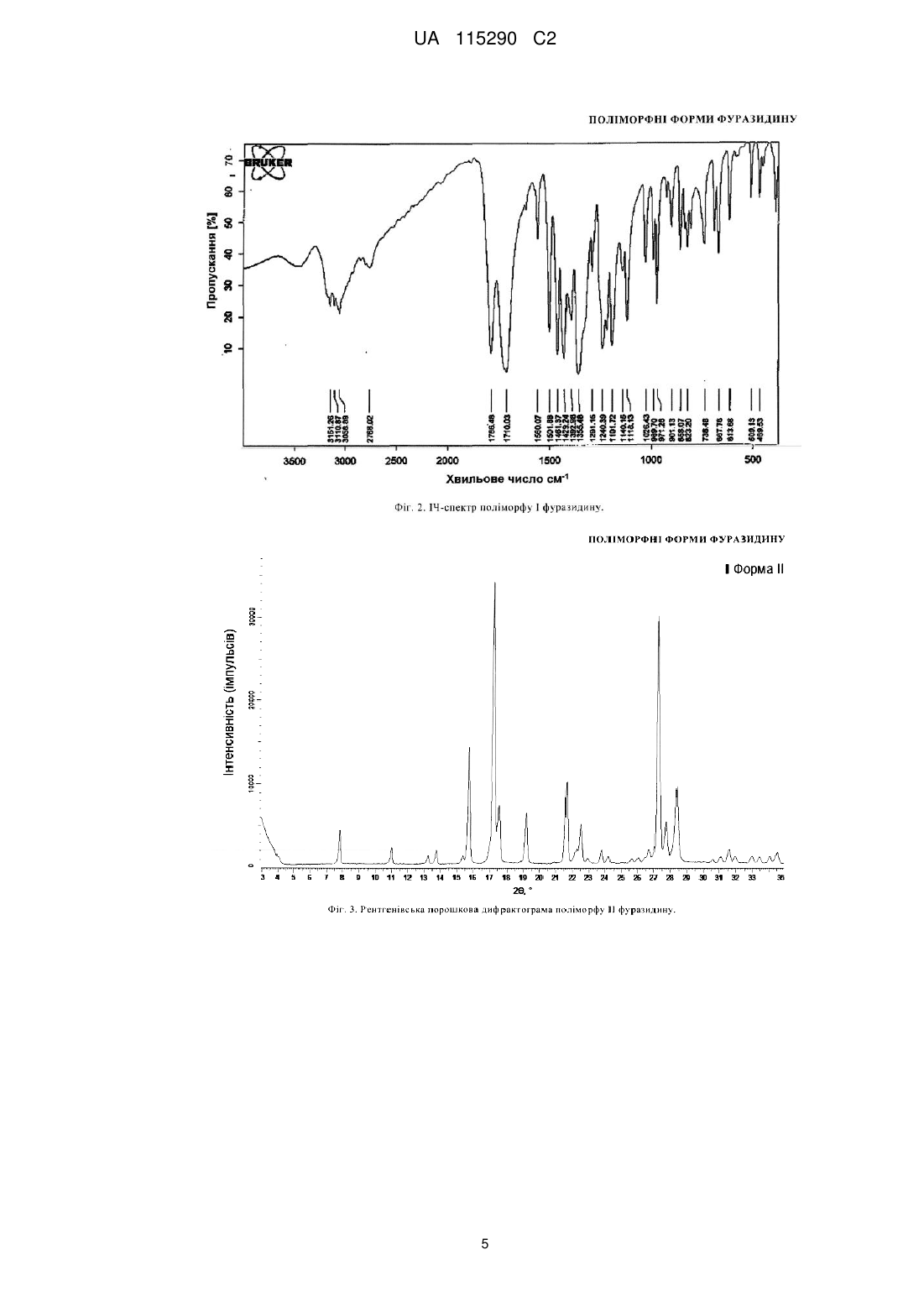
5. Кристалічна форма II фуразидину, яка відрізняється тим, що її РПД-дифрактограма має піки при кутах дифракції 2θ 7,8±0,2; 11,0±0,2; 13,7±0,2; 15,8±0,2; 17,3±0,2; 17,5±0,2; 19,2±0,2; 21,6±0,2; 22,5±0,2; 27,3±0,2; 27,8±0,2; 28,4±0,2.
6. Кристалічна форма II фуразидину за п. 5, що характеризується РПД-дифрактограмою, як показано на Фіг. 3.
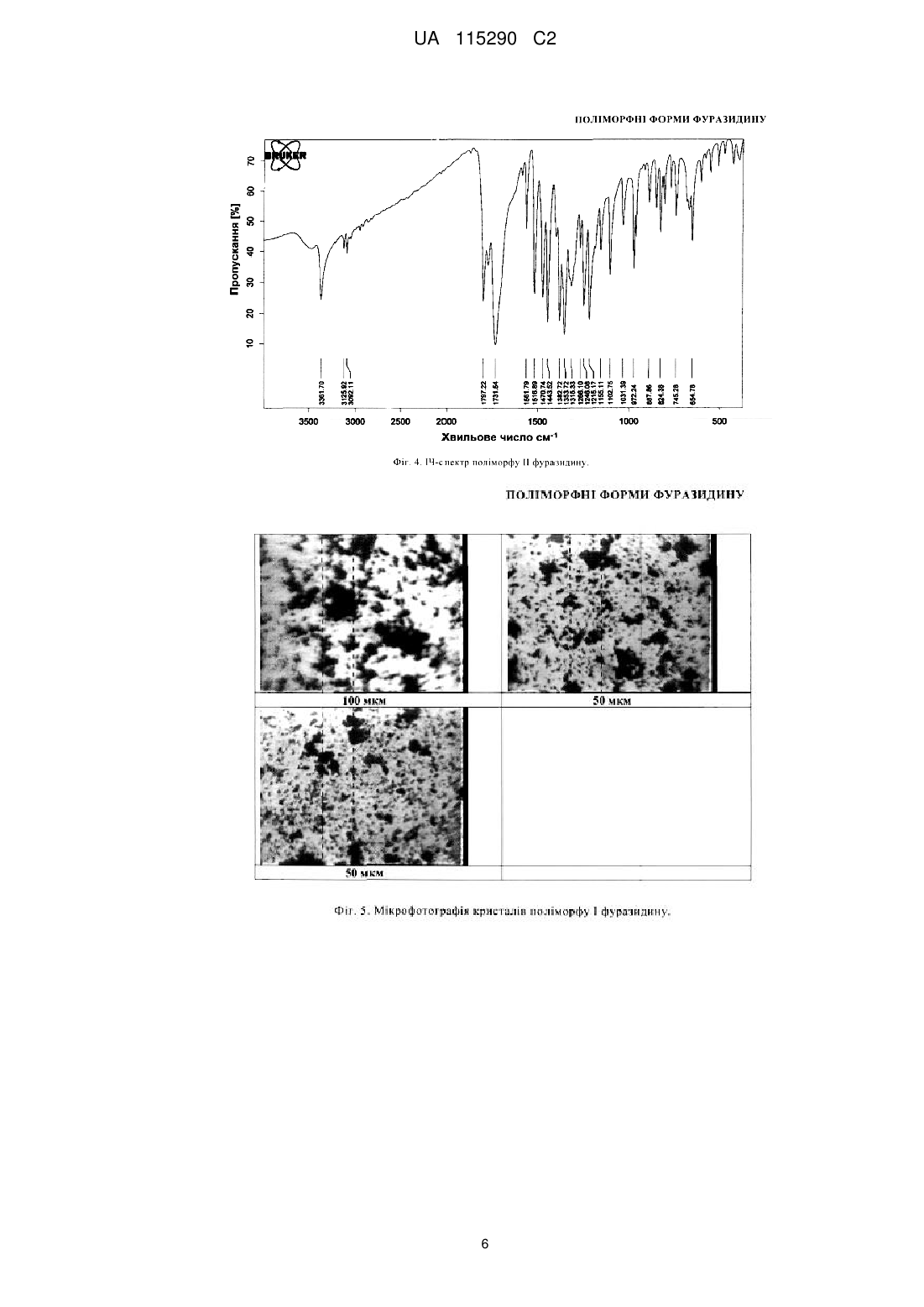
7. Кристалічна форма II фуразидину за п. 5, що характеризується ІЧ-спектром, як показано на Фіг. 4.
8. Кристалічна форма І фуразидину за будь-яким з пп. 5-7, що містить менше ніж 10 % іншої кристалічної форми фуразидину.
9. Кристалічна форма фуразидину за будь-яким з пп. 1-8 для використання у фармацевтичній композиції.
Текст
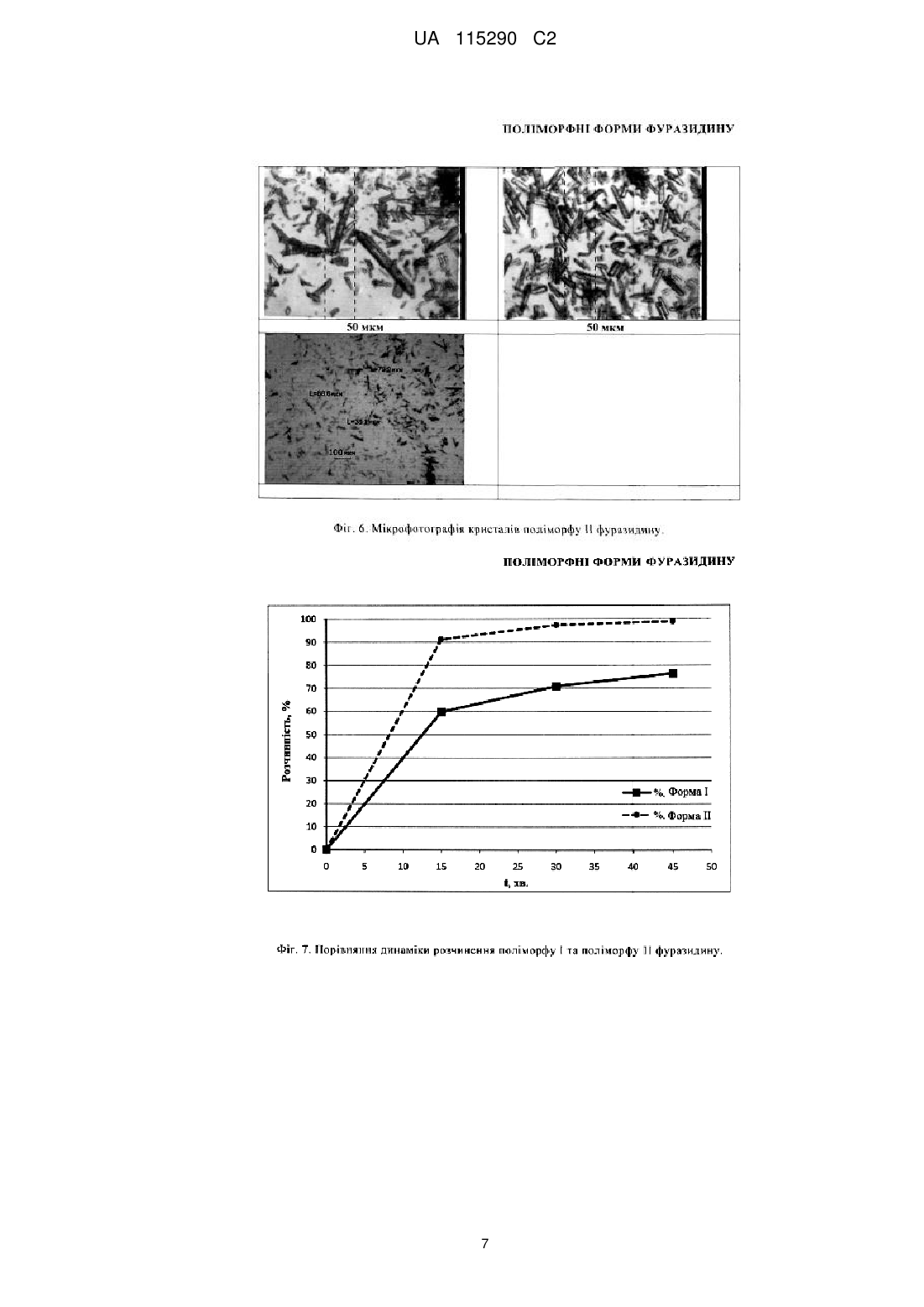
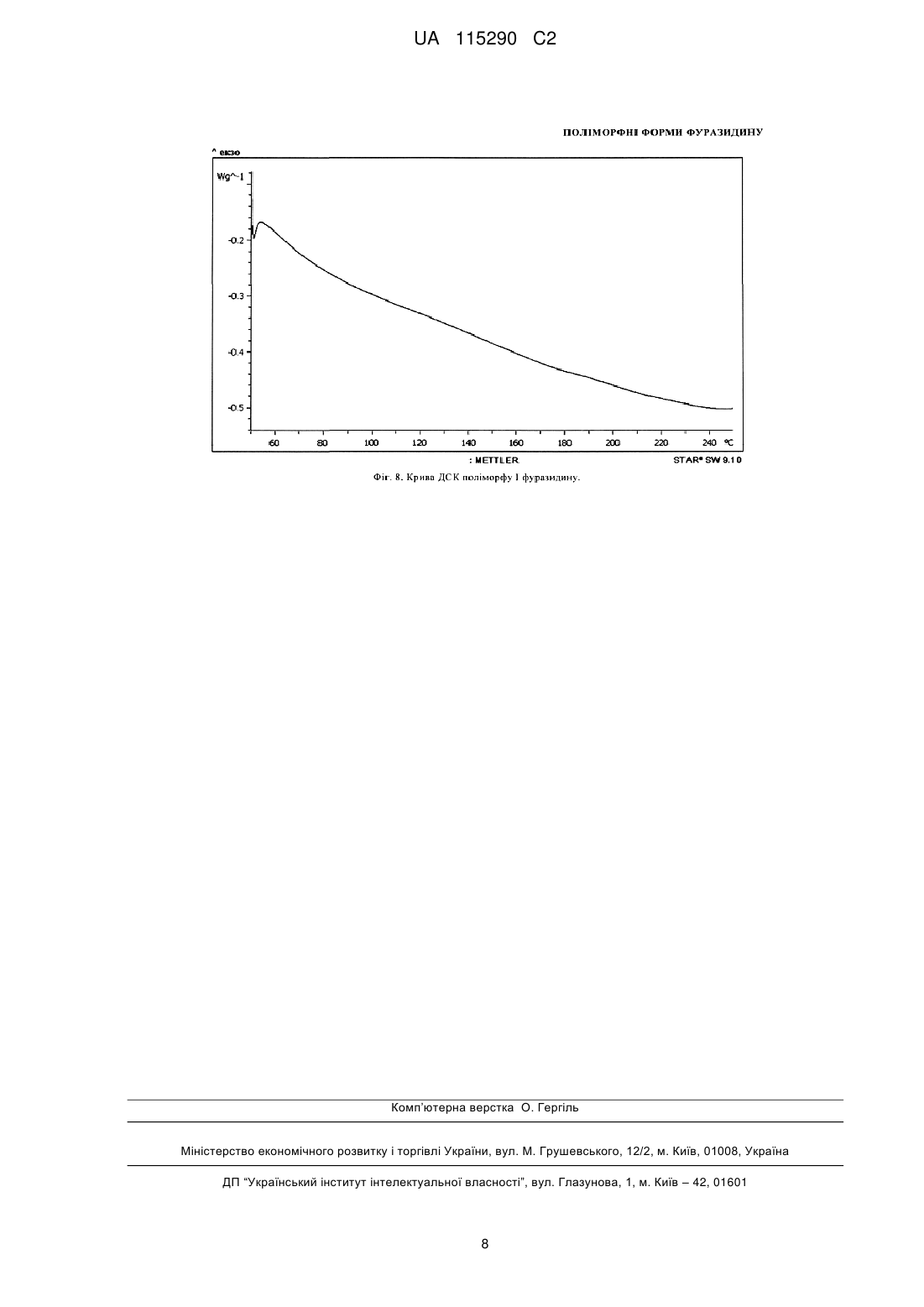
Реферат: Винахід стосується кристалічних форм фуразидину (1-{[(1Е,2Е)-3-(5-нітрофуран-2-іл)проп-2-ен1-іліден]аміно}імідазолідин-2,4-діону) та способів його виготовлення. UA 115290 C2 (12) UA 115290 C2 UA 115290 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь винаходу Запропонований винахід належить до галузі медичної хімії, зокрема до кристалічних поліморфних форм фармацевтичного промислового продукту Фуразидину та способу його виготовлення. Запропонований винахід також стосується застосування зазначених поліморфних форм для виготовлення фармацевтичної композиції. Рівень техніки Фуразидин (1-{[(1E,2E)-3-(5-нітрофуран-2-іл)проп-2-ен-1-іліден]аміно}-імідазолідин-2,4-діон) відомий на фармацевтичному ринку під торговим найменуванням Фурагін® (Furaginum, INN). Це антибактеріальний агент бактеріостатичної дії, що ефективний як проти грампозитивних (Staphylococcus epidermidis, Staphylococcus aureus, Staphylococcus faecalis), так і проти грамнегативних (Enterobacteriaceae, Escherichia coli, Klebsiella spp, Salmonella, Shygella, Proteus, Enterobacter, і т.д.) бактерій. Цей лікарський засіб широко використовується у лікуванні інфекцій сечових шляхів у дорослих та дітей. У виробництві фармацевтичного продукту дуже важливо контролювати кристалічну форму активної речовини. Тверді кристалічні субстанції можуть існувати у різних кристалічних формах, які називають поліморфами. Різні поліморфи можуть мати різні фізичні і/або хімічні властивості, такі як розчинність, швидкість розчинення, температура плавлення, стабільність тощо. Ці властивості можуть прямо впливати на можливість виготовлення активної субстанції та відповідного їй фармацевтичного продукту, а також на стабільність та біодоступність такого продукту. Тому поліморфізм може вплинути на якість фармацевтичного продукту і/або його безпечність та ефективність. Виготовлення чистого поліморфу та дослідження його властивостей забезпечує кращий контроль процесу виробництва фармацевтичного продукту. Контрольовані та відтворювані способи виготовлення чистих поліморфів придатні для промислового використання; чисті поліморфи можуть бути застосовані для поліпшення властивостей фармацевтичних композицій. Для характеристики поліморфних форм кристалічної субстанції відомі декілька методів. Поліморфізм можна підтвердити демонстрацією нееквівалентних структур шляхом рентгеноструктурного аналізу на монокристалах. Для підтвердження поліморфізму може також бути використана рентгенівська порошкова дифракція. Для характеристики індивідуальних поліморфних форм використовують різноманітні аналітичні методи, що включають мікроскопію, термічний аналіз (ДСК, ТГА), спектроскопію (ІЧ, Раман, твердофазний ЯМР). Фуразидин синтезують реакцією між 3-(5-нітро-2-фурил)акролеїном та 1-аміногідантоїном або 3-(5-нітро-2-фурил)акролеїном та похідним семікарбазидоцтової кислоти з наступним утворенням гідантоїнового циклу (J. Pharm. Soc. Japan, 1955, 75; 117, FR1489091, 1966). Також були описані декілька способів добування фуразидину з 1-ариламіногідантоїнів у присутності мінеральних кислот (сульфатної кислоти, соляної кислоти, сульфонових кислот) (US 2990402; WO97/19930; WO98/41520). Поліморфні форми фуразидину на даний момент описані не були. Якщо кристалічну форму виготовляти у суміші з іншими кристалічними формами, це може призвести до нестабільності лікарської форми у процесі виробництва та до її перетворення на іншу поліморфну форму. Тому надзвичайно важливе одержання поліморфних форм високої поліморфної чистоти. Короткий опис фігур Фіг. 1. Рентгенівська порошкова дифрактограма поліморфу І фуразидину. Фіг. 2. ІЧ-спектр поліморфу І фуразидину. Фіг. 3. Рентгенівська порошкова дифрактограма поліморфу ІІ фуразидину. Фіг. 4. ІЧ-спектр поліморфу ІІ фуразидину. Фіг. 5. Мікрофотографія кристалів поліморфу І фуразидину. Фіг. 6. Мікрофотографія кристалів поліморфу ІІ фуразидину. Фіг. 7. Порівняння динаміки розчинення поліморфу І та поліморфу ІІ фуразидину. Фіг. 8. Крива ДСК поліморфу І фуразидину. Фіг. 9. Крива ДСК поліморфу ІІ фуразидину. Опис винаходу Неочікувано було виявлено, що у процесі виготовлення фуразидину утворюються неідентичні субстанції. ІЧ-спектри, використані для перевірки ідентичності, були також неідентичними. Нами було ізольовано стабільні кристалічні форми, ідентифіковані як Поліморф І та Поліморф ІІ. Вказані поліморфи були охарактеризовані різними аналітичними методами, включаючи рентгенівську порошкову дифракцію (РПД) та інфрачервону (ІЧ) спектроскопію. Характерна РПД-дифрактограма поліморфу І представлена на Фіг. 1. Положення піків дифрактограми та їх відносна інтенсивність підсумовані у Таблиці 1. Кути 2θ положень піків представлені як ±0,2°. ІЧ-спектр поліморфу І представлений на Фіг. 2. 1 UA 115290 C2 5 10 15 Характерна РПД-дифрактограма поліморфу ІІ представлена на Фіг. 3. Положення піків дифрактограми та їх відносна інтенсивність підсумовані у Таблиці 1. Кути 2θ положень піків представлені як ±0,2°. ІЧ-спектр поліморфу ІІ представлений на Фіг. 4. Згідно запропонованого винаходу, чисті поліморфи фуразидину І та ІІ можуть бути отримані конденсацією 3-(5-нітрофуран-2-іл)акролеїну з 1-аміногідантоїном у присутності кристалічних зародків бажаного поліморфу. Залежно від використовуваного кристалічного зародку, поліморф І або поліморф ІІ можна отримати з поліморфною чистотою більше 90 %. Якщо зазначену реакцію виконувати без кристалічних зародків, то зазвичай отримують поліморф І або суміш поліморфів І та ІІ. Згідно даного винаходу ми неочікувано виявили, що при синтезі поліморфу ІІ отримуваний фуразидин має вищу якість, ніж при синтезі поліморфу І. Поліморф ІІ містить менше домішок порівняно з поліморфом І. Поліморф ІІ піддається фільтрації набагато краще, ніж поліморф І. При візуальному порівнянні розміру кристалів за допомогою мікроскопії було виявлено, що поліморф ІІ має більші кристали (Фіг. 5, 6). При ситовому аналізі було виявлено, що поліморф І прилипає до вічок сита, злежується та забиває вічка, таким чином ускладнюючи виготовлення фармацевтичної композиції та погіршуючи її властивості. Таблиця 1 Положення та відносна інтенсивність піків дифрактограм поліморфів І та ІІ 2θ 9,306 10,51 10,99 11,724 12,981 13,647 17,335 18,097 18,719 19,223 19,619 20,159 21,187 22,241 22,499 23,954 24,817 25,587 25,83 26,88 27,389 27,764 28,344 28,557 29,055 29,437 30,159 30,805 31,734 32,057 33,663 34,105 20 Поліморф І Відносна інтенсивність, % 2,50 4,50 6,40 11,80 9,50 10,30 0,50 20,10 5,80 24,10 3,80 9,10 67,30 4,20 2,70 10,90 0,70 2,10 1,10 1,00 12,40 13,70 100,00 13,50 3,40 1,00 3,60 0,90 1,70 2,30 3,30 0,70 2θ 7,833 10,968 13,253 13,729 15,411 15,773 17,281 17,54 19,173 20,916 21,649 22,311 22,53 22,939 23,789 24,213 25,035 25,644 26,027 26,611 26,708 27,296 27,75 28,398 29,723 30,043 30,594 31,075 31,577 31,971 32,991 33,47 34,075 Поліморф ІІ Відносна інтенсивність, % 11,40 5,40 3,20 4,40 2,70 40,80 100,00 18,10 18,00 0,60 29,20 4,90 13,60 1,80 4,40 2,60 0,20 1,60 1,60 2,80 4,50 90,10 14,90 26,80 0,40 0,30 1,20 2,10 4,70 2,50 2,60 2,40 2,40 Винахідники також дослідили та порівняли динаміку розчинення обох поліморфів у водному розчині гідрокарбонату натрію (Фіг. 7, Таблиця 2). 2 UA 115290 C2 Таблиця 2 Час, хв 0 15 30 45 5 10 15 20 25 30 35 40 45 50 Поліморф І 0 59,9 70,9 76,4 Динаміка розчинення, % Поліморф ІІ 0 91,3 97,4 99,0 Із одержаних результатів видно, що поліморф ІІ розчиняється краще, ніж поліморф І. Динаміка розчинення поліморфу ІІ також значно краща, ніж у поліморфу І. Вже через 15 хвилин 91,3 % поліморфу ІІ розчинилось, порівняно з 59,9 % поліморфу І. Швидше розчинення може позитивно вплинути на біодоступність фармацевтичної субстанції після розчинення лікарської форми у тілі. Характерні криві ДСК для поліморфів І та ІІ показані на Фіг. 8 та 9 та розкривають різницю між двома поліморфами. Крива поліморфу ІІ демонструє екзотермічний ефект з максимумом при 212 °C, що відповідає переходу форми ІІ в форму І. Отримані згідно запропонованого винаходу поліморфи підходять для виготовлення фармацевтичних композицій. Фармацевтична композиція, що містить поліморф фуразидину згідно даного винаходу, придатна для застосування як антибактеріальний лікарський засіб. Приклади Рентгенівська порошкова дифракція (РПД) РПД записували з використанням апарату Bruker D8 Advance, обладнаного детектором o o положення LynxEye. Режим запису: 3-35 2θ, швидкість 0,2с/0,02 . Зразки попередньо подрібнювали в агатовій ступці. Інфрачервоні спектри (ІЧ) Інфрачервоні спектри отримували за допомогою фотометра Nicolet IR200 у пластинках KBr в -1 діапазоні 4000 – 650 см . Диференційна скануюча калориметрія (ДСК) Криві диференційної скануючої калориметрії одержували, використовуючи калориметр Mettler TA 4000 згідно інструкцій виробника. Криві ДСК записували в діапазоні температур від 50 °C до 250 °C при швидкості нагрівання 5,0 °C/хв в атмосфері азоту. Даний винахід проілюстровано наступними необмежуючими прикладами. Приклад 1. Одержання поліморфу ІІ фуразидину 3-(5-нітрофуран-2-іл)акролеїн (45 г) поміщали у тригорлу колбу об'ємом 2 л, обладнану мішалкою, термометром і зворотним холодильником та додавали туди ізопропанол (750 мл), воду (150 мл) і оцтову кислоту (15 мл). Реакційну суміш змішували при 60-80 °C до повного розчинення 3-(5-нітрофуран-2-іл)акролеїну. Розчин 1-аміногідантоїну (49 г) у воді (250 мл) готували у окремій колбі при нагріванні розчину до 50-60 °C. Кристалічні зародки поліморфу фуразидину ІІ (3 г) додавали до теплого розчину 3-(5нітрофуран-2-іл)акролеїну та доливали теплий розчин 1-аміногідантоїну. При цьому в розчині починалось випадіння осаду, а температура розчину підвищувалась. Отриману суміш розчинів підтримували в такому стані протягом 1 год. і потім залишали охолонути. Осад відфільтровували, промивали водою та висушували при 50-60 °C. Одержували 1-{[(1E,2E)-3-(5нітрофуран-2-іл)проп-2-ен-1-іліден]аміно}імідазолідин-2,4-діон (69 г, 97 %). Приклад 2. Одержання поліморфу І фуразидину Поліморф І отримували так само, як описано у Прикладі 1 для поліморфу ІІ, але необов'язково додаючи кристалічні зародки поліморфу І. Приклад 3. Вивчення динаміки розчинення Зразок фуразидину для аналізу (0,05 г) поміщали у капсулу № 3. Для вивчення розчинення використовували апарат для розчинення твердих лікарських форм, обладнаний мішалкою та допоміжним пристроєм занурення капсули. Як середовище розчинення використовували 900 мл 1,5 %-го водного розчину гідрокарбонату натрію. Розчин нагрівали до 37±0,5 °C. У кожну посудину поміщали одну капсулу за допомогою пристрою занурення і вмикали апарат. Аліквоти розчину відбирали, охолоджували та фільтрували через паперовий фільтр, відкидаючи першу порцію фільтрату. Фільтрат (5,0 мл) поміщали у мірну колбу на 50 мл, розбавляли 1,5 %-вим розчином гідрокарбонату натрію до рівня відмітки і добре розмішували. Максимум поглинання 3 UA 115290 C2 світла аналізованим розчином вимірювали за допомогою спектрофотометра Agilent 8453 No. CN22805904 при довжині хвилі 410±2 нм відносно поглинання стандартного зразка. З отриманих даних креслили криві розчинення. 5 10 15 20 25 ФОРМУЛА ВИНАХОДУ 1. Кристалічна форма І фуразидину, яка відрізняється тим, що її РПД-дифрактограма має піки при кутах дифракції 2θ: 10,5±0,2; 11,0±0,2; 11,7±0,2; 13,0±0,2; 13,7±0,2; 18,1±0,2; 18,7±0,2; 19,2±0,2; 20,2±0,2; 21,2±0,2; 22,2±0,2; 24,0±0,2; 27,4±0,2; 27,8±0,2; 28,3±0,2. 2. Кристалічна форма І фуразидину за п. 1, що характеризується РПД-дифрактограмою, як показано на Фіг. 1. 3. Кристалічна форма І фуразидину за п. 1, що характеризується ІЧ-спектром, як показано на Фіг. 2. 4. Кристалічна форма І фуразидину за будь-яким з пп. 1-3, що містить менше ніж 10 % іншої кристалічної форми фуразидину. 5. Кристалічна форма II фуразидину, яка відрізняється тим, що її РПД-дифрактограма має піки при кутах дифракції 2θ: 7,8±0,2; 11,0±0,2; 13,7±0,2; 15,8±0,2; 17,3±0,2; 17,5±0,2; 19,2±0,2; 21,6±0,2; 22,5±0,2; 27,3±0,2; 27,8±0,2; 28,4±0,2. 6. Кристалічна форма II фуразидину за п. 5, що характеризується РПД-дифрактограмою, як показано на Фіг. 3. 7. Кристалічна форма II фуразидину за п. 5, що характеризується ІЧ-спектром, як показано на Фіг. 4. 8. Кристалічна форма І фуразидину за будь-яким з пп. 5-7, що містить менше ніж 10 % іншої кристалічної форми фуразидину. 9. Кристалічна форма фуразидину за будь-яким з пп. 1-8 для використання у фармацевтичній композиції. 4 UA 115290 C2 5 UA 115290 C2 6 UA 115290 C2 7 UA 115290 C2 Комп’ютерна верстка О. Гергіль Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 8
ДивитисяДодаткова інформація
Назва патенту англійськоюPolymorphic forms of furazidin
Автори англійськоюLiepins, Vilnis, Skomorokhov, Mikhail, Lukjanova, Nina, Matiushenkov, Evgenij, Revjuka, Jekaterina
Автори російськоюЛиепинс Вилнис, Скоморохов Михаил, Лукянова Нина, Матиушенков Евгений, Ревюка Екатерина
МПК / Мітки
МПК: A61K 31/4166, C07D 405/12
Мітки: поліморфні, фуразидину, форми
Код посилання
<a href="https://ua.patents.su/10-115290-polimorfni-formi-furazidinu.html" target="_blank" rel="follow" title="База патентів України">Поліморфні форми фуразидину</a>
Попередній патент: Спосіб і пристрій для покриття прокладок
Наступний патент: Спосіб оперативного лікування хронічного панкреатиту
Випадковий патент: Спосіб оцінки тяжкості хвороби в осіб із ко-інфекцією вірусу імунодефіциту людини та хронічного гепатиту с