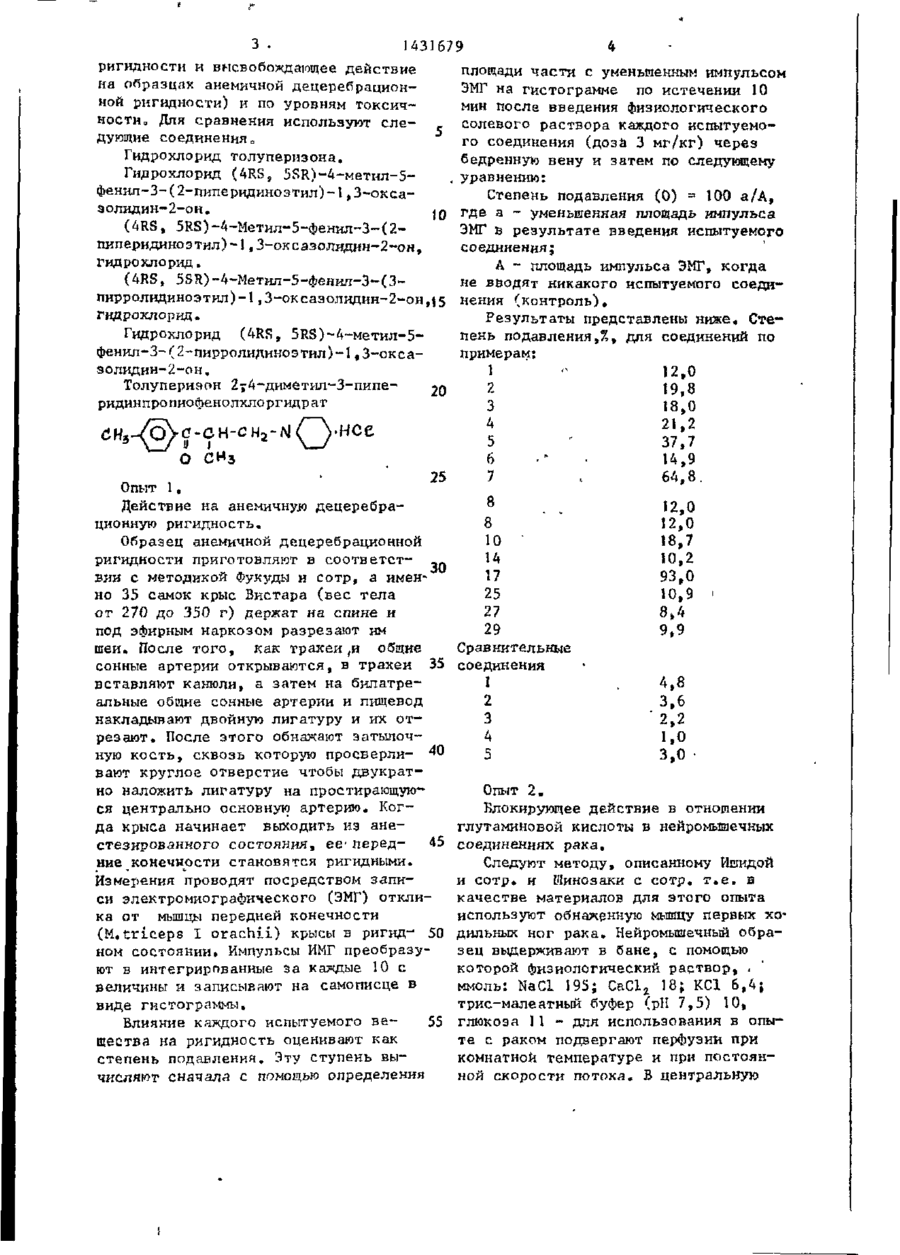
Спосіб отримання похідних 1,3-оксазолідин-2 она чи їх кислотно-адитивних солей
Номер патенту: 4758
Опубліковано: 28.12.1994
Автори: Харухіко Сінозакі, Наойя Моріто, Коіті Хасімото, Тосіро Камісіро, Мазару Сато, Міцуо Масакі
Формула / Реферат
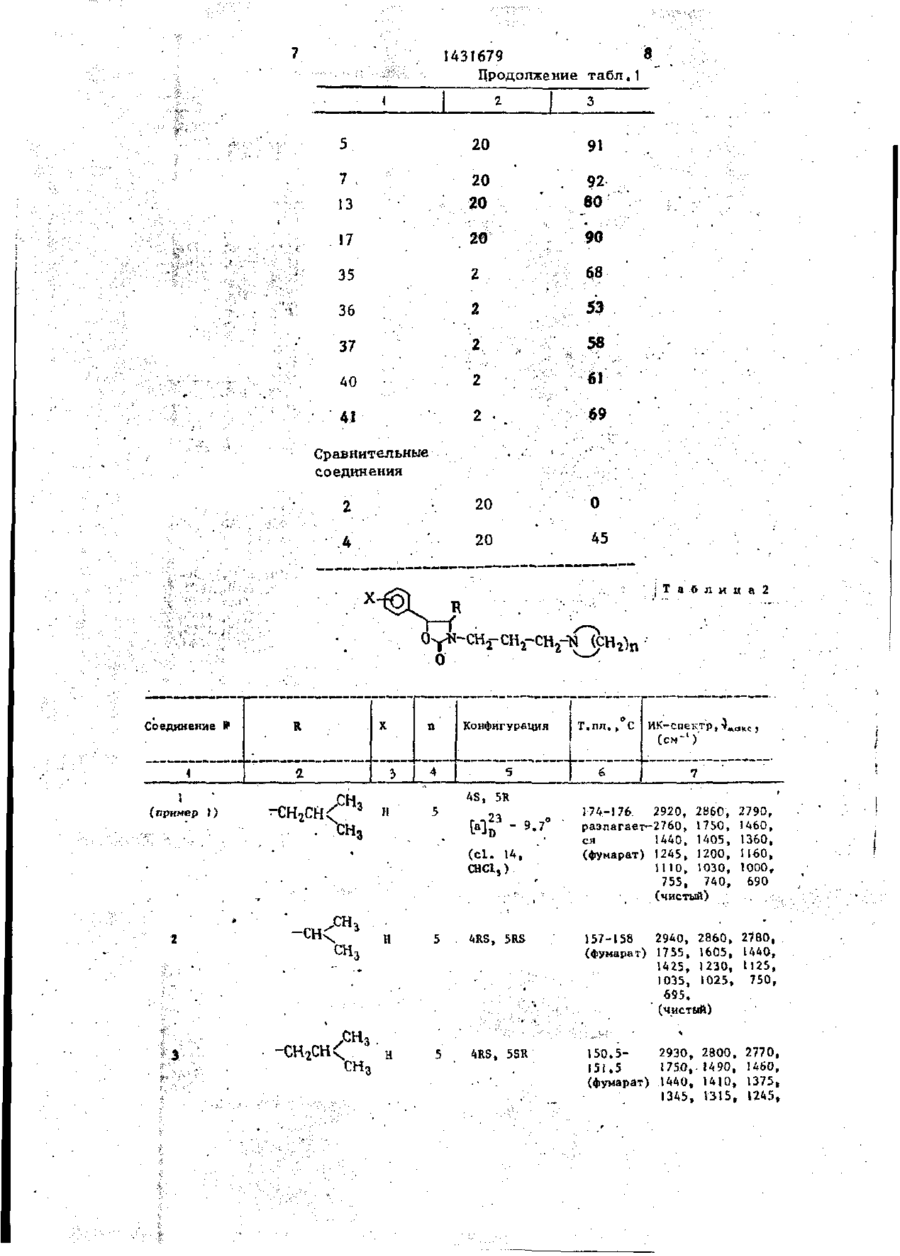
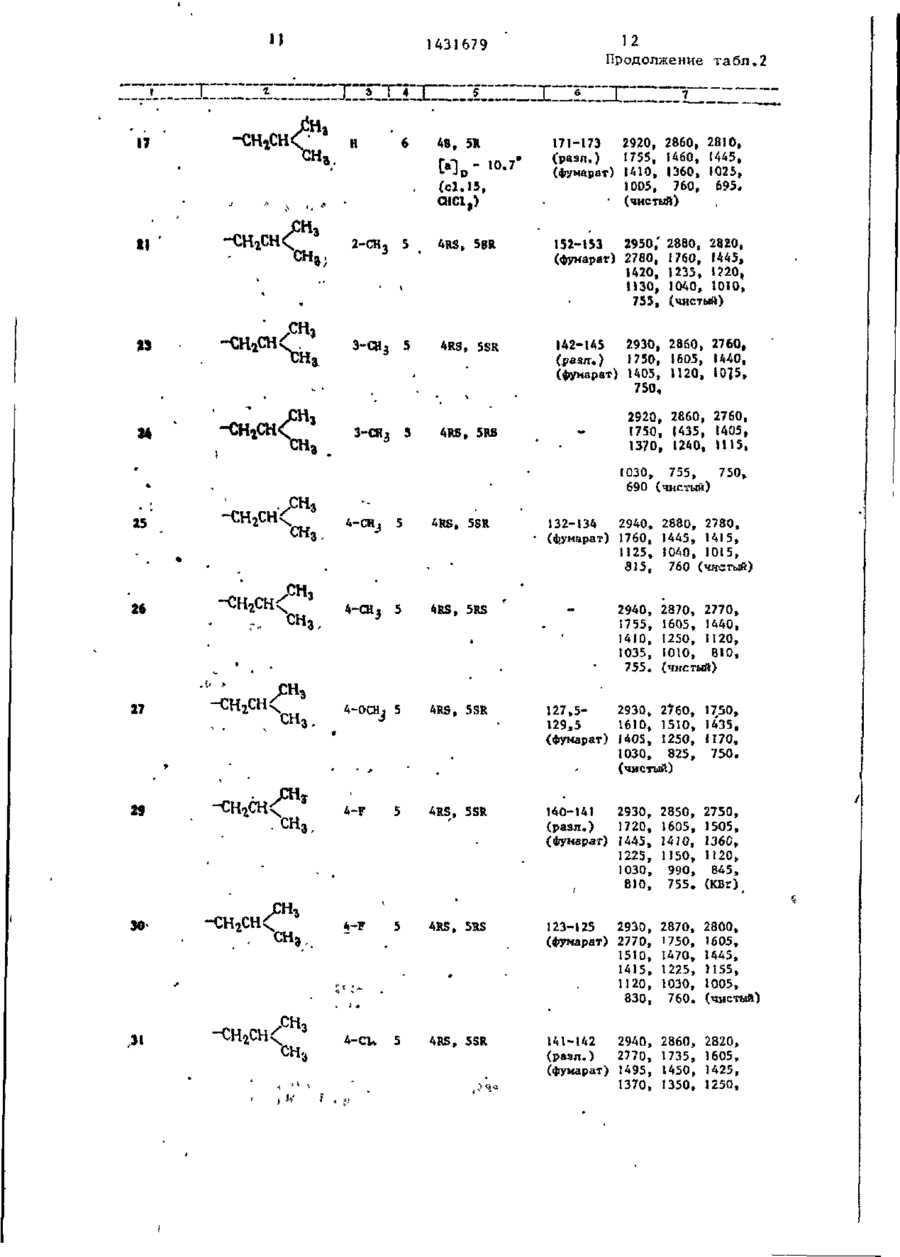
Способ получения производных 1,3 оксазолидин-2-она общей формулы I
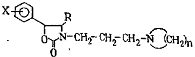
где R-C3-C8-прямой или разветвленный алкил;
X - водород, галоид,
С1-С3-алкил или С1-С3-алкоксил;
n = 4-6, или их кислотно-аддитивных солей, о т л и ч а ю щ и й с я тем, что, соединения общей формулы II
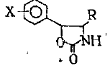
где R и X имеют указанные значения, подвергают взаимодействию с соединением общей формулы III
![]()
где Z - атом галоида, тозилокси или мезилоксигруппа;
n имеет указанные значения, в присутствии карбоната калия или натрия, с последующим выделением целевого продукта в свободном виде или в виде кислотно-аддитивной соли.
Текст
Изобретение к а с а е т с я производных І,3-оксазолидин-2-она, в ч а с т ности получения соединений общей фор (ctu, где R - С э -Cg-н- или изо-алкил; X Н, атом ч галокда, С^-С 3 -алкил или С , - С э - а л к о к с и л ; п = 4-6, или их кис-лотно-адцитивных солей, являющихся селективными блокаторами глутаминовой кислоты. Цель - создание новых активных веществ указанного к л а с с а . Их синтез ведут из незамещенного по "N" - 1,3-оксазолидинона-2, который обрабатывают соединением ф-лы Z - ( C H 2 ) ? -N ( C H , ) n , где п имеет указанные значения^ Z - галоид» тозилокси- или мезилоксигруппа, Б присутствии К 2 С О 3 или Na ? CO 3 . Выделение целевого продукта ведут либо в свободном виде, либо в виде кислотноаддитивной соли. Новые вещества оказывают действие на анемичную децет1 ребрационную регидность со степенью подавления 10—93%э а также блокирующее действие в отноиении глутаминовой кислоты в нейромыиечных соединениях рака со степенью подавления 53-* 92%. Токсичность LI>S0 = 18,8 75,1 мг/кго 2 табл. 8 С 1 1431679 Изобретение относится к области потом (30 мл) и сушат,получая 19,04 г лучения гетероциклических соединений, неочищенных кристаллов о Неочищенные в частности производных 1,3-оксазокристаллы подвергают перекристаллилидин-2-она общей формулы 1 зации из воды (70 мл), получая 5 16,73 г целевого соединения в виде белых кристаллов (выход 737.). Т.пл. 174-176 С (разлагается) ,[оі.^ 4-12,0° 1 (концентрация 1,00, в метаноле), ИК~ І0 спектр, К В г , ^ я к с см"1 : 3560, 3450, 2950, 2640, 2350, 1740, 1725, 1690, прямой или разветвлен1635, 1540, 1450, 1405, 1240, 1200, где Я-С ъ -С 6 ный алкил; 995, 975, 765, 745, 695. X - водород, галоид, С 4 - ' П р и м е р 2. По методике приCj-алкил или С ( -С ? -ал- 15 мера 1,получают вещества, приведенкоксил, ные в табл.2. 4-6, или ігл кислотно-аддитивным солям, обладающим свойствами селективных блокаторов глутаминовой кислоты. 20 Целью изобретения является создание на основе известных методов способа получения новых соединений, обладающих ценными фармакологическими свойствами» П р и м е р 1. (4S, 5R) 4-(2-Метилпропил)-5-фенил-3-(3-пиперидннопропил)-!,3-оксазолидин-2-он, фумарат Смесь (4S t 5К)-4-(2-Метилпропил)5-фенил-І,3-оксазолидин-2-она 30 (10,97 г, 50 ммоль), гидрохлорида і-(З-хлорпропил) пиперидина (12,38 г 62,5 ммоло), безводного порошка карбоната калия (17,28 г, 65,2 ммоль), безводного порошка карбоната калия, (17,2В г , 125 ммоль) и 130 мл метил- 35 этилкетона нагревают и кипятят с обратным холодильником при перемешивании в течение 24 ч. После- завершения взаимодействия реакционную смесь охлаждают и нерастворивгаееся вещест- 40 во удаляют посредством фильтрации» Керастворившееся вещество промывают метилэтилкетаном» Промывочную жидкость н фильтрат объединяют и концентрируют при пониженном давлении. Остаток растворяют в 70 мл толуола. Толуольный раствор трижды промывают водсхЗ (70 мл) н толуол выпаривают * При пониженном давлении. Остаток 50 растворяют в 50 мл этанола, после чего добавляют фумаровую кислоту (5,80 г, 50 ммоль). Образовавшуюся смесь нагревают чтобы растворить фумаровую кислоту. Раствору дают отстояться в течение ночи при комнатной 55 температуре. Выпавшие в осаДок кристаллы собирают посредством фильтрации, трижды промывают этиловым спир П р и м є р 3. (4S, 5R)-4-(2-Meтилпропил)-5-фенил-3(3-пиперидинопропил)-1,3~оксазолидич-2-он, метансульфона. ' Смесь (4S, 5&)-4-(2~метилпропил)5-фенил-1„З-оксазолндин-2-она (10,97 г 50 ммоль), хлоргидрата 3-пиперидинопропил-п-толуолсульфоната (25,04 г, 75 ммоль), порошкообразного безводнот го карбоната калия (20,73 г, 150 ммоль) и метилэтилкетона (200 мл) перемешивают и кипятят 24 ч . Реакционную смесь охлаждают и нерастворимую часть отфильтровывают. Для удаления растворителя фильтра испаряют при пониженном давлении. Остаток растворяют в хлороформе (200 мл). После трехкратного промывания 2н. НС1 (100 мл) раствор смешивают с 2 а. NaOH (100 мл), после чего 30 мин перемешивают. Органический слой отделяют и промывают насыщенным раствором NaCl, сушат над безводным сульфатом натрия, после чего растворитель испаряют. К раствору добавляют метан сул ьф о но вую кислоту (4,8 г, 5(У ммоль) , после чего перемешивают при комнатной температуре. Полученный осадок собирают фильтрованием, промывают раствором этанола с этилацетатом (1:20,2*17 мл), затем этилацетатом (17 мл) и высушивают с получением указанного соединения (16,83 г ) в виде бесцветных кристаллов (выход 76%), т.пл, 129-13Г.С. Исследование фармакологической активности соединения общей формулы 1. Эффективность соединения общей формулы 1 определяют по блокирующему действию в отношении глутаминовой кислоты, по релаксирующему действию на мышцы спинного мозга (понижение 43J679 ригидности и высвобождающее действие площади части с уменьшенным импульсом на образцах анемичной децеребрационЭМГ на гистограмме по истечении 10 нои ригидности) и по уровням токсичмин после введения физиологического ности,, Для сравнения используют с л е солевого раствора каждого испытуемодующие соединения 0 го соединения (доза 3 мг/кг) через Гидрохлорид толуперизона. бедренную вену и затем по следующему Гидрохлорид (4RS, 5SR)-4-MeTmi-5уравнению: фенил-3-(2-пиперидинозтил)-1,3-оксаСтепень подавления (0) = 100 а/А, эолидин-2-он. ,Q где а - уменьшенная площадь импульса (4RS, 5И8)-4-Метил-5-фенил-3-(2ЭМГ в результате введения испытуемого пиперидиноэтил)-!,3-оксазолидин-2~он, соединения; гидрохлорид. А ~ площадь импульса ЭМГ, когда (4RS, 55К)-4-Метил-5-фенил-3-(3не вводят никакого испытуемого соедипирролидиноэтил)-1,3-оксазолидин-2-он,^5 нения (контроль). гидрохлорид. Результаты представлены ниже. СтеГидрохлорид (4RR, 5RS)-4-MeTmi-5пень подавления,%, для соединений по фенил-3-(2-пирролидиноэтил)-1,3-оксапримерам: эолидин-2-он, 1 ' 12,0 Толуперизон 2^4-дим&тил*-3-пипе20 2 19,8 ридинпропиофенолхлоргидрат 3 18,0 4 21,2 5 37,7 s 6 • 14,9 си 3 25 7 , 64,8. Опыт 1, 8 Действие на анемичную децеребра12,0 8 12,0 ционную ригидность. 10 ' 18,7 Образец анемичной децеребрационнои 14 10,2 ригидности приготовляют в соответст30 17 93,0 вии с методикой Фукуды и сотр, а именно 35 самок крыс Вистара (вес тела 25 10,9 от 270 до 350 г) держат на спине и 27 8,4 под эфирным наркозом разрезают им 29 9,9 шеи. После того, как трахеи ,и общие Сравнительные сонные артерии открываются, в трахеи 35 соединения вставляют канюли, а затем на бнлатре1 4,8 альные общие сонные артерии и пищевод 2 3,6 накладывают двойную лигатуру и их от3 ' 2,2 резают. После этого обнажают затылоч4 1,0 ную кость, сквозь которую просверли- 40 5 3,0 вают круглое отверстие чтобы двукратно наложить лигатуру на простирающуюОпыт 2. ся центрально основную артерию. КогБлокирующее действие в отношении да крыса начинает выходить из анеглутаминовой кислоты в нейромышечных стезированного состояния, ее-перед- 45 соединениях рака. ние конечности становятся ригидными. Следуют методу, описанному ИшидоЙ Измерения проводят посредством запии сотр. и Шинозакн с сотр. т . е . в си электромиографического (ЭМГ) откликачестве материалов для этого опыта ка от мышцы передней конечности используют обнаженную мышцу первых хо(М.triceps I orachii) крысы в ригид- 50 дильных ног рака, Нейромышечный обраном состоянии. Импульсы ИМГ преобразузец выдерживают в бане, с помощью ют в интегрированные за каждые 10 с которой физиологический раствор, . величины и записывают на самописце в ммоль: NaCl 195; СаС1 2 18; КС1 6,4; виде гистограммы. трис-малеатный буфер (рИ 7,5) 10, Влияние каждого испытуемого ве55 глюкоза 11 - для использования в опыте с раком подвергают перфузии при щества на ригидность оценивают как комнатной температуре и при постоянстепень подавления. Эту ступень выной скорости потока* В центральную числяют сначала с помощью определения ь часть мытечного волокна вставляют стеклянные микроэлектроды, каждый из которых заполнен З М раствором хлористого калия, для того, чтобы записывать внутриклеточные изменения потенциала мембраны мышечной клетки» Блокирующее действие каждого испытуемого вещества в отношении глутаминовой кислоты оценивают как степень подавления деполяризации, которая вызывается применением ванны из о -глуб таминовой кислоты (моль/л 10 ) при пятиминутной предварительной обработке раствором испытуемого соединения. Результаты представлены в табл.1. Опыт 3. Острая токсичность, Используя 10 самцов мыши dot N в соответствии с методом "вверх и вниз" определяют уровень острой токсичности каждого испытуемого соедине- 20 ния. Некоторые из них растворяют в физиологическом солевом растворе и вводят через хвостовую вену. Результаты представлены ниже. Дозы, вызывающие 50% смертности при внутривенном введении, Ы ) 5 0 (мг/кг) в»в., для соединений по примерам: 1 2 3 4 5 7 10 13 14 17 25 27 29 40 6 1431679 " 29,7 18,8 55,5 29,9 69,0 30,4 54,6 75,1 53,2 40,1 34,9 39,8 66,1 ^3.6 Ф о р м у л а изо б р е т е н н я Способ получения производных 1?3оксазолидин-2-она общей формулы I где R-C ,-Cg-прямой или разветвленный алкнл; X - водород, галоид, С, -С 3 -алкил или С,,-Сз-алкоксил; п = 4-6, или их кислотно-аддитивных солей, о т л и ч а ю щ и й с я тем, что, соединения общей формулы I I где R и X имеют указанные значения, подвергают взаимодействию с соединением общей формулы III 35 где Z - атом галоида, тозилокси или мезилоксигруппа; и имеет указанные значения, в присутствии карбоната калия или натрия, с последующим выделением це40 левого продукта в свободном виде или в виде кислотно-аддитивной соли. Т а б л и ц а Испытуемое соединение по примерам Концентрация испытываемого вещества в растворе моль/л '10" і 1 I Степень блокирования по отношению к глутаминовой кислоте ,% 3 20 89 20 88 І431679 8 Продолжение табл.1 5 20 91 1 13 20 20 92 80 17 . 20 90 35 2 68 2 S3 2 58 2 61 2 • 69 0 0 36 ; 37 40 • 41 • Сравнительные соединения 2 . • .4 ' 2 45 20 -*Ы • Т а б л и ц а 2 О Соединение № R І 1 1 (пример J) п X ь Конфигурация 4 в 5 ИК-спектр,^акс, Сем-') Т.пл.,°С і 7 • 4S, 5R 3 -СН 2 СНсн - с н < ач Ш н 4RS, 5RS 174-176 2920, 2860, 2790, разлагает-2760, 1750, 1460, ся 1440, 1405, 1360, (фумарат) 1245, 1200, П 6 0 , 1110, 1030, Ю О О Г 755, 740, 690 (чистый) 157-158 2940, 2860, 2780, (фумарат) 1755, 1605, 1440, 1425, 1230, М25, 1035, 1025, 750, (чистый) -СНгСН< сн 4RS, 5SR 150.52930, 2800, 151.5 1750,-1*90, (фумарат) 1440, 14Ю, 1345, 1315, 2770, 1460, 1375, 1245, 1431679 х 10 Продолжение т а б л . 2 і: 12ІІ, 1170, 1120, 1035, 1010, 755, 695 (КВг) 5 сн3 4RS, 5RS 137-140 2930, 2810, 2760, (Фумарат) 1740, 1435, U 2 5 , 1375, Ї315, 1245, 1170, 1150, П25.І П 1 5 , 1055, 1030, 1000, 935, 755, 750, 695 (КВг) ' -сн< 5 -СН 2 СН 10 ~сн5, 1240, 1120, 1030, 1000, 755, 695. (чистый) 126-128 2930, 2870, 2770, (фумарат) .1740, 1440, 1410, 1010, 770, 703. (КВг) 118-120 2930, 2860, 2760, (фумврат) 1750, 1605, 1450, 1410, 1120, 1030, 1010, 755, 695 (чистый) 4RS, 5RS 37 98-ІОО 2940, 2860, 2770, (фуиарат) 1750, 1605, 1450, 1415, 1230, 1120, 1035г 1000, 755, 695. (чистый) 4RS, 5SR * 36 4RS, 5RS 134-136 2940,-2860,'2800, (оксалат) 2770, 1755, 1450, 1415, 1375, 1240, 1230, 1120, 1035, 1000, 755, 695. (neat) . • 38 ДО, 58R 113-115 2930,2860, 2800, (фумарат) 2760, 1750, 1445, 1410, 1245, 1225, 1120, 1030, 1010, 755, 695. (чистый) 39 4RS, 5RS 125-126 (маяеат) 4RS, 5SR 138-139 2920, 2850, 2740, (фумарат) 1740, 1600, 1440, U05, 1115, 1025, 1005, 745, 690 (чистый) 4RS, 5RS 92-94 2920, 2850,,2770, .(фумарат) 1750, 1600, 1450, •(СНг1гСНч -(СНг)5СНз И 2940, 2870, 2780, 1755, 1610, І45О, 1420, 1240, И З О , 1040, 1010, 760, 700 (чистый) U31679 16 Продолжение т а б л . 2 1 ~(СН2)5СНз Редактор О.Спесивых - Н 5 ARS, 58R 1410, 1230, П20, 1030, 1010, 755, 695 ("чистый) 121-123 2930, 2850, 2770, (фунарят) }750, 1605, 1450, UI0, П20, 1035, 760, 700. (чистый) Составитель Н 0 Банникова Техред А.Кравчук Корректор М.Шароши Заказ 5357/59 Тираж 370 Подписное ВНИИПИ Государственного комитета СССР по делам изобретений и открытий 113035, Москва, Ж-35, Раушская н а б . , д . 4/5 Производственно-полиграфическое предприятие, г . Ужгород, ул. Проектная, 4 I \
ДивитисяДодаткова інформація
МПК / Мітки
Мітки: солей, отримання, похідних, кислотно-адітивних, 1,3-оксазолідин-2, спосіб
Код посилання
<a href="https://ua.patents.su/10-4758-sposib-otrimannya-pokhidnikh-13-oksazolidin-2-ona-chi-kh-kislotno-aditivnikh-solejj.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання похідних 1,3-оксазолідин-2 она чи їх кислотно-адитивних солей</a>
Попередній патент: Спосіб отримання похідних оксимів 1,2,5,6,-тетрагідропірідін-3-карбоксальдегіду
Наступний патент: Спосіб отримання комплексних сполучень платіни
Випадковий патент: Спосіб відбору високоцукристих генотипів цукрових буряків на ранніх етапах розвитку