Спосіб одержання кристалічного периндоприлу
Формула / Реферат
1. Спосіб одержання кристалічного периндоприлу, що включає наступні стадії:
(a) перетворення неочищеного периндоприлу на сіль алкіламонію, яку вибирають з групи, що включає сіль трет-октиламонію і периндоприлу та сіль неопентиламонію і периндоприлу, та
(b) одержання периндоприлу з вказаних солей алкіламонію і виділення кристалічного периндоприлу.
2. Спосіб за п. 1, в якому вказаною сіллю алкіламонію і периндоприлу є сіль трет-октиламонію і периндоприлу.
3. Спосіб за п. 1, в якому вказаною сіллю алкіламонію і периндоприлу є сіль неопентиламонію і периндоприлу.
4. Спосіб за п. 1, в якому стадія (а) включає наступні підстадії:
(а1) розчинення неочищеного периндоприлу в органічному розчиннику або в суміші органічних розчинників, або в суміші органічного розчинника і води,
(а2) додавання аміну, вибраного з групи, що включає трет-октиламін та неопентиламін,
(а3) необов'язкове охолодження одержаного розчину до температури менше 40 °С, та
(а4) відділення одержаного осаду.
5. Спосіб за п. 4, в якому вказаний органічний розчинник вибирають з групи, що включає складні ефіри, нітрили, кетони, прості ефіри, хлоровані вуглеводні та С4-С8-алкілові спирти.
6. Спосіб за п. 4, в якому вказаним органічним розчинником є ацетонітрил, а вказаним аміном є трет-октиламін.
7. Спосіб за п. 4, в якому вказаним органічним розчинником є ацетонітрил, що містить менше 5 мас. % води, а вказаним аміном є трет-октиламін.
8. Спосіб за п. 4, в якому вказаним органічним розчинником є етилацетат, а вказаним аміном є неопентиламін.
9. Спосіб за п. 1, в якому стадія (b) включає підстадії:
(bi1) розчинення солі алкіламонію і периндоприлу, одержаної на стадії (а), у воді або у водному розчині хлориду натрію,
(bі2) підкислення одержаного водного розчину до рН, при якому периндоприл знаходиться у формі вільної кислоти, переважно при додаванні принаймні однієї органічної або неорганічної кислоти або їх суміші,
(bі3) екстракція одержаного периндоприлу з водної фази органічним розчинником,
(bі4) випарювання вказаного органічного розчинника,
(bі5) обробка одержаного залишку органічним розчинником, та
(bі3) відділення одержаного осаду фільтруванням та виділення кристалічного периндоприлу.
10. Спосіб за п. 9, в якому кислотою, яку додають на підстадії (bі2), є суміш оцтової кислоти і соляної кислоти.
11. Спосіб за п. 9, в якому органічний розчинник для використання на підстадії (bі3) вибирають з групи, що включає складні ефіри, хлоровані вуглеводні,прості ефіри або ароматичні вуглеводні.
12. Спосіб за п. 9, в якому органічним розчинником для використання на підстадії (bі3) є дихлорометан.
13. Спосіб за п. 9, в якому органічний розчинник для використання на підстадії (bі5) вибирають з групи, що включає прості ефіри або вуглеводні.
14. Спосіб за п. 9, в якому органічним розчинником для використання на підстадії (bі5) є гексан.
15. Спосіб за п. 1, в якому стадія (b) включає підстадії:
(bii1) розчинення солі трет-октиламонію і периндоприлу, одержаної на стадії (а), в органічному розчиннику,
(bіі2) видалення катіону трет-октиламонію з одержаного розчину, і
(bіі3) випарювання вказаного органічного розчинника, при цьому одержують кристалічний периндоприл.
16. Спосіб за п. 1, в якому стадія (b) включає підстадії:
(bii1) розчинення солі трет-октиламонію і периндоприлу, одержаної на стадії (а), в органічному розчиннику,
(bіі2) обробка одержаного розчину, принаймні, однією кислотою, з подальшим видаленням одержаної нерозчинної солі трет-октиламонію, і
(bіі3) випарювання вказаного органічного розчинника, при цьому одержують кристалічний периндоприл.
17. Спосіб за п. 15 або п. 16, в якому вказаний органічний розчинник, використовуваний на підстадії (bii1), вибирають з групи, що включає спирти, ацетонітрил та етилацетат.
18. Спосіб за п. 15 або п. 16, в якому вказаним органічним розчинником, використовуваним на підстадії (bii1), є ізопропанол.
19. Спосіб за п. 16, в якому вказаною кислотою, використовуваною на підстадії (bіі2), є сірчана кислота.
20. Спосіб за будь-яким з пп. 1-19, в якому на додатковій стадії периндоприл, одержаний на стадії (b), або його нові солі алкіламонію, одержані на стадії (а), переробляють у фармацевтично прийнятну лікарську форму.
21. Сіль трет-октиламонію і периндоприлу.
22. Кристалічна сіль трет-октиламонію і периндоприлу, яка характеризується порошковою рентгенограмою з наступними характеристичними кутами 2θ:
Кут 2θ (°)
Відносна інтенсивність (%)
5,76
61,42
7,34
17,79
9,68
50,79
13,95
18,85
14,38
23,78
14,75
100,00
15,35
43,69
16,52
73,52
17,30
17,44
19,44
41,22
19,99
34,35
20,80
57,66
22,22
33,41
22,72
54,67
23,98
34,82
26,40
45,04
26,87
19,08
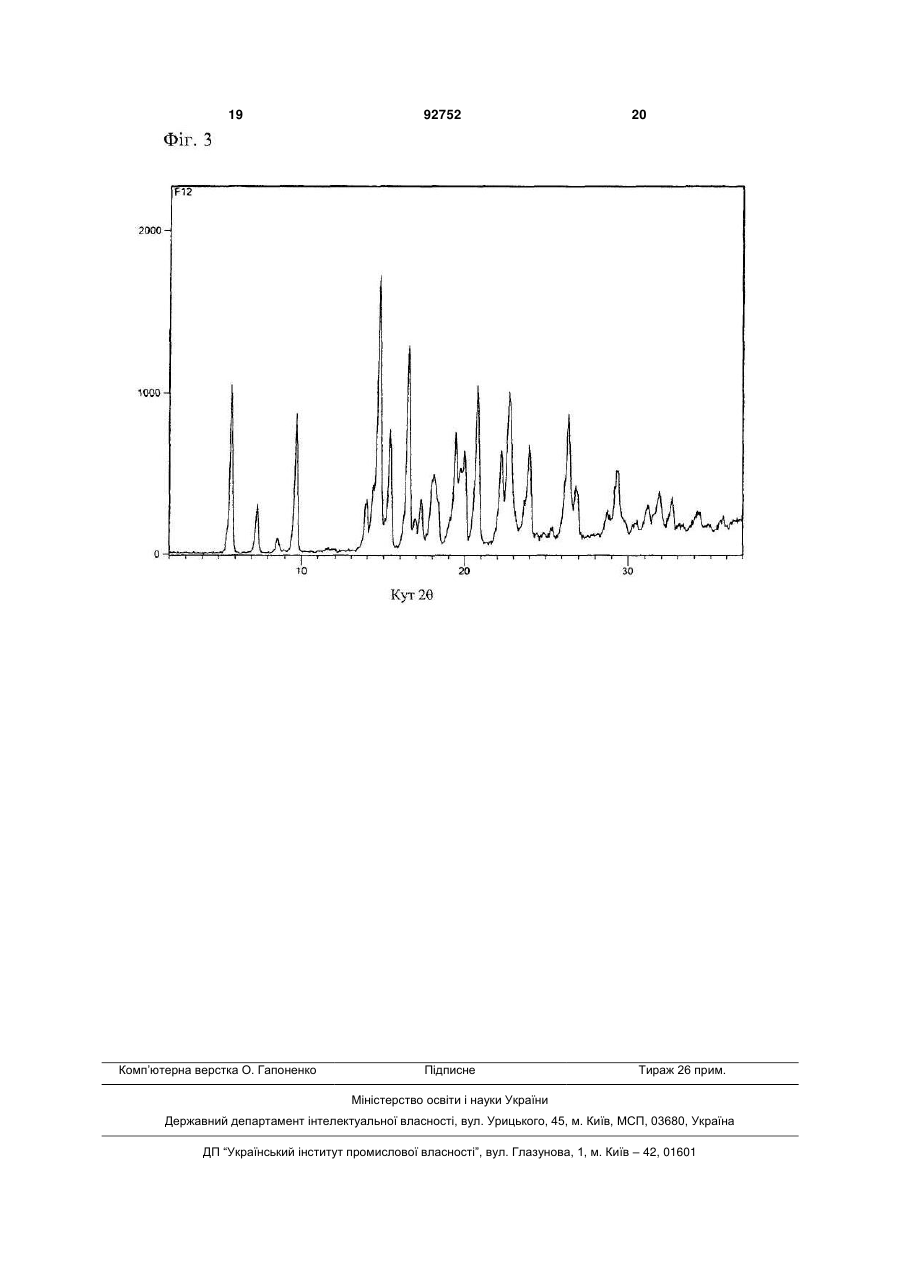
23. Кристалічна сіль трет-октиламонію і периндоприлу, яка характеризується порошковою рентгенограмою, як показано на Фіг. 3.
24. Спосіб одержання солі трет-октиламонію і периндоприлу, що включає наступні стадії:
(а1) розчинення неочищеного периндоприлу в органічному розчиннику або в суміші органічних розчинників, або в суміші органічного розчинника і води,
(а2) додавання трет-октиламіну,
(а3) необов'язкове охолодження одержаного розчину до температури менше 40 °С, і
(а4) відділення одержаного осаду.
25. Сіль неопентиламонію і периндоприлу.
26. Спосіб одержання солі неопентиламонію і периндоприлу, що включає наступні стадії:
(а1) розчинення неочищеного периндоприлу в органічному розчиннику або в суміші органічних розчинників, або в суміші органічного розчинника і води,
(а2) додавання неопентиламіну,
(а3) необов'язкове охолодження одержаного розчину до температури менше 40 °С, і
(а4) відділення одержаного осаду.
27. Спосіб одержання ербуміну периндоприлу, що включає спосіб одержання кристалічного периндоприлу за будь-яким з пп. 1-19.
28. Застосування солі трет-октиламонію і периндоприлу або солі неопентиламонію і периндоприлу для одержання ербуміну периндоприлу.
29. Фармацевтична композиція, що містить терапевтично ефективну кількість солі неопентиламонію і периндоприлу, солі трет-октиламонію і периндоприлу або високоочищеного кристалічного периндоприлу, хроматографічна чистота якого складає, принаймні, 99 %, в суміші з одним або більшою кількістю фармацевтично прийнятних носіїв або інших ексципієнтів.
30. Фармацевтична композиція, що включає комплекси включення солі неопентиламонію і периндоприлу, солі трет-октиламонію і периндоприлу або високоочищеного кристалічного периндоприлу, хроматографічна чистота якого складає принаймні 99 %, з циклодекстринами або їх алкілованими і гідроксіалкілованими похідними, в суміші з одним або більшою кількістю фармацевтично прийнятних носіїв або інших ексципієнтів.
31. Застосування солі неопентиламонію і периндоприлу, солі трет-октиламонію і периндоприлу або високоочищеного кристалічного периндоприлу, хроматографічна чистота якого складає принаймні 99 %, для одержання фармацевтичної композиції, призначеної для використання при лікуванні серцево-судинних захворювань.
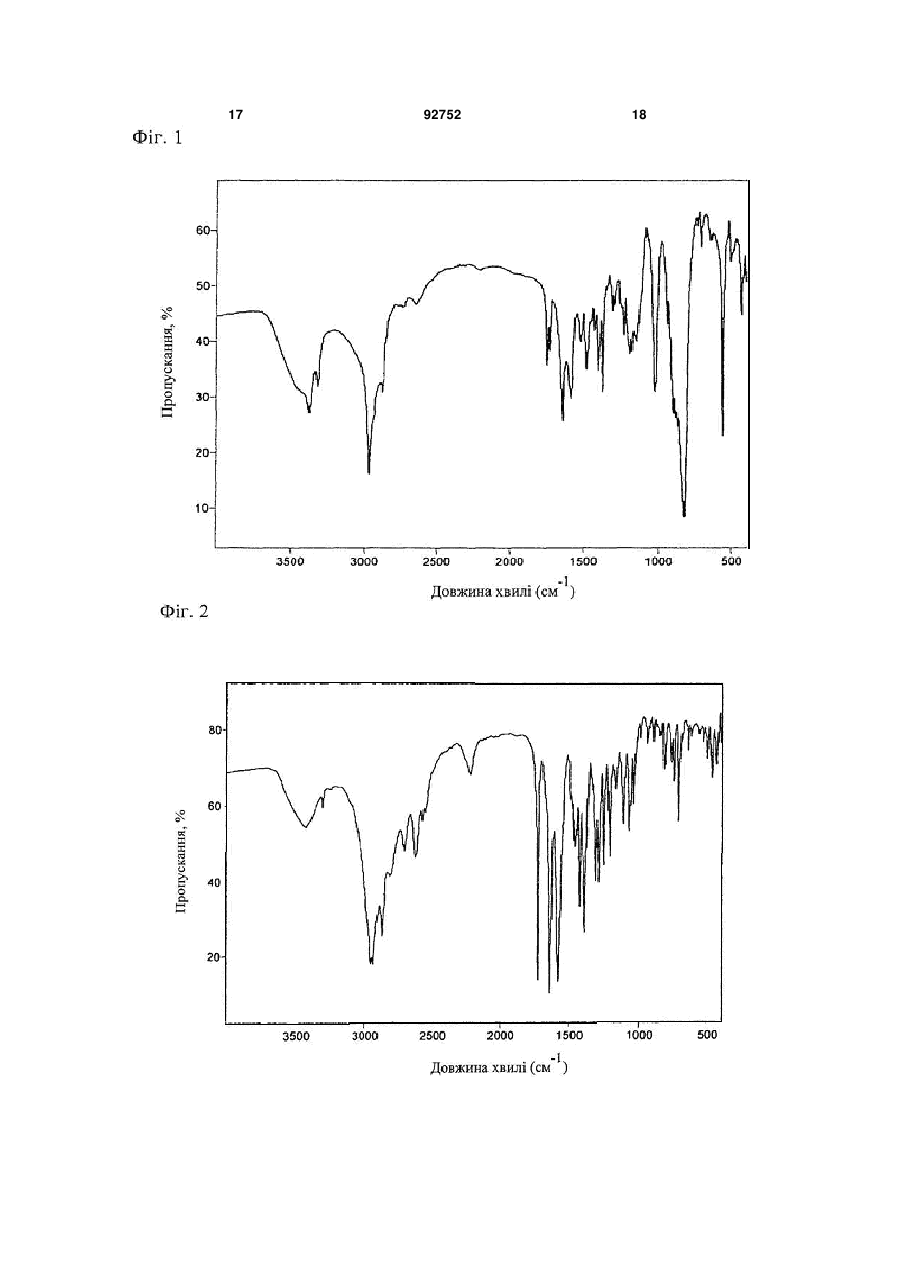
Текст
1. Спосіб одержання кристалічного периндоприлу, що включає наступні стадії: (a) перетворення неочищеного периндоприлу на сіль алкіламонію, яку вибирають з групи, що включає сіль трет-октиламонію і периндоприлу та сіль неопентиламонію і периндоприлу, та (b) одержання периндоприлу з вказаних солей алкіламонію і виділення кристалічного периндоприлу. 2. Спосіб за п. 1, в якому вказаною сіллю алкіламонію і периндоприлу є сіль трет-октиламонію і периндоприлу. 3. Спосіб за п. 1, в якому вказаною сіллю алкіламонію і периндоприлу є сіль неопентиламонію і периндоприлу. 4. Спосіб за п. 1, в якому стадія (а) включає наступні підстадії: (а1) розчинення неочищеного периндоприлу в органічному розчиннику або в суміші органічних розчинників, або в суміші органічного розчинника і води, (а2) додавання аміну, вибраного з групи, що включає трет-октиламін та неопентиламін, (а3) необов'язкове охолодження одержаного розчину до температури менше 40 °С, та 2 (19) 1 3 92752 4 13. Спосіб за п. 9, в якому органічний розчинник 22,22 33,41 для використання на підстадії (bі5) вибирають з 22,72 54,67 групи, що включає прості ефіри або вуглеводні. 23,98 34,82 14. Спосіб за п. 9, в якому органічним розчинником 26,40 45,04 для використання на підстадії (bі5) є гексан. 26,87 19,08 15. Спосіб за п. 1, в якому стадія (b) включає підс23. Кристалічна сіль трет-октиламонію і периндоптадії: рилу, яка характеризується порошковою рентгено(bii1) розчинення солі трет-октиламонію і периндограмою, як показано на Фіг. 3. прилу, одержаної на стадії (а), в органічному роз24. Спосіб одержання солі трет-октиламонію і печиннику, риндоприлу, що включає наступні стадії: (bіі2) видалення катіону трет-октиламонію з одер(а1) розчинення неочищеного периндоприлу в оржаного розчину, і ганічному розчиннику або в суміші органічних роз(bіі3) випарювання вказаного органічного розчинчинників, або в суміші органічного розчинника і ника, при цьому одержують кристалічний периндоводи, прил. (а2) додавання трет-октиламіну, 16. Спосіб за п. 1, в якому стадія (b) включає підс(а3) необов'язкове охолодження одержаного розтадії: чину до температури менше 40 °С, і (bii1) розчинення солі трет-октиламонію і периндо(а4) відділення одержаного осаду. прилу, одержаної на стадії (а), в органічному роз25. Сіль неопентиламонію і периндоприлу. чиннику, 26. Спосіб одержання солі неопентиламонію і пе(bіі2) обробка одержаного розчину, принаймні, риндоприлу, що включає наступні стадії: однією кислотою, з подальшим видаленням одер(а1) розчинення неочищеного периндоприлу в оржаної нерозчинної солі трет-октиламонію, і ганічному розчиннику або в суміші органічних роз(bіі3) випарювання вказаного органічного розчинчинників, або в суміші органічного розчинника і ника, при цьому одержують кристалічний периндоводи, прил. (а2) додавання неопентиламіну, 17. Спосіб за п. 15 або п. 16, в якому вказаний ор(а3) необов'язкове охолодження одержаного розганічний розчинник, використовуваний на підстадії чину до температури менше 40 °С, і (bii1), вибирають з групи, що включає спирти, аце(а4) відділення одержаного осаду. тонітрил та етилацетат. 27. Спосіб одержання ербуміну периндоприлу, що 18. Спосіб за п. 15 або п. 16, в якому вказаним включає спосіб одержання кристалічного периндоорганічним розчинником, використовуваним на прилу за будь-яким з пп. 1-19. підстадії (bii1), є ізопропанол. 28. Застосування солі трет-октиламонію і перин19. Спосіб за п. 16, в якому вказаною кислотою, доприлу або солі неопентиламонію і периндоприлу використовуваною на підстадії (bіі2), є сірчана кидля одержання ербуміну периндоприлу. слота. 29. Фармацевтична композиція, що містить тера20. Спосіб за будь-яким з пп. 1-19, в якому на допевтично ефективну кількість солі неопентиламодатковій стадії периндоприл, одержаний на стадії нію і периндоприлу, солі трет-октиламонію і пери(b), або його нові солі алкіламонію, одержані на ндоприлу або високоочищеного кристалічного стадії (а), переробляють у фармацевтично прийнпериндоприлу, хроматографічна чистота якого ятну лікарську форму. складає, принаймні, 99 %, в суміші з одним або 21. Сіль трет-октиламонію і периндоприлу. більшою кількістю фармацевтично прийнятних 22. Кристалічна сіль трет-октиламонію і периндопносіїв або інших ексципієнтів. рилу, яка характеризується порошковою рентгено30. Фармацевтична композиція, що включає комграмою з наступними характеристичними кутами плекси включення солі неопентиламонію і перин2θ: доприлу, солі трет-октиламонію і периндоприлу Кут 2θ (°) Відносна інтенсивність (%) або високоочищеного кристалічного периндоприлу, хроматографічна чистота якого складає при5,76 61,42 наймні 99 %, з циклодекстринами або їх алкілова7,34 17,79 ними і гідроксіалкілованими похідними, в суміші з 9,68 50,79 одним або більшою кількістю фармацевтично при13,95 18,85 йнятних носіїв або інших ексципієнтів. 14,38 23,78 31. Застосування солі неопентиламонію і перин14,75 100,00 доприлу, солі трет-октиламонію і периндоприлу 15,35 43,69 або високоочищеного кристалічного периндопри16,52 73,52 лу, хроматографічна чистота якого складає при17,30 17,44 наймні 99 %, для одержання фармацевтичної ком19,44 41,22 позиції, призначеної для використання при 19,99 34,35 лікуванні серцево-судинних захворювань. 20,80 57,66 Дійсний винахід відноситься до нового способу одержання високоочищеного кристалічного перин доприлу. Дійсний винахід також відноситься до нових солей алкіламонію і периндоприлу. 5 92752 6 Периндоприл і його фармацевтично прийнятні промисловому масштабі і який дозволяє одержати солі відомі як інгібітори ангіотензин-конвертуючого високоочищений кінцевий продукт. ферменту і використовуються для лікування серУ дійсному винаході пропонується новий споцево-судинних захворювань, перш за все для лікусіб одержання кристалічного периндоприлу з вивання гіпертензії та серцевої недостатності. Перикористанням нових солей алкіламонію і периндопндоприл (2S,3aS,7aS)((2-(1-(етоксикарбоніл)-(S)рилу, які вибирають з групи, що включає солі третбутиламіно)-(S)-пропіоніл)октагідроіндол-2октиламонію і периндоприлу і неопентиламонію і карбонова кислота, характеризується формулою периндоприлу. (І) Спосіб за дійсним винаходом дозволяє усунути недоліки, відомі в попередньому рівні техніки, тобто виключити стадію фільтрації через колонку, і дозволяє одержувати кристалічний периндоприл формули (І) високої хроматографічної чистоти в промисловому масштабі. Перший об'єкт дійсного винаходу відноситься до способу одержання кристалічного периндоприлу, хроматографічна чистота якого переважно складає, принаймні, 99%, причому спосіб включає наступні стадії: (a) перетворення неочищеного периндоприлу на сіль алкіламонію, яку вибирають з групи, що Периндоприл вперше був описаний в патентах включає солі трет-октиламонію і периндоприлу і ЕР 0049658 В1 і US 4508729 у формі оптично чиснеопентиламонію і периндоприлу, і того S,S,S,S,S-ізомepy і у формі натрієвої солі. (b) одержання периндоприлу з вказаних солей Потім в численних патентах і заявках, таких як ЕР алкіламонію і периндоприлу і виділення кристаліч0308341 В1, ЕР 1279665 А1, WO 2004/099236 опиного периндоприлу. сані різні способи одержання периндоприлу. Згідно переважного способу за дійсним винаНесольова форма периндоприлу є маслоподіходом стадія (а) включає наступні підстадії: бним, аморфним або, в основному, не кристаліч(а1) розчинення неочищеного периндоприлу в ним матеріалом залежно від використовуваного органічному розчиннику або в суміші органічних способу одержання і присутності домішок. До терозчинників, або в суміші органічного розчинника і перішнього часу тільки сіль трет-бутиламіну і певоди, риндоприлу, тобто ербумін периндоприлу, вперше (а2) додавання аміну, вибраного з групи, що описана в патенті ЕР 0308341, характеризується включає трет-октиламін і неопентиламін, достатньо високими кристалічними властивостя(а3) необов'язкове охолодження одержаного ми, що дозволяє використовувати її у фармацеврозчину до температури менше 40°С, і тиці (тобто характеризується певними і стабільни(а4) відділення одержаного осаду. ми фізичними властивостями). У патентах ЕР Органічний розчинник, використовуваний для 1296947 В1, ЕР 1294689 А і ЕР 1296948 В1 предпідстадії (а1), наприклад, вибирають з групи, що ставлені відповідно -, - і -кристалічні форми включає складні ефіри, нітрили, кетони, прості ербуміну периндоприлу. У заявці WO 2004/113293 ефіри, хлоровані вуглеводні і С4-С8-алкілові спирти описані - і -кристалічні форми ербуміну периндоабо їх суміші. Переважними розчинниками для прилу і в заявці WO 2004/046172 описаний моногівикористання на підстадії (a1) є складні ефіри або драт ербуміну периндоприлу. нітрили. Переважнішими розчинниками для викоСлід також згадати документи попереднього ристання на підстадії (a1) є ізопропілацетат, етирівня техніки, в яких описані способи одержання лацетат або ацетонітрил. очищеного ербуміну периндоприлу. Наприклад, в Найбільш переважним розчинником для викозаявці WO 2005/019173 описаний спосіб одержанристання на підстадії (a1) для одержання солі ня очищеного ербуміну периндоприлу екстракцією трет-октиламонію і периндоприлу є ацетонітрил, водного розчину периндоприлу або його солі відперш за все ацетонітрил, що містить невелику повідним органічним розчинником при рН від 4,0 кількість води, переважно до 5мас.% води, передо 6,5, з подальшим відділенням органічного шару важніше від приблизно 0,5мас.% до приблизно і одержанням ербуміну периндоприлу при дода3,5мас.% води. ванні трет-бутиламіну. Проте, ні у вказаному, ні в Найбільш переважним розчинником для викобудь-якому іншому опублікованому документі пористання на підстадії (a1) для одержання солі непереднього рівня техніки не описано виділення опентиламонію і периндоприлу є етилацетат. кристалічного периндоприлу. Розчин, одержаний на підстадії (a1), необов'яКристалічний периндоприл і спосіб його одерзково фільтрують перед додаванням аміну на піджання описані тільки в заявці РСТ/ЕР/2005/00283. стадії (а2) з метою видалення можливих нерозЗгідно вказаного способу, неочищений периндопчинних домішок. рил очищають методом фільтрації через колонку. Амін, використовуваний на підстадії (а2), можПроте фільтрація через колонку є непридатною на додавати однією порцією, декількома порціями для масштабування в промисловості. або по краплях в нерозбавленій або розчиненій У зв'язку з цим існує необхідність в розробці формі, переважно при температурі від приблизно вдосконаленого способу одержання кристалічного 20°С до температури кипіння використовуваного периндоприлу, який можна використовувати в органічного розчинника. Переважно амін додають 7 92752 8 при температурі від приблизно 30°С до приблизно тить оцтову кислоту і соляну кислоту. На стадії 40°С. Аміни додають в надлишку в співвідношенні (bі2) переважного додають кислоту і початкову від приблизно 1:1,1 до приблизно 1:5 екв., пересіль алкіламонію і периндоприлу в кількості від важно від приблизно 1:1,5 до приблизно 1:3 екв. приблизно 1 до приблизно 4 екв., переважніше від На підстадії (a3) розчин переважно охолоджуприблизно 1 до приблизно 2 екв., найпереважніше ють до температури менше 20°С. Розчин, що місвід приблизно 1,05 до приблизно 1,15 екв. кислоти тить трет-октиламін, переважніше охолоджують до на 1 екв. початкової солі. температури менше 10°С, найпереважніше до 0°С. Суспензію, одержану на підстадії (bі2), необоПереважніше розчин, що містить неопентилав'язково нагрівають до температури від приблизно мін, охолоджують до температури менше 0°С, 30°С до приблизно 50°С, переважно до приблизно найпереважніше до -10°С. 35°С, при цьому одержують розчин солі алкіламоНа підстадії (а4) осад переважно відокремлюнію і периндоприлу. ють фільтруванням. Органічний розчинник для використання на Фільтрування осаду на підстадії (а4) переважстадії (bі3) переважно вибирають з групи, що но проводять протягом від приблизно 0,5 до прибвключає складні ефіри, хлоровані вуглеводні, пролизно 24 год. після завершення підстадії (a3), песті ефіри або ароматичні вуглеводні, переважніреважніше протягом від приблизно 2 до приблизно шим органічним розчинником на стадії (bі3) є ети6 год. після завершення підстадії (a3). лацетат або дихлорометан, найбільш переважним Осад, одержаний на підстадії (а4), необов'язє дихлорометан. ково перекристалізовують перед проведенням Органічний розчинник для використання на стадії (b). Перекристалізацію необов'язково простадії (bi5) переважно вибирають з групи, що водять в одному і тому ж розчиннику, що і на стадії включає прості ефіри або вуглеводні, переважні(а) або в іншому розчиннику, який вибирають з шим органічним розчинником на стадії (bі5) є діегрупи, що включає складні ефіри, нітрили, кетони, тиловий ефір або гексан, найбільш переважним є прості ефіри, хлоровані вуглеводні і С4-С8-алкілові гексан. спирти або їх суміші з водою. Переважно як розУ першому переважнішому варіанті способу чинники для перекристалізації використовують (bі) за дійсним винаходом пропонується стадія (b), складні ефіри, нітрили, їх суміші або їх суміші з що включає наступні підстадії: водою. Найбільш переважною для перекристалі(bi1') розчинення солі трет-октиламонію і пезації є суміш ацетонітрилу з водою. риндоприлу, одержаної на стадії (а), у водному Згідно переважнішого способу за дійсним вирозчині хлориду натрію, находом, що забезпечує відмінні результати, про(bі2') підкислення одержаного водного розчину понується стадія (а), що включає наступні підстадо рН, при якому периндоприл знаходиться у фодії: рмі вільної кислоти, при додаванні суміші оцтової (а1') розчинення неочищеного периндоприлу в кислоти і соляної кислоти, ацетонітрилі, що містить переважно невелику кіль(bі3') екстракція одержаного периндоприлу з кість води, переважно до 5мас.% води, переважводної фази дихлорометаном, ніше від 0,5мас.% до 3,5мас.% води, (bі4') випарювання дихлорометану, (а2') додавання трет-октиламіну, переважно (bі5') обробка одержаного залишку гексаном, при 40°С, (bі6') відділення одержаного осаду фільтру(а3') охолодження одержаного розчину до теванням і виділення кристалічного периндоприлу. мператури менше 10°С, переважно до 0°С, і У другому переважному варіанті способу (bіі) (а4') відділення одержаного осаду фільтруза дійсним винаходом пропонується стадія (b), що ванням. включає наступні підстадії: У першому переважному варіанті способу (bі) (bii1) розчинення солі трет-октиламонію і пеза дійсним винаходом пропонується стадія (b), що риндоприлу, одержаної на стадії (а), в органічному включає наступні підстадії: розчиннику, (bi1) розчинення солі алкіламонію і периндоп(bіі2) видалення катіону трет-октиламонію з рилу, одержаної на стадії (а), у воді або у водному одержаного розчину, і розчині хлориду натрію, (bіі3) випарювання вказаного органічного роз(bі2) підкислення одержаного водного розчину чинника, при цьому одержують кристалічний перидо рН, при якому периндоприл знаходиться у фондоприл. рмі вільної кислоти, переважно при додаванні, На підстадії (bii1) сіль трет-октиламонію і пепринаймні, однієї органічної або неорганічної кисриндоприлу переважно розчиняють в органічному лоти або їх суміші, розчиннику, який вибирають з групи, що включає (bі3) екстракція одержаного периндоприлу з спирти, ацетонітрил і етилацетат, переважно ізопводної фази органічним розчинником, ропанол. Одержану суміш необов'язково нагріва(bі4) випарювання вказаного органічного розють для повного розчинення солі алкіламонію і чинника, периндоприлу. (bі5) обробка одержаного залишку органічним На підстадії (bіі2) катіон трет-октиламонію перозчинником, реважно видаляють з розчину, одержаного на під(bі6) відділення одержаного осаду фільтрустадії (bii1), осадженням у формі нерозчинної солі, ванням і виділення кристалічного периндоприлу. яку потім відокремлюють фільтруванням. Для цьоНа підстадії (bі2) переважно додають суміш, го розчин, одержаний на підстадії (bii1), оброблящо включає С1-С6-алканову кислоту або сильну ють, принаймні, однією кислотою, що приводить неорганічну кислоту, переважніше суміш, що місдо утворення аніону у використовуваному розчин 9 92752 10 нику, який утворює нерозчинну сіль з катіоном як показано на Фіг. 3, з наступними характериститрет-октиламонію. Органічний розчинник на підсчними величинами кута 2 : тадії (bii1) переважно вибирають з групи, що включає спирт і етилацетат. На підстадії (bіі2) переважВідносна інтенсівність (%) Кут 2 (°) но використовують неорганічну кислоту. У 5,76 61,42 переважнішому варіанті на підстадії (bii1) як орга7,34 17,79 нічний розчинник використовують ізопропанол, а 9,68 50,79 на підстадії (bіі2) як кислоту використовують сірча13,95 18,85 ну кислоту. 14,38 23,78 На підстадії (bіі2) кислоту переважно додають 14,75 100,00 при температурі від приблизно 30°С до приблизно 15,35 43,69 40°С. 16,52 73,52 У другому переважнішому варіанті способу 17,30 17,44 (bіі) за дійсним винаходом пропонується стадія (b), 19,44 41,22 що включає наступні підстадії: 19,99 34,35 (bii1') розчинення солі трет-октиламонію і пе20,80 57,66 риндоприлу, одержаної на стадії (а), в органічному 22,22 33,41 розчиннику, 22,72 54,67 (bіі2') обробка одержаного розчину, принаймні, 23,98 34,82 однією кислотою, з подальшим видаленням одер26,40 45,04 жаної нерозчинної солі трет-октиламонію, і (bіі3') випарювання вказаного органічного роз26,87 19,08 чинника, при цьому одержують кристалічний периндоприл. Згідно способу за дійсним винаходом осаУ другому найбільш переважному варіанті дження нової солі алкіламонію і периндоприлу на способу (bіі) за дійсним винаходом пропонується стадії (а) забезпечує ефективність очищення пестадія (b), що включає наступні підстадії: риндоприлу. Очищення означає, що одержана сіль (bіі1') розчинення солі трет-октиламонію і петрет-октиламонію містить істотно менше домішок в риндоприлу, одержаної на стадії (а), в ізопропанопорівнянні з початковим матеріалом (тобто нелі, очищеним периндоприлом). Наприклад, очищення (bіі2') обробка одержаного розчину сірчаною периндоприлу повторною перекристалізацією солі кислотою з подальшим видаленням одержаного трет-октиламонію з ацетонітрилу, як описано в нерозчинного сульфату трет-октиламонію, прикладі 3 і показано в таблиці 2, дозволяє підви(bіі3') випарювання ізопропанолу, при цьому щити хроматографічну чистоту, яка складає від одержують кристалічний периндоприл. 72,5% до 99,8%. Кристалічний периндоприл, одержаний згідно Згідно способу за дійсним винаходом нову сіль способу за дійсним винаходом, є високоочищеним, алкіламонію і периндоприлу можна використовухроматографічна чистота якого складає, принаймвати для одержання високоочищеного ербуміну ні, 99%, і його можна використовувати для одерпериндоприлу, причому в першому варіанті вказажання високоочищеного ербуміну периндоприлу. ну сіль перетворюють на ербумін периндоприлу Хроматографічна чистота такого очищеного ербучерез кристалічний периндоприл, згідно способу міну периндоприлу складає більше 99,6%, переза дійсним винаходом як описано вище. У другому важно більше 99,8%. Способи одержання ербуміну варіанті розчин периндоприлу, одержаний на підспериндоприлу з периндоприлу відомі в попередтадіях (bі3), (bіі2) або (bіі2'), обробляють третньому рівні техніки. бутиламіном, при цьому одержують ербумін периДругий об'єкт дійсного винаходу відноситься ндоприлу у вигляді осаду. У третьому варіанті роздо нових солей алкіламонію і периндоприлу. При чин периндоприлу, одержаний на підстадіях (bі3), дослідженні солей периндоприлу і множини різних (bіі2) або (bіі2'), концентрують, одержаний конценкатіонів металів і органічного амонію несподівано трат розбавляють органічним розчинником, перебуло встановлено, що тільки дві солі периндоприважно етилацетатом, і одержаний розчин оброблу, окрім солі трет-бутиламіну і периндоприлу, ляють трет-бутиламіном, при цьому одержують характеризуються задовільною негігроскопічністю і ербумін периндоприлу у вигляді осаду. певними фізичними властивостями. Ці солі вклюБільше того, нова сіль алкіламонію і периндочають сіль неопентиламонію і периндоприлу (тобприлу характеризується достатньо високою стабіто сіль 2,2-диметилпропіламонію і периндоприлу) і льністю при зберіганні протягом тривалого періоду сіль трет-октиламонію і периндоприлу (тобто сіль часу і може використовуватися у фармацевтичних 2,4,4-триметил-2-пентиламонію і периндоприлу). композиціях. Вказані нові солі одержують на стадії (а) згідно Інший варіант здійснення дійсного винаходу способу за дійсним винаходом, як описано вище. відноситься до способу, описаного вище, в якому Нові солі алкіламонію і периндоприлу за дійсна додатковій стадії периндоприл, одержаний на ним винаходом виділяють в кристалічному стані з стадії (b), або його нові солі алкіламонію, одержані певними характеристиками, що спрощує подальшу на стадії (а), переробляють у фармацевтично приобробку. Наприклад, сіль трет-октиламонію і перийнятні лікарські форми, перш за все в пігулки, піндоприлу характеризується визначуваною темпелюлі, капсули або ін'єкційні препарати. ратурою плавлення, порошковою рентгенограмою, Інший об'єкт дійсного винаходу відноситься до способів одержання солі неопентиламонію і пери 11 92752 12 ндоприлу і/або солі трет-октиламонію і периндопциклодекстрини і їх алкіловані або гідроксиалкілорилу, що включає стадію (а), згідно способу за вані похідні, переважніше комплекси включення дійсним винаходом, описаного вище. гідроксипропіл- -циклодекстрину. Переважний спосіб одержання солі неопенти"Терапевтично ефективна кількість" солі периламонію і периндоприлу включає наступні стадії: ндоприлу означає кількість солі периндоприлу, що (a1) розчинення неочищеного периндоприлу в включає кількість периндоприлу у складі лікарської органічному розчиннику або в суміші органічних форми, призначеної для лікування гіпертензії або розчинників, або в суміші органічного розчинника і серцево-судинних захворювань. Зазвичай, фарводи, мацевтично ефективна кількість периндоприлу (а2) додавання неопентиламіну, складає від 1 до 15 мг, переважно від 2 до 8 мг. (a3) необов'язкове охолодження одержаного Фармацевтично прийнятні ексципієнти вибирозчину до температури менше 40°С, і рають з групи, що включає зв'язуючі агенти, роз(а4) відділення одержаного осаду. чинники, дезінтегруючі агенти, стабілізатори, конУмови проведення стадій (a1), (а2), (a3) і (а4) серванти, замаслювані, ароматизатори, смакові детально описані вище. добавки, підсолоджувачі та інші ексципієнти, викоПереважний спосіб одержання солі третристовувані у фармацевтиці. Переважно носії та октиламонію і периндоприлу включає наступні ексципієнти вибирають з групи, що включає гідростадії: ксипропілцелюлозу, лактозу, мікрокристалічну це(a1) розчинення неочищеного периндоприлу в люлозу, карбонат кальцію, крохмаль, колоїдний органічному розчиннику або в суміші органічних діоксид кремнію, натрієву сіль гліколяту крохмалю, розчинників, або в суміші органічного розчинника і тальк, стеарат магнію, полівінілпіролідон та інші води, ексципієнти, прийнятні у фармацевтиці. (а2) додавання трет-октиламіну, Фармацевтичні композиції за дійсним винахо(a3) необов'язкове охолодження одержаного дом необов'язково можуть містити комбіновані розчину до температури менше 40°С, і продукти, що включають один або більше інших (а4) відділення одержаного осаду. фармацевтично активних компонентів окрім периУмови проведення стадій (a1), (а2), (a3) і (а4) ндоприлу. Як додаткові фармацевтично активні детально описані вище. компоненти переважно використовують діуретики, Переважніший спосіб одержання солі третнаприклад, індапамід. октиламонію і периндоприлу включає наступні Придатними фармацевтичними композиціями стадії: є тверді лікарські форми, такі як пігулки з швидким (а1’) розчинення неочищеного периндоприлу в вивільненням і сповільненим вивільненням активацетонітрилі, що містить переважно невелику кільного компоненту, шипучі пігулки, диспергуючі пігукість води, переважно до 5мас.% води, переважлки і капсули. ніше від 0,5мас.% до 3,5мас.% води, Фармацевтичні композиції одержують метода(а2') додавання трет-октиламіну, переважно ми, відомими у фармацевтиці. при 40°С, Інший об'єкт дійсного винаходу відноситься до (а3') охолодження одержаного розчину до тезастосування солі неопентиламонію і периндопримператури менше 10°С, переважно до 0°С, і лу, солі трет-октиламонію і периндоприлу або ви(а4') відділення одержаного осаду фільтрусокоочищеного кристалічного периндоприлу, хрованням. матографічна чистота якого складає, принаймні, Інший об'єкт дійсного винаходу відноситься до 99%, для одержання фармацевтичної композиції, фармацевтичних композицій, що містять терапевпризначеної для лікування серцево-судинних затично ефективну кількість солі неопентиламонію і хворювань, наприклад, гіпертензії або серцевої периндоприлу, солі трет-октиламонію і периндопнедостатності. рилу або високоочищеного кристалічного перинЩе один об'єкт дійсного винаходу відноситься доприлу, хроматографічна чистота якого складає, до способу лікування серцево-судинних захворюпринаймні, 99%, в суміші з одним або більшою вань, наприклад, гіпертензії або серцевої недостакількістю фармацевтично прийнятних носіїв або тності, що включає введення пацієнтові, що потінших ексципієнтів. ребує такого лікування, терапевтично ефективної Ще один об'єкт дійсного винаходу відноситься кількості солі неопентиламонію і периндоприлу, до фармацевтичних композицій, що містять комсолі трет-октиламонію і периндоприлу або високоплекси включення солі неопентиламонію і периночищеного кристалічного периндоприлу, хроматодоприлу з циклодекстринами або їх алкілованими і графічна чистота якого складає, принаймні, 99%. гідроксиалкілованими похідними, комплекси вклюНаступні приклади представлені для ілюстрачення солі трет-октиламонію і периндоприлу з циції дійсного винаходу і не обмежують його об'єм. клодекстринами або їх алкілованими і гідроксиалНа Фіг. 1 представлений ІЧ-спектр солі неопекілованими похідними, або комплекси включення нтиламонію і периндоприлу. високоочищеного кристалічного периндоприлу, На Фіг. 2 представлений ІЧ-спектр солі третхроматографічна чистота якого складає, принаймоктиламонію і периндоприлу. ні, 99%, з циклодекстринами або їх алкілованими і На Фіг. 3 представлені дані рентгеноструктургідроксиалкілованими похідними, в суміші з одним ного аналізу солі трет-октиламонію і периндоприабо більшою кількістю фармацевтично прийнятних лу. носіїв або інших ексципієнтів. Циклодекстрини або Приклад 1 їх алкіловані і гідроксиалкіловані похідні переважОдержання неочищеного периндоприлу но вибирають з групи, що включає -, -, - і 13 92752 14 Суміш бензилового ефіру (2S,3аS,7аS)-2карбоксипергідроіндолу (9,54 г), N-((S)-1Таблиця 1 карбетоксибутил)-(S)-аланіну (7,26 г) і гексафторофосфату О-(бензотріазол-1-іл)-N,N,N',N'Відносна інтенсівність (%) Кут 2 (°) тетраметилуронію (12,7 г) в ацетонітрилі (225 мл) 5,76 61,42 перемішували при кімнатній температурі протягом 7,34 17,79 30 хв., потім додавали сольовий розчин (560 мл). 9,68 50,79 Продукт двічі екстрагували етилацетатом (по 400 13,95 18,85 мл), об'єднані екстракти промивали спочатку во14,38 23,78 дою (800 мл), підкисляли конц. соляною кислотою і 14,75 100,00 потім знову промивали водою (1,5 л). 15,35 43,69 Органічну фазу сушили над безводним суль16,52 73,52 фатом натрію і упарювали у вакуумі при 40°С, при 17,30 17,44 цьому одержували бензиловий ефір (2S,3aS,7aS)19,44 41,22 ((2-(1-(етоксикарбоніл)-(S)-бутиламіно)-(S)19,99 34,35 пропіоніл)октагідроіндол-2-карбонової кислоти 20,80 57,66 (бензиловий ефір периндоприлу) (13,5 г, 88%). 22,22 33,41 Неочищений бензиловий ефір периндоприлу 22,72 54,67 (13,5 г) розчиняли в метанолі (300 мл), в одержа23,98 34,82 ний розчин додавали каталізатор (10% паладій на 26,40 45,04 вугіллі, 1,35 г). Суміш перемішували при помірній 26,87 19,08 швидкості потоку водню при кімнатній температурі протягом ще 5 год. Потім каталізатор фільтрували, У таблиці 2 представлений ступінь очищення промивали метанолом (50 мл) і розчин упарювали периндоприлу, одержаного згідно способу, описау вакуумі при 50°С. Неочищений периндоприл ного в прикладі 3, тобто хроматографічна чистота, одержували у вигляді прозорого безбарвного масрозрахована за площею піку (у %) ла (72,5% периндоприлу, розраховано за площею піку). Таблиця 2 Приклад 2 Одержання солі неопентиламонію і периндоприлу ((2S,3aS,7aS)-((2-(1-(етоксикарбоніл)-(S)Хроматографічна бутиламіно)-(S)-пропіоніл)октагідроіндол-2чистота (%, за карбоксилат 2,2-диметилпропіламонію) площею піку) Неочищений периндоприл (2,85 г), одержаний, Неочищений периндоприл 72,5 як описано в прикладі 1, розчиняли в етилацетаті Неочищена сіль трет98,7 (30 мл), потім розчин нагрівали до 35°С і додавали октиламонію і периндоприлу неопентиламін (2,4 мл). Суміш охолоджували до Крісталічна сіль трет99,8 10°С і через 24 год. осад відокремлювали фільтоктиламонію і периндоприлу руванням і сушили. Одержували сіль неопентиламонію і периндоприлу (2,23 г, 63%). tпл.: 80-130°С Приклад 4 (розкл.) - мікроскоп Кофлера, 85°С (початок плавОдержання солі трет-октиламонію і периндоплення) (метод диференціальної скануючої калорилу риметрії, ДСК). ІЧ-спектр представлений на Фіг. 2. Периндоприл (13,6 г, вміст 91%), одержаний, Приклад 3 як описано в прикладі 1, розчиняли в ацетонітрилі Одержання солі трет-октиламонію і периндоп(200 мл) і при перемішуванні додавали воду (1,25 рилу ((2S,3aS,7aS)-((2-(1-(етоксикарбоніл)-(S)мл). Потім розчин нагрівали до 40°С і додавали бутиламіно)-(S)-пропіоніл)октагідроіндол-2трет-октиламін (8,0 мл), повільно нагрівали до текарбоксилат 2,2,4-триметил-2-пентиламонію) мператури кипіння суміші і, нарешті, охолоджували Неочищений периндоприл (26,3 г), одержаний, до 0°С. Після витримки протягом 6 год. при 0°С як описано в прикладі 1, розчиняли в ацетонітрилі осаджені кристали відокремлювали фільтруван(300 мл), потім розчин нагрівали до 40°С і додаваням і сушили, при цьому одержували сіль (13,1 г, ли трет-октиламін (21 мл). При утворенні перших 78%). кристалів в суміш додавали воду (2,5 мл) і суміш Приклад 5 нагрівали до температури кипіння до розчинення Одержання очищеного периндоприлу кристалів. Потім розчин охолоджували до 0°С і ((2S,3aS,7aS)-((2-(1-(етоксикарбоніл)-(S)через 4 год. осад солі трет-октиламонію відокрембутиламіно)-(S)-пропіоніл)октагідроіндол-2лювали фільтруванням і сушили. При цьому одеркарбонової кислоти) з солі трет-октиламонію і пежували неочищену сіль (21 г, 59%), яку перекрисриндоприлу талізовували з суміші ацетонітрилу (300 мл) і води Сіль трет-октиламонію і периндоприлу (8,11 г), (10 мл), при цьому одержували очищену кристаліодержану, як описано в прикладі 4, суспендували чну сіль (вихід після кристалізації 85%). tпл.: 154°С в ізопропанолі (100 мл), суміш нагрівали до 60°С, (розкл.) - (початок плавлення, ДСК). ІЧ-спектр при цьому одержували розчин, який потім охолопредставлений на Фіг. 2. джували до 25°С і по краплях додавали сірчану На Фіг. 3 зображена порошкова рентгеногракислоту (936 мг, 96%, d 1,84). Одержану суміш ма, на якій спостерігаються наступні характерисперемішували протягом 30 хв. при кімнатній темтичні величини кутів 2 : пературі і осад відокремлювали фільтруванням. 15 92752 16 Фільтрат упарювали досуха при 45°С, залишок тиском і охолоджували до кімнатної температури. розтирали в діізопропіловому ефірі (15 мл) і знову Осад відокремлювали фільтруванням і сушили у упарювали досуха. Розтирання повторювали двічі, вакуумі, при цьому одержували ербумін периндоппри цьому одержували в'язку масу, яку сушили рилу (1,12 г, 99,83% за площею піку). протягом 30-60 хв. при кімнатній температурі у Аналіз одержаних в експериментах продуктів високому вакуумі, при цьому одержували очищепроводили з використанням наступного устаткуний периндоприл (6,0 г, 100%) у вигляді твердого вання: склоподібного матеріалу (вміст 97%). Температуру плавлення визначали на мікросПриклад 6 копі Кофлера і диференціальному скануючому Одержання кристалічного периндоприлу з солі калориметрі Mettler Toledo DSC822e. трет-октиламонію і периндоприлу ІЧ-спектри реєстрували на спектрофотометрі Сіль трет-октиламонію і периндоприлу (994 Nicolet Nexus FTIR (пігулки KВr). мг), одержану, як описано в прикладі 4, суспендуПорошкові рентгенограми зразків одержували вали в розчині NaCl (32 мл, 10%), потім додавали на приладі Siemens D-5000, метод віддзеркаленоцтову кислоту (0,56 мл) і суміш конц. НСІ/вода, ня: випромінювання СuK , діапазон кута 2 від 2° 1:1 (0.30 мл). Суспензію нагрівали до 35°С протядо 37°, крок 0,04° 2 , час інтегрування 1 с. гом 10 хв., при цьому одержували розчин солі і Умови хроматографії: одержаний розчин двічі екстрагували дихлоромеРухома фаза: таном (по 20 мл). Об'єднані екстракти знову проА: гептансульфонат натрію (0,92 г) розчиняли мивали двічі 10% розчином NaCl (по 40 мл). Потім у воді (1000 мл), додавали триметиламін (1 мл) і дихлорометан видаляли при упарюванні, залишок доводили до рН 2,0 додаванням суміші хлорної обробляли гексаном (10 мл), суміш перемішували кислоти і води, протягом 5 год. і тверду речовину відокремлювали В: ацетонітрил, фільтруванням, при цьому одержували кристалічКолонка: С8, 4 мкм, розмір пор 6 нм, 250 4,0 ний периндоприл (655 мг, 99,1%). mm (Merck Supersphere 60 RP-8), Приклад 7 температура: 70°С, Одержання ербуміну периндоприлу з солі швидкість потоку: 1,5 мл/хв., трет-октиламонію і периндоприлу довжина хвилі: 215 нм, Сіль трет-октиламонію і периндоприлу (5,0 г), об'єм проби: 20 мкл. одержану, як описано в прикладі 4, розчиняли в Градієнт: етилацетаті (150 мл) і воді (3 мл), суміш нагрівали до кипіння, при цьому одержували розчин, який t %А %В потім охолоджували до 55°С і по краплях додава0 73 27 ли сірчану кислоту (564 мг, 96%, d 1,84). Одержану 8 73 27 суспензію охолоджували до кімнатної температу25 40 60 ри, і осаджений сульфат відокремлювали фільтру30 40 60 ванням. Фільтрат упарювали досуха при темпера40 20 80 турі менше 45°С і залишок сушили у високому 45 0 100 вакуумі (1 мбар), при цьому одержували очищений 50 73 27 периндоприл (3,55 г). Залишок (вміст периндоприлу 97,96% за плоУстаткування: хроматографічна система щею піку, 1,49 г) розчиняли в етилацетаті (18 мл), Waters Alliance 2695, детектор PDA 2996, програмдодавали трет-бутиламін (1,0 мл). Суміш нагріване забезпечення Empower 5.0. ли до кипіння, гарячий розчин фільтрували під 17 92752 18 19 Комп’ютерна верстка О. Гапоненко 92752 Підписне 20 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of crystalline perindopril
Автори англійськоюJenko Branko, Copar Anton
Назва патенту російськоюСпособ получения кристаллического периндоприла
Автори російськоюЭнко Бранко, Копар Антон
МПК / Мітки
МПК: A61K 31/404, A61P 9/00, C07K 1/00, C07D 209/42
Мітки: кристалічного, периндоприлу, одержання, спосіб
Код посилання
<a href="https://ua.patents.su/10-92752-sposib-oderzhannya-kristalichnogo-perindoprilu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання кристалічного периндоприлу</a>
Попередній патент: Спосіб видалення оксиду титану та заліза з руди
Наступний патент: Спосіб виготовлення магнітної рідини
Випадковий патент: Циклон з вхідними трубопроводами