Похідна піролідиндикарбонової кислоти та її застосування у лікуванні проліферативних захворювань
Номер патенту: 104147
Опубліковано: 10.01.2014
Автори: Фуре Паскаль, Фейрхерст Робін Алек, Караватті Джорджо, Імбах Патриція, Гуаньяно Віто
Формула / Реферат
1. Сполука, яка являє собою 2-амід 1-({4-метил-5-[2-(2,2,2-трифтор-1,1-диметилетил)піридин-4-іл]тіазол-2-іл}амід) (S)-піролідин-1,2-дикарбонової кислоти, структури:
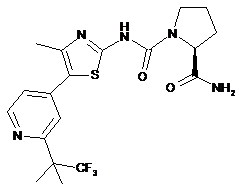 ,
,
у вільній формі або у формі фармацевтично прийнятної солі.
2. Сполука за п. 1 у вільній формі або у формі фармацевтично прийнятної солі для застосування як лікарського засобу.
3. Сполука за п. 1 або її фармацевтично прийнятна сіль для застосування у лікуванні проліферативного захворювання; доброякісної або злоякісної пухлини; раку, вибраного з групи, що включає саркому, рак легенів, бронхів, передміхурової залози, молочної залози (включаючи спорадичні типи раку молочної залози та страждаючих хворобою Коудена), підшлункової залози, шлунково-кишковий рак, товстої кишки, прямої кишки, карциноми товстої кишки, колоректальної аденоми, щитовидної залози, печінки, внутріпечінкової жовчної протоки, гепатоцелюлярний рак, наднирників, шлунка, шлунково-кишкового тракту, гліоми, гліобластоми, ендометрія, меланоми, нирок, ниркової миски, сечового міхура, тіла матки, шийки матки, піхви, яєчників, множинної мієломи, стравоходу, лейкозу, гострого мієлолейкозу, хронічного мієлолейкозу, лімфолейкозу, мієлолейкозу, головного мозку, карциноми головного мозку, порожнини рота та глотки, гортані, тонкого кишечнику, неходжкінської лімфоми, меланоми, ворсинчастої аденоми товстої кишки, неоплазії, неоплазії епітеліального характеру, лімфом, карциноми молочної залози, базально-клітинної карциноми, плоскоклітинної карциноми, старечого кератозу, пухлинних захворювань, включаючи солідні пухлини, пухлину голови або шиї, справжньої поліцитемії, есенціальної тромбоцитемії, мієлофіброзу з мієлоїдною метаплазією та хвороби Вальденстрема.
4. Застосування сполуки за п. 1, у вільній формі або у формі фармацевтично прийнятної солі, для приготування лікарського засобу для лікування одного або більшої кількості з проліферативного захворювання; доброякісної або злоякісної пухлини; раку, вибраного з групи, що включає саркому, рак легенів, бронхів, передміхурової залози, молочної залози (включаючи спорадичні типи раку молочної залози та страждаючих хворобою Коудена), підшлункової залози, шлунково-кишковий рак, товстої кишки, прямої кишки, карциноми товстої кишки, колоректальної аденоми, щитовидної залози, печінки, внутріпечінкової жовчної протоки, гепатоцелюлярний рак, наднирників, шлунка, шлунково-кишкового тракту, гліоми, гліобластоми, ендометрія, меланоми, нирок, ниркової миски, сечового міхура, тіла матки, шийки матки, піхви, яєчників, множинної мієломи, стравоходу, лейкозу, гострого мієлолейкозу, хронічного мієлолейкозу, лімфолейкозу, мієлолейкозу, головного мозку, карциноми головного мозку, порожнини рота та глотки, гортані, тонкого кишечнику, неходжкінської лімфоми, меланоми, ворсинчастої аденоми товстої кишки, неоплазії, неоплазії епітеліального характеру, лімфом, карциноми молочної залози, базально-клітинної карциноми, плоскоклітинної карциноми, старечого кератозу, пухлинних захворювань, включаючи солідні пухлини, пухлину голови або шиї, справжньої поліцитемії, есенціальної тромбоцитемії, мієлофіброзу з мієлоїдною метаплазією та хвороби Вальденстрема.
5. Фармацевтична композиція, що містить сполуку за п. 1 у вільній формі або у формі фармацевтично прийнятної солі у терапевтично ефективній кількості та один або більшу кількість фармацевтично прийнятних інертних наповнювачів.
6. Фармацевтична композиція за п. 5 для застосування у лікуванні проліферативного захворювання; доброякісної або злоякісної пухлини; раку, вибраного з групи, що включає саркому, рак легенів, бронхів, передміхурової залози, молочної залози (включаючи спорадичні типи раку молочної залози та страждаючих хворобою Коудена), підшлункової залози, шлунково-кишковий рак, товстої кишки, прямої кишки, карциноми товстої кишки, колоректальної аденоми, щитовидної залози, печінки, внутріпечінкового жовчного протоку, гепатоцелюлярний рак, наднирників, шлунка, шлунково-кишкового тракту, гліоми, гліобластоми, ендометрію, меланоми, нирок, ниркової миски, сечового міхура, тіла матки, шийки матки, піхви, яєчників, множинної мієломи, стравоходу, лейкозу, гострого мієлолейкозу, хронічного мієлолейкозу, лімфолейкозу, мієлолейкозу, головного мозку, карциноми головного мозку, порожнини рота та глотки, гортані, тонкого кишечнику, неходжкінської лімфоми, меланоми, ворсинчастої аденоми товстої кишки, неоплазії, неоплазії епітеліального характеру, лімфом, карциноми молочної залози, базально-клітинної карциноми, плоскоклітинної карциноми, старечого кератозу, пухлинних захворювань, включаючи солідні пухлини, пухлину голови або шиї, справжньої поліцитемії, есенціальної тромбоцитемії, мієлофіброзу з мієлоїдною метаплазією та хвороби Вальденстрема.
Текст
Реферат: UA 104147 C2 (12) ОПИС ДО ПАТЕНТУ НА ВИНАХІД UA 104147 C2 Представлений винахід стосується сполуки формули (І) R 3 H N N S N O O NH2 A 1 R 2 R (I) або її солі, у якій замісники визначені в описі, композиції та застосування сполук для лікування захворювань, перебіг яких полегшується шляхом інгібування фосфатидилінозит-3-кінази. R 3 H N N S N O O N R 1 NH2 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід відноситься до особливих 2-карбоксамідциклоаміно-похідних сечовини як нових інгібіторів фосфатидилінозит (PI) 3-кінази-альфа, їх фармацевтично прийнятних солей, проліків та способів їх одержання. Даний винахід також відноситься до композицій цих сполук окремо або в комбінації щонайменше з одним додатковим терапевтичним засобом та необов'язково у комбінації з фармацевтично прийнятним носієм. Даний винахід також відноситься до способів застосування цих сполук окремо або в комбінації щонайменше з одним додатковим терапевтичним засобом для профілактики або лікування цілого ряду захворювань, переважно опосередкованих аномальною активністю однієї або більшої кількості наступних речовин: факторів росту, рецепторних тирозинкіназ, протеїнсерін/треонінкіназ, пов'язаних з білком G рецепторів та фосфоліпідкіназ та фосфатаз. Фосфатидилінозит-3-кінази (PI3K) являють собою сімейство ліпідних кіназ, які каталізують перенос фосфату в D-3’-положення інозитвмісних ліпідів з утворенням фосфоінозит-3-фосфату (PIP), фосфоінозит-3,4-дифосфату (PIP2) та фосфоінозит-3,4,5-трифосфату (PIP3), які, у свою чергу, діють як вторинні месенджери в каскадах передачі сигналів шляхом залучення білків, які містять гомологічні плекстрину FYVE, Phox та інші зв'язуючі фосфоліпіди домени, в різні передаючі сигнали комплекси, які часто є присутніми на плазматичній мембрані ((Vanhaesebroeck et al., Annu. Rev. Biochem 70:535 (2001); Katso et al., Annu. Rev. Cell Dev. Biol. 17:615 (2001)). Середовища PI3K, що належать до двох класів, які є підкласами класу 1, PI3K класу 1A являють собою гетеродимери, що складаються з каталітичної субодиниці p110 (ізоформи , , ), конститутивно асоційованої з регуляторною субодиницею, яка може являти собою p85, p55, p50, p85 або p55. Підклас, що являє собою клас 1B, складається з одного представника сімейства, а саме, гетеродимеру, який включає каталітичну субодиницю p110, асоційовану з двома регуляторними субодиницями p101 або p84 (Fruman et al., Annu Rev. Biochem. 67:481 (1998); Suire et al., Curr. Biol. 15:566 (2005)). Модулярні домени субодиниць p85/55/50 включають домени, гомологічні Src (SH2), які зв'язують залишки фосфотирозину в контексті специфічної послідовності на активованому рецепторі та цитоплазматичних тирозинкіназах, що приводить до активації та локалізації PI3K класу 1А. PI3K класу 1B активуються безпосередньо зшитими з протеїном G рецепторами, з якими зв'язується багато різнорідних пептидних та непептидних лігандів (Stephens et al., Cell 89:105 (1997)); Katso et al., Annu. Rev. Cell Dev. Biol. 17:615-675 (2001)). В результаті утворені фосфоліпідні продукти PI3K класу I зв'язують рецептори, розташовані вище в шляху передачі сигналу, з розташованими нижче в шляху передачі сигналу клітинними елементами, що роблять вплив на проліферацію, виживання, хемотаксис, направлену міграцію клітин, рухливість, метаболізм, запальні та алергійні відповіді, транскрипцію та трансляцію (Cantley et al., Cell 64:281 (1991); Escobedo and Williams, Nature 335:85 (1988); Fantl et al., Cell 69:413 (1992)). У багатьох випадках PIP2 та PIP3 приводять до рекрутменту Akt, людського продукту, гомологічного вірусному онкогену v-Akt, на плазматичній мембрані, де він діє як вузлова точка для багатьох внутріклітинних шляхів передачі сигналів, важливих для росту та виживання (Fantl et al., Cell 69:413-423(1992); Bader et al., Nat Rev. Cancer 5:921 (2005); Vivanco and Sawyer, Nat. Rev. Cancer 2:489 (2002)). Аномальна регуляція PI3K, яка часто підвищує виживання завдяки активації Akt, є одним з найбільш превалюючих явищ при раку у людини та, як встановлено, відбувається на декількох рівнях. У гена-супресора пухлин PTEN, який дефосфорилює фосфоінозитиди в 3’-положенні інозитного кільця та тому має здатність антагонізувати активність PI3K, у багатьох типах пухлин відсутня функціональна активність. В інших типах пухлин відбувається ампліфікація генів, кодуючих ізоформу p110, PIK3CA та Akt, та підвищений рівень експресії білкових продуктів цих генів був продемонстрований при деяких видах раку людини. Крім того, для деяких видів раку людини описані мутації та транслокації субодиниці p85, яка служить для підвищуючої регуляції комплексу p85-p110. Та, нарешті, встановлено, що соматичні міссенс-мутації PIK3CA, які активують шляхи подальшої передачі сигналу, достатньо часто зустрічаються при багатьох видах раку людини (Kang at el., Proc. Natl. Acad. Sci. USA 102:802 (2005); Samuels et al., Science 304:554 (2004); Samuels et al., Cancer Cell 7:561-573(2005)). Ці дані свідчать про те, що порушення регуляції фосфоінозит-3-кінази та компонентів, що знаходяться вище та нижче в цьому шляху передачі сигналу, є одним з найбільш розповсюджених видів порушення регуляції, асоційованих з раком та проліферативними захворюваннями людини (Parsons et al., Nature 436:792(2005); Hennessey at el., Nature Rev. Drug Dis. 4:988-1004 (2005)). Тому інгібітори PI3K-альфа повинні бути корисними для лікування проліферативного захворювання та інших порушень. В WO 2004/096797 розкриті деякі похідні тіазолу як інгібітори PI3K-гама та їх застосування як лікарські засоби, зокрема, для лікування запальних та алергійних патологічних станів. 1 UA 104147 C2 5 10 15 20 В WO 2005/021519 також розкриті деякі похідні тіазолу як інгібітори PI3K-гама та їх застосування як лікарські засоби, зокрема, для лікування запальних та алергічних патологічних станів. В WO 2006/051270 також розкриті деякі похідні тіазолу як інгібітори PI3K-альфа та їх застосування як лікарські засоби, зокрема, внаслідок їх протипухлинної активності. В WO 2007/129044 також розкриті деякі похідні тіазолу як інгібітори PI3K-альфа та їх застосування як лікарські засоби, зокрема, внаслідок їх протипухлинної активності. З урахуванням попереднього рівня техніки необхідно одержання додаткових сполук, застосовних для лікування проліферативних захворювань, зокрема, сполук, що мають покращену селективність та/або більшу/покращену активність. Згідно винаходу було встановлено, що 2-карбоксамідциклоамінопохідні сечовини формули (I), приведені нижче, мають сприятливі фармакологічні характеристики та інгібують, наприклад, PI3K (фосфатидилінозит-3-кіназа). Зокрема, за даними біохімічних та/або проведених з використанням клітин аналізів ці сполуки переважно мають високий ступінь селективності по відношенню до PI3K-альфа у порівнянні з селективністю по відношенню до підтипів бета та/або дельта, та/або гама. Тому сполуки формули I застосовні, наприклад, для лікування захворювань, що залежать від кіназ PI3 (переважно PI3K-альфа, таких як при яких спостерігаються надекспресування або ампліфікація PI3K-альфа, соматичні мутації PIK3CA або мутації зародкового типу або соматичні мутації PTEN або мутації та транслокації p85, які забезпечують підвищуючу регуляцію комплексу p85-p110), особливо проліферативних захворювань, таких як пухлинні захворювання та лейкози. Крім того, ці сполуки переважно мають покращену метаболічну стабільність та тому знижений кліренс, що приводить до покращених фармакокінетичних профілів. Першим об'єктом даного винаходу є сполуки формули (I) R3 H N N N S O O NH2 A R2 25 30 35 40 45 50 R1 (I) або їх солі, у якій A позначає гетероарил; 1 R позначає (1) необов'язково заміщений алкіл; (2) необов'язково заміщений циклоалкіл; (3) необов'язково заміщений арил; (4) необов'язково заміщений амін; (5) необов'язково заміщений сульфоніл; (6) галоген; 2 1 R позначає водень, дейтерій або замісник, визначений для R ; 3 R позначає водень, галоген, необов'язково заміщений алкіл; виключаючи 2-амід, 1-({5-[2-(трет-бутил)-піримідин-4-іл]-4-метилтіазол-2-іл}-амід) (S)піролідин-1,2-дикарбонової кислоти. Даний винахід можна краще зрозуміти за допомогою наведеного нижче опису, включаючи наведений нижче словник термінів та наступні приклади. Для стислості вкажемо, що розкриття та публікації, процитовані в даному описі, включені в даний винахід як посилання. При використанні в даному винаході терміни "включаючи", "що містить" та "що включає" застосовуються в широкому, не обмежувальному сенсі. Будь-яка формула, наведена в даному винаході, призначена для опису сполук, що мають структуру, представлену структурною формулою, а також деяких їх варіантів та форм. Зокрема, сполуки будь-якої формули, наведеної в даному винаході, можуть містити асиметричні центри та тому існувати в різних енантіомерних формах. Якщо в сполуці формули (I) міститься щонайменше один асиметричний атом вуглецю, то така сполука може існувати в оптично активній формі або у вигляді суміші оптичних ізомерів, наприклад, у вигляді рацемічної суміші. Усі оптичні ізомери та їх суміші, включаючи рацемічні суміші, входять в обсяг даного винаходу. Таким чином, будь-яка конкретна формула, наведена в даному винаході, означає рацемат, одну або більшу кількість енантіомерних форм, одну або більшу кількість діастереоізомерних форм, одну або більшу кількість атропоізомерних форм та їх сумішей. Крім того, деякі структури можуть існувати у вигляді геометричних ізомерів (тобто цис- та транс-ізомерів), у вигляді таутомерів або у вигляді атропоізомерів. 2 UA 104147 C2 5 10 15 20 25 30 35 4045 50 55 Будь-яка формула, наведена в даному винаході, характеризує гідрати, сольвати та поліморфні форми таких сполук та їх суміші. Будь-яка формула, наведена в даному винаході, також характеризує немічені форми, а також ізотопно-мічені форми сполук. Ізотопно-мічені сполуки мають структури, що описуються формулами, наведеними в даному винаході, за виключенням того, що один або більша кількість атомів замінені на атоми, що мають зазначені атомні маси або масові числа. Приклади ізотопів, які можна вводити в сполуки, запропоновані в даному винаході, включають ізотопи водню, 2 3 11 13 14 15 18 31 вуглецю, азоту, кисню, фосфору, сірки, фтору та хлору, такі як H, H, C, C, C, N, F P, 32 35 36 125 P, S, Cl, I, відповідно. В обсяг даного винаходу входять різні ізотопно-мічені сполуки, 3 13 запропоновані в даному винаході, наприклад, у які включені радіоактивні ізотопи, такі як H, C, 14 та C. Такі ізотопно-мічені сполуки застосовні для вивчення метаболізму (переважно, що 14 2 3 містять C), кінетики реакцій (що містять, наприклад, H або H), у методологіях детектування та візуалізації [таких як позитронна емісійна томографія (ПЕТ) або однофотонна емісійна комп'ютерна томографія (ОФЕКТ), включаючи дослідження розподілу лікарського засобу або 18 субстрату в тканинах або променеву терапію пацієнтів. Зокрема, сполука, що містить F або мічена ним, може бути особливо кращою для досліджень за допомогою ПЕТ або ОФЕКТ. Ізотопно-мічені сполуки, запропоновані в даному винаході, та їх проліки звичайно можна одержати за методиками, розкритими у схемах або у прикладах та синтезах, описаних нижче, шляхом заміни реагенту, що не містить ізотопу, на легко доступний ізотопно-мічений реагент. 2 Крім того, заміщення більш важкими ізотопами, переважно дейтерієм (тобто H або D), може забезпечити деякі терапевтичні переваги, обумовлені їх більш високою метаболічною стабільністю, наприклад, збільшеною тривалістю напіввиведення in vivo або можливістю використання менших доз, або поліпшенням терапевтичного індексу. Слід розуміти, що в цьому контексті дейтерій розглядається як замісник в сполуці формули (I). Концентрацію такого більш важкого ізотопу, зокрема, дейтерію, можна визначити за допомогою коефіцієнта ізотопного збагачення. Термін "коефіцієнт ізотопного збагачення" при використанні в даному винаході означає відношення вмісту ізотопу до вмісту конкретного ізотопу в природі. Якщо замісник у сполуці, запропонованій в даному винаході, означає дейтерій, то така сполука характеризується коефіцієнтом ізотопного збагачення для кожного позначеного атому дейтерію, рівним не менше 3500 (вміст дейтерію для кожного позначеного атома дейтерію дорівнює 52,5 %), не менше 4000 (вміст дейтерію дорівнює 60 %), не менше 4500 (вміст дейтерію дорівнює 67,5 %), не менше 5000 (вміст дейтерію дорівнює 75 %), не менше 5500 (вміст дейтерію дорівнює 82,5 %), не менше 6000 (вміст дейтерію дорівнює 90 %), не менше 6333,3 (вміст дейтерію дорівнює 95 %), не менше 6466,7 (вміст дейтерію дорівнює 97 %), не менше 6600 (вміст дейтерію дорівнює 99 %) або не менше 6633,3 (вміст дейтерію дорівнює 99,5 %). У сполуках, запропонованих у даному винаході, будь-який атом, спеціально не позначений як конкретний ізотоп, означає будь-який стабільний ізотоп цього атому. Якщо не зазначене інше, коли спеціально зазначено "H" або "водень", це означає водень, що має природний ізотопний склад. Відповідно, у сполуках, запропонованих у даному винаході, будь-який атом, спеціально позначений, як дейтерій (D) означає атом із вмістом дейтерію, наприклад, у зазначених вище діапазонах. Вибір значення конкретного фрагменту з переліку можливих значень при описі будь-якої формули, наведеної в даному винаході, не означає завдання значення цього фрагменту для іншої частини даного опису. Інакше кажучи, якщо змінна міститься більш одного разу, тоді вибір її значень з переліку значень не залежить від вибору значень цієї змінної у формулі, що знаходиться в іншій частині даного опису (де у варіантах здійснення одне або більша кількість та аж до всіх більш загальних значень, охарактеризованих вище або нижче, як кращі, можна замінити на більш краще визначення та в такий спосіб утворювати відповідний більш кращий варіант здійснення даного винаходу). Якщо використовується множина (наприклад, сполуки, солі), тоді вона включає і однину (наприклад, одну сполуку, одну сіль). Використання терміну "сполука" не виключає того, що (наприклад, у фармацевтичному препараті) міститься більше, ніж одна сполука формули (I) (або її сіль). Якщо не зазначено інше, то в даному описі застосовні зазначені нижче загальні визначення: Галоген означає фтор, бром, хлор або йод, переважно фтор, хлор. Галогензаміщені групи та фрагменти, такі як алкіл, заміщений галогеном (галогеналкіл), можуть бути моно-, полі- або пергалогенованими. Гетероатоми являють собою атоми, що не є атомами вуглецю та водню, переважно азот (N), кисень (O) або сірку (S), більш переважно азот. 3 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 60 Вуглецевмісні групи, фрагменти або молекули містять від 1 до 7, переважно від 1 до 6, більш переважно від 1 до 4, найбільш переважно 1 або 2 атоми вуглецю. Будь-яка нециклічна вуглецевмісна група або фрагмент, що містить більше 1 атому вуглецю, має лінійний або розгалужений ланцюг. Приставка "нижч." або "C1-C7" означає радикал, що містить максимально до 7 включно, переважно - максимально до 4 включно атомів вуглецю, використовувані радикали є лінійними або розгалуженими та містять одне або декілька розгалужень. "Алкіл" означає алкільну групу, що має лінійний або розгалужений ланцюг, переважно являє собою C1-C12-алкіл, що має лінійний або розгалужений ланцюг, особливо переважно являє собою C1-C7-алкіл, що має лінійний або розгалужений ланцюг, наприклад, метил, етил, н- або ізопропіл, н-, ізо-, втор- або трет-бутил, н-пентил, н-гексил, н-гептил, н-октил, н-ноніл, н-децил, н-ундецил, н-додецил, особливо кращими є метил, етил, н-пропіл, ізопропіл та н-бутил та ізобутил. Алкіл може бути незаміщеним або заміщеним. Типові замісники включають, але не обмежуються тільки ними, гідроксигрупу, алкоксигрупу, галоген та аміногрупу. Прикладом заміщеного алкілу є трифторметил. Циклоалкіл також може бути замісником алкілу. Прикладом такого випадку є фрагмент (алкіл)-циклопропіл або алкандіілциклопропіл, наприклад, –CH2циклопропіл. C1-C7-Алкіл переважно являє собою алкіл, що містить від 1 включно до 7 включно, переважно від 1 включно до 4 включно атомів вуглецю, та є лінійним або розгалуженим; нижч. алкіл переважно являє собою бутил, такий як н-бутил, втор-бутил, ізобутил, трет-бутил, пропіл, такий як н-пропіл або ізопропіл, етил або, переважно, метил. Кожен алкільний фрагмент інших груп, таких як "алкоксигрупа", "алкоксиалкіл", "алкоксикарбоніл", "алкоксикарбонілалкіл", "алкілсульфоніл", "алкілсульфоксил", "алкіламіногрупа", "галогеналкіл" має таке ж значення, як зазначено в приведеному вище визначенні "алкілу". "Алкандіїл" означає алкандіільну групу, що має лінійний або розгалужений ланцюг, за допомогою двох різних атомів вуглецю зв'язану з фрагментом, він переважно являє собою C 1C12-алкандііл, що має лінійний або розгалужений ланцюг, особливо переважно являє собою C 1C6-алкандііл, що має лінійний або розгалужений ланцюг; наприклад, метандііл (-CH2-), 1,2етандііл (-CH2-CH2-), 1,1-етандііл ((-CH(CH3)-), 1,1-, 1,2-, 1,3-пропандііл та 1,1-, 1,2-, 1,3-, 1,4бутандііл, особливо переважно метандііл, 1,1-етандііл, 1,2-етандііл, 1,3-пропандііл, 1,4бутандііл. "Алкендііл" означає алкендіільну групу, що має лінійний або розгалужений ланцюг, за допомогою двох різних атомів вуглецю зв'язану з фрагментом, він переважно являє собою C 2C6-алкендїїл, що має лінійний або розгалужений ланцюг; наприклад, -CH=CH-, -CH=C(CH3)-, CH=CH-CH2-, -C(CH3)=CH-CH2-, -CH=C(CH3)-CH2-, -CH=CH-C(CH3)H-, -CH=CH-CH=CH-, C(CH3)=CH-CH=CH-, -CH=C(CH3)-CH=CH-, особливо переважно -CH=CH-CH2-, -CH=CH-CH=CH. Алкендііл може бути заміщеним або незаміщеним. "Циклоалкіл" означає насичений або частково насичений моноциклічний, конденсований поліциклічний або спірозчленований поліциклічний карбоцикл, що містить від 3 до 12 кільцевих атомів в одному карбоциклі. Ілюстративні приклади циклоалкільних груп включають наступні фрагменти: циклопропіл, циклобутил, циклопентил та циклогексил. Циклоалкіл може бути незаміщеним або заміщеним; типові замісники вказані у визначенні алкілу та також включають сам алкіл (наприклад, метил). Фрагмент типу –(CH3)циклопропіл вважається заміщеним циклоалкілом. "Арил" означає ароматичну гомоциклічну кільцеву систему, що містить 6 або більшу кількість атомів вуглецю; арил переважно являє собою ароматичний фрагмент, що містить від 6 до 14 кільцевих атомів вуглецю, більш переважно від 6 до 10 кільцевих атомів вуглецю, таку як феніл або нафтил, переважно феніл. Арил може бути незаміщеним або містити один або більшу кількість, переважно до трьох, більш переважно до двох замісників, незалежно вибраних з групи, що включає незаміщений або заміщений гетероцикліл, описаний вище, переважно піролідиніл, такий як піролідинову групу, оксопіролідиніл, такий як оксопіролідинову групу, C1-C7алкілпіролідиніл, 2,5-ди-(C1-C7-алкіл)піролідиніл, такий як 2,5-ди-(C1-C7-алкіл)-піролідинову групу, тетрагідрофураніл, тіофеніл, C1-C7-алкілпіразолідиніл, піридиніл, C1-C7-алкілпіперидиніл, піперидинову групу, піперидинову групу, що містить як замісники аміногрупу або N-моно- або N, N-ди-[нижч. алкіл, феніл, C1-C7-алканоїл та/або феніл-нижч. алкіл)-аміногрупу, незаміщений або N-нижч. алкілзаміщений піперидиніл, приєднаний через кільцевий атом вуглецю, піперазинову групу, нижч. алкілпіперазинову групу, морфолінову групу, тіоморфолінову групу, Sоксотіоморфолінову групу або S, S-діоксотіоморфолінову групу; C1-C7-алкіл, аміно-C1-C7-алкіл, N-C1-C7-алканоїламіно-C1-C7-алкіл, N-C1-C7-алкансульфоніламіно-C1-C7-алкіл, карбамоїл-C1-C7алкіл, [N-моно- або N, N-ди-(C1-C7-алкіл)-карбамоїл]-C1-C7-алкіл, C1-C7-алкансульфініл-C1-C7 4 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 алкіл, C1-C7-алкансульфоніл-C1-C7-алкіл, феніл, нафтил, моно- – три-[C1-C7-алкіл, галоген та/або ціано]-феніл або моно- – три-[C1-C7-алкіл, галоген та/або ціано]-нафтил; C3-C8циклоалкіл, моно- – три-[C1-C7-алкіл та/або гідрокси]-C3-C8-циклоалкіл; галоген, гідроксигрупу, нижч. алкоксигрупу, нижч.-алкокси-нижч. алкоксигрупу, (нижч.-алкокси)-нижч. алкокси-нижч. алкоксигрупу, галоген-C1-C7-алкоксигрупу, феноксигрупу, нафтилоксигрупу, феніл- або нафтилнижч. алкоксигрупу; аміно-C1-C7-алкоксигрупу, нижч.-алканоїлоксигрупу, бензоїлоксигрупу, нафтоїлоксигрупу, форміл (CHO), аміногрупу, N-моно- або N, N-ди-(C1-C7-алкіл)-аміногрупу, C1C7-алканоїламіногрупу, C1-C7-алкансульфоніл-аміногрупу, карбоксигрупу, нижч. алкоксикарбоніл, наприклад; феніл- або нафтил-нижч. алкоксикарбоніл, такий як бензилоксикарбоніл; C1-C7-алканоїл, такий як ацетил, бензоїл, нафтоїл, карбамоїл, N-моно- або N, N-дизаміщений карбамоїл, такий як N-моно- або N, N-дизаміщений карбамоїл, де замісники вибрані з групи, що включає нижч. алкіл, (нижч.-алкокси)-нижч. алкіл та гідрокси-нижч. алкіл; амідинову групу, гуанідинову групу, уреїдну групу, меркаптогрупу, нижч. алкілтіогрупу, фенілабо нафтилтіогрупу, феніл- або нафтил-нижч. алкілтіогрупу, нижч. алкілфенілтіогрупу, нижч. алкілнафтилтіогрупу, галоген-нижч. алкілмеркаптогрупу, сульфогрупу (-SO3H), нижч. алкансульфоніл, феніл- або нафтилсульфоніл, феніл- або нафтил-нижч. алкілсульфоніл, алкілфенілсульфоніл, галоген-нижч. алкілсульфоніл, такий як трифторметансульфоніл; сульфонамідну групу, бензосульфонамідну групу, азидну групу, азидо-C1-C7-алкіл, переважно азидометил, C1-C7-алкансульфоніл, сульфамоїл, N-моно- або N, N-ди-(C1-C7-алкіл)-сульфамоїл, морфоліносульфоніл, тіоморфоліносульфоніл, ціаногрупу та нітрогрупу; де кожен феніл або нафтил (також в феноксигрупі або нафтоксигрупі), зазначений вище як замісник або частина заміснику заміщеного алкілу (або також заміщеного арилу, гетероциклілу та т. п., вказаного в даному винаході), сам є незаміщеним або містить один або більшу кількість, наприклад, до трьох, переважно 1 або 2 замісники, незалежно вибраних з групи, що включає галоген, галогеннижч. алкіл, такий як трифторметил, гідроксигрупу, нижч. алкоксигрупу, азидну групу, аміногрупу, N-моно- або N, N-ди-(нижч. алкіл та/або C1-C7-алканоїл)-аміногрупу, нітрогрупу, карбоксигрупу, нижч.-алкоксикарбоніл, карбамоїл, ціаногрупу та/або сульфамоїл. "Гетероцикліл" означає гетероциклічний радикал, який є ненасиченим (= що містить в кільці (кільцях) найбільш можливу кількість спряжених подвійних зв'язків), насиченим або частково насиченим та переважно являє собою моноциклічне або, в більш широкому об'єкті даного винаходу, біциклічне, трициклічне або спірозчленоване поліциклічне кільце; та містить від 3 до 24, більш переважно від 4 до 16, найбільш переважно від 5 до 10 та найбільш переважно 5 або 6 кільцевих атомів; де один або більша кількість, переважно від 1 до 4, переважно 1 або 2 кільцевих атоми вуглецю замінені на гетероатом, приєднане кільце переважно містить від 4 до 12, переважно від 5 до 7 кільцевих атомів. Гетероциклічний радикал (гетероцикліл) може бути незаміщеним або містити один або більшу кількість, переважно від 1 до 3 замісників, незалежно вибраних з групи, що включає замісники, визначені вище для заміщеного алкілу, та/або один або більшу кількість наступних замісників: оксогрупу (=O), тіокарбоніл (=S), іміногрупу (=NH), іміно-нижч. алкіл. Крім того, гетероцикліл переважно являє собою гетероциклільний радикал, вибраний з групи, що включає оксираніл, азириніл, азиридиніл, 1,2-оксатіоланіл, тієніл (= тіофеніл), фураніл, тетрагідрофурил, піраніл, тіопіраніл, тіантреніл, ізобензофураніл, бензофураніл, хроменіл, 2H-піроліл, піроліл, піролініл, піролідиніл, імідазоліл, імідазолідиніл, бензімідазоліл, піразоліл, піразиніл, піразолідиніл, тіазоліл, ізотіазоліл, дитіазоліл, оксазоліл, ізоксазоліл, піридил, піразиніл, піримідиніл, піперидиніл, піперазиніл, піридазиніл, морфолініл, тіоморфолініл, (S-оксо- або S, S-діоксо)-тіоморфолініл, індолізиніл, азепаніл, діазепаніл, переважно 1,4-діазепаніл, ізоіндоліл, 3H-індоліл, індоліл, бензімідазоліл, кумарил, індазоліл, триазоліл, тетразоліл, пуриніл, 4H-хінолізиніл, ізохіноліл, хіноліл, тетрагідрохіноліл, тетрагідрізохіноліл, декагідрохіноліл, октагідрізохіноліл, бензофураніл, дибензофураніл, бензотіофеніл, дибензотіофеніл, фталазиніл, нафтиридиніл, хіноксаліл, хіназолініл, хіназолініл, циннолініл, птеридиніл, карбазоліл, бета-карболініл, фенантридиніл, акридиніл, піримідиніл, фенантролініл, фуразаніл, феназиніл, фенотіазиніл, феноксазиніл, хроменіл, ізохроманіл, хроманіл, бензо[1,3]діоксол-5-іл та 2,3-дигідробензо[1,4]діоксин-6-іл, кожен з цих радикалів є незаміщеним або містить один або більшу кількість, переважно до трьох, замісників, вибраних з числа вказаних вище для заміщеного арилу, та/або один або більшу кількість наступних замісників: оксогрупу (=O), тіокарбоніл (=S), іміногрупу (=NH), іміно-нижч. алкіл. "Арилалкіл" означає арильну групу, приєднану до молекули через алкільну групу, таку як метильну або етильну групу, переважно фенетильну або бензильну, більш переважно бензильну. Аналогічним чином, циклоалкілалкіл та гетероцикліл означає циклоалкільну групу, приєднану до молекули через алкільну групу, або гетероциклільну групу, приєднану до 5 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 молекули через алкільну групу. В кожному випадку арил, гетероцикліл, циклоалкіл та алкіл може бути заміщеним, як визначено вище. "Лікування" включає профілактичне (попереджувальне) та терапевтичне лікування, а також затримку прогресування захворювання або порушення. "Опосередковані PI3 кіназою захворювання" (переважно опосередковані PI3K-альфа захворювання та захворювання, опосередковані надекспресуванням або ампліфікацією PI3Kальфа, соматичними мутаціями PIK3CA або мутаціями зародкового типу або соматичними мутаціями PTEN або мутаціями та транслокаціями p85, які забезпечують підвищуючу регуляцію комплексу p85-p110) переважно являють собою порушення, які реагують сприятливим чином (наприклад, відбувається ослаблення одного або більшої кількості симптомів, затримка початку захворювання, аж до тимчасового або повного виліковування захворювання) на інгібування кінази PI3, переважно на інгібування PI3K-альфа або її мутантної форми (де з числа захворювань, що піддаються лікуванню, в особливо можна відмітити проліферативні захворювання, такі як пухлинні захворювання та лейкози). "Солі" (те, що означає вираз "або її солі" або "або її сіль") можуть міститися окремо або в суміші з вільною сполукою формули (I) та переважно являють собою фармацевтично прийнятні солі. Такі солі, наприклад, утворюються у вигляді солей приєднання з кислотами, переважно з органічними або неорганічними кислотами, зі сполук формули (I), що містять основний атом азоту, переважно фармацевтично прийнятні солі. Підходящими неорганічними кислотами є, наприклад, галогеноводневі кислоти, такі як хлористоводнева кислота, сірчана кислота або фосфорна кислота. Підходящими органічними кислотами є, наприклад, карбонові кислоти або сульфонові кислоти, такі як фумарова кислота або метансульфонова кислота. Для виділення та очищення також можна використовувати фармацевтично неприйнятні солі, наприклад, пікрати або перхлорати. Для терапевтичного застосування використовують тільки фармацевтично прийнятні солі або вільні сполуки (якщо вони застосовні у вигляді фармацевтичних препаратів) та тому вони є кращими. Внаслідок близької спорідненості нових сполук у вільній формі та у формі їх солей, включаючи солі, які можна використовувати як проміжні продукти, наприклад, при очищенні або ідентифікації нових сполук, будь-яку вказівку на вільну сполуку вище та нижче в даному винаході слід розуміти також і як вказівку на відповідні солі, якщо це є підходящим або доцільним. Солі сполук формули (I) переважно являють собою фармацевтично прийнятні солі; підходящі протиіони, що утворюють фармацевтично прийнятні солі, відомі в даній галузі техніки. "Комбінація" означає фіксовану комбінацію в одній разовій дозованій формі або набір компонентів для комбінованого введення, при якому сполуку формули (I) та компонент комбінації (наприклад, інший лікарський засіб, як зазначено нижче, що також називається як "терапевтичний засіб" або "засіб, що спільно вводиться") можна незалежно вводити одночасно або окремо через певні проміжки часу, переважно таким чином, щоб ці проміжки часу дозволяли компонентам комбінації виявляти спільний, наприклад, синергетичний вплив. Терміни "спільне введення" або "комбіноване введення" та т.п. при використанні в даному винаході означають введення обраного компоненту комбінації одному суб'єкту, який цього потребує, (наприклад, пацієнтові) та включають режими лікування, при яких засіб необов'язково вводять одним та тим же шляхом або в один та той же час. Термін "фармацевтична комбінація" при використанні в даному винаході означає препарат, отриманий змішуванням або комбінуванням більше одного активного інгредієнту, та включає фіксовані та нефіксовані комбінації активних інгредієнтів. Термін "фіксована комбінація" означає, що активні інгредієнти, наприклад, сполуку формули (I) та компонент комбінації, обидва вводять пацієнтові одночасно у вигляді одного об'єкта або дози. Термін "нефіксована комбінація" означає, що активні інгредієнти, наприклад, сполуку формули (I) та компонент комбінації, обидва вводять пацієнтові у вигляді окремих об'єктів спільно, одночасно або послідовно без встановлених часових обмежень та таке введення забезпечує терапевтично ефективні вмісти цих двох сполук в організмі пацієнта. Останнє також відноситься до змішаного лікування, наприклад, введенню трьох або більшої кількості активних інгредієнтів. В кращих варіантах здійснення, які є переважними незалежно, разом або в будь-якій комбінації або субкомбінації, даний винахід відноситься до сполуки формули (I) у формі вільної основи або у формі солі приєднання з кислотою, у якій замісники є такими, як визначено в даному винаході. В одному кращому варіанті здійснення даний винахід відноситься до сполуки формули IA 6 UA 104147 C2 3 H N N R S N O O NH2 N 1 R IA у якій замісники є такими, як визначено для сполуки формули (I). В іншому кращому варіанті здійснення даний винахід відноситься до сполуки формули IB 3 H N N R S N O O N NH2 N 1 R 5 10 IB у якій замісники є такими, як визначено для сполуки формули (I). Таким чином, сполука формули (I) також включає сполуки формули (IA) та (IB). В контексті даного винаходу також застосовні наступні визначення. A переважно позначає гетероарил, що містить 1 або 2 атоми азоту та від 5 до 10 атомів, що утворюють цикл. A особливо переважно позначає гетероарил, вибраний з групи, що включає: N N N N N N NH A ще більш переважно позначає гетероарил, вибраний з групи, що включає: N N N N N N NH A найбільш переважно позначає гетероарил, вибраний з групи, що включає: 15 20 25 30 1 R переважно позначає один з наступних замісників: (1) незаміщений або заміщений, переважно заміщений C1-C7-алкіл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно з 1-9 наступних замісників: дейтерій, галоген, ціаногрупу, C3-C12-циклоалкіл, C1-C7-алкіламіногрупу, ди(C1-C7алкіл)аміногрупу, C1-C7-алкіламінокарбоніл, ди(C1-C7-алкіл)амінокарбоніл, C1-C7-алкоксигрупу, феніл (який є незаміщеним або містить один або більшу кількість, переважно один наступний замісник: C1-C7-алкіл, C1-C7-алкоксигрупу, ди(C1-C7-алкіл)аміно-C1-C7-алкоксигрупу), феноксигрупу (яка є незаміщеною або містить один або більшу кількість, переважно один наступний замісник: C1-C7-алкіл, C1-C7-алкоксигрупу, ди(C1-C7-алкіл)аміно-C1-C7-алкоксигрупу); (2) незаміщений або заміщений C3-C12-циклоалкіл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно з 1-4 наступних замісників: дейтерій, галоген, ціаногрупу, C1-C7-алкіл, C1-C7-алкіламіногрупу, ди(C1-C7-алкіл)аміногрупу, амінокарбоніл, C1-C7алкіламінокарбоніл, ди(C1-C7-алкіл)амінокарбоніл, C1-C7-алкоксигрупу, феніл (який є незаміщеним або містить один або більшу кількість, переважно один наступний замісник: C1-C7алкіл, C1-C7-алкоксигрупу, ди(C1-C7-алкіл)аміно-C1-C7-алкоксигрупу), феноксигрупу (яка є 7 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 60 незаміщеною або містить один або більшу кількість, переважно один наступний замісник: C 1-C7алкіл, C1-C7-алкоксигрупу, ди(C1-C7-алкіл)аміно-C1-C7-алкоксигрупу); (3) незаміщений або заміщений феніл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно 1-2 наступних фрагментів: дейтерій, галоген, ціаногрупу, C 1-C7алкіл, C1-C7-алкіламіногрупу, ди(C1-C7-алкіл)аміногрупу, C1-C7-алкіламінокарбоніл, ди(C1-C7алкіл)амінокарбоніл, C1-C7-алкоксигрупу; (4) незаміщений, моно- або дизаміщений амін; де вказані замісники незалежно вибрані з числа наступних фрагментів: дейтерій, C1-C7-алкіл (який є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, фтор, хлор, гідроксигрупу), C1-C7-алкілкарбоніл, феніл (який є незаміщеним або містить один або більшу кількість, переважно один з наступних замісників: C1-C7-алкіл, C1-C7-алкоксигрупу, ди(C1-C7-алкіл)аміноC1-C7-алкоксигрупу), фенілсульфоніл (який є незаміщеним або містить один або більшу кількість, переважно один з наступних замісників: C 1-C7-алкіл, C1-C7-алкоксигрупу, ди(C1-C7алкіл)аміно-C1-C7-алкоксигрупу), (5) заміщений сульфоніл; де вказаний замісник вибраний з числа наступних фрагментів: C 1C7-алкіл (який є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, фтор, хлор, гідроксигрупу), C 1-C7-алкіламіногрупу (де алкільний фрагмент є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, фтор, хлор, гідроксигрупу), ди-C1-C7-алкіламіногрупу (де алкільний фрагмент є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, фтор, хлор, гідроксигрупу); (6) фтор, хлор. 1 R особливо переважно позначає один з наступних замісників: (1) незаміщений або заміщений, переважно заміщений C1-C7-алкіл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно з 1-9 наступних замісників: дейтерій, фтор, або 1-2 наступних фрагментів: C3-C5-циклоалкіл; (2) необов'язково заміщений C3-C5-циклоалкіл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно з 1-4 наступних замісників: дейтерій, C1-C4-алкіл (переважно метил), фтор, ціаногрупу, амінокарбоніл; (3) необов'язково заміщений феніл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно 1-2 наступних фрагментів: дейтерій, галоген, ціаногрупу, C 1-C7алкіл, C1-C7-алкіламіногрупу, ди(C1-C7-алкіл)аміногрупу, C1-C7-алкіламінокарбоніл, ди(C1-C7алкіл)амінокарбоніл, C1-C7-алкоксигрупу; (4) необов'язково моно- або дизаміщений амін; де вказані замісники незалежно вибрані з числа наступних фрагментів: дейтерій, C1-C7-алкіл (який є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, фтор, хлор, гідроксигрупу), фенілсульфоніл (який є незаміщеним або містить один або більшу кількість, переважно один з наступних замісників: C1-C7-алкіл, C1-C7-алкоксигрупу, ди(C1-C7-алкіл)аміно-C1-C7-алкоксигрупу), (5) заміщений сульфоніл; де вказаний замісник вибраний з числа наступних фрагментів: C 1C7-алкіл (який є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, фтор), піролідинову групу, (який є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, гідроксигрупу, оксогрупу; переважно одну оксогрупу), (6) фтор, хлор. 1 R ще більш переважно позначає: (1) циклопропілметил або необов'язково заміщений розгалужений C 3-C7-алкіл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно з 1-9 наступних замісників: дейтерій, фтор; (2) необов'язково заміщений циклопропіл або циклобутил, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно з 1-4 наступних замісників: метил, дейтерій, фтор, ціаногрупу, амінокарбоніл; (3) необов'язково заміщений феніл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно 1-2 наступних фрагментів: дейтерій, галоген, ціаногрупу, C 1-C7алкіл, C1-C7-алкіламіногрупу, ди(C1-C7-алкіл)аміногрупу, C1-C7-алкіламінокарбоніл, ди(C1-C7алкіл)амінокарбоніл, C1-C7-алкоксигрупу; (4) необов'язково моно- або дизаміщений амін; де вказані замісники незалежно вибрані з числа наступних фрагментів: дейтерій, C1-C7-алкіл (який є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, фтор, хлор, гідроксигрупу), фенілсульфоніл (який є незаміщеним або містить один або більшу кількість, переважно один з наступних замісників: C1-C7-алкіл, C1-C7-алкоксигрупа, ди(C1-C7-алкіл)аміно-C1-C7-алкоксигрупа), 8 UA 104147 C2 5 10 15 20 25 30 (5) заміщений сульфоніл; де вказаний замісник вибраний з числа наступних фрагментів: C1C7-алкіл (який є незаміщеним або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, фтор), піролідинова група (яка є незаміщеною або містить один або більшу кількість замісників, вибраних з групи, що включає дейтерій, гідроксигрупу, оксогрупу; переважно одну оксогрупу), (6) фтор, хлор. 1 R ще більш переважно позначає один з наступних замісників: -C(CH3)2CF3, C(CD3)3, 1метилциклопропіл, переважно в контексті (I-A) та (I-B). 2 1 R переважно позначає замісник, визначений для R . 2 R більш переважно позначає водень або дейтерій. 2 R особливо переважно позначає водень. 2 R в альтернативному варіанті здійснення позначає метил. 3 R переважно позначає (1) водень, (2) галоген, (3) необов'язково заміщений C 1-C7-алкіл, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно 1-3 наступних фрагментів: дейтерій, галоген, C1-C7-алкіламіногрупа, ди(C1-C7-алкіл)аміногрупа. 3 R особливо переважно позначає (1) водень, (2) фтор, хлор, (3) необов'язково заміщений метил, де вказані замісники незалежно вибрані з одного або більшої кількості, переважно 1-3 наступних фрагментів: дейтерій, фтор, хлор, диметиламіногрупа. 3 R ще більш переважно позначає водень, метил, CD3, CH2Cl, CH2F, CH2N(CH3)3; переважно метил. Даний винахід також відноситься до сполуки формули (I), визначеної в даному винаході, за 1 2 виключенням таких сполук, у яких R та/або R позначає трет-бутил. Даний винахід також відноситься до фармацевтично прийнятних проліків сполуки формули (I). Даний винахід також відноситься до фармацевтично прийнятних метаболітів сполуки формули (I). Даний винахід переважно відноситься до сполук формули (I), приведених в прикладах, а також до способів одержання, описаних в даному винаході. Даний винахід також відноситься до способів одержання сполуки формули (I). В принципі є підходящими всі відомі методики перетворення різних амінів в відповідні похідні сечовини та їх можна використовувати із застосуванням відповідної вихідної речовини. Таким чином, даний винахід переважно відноситься до способу одержання сполуки формули (I), який включає реакцію сполуки формули (II) HN O 35 NH2 (II) або зі сполукою формули (IIIA) 3 N R NH2 S A 2 R 1 R (IIIA) 3 у якій замісники є такими, як визначено в даному винаході, та R додатково може позначати хлор, в присутності активуючого реагенту ("спосіб A"), або зі сполукою формули (IIIB) H 3 N R N RG S A 2 R 1 R (IIIB) 9 UA 104147 C2 1 2 3 у якій R та R є такими, як визначено в даному винаході, R є таким, як визначено в даному винаході та додатково може позначати хлор та RG позначає реакційноздатну групу, таку як імідазолілкарбоніл, яка може реагувати безпосередньо або шляхом утворення проміжного ізоціанату формули (IIIE) ("спосіб B"), O C 3 N R N S A 2 R 1 5 10 15 20 25 30 35 40 45 R (IIIE) у якій замісники є такими, як визначено в (IIIB), в кожному випадку необов'язково в присутності розріджувача та необов'язково в присутності засобу, що сприяє протіканню реакції, та вилучення отриманої сполуки формули (I) у вільній формі або у формі солі та, необов'язково перетворення сполуки формули (I), отриманої за способом A або способом B, в іншу сполуку формули (I), та/або перетворення отриманої солі сполуки формули (I) в іншу її сіль, та/або перетворення отриманої вільної сполуки формули (I) в її сіль, та/або відділення отриманого ізомеру сполуки формули (I) від одного або більшої кількості різних отриманих ізомерів формули I. Умови проведення реакцій Спосіб можна здійснити за методиками, відомими у даній галузі техніки, або описаними нижче в прикладах. Наприклад, сполуку формули II можна ввести в реакцію із сполукою формули III у розчиннику, наприклад, диметилформаміді, у присутності основи, наприклад, органічного аміну, наприклад, триетиламіну. Коли вище або нижче в даному винаході зазначені значення температури, до них слід додати слово "приблизно", як вказівка на невеликі відхилення від наведених числових значень, наприклад, припустимими є відхилення, що становлять ±10 %. Усі реакції можуть протікати в присутності одного або більшої кількості розріджувачів та/або розчинників. Вихідні речовини можна використовувати в еквімолярних кількостях; альтернативно, сполуки можна використовувати в надлишку, наприклад, як розчинник або для зсуву рівноваги, або для загального підвищення швидкостей реакцій. Засоби, що сприяють протіканню реакцій, такі як кислоти, основи або каталізатори, можна додати в підходящих кількостях, як це відомо в даній області техніки, необхідних для протікання реакції та відповідно до загальновідомих методик. Захисні групи Якщо у вихідній речовині, описаній в даному винаході, або в будь-якому попереднику одну або більшу кількість інших функціональних груп, наприклад, карбоксигрупу, гідроксигрупу, аміногрупу сульфгідрил та т.п., необхідно забезпечити захисною групою, оскільки вони не повинні брати участь у реакції або впливати на реакцію, тоді ними є захисні групи, які звичайно використовуються при синтезі пептидних сполук, а також цефалоспоринів та пеніцилінів, а також похідних нуклеїнових кислот та цукрів. Захисні групи є такими групами, які після видалення не повинні міститися в кінцевих сполуках, а групи, які залишаються як замісники, у використаному в даному описі сенсі не є захисними групами, які вводять у вихідну речовину або на проміжній стадії та видаляють для одержання кінцевої сполуки. Також і у випадку перетворень сполуки формули (I) в іншу сполуку формули (I) захисні групи можна вводити та видаляти, якщо це доцільно або необхідно. Захисні групи можуть вже міститися в попередниках та повинні захищати відповідні функціональні групи від вступу в небажані вторинні реакції, такі як ацилювання, утворення простого ефіру, утворення складного ефіру, окиснення, сольволіз та аналогічні реакції. Особливістю захисних груп є те, що їх можна легко, тобто без небажаних вторинних реакцій, видаляти, звичайно за допомогою ацетолізу, протолізу, сольволізу, відновлення, фотолізу, а також при впливі ферментів, наприклад, при умовах, аналогічних фізіологічним умовам, та вони не містяться в кінцевих продуктах. Фахівцеві в даній галузі техніки відомо або він легко може 10 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 60 встановити, які захисні групи є підходящими для проведення реакцій, зазначених вище та нижче в даному винаході. Захист таких функціональних груп за допомогою таких захисних груп, самі захисні групи та реакції їх видалення описані, наприклад, в стандартних довідниках, таких як J. F. W. McOmie, "Protective Groups in Organic Chemistry", Plenum Press, London and New York 1973, у T. W. Greene, "Protective Groups in Organic Synthesis", Third edition, Wiley, New York 1999, у "The Peptides"; Volume 3 (editors: E. Gross and J. Meienhofer), Academic Press, London and New York 1981, у "Methoden der organischen Chemie" (Методи органічної хімії), Houben Weyl, 4th edition, Volume 15/I, Georg Thieme Verlag, Stuttgart 1974, у H.-D. Jakubke and H. Jescheit, "Aminosäuren, Peptide, Proteine" (Амінокислоти, пептиди, білки), Verlag Chemie, Weinheim, Deerfield Beach, and Basel 1982 та у Jochen Lehmann, "Chemie der Kohlenhydrate: Monosaccharide und Derivate" (Хімія карбогідратів: карбогідрати та похідні), Georg Thieme Verlag, Stuttgart 1974. Необов'язкові реакції та перетворення Сполуку формули (I) можна перетворити в іншу сполуку формули I. 3 Сполуку формули (I), у якій R позначає фтор, можна одержати шляхом перетворення відповідної хлорпохідної в сполуку, що містить фтор. Такі реакції відомі та називаються реакціями заміщення. Це перетворення може протікати на стадії, що включає вихідну речовину формули (IIIA або B), або шляхом перетворення відповідної сполуки формули I. В сполуці формули (I), у якій замісник містить аміногрупу або аміно-C1-C7-алкіл як замісник, аміногрупу можна перетворити в аціламіногрупу, наприклад, C1-C7-алканоїламіногрупу або C1C7-алкансульфоніламіногрупу, за реакцією з відповідним C 1-C7-алканоїлгалогенідом або C1-C7алкансульфонілгалогенідом, наприклад, відповідним хлоридом, в присутності третинної азотистої основи, такої як триетиламін або піридин, за відсутності або в присутності підходящого розчиннику, такого як метиленхлорид, наприклад, при температурах в діапазоні від –20 до 50 °C, наприклад, приблизно при кімнатній температурі. В сполуці формули (I), у якій замісник містить ціаногрупу як замісник, ціаногрупу можна перетворити в амінометильну групу, наприклад, шляхом гідрування в присутності підходящого каталізатору на основі металу, такого як нікель Ренея або кобальт Ренея, в підходящому розчиннику, наприклад, нижч. алканолі, такому як метанол та/або етанол, наприклад, при температурах в діапазоні від –20 до 50 °C, наприклад, приблизно при кімнатній температурі. Солі сполуки формули (I) із солеутворюючою групою можна одержати за відомими методиками. Так, солі приєднання сполук формули (I) з кислотами можна одержати обробкою кислотою або підходящим аніонообмінним реагентом. Сіль із двома молекулами кислоти (наприклад, дигалогенід сполуки формули I) також можна перетворити в сіль із однією молекулою кислоти на молекулу сполуки (наприклад, моногалогенід); це можна виконати шляхом нагрівання до плавлення або наприклад, шляхом нагрівання у вигляді твердої речовини у високому вакуумі при підвищеній температурі, наприклад, рівній від 130 до 170 °C, у результаті чого з однієї молекули сполуки формули I віддаляється одна молекула кислоти. Солі звичайно можна перетворити у вільні сполуки, наприклад, шляхом обробки підходящими основними сполуками, наприклад, карбонатами лужних металів, гідрокарбонатами лужних металів або гідроксидами лужних металів, звичайно карбонатом калію або гідроксидом натрію. Суміші стереоізомерів, наприклад, суміші діастереоізомерів можна розділити на відповідні ізомери за відомими методиками, за допомогою підходящих методик розділення. Наприклад, суміші діастереоізомерів можна розділити на індивідуальні діастереоізомери за допомогою фракціонованої кристалізації, хроматографії, розподілу в розчинниках та аналогічних методик. Це розділення можна проводити або для вихідної сполуки або для самої сполуки формули (I). Енантіомери можна розділити шляхом утворення діастереоізомерних солей, наприклад, шляхом утворення солі з енантіомерно чистою хіральною кислотою або за допомогою хроматографії, наприклад, ВЕРХ (високоефективна рідинна хроматографія), з використанням хроматографічних субстратів, що містять хіральні ліганди. Слід підкреслити, що реакції, аналогічні реакціям перетворення, зазначеним у цьому розділі, також можна проводити з підходящими проміжними продуктами (і таким чином, вони застосовні для одержання відповідних вихідних речовин). Вихідні речовини: Вихідні речовини формул II та III, а також інші вихідні речовини, зазначені в даному винаході, наприклад, нижче, можна одержати за методиками, які відомі в даній галузі техніки, або за аналогічними методиками, або вони є в продажу. Якщо одержання вихідних речовин спеціально не описане, тоді сполуки є відомими або їх можна одержати за методиками, аналогічними відомим у даній галузі техніки, наприклад, описаним у WO 05/021519 або WO04/096797, або розкритим нижче в даному винаході. Нові вихідні речовини, а також способи 11 UA 104147 C2 5 їх одержання також є варіантами здійснення даного винаходу. У кращих варіантах здійснення використовують такі вихідні речовини та реакцію вибирають таким чином, щоб можна було одержати кращі сполуки. У вихідних речовинах (включаючи проміжні продукти), які також можна використовувати та/або одержувати у вигляді солей якщо це є підходящим та доцільним, замісники переважно є такими, як визначено для сполуки формули (I). Даний винахід також відноситься до сполук формули (IIIA) або їх солей 3 N R NH2 S A 2 R 1 R 10 15 (IIIA) у якій замісники є такими, як визначено для сполуки формули (I). Даний винахід також відноситься до способів одержання сполуки формули (IIIA). У принципі, усі відомі способи, які приводять до комбінації двох компонентів арил/гетероарил (такі як реакції типу реакції Хека) з утворенням відповідної похідної сечовини, є підходящими та можуть бути використані із застосуванням відповідної вихідної речовини. Таким чином, даний винахід також відноситься до способу одержання сполуки формули (IIIA), який включає (стадія 1) реакцію сполуки формули (IV) H N R3 N PG S (IV) у якій R є таким, як визначено в даному винаході, та додатково може позначати галоген, PG позначає захисну групу, таку як ацильна група, із сполукою формули (V) Hal A 3 2 R 1 R 20 25 30 (V) 1 2 у якій R , R , A є такими, як визначено в даному винаході та Hal позначає галоген, такий як бром, за реакцією Хека; необов'язково в присутності розріджувача та необов'язково в присутності засобу, що сприяє проходженню реакції; (стадія 2), з наступним видаленням захисної групи, наприклад, в кислому середовищі; необов'язково в присутності розріджувача та необов'язково в присутності засобу, що сприяє протіканню реакції; та вилучення отриманої сполуки формули (IIIA) у вільній формі або у формі солі та, необов'язково перетворення отриманої сполуки формули (IIIA) в іншу сполуку формули (IIIA), та/або перетворення отриманої солі сполуки формули (IIIA) в іншу її сіль, та/або перетворення отриманої вільної сполуки формули (IIIA) в її сіль, та/або відділення отриманого ізомеру сполуки формули (IIIA) від одного або більшої кількості різних отриманих ізомерів формули (IIIA). Даний винахід також відноситься до сполук формули (IIIB) або їх солей 3 H N N R RG S A 2 R 1 R 35 (IIIB) 1 2 у якій R , R , A є такими, як визначено для сполуки формули (I), RG позначає реакційноздатну групу, переважно імідазолілкарбоніл, яка може реагувати безпосередньо або 12 UA 104147 C2 3 5 шляхом утворення проміжного ізоціанату формули (IIIE), та R є таким, як визначено в даному винаході, та додатково може позначати галоген. Даний винахід також відноситься до способів одержання сполуки формули (IIIB). В принципі, всі відомі способи, які забезпечують перетворення аміну або його солі у відповідну активовану похідну, є підходящими та можуть бути використані із застосуванням відповідної вихідної речовини. Таким чином, даний винахід також відноситься до способу одержання сполуки формули (IIIB), який включає реакцію сполуки формули (IIIA) 3 N R NH2 S A 2 R 1 R 10 15 (IIIA) у якій замісники є такими, як визначено в даному винаході, з активуючим реагентом, таким як 1,1’-карбонілдіімідазол, необов'язково в присутності розріджувача та необов'язково в присутності засобу, що сприяє протіканню реакції; та вилучення отриманої сполуки формули (IIIB) у вільній формі або у формі солі, та необов'язково перетворення отриманої сполуки формули (IIIB) в іншу сполуку формули (IIIB), та/або перетворення отриманої солі сполуки формули (IIIB) в іншу її сіль, та/або перетворення отриманої вільної сполуки формули (IIIB) в її сіль, та/або відділення отриманого ізомеру сполуки формули (IIIB) від одного або більшої кількості різних отриманих ізомерів формули (IIIB). Даний винахід також відноситься до сполук формули (IIIC) або їх солей R3 N NH2 S N N R1 20 (IIIC) у якій замісники є такими, як визначено для сполуки формули (I). Даний винахід також відноситься до способів одержання сполуки формули (IIIC). В принципі, всі реакції замикання циклу є підходящими та можуть бути використані із застосуванням відповідної вихідної речовини. Таким чином, даний винахід також відноситься до способу одержання сполуки формули (IIIC), який включає реакцію сполуки формули (VI) R3 N N N N 25 30 35 S O (VI) у якій R є таким, як визначено в даному винаході, та додатково може позначати галоген, із сполукою формули (VII) NH R1 NH2 (VII) 1 у якій R є таким, як визначено в даному винаході; необов'язково в присутності розріджувача та необов'язково в присутності засобу, що сприяє проходженню реакції; та вилучення отриманої сполуки формули (IIIC) у вільній формі або у формі солі, та необов'язково перетворення отриманої сполуки формули (IIIC) в іншу сполуку формули (IIIC), та/або перетворення отриманої солі сполуки формули (IIIC) в іншу її сіль, та/або перетворення отриманої вільної сполуки формули (IIIC) в її сіль, та/або відділення отриманого ізомеру сполуки формули (IIIC) від одного або більшої кількості різних отриманих ізомерів формули (IIIC). Даний винахід також відноситься до сполук формули (IIID) або їх солей 3 13 UA 104147 C2 R3 N S N NH RG N R1 (IIID) у якій R є таким, як визначено в даному винаході, RG позначає реакційноздатну групу, 3 переважно імідазолілкарбоніл, R є таким, як визначено в даному винаході, та додатково може позначати галоген. Даний винахід також відноситься до способів одержання сполуки формули (IIID). В принципі, всі відомі способи, які забезпечують перетворення аміну або його солі у відповідну активовану похідну, є підходящими та можуть бути використані із застосуванням відповідної вихідної речовини. Таким чином, даний винахід також відноситься до способу одержання сполуки формули (IIID), який включає реакцію сполуки формули (IIIC) R3 N NH2 S 1 5 N 10 15 20 N R1 (IIIC) у якій замісники є такими, як визначено вище, з активуючим реагентом, таким як 1,1’карбонілдіімідазол, необов'язково в присутності розріджувача та необов'язково в присутності засобу, що сприяє проходженню реакції; та вилучення отриманої сполуки формули (IIID) у вільній формі або у формі солі, та необов'язково перетворення отриманої сполуки формули (IIID) в іншу сполуку формули (IIID), та/або перетворення отриманої солі сполуки формули (IIID) в іншу її сіль, та/або перетворення отриманої вільної сполуки формули (IIID) в її сіль, та/або відділення отриманого ізомеру сполуки формули (IIID) від одного або більшої кількості різних отриманих ізомерів формули (IIID). Даний винахід також відноситься до сполук формули (VI) або їх солей R3 N N N N S O (VI) у якій R є таким, як визначено в даному винаході, та додатково може позначати галоген. Даний винахід також відноситься до способів одержання сполуки формули (VI). В принципі, можна використовувати всі відомі способи, що підходять для такого перетворення, із застосуванням відповідної вихідної речовини. Таким чином, даний винахід також відноситься до способу одержання сполуки формули (IIID), який включає реакцію сполуки формули (IIX) R3 N NH2 S 3 25 O (IIX) у якій R є таким, як визначено для формули (I), та додатково може позначати галоген, з ацеталем диметилформаміду, таким як диметилацеталь ДМФА, з одержанням сполуки формули (VI); вилучення отриманої сполуки формули (IIID) у вільній формі або у формі солі, та необов'язково перетворення отриманої сполуки формули (IIX) в іншу сполуку формули (IIX), та/або перетворення отриманої солі сполуки формули (IIX) в іншу її сіль, та/або перетворення отриманої вільної сполуки формули (IIX) в її сіль, та/або відділення отриманого ізомеру сполуки формули (IIX) від одного або більшої кількості різних отриманих ізомерів формули (IIX). Сполуки формули (I), 3 30 35 14 UA 104147 C2 3 H N N R S N O O NH2 A 2 R 1 R 5 10 15 20 25 30 35 40 45 50 (I), також включають сполуки субформул (IA), (IB) та їх фармацевтично прийнятні солі, у якій A позначає гетероарил; 1 R позначає (1) необов'язково заміщений алкіл; (2) необов'язково заміщений циклоалкіл; (3) необов'язково заміщений арил; (4) необов'язково заміщений амін; (5) необов'язково заміщений сульфоніл; (6) галоген; 2 1 R позначає водень, дейтерій або замісник, визначений для R ; 3 R позначає водень, галоген, необов'язково заміщений алкіл; застосовні як лікарські засоби. Тому в одному варіанті здійснення даний винахід відноситься до композицій, призначеним для застосування в медицині або ветеринарії, коли показано інгібування PI3K. Цей варіант здійснення також включає сполуку (S)-піролідин-1,2-дикарбонової кислоти 2-амід, 1-({5-[2-(трет-бутил)-піримідин-4-іл]-4-метилтіазол-2-іл}-амід, але альтернативно виключає вказану сполуку. В одному варіанті здійснення даний винахід відноситься до лікування клітинних проліферативних захворювань, таких як пухлини та/або ріст ракових клітин, опосередковуваних за допомогою PI3K. Захворювання можуть включати такі, при яких спостерігаються надекспресування або ампліфікація PI3K-альфа, соматичні мутації PIK3CA або мутації зародкового типу або соматичні мутації PTEN або мутації та транслокації p85, які забезпечують підвищувальну регуляцію комплексу p85-p110. Зокрема, ці сполуки застосовні для лікування ракових захворювань людини або тварини (наприклад, миші), включаючи, наприклад, саркому, ракові захворювання легенів, бронхів, передміхурової залози, молочної залози (включаючи спорадичні ракові захворювання молочної залози та страждаючих на хворобу Коудена), підшлункової залози, шлунково-кишковий рак, товстої кишки, прямої кишки, карциному товстої кишки, колоректальну аденому, щитовидної залози, печінки, внутрішньопечіночних жовчних проток, гепатоцелюлярні, надниркових залоз, шлунку, гліому, гліобластому, ендометрію, меланому, нирок, ниркових лоханок, сечового міхура, тіла матки, шейки матки, піхви, яєчників, множинну мієлому, стравоходу, лейкоз, гострий мієлолейкоз, хронічний мієлолейкоз, лімфолейкоз, мієлолейкоз, головного мозку, карциному головного мозку, порожнини рота та глотки, гортані, тонкого кишечнику, неходжкінську лімфому, меланому, ворсинчасту аденому товстої кишки, неоплазію, неоплазію епітеліального характеру, лімфоми, карциному молочної залози, базально-клітинну карциному, плоскоклітинну карциному, старечий кератоз, пухлинні захворювання, включаючи сóлідні пухлини, пухлини голови та шиї, справжню поліцитемію, есенціальну тромбоцитемію, мієлофіброз із мієлоїдною метаплазією та хворобу Вальденстрема. В інших варіантах здійснення патологічний стан або порушення (наприклад, опосередковане за допомогою PI3K) вибране з групи, що включає: справжню поліцитемію, есенціальну тромбоцитемію, мієлофіброз із мієлоїдною метаплазією, астму, ХОЗЛ (хронічне обструктивне захворювання легенів), ГРДС (гострий респіраторний дистресс синдром), синдром Леффлера, еозинофільну пневмонію, зараження паразитами (зокрема, багатоклітинними) (включаючи тропічну еозинофілію), бронхолегеневий аспергілез, нодозний поліартерііт (включаючи синдром Черджа-Строса), еозинофільну гранулему, пов'язані з еозинофілами порушення, що впливають на дихальні шляхи, викликані реакцією на лікарський засіб, псоріаз, контактний дерматит, атопічний дерматит, гніздну алопецію, багатоформну еритему, герпетриформний дерматит, склеродерму, вітиліго, алергійний васкуліт, уртикарію, булезний пемфігоїд, червоний вовчак, пухирчатку, вроджений булезний епідермоліз, аутоімуннізахворювання крові (наприклад, гемолітичну анемію, апластичну анемію, справжню еритроцитарну анемію та ідіопатичну тромбоцитопенію), системний червоний вовчак, поліхондрію, склеродерму, гранулематоз Вегенера, дерматоміозит, хронічний активний гепатит, злоякісну міастенію, синдром СтівенсаДжонсона, ідіопатичне спру, аутоімунне запальне захворювання кишечнику (наприклад, виразковий коліт та хвороба Крона), ендокринну офтальмопатію, дифузійний токсичний зоб, саркоїдоз, альвеоліт, хронічний гіперчутливий пневмоніт, розсіяний склероз, первинний біліарний цироз, увеїт (передній та задній), інтерстиціальний фіброз легенів, псоріатичний 15 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 60 артрит, гломерулонефрит, серцево-судинні захворювання, атеросклероз, гіпертензію, тромбоз глибоких вен, удар, інфаркт міокарда, нестабільну стенокардію, тромбоемболію, емболію легенів, тромболітичні захворювання, гостру артеріальну ішемію, тромботичні оклюзії периферійних судин та ішемічну хворобу серця, реперфузійні ураження, ретинопатію, таку як діабетична ретинопатія або викликана киснем гіпербарична ретинопатія, та патологічні стани, що характеризуються підвищеним внутрішньоочним тиском або секрецією внутрішньоочної рідини, такі як глаукома. Для зазначених вище випадків застосування необхідна доза, зрозуміло, буде мінятися залежно від шляху введення, конкретного патологічного стану, що піддається лікуванню, та необхідного ефекту. Звичайно вказують, що задовільні результати систематично забезпечуються при добових дозах, рівних від приблизно 0,03 до приблизно 100,0 мг/(кг маси тіла), наприклад, від приблизно 0,03 до приблизно 10,0 мг/(кг маси тіла). Показана добова доза для великого ссавця, наприклад, людини, знаходиться в діапазоні від приблизно 0,5 мг до приблизно 3 г, наприклад, від приблизно 5 мг до приблизно 1,5 г, та її звичайно вводять, наприклад, у вигляді розділених доз до 4 разів на добу або у формі пролонгованої дії. Разові дозовані форми, що підходять для перорального введення, містять від приблизно 0,1 до приблизно 500 мг, наприклад, від приблизно 1,0 до приблизно 500 мг активного інгредієнту. Сполуки формули (I) можна вводити будь-яким підходящим шляхом, зокрема, ентерально, наприклад, перорально, наприклад, у вигляді таблеток або капсул, або парентерально, наприклад, у вигляді розчинів або суспензій для ін'єкцій, місцево, наприклад, у вигляді лосьйонів, гелів, мазей або кремів, шляхом інгаляції, назально або у формі супозиторію. Сполуки формули (I) можна вводити у вільній формі або у формі фармацевтично прийнятної солі, наприклад, як зазначено вище. Такі солі можна одержати звичайним чином та вони мають активність такого ж порядку, як вільні сполуки. Таким чином, даний винахід також відноситься до: - способу попередження або лікування патологічних станів, порушень або захворювань, опосередкованих активацією ферменту PI3K (наприклад, кінази PI3-альфа), наприклад, таких, як вказано вище, у суб'єкта, що потребує такого лікування, який включає введення зазначеному суб'єкту сполуки формули (I) або її фармацевтично прийнятної солі у ефективній кількості; - сполуки формули (I) у вільній формі або у формі фармацевтично прийнятної солі як лікарського засобу, наприклад, у будь-якому зі способів, зазначених в даному винаході; - сполуки формули (I) у вільній формі або у формі фармацевтично прийнятної солі, призначеної для застосування як лікарського засобу, наприклад, у будь-якому зі способів, зазначених в даному винаході, переважно для застосування при одному або більшій кількості захворювань, що опосередковуються фосфатидилінозит-3-кіназою; - застосування сполуки формули (I) у вільній формі або у формі фармацевтично прийнятної солі у будь-якому зі способів, зазначених в даному винаході, зокрема, для лікування одного або більшої кількості захворювань, опосередкованих фосфатидилінозит-3-кіназою; - застосування сполуки формули (I) у вільній формі або у формі фармацевтично прийнятної солі у будь-якому зі способів, зазначених в даному винаході, зокрема, для приготування лікарського засобу, призначеного для лікування одного або більшої кількості захворювань, опосередкованих фосфатидилінозит-3-кіназою. PI3K виступають як вузол других месенджерів, який об'єднує паралельні шляхи передачі сигналів, та з'являється все більше даних про те, що комбінація інгібітору PI3K з інгібіторами інших шляхів буде застосовна для лікування раку та проліферативних захворювань у людей. Приблизно у 20-30 % людей, що страждають на рак молочної залози, надекспресується Her2/neu-ErbB2, мішень для лікарського препарату трастузумаб. Хоча показано, що трастузумаб приводить до тривалих відповідей у деяких пацієнтів, у яких експресується Her2/neu-ErbB2, відповідь спостерігається тільки у частини цих пацієнтів. Останні дослідження показали, що таку обмежену відповідь можна суттєво покращити за допомогою комбінації трастузумаба з інгібіторами шляху PI3K або PI3K/AKT (Chan et al., Breast Can. Res. Treat. 91:187 (2005), Woods Ignatoski et al., Brit. J. Cancer 82:666 (2000), Nagata et al., Cancer Cell 6:117 (2004)). При різних злоякісних захворюваннях людей відбуваються активуючі мутації або спостерігається підвищений вміст Her1/EGFR та для впливу на цю рецепторну тирозинкіназу розроблений цілий ряд антитіл та невеликих молекул-інгібіторів, у тому числі тарцева, гефітиніб та ербитукс. Однак, хоча інгібітори EGFR проявляють протипухлинну активність по відношенню до деяких пухлин людини (наприклад, NSCLC), вони не збільшують загальну виживаність для всіх пацієнтів, у яких є пухлини, що експресують EGFR. Це можна пояснити тим, що для багатьох мішеней Her1/EGFR, розташованих нижче в шляху передачі сигналу, включаючи шлях PI3K/Akt, з високою частотою відбуваються мутації або порушення регуляції при різних 16 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 60 злоякісних проявах. Наприклад, за даними досліджень in vitro гефітиніб пригнічує ріст лінії клітин аденокарциноми. Однак можна вибрати субклони цих ліній клітин, які резистентні до впливу гефітинібу та в яких спостерігається посилена активація шляху PI3/Akt. Понижувальна регуляція або інгібування цього шляху робить резистентні субклони чутливими до гефітинібу (Kokubo et al., Brit. J. Cancer 92:1711 (2005)). Крім того, у моделі раку молочної залози in vitro з використанням лінії клітин, у яких схована мутація PTEN та відбувається надекспресування EGFR, інгібування та шляху PI3K/Akt, та EGFR приводить до синергетичного ефекту (She et al., Cancer Cell 8:287-297(2005)). Ці результати показують, що комбінація гефітинібу та інгібіторів шляху PI3K/Akt, імовірно, буде привабливою методологією для лікування раку. У моделі ксенотрансплантату гліобластоми комбінація AEE778 (інгібітор Her-2/neu/Erbb2, VEGFR та EGFR) та RAD001 (інгібітор mTOR, розташований у прямому напрямку в шляху передачі сигналу мішені Akt) приводить до більшої сумарної ефективності, ніж при використанні цих засобів окремо (Goudar et al., Mol. Cancer. Ther. 4:101-112 (2005)). Антиестрогени, такі як тамоксифен, пригнічують ріст раку молочної залози, викликаючи зупинку клітинного циклу, для якої необхідний вплив інгібітору p27Kip клітинного циклу. Нещодавно показано, що активація шляху кінази Ras-Raf-MAP змінює стан фосфорилювання p27Kip, таким чином, що послабляється його інгібуючий вплив при зупинці клітинного циклу, що сприяє резистентності до антиестрогенів (Donovan, et al, J. Biol. Chem. 276:40888, 2001). Як показано в публікації Donovan et al., інгібування сигнального шляху MAPK шляхом лікування інгібітором MEK обертає аномальний стан фосфорилювання p27 у випадку резистентних до гормону ліній клітин раку молочної залози та тим самим відновлює чутливість до гормону. Аналогічним чином, фосфорилюваня p27Kip за допомогою Akt також усуває його вплив при зупинці клітинного циклу (Viglietto et al., Nat Med. 8:1145 (2002)). Відповідно до цього в іншому об'єкті сполуки формули (I) застосовуються для лікування залежних від гормонів типів раку, таких як рак молочної та передміхурової залози. Їх застосування спрямоване на обернення резистентності до гормонів, що звичайно спостерігається для цих типів раку при використанні звичайних протиракових засобів. При ракових захворюваннях крові, таких як хронічний мієлолейкоз (ХМЛ), транслокація хромосом відповідальна за конститутивно активовану BCR-Abl тирозинкіназу. Страждаючі цими захворюваннями пацієнти реагують на іматиніб, невелику молекулу - інгібітор тирозинкінази, внаслідок інгібування активності кінази Abl. Однак на прогресуючій стадії захворювання багато пацієнтів спочатку реагують на іматиніб, але потім відбувається рецидив внаслідок мутацій, що приводять до резистентності, у домені кінази Abl. Дослідження in vitro показали, що для надання впливу BCR-Ab1 використовує шлях кінази Ras-Raf. Крім того, інгібування на тому ж шляху більше однієї кінази приводить до додаткового захисту від мутацій, що приводять до резистентності. Відповідно до цього в іншому об'єкті сполуки формули (I) застосовують у комбінації щонайменше з одним додатковим засобом, вибраним з групи інгібіторів кінази, таким як глеєвек, для лікування ракових захворювань крові, таких як хронічний мієлолейкоз (ХМЛ). Їх застосування спрямоване на обернення або попередження резистентності по відношенню до зазначеного щонайменше одного додаткового засобу. Оскільки активація шляху PI3K/Akt сприяє виживанню клітин, інгібування цього шляху в комбінації із засобами, які сприяють апоптозу ракових клітин, включаючи променеву терапію та хіміотерапію, приведе до поліпшеної відповіді (Ghobrial et al., CA Cancer J. Clin 55:178-194 (2005)). Прикладом є комбінація інгібітору кінази PI3 з карбоплатином, яка виявляє синергетичний ефект при дослідженнях проліферації та апоптозу in vitro, а також при дослідженнях ефективності впливу на пухлину in vivo з використанням моделі ксенотрансплантату раку яєчників (Westfall та Skinner, Mol. Cancer Ther 4:1764-1771 (2005)). З'являється усе більше даних про те, що інгібітори PI3-кіназ класів 1A та 1B можуть мати терапевтичну цінність не тільки при раку та проліферативних захворюваннях, але та при інших типах захворювань. Встановлене, що інгібування p110, ізоформи PI3K, що є продуктом гену PIK3CB, може брати участь в індукуємій зрушенням активації тромбоцитів (Jackson et al., Nature Medicine 11:507-514 (2005)). Таким чином, інгібітор PI3K, який інгібує p110, можна застосовувати як єдиний засіб або в комбінації з антитромботичною терапією. Ізоформа p110, яка є продуктом гену PIK3CD, є важливою для B- клітинної функції та диференціації (Clayton et al., J. Exp. Med. 196:753-763 (2002)), а також для залежних та незалежних від Т-клітин імунних відповідей (Jou et al., Mol. Cell. Biol. 22:8580-8590 (2002)) та диференціації мастоцитів (Ali et al., Nature 431:1007-1011 (2004)). Таким чином, слід очікувати, що інгібітори p110 можуть бути застосовними для лікування пов'язаних з В-клітинами аутоімунних захворювань та астми. Нарешті, інгібування p110, ізоформи, що є продуктом гену PI3KCG, приводить до зниженої Т 17 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 60 клітинної, але не В-клітинної відповіді (Reif et al., J. Immunol. 173:2236-2240 (2004)) та ефективність інгібування цієї ізоформи продемонстрована на моделях аутоімунних захворювань на тваринах (Camps et al., Nature Medicine 11:936-943 (2005), Barber et al., Nature Medicine 11:933-935 (2005)). Даний винахід також відноситься до фармацевтичних композицій, що включають щонайменше одну сполуку формули (I) разом з фармацевтично прийнятним інертним наповнювачем, придатним для введення людині або тварині окремо або разом з іншими протираковими засобами. Даний винахід також відноситься до способів лікування людей або тварин, що страждають від клітинного проліферативного захворювання, такого як рак. Таким чином, даний винахід відноситься до способів лікування людини або тварини, що потребує такого лікування, що включають введення суб'єкту сполуки формули (I) окремо або в комбінації з іншими протираковими засобами в терапевтично ефективній кількості. Зокрема, композиції можна приготувати спільно у вигляді комбінованого лікарського засобу або вводити окремо. Протиракові засоби, що підходять для застосування разом із сполукою формули (I), включають, але не обмежуються тільки ними, одну або більшу кількість сполук, вибраних з групи, що включає інгібітори кінази, антиестрогени, антиандрогени, інші інгібітори, хіміотерапевтичні протиракові лікарські засоби, алкілуючі засоби, хелатні засоби, модифікатори біологічної відповіді, протиракові вакцини, засоби антизначеннєвої терапії, наведені нижче: A. Інгібітори кінази: Інгібітори кінази, призначені для застосування як протиракові засоби разом із сполукою формули (I), включають інгібітори кіназ рецептору епідермального фактору росту (EGFR), такі як невеликі молекули хіналозинів, наприклад, гефітиніб (US 5457105, US 5616582 та US 5770599), ZD-6474 (WO 01/32651), ерлотиніб (тарцева, US 5747498 та WO 96/30347) та лапатиніб (US 6727256 та WO 02/02552), інгібітори кіназ рецептору судинного ендотеліального фактору росту (VEGFR), включаючи SU-11248 (WO 01/60814), SU 5416 (US 5883113 та WO 99/61422), SU 6668 (US 5883113 та WO 99/61422), CHIR-258 (US 6605617 та US 6774237), ваталаніб або PTK-787 (US 6258812), VEGF-Trap (WO 02/57423), B43-геністеїн (WO09606116), фенретинід (п-гідроксифеніламіноретиноєва кислота) (US 4323581), IM-862 (WO 02/62826), бевацизумаб або авастин (WO 94/10202), KRN-951, 3-[5(метилсульфонілпіперидинметил)-індоліл]-хінолон, AG-13736 та AG-13925, піроло[2,1f][1,2,4]триазини, ZK-304709, веглін, VMDA-3601, EG-004, CEP-701 (US 5621100), Cand5 (WO 04/09769), інгібітори тирозинкінази Erb2, такі як пертузумаб (WO 01/00245), трастузумаб та ритуксимаб, інгібітори Akt протеїнкінази, такі як RX-0201, інгібітори протеїнкінази C (PKC), такі як LY-317615 (WO 95/17182) та перифосин (US 2003171303), інгібітори кінази Raf/Map/MEK/Ras, включаючи сорафеніб (BAY 43-9006), ARQ-350RP, LErafAON, BMS-354825 AMG-548 та інші, розкриті в WO 03/82272, інгібітори кінази рецептору фактору росту фібробластів (FGFR), інгібітори клітинно-залежної кінази (CDK), включаючи CYC-202 та росковітин (WO 97/20842 та WO 99/02162), інгібітори кіназ рецептору тромбоцитарного фактору росту (PDGFR), такі як CHIR-258, 3G3 mAb, AG-13736, SU-11248 та SU6668, та інгібітори кінази Bcr-Abl та білків злиття, такі як STI-571 або глеєвек (іматиніб). B. Антиестрогени: Впливаючі на естрогени засоби, призначені для застосування в протираковій терапії разом із сполукою формули (I), включають селективні модулятори естрогенного рецептору (SERMs), включаючи тамоксифен, тореміфен, ралоксифен, інгібітори ароматази, включаючи аримідекс або анастрозол, негативні регулятори естрогенного рецептору (ERDs), включаючи фаслодекс або фульвестрант. C. Антиандрогени: Впливаючі на андрогени засоби, призначені для застосування в протираковій терапії разом із сполукою формули (I), включають флутамід, бікалутамід, фінастерид, аміноглютетамід, кетоконазол та кортикостероїди. D. Інші інгібітори: Інші інгібітори, призначені для застосування як протиракові засоби разом із сполукою формули (I), включають інгібітори протеїнфарнезилтрансферази, включаючи типіфарніб або R-115777 (US 2003134846 та WO 97/21701), BMS-214662, AZD-3409 та FTI-277, інгібітори топоізомерази, включаючи мербарон та дифломотекан (BN-80915), інгібітори мітотичних кінезинових білків веретена (KSP), включаючи SB-743921 та MKI-833, модулятори протеосоми, такі як бортезоміб або велкаде (US 5780454), XL-784, та інгібітори циклооксигенази 2 (COX-2), включаючи нестероїдні протизапальні лікарські засоби I (NSAIDs). E. Хіміотерапевтичні протиракові лікарські засоби: Конкретні протиракові хіміотерапевтичні засоби, призначені для застосування як протиракові засоби разом із сполукою формули (I), включають анастрозол (аримідекс ), бікалутамід (казодекс ), блеоміцинсульфат (бленоксан), бусульфан (мілеран), бусульфан для ін'єкцій (бусульфекс ), капецитабін (кселода), N4пентоксикабоніл-5-дезокси-5-фторцитидин, карбоплатин (параплатин ), кармустин (BiCNU), 18 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 хлорамбуцил (лейкеран), цисплатин (платинол), кладрибін (лейстатин), циклофосфамід (цитоксан або неосар), цитарабін, цитозинарабінозид (цитосар-U), ліпосомний цитарабін для ін'єкцій (DepoCyt), дакарбазин (DTIC-Dome), дактиноміцин (актиноміцин D, космеган), даунорубіцингідрохлорид (церубідин ), ліпосомний даунорубіцинцитрат для ин'єкцій (DaunoXome), дексаметазон, доцетаксел (таксотер, US 2004073044), доксорубіцингідрохлорид (адріаміцин , рубекс ), етопозид (вепезид), флударабінфосфат (флудара), 5-фторурацил (адруцил, ефудекс), флутамід (ейлексин), тезацитибін, гемцитабін (дифтордезоксицитидин), гідроксисечовина (гідреа ), ідарубіцин (ідаміцин ), іфосфамід (IFEX), іринотекан (камптосар), L-аспарагіназа (ЕЛСПАР), лейковорин-кальцій, мелфалан (алкеран), 6-меркаптопурин (пуринетол), метотрексат (фолекс), мітоксандрон (новантрон), міотарг, паклітаксел (таксол), фенікс (іттрій-90/MX-DTPA), пентостатин, поліфепросан 20 з імплантатом кармустину (глиадел ), тамоксифенцитрат (нолвадекс), теніпозид (вумон), 6-тіогуанін, тіотепа, трирапазамін (тиразон), топотекангідрохлорид для ін'єкцій (гікамптин), вінбластин (велбан), вінкристин (онковін) та вінорелбін (навелбін). F. Алкілуючі засоби: Алкілуючі засоби, призначені для застосування разом із сполукою формули (I), включають VNP-40101M або клоретизин, оксаліплатин (US 4169846, WO 03/24978 та WO 03/04505), глюфосфамід, мафосфамід, етопофос (US 5041424), преднімустин, треосульфан, бусульфан, ірофлувен (ацилфульвен), пенкломедин, піразолоакридин (PD115934), O6-бензилгуанін, децитабін (5-аза-2-дезоксицитидин), бросталіцин, мітоміцин C (MitoExtra), TLK-286 (телцита), темозоломід, трабектедин (US 5478932), AP-5280 (композиція цисплатину на основі платинату), порфіроміцин, та клеаразид (меклоретамін). G. Хелатні засоби: Хелатні засоби, призначені для застосування разом із сполукою формули (I), включають тетратіомолібдат (WO 01/60814), RP-697, хімерик T84.66 (cT84.66), гадофосвесет (вазовіст), дефероксамін та блеоміцин, необов'язково у сполученні з електропорацією (EPT). H. Модифікатори біологічної відповіді: Модифікатори біологічної відповіді, такі як імунномодулятори, призначені для застосування разом із сполукою формули (I), включають стауроспорин та його макроциклічні аналоги, включаючи UCN-01, CEP-701 та мідостаурин (див. WO 02/30941, WO 97/07081, WO 89/07105, US 5621100, WO 93/07153, WO 01/04125, WO 02/30941, WO 93/08809, WO 94/06799, WO 00/27422, WO 96/13506 та WO 88/07045), скваламін (WO 01/79255), DA-9601 (WO 98/04541 та US 6025387), алемтузумаб, інтерферони (наприклад, IFN-a, IFN-b та т. п.), інтерлейкіни, переважно IL-2 або алдеслейкін, а також IL-1, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12 та їх активні біологічні варіанти, що містять амінокислотні послідовності, що становлять більше 70 % від нативної послідовності людини, алтретамін (гексален), SU 101 або лефлуномід (WO 04/06834 та US 6331555), імідазохіноліни, такі як ресихімод та іміхімод (US 4689338, 5389640, 5268376, 4929624, 5266575, 5352784, 5494916, 5482936, 5346905, 5395937, 5238944 та 5525612), та SMIPs (невеликі молекули, що модулюють імунофармацевтичні засоби), включаючи бензазоли, антрахінони, тіосемікарбазони та триптантрини (WO 04/87153, WO 04/64759 та WO 04/60308). I. Протиракові вакцини: Протиракові вакцини, призначені для застосування разом із сполукою формули (I), включають авіцин (Tetrahedron Lett. 26:2269-70 (1974)), ореговомаб (OvaRex), тератоп (STn-KLH), вакцини проти мелатоми, серія GI-4000 (GI-4014, GI-4015 та GI4016), націлені на 5 мутацій білку Ras, GlioVax-1, MelaVax, адвексин або INGN-201 (WO 95/12660), Sig/E7/LAMP-1, кодуючий HPV-16 E7, вакцину MAGE-3 або M3TK (WO 94/05304), HER-2VAX, ACTIVE, який стимулює T-клітини, специфічні для пухлин, протиракову вакцину GMCSF та вакцини на основі моноцитогенів Listeria. J. Засоби антисмислової терапії: Протиракові засоби, призначені для застосування разом із сполукою формули (I), також включають анти смислові композиції, такі як AEG-35156 (GEM640), AP-12009 та AP-11014 (TGF-бета-2-специфічні антисмислові олігонуклеотиди), AVI-4126, AVI-4557, AVI-4472, облімерсен (генасенсе), JFS2, апринокарсен (WO 97/29780), GTI-2040 (антисмисловий олігонуклеотид, що впливає на R2 рибонуклеотидредуктази мРНК) (WO 98/05769), GTI-2501 (WO 98/05769), капсульовані в ліпосомах антисмислові олігодезоксинуклеотиди c-Raf (LErafAON) (WO 98/43095), та Sirna-027 (основані на імунній РНК лікарські засоби, що впливають на VEGFR-1 мРНК). Сполуку формули (I) також можна об'єднати в фармацевтичній композиції з бронхорозширюючими або антигістамінними лікарськими речовинами. Такі бронхорозширюючі лікарські засоби включають антихолінергічні або антимускаринові засоби, зокрема, глікопіролат, іпратропійбромід, окситропійбромід та тіотропійбромід, OrM3, аклідиній, CHF5407, GSK233705 та агоністи β-2-адренорецептору, такі як салбутамол, тербуталін, салметерол, кармотерол, мілветерол та, переважно, індакатерол та формотерол. Разом застосовні терапевтичні 19 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 60 антигістамінні лікарські речовини включають цетиризингідрохлорид, клемастин фумарат, прометазин, лоратадин, дезлоратадин, дифенгідрамін та фексофенадингідрохлорид. Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та одну або більшу кількість сполук, які застосовні для лікування тромболітичного захворювання, захворювання серця, удару тощо. Такі сполуки включають аспірин, стрептокіназу, активатор плазміногену тканини, урокіназу, антикоагулянт, лікарські засоби, що перешкоджають агрегації тромбоцитів (наприклад, ПЛАВІКС; клопідогрелбісульфат), статин (наприклад, ЛІПІТОР або кальцієва сіль аторвастатину), ЗОКОР (симвастатин), КРЕСТОР (росувастатин) та т. п.), бетаблокатор (наприклад, атенолол), НОРВАСК (амлодипінбезилат) та інгібітор АХЕ (ацтилхолинестерази) (наприклад, лізиноприл). Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та одну або більшу кількість сполук, які застосовні для лікування гіпертензії. Такі сполуки включають інгібітори АХЕ, засоби, що знижують вміст ліпідів, такі як статини, ЛІПІТОР (кальцієва сіль аторвастатину), блокатори кальцієвих каналів, такі як НОРВАСК (амлодипінбезилат). Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та одну або більшу кількість сполук, вибраних з групи, що включає фібрати, бета-блокатори, інгібітори NEPI, антагоністи ангіотензинового рецептору 2 та засоби, що перешкоджають агрегації тромбоцитів. Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та сполуку, застосовну для лікування запальних захворювань, включаючи ревматоїдний артрит. Таку сполуку можна вибрати з групи, що включає інгібітори TNF-, такі як анти-TNF- моноклональні антитіла (такі як РЕМІКАДЕ, CDP-870) та D2E7 (ГУМІРА) та молекули імуноглобуліну злиття рецептору TNF (такі як ЕМБРЕЛ), інгібітори IL-1, антагоністи рецептору розчинного IL-1R (наприклад, КІНЕРЕТ або інгібітори ICE), нестероїдні протизапальні лікарські засоби (НПЗЛЗ), піроксикам, диклофенак, напроксен, флурбіпрофен, фенопрофен, кетопрофен, ібупрофен, фенамати, мефенамінову кислоту, індометацин, суліндак, апазон, піразолони, фенілбутазон, аспірин, інгібітори COX-2 (такі як ЦЕЛЕБРЕКС (целекоксиб), ПРЕКСИГ (луміракоксиб)), інгібітори металопротеази (переважно селективні інгібітори MMP-13), p2 × 7 інгібітори, α2α інгібітори, НЕЙРОТИН, прегабалін, що застосовується в низькій дозі метотрексат, лефлуномід, гідроксихлорхін, d-пеніциламін, ауранофін або препарати золота, що вводять парентерально або перорально. Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та сполуку, застосовну для лікування остеоартриту. Таку сполуку можна вибрати з групи, що включає стандартні нестероїдні протизапальні лікарські засоби (далі НПЗЛЗ), такі як піроксикам, диклофенак, пропіонові кислоти, такі як, напроксен, флурбіпрофен, фенопрофен, кетопрофен та ібупрофен, фенамати, такі як мефенамінова кислота, індометацин, суліндак, апазон, піразолони, такі як фенілбутазон, саліцилати, такі як аспірин, інгібітори COX-2, такі як целекоксиб, валдекоксиб, луміракоксиб та еторикоксиб, анальгетики та внутрісуглобні лікарські засоби, такі як кортикостероїди, та гіалуронові кислоти, такі як гіалган та синвіск. Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та противірусний засіб та/або антисептичну сполуку. Такий противірусний засіб можна вибрати з групи, що включає вірацепт, AZT, ацикловір та фамцикловір. Таку антисептичну сполуку можна вибрати з групи, що включає валант. Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та один або більшу кількість засобів, вибраних з групи, що включає засоби, що діють на ЦНС (центральна нервова система), такі як антидепресанти (сертралін), лікарські засоби для лікування хвороби Паркінсона (такі як депреніл, L-дофа, реквіп, мірапекс, інгібітори MAOB, такі як селегін та расагілін, інгібітори comP, такі як тасмар, інгібітори A-2, інгібітори повторного всмоктування допаміну, антагоністи NMDA, агоністи нікотину, агоністи допаміну та інгібітори нейронної синтази оксиду азоту). Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та один або більшу кількість лікарських засобів для лікування хвороби Альцгеймера. Такий лікарський засіб для лікування хвороби Альцгеймера можна вибрати з групи, що включає донепезил, такрин, α2δ-інгібітори, НЕЙРОТИН, прегабалін, інгібітори COX-2, пропентофілін та метрифонат. Іншим об'єктом даного винаходу є комбінація, що включає сполуку формули (I) та засоби для лікування остеопорозу та/або імунодепресивний засіб. Такі засоби для лікування остеопорозу можна вибрати з групи, що включає ЕВІСТА (ралоксифенгідрохлорид), дролоксифен, лазофоксифен та фосамакс. Такі імунодепресивні засоби можна вибрати з групи, що включає FK-506 та рапаміцин. В інших кращих варіантах здійснення даний винахід відноситься до наборів, які включають одну або більшу кількість сполук формули (I) компонент комбінації, розкритий в даному 20 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 55 винаході. Типові набори включають інгібітор PI3K (наприклад, сполука формули (I)) та аркушвкладиш або інше маркування, що містить вказівку для лікування клітинного проліферативного захворювання шляхом введення інгібуючої PI3K кількості сполуки (сполук). Звичайно сполуки формули (I) вводять в терапевтично ефективній кількості за будь-яким із загальноприйнятих шляхів введення засобів, які призначені для аналогічних цілей. Використовувана кількість сполуки формули (I), тобто активного інгредієнту, буде залежати від безлічі факторів, таких як важкість захворювання, що піддають лікуванню, вік та відносний стан здоров'я суб'єкта, активність сполуки, що використовується, шлях та форма введення та інших факторів. Лікарський засіб можна вводити більше одного разу на добу, переважно один або два рази на добу. Усі ці фактори знаходяться у межах компетенції лікаря. Терапевтично ефективні кількості сполук формули I можуть бути в діапазоні від приблизно 0,05 до приблизно 50 мг/(кг маси тіла) реципієнта на добу; переважно приблизно 0,1-25 мг/кг/добу, більш переважно приблизно від 0,5 до 10 мг/кг/добу. Так, для введення пацієнтові масою 70 кг найбільш кращий діапазон доз становить приблизно 35-70 мг на добу. Звичайно сполуки формули (I) вводять у вигляді фармацевтичних композицій за будь-яким з наступних шляхів: перорально, системно (наприклад, крізьшкірно, назально або за допомогою супозиторію) або парентерально (наприклад, внутрім'єязово, внутрішньовенно або підшкірно). Кращим шляхом введення є пероральний з використанням звичайного добового режиму, який можна змінити у відповідності зі ступенем ураження. Композиції можуть бути у формі таблеток, пігулок, капсул, напіврідких речовин, порошків, препаратів пролонгованої дії, розчинів, суспензій, еліксирів, аерозолів або будь-яких інших підходящих композицій. Іншим кращим шляхом введення сполук формули (I) є інгаляція. Вона є ефективною методикою доставки терапевтичного засобу безпосередньо в дихальні шляхи. Вибір композиції залежить від різних факторів, таких як шлях введення лікарського засобу та біологічна доступність лікарської речовини. Для доставки шляхом інгаляції сполуки можна приготувати у вигляді рідкого розчину, суспензій, аерозольного препарату або сухого порошку та помістити в дозуючий пристрій, що підходить для введення. Є кілька типів фармацевтичних пристроїв для інгаляції - інгалятори типу небулайзера, мірні дозуючі інгалятори (МДІ) та інгалятори для сухих порошків (ІСП). В обладнаннях типу небулайзера утворюється потік повітря високої швидкості, який розпорошує терапевтичний засіб (який приготовлено в рідкій формі) у повітряну дисперсію, яка попадає в дихальні шляхи пацієнта. МДІ звичайно містять композицію разом із стисненим газом. Після активації пристрою викидає відмірену кількість терапевтичного засобу за допомогою стисненого газу та в такий спосіб є надійним засобом введення заданої кількості засобу. ІСП дозує терапевтичні засоби у вигляді сипучого порошку, який може диспергуватися у вдихуваному пацієнтом потоці повітря. Для одержання сипучого порошку терапевтичний засіб готують разом з інертним наповнювачем, таким як лактоза. Певна кількість терапевтичного засобу зберігається у вигляді капсули та подається при кожному спрацьовуванні. Даний винахід також відноситься до композицій, у яких розмір часток сполуки формули (I) знаходиться в діапазоні 10 – 1000 нм, переважно 10 - 400 нм. Такі фармацевтичні композиції розроблені спеціально для лікарських засобів, що мають низьку біологічну доступність, основані на тому, що біологічну доступність можна поліпшити шляхом збільшення площі поверхні, тобто зменшення розміру часток. Наприклад, в U.S. № 4107288 описана фармацевтична композиція, що має частки з розміром у діапазоні приблизно від 10 до 1000 нм, у якій активна речовина нанесена на матрицю з зшитих макромолекул. В U.S. № 5145684 описане приготування фармацевтичної композиції, у якій лікарську речовину розпорошують у наночастинки (середній розмір часток становить 400 нм) у присутності модифікатора поверхні та потім диспергують у рідкому середовищі та отримують фармацевтичну композицію, що має досить високу біологічну доступність. Обидва документа включені в даний винахід як посилання. Іншим об'єктом даного винаходу є фармацевтичні композиції, що містять (терапевтично ефективну кількість) сполуки формули (I) та щонайменше один фармацевтично прийнятний інертний наповнювач. Прийнятні інертні наповнювачі є нетоксичними, сприяють введенню та не виявляють несприятливого впливу на терапевтичні характеристики сполуки формули I. Такий інертний наповнювач може бути будь-яким твердим, рідким, напіврідким або, у випадку аерозольної композиції, газоподібним інертним наповнювачем, які звичайно є в розпорядженні фахівця в даній галузі техніки. Тверді фармацевтичні інертні наповнювачі включають крохмаль, целюлозу, тальк, глюкозу, лактозу, сахарозу, желатин, солод, рис, борошно, крейду, силікагель, стеарат магнію, стеарат натрію, гліцеринмоностеарат, хлорид натрію, сухе знежирене молоко тощо. 21 UA 104147 C2 5 10 15 20 25 30 35 40 45 50 Рідкі та напіврідкі інертні наповнювачі можна вибрати з групи, що включає гліцерин, пропіленгліколь, воду, етанол та різні масла, включаючи отримані з нафти, тварин, рослинного або синтетичного походження, наприклад, арахісове масло, соєве масло, мінеральне масло, кунжутне масло тощо. Кращі рідкі носії, особливо призначені для розчинів для ін'єкцій, включають воду, фізіологічний розчин, водний розчин декстрози та гліколі. Стиснені гази можна використовувати для диспергування сполуки формули I в аерозольній формі. Інертними газами, що підходять для цієї мети, є азот, діоксид вуглецю та т.п. Інші підходящі фармацевтично прийнятні інертні наповнювачі та їх композиції описані в публікації Remington's Pharmaceutical Sciences, edited by E. W. Martin (Mack Publishing Company, l8th ed., l990). Кількість сполуки в композиції може мінятися в широких межах, що використовуються фахівцями в даній галузі техніки. Звичайно, композиція містить, у мас. %, приблизно 0,01-99,99 мас. % сполуки формули (I) у перерахуванні на повну масу композиції, а решта являють собою один або більшу кількість підходящих фармацевтичних інертних наповнювачів. Переважно, якщо сполука міститься в кількості, що становить приблизно 1-80 мас. %. Даний винахід також відноситься до фармацевтичної композиції, що включає (тобто містить або вміщує у собі) щонайменше одну сполуку формули (I) та щонайменше один фармацевтично прийнятний інертний наповнювач. Фармацевтичні композиції, що включають сполуку формули (I) у вільній формі або у формі фармацевтично прийнятної солі разом щонайменше з одним фармацевтично прийнятним інертним наповнювачем (таким як носій та/або розріджувач), можна приготувати звичайним чином шляхом змішування компонентів. Об'єднані фармацевтичні композиції, що включають сполуку формули (I) у вільній формі або у формі фармацевтично прийнятної солі та що додатково включають компонент комбінації (в одній дозованій разовій формі або у вигляді набору компонентів) разом щонайменше з одним фармацевтично прийнятним носієм та/або розріджувачем, можна приготувати звичайним чином шляхом змішування зазначених активних інгредієнтів з фармацевтично прийнятним носієм та/або розріджувачем. Таким чином, іншими об'єктами даного винаходу є: - об'єднана фармацевтична композиція, наприклад, призначена для застосування в будьякому із способів, описаних у даному винаході, що включає сполуку формули (I) у вільній формі або у формі фармацевтично прийнятної солі разом з фармацевтично прийнятним розріджувачем та/або носієм; - об'єднана фармацевтична композиція, що включає сполуку формули (I) у вільній формі або у формі фармацевтично прийнятної солі як активний інгредієнт; один або більшу кількість фармацевтично прийнятних носіїв та/або розріджувачів та необов'язково одну або більшу кількість додаткових лікарських речовин. Така об'єднана фармацевтична композиція може бути у вигляді однієї разової дози або у вигляді набору компонентів; - об'єднана фармацевтична композиція, що включає сполуку формули (I) у вільній формі або у формі фармацевтично прийнятної солі в терапевтично ефективній кількості, та другу лікарську речовину, призначену для одночасного або послідовного введення; - спосіб, визначений вище, що включає спільне введення, наприклад, одночасне або послідовне, сполуки формули (I) або її фармацевтично прийнятної солі в терапевтично ефективній нетоксичній кількості, та щонайменше другої лікарської речовини, наприклад, зазначеної вище; - фармацевтична комбінація, наприклад, набір, що включає a) перший засіб, який являє собою сполуку формули (I), розкриту в даному винаході, у вільній формі або у формі фармацевтично прийнятної солі, та b) щонайменше один засіб, що спільно вводиться, зазначений вище, та такий набір може містити інструкції з його введення. Приведені нижче приклади сполук формули (I) ілюструють даний винахід, не обмежуючи його обсяг. Способи одержання таких сполук описані нижче в даному винаході. Приклад 1: 2-Амід, 1-{[5-(2-трет-бутилпіридин-4-іл)-4-метилтіазол-2-іл]-амід} (S)-піролідин1,2-дикарбонової кислоти 22 UA 104147 C2 O O O OH O O O Толуол/ TФК NH4OH O LiHMDS, TГФ Cl Стадія 1.7 S POBr3 Стадія 1.5 Стадія 1.6 H N N Br NH2 S S O N H N N Pd(OAc)2, tBu3P.HBF4 N N H O O HCl 6N N N EtOH Cs2CO3, ДМФА Стадія 1.4 Стадія 1.3 N N N N H N N N S HN O O S NH2 L-пролінамід N NEt3 / ДМФА Стадія 1.1 5 10 15 H N N N O CH2Cl2 Стадія 1.2 N O O NH2 N Приклад 1 Et3N (1,54 мл, 11,1 ммоля, 3 екв.) додають до розчину [5-(2-трет-бутилпіридин-4-іл)-4метилтіазол-2-іл]-аміду імідазол-1-карбонової кислоти (стадія 1.1) (1,26 г, 3,7 ммоля) та Lпролінаміду (0,548 г, 4,8 ммоля, 1,3 екв.) в ДМФА (25 мл) в атмосфері аргону. Реакційну суміш перемішують впродовж 14 год. при КТ, реакцію зупиняють шляхом додавання насиченого розчину NaHCO3 та екстрагують за допомогою EtOAc. Органічну фазу промивають насиченим розчином NaHCO3, сушать (Na2SO4), фільтрують та концентрують. Залишок очищують за допомогою колонкової хроматографії на силікагелі (ДХМ/MeOH, 1:0 → 94:6), потім розтирають з Et2O та отримують 1,22 г шуканої сполуки у вигляді майже білої твердої речовини: ІЕР-МС: + 1 388,1 [M+H] ; tR=2,35 хвил. (система 1); ТШХ: Rf=0,36 (ДХМ/MeOH, 9:1). H ЯМР (400 МГц, ДМСО-d6) (част./млн): 1,32 (s, 9 H) 1,75-1,95 (m, 3 H) 1,97-2,13 (m, 1 H) 2,39 (s, 3 H) 3,38-3,50 (m, 1 H) 3,52-3,65 (m., 1 H) 4,10-4,40 (m, 1 H) 6,94 (br. s., 1 H) 7,22 (d, 1 H) 7,30-7,48 (m, 2 H) 8,49 (d, 1 H) 10,87 (br. s., 1 H). Стадія 1.1: [5-(2-Трет-бутилпіридин-4-іл)-4-метилтіазол-2-іл]-амід імідазол-1-карбонової кислоти N N S NH N 20 N O Суміш 5-(2-трет-бутилпіридин-4-іл)-4-метилтіазол-2-іламіну (стадія 1.2) (1 г, 4,05 ммоля) та 1,1’-карбонілдіімідазолу (0,984 г, 6,07 ммоля, 1,5 екв.) в ДХМ (50 мл) перемішують впродовж 4 год. при кип'ятінні із зворотним холодильником та дають охолодитися. Отриманий осад збирають фільтруванням та отримують 1,26 г шуканої сполуки у вигляді білої твердої речовини: ІЕР-МС: 340,2 [M-H] ; tR=2,85 хвил. (система 1). Стадія 1.2: 5-(2-трет-Бутилпіридин-4-іл)-4-метилтіазол-2-іламін N N S NH2 25 Суміш N-[5-(2-трет-бутилпіридин-4-іл)-4-метилтіазол-2-іл]-ацетаміду (стадія 1.3) (2 г, 7 ммоля), 6 н. водного розчину HCl (10 мл) та EtOH (50 мл) перемішують впродовж 2 год. при 85 °C, дають охолодитися, реакцію зупиняють шляхом додавання насиченого розчину NaHCO 3 23 UA 104147 C2 5 та екстрагують сумішшю ДХМ/MeOH (9:1, об./об.). Органічну фазу промивають насиченим розчином NaHCO3, сушать (Na2SO4), фільтрують та концентрують. Залишок очищують за допомогою колонкової хроматографії на силікагелі (ДХМ/MeOH, 1:0 → 96:4) та отримують 1,21 г + шуканої сполуки у вигляді жовтої твердої речовини: ІЕР-МС: 248,1 [M+H] ; ТШХ: Rf=0,36 (ДХМ/MeOH, 9:1). Стадія 1.3: N-[5-(2-трет-Бутилпіридин-4-іл)-4-метилтіазол-2-іл]-ацетамід N N S NH O 10 15 Суміш 2-ацетамідо-4-метилтіазолу (1,2 г, 7,7 ммоля, 1,1 екв.), карбонату цезію (4,55 г, 14 ммоля, 2 екв.), три-трет-бутилфосфінійтетрафторборату (0,406 г, 1,4 ммоля, 0,2 екв.), ацетату паладію(II) (0,15 г, 0,7 ммоля, 0,1 екв.) та 4-бром-2-трет-бутилпіридину (стадія 1.4) (1,5 г, 7 ммоля) в ДМФА (50 мл) перемішують впродовж 1,5 год. при 90 °C в атмосфері аргону, дають охолодитися, реакцію зупиняють шляхом додавання насиченого розчину NaHCO 3 та фільтрують через шар целіту. Фільтрат екстрагують за допомогою EtOAc. Органічну фазу промивають насиченим розчином NaHCO3, сушать (Na2SO4), фільтрують та концентрують. Залишок очищують за допомогою колонкової хроматографії на силікагелі (ДХМ/MeOH, 1:0 → 97:3) та + отримують 2,02 г шуканої сполуки у вигляді жовтої твердої речовини: ІЕР-МС: 290,1 [M+H] ; ТШХ: Rf=0,35 (ДХМ/MeOH, 9:1). Стадія 1.4: 4-Бром-2-трет-бутилпіридин Br N 20 25 Суміш 2-трет-бутил-1H-піридин-4-ону (стадія 1.5) (4,25 г, 28 ммоля) та POBr 3 (8,88 г, 31 ммоля, 1,1 екв.) нагрівають при 120 °C, перемішують впродовж 15 хвил., дають охолодитися, реакцію зупиняють шляхом додавання насиченого розчину NaHCO 3 та екстрагують сумішшю ДХМ/MeOH (9:1, об./об.). Органічну фазу промивають насиченим розчином NaHCO 3, сушать (Na2SO4), фільтрують та концентрують. Залишок очищують за допомогою колонкової хроматографії на силікагелі (Hex/EtOAc, 95:5) та отримують 5,18 г шуканої сполуки у вигляді + жовтого масла: ІЕР-МС: 214,0/216,0 [M+H] ; tR=2,49 хвил. (система 1); ТШХ: Rf=0,35 (Hex/EtOAc, 1:1). Стадія 1.5: 2-трет-Бутил-1H-піридин-4-он O N H 30 35 Суміш 2-трет-бутилпіран-4-ону (стадія 1.6) (5,74 г, 37,7 ммоля) та 30 % водного розчину гідроксиду амонію (100 мл) перемішують впродовж 1 год. при кип'ятінні із зворотним холодильником, дають охолодитися та концентрують. Залишок розтирають з MeOH (200 мл) та фільтрують. Фільтрат концентрують та залишок очищують за допомогою колонкової водн. хроматографії на силікагелі (ДХМ/MeOH/NH3 , 94:5:1 → 92:7:1) та отримують 4,46 г шуканої + сполуки у вигляді жовтої твердої речовини: ІЕР-МС: 152,0 [M+H] ; tR=1,45 хвил. (система 1); ТШХ: Rf=0,11 (ДХМ/MeOH, 9:1). Стадія 1.6: 2-трет-Бутилпіран-4-он O O 40 Суміш 5-гідрокси-1-метокси-6,6-диметилгепта-1,4-дієн-3-ону (стадія 1.7) (6,8 г, 36,9 ммоля) та ТФК (5,65 мл, 74 ммоля, 2 екв.) в бензолі (250 мл) перемішують впродовж 14 год. при КТ та 24 UA 104147 C2 концентрують. Очищення залишку за допомогою колонкової хроматографії на силікагелі (Hex/EtOAc, 1:0 → 75:25) забезпечує одержання 5,74 г шуканої сполуки у вигляді жовтого масла: + ІЕР-МС: 153,1 [M+H] ; tR=3,21 хвил. (система 1); ТШХ: Rf=0,22 (Hex/EtOAc, 1:1). Стадія 1.7: 5-Гідрокси-1-метокси-6,6-диметилгепта-1,4-дієн-3-он OH O O 5 10 15 LiHMDS (1M в ТГФ, 100 мл, 2 екв.) по краплям додають до холодного (-78 °C) розчину 4метокси-3-бутен-2-ону (10 мл, 100 ммоля, 2 екв.) в ТГФ (400 мл). Після 30 хвил. перемішування при -78 °C додають розчин півалоїлхлорид (6,12 мл, 50 ммоля) в ТГФ (100 мл). Отриманій суміші дають нагріватися до КТ впродовж 2 год. та реакцію зупиняють шляхом додавання насиченого розчину NH4Cl. ТГФ видаляють у вакуумі. Концентровану суміш екстрагують за допомогою Et2O. Органічну фазу промивають сольовим розчином, сушать (Na 2SO4), фільтрують та концентрують. Залишок очищують за допомогою колонкової хроматографії на силікагелі (Hex/EtOAc, 1:0 → 85:15) та отримують 6,83 г шуканої сполуки у вигляді жовтого масла: ІЕР-МС: + 185,1 [M+H] ; ТШХ: Rf=0,87 (Hex/EtOAc, 1:1). Приклад 2: 2-Амід, 1-{[5-(2-циклопропілпіридин-4-іл)-4-метилтіазол-2-іл]-амід} (S)-піролідин1,2-дикарбонової кислоти H N N S N O O NH2 N 20 Шукану сполуку отримують за аналогією з методикою, описаною в прикладі 1, але з наступними змінами. На стадії 1.1 реакційну суміш перемішують впродовж 4 год. при кип'ятінні із зворотним холодильником. На стадії 1.2 реакційну суміш перемішують впродовж 2 год. при 85 °C. На стадії 1.3 використовують 4-хлор-2-(1-метилциклопропіл)-піридин (стадія 2.1) та реакційну суміш перемішують впродовж 2 год. при 150 °C. Шукана сполука: ІЕР-МС: 372,1 + [M+H] ; ТШХ: Rf=0,35 (ДХМ/MeOH, 9:1). Стадія 2.1: 4-Хлор-2-циклопропілпіридин Cl N 25 30 35 40 45 Шукану сполуку отримують за модифікованою методикою, описаною в літературі [Comins, D. L.; Mantlo, N. B., Journal of Organic Chemistry, (1985), 50, 4410-4411]. Циклопропілмагнійбромід (0,5M в ТГФ, 100 мл, 50 ммоля, 2,2 екв.) однією порцією додають до холодної (-78 °C) суспензії 4-хлорпіридингідрохлориду (3,4 г, 22 ммоля) в ТГФ (68 мл). Після 10 хвил. перемішування при -78 °C по краплям додають фенілхлорформіат (2,76 мл, 22 ммоля). Реакційну суміш перемішують при -78 °C впродовж 15 хвил., дають нагрітися до КТ, реакцію зупиняють шляхом додавання 20 % водного розчину NH4Cl та екстрагують за допомогою Et2O (2100 мл). Органічну фазу промивають насиченим розчином NaHCO3 (50 мл), сушать (Na2SO4), фільтрують та концентрують. До залишку, розчиненого у толуолі (100 мл), додають розчин охлоранілу (6 г, 24,2 ммоля, 1,1 екв.) в льодяній AcOH (50 мл). Реакційну суміш перемішують впродовж 14 год. при КТ, охолоджують до 0 °C, підлужують шляхом додавання 10 % водного розчину NaOH та фільтрують через шар целіту. Органічний шар фільтрату промивають за допомогою H2O (20 мл) та екстрагують 10 % водним розчином HCl (325 мл). Об'єднані кислі шари підлужують шляхом додавання 20 % водного розчину NaOH та екстрагують за допомогою ДХМ (325 мл). Органічну фазу промивають за допомогою H 2O (50 мл), сушать (Na2SO4), фільтрують та концентрують. Залишок очищують за допомогою колонкової хроматографії на силікагелі (ДХМ/MeOH, 1:0 → 99:1) та отримують 0,951 г шуканої сполуки у вигляді безбарвного + масла: ІЕР-МС: 154,1 [M+H] ; tR=1,41 хвил. (система 1); ТШХ: Rf=0,85 (ДХМ/MeOH, 9:1). Приклад 3: 2-Амід, 1-({5-[2-(2-фторфеніл)-піридин-4-іл]-4-метилтіазол-2-іл}-амід) (S)піролідин-1,2-дикарбонової кислоти 25 UA 104147 C2 H N N S N O O N 5 NH2 F Шукану сполуку отримують за аналогією з методикою, описаною в прикладі 1, але з використанням 4-хлор-2-(2-фторфеніл)-піридину (стадія 3.1) та перемішування відповідної + суміші впродовж 2 год. при 150 °C на стадії 1.3: ІЕР-МС: 426,1 [M+H] ; tR=2,60 хвил. (система 1); ТШХ: Rf=0,40 (ДХМ/MeOH, 9:1). Стадія 3.1: 4-Хлор-2-(2-фторфеніл)-піридин Cl F N 10 15 Суміш 2-фторфенілборонової кислоти (141 мг, 1 ммоля, 1,2 екв.) з EtOH (1 мл) при 105 °C в атмосфері аргону додають до суміші 4-хлор-2-йодпіридину [Choppin, S.; Gros, P.; Fort, Y., European Journal of Organic Chemistry (2001), (3), 603-606] (200 мг, 0,84 ммоля), PdCl2(dppf) (18 мг, 0,025 ммоля, 0,03 екв.) та Na2CO3 (2 M розчин в H2O, 1,68 мл, 3,36 ммоля, 4 екв.) в толуолі (2 мл). Реакційну суміш перемішують при 105 °C впродовж 1 год., дають охолодитися до КТ, реакцію зупиняють шляхом додавання насиченого розчину NaHCO 3 та екстрагують за допомогою EtOAc. Органічну фазу промивають насиченим розчином NaHCO 3, сушать (Na2SO4), фільтрують та концентрують. Залишок очищують за допомогою колонкової хроматографії на силікагелі (Hex/EtOAc, 1:0 → 97:3) та отримують 127 мг шуканої сполуки у вигляді білої твердої + речовини: ІЕР-МС: 208,1 [M+H] ; tR=4,66 хвил. (система 1); ТШХ: Rf=0,27 (Hex/EtOAc, 9:1). Приклад 4: 2-Амід, 1-{[5-(2-циклобутилпіридин-4-іл)-4-метилтіазол-2-іл]-амід} (S)-піролідин1,2-дикарбонової кислоти H N N S N O O NH2 N 20 25 30 Шукану сполуку отримують за аналогією з методикою, описаною в прикладі 1, але з наступними змінами. В прикладі 1 реакційну суміш перемішують впродовж 4 год. при КТ, розводять за допомогою EtOAc та H2O та екстрагують за допомогою EtOAc. Після сушки та концентрування органічної фази, залишок очищують шляхом розтирання з ДХМ. На стадії 1.3 реакційну суміш перемішують впродовж 2 год. при 120 °C, охолоджують, розводять за допомогою EtOAc та H2O, фільтрують через шар целіту та екстрагують за допомогою EtOAc. Після сушки та концентрування органічної фази залишок очищують шляхом розтирання з Et 2O. На стадії 1.5 реакційну суміш перемішують впродовж 1 год. при 80 °C та розтирання з MeOH не проводять. На стадії 1.7 4-метокси-3-бутен-2-он в ТГФ додають до холодного (-78 °C) розчину LiHMDS в ТГФ. Через 30 хвил. додають циклобутилкарбонілхлорид в ТГФ та реакційній суміші дають нагріватися до КТ впродовж 18 год. + Шукана сполука: ІЕР-МС: 386,1 [M+H] ; ТШХ: Rf=0,11 (ДХМ/MeOH, 95:5). Приклад 5: 2-Амід, 1-({4-метил-5-[2-(1-метилциклопропіл)-піридин-4-іл]-тіазол-2-іл}-амід) (S)піролідин-1,2-дикарбонової кислоти 26 UA 104147 C2 H N N S N O O NH2 N 5 10 Шукану сполуку отримують за аналогією з методикою, описаною в прикладі 1, але з наступними змінами. На стадії 1.1 реакційну суміш перемішують впродовж 14 год. при кип'ятінні із зворотним холодильником. На стадії 1.2 реакційну суміш перемішують впродовж 1 год. при 85 °C. На стадії 1.3 реакційну суміш перемішують впродовж 3 год. при 120 °C. На стадії 1.5 реакційну суміш перемішують впродовж 1 год. при 65-70 °C та розтирання з MeOH не проводять. На стадії 1.7 використовують 1-метил-циклопропанкарбонілхлорид (стадія 5.1). + 1 Шукана сполука: ІЕР-МС: 386,1 [M+H] ; ТШХ: Rf=0,40 (ДХМ/MeOH, 9:1). H ЯМР (400 МГц, ДМСО-d6) (част./млн): 0,71-0,87 (m, 2 H) 1,11-1,26 (m, 2 H) 1,47 (s, 3 H) 1,74-1,96 (m, 3 H) 2,002,15 (m, 1 H) 2,39 (s, 3 H) 3,35-3,52 (m, 1 H) 3,52-3,73 (m, 1 H) 4,10-4,40 (m, 1 H) 6,93 (br. s., 1 H) 7,15 (dd, 1 H) 7,27 (s, 1 H) 7,35 (s, 1 H) 8,40 (d, 1 H) 10,99 (br. s., 1 H). Стадія 5.1: 1-Метилциклопропанкарбонілхлорид COCl 15 Суміш 1-метилциклопропанкарбонової кислоти (10 г, 100 ммоля) та оксалілхлориду (10,49 мл, 120 ммоля, 1,2 екв.) в CHCl3 (80 мл) перемішують впродовж 4 год. при 70 °C. Реакційну суміш концентрують та отримують 11,8 г шуканої сполуки у вигляді жовтого масла, яке використовують без додаткового очищення. Приклад 6: 2-Амід, 1-({4-метил-5-[2-(1-метилциклобутил)-піридин-4-іл]-тіазол-2-іл}-амід) (S)піролідин-1,2-дикарбонової кислоти H N N S N O O NH2 N 20 25 30 Шукану сполуку отримують за аналогією з методикою, описаною в прикладі 1, але з наступними змінами. В прикладі 1, реакцію зупиняють шляхом розведення сумішшю EtOAc та H2O та екстрагують за допомогою EtOAc. На стадії 1.2 реакційну суміш перемішують впродовж 2 год. при 100 °C. На стадії 1.3 реакційну суміш перемішують впродовж 3 год. при 100 °C, розводять сумішшю EtOAc/H2O та екстрагують за допомогою EtOAc. Після сушки та концентрування органічної фази залишок очищують за допомогою колонкової хроматографії на силікагелі (Hex/EtOAc, 1:4). На стадії 1.5 реакційну суміш перемішують впродовж 2 год. при 80 °C та розтирання з MeOH не проводять. На стадії 1.7 4-метокси-3-бутен-2-он (50 ммоля) в ТГФ (100 мл) додають до холодного (-78 °C) розчину LiHMDS (1M в ТГФ, 100 мл) в ТГФ (200 мл). Через 30 хвил. додають 1-метилциклобутанхлорид (стадія 6.1) та реакційній суміші дають нагріватися до КТ впродовж 18 год. + водн. Шукана сполука: ІЕР-МС: 400,1 [M+H] ; ТШХ: Rf=0,06 (ДХМ/MeOH/NH3 , 94:5:1). Стадія 6.1: 1-Метилциклобутанкарбонілхлорид COCl 35 Шукану сполуку отримують за аналогією з методикою, описаною на стадії 5.1, але з використанням 1-метилциклобутанкарбонової кислоти [Cowling, S. J.; Goodby, J. W., Chemical Communications, (2006), (39), 4107-4109]. Приклад 7: 2-Амід, 1-{[5-(2-трет-бутилпіридин-4-іл)-тіазол-2-іл]-амід} (S)-піролідин-1,2дикарбонової кислоти 27 UA 104147 C2 H N N S N O O NH2 N 5 10 Шукану сполуку отримують за аналогією з методикою, описаною в прикладі 1, з наступними змінами. В прикладі 1 реакційну суміш перемішують впродовж 16 год. при КТ, реакцію зупиняють шляхом розведення сумішшю EtOAc/H2O та екстрагують за допомогою EtOAc. На стадії 1.1 реакційну суміш перемішують впродовж 2 год. при кип'ятінні із зворотним холодильником. На стадії 1.2 реакційну суміш перемішують впродовж 1 год. при 100 °C. На стадії 1.3 використовують N-тіазол-2-ілацетамід. Реакційну суміш перемішують впродовж 2 год. при 120 °C, розводять сумішшю EtOAc/H2O та екстрагують за допомогою EtOAc. Після сушки та концентрування органічної фази залишок очищують за допомогою колонкової хроматографії на силікагелі (Hex/EtOAc, 1:1), потім розтирають з Et2O. + Шукана сполука: ІЕР-МС: 374,1 [M+H] ; tR=2,16 хвил. (система 1); ТШХ: Rf=0,10 водн. (ДХМ/MeOH/NH3 , 94:5:1). Приклад 8: 2-Амід, 1-{[5-(2-ізопропілпіридин-4-іл)-4-метилтіазол-2-іл]-амід} (S)-піролідин-1,2дикарбонової кислоти H N N S N O O NH2 N 15 20 25 Шукану сполуку отримують за аналогією з методикою, описаною в прикладі 1, але з наступними змінами. В прикладі 1 реакційну суміш перемішують впродовж 16 год. при КТ, реакцію зупиняють шляхом розведення сумішшю EtOAc/H2O та екстрагують за допомогою EtOAc. На стадії 1.2 реакційну суміш перемішують впродовж 2 год. при 100 °C. На стадії 1.3 використовують 4-хлор-2-ізопропілпіридин (стадія 8.1). Реакційну суміш перемішують впродовж 3 год. при 150 °C, розводять сумішшю EtOAc/H2O та екстрагують за допомогою EtOAc. Після сушки та концентрування органічної фази залишок очищують за допомогою колонкової хроматографії на силікагелі (Hex/EtOAc, 25:75). + Шукана сполука: ІЕР-МС: 374,1 [M+H] ; tR=1,99 хвил. (система 1); ТШХ: Rf=0,10 водн. (ДХМ/MeOH/NH3 , 94:5:1). Стадія 8.1: 4-Хлор-2-ізопропілпіридин Cl N 30 Шукану сполуку отримують за аналогією з методикою, описаною на стадії 2.1, але з + використанням ізопропілмагнійхлориду (2M в ТГФ): ІЕР-МС: 156,0 [M+H] ; ТШХ: Rf=0,32 (ДХМ). Приклад 9: 2-Амід, 1-{[5-(2-циклобутилпіридин-4-іл)-тіазол-2-іл]-амід} (S)-піролідин-1,2дикарбонової кислоти H N N S N O O N 28 NH2
ДивитисяДодаткова інформація
Назва патенту англійськоюOrganic compounds
Автори англійськоюCaravatti, Giorgio, Fairhurst, Robin Alec, Furet, Pascal, Guagnano, Vito, Imbach, Patricia
Автори російськоюФуре Паскаль
МПК / Мітки
МПК: C07D 417/14, A61K 31/4439, A61P 35/00
Мітки: проліферативних, кислоти, застосування, похідна, лікуванні, піролідиндикарбонової, захворювань
Код посилання
<a href="https://ua.patents.su/119-104147-pokhidna-pirolidindikarbonovo-kisloti-ta-zastosuvannya-u-likuvanni-proliferativnikh-zakhvoryuvan.html" target="_blank" rel="follow" title="База патентів України">Похідна піролідиндикарбонової кислоти та її застосування у лікуванні проліферативних захворювань</a>












