Олігонуклеотидний праймер, призначений для ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини типу 1 (віл-1) (варіанти), пара олігонуклеотидних праймерів (варіанти), набір олігонуклеотидних праймерів
Номер патенту: 47432
Опубліковано: 15.07.2002
Автори: ЛУ Ші-Да Ю, КВОК Шірлі Ї, Крістоферсон Сінді Доун
Формула / Реферат
1. Олігонуклеотидний праймер, призначений для ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини типу 1 (ВІЛ-1), де вказаний олігонуклеотидний праймер SKCC1 включає нуклеотидну послідовність
2. Олігонуклеотидний праймер, призначений для ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, де вказаний олігонуклеотидний праймер SKCC3 включає нуклеотидну послідовність
3. Пара олігонуклеотидних праймерів, що складається з праймеру SK145 з нуклеотидною послідовністю
та праймеру SKCC1 з нуклеотидною послідовністю
4. Набір олігонуклеотидних праймерів, що складається з пари олігонуклеотидних праймерів за п. 3 та праймеру SK145M2 з нуклеотидною послідовністю
.
5. Пара олігонуклеотидних праймерів, що складається з праймеру SK145 з нуклеотидною послідовністю
та праймеру SKCC3 з нуклеотидною послідовністю
6. Набір олігонуклеотидних праймерів, що складається з пари олігонуклеотидних праймерів за п. 5 та праймеру SK145M2 з нуклеотидною послідовністю
7. Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає олігонуклеотидний праймер за п. 1.
8. Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає олігонуклеотидний праймер за п. 2.
9. Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає пару олігонуклеотидних праймерів за п. 3.
10. Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає набір олігонуклеотидних праймерів за п. 4.
11. Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає пару олігонуклеотидних праймерів за п. 5.
12. Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає набір олігонуклеотидних праймерів за п. 6.
13. Спосіб ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає здійснення полімеразної ланцюгової реакції з використанням праймера SKCC1 з нуклеотидною послідовністю
або праймера SKCC3 з нуклеотидною послідовністю
14. Спосіб за п. 13, який відрізняється тим, що при полімеразній ланцюговій реакції додатково використовують праймер SK145 з нуклеотидною послідовністю
.
15. Спосіб за п. 14, який відрізняється тим, що при полімеразній ланцюговій реакції додатково використовують праймер SK145M2 з нуклеотидною послідовністю
16. Спосіб за п. 13, який відрізняється тим, що при полімеразній ланцюговій реакції додатково використовують праймер SK145M2 з нуклеотидною послідовністю
Текст
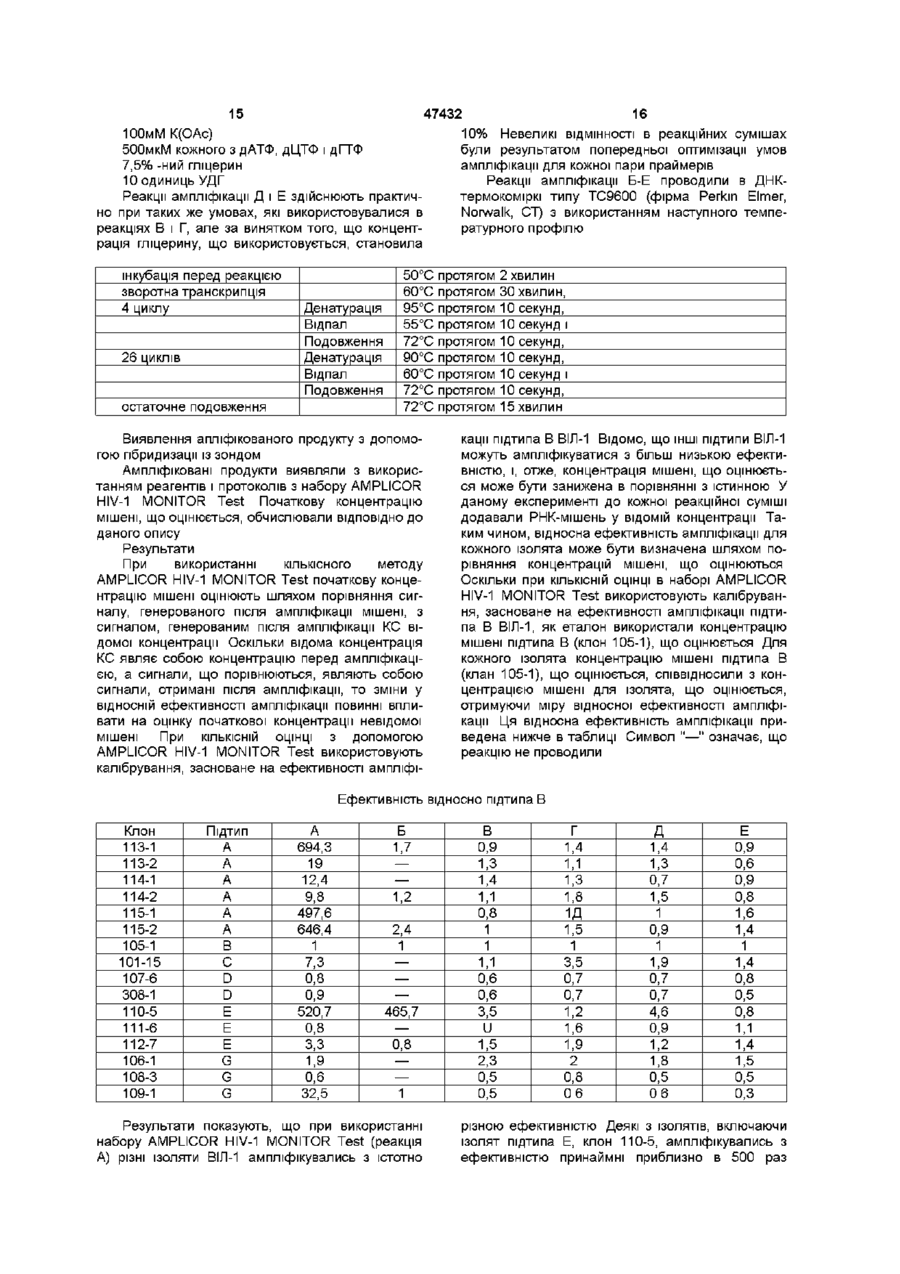
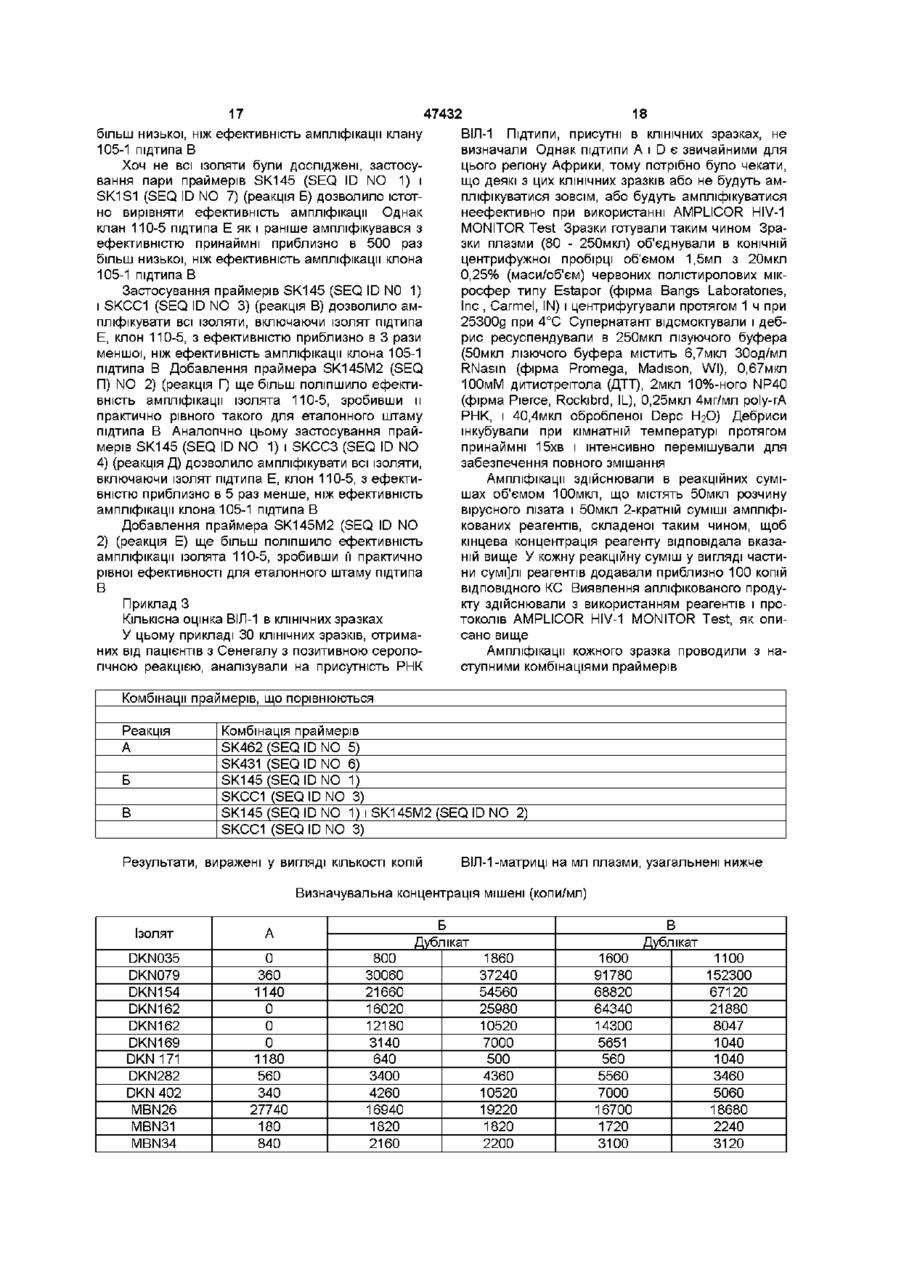
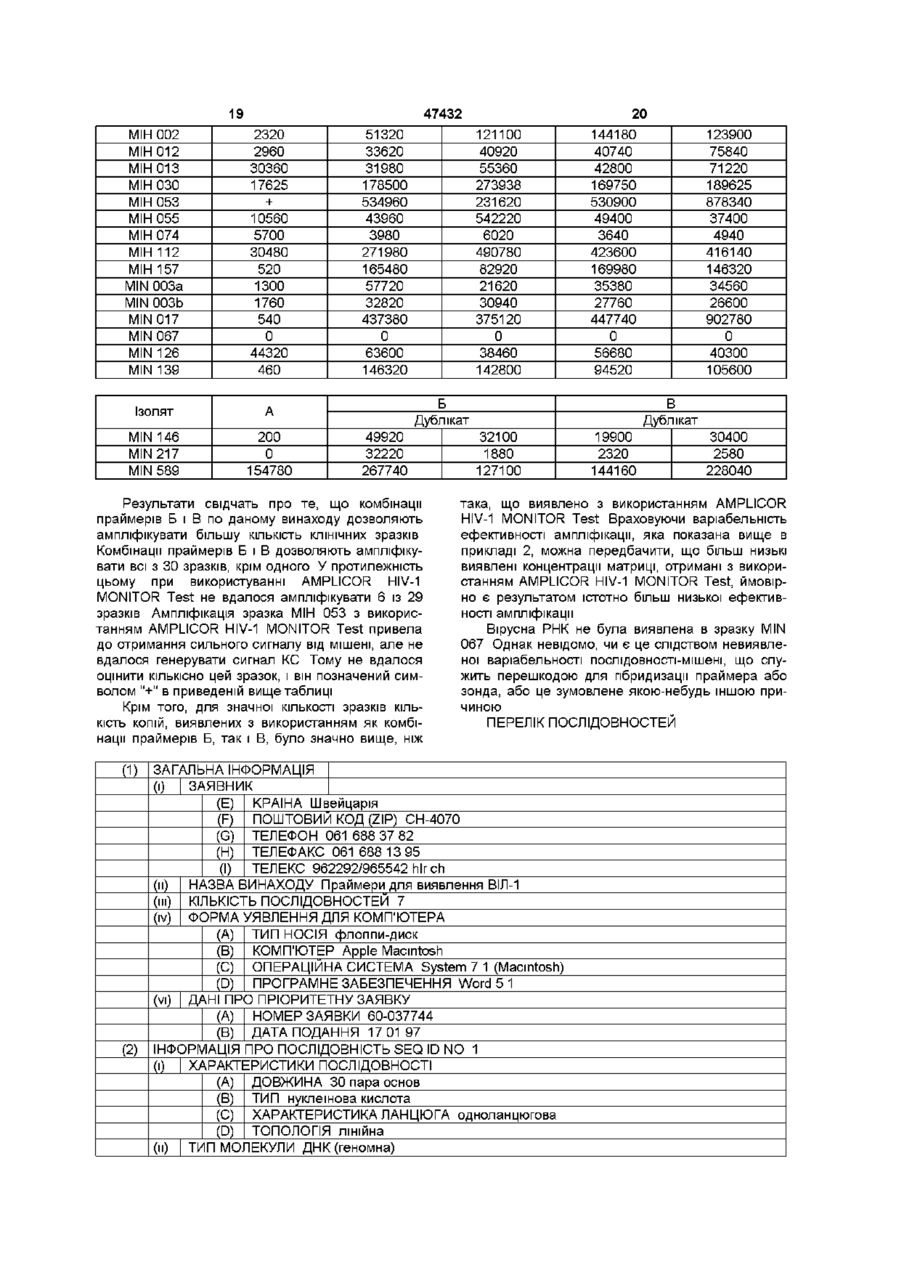
1 Олігонуклеотидний праймер, призначений для ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини типу 1 (ВІЛ-1), де вказаний олігонуклеотидний праймер SKCC1 включає нуклеотидну ПОСЛІДОВНІСТЬ TACTAGTAGTTCCTGCTATGTCACTTCG, 2 Олігонуклеотидний праймер, призначений для ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, де вказаний олігонуклеотидний праймер SKCC3 включає нуклеотидну ПОСЛІДОВНІСТЬ О TGAAGGGTACTAGTAGTTCCTGCTAT. 3 Пара олігонуклеотидних праймерів, що складається з праймеру SK145 з нуклеотидною ПОСЛІДОВНІСТЮ AGTGGGGGGACATCAAGCAGCCATGCAAAT та праймеру SKCC1 з нуклеотидною ПОСЛІДОВНІСТЮ TACTAGTAGTTCCTGCTATGTCACTTCC. 4 Набір олігонуклеотидних праймерів, що складається з пари олігонуклеотидних праймерів за п З та праймеру SK145M2 з нуклеотидною ПОСЛІДОВНІСТЮ AGTGGGGGGACACCAGGGAGCAATGCAAAT 5 Пара олігонуклеотидних праймерів, що складається з праймеру SK145 з нуклеотидною ПОСЛІДОВНІСТЮ AGTGGGGGGACATCAAGCAGCCATGCAAAT та праймеру SKCC3 з нуклеотидною ПОСЛІДОВНІСТЮ TGAAGGGTACTAGTAGTTCCTGCTAT. 6 Набір олігонуклеотидних праймерів, що складається з пари олігонуклеотидних праймерів за п 5 та праймеру SK145M2 з нуклеотидною ПОСЛІДОВНІСТЮ со 47432 AGTGGGGGGACACCAGGCAGCAATGCAAAT. 7 Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає олігонуклеотидний праймер за п 1 8 Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає олігонуклеотидний праймер за п 2 9 Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає пару олігонуклеотидних праймерів за п З 10 Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає набір олігонуклеотидних праймерів за п 4 11 Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає пару олігонуклеотидних праймерів за п 5 12 Набір для виявлення нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає набір олігонуклеотидних праймерів за п 6 13 Спосіб ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини ВІЛ-1, який включає здійснення полімеразної ланцюгової реакції з використанням праймера SKCC1 з нуклеотидною послідо Даний винахід відноситься до молекулярної біологи і хімії нуклеїнових кислот Зокрема воно відноситься до способів і реагентів, призначених для виявлення вірусу імунодефіциту людини типу 1 (ВІЛ-1) Отже, областю застосування винаходу є медицина загалом, і більш конкретно медична діагностика і молекулярна біологія Створення способів ампліфікації певних послідовностей нуклеїнових кислот, зокрема полімеразної ланцюгової реакції (ПЛР), робить можливим швидке виявлення нуклеїнових кислот, присутніх в зразку в таких малих кількостях, що їх раніше було неможливо виявити (див патенти США 4683195, 4683202 і 4965188) У літературі є численні дані про вдосконалення і застосування ПЛР Наприклад, широкий спектр пов'язаних з бензоксазиндиона проблем представлений в таких виданнях, як PCR Technology principles and applications for DNA amplmcation, 1989 (ред НА Erhch), Stockton Press, New York, NY, PCR Protocols A guide to methods and applications, 1990 (ред М A Innis і інш ,), Academic Press, San Diego, CA, і в PCR Strategies, 1995 (ред М A Innis і інш ,), Academic Press, San Diego, CA Комерційні постачальники, такі, як фірма Perkm Ebner (Norwalk, CT), постачають на ринок реагенти для ПЛР і публікують ПЛР-протоколи Огляд даних по застосуванню ПЛР і гібридизації з використанням зондів для ампліфікації і виявлення нуклеїнової кислоти ВІЛ-1 представлений у Kwok, 1992, Ann Med 24 211-214, і у Coutlee і інш, 1991, Мої Ceu Probes 5 241-259 Засновані на використанні ПЛР методи виявлення ВІЛ-1 описані, наприклад, в патентах США 5008182 і 5176775, у Kellogg і Kwok, 1990, в PCR Protocols A Guide to Methods and Applications, (ред Innis і інш ,), Academic Press, San Diego, CA, 337-347, у Holodmy і інш , 1991, J Inf Dis 163 802 4 ВНІСТЮ TACTAGTAGTTCCTGCTATGTCACTTCC або праймера SKCC3 з нуклеотидною ПОСЛІДОВНІСТЮ TGAAGGGTACTAGTAGTTCCTGCTAT. 14 Спосіб за п 13, який відрізняється тим, що при полімеразній ланцюговій реакції додатково використовують праймер SK145 з нуклеотидною ПОСЛІДОВНІСТЮ AGTGGGGGGACATCAAGCAGCCATGCAAAT 15 Спосіб за п 14, який відрізняється тим, що при полімеразній ланцюговій реакції додатково використовують праймер SK145М2 з нуклеотидною ПОСЛІДОВНІСТЮ AGTGGGGGGACACCAGGCAGCAATGCAAAT. 16 Спосіб за п 13, який відрізняється тим, що при полімеразній ланцюговій реакції додатково використовують праймер SK145М2 з нуклеотидною ПОСЛІДОВНІСТЮ AGTGGGGGGACACCAGGCAGCAATGCAAAT. 865, Jackson і інш, 1991, AIDS 5 1463-1467, і у Mulder і інш , 1994, У Chn Microbiol 32(2) 292-300 Комерційні набори для ампліфікації і виявлення ВІЛ-1 постачаються фірмою Hoffmann-La Roche (Nutley, NY) Набір Amphcor™ HIV-1 Test призначений для виявлення in vitro провирусної ДНК ВІЛ1 набір AMPLICOR HIV-1 MONITOR™ Test призначений для кількісної оцінки in vitro РНК ВІЛ-1 У обох тест-наборах Amphcor для ампліфікації нуклеїнових кислот ВІЛ-1 використовується пара праймерів SK462 (SEQ ID NO 5) і SK431 (SEQ ID NO 6), описаних у Mulder і інш, 1994, J Chn Microbiol 32(2) 292-300, званих в даному описі Amplicor-праймерами для ВІЛ-1 ВІЛ-1 володіє значною варіабельнцістю геномної ПОСЛІДОВНОСТІ Філогенетичний аналіз послідовностей нуклеїнових кислот генів gag і env ВІЛ-1 описаний в роботі Myers і інш , 1993, Human Retrovirus and AIDS, 1993, Los Alamos National Laboratory, Los Alamos, NM, включеній в даний опис і якості посилання Всередині групи М були виявлені підтипи A-J У літературі описані загальноприйняті методи молекулярної біологи і хімії нуклеїнових кислот, що відносяться до області даного винаходу (див , наприклад, Sambrook і інш , 1989, Molecular Cloning A Laboratory Manual, Cold Spi-mg Harbor Laboratory, Cold Spring Harbor, New York, Ohgonucleotide Synthesis (ред M J Gait, 1984), Nucleic Acid Hybridization (ред В D Hamnes і S J Higgms, 1984), і серп Methods in Enzymology (Academic Press, Inc)) Були виявлені численні ізоляти групи М вірусу імунодефіциту людини типу 1 (ВІЛ-1), які або не ампліфікуються, або недостатньо ефективно ампліфікуються з раніше описаними праймерами для гена gag, зокрема з використанням Amphcor 47432 праймерів для ВІЛ-1 SK462 (SEQ ID NO 5) і SK431 (SEQ ID NO 6) Ці ІЗОЛЯТИ ВИЯВЛЯЮТЬ не описану раніше варіабельність послідовностей в області, що включає сайти скріплення праймерів Amphcorпраймерів для ВІЛ-1 Даний винахід відноситься до поліпшених праймерів, які здатні ефективно ампліфікувати ці недавно виявлені ізоляти, в доповнення до всіх ізолятам, які здатні ампліфікуватися з використанням Amphcor-праймерів для ВІЛ-1 Крім того, праймери по винаходу здатні ампліфікувати всі ВІДОМІ ізоляти групи М ВІЛ-1 з приблизно однаковою ефективністю Даний винахід відноситься далі до поліпшених олігонуклеотидних праймерів, які здатні здійснювати ампліфікацію з використанням полімеразної ланцюгової реакції (ПЛР) області гена gag ІЗОЛЯТІВ ПІДТИПІВ А групи М ВІЛ-1 з приблизно однаковою ефективністю і без одночасної ампліфікації послідовностей, що не є мішенями Зокрема, даний винахід відноситься до олігонуклеотидних праймерів, призначених для ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини типу 1 (ВІЛ-1), причому вказаний олігонуклеотидний праймер вибирають з групи, що складається з SKCC1 (SEQ ID NO 3) і SKCC3 (SEQ ID N0 4) Переважно кожний з цих праймерів об'єднаний в пару олігонуклеотидних праймерів, що складається з SK145 (SEQ ID NO 1) і SKCC1 (SEQ ID NO 3), або в пару олігонуклеотидних праймерів, що складається з SK145 (SEQ ID NO 1) і SKCC3 (SEQ ID NO 4) У іншому варіанті ці пари праймерів можуть бути об'єднані з праймером SK145M2 (SEQ ID NO 2) в набір олігонуклеотидних праймерів, які складаються з олігонуклеотидних праймерів SK145 (SEQ ID NO 1), SKCC1 (SEQ ID NO 3) і SK145M2 (SEQ ID NO 2), або в набір олігонуклеотидних праймерів, що складається з олігонуклеотидних праймерів SK145 (SEQ ID NO 1), SKCC3 (SEQ ID N0 4) і SK145M2 (SEQ ID NO 2) Винахід відноситься також до поліпшених способів ампліфікації області гена gag з ПІДТИПІВ групи М ВІЛ-1, що включають здійснення ПЛР з використанням праймерів по винаходу Даний винахід далі відноситься до наборів, що містять ампліфіцируючий праймер по даному винаходу Ці набори можуть включати додаткові реагенти, такі, як зонди для виявлення або один або декілька реагентів для ампліфікації, наприклад, полімеразу, буфери і нуклеозидтрифосфати Для кращого розуміння винаходу нижче визначені деякі поняття "Нуклеїнова кислота" і "олігонуклеотид" відносяться до полідезоксирибонуклеотидам (утримуючим 2-дезокси-О-рибозу), до полірибонуклеотидам (утримуючим D-рибозу) і до будь-якого іншого типу полінуклеотида, що являє собою М-ГЛІКОЗІД пуринової або пиримидинової основи або модифіковану пуринову або пиримидинову основу Поняття "нуклеїнова кислота" і "олігонуклеотид" не мають на увазі ВІДМІННОСТІ В ДОВЖИНІ ланцюга і можуть використовуватися взаємозамінне Ці поняття відносяться тільки до первинної структури молекули Таким чином, ці поняття включають двох- і одно ланцюгову ДНК, а також двох- і однолінцюгову РНК Олігонуклеотиди можуть бути отримані будьяким придатним для цієї мети способом, включаючи, наприклад, тонування і рестрикцію ВІДПОВІДНИХ послідовностей і прямий ХІМІЧНИЙ синтез за допомогою такого методу, як фосфотриефірний метод, описаний у Narang і інш , 1979, Meth Enzymol 68 90-99, фосфодіефирний метод, описаний у Brown і інш , 1979, Meth Enzymol 68 109151, діетилфосфорамідитний метод, описаний у Beaucage і інш, 1981, Tetrahedron Lett 22 18591862, і метод з використанням твердої підкладки, описаний в патенті США 4458066 Огляд методів синтезу представлений у Goodchild, 1990, Bioconjugate Chemistry, 1(3) 165-187 Поняття "гібридизація" відноситься до утворення дуплексної структури двома одноланцюговими нуклеїновими кислотами внаслідок комплементарного спаровування основ Гібридизація може відбуватися між повністю комплементарними ланцюжками нуклеїнової кислоти або між "практично комплементарними" ланцюжками нуклеїнової кислоти, які містять мінорні області помилкового спаровування Умови, при яких можуть пбридуватися тільки повністю комплементарні ланцюжки нуклеїнової кислоти, називаються "суворими умовами гібридизації" або "умовами гібридизації, специфічними для ПОСЛІДОВНОСТІ" Стабільні дуплекси практично комплементарних послідовностей можуть бути отримані при менш суворих умовах гібридизації, міра допустимих помилкових спарувань може контролюватися за допомогою ВІДПОВІДНОГО регулювання умов гібридизації Фахівці в області технології нуклеїнових кислот можуть визначити стабільність дуплекса емпіричного шляхом, враховуючи різні параметри, в тому числі, наприклад, довжину і концентрацію пар основ олігонуклеотидів, іонну силу і частоту помилкових спарувань основ, використовуючи для цієї мети відомий в даній області техніки посібник (див , наприклад, Sambrook і інш , 1989, Molecular Cloning A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, і Wetmur, 1991, Critical Reviews in Biochem and Мої Biol , 26(3/4) 227-259) Поняття "праймер" відноситься до природного або синтетичного олігонуклеотиду, здатному діяти як точка ініціація синтезу ДНК в умовах, при яких індукується синтез продукту подовження праймера, комплементарного ланцюга нуклеїнової кислоти, тобто в присутності чотирьох різних нуклеозидтрифосфатів і агента, що забезпечує полімеризацію (тобто ДНК-полімерази або зворотної транскриптази) у відповідному буфері і при ВІДПОВІДНІЙ температурі Праймер переважно являє собою одноланцюговий олігодезоксирибонуклеотид Відповідна довжина праймера залежить від цілей застосування праймера, але звичайно складає від 15 до 35 нуклеотидів Короткі молекули праймера звичайно вимагають більш низьких температур для формування досить стабільних гібридних комплексів з матрицею Не потрібно, щоб праймер відображав точну ПОСЛІДОВНІСТЬ нуклеїнової кислоти-матриці, але він повинен бути в достатній мірі комплементарним, щоб пбридизува 47432 тися з матрицею Праймери можуть включати додаткові структури, які дозволяють виявляти або іммобілізувати праймер, але не змінюють основну властивість праймера, а саме, здатність діяти як точка ініціації синтезу ДНК Наприклад, праймери можуть містити додаткову нуклеотидну ПОСЛІДОВНІСТЬ на 5'-КІНЦІ, якій не гібридизується з нуклеїновою кислотою-мішенню, але яка сприяє клонуванню ампліфікованого продукту Область праймера, комплементарна матриці в достатній для гібридизації міри, в контексті даного опису означається як "область гібридизації" У контексті даного опису поняття "праймер, що ІНІЦІЮЄ синтез проти ходу транскрипції" відноситься до праймеру, продукт подовження якого являє собою субпослідовність кодуючого ланцюжка "Праймер, що ІНІЦІЮЄ синтез по ходу транскрипції", відноситься до праймера, продукт подовження якого являє собою субпослідовність, комплементарну некодуючого ланцюжку Поняття "послідовність-мішень", "областьмішень" і "нуклеїнова кислота-мішень" відносяться до області нуклеїнової кислоти, що підлягає амлификацм, виявленню або іншому аналізу У контексті даного опису праймер є "специфічним" для ПОСЛІДОВНОСТІ-МІШЄНІ, ЯКЩО КІЛЬКІСТЬ ПОМИЛКОВИХ спарувань, що утворюються між праймером і послідовністю-мішенню, менше, чим КІЛЬКІСТЬ помилкових спарувань, що утворюються між праймером і послідовностями, що не є мішенями, які можуть бути присутними в зразку Можуть бути вибрані такі умови гібридизації, при яких стабільні дуплекси формуються тільки в тоді, коли КІЛЬКІСТЬ присутніх помилкових спарувань не більше КІЛЬКОСТІ помилкових спарувань, що утворюються між праймером і послідовністю-мішенню При таких умовах праймер, специфічний для мішені, може утворювати стабільний дуплекс тільки з послідовністю-мішенню Таким чином, застосування праймерів, специфічних для мішені, в умовах ампліфікації відповідної суворості дозволяє здійснювати специфічну ампліфікацію тих послідовностей, які мають сайти скріплення, що є мішенями для праймера Аналогічно цьому застосування зондів, специфічних для мішені, в умовах гібридизації відповідної суворості дає можливість виявляти конкретну послідовність-мішень Поняття "суміш для реакції ампліфікації" відноситься до розчину, який містить реагенти, необхідні для здійснення реакції ампліфікації, і який звичайно містить праймери, термостабільну ДНКполімеразу, дНТФ і катион двовалентного металу у відповідному буфері Реакційна суміш називається повної, якщо вона містить всі реагенти, необхідні для здійснення реакції, і називається неповної, якщо вона містить неповний набір необхідних реагентів Для фахівця в даній області техніки очевидно, що для зручності, збереження стабільності при зберіганні або ж для можливості регулювати концентрації компонентів в залежності від призначення, компоненти реакції звичайно зберігають у вигляді окремих розчинів, кожний з яких містить неповний набір всіх компонентів, а самі компоненти реакції об'єднують до реакції для створення повної реакційної суміші Крім того, для фахівця в даній області техніки очевидно, що для 8 продажу компоненти реакції упаковують по окремості і що придатні комерційні набори можуть містити будь-який неповний набір компонентів реакції, включаючого праймери поданому винаходу Праймери для ампліфікації ВІЛ-1 Праймери по даному винаходу володіють здатністю ампліфікувати нуклеїнову кислоту ПІДТИПІВ групи М ВІЛ-1 Праймери є істотно поліпшеними в порівнянні з раніше описаними праймерами в тому відношенні, що вони володіють здатністю ампліфікувати практично з однаковою ефективністю нуклеїнову кислоту з області гена gag всіх ІЗОЛЯТІВ ПІДТИПІВ A-G, що належать групі М, включаючи недавно відкриті ізоляти Нуклеотидні ПОСЛІДОВНОСТІ праймерів приведені нижче в орієнтації зліва направо 5'^3' Праймери, що ІНІЦІЮЮТЬ синтез проти ходу транскрипції SK145 (SEQ ID NO 1) AGTGGGGGGACATCAAGCAGCCATGCAAAT SK145M2 (SEQ ID NO 2) AGTGGGGGGACACCAGGCAGCAATGCAAAT Праймери, що ІНІЦІЮЮТЬ синтез по ходу транскрипції SKCC1 (SEQ ID NO 3) TACTAGTAGTTCCTGCTATGTCACTTCC SKCC3 (SEQ ID NO 4) TGAAGGGTACTAGTAGTTCCTGCTAT Праймери по даному винаходу, що ІНІЦІЮЮТЬ синтез по ходу транскрипції, можуть застосовуватися з будь-яким приведеним в даному описі праймером, що ІНІЦІЮЄ синтез проти ходу транскрипції Праймери по даному винаходу, що ІНІЦІЮЮТЬ синтез по ходу транскрипції, переважно застосовують з тим праймером SK145 (SEQ ID NO 1), який ІНІЦІЮЄ синтез проти ходу транскрипції, необов'язково в поєднанні з праймером SK145M2 (SEQ ID NO 2), що ІНІЦІЮЄ синтез проти ходу транскрипції ІНІЦІЮЮЧИЙ синтез проти ходу транскрипції праймер SK145 (SEQ ID NO 1), описаний у Kellogg і Kwok, 1990, в PCR Protocols A Guide to Methods and Applications, (ред Innis і інш ,), Academic Press, San Diego, CA 337-347 Другий ІНІЦІЮЮЧИЙ синтез проти ходу транскрипції праймер SK145M2 (SEQ ID NO 2) гібридизується з такою ж областю, що і SK145 (SEQ ID NO 1), але він створений для більш точного спаровування з нуклеотидною ПОСЛІДОВНІСТЮ певних ІЗОЛЯТІВ підтипа А і Е ВІЛ-1 Як зазначено нижче в прикладах, застосування що обох праймерів, що ІНІЦІЮЮТЬ синтез проти ходу транскрипції, може сприяти вирівнюванню ефективності ампліфікації певних ПІДТИПІВ Ампліфікація Ампліфікації здійснюють в умовах, які дозволяють ампліфікувати всі підтипи групи М ВІЛ-1, але які володіють достатньою суворістю для того, щоб уникнути ампліфікації послідовностей, що не є мішенями Переважні умови реакції ампліфікації описані в прикладах у Mulder і інш , 1994, J СІїп Microbiol 32(2) 292-300, і в інструкції, включеній в тест-набір AMPLICOR HIV-1 MONITOR Test Точні умови не мають вирішального значення при практичному здійсненні винаходу Оптимізація умов ампліфікації може бути проведена звичайним способом, засновуючись вказівками, які представлені 47432 в даному описі Праймери і способи, які пропонуються, можуть застосовуватися для виявлення або провірусній ДНК ВІЛ-1, або РНК ВІЛ-1 Ампліфікація РНК з використанням полімеразної ланцюгової реакції із зворотною транскриптазою (ЗТ-ПЛР) добре відома в даній області техніки і описана в патентах США 5322770 і 5310652, у Myers і Gehand, 1991, Biochemistry, 30(31) 7661-7666, і у Young і інш , 1993, J Clin Microbiol , 31 (4) 882-886 Ампліфікація РНК ВІЛ-1 з використанням ЗТ-ПЛР описана у Mulder і інш , 1994, J Clin Microbiol 32(2) 292-300 і у Holodmy і інш , 1991, J Inf Dis 163_802-865 Методи підготовки зразка, придатні для ампліфікації ДНК і РНК ВІЛ-1, описані в літературі Вибір конкретного методу не має істотного значення при практичному здійсненні даного винаходу Фахівець в даній області техніки може вибрати і оптимізувати придатні методи отримання зразка, засновуючись на даних, представлених в описі винахода Переважні методи підготовки зразка, що застосовуються для виявлення провірусної ДНК ВІЛ-1, описані у Casareale і інш, 1992, PCR Methods and Applications, 2 149-153, і у Butcher і Spadoro, 1992, Clin Immunol Newsletter, 12 73-76 Переважний набір для підготовки зразка для виявлення провірусної ДНК ВІЛ-1 є на ринку у вигляді частини набору Amphcor HIV-1 Test Переважні методи підготовки зразка, що застосовуються для виявлення РНК ВІЛ-1 в плазмі, описані у Mulder і інш, 1994, J Clin Microbiol 32(2) 292-300 Переважний набір для підготовки зразка для виявлення і/або кількісної оцінки РНК ВІЛ-1 є на ринку у вигляді частини набору AMPLICOR HIV-1 MONITOR Test Аналіз апліфікованого продукту Праймери для ампліфікації і способи по даному винаходу придатні для будь-якого застосування, заснованого на використанні ампліфікованої нуклеїнової кислоти Наприклад, клонування і/або секвенування послідовностей ВІЛ-1 полегшується при використанні праймерів по даному винаходу Методи виявлення нуклеїнових кислот, ампліфікованих з допомогою ПЦР, добре ВІДОМІ В даній області техніки Метод, який застосовується для аналізу ампліфікованої нуклеїнової кислоти, не має істотного значення при практичному здійсненні винаходу, і тому може використовуватися будьякий придатний метод Переважно використовують ампліфікацію РНК ВІЛ-1, як описано в прикладах, що стосуються кількісної оцінки вмісту вірусу Приклади способів виявлення ампліфікованої нуклеїнової кислоти включають аналіз продукту ампліфікації з допомогою гель-електрофореза і виявлення з допомогою гібридизації з комплементарними олігонуклеотидними зондами Придатні методи аналізу для дослідження гібридизації мішень-зонд добре ВІДОМІ в даній області техніки і включають такі методи, як дот-блотинг і зворотний дот-блотинг При використанні методу дот-блотинга ампліфіковану ДНК- мішень іммобілізуються на твердій підкладці, такій, як найлонова мембрана Комплекс мембрана-мішень шкубують з міченим зондом при ВІДПОВІДНИХ умовах гібридизації, непбридизований зонд видаляють шляхом промивки в умовах ВІДПО 10 ВІДНІЙ суворості і мембрану досліджують на присутність св'язаного зонда Виявлення за допомогою дот-блотинга продуктів ПЛР-ампліфікацм описане, наприклад, у Saiki і інш, 1986, Nature, 324 163166, і в патенті США 5468613 При використанні методу зворотного дотблотинга зонди іммобілізуються на твердій підкладці, такій, як найлонова мембрана, і мітять ампліфікуєму ДНК-мішень ДНК-мішень звичайно мітять в процесі ампліфікації включенням мічених праймерів Один або обидва праймера можуть бути міченими Комплекс мембрана-зонд шкубують з міченою ампліфікованою ДНК-мішенню при ВІДПОВІДНИХ умовах гібридизації, непбридизовану ДНКмішень видаляють шляхом промивки в умовах ВІДПОВІДНІЙ суворості і потім фільтр досліджують на присутність пов'язаної ДНК-мішені Виявлення за допомогою методів зворотного дот-блотинга описане, наприклад, у Saiki і інш , 1989, Proc Natl Acad Sei USA, 86 6230, і в патенті США 5468613 У альтернативному варіанті аналіз на основі зворотного дот-блотинга може бути проведений з використанням твердої підкладки, що має множину сайтів для відпалу зонда або лунок Наприклад, мікролунковий планшет найбільш придатний для крупномасштабних КЛІНІЧНИХ застосувань методів по даному винаходу Зонди можуть бути іммобілізовані на мікролунковому планшеті або шляхом пасивного скріплення, або за допомогою проміжного протеїну, такого, як бичачий сироватковий альбумін (БСА), який прилипає до мікролункових планшетів (див Tung і інш , 1991, Bioconjugate Chem , 2 464-465) Методи на основі зворотного дот-блотинга, в яких використовується мікролунковий планшет, описані в патенті США 5232829, у Loeffelholz і інш, 1992, J Clin Microbiol, 30(11) 2847-2851, у Jackson і інш, 1991, AIDS, 5 14631467, у Mulder і інш , 1994, J Clin Microbiol 32(2) 292-300, в інструкції, включеній в комерційний набір Amphcor HIV- 1 Test, і в інструкції, включеній в комерційний набір AMPLICOR HIV-1 MONITOR Test Переважно виявлення і/або кількісну оцінку апліфікованого продукту здійснюють з допомогою гібридизації з олігонуклеотидним зондом, іммобілізованим на мікролунковому планшеті, з використанням реагентів і протоколів Amphcor HIV-1 Test або AMPLICOR HIV-1 MONITOR Test Застосування методів по даному винаходу для кількісної оцінки РНК ВІЛ-1 описане нижче в прикладах У іншому варіанті зонди, кон'юговані з БСА, зв'язують з магнітними мікрочастками Пов'язані зонди гібридизують в розчині з міченим продуктом ампліфікації і продукт, що утворився видаляють з розчину магнітного шляхом Іммобілізовані магнітним шляхом гібридні дуплекси потім виявляють описаними вище способами Інший придатний метод аналізу, названий 5'нуклеазним методом, описаний в патентах США 5210015 і 5487972 і у Holland і інш, 1988, Ргос Natl Acad Sei USA, 88 7276-7280 В 5'нуклеазном методі мічені зонди, що виявляються, модифіковані таким чином, щоб вони не могли діяти в якості праймерів в синтезі ДНК, додають в реакційну суміш в процесі ампліфікації Будь-який зонд, який гібридизується з ДНК-мішенню протя 12 11 47432 гом кожної стадії синтезу, тобто в процесі подовніки на основі вищенаведеного опису і подальших ження праймера, розщеплюють за допомогою прикладів 5'^3' екзонуклеазній активності ДНК-полімерази, Приклад 1 наприклад, ДНК-полімерази Taq Потім виявляють Конструювання КІЛЬКІСНОГО стандарту продукт розкладання зонда Таким чином, присутДля кількісної оцінки змісту вірусу, здійснюваність продукту розкладання зонда свідчить як про ної з допомогою AMPLICOR HIV-1 MONITOR Test, те, що сталася гібридизація між зондом і ДНКвикористовують КІЛЬКІСНИЙ стандарт (КС), який мішенню, так і про те, що сталася реакція ампліфіампліфікують із застосуванням тієї ж самої пари кації У патентах США 5491063 і 5571673 описані праймерів, але який виявляють з використанням поліпшені способи виявлення розщеплення зонда, іншого зонда КС додають до зразка, що тестуєтьяке супроводить ампліфікацію ся, у ВІДОМІЙ концентрації з метою отримати відомий еталонний сигнал Для широкого діапазону У описаних вище методах аналізу для полегконцентрацій мішені сигнал, що генерується ампшення виявлення гібридних дуплексів звичайно ліфікованій мішенню або ампліфікованим КС, провикористовують мічені олігонуклеотиди Олігонукпорційній КІЛЬКОСТІ, що є КІЛЬКІСТЬ КОПІЙ мішені леотиди можуть бути помічені шляхом включення оцінюють шляхом порівняння сигналу, що генерумітки, що виявляється спектроскопічним, фотохіється при ампліфікації невідомої мішені, і сигналу, мічним, біохімічним, імунохімічним або ХІМІЧНИМ що генерується відомим КС методами Придатні мітки включають 32 Р, флуоресцентні фарби, електронно-щільні реагенти, ферПраймери по даному винаходу ампліфікують менти (наприклад, такі, які використовуються в область, яка не повністю охоплюється КС, вклюметоді ELISAS), біотин або гаптени і протеїни, для ченим в набір AMPLICOR HIV-1 MONITOR Test яких доступні антисироватка або моноклональні (KC-Amplicor) Тому для застосування праймерів антитіла Мічені олігонуклеотиди по винаходу мопо даному винаходу конструювали новий КС Ножуть бути синтезовані і помічені з використанням вий КС конструювали з KC-Amplicor шляхом поспособів, описаних вище для олігонуклеотидів, що довження ПОСЛІДОВНОСТІ KC-Amplicor з метою синтезуються включити сайти скріплення SKCC1 (SEQ Ю N0 3) і SKCC3 (SEQ ID NO 4) КС, що утворився, може Альтернативний метод виявлення ампліфікації бути виявлений за допомогою КС-специфічного нуклеїнової кислоти ВІЛ-1 шляхом оцінки збільзонда, що використовується в AMPLICOR HIV-1 шення загальної КІЛЬКОСТІ двохланцюгової ДНК в MONITOR Test Конструювання плазміди, що місреакційній суміші описаний у Higuchi і інш , 1992, тить ПОСЛІДОВНІСТЬ нового КС, з якої транскрибуBio/Technology, 10 413-417, Higuchi і інш , 1993, ють РНК КС, може бути здійснене з використанням Bio/Technology, 11 1026-1030, і в публікації євростандартних методів, як описане нижче пейської заявки 512334 Виявлення двохланцюгової ДНК-мішені засноване на зростанні флуоресKC-Amplicor, отриманий з AMPLICOR HIV-1 ценції, яка виявляється, коли етидійбромид (EtBr) і MONITOR Test, ампліфікують з використанням ІНШІ мітки, що зв'язуються з ДНК, зв'язуються з праймерів SK145 (SEQ ID NO 1) і SK151 (SEQ ID двохланцюгової ДНК Мітку, що зв'язується з ДНК, NO 7) в умовах, практично ВІДПОВІДНИХ таким, які додають в реакційну суміш для ампліфікації Ампописані нижче в прикладі 2 В результаті ампліфіліфікація ПОСЛІДОВНОСТІ-МІШЄНІ приводить до збікації отримували ДНК- продукт, що містить сайти льшення КІЛЬКОСТІ двохланцюгової ДНК, що в свою скріплення для SK145 (SEQ ID NO 1) і SK151 чергу приводить до збільшення, що виявляється (SEQ ID NO 7) і що зберігає внутрішню ПОСЛІДОВфлуоресценції НІСТЬ, що містить сайт скріплення КС-специфічного зонда Даний винахід також відноситься до наборів, Ампліфікований продукт, що далі утворився, багатоконтейнерних наборів, що містять ВІДПОВІДНІ подовжують для включення сайта скріплення компоненти для практичного здійснення способу праймера SKCC1 (SEQ ID NO 3) і додають лінкер по даному винаходу Такий набір містить, напридля можливості тонування продукту Цього досяклад, праймери для ПЛР-ампліфікацм нуклеїнової гають за допомогою повторної ампліфікації продукислоти ВІЛ-1 Набір також може містити засоби кту з використанням праймера SK145 (SEQ ID NO для виявлення ампліфікованіи нуклеїнової кислоти 1), подовженого на 5'-КІНЦІ з тією метою, щоб ВІЛ-1, такі, як олігонуклеотидні зонди У деяких включити лінкер Hmdlll і SKCC1 (SEQ ID NO 3) випадках зонди фіксують на ВІДПОВІДНІЙ підкладціВІДПОВІДНІ умови ампліфікації описані у Kellogg і мембрані Інші необов'язкові компоненти набору Kwok, 1990, в PCR Protocols A Guide to Methods включають, наприклад, агент, придатний як каталіand Applications, (ред Innis і інш ,), Academic Press, затор синтезу продуктів подовження праймера, San Diego, CA 337-347, за винятком того, що винуклеозидтрифосфати як субстрат, засоби, що користовують більш низьку температуру відпазастосовуються для мічення (наприклад, кон'югат лу/подовження (наприклад, 42°С) для гібридизації авидин-фермент, або ферментний субстрат і хроSKCC1 (SEQ ID NO 3) моген, в тому випадку, коли мітка являє собою біотин), ВІДПОВІДНІ буфери для ПЛР або реакцій Після ЦЬОГО ампліфікований продукт, що утвогібридизації і інструкції по здійсненню даного мерився, ще раз подовжують для включення сайта тоду скріплення праймера SKCC3 (SEQ ID NO 4) і до Нижче винахід детальніше проілюстрований на прикладах, які не обмежують об'єм винаходу Численні варіанти здійснення винаходу в об'ємі формули винаходу, які витікають з прикладів, повинні бути очевидні фахівцям в даній області тех дають другу лінкер до іншого кінця для забезпечення можливості клонування продукція Цього досягають за допомогою ампліфікації продукту з використанням праймера SK145 (SEQ ID NO 1), подовженого на 5'-КІНЦІ з тією метою, щоб включи 14 13 47432 ти лінкер Hindlll, як описано вище, поряд з прайаналізі ПОСЛІДОВНОСТІ Був виявлений ряд нових мером SKCC3 (SEQ 11) N0 4), подовженим на 5'ІЗОЛЯТІВ ВІЛ-1 Для цієї мети на основі нуклеотидКІНЦІ для включення лінкера ХваІ з використанням них послідовностей вибирали певні ізоляти, для описаних вище умов ампліфікації яких передбачається наявність проблем при використанні набору AMPLICOR HIV-1 MONITOR Test Потім ампліфікований продукт вбудовують в Крім того, використали ізоляти, яким була властиплазміду Ампліфіковану ванну ДНК і плазміду ва варіабельність ПОСЛІДОВНОСТІ, характерна для pSP64 (фірма Promega, Madison, WI) по окремості ПІДТИПІВ групи М розщеплюють з допомогою Hindlll і Хваї, а потім лигують з використанням стандартних методів Нуклеїнова кислота-мішень Компетентні клітки трансформують рекомбінантКонструювали плазміди, що містять область ними плазмідами і отримують клон, який містить гена gag ВІЛ-1 з кожного ізолята, і РНК-матриці правильну вставку Клоновану вставку в отриманої ВІЛ-1 транскрибували практично ВІДПОВІДНО ДО рекомбінантної плазміді необхідно секвенувати з методу, описаного у Holodniy і інш , 1991, J Inf метою визначити, що в сайти скріплення праймера Dis , 163 802-865 Готували маточні розчини кожабо зонда не введені мутації ної матриці і визначали концентрації матриць Маточні розчини розбавляли, засновуючись на виРНК КІЛЬКІСНОГО стандарту транскрибують визначенні відносних концентрацій, таким чином, ходячи з рекомбінантної плазміди, що містить КСщоб концентрація матриць, що додаються в кожну ПОСЛІДОВНІСТЬ, з використанням набору реакційну суміш, була однаковою Абсолютна КІЛЬMEGAscnptT" SP6 (фірма Ambion, Inc , Austin, TX) КІСТЬ КОПІЙ матриці, що додаються в реакційні суПриклад 2 міші, становила приблизно 4000-8000 Кількісна оцінка РНК В1Л-1 У цьому прикладі описаний спосіб оцінки відКІЛЬКІСНИЙ стандарт носної ефективності ампліфікації різних ІЗОЛЯТІВ КС, описаний в прикладі 1, вносили в кожну ВІЛ-1 Для порівняння також здійснювали ампліфіреакційну суміш у ВІДОМІЙ концентрації, звичайно кації з використанням набору AMPLICOR HIV-1 приблизно 100 копій на реакційну суміш MONITOR Test Праймери Ізоляти ВІЛ-1 отримували з ВІЛ-1-позитивних Реакції А-Е здійснювали з використанням наКЛІНІЧНИХ зразків Область гена gag тонували і ступних комбінацій праймерів секвенували по стандартних методах, а підтип Комбінації праймерів, що зрівнюються клонуємого ВІЛ-1 визначали, засновуючись на Реакція Комбінація праймерів А SK462 (SEQ ID NO 5) SK431 (SEQ ID NO 6) SK145(SEQIDNO 1) SK151 (SEQ ID NO 7) SK145(SEQIDNO 1) SKCC1 (SEQ ID NO 3) SK145 (SEQ ID NO 1) і SK145M2 (SEQ ID NO 2) SKCC1 (SEQ ID NO 3) SK145(SEQIDNO 1) SKCC3 (SEQ ID NO 4) SK145 (SEQ ID NO 1) і SK145M2 (SEQ ID NO 2) SKCC3 (SEQ ID NO 4) Б В Г Д Е Всі праймери бютинували на 5'-КІНЦІ для виявлення методом зворотного дот-блотинга на мікролунковому планшеті ПОСЛІДОВНОСТІ додаткових, не описаних вище праймерів, приведені нижче в орієнтації 5 ' ^ 3 ' Праймери, що ІНІЦІЮЮТЬ синтез проти ходу транскрипції SK462 (SEQ ID NO 5) AGTTGGAGGACATCAAGCAGCCATGCAAAT Праймери, що ІНІЦІЮЮТЬ синтез по ходу транскрипції SK431 (SEQ ID NO 6) TGCTATGTCAGTTCCCCTTGGTTCTCT SKI51 (SEQ ID NO 7) TGCTATGTCACTTCCCCTTGGTTCTCT Ампліфікація Реакцію ампліфікації А проводили з використанням реагентів і умов з набору AMPLICOR HIV-1 MONITOR Test Реакцію ампліфікації Б проводили в об'ємах по ЮОмкл, що містять наступні реагенти РНК-матриця ВІЛ-1 РНК КС 50мМ біцин, рН 8,3 111мМ К(ОАс) З, 6мМ Мп(ОАс)2 500мкМ дУТФ ЗООмкМ кожного з дАТФ, дЦТФ і дГТФ 50мкМ дТТФ 15%- ний гліцерин 0,2мкМ кожного бютинованого праймера 2 одиниці урацил-ДНК-гликозилази (УДГ) * 10 одиниць ДНК-полімерази rTth * * Виробництво і розробка фірми Hoffman-La Roche і продаж фірмою Perkm Elmer (Norwalk, CT) Реакції ампліфікації В і Г здійснювали практично при таких же умовах, які використовувалися в реакції Б, але з наступними змінами 16 15 47432 ЮОмМ К(ОАс) 10% Невеликі ВІДМІННОСТІ в реакційних сумішах були результатом попередньої оптимізацм умов 500мкМ кожного з дАТФ, дЦТФ і дГТФ ампліфікації для кожної пари праимерів 7,5% -ний гліцерин 10 одиниць УДГ Реакції ампліфікації Б-Е проводили в ДНКтермокоміркі типу ТС9600 (фірма Perkm Elmer, Реакції ампліфікації Д і Е здійснюють практичNorwalk, СТ) з використанням наступного темпено при таких же умовах, які використовувалися в ратурного профілю реакціях В і Г, але за винятком того, що концентрація гліцерину, що використовується, становила інкубація перед реакцією зворотна транскрипція 4 циклу 26 циклів Денатурація Відпал Подовження Денатурація Відпал Подовження остаточне подовження 50°С 60°С 95°С 55°С 72°С 90°С 60°С 72°С 72°С Виявлення апліфікованого продукту з допомогою гібридизації із зондом Ампліфіковані продукти виявляли з використанням реагентів і протоколів з набору AMPLICOR HIV-1 MONITOR Test Початкову концентрацію мішені, що оцінюється, обчислювали ВІДПОВІДНО ДО даного опису Результати При використанні КІЛЬКІСНОГО методу AMPLICOR HIV-1 MONITOR Test початкову концентрацію мішені оцінюють шляхом порівняння сигналу, генерованого після ампліфікації мішені, з сигналом, генерованим після ампліфікації КС відомої концентрації Оскільки відома концентрація КС являє собою концентрацію перед ампліфікацією, а сигнали, що порівнюються, являють собою сигнали, отримані після ампліфікації, то зміни у ВІДНОСНІЙ ефективності ампліфікації повинні впливати на оцінку початкової концентрації невідомої мішені При КІЛЬКІСНІЙ ОЦІНЦІ з допомогою AMPLICOR HIV-1 MONITOR Test використовують калібрування, засноване на ефективності ампліфі протягом 2 хвилин протягом ЗО хвилин, протягом 10 секунд, протягом 10 секунд і протягом 10 секунд, протягом 10 секунд, протягом 10 секунд і протягом 10 секунд, протягом 15 хвилин кації підтипа В ВІЛ-1 Відомо, ЩО ІНШІ ПІДТИПИ ВІЛ-1 можуть ампліфікуватися з більш низькою ефективністю, і, отже, концентрація мішені, що оцінюється може бути занижена в порівнянні з істинною У даному експерименті до кожної реакційної суміші додавали РНК-мішень у ВІДОМІЙ концентрації Таким чином, відносна ефективність ампліфікації для кожного ізолята може бути визначена шляхом порівняння концентрацій мішені, що оцінюються Оскільки при КІЛЬКІСНІЙ ОЦІНЦІ В наборі AMPLICOR HIV-1 MONITOR Test використовують калібрування, засноване на ефективності ампліфікації підтипа В ВІЛ-1, як еталон використали концентрацію мішені підтипа В (клон 105-1), що оцінюється Для кожного ізолята концентрацію мішені підтипа В (клан 105-1), що оцінюється, СПІВВІДНОСИЛИ З концентрацією мішені для ізолята, що оцінюється, отримуючи міру відносної ефективності ампліфікації Ця відносна ефективність ампліфікації приведена нижче в таблиці Символ "—" означає, що реакцію не проводили Ефективність відносно підтипа В Клон 113-1 113-2 114-1 114-2 115-1 115-2 105-1 101-15 107-6 308-1 110-5 111-6 112-7 106-1 108-3 109-1 Підтип А А А А А А А В С D D Е Е Е G G G 694,3 19 12,4 9,8 497,6 646,4 Б 1,7 — — 1,2 1 7,3 0,8 0,9 2,4 1 — — — 520,7 465,7 0,8 3,3 1,9 0,6 — 0,8 — — 1 32,5 Результати показують, що при використанні набору AMPLICOR HIV-1 MONITOR Test (реакція А) різні ізоляти ВІЛ-1 ампліфікувались з істотно В 0,9 1,3 1,4 1,1 0,8 1 1 1,1 0,6 0,6 3,5 и 15 , 2,3 0,5 0,5 Г 1,4 1,1 1,3 1,8 1Д 1,5 1 3,5 0,7 0,7 1,2 1,6 1,9 2 0,8 06 Д 1,4 1,3 0,7 1,5 1 0,9 1 1,9 0,7 0,7 4,6 0,9 1,2 1,8 0,5 06 Е 0,9 0,6 0,9 0,8 1,6 1,4 1 1,4 0,8 0,5 0,8 1,1 1,4 1,5 0,5 0,3 різною ефективністю Деякі з ІЗОЛЯТІВ, включаючи ізолят підтипа Е, клон 110-5, ампліфікувались з ефективністю принаймні приблизно в 500 раз 17 18 47432 більш низької, ніж ефективність ампліфікації клану 105-1 підтипа В Хоч не всі ізоляти були досліджені, застосування пари праймерів SK145 (SEQ ID NO 1) і SK1S1 (SEQ ID NO 7) (реакція Б) дозволило істотно вирівняти ефективність ампліфікації Однак клан 110-5 підтипа Е як і раніше ампліфікувався з ефективністю принаймні приблизно в 500 раз більш низької, ніж ефективність ампліфікації клона 105-1 підтипа В ВІЛ-1 Підтипи, присутні в КЛІНІЧНИХ зразках, не визначали Однак підтипи А і D є звичайними для цього регіону Африки, тому потрібно було чекати, що деякі з цих КЛІНІЧНИХ зразків або не будуть ампліфікуватися зовсім, або будуть ампліфікуватися неефективно при використанні AMPLICOR HIV-1 MONITOR Test Зразки готували таким чином Зразки плазми (80 - 250мкл) об'єднували в КОНІЧНІЙ центрифужної пробірці об'ємом 1,5мл з 20мкл 0,25% (маси/об'єм) червоних полістиролових мікросфер типу Estapor (фірма Bangs Laboratories, Inc , Carmel, IN) і центрифугували протягом 1 ч при 25300g при 4°С Супернатант відсмоктували і дебрис ресуспендували в 250мкл лізуючого буфера (50мкл лізючого буфера містить 6,7мкл 30од/мл RNasm (фірма Promega, Madison, Wl), 0,67мкл ЮОмМ дитиотреїтола (ДТТ), 2мкл 10%-ного NP40 (фірма Pierce, Rockibrd, IL), 0,25мкл 4мг/мл poly-rA РНК, і 40,4мкл обробленої Depc H2O) Дебриси шкубували при кімнатній температурі протягом принаймні 15хв і інтенсивно перемішували для забезпечення повного змішання Застосування праймерів SK145 (SEQ ID NO 1) і SKCC1 (SEQ ID NO 3) (реакція В) дозволило ампліфікувати всі ізоляти, включаючи ізолят підтипа Е, клон 110-5, з ефективністю приблизно в 3 рази меншої, ніж ефективність ампліфікації клона 105-1 підтипа В Добавлення праймера SK145M2 (SEQ П) N 0 2) (реакція Г) ще більш поліпшило ефективність ампліфікації ізолята 110-5, зробивши и практично рівного такого для еталонного штаму підтипа В Аналогічно цьому застосування праймерів SK145 (SEQ ID NO 1) і SKCC3 (SEQ ID NO 4) (реакція Д) дозволило ампліфікувати всі ізоляти, включаючи ізолят підтипа Е, клон 110-5, з ефективністю приблизно в 5 раз менше, ніж ефективність ампліфікації клона 105-1 підтипа В Ампліфікації здійснювали в реакційних сумішах об'ємом ЮОмкл, що містять 50мкл розчину вірусного лізата і 50мкл 2-кратній суміші ампліфікованих реагентів, складеної таким чином, щоб кінцева концентрація реагенту відповідала вказаній вище У кожну реакційну суміш у вигляді частини сумі]лі реагентів додавали приблизно 100 копій ВІДПОВІДНОГО КС Виявлення апліфікованого продукту здійснювали з використанням реагентів і протоколів AMPLICOR HIV-1 MONITOR Test, як описано вище Добавлення праймера SK145M2 (SEQ ID NO 2) (реакція Е) ще більш поліпшило ефективність ампліфікації ізолята 110-5, зробивши її практично рівної ефективності для еталонного штаму підтипа В Приклад З Кількісна оцінка ВІЛ-1 в КЛІНІЧНИХ зразках У цьому прикладі ЗО КЛІНІЧНИХ зразків, отриманих від пацієнтів з Сенегалу з позитивною серологічною реакцією, аналізували на присутність РНК Ампліфікації кожного зразка проводили з наступними комбінаціями праймерів Комбінації праймерів, що порівнюються Реакція А Б В Комбінація праймерів SK462 (SEQ ID NO 5) SK431 (SEQ ID NO 6) S K 1 4 5 ( S E Q I D N O 1) SKCC1 (SEQ ID NO 3) SK145 (SEQ ID NO 1) і SK145M2 (SEQ ID NO 2) SKCC1 (SEQ ID NO 3) Результати, виражені у вигляді КІЛЬКОСТІ КОПІЙ ВІЛ-1-матриці на мл плазми, узагальнені нижче Визначувальна концентрація мішені (копи/мл) Ізолят DKN035 DKN079 DKN154 DKN162 DKN162 DKN169 DKN 171 DKN282 DKN 402 MBN26 MBN31 MBN34 0 360 1140 0 0 0 1180 560 340 27740 180 840 Б 800 30060 21660 16020 12180 3140 640 3400 4260 16940 1820 2160 В Дублікат А Дублікат 1860 37240 54560 25980 10520 7000 500 4360 10520 19220 1820 2200 1600 91780 68820 64340 14300 5651 560 5560 7000 16700 1720 3100 1100 152300 67120 21880 8047 1040 1040 3460 5060 18680 2240 3120 19 47432 МІН 002 МІН 012 МІН 013 МІН 030 МІН 053 МІН 055 МІН 074 МІН 112 МІН 157 MIN 003а MIN 003b MIN017 MIN 067 MIN 126 MIN 139 2320 2960 30360 17625 + 10560 5700 30480 520 1300 1760 540 0 44320 460 Ізолят А MIN 146 MIN217 MIN 589 200 0 154780 51320 33620 31980 178500 534960 43960 3980 271980 165480 57720 32820 437380 0 63600 146320 121100 40920 55360 273938 231620 542220 6020 490780 82920 21620 30940 375120 0 38460 142800 Б Дублікат 49920 32220 267740 Результати свідчать про те, що комбінації праймерів Б і В по даному винаходу дозволяють ампліфікувати більшу КІЛЬКІСТЬ КЛІНІЧНИХ зразків Комбінації праймерів Б і В дозволяють ампліфікувати всі з ЗО зразків, крім одного У протилежність цьому при використуванні AMPLICOR HIV-1 MONITOR Test не вдалося ампліфікувати 6 із 29 зразків Ампліфікація зразка МІН 053 з використанням AMPLICOR HIV-1 MONITOR Test привела до отримання сильного сигналу від мішені, але не вдалося генерувати сигнал КС Тому не вдалося оцінити КІЛЬКІСНО цей зразок, і він позначений символом "+" в приведеній вище таблиці Крім того, для значної КІЛЬКОСТІ зразків КІЛЬКІСТЬ КОПІЙ, виявлених з використанням як комбінації праймерів Б, так і В, було значно вище, ніж (1) (2) 20 144180 40740 42800 169750 530900 49400 3640 423600 169980 35380 27760 447740 0 56680 94520 123900 75840 71220 189625 878340 37400 4940 416140 146320 34560 26600 902780 0 40300 105600 В Дублікат 32100 1880 127100 19900 2320 144160 30400 2580 228040 така, що виявлено з використанням AMPLICOR HIV-1 MONITOR Test Враховуючи варіабельність ефективності ампліфікації, яка показана вище в прикладі 2, можна передбачити, що більш низькі виявлені концентрації матриці, отримані з використанням AMPLICOR HIV-1 MONITOR Test, ймовірно є результатом істотно більш низької ефективності ампліфікації Вірусна РНК не була виявлена в зразку MIN 067 Однак невідомо, чи є це слідством невиявленоі варіабельності послідовності-мішені, що служить перешкодою для гібридизації праймера або зонда, або це зумовлене якою-небудь іншою причиною ПЕРЕЛІК ПОСЛІДОВНОСТЕЙ ЗАГАЛЬНА ІНФОРМАЦІЯ ЗАЯВНИК (і) (Е) КРАЇНА Швейцарія ПОШТОВИЙ КОД (ZIP) CH-4070 (R (G) ТЕЛЕФОН 061 688 37 82 (Н) ТЕЛЕФАКС 061 688 13 95 ТЕЛЕКС 962292/965542 hlrch (І) НАЗВА ВИНАХОДУ Праймери для виявлення ВІЛ-1 00 КІЛЬКІСТЬ ПОСЛІДОВНОСТЕЙ 7 (ні) ФОРМА УЯВЛЕННЯ ДЛЯ КОМП'ЮТЕРА (IV) (А) ТИП НОСІЯ флоппи-диск (В) КОМП'ЮТЕР Apple Macintosh (С) ОПЕРАЦІЙНА СИСТЕМА System 7 1 (Macintosh) (D) ПРОГРАМНЕ ЗАБЕЗПЕЧЕННЯ Word 5 1 ДАНІ ПРО ПРІОРИТЕТНУ ЗАЯВКУ (VI) (А) НОМЕР ЗАЯВКИ 60-037744 (В) ДАТА ПОДАННЯ 17 01 97 ІНФОРМАЦІЯ ПРО ПОСЛІДОВНІСТЬ SEQ ID NO 1 ( О ХАРАКТЕРИСТИКИ ПОСЛІДОВНОСТІ (А) ДОВЖИНА ЗО пара основ (В) ТИП нуклеїнова кислота (С) ХАРАКТЕРИСТИКА ЛАНЦЮГА одноланцюгова (D) ТОПОЛОГІЯ лінійна (и) ТИП МОЛЕКУЛИ ДНК (геномна) 21 47432 ОПИС ПОСЛІДОВНОСТІ SEQ ID NO 1 (XI) AGTGGGGGGA CATCAAGCAG ССАТЄСАААТ (2) ІНФОРМАЦІЯ ПРО ПОСЛІДОВНІСТЬ SEQ ID NO 2 ХАРАКТЕРИСТИКИ ПОСЛІДОВНОСТІ (А) ДОВЖИНА ЗО пара основ (В) ТИП нуклеїнова кислота (С) ХАРАКТЕРИСТИКА ЛАНЦЮГА одноланцюгова (D) ТОПОЛОГІЯ лінійна ТИП МОЛЕКУЛИ ДНК (геномна) 00 (XI) ОПИС ПОСЛІДОВНОСТІ SEQIDNO 2 AGTGGGGGGA CACCAGGCAG СААТФСАААТ (і) (2) ІНФОРМАЦІЯ ПРО ПОСЛІДОВНІСТЬ SEQ ID NO 3 ( О ХАРАКТЕРИСТИКИ ПОСЛІДОВНОСТІ (А) ДОВЖИНА 28 пара основ (В) ТИП нуклеїнова кислота (С) ХАРАКТЕРИСТИКА ЛАНЦЮГА одноланцюгова (D) ТОПОЛОГІЯ лінійна (и) ТИП МОЛЕКУЛИ ДНК (геномна) (XI) ОПИС ПОСЛІДОВНОСТІ SEQIDNO 3 TACTAGTAGT TCCTGCTATG TCACTTCC (2) ІНФОРМАЦІЯ ПРО ПОСЛІДОВНІСТЬ SEQ ID NO 4 ( О ХАРАКТЕРИСТИКИ ПОСЛІДОВНОСТІ (А) ДОВЖИНА 26 пара основ (В) ТИП нуклеїнова кислота (С) ХАРАКТЕРИСТИКА ЛАНЦЮГА одноланцюгова (D) ТОПОЛОГІЯ лінійна ТИП МОЛЕКУЛИ ДНК (геномна) (и) (XI) ОПИС ПОСЛІДОВНОСТІ SEQIDNO 4 TGAAGGGTAC TAGTAGTTCC TGCTAT (2) ІНФОРМАЦІЯ ПРО ПОСЛІДОВНІСТЬ SEQ ID NO 5 ( О ХАРАКТЕРИСТИКИ ПОСЛІДОВНОСТІ (А) ДОВЖИНА ЗО пара основ (В) ТИП нуклеїнова кислота (С) ХАРАКТЕРИСТИКА ЛАНЦЮГА одноланцюгова (D) ТОПОЛОГІЯ лінійна ТИП МОЛЕКУЛИ ДНК (геномна) (и) (XI) ОПИС ПОСЛІДОВНОСТІ SEQIDNO 5 AGTTGGAGGA CATCAAGCAG CCATGCAAAT (2) ІНФОРМАЦІЯ ПРО ПОСЛІДОВНІСТЬ SEQ ID NO 6 ( О ХАРАКТЕРИСТИКИ ПОСЛІДОВНОСТІ (А) ДОВЖИНА 27 пара основ (В) ТИП нуклеїнова кислота (С) ХАРАКТЕРИСТИКА ЛАНЦЮГА одноланцюгова (D) ТОПОЛОГІЯ лінійна (и) ТИП МОЛЕКУЛИ ДНК (геномна) (XI) ОПИС ПОСЛІДОВНОСТІ SEQIDNO 6 TGCTATGTCA GTTCCCCTTG GTTCTCT (2) ІНФОРМАЦІЯ ПРО ПОСЛІДОВНІСТЬ SEQ ID NO 7 ( О ХАРАКТЕРИСТИКИ ПОСЛІДОВНОСТІ (А) ДОВЖИНА 27 пара основ (В) ТИП нуклеїнова кислота (С) ХАРАКТЕРИСТИКА ЛАНЦЮГА одноланцюгова (D) ТОПОЛОГІЯ лінійна (и) ТИП МОЛЕКУЛИ ДНК (геномна) (XI) ОПИС ПОСЛІДОВНОСТІ SEQIDNO 7 TGCTATGTCA CTTCCCCTTG GTTCTCT 22 23 47432 ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71 24
ДивитисяДодаткова інформація
Назва патенту англійськоюOligonucleotic primer for amplification of nucleic acid of the human immunodeficiency virus of type 1 (hiv-1) (variants), a pair of oligonucleotic primers (variants), a set of oligonucleotic primers (variants), a set for identification of nucleic acid of the human immunodeficiency virus hiv-1 (variants), a method of amplification of nucleic acid of the human immunodeficiency virus hiv-1
Назва патенту російськоюОлигонуклеотидный праймер, предназначенный для амплификации нуклеиновой кислоты вируса иммунодефицита человека типа 1 (вич-1) (варианты), пара олигонуклеотидных праймеров (варианты), набор олигонуклеотидных праймеров (варианты), набор для выявления нуклеиновой кислоты вируса иммунодефицита человека вич-1 (варианты), способ амплификации нуклеиновой кислоты вируса иммунодефицита человека вич-1
МПК / Мітки
МПК: C12N 15/09, C12Q 1/68, C12Q 1/70
Мітки: варіанти, праймерів, людини, нуклеїнової, олігонуклеотидний, вірусу, віл-1, набір, праймер, типу, призначений, імунодефіциту, олігонуклеотидних, кислоти, ампліфікації, пара
Код посилання
<a href="https://ua.patents.su/12-47432-oligonukleotidnijj-prajjmer-priznachenijj-dlya-amplifikaci-nuklenovo-kisloti-virusu-imunodeficitu-lyudini-tipu-1-vil-1-varianti-para-oligonukleotidnikh-prajjmeriv-varianti-nabir-ol.html" target="_blank" rel="follow" title="База патентів України">Олігонуклеотидний праймер, призначений для ампліфікації нуклеїнової кислоти вірусу імунодефіциту людини типу 1 (віл-1) (варіанти), пара олігонуклеотидних праймерів (варіанти), набір олігонуклеотидних праймерів</a>
Попередній патент: Спосіб налагодження резонансного нвч підсилювача на задану частоту та пристрій для його здійснення
Наступний патент: Вакцини проти живого вірусу prrs з низькою патогенністю і способи їх одержання
Випадковий патент: Сировиготовлювач