Ацильовані амінофенілсульфонілсечовини та їх солі, проміжні фенілсульфоніли, гербіцидний засіб на основі ацильованих амінофенілсульфонілсечовин та спосіб боротьби з бур’яновою рослинністю
Номер патенту: 48134
Опубліковано: 15.08.2002
Автори: БАУЕР Клаус, Бірінгер Херманн, Шнабель Герхард, Вілльмс Лотар
Формула / Реферат
1. Ацилированные аминофенилсульфонилмочевины общей формулы (I):
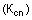
где R1 и R2 - водород или алкил с 1 или 2 атомами углерода или вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 3-8 кольцевыми атомами,
R3 - группа -COR5, где R5 означает водород, алкоксил с 1-4 атомами углерода, алкил с 1-6 атомами углерода, которые могут быть замещены в алкильной части 1-3 атомами галогена, циклоалкил с 3-8 атомами углерода, моно- или диалкиламино с 1-4 атомами углерода в каждой алкильной части, группа -NH-R6, где R6 означает пиримидиновое кольцо, незамещенное или замещенное двумя алкоксильными группами с 1-4 атомами углерода, или -SO2R7, где R7 имеет значение радикала R5, кроме алкоксила с 1-4 атомами углерода,
R4 - водород, алкил с 1-4 атомами углерода,
X, Υ - галоген, алкил с 1-6 атомами углерода, алкоксил с 1-6 атомами углерода, моно- или диалкиламино с 1-14 атомами углерода в каждой алкильной части,
Z - CH или Ν,
или их соли.
2. Ацилированные аминофенилсульфонилмочевины общей формулы (I) по п.1, где R1 и R2 вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 4-8 кольцевыми атомами,
или их соли.
3. Ацилированные аминофенилсульфонилмочевины общей формулы (I) по п. 1,
где X и Υ означают галоген, алкил с 1-4 атомами углерода, алкоксил с 1-4 атомами углерода, или их соли.
4. Ацилированные аминофенилсульфонилмочевины общей формулы (I) по п. 1, где R1 и R2 вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 5 или 6 кольцевыми атомами,
R3 - группа -COR5, где R5 означает водород, алкил с 1-4 атомами углерода, алкоксил с 1-4 атомами углерода, которые могут быть замещены в алкильной части 1-3 атомами галогена, циклоалкил с 3-6 атомами углерода, моно- или диалкиламино с 1-4 атомами углерода в каждой алкильной части, или группа -SO2R7, где R7 означает алкил с 1-3 атомами углерода, который может быть замещен 1-3 атомами галогена,
R4-водород, метил,
X, Υ - галоген, алкил с 1-2 атомами углерода, алкоксил с 1-2 атомами углерода,
или их соли.
5. Производные фенилсульфонила общей формулы (XVI):
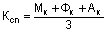
где
R1 и R2 имеют указанные в пп. 1-4 значения, а R8 и R9 имеют следующее значение:
если R8 означает группу NН-трет-бутил, то R9 означает нитро, амино или группу NHR10, в которой R10 имеет указанное в пп. 1-4 для радикала R3 значение, либо R8 означает хлор, амино или изоцианато, а R9 - группа NHR10, где R10 имеет вышеуказанное значение, представляющие собой промежуточные продукты для получения ацилированных аминофенилсульфонилмочевин общей формулы (І) по пп. 1-4.
6. Гербицидное средство, содержащее активное вещество на основе ацилированных аминофенилсульфонилмочевин и целевые добавки, отличающееся тем, что в качестве ацилированных аминофенилсульфонилмочевин оно содержит соединения общей формулы (І) по пп. 1-4 или их соль в эффективном количестве.
7. Способ борьбы с сорной растительностью путем обработки последней или ее биотопа, или растений, их семян или посевных участков ацилированными аминофенилсульфонилмочевинами, отличающийся тем, что в качестве ацилированных аминофенилсульфонилмочевин используют соединения общей формулы (І) по пп. 1-4 или их соль в эффективном количестве.
Текст
1 Ацилированные аминофенилсульфонилмочевины общей формулы (І) О C-NR/R2 X SCX-NH-C-NІ 11 O R 4 О N Z Y где R1 и R2 - водород или алкил с 1 или 2 атомами углерода или вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 3-8 кольцевыми атомами, R3 - группа -COR5, где R5 означает водород, алкоксил с 1-4 атомами углерода, алкил с 1-6 атомами углерода, которые могут быть замещены в алкильной части 1-3 атомами галогена, циклоалкил с 3-8 атомами углерода, моно- или диалкиламино с 1-4 атомами углерода в каждой алкильной части, группа -NH-R6, где R6 означает пиримидиновое кольцо, незамещенное или замещенное двумя алкоксильными группами с 1-4 атомами углерода, или -SO2R7, где R7 имеет значение радикала R5, кроме алкоксила с 1-4 атомами углерода, R4 - водород, алкил с 1-4 атомами углерода, X, Y - галоген, алкил с 1-6 атомами углерода, алкоксил с 1-6 атомами углерода, моно- или диалкиламино с 1-14 атомами углерода в каждой алкильной части, Z-CH или N, или их соли 2 Ацилированные аминофенилсульфонилмочевины общей формулы (I) по п 1 , где R1 и R2 вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 4-8 кольцевыми атомами, или их соли 3 Ацилированные аминофенилсульфонил мочевины общей формулы (I) по п 1, где X и Y означают галоген, алкил с 1-4 атомами углерода, алкоксил с 1-4 атомами углерода, или их соли 4 Ацилированные аминофенилсульфонил мочевины общей формулы (І) по п 1, где R1 и R2 вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 5 или 6 кольцевыми атомами, R3 - группа -COR5, где R5 означает водород, алкил с 1-4 атомами углерода, алкоксил с 1-4 атомами углерода, которые могут быть замещены в алкильной части 1-3 атомами галогена, циклоалкил с 3-6 атомами углерода, моно- или диалкиламино с 1-4 атомами углерода в каждой алкильной части, или группа -SO2R7, где R7 означает алкил с 1-3 атомами углерода, который может быть замещен 1-3 атомами галогена, R4-BOflopofl, метил, X, Y - галоген, алкил с 1-2 атомами углерода, алкоксил с 1-2 атомами углерода, или их соли 5 Производные фенилсульфонила общей формулы (XVI) SO2-R (XVI) где R1 и R2 имеют указанные в пп 1-4 значения, а R8 и R9 имеют следующее значение если R8 означает группу NH-трет-бутил, то R9 означает нитро, амино или группу NHR10, в которой R10 имеет указанное в пп 1-4 для радикала R3 значение, либо R8 означает хлор, амино или изоцианато, a R9 - группа NHR10, где R10 имеет О ГО 00 48134 вышеуказанное значение, представляющие собой промежуточные продукты для получения ацилированных аминофенилсульфонилмочевин общей формулы (I) по пп 1-4 6 Гербицидное средство, содержащее активное вещество на основе ацилированных аминофенилсульфонилмочевин и целевые добавки, отличающееся тем, что в качестве ацилированных аминофенилсульфонилмочевин оно содержит соединения общей формулы (I) по пп 1-4 или их Изобретение относится к новым производным аминофенилмочевины, обладающим биологической активностью, более конкретно, к эмулированным аминофе-нилсульфонил мочевинам, промежуточным фенилсульфо'нилам, гербицидному средству и способу борьбы с сорной растительностью Известны ацилированные аминофенилсульфонилмочевины, обладающие гербицидной активностью (см патент США № 4 892*946, кл С 07,0 239/28, опуб 9-го января 1990 г) Задачей изобретения является расширение ассортимента ациллированных аминофенилсульфонилмочевин, которые могут представлять собой активное вещество гербицидного средства Поставленная задача решается предлагаемыми ацилированными аминофенилсульфонилмочевинами общей формулы (I) О соль в эффективном количестве 7 Способ борьбы с сорной растительностью путем обработки последней или ее биотопа, или растений, их семян или посевных участков ацилированными аминофенилсульфонил мочевинами, отличающийся тем, что в качестве ацилированных аминофенилсульфонилмочевин используют соединения общей формулы (I) по пп 1-4 или их соль в эффективном количестве (і) де стереоизомеров, таких, как, например, энантиомеры, диастереомеры, Z- и Е-изомеры, или их солей Стереоизомеры можно получать обычными методами из смесей стереоизомеров или также путем стереоизбирательной реакции с использованием стереохими-чески чистых исходных веществ Соли соединений формулы (I) получают за счет того, что водород группы -SO2NH- или также другие ацидные атомы водорода (например, в группе СООН) заменяют пригодным для сельского хозяйства катионом Такими солями являются, например, соли металлов, в частности соли щелочных или щелочноземельных металлов, в частности, соли натрия и калия, или также аммониевые соли или соли с органическими аминами Кроме того, солеобразование можно осуществлять путем присоединения кислоты к основным группам, как, например, к амино- и алкиламиногруппе Пригодными для этого кислотами являются сильные неоганические или органические кислоты как, например, соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота T 2 R и R - водород или алкил с 1 или 2 атомами углерода или вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 3 - 8 кольцевыми атомами, R3 - группа -COR5, где R5 означает водород, алкокси с 1 - 4 атомами углерода, алкил с 1 - б атомами углерода, которые могут быть замещены в алкильной части 1 - 3 атомами галогена, циклоалкил с 3 - 8 атомами углерода, моно- или диалкиламино с 1 - 4 атомами углерода в каждой алкильной части, группа -NH-R , где R6 означает пиримидиновое кольцо, незамещенное или замещенное двумя алкоксильными группами с 1 - 4 атомами углерода или -SO2R7, где R7 имеет значение радикала R , кроме алкокси с 1 - 4 атомами углерода, R4 - водород, алкил с 1 - 4 атомами углерода, X, Y - галоген, алкил с 1 - 6 атомами углерода, алкокси с 1 - 6 атомами углерода, моно- или диалкиламино с 1 - 4 атомами углерода в каждой алкильной части, Z - СН или N, или их солями Соединения формулы (I) могут иметься в ви В первую группу предпочтительных ацилированных аминофенилсульфонилмо-чевин общей формулы (II) входят соединения, у которых R1 и R2 вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 4 - 8 кольцевыми атомами, или их соли Во вторую группу предпочтительных ацилированных аминофенилсульфонил-мочевин общей формулы (I) входят соединения, у которых X и У означают галоген, ал кил с 1 - 4 атомами углерода, алкокси с 1 - 4 атомами углерода, или их соли В третью группу предпочтительных ацилированных аминофенилсульфонил мо-чевин общей формулы (I) входят соединения, у которых R1 и R2 вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо с 5 или б кольцевыми атомами, R3 - группа -COR5, где R5 означает водород, алкил с 1 - 4 атомами углерода, алкокси с 1 - 4 атомами углерода, которые могут быть замещены в алкильной части 1-3 атомами галогена, циклоалкил с 3 - 6 атомами углерода, моно- или диалкиламино с 1 - 4 атомами углерода в каждой алкильной части, или группа -SO2R7, где R7 означает алкил с 1 - 3 атомами углерода, который может быть замещен 1-3 атомами галогена, C-NR'R* SOr-NH~C~-N N UJ і I, N О R4 48134 R - водород, метил, X, У - галоген, алкил с 1 - 2 атомами углерода, алкокси с 1 - 2 атомами углерода, или их соли Соединения общей формулы (I) или их соли можно получать известными способами, например, за счет того, что а) соединение формулы (II) 1 CO-NR R 2 00, SO2NH2 Т з R - R имеют вышеуказанное значение, подвергают взаимодействию с гетероциклическим карбаматом формулы (III) X (HI), R*O-CG-NR 4 —(О где X, У и Z имеют вышеуказанное значение, а R* означает незамещенный или замещенный фенил или алкил с 1 - 4 атомами углерода, или б) сульфонилизоцианат формулы (IV) 1 .CO-NR R X (VII), O=C=I где X, У и Z имеют вышеуказанное значение, в присутствии пригодного основания, например, карбоната калия или триэтиламина Сульфонамиды формулы (II), сульфонилизоцианаты формулы (IV) и сульфо-нилхлориды формулы (VI) являются новыми соединениями Реакцию соединений формул (II) и (III) предпочтительно осуществляют в присутствии служащего в качестве катализатора основания в среде инертных растворителей, например, дихлорметана, ацетонитрила, диоксана или тетраги-дрофурана, при температуре от -10°С до точки кипения используемого растворителя При этом в качестве оснований используют, например, органические аминооснования как, например, 1,8диазабицикло[5 4 0]-ундец-7-ен, в частности при R* = (замещенный) фенил или триметил- или триэтилалюминий, в частности, при R* = алкил Соединения формулы (II) получают, например, из г\І-(т-бутил)-сульфонамидов формул (VIII), (IX) и (X) (см формулу VIII, Z* = R3NH-) СО—NR'R' (Vill), 2 SO2NH SO2NCO ' = NHR3 R - R имеют вышеуказанное значение, подвергают взаимодействию с гетероциклическим амином формулы (V) R HN> W (V). N W Z где R , X, Y и Z имеют вышеуказанное значение, или в) сульфохлорид формулы (VI) (VI), SO2CI где R1 - R имеют вышеуказанное значение, подвергают взаимодействию с гетероциклическим амином вышеуказанной формулы (V) в присутствии цианата, например, цианата щелочного металла как, например, цианата натрия или калия, или г) сульфонамид вышеуказанной формулы (II) подвергают взаимодействию с (тио-)изоцианатом формулы (VII) NH2 Исходя из соединений формулы (VIII), в которых R1 , R2, R3 имеют указанные для формулы (I) значения, получают соединения формулы (II) путем взаимодействия с сильной кислотой В качестве сильной кислоты пригодны, например, минеральные кислоты как, например, серная кислота или хлористоводородная кислота, или сильные органические кислоты как, например, три фтору ксусная кислота Снятие т-бутила осуществляют при температуре от -20°С до температуры флегмы реакционной смеси, предпочтительно при температуре О -40°С Взаимодействие можно осуществлять в среде растворителя, например, дихлорметана или трихлорметана Соединения формулы (VIII) можно получать, например, из анилиновых производных формулы (IX) (см формулу (VIII), Z* = МН2) путем взаимодействия с пригодными электрофильными соединениями, например, ангидридами или хлорангидридами кислот, изоцианатами, тиоизоцианатами, сульфохлоридами или амидосульфохлоридами Указанные анилины формулы (IX) получают путем известных из литературы методов, например, из соединений формулы (X) (см формулу 48134 (VIII), Z* = NO2) путем восстановления нитрогрупп, например, путем каталитического гидрирования или восстановления железном в уксуснокислой среде Соединения формулы (X) можно получать из бензоатов формулы (XI) путем амидирования (XI) (XII) Образование амидов осуществляется путем реакции бензоатов формулы (XI), в которой R° означает алкил, с аминами формулы (XII) Соединения формул (XI) и (XII) известны, или они представляют собой эдукты, которые можно приобретать на рынке или эти соединения можно получать аналогично общеизвестным методам Амиды формул (VIII), (IX) и (X) являются новыми соединениями Альтернативный метод получения соединений формулы (XI) Представляет собой нижеследующий синтез Исходя из 2-амино-нитробензойных кислот формулы (XIII), например, 2-амино-4нитробензойной кислоты формулы (ХШа), получают соответствующие сложные эфиры бензойной кислоты формулы (XIV), в которых R° означает алкил, путем обычной этерификации с применением соответствующих спиртов формулы R°OH и пригодной кислоты, например, серной кислоты СООН (XIII) COOR0 (XIV) Путем диазотирования аминогруппы и последующего взаимодействия с двуокисью серы в присутствии хлористой меди получают сульфохлорид формулы (XV) СО—OR0 (XV) O2N SO2CI Путем аммонолиза соединений формулы (XV) с использованием т-бутиламина получают сульфонамиды формулы (XI) Требуемые для реакции соединений формулы (II) согласно варианту а) кар-баматы формулы (III) известны из литературы, или их можно получать аналогично известным методам Фенилсульфонилизоцианаты формулы (IV) можно получать известными способами, например, путем взаимодействия соединений формулы (III), например, с фосгеном Взаимодействие соединений формулы (IV) с аминогетероциклами формулы (V) проводят предпочтительно в среде инертных апротонных растворителей как, например, диоксана, ацетонитрила или тетрагидрофурана, при температурах от 0°С до температуры кипения растворителя Взаимодействие сульфохлоридов формулы (VI) с аминогетероциклами формулы (V) и цианатами, например, цианатом натрия или калия, проводят, например, в среде инертных апротонных растворителей как, например, ацетонитрила, в случае необходимости в присутствии осований, например, 0,5 - 2 эквивалентов основания, или в среде основного апротонного растворителя, при температурах от -10°С до 100°С, предпочтительно от -10°С до 60°С, в частности, от 15°С до 40°С В качестве основания или основного апротонного растворителя пригодны, например, пиридин, пиколин или лутидин, или их смесь (Тио)изоцианаты формулы (VII) можно получать путем известных из литературы методов Взаимодействие (тио)изоцианатов формулы (VII) с соединениями формулы (II) осуществляют при температуре от -10°С до 100°С, предпочтительно от 20°С до 100°С, в среде инертного апротонного растворителя, например, ацетона или ацетонитрила, в присутствии пригодного основания, например, триэтиламина или карбоната калия Соли соединений формулы (I) предпочтительно получают в среде инертного растворителя, например, воды, метанола, ацетона, дихлорметана, тетрагидро-фурана, толуола или гептана, при температуре от 0°С до 100°С Пригодными основаниями для получения предлагаемых солей являются, например, карбонаты щелочных металлов как, например, карбонат калия, гидроокиси щелочных и щелочноземельных металлов как, например, гидроокись натрия, калия или кальция, аммиак, или пригодное аминооснование как, например, триэтиламин или этаноламин В качестве кислот для солеобразования пригодны, например, хлористоводородная кислота, бромистоводородная кислота, серная кислота или азотная кислота Под термином "инертные растворители" понимаются растворители, которые являются инертными в соответствующих условиях реакции, но которые не должны быть инертными в любых условиях 48134 С учетом вышеприведенной информации о том, что некоторые промежуточные соединения являются новыми, дополнительным объектом являются производные фенилсульфонила общей формулы (XVI) (XVI), SO,—R где R и R имеют вышеуказанное значение, a R и R имеют следующее значение если R8 означает группу NH-трет-бутил, то R9 означает нитро, амино или группу NHR10, в которой R10 имеет указанное в формуле (I) для радикала R3 значение, либо R8 означает хлор, амино или изоцианато, a R - группа NHR , где R имеет вышеуказанное значение Благодаря гербицидной активности соединения вышеприведенной формулы (I) (далее «предлагаемые соединения») и их соли могут представлять собой активное вещество гербицидного средства, которое является дальнейшим объектом изобретения Данное средство содержит эффективное количество активного вещества Гербицидное средство может иметься в виде любого стандартного препарата, такого, как, например, смачивающиеся порошки, водорастворимые порошки, водорастворимые концентраты, эмульгируемые концентраты, эмульсии как, например, эмульсии типа масла в воде или вода в масле, разбрызгиваемые растворы, суспендируемые концентраты, дисперсии на основе масла или воды, смешиваемые с маслом растворы, заключенные в капсулы суспензии, пылевидные средства, протравливатели, рарбрасываемые грануляты, грануляты для нанесения на почву, микрогрануляты, разбрызгиваемые грануляты, суспен-зионные грануляты и адсорбционные грануляты, вододиспергируемые грануляты, препараты для распределения активного вещества в чрезвычайно низком объеме, микрокапсул и и воски Данные препараты могут содержать еще необходимые вспомогательные вещества, как, например, инертные вещества, поверхностноактивные вещества, растворители и дальнейшие целевые добавки 9 На основе указанных препаратов можно готовить смеси предлагаемых активных веществ с другими пестицидными веществами, например, инсектицидами, акарицидами, другими гербицидами, фунгицидами, антидотами, удобрениями и/или регуляторами роста растений Такие комбинационные препараты могут поступать в торговлю в готовом виде или же их можно приготовлять в баках непосредственно перед употреблением Смачивающиеся порошки являются равномерно диспергируемыми в воде препаратами, которые кроме активного вещества и разбавителя или инертного вещества содержат еще поверхностно-активные вещества ионного и/или неионогенного типа смачиватели (смачиватели, диспергаторы), например, полиок 10 сиэтилированные алкилфенолы, полиоксиэтилированные спирты жирного ряда, полиоксиэтилированные жирные амины, сульфаты простого полигликолевого эфира спирта жирного ряда, алкансульфонаты, алкилбензолсульфонаты, лигнинсульфокислый натрий, 2,2'-динафтилметан6,6'-дисульфокислый натрий, ди-бутилнафталинсульфокислый натрий или также олеоилметилтауринкислый натрий Для получения смачивающегося порошка гербицидные активные вещества тонко измельчают в обычной аппаратуре, например, молотковой мельнице, воздуходувной мельнице или мельнице со струйной воздуходувкой, и одновременно с измельчением или после него смешивают со вспомогательными веществами Эмульгируемые концентраты получают путем растворения активного вещества в органическом растворителе, например, бутаноле, циклогексаноне, диметил-формамиде, ксилоле, или же высококипящих ароматах или углеводородах или смесях органических растворителей, при добавлении одного или нескольких поверхностноактивных веществ ионного или неионогенного типа (эмульгаторы) В качестве эмульгаторов можно применять, например, алкиларилсульфокислые кальциевые соли как, например, додеци л бензол сул ьфонат кальция, или неионогенные эмульгаторы как, например, сложный политиколевый эфир жирной кислоты, простой алкиларилполигликолевый эфир, простой полигликолевый эфир спирта жирного ряда, продукты конденсации окисей пропилена и этилена, простой ал кил полиэфир, сложный сорбитановый эфир как, например, сложный сорбитановый эфир жирной кислоты, или сложный полиоксиэтиленсорбитановый эфир как, например, сложный полиоксиэтиленсорбитановый эфир жирной кислоты Пылевидные препараты получают путем размалывания активного вещества вместе с тонкодисперсными твердыми веществами как, например, тальком, естественным глинами, например, каолином, бентонитом или пирофиллитом, или диатомовыми землями Суспензионные концентраты могут иметься на основе воды или масла Их можно получать, например, путем мокрого помола посредством имеющихся в торговле мельниц, и в случае необходимости, при добавлении вышеупомянутых поверхностно-активных веществ Эмульсии как, например, эмульсии типа масла в воде, можно получать, например, с помощью мешалок, коллоидальных мельниц и/или статических смесителей при использовании водных органических растворителей и, в случае необходимости, вышеупомянутых поверхностноактивных веществ Грануляты можно получать или путем напыления активного вещества на способный к адсорбции, гранулированный инертный материал, или путем нанесения концентрата активного вещества посредством клеящих веществ, как, например, поливинилового спирта, полиакрил кислого натрия, или также минеральных масел, на поверхность носителей, например, песка, каоли 48134 12 11 нитов или гранулированного инертного материаНеобходимая норма расхода предлагаемых ла Кроме того, пригодные аісгивньїе вещества соединений зависит от внешних условий, наприможно гранулировать известными для получения мер, температуры, влажности и вида применяегранулированных удобрений приемами, в случае мого гербицида Она может колебаться в широнеобходимости в смеси с удобрениями ких пределах, например, от 0,001 до 10,0кг/га или больше активного вещества, однако, предпочтиДиспергируемые в воде грануляты получают, тельно она составляет 0,005 - 5кг/га как правило, обычными способами, например, путем распылительной сушки, гранулирования в Еще одним объектом изобретения является псевдо-ожиженном слое, гранулирования на таспособ борьбы с сорной растительностью путем релках, смешивания при помощи высокоскоростобработки последней или ее биотопа или растеных смесителей или экструзии без применения ний их семян или посевных участков предлагаетвердого инертного материала мыми соединениями формулы (I) или их солями в эффективном количестве Агрохимические препараты, как правило, содержат 0,1 - 99вес %, в частности 0,1 - 95вес % Получение предлагаемых соединений форактивного вещества формулы (I) или его соли мулы (I) поясняется следующими примерами Концентрация активного вещества в смачиПример 1 Сложный метиловый эфир 2вающихся порошках составляет, например, окоамино-4-нитробензойной кислоты ло 10 - 90вес %, а остаток до ЮОвес % состоит Смесь 118,8г 2-амино-4-нитробензойной кииз обычных вспомогательных веществ В эмульслоты, 1000мл метанола и 120мл концентрирогируемых концентратах концентрация активного ванной серной кислоты нагревают до кипения в вещества может составлять около 1 - 90вес %, течение 16 часов Смесь сгущают при пониженпредпочтительно 5 - 80вес % Пылевидные преном давлении, поглощают в сложном этиловом параты содержат 1 - ЗОвес %, в большинстве эфире уксусной кислоты и промывают насыщенслучаев 5 - 20вес % активного вещества, а разным раствором бикарбоната натрия После сушбрызгиваемые растворы содержат около 0,05 ки над сульфатом натрия органическую фазу 80, предпочтительно 2 - 50вес % активного весгущают щества В случае диспергирующихся в воде граПолучают 114,2г (89%) сложного метилового нулятов содержание активного вещества частичэфира 2-амино-4-нитробен-зойной кислоты, точно зависит от того, является ли активное ка плавления 156-158°С вещество жидким или твердым, и от вида вспоПример 2 Сложный метиловый эфир 2могательных веществ, наполнителей и т д В хлорсульфонил-4-нитробензойной кислоты диспергирующихся в воде гранулятах содержаК суспензии 1300мл ледяной уксусной кисние активного вещества составляет, например, 1 лты, 516мл концентрированной соляной кислоты - 95вес %, предпочтительно 10 - 80вес % и 441,7г (1,689моль) сложного метилового эфира 2-амино-4-нитробензойной кислоты, полученного Кроме того, вышеупомянутые препараты мосогласно примеру 1, при температуре 13 - 15°С гут содержать еще обычные адгезивы, смачивакаплями добавляют раствор 122,3г нитрита натели, диспергаторы, эмульгаторы, способствуютрия в 180мл воды Размешивают в течение 30 щие прониканию вещества, консерванты, минут, затем данную реакционную смесь капляантифризы, растворители, наполнители, носитеми при температуре примерно 26°С добавляют к ли и красители, пеногасители, тормозящие испараствору 17г хлорида меди(И) и 1300мл ледяной рение средства и влияющие на значение рН и уксусной кислоты, насыщенному двуокисью севязкость средства ры По окончании выделения газа выливают на Известные пестициды, которые можно приледяную воду, выпавший сульфорхлорид отсаменять в смеси с предлагаемыми активными весывают, промывают водой, и в результате сушки ществами для приготовления вышеуказанных получают 354,Зг сложного метилового эфира 2готовых препаратов или препаратов, получаемых хлорсульфонил-4-нитробензойной кислоты, точка в баках непосредственно перед употреблением, плавления 88 - 90°С описаны, например, в Weed Research 26, 441-445 (1986г), "The Pesticide Manual", 9-е издание, The British Crop Protection Council, 1990/91 rr, Bracknell, Англия, и указанной там литературе Перед применением вышеуказанные препараты, например, смачивающиеся порошки, эмульгируемые концентраты, дисперсии и диспергируемые в воде грануляты, можно разбавлять водой известными приемами, и получаемые при этом рабочие препараты наносят на растения, части растений или на используемую в сельском хозяйстве или промышленности почву, на которой растут растения, или в которой они подрастают или которые имеются в виде посевного материала Пылевидные препараты, наносимые на почву грануляты или разбрасываемые грануляты, а также разбрызгиваемые растворы до применения обычно не разбавляют дальнейшими инертными веществами Пример 3 N-трет бутил-2-метоксикарбонил-5нитро-бензолсульфонамид К раствору 384г сложного метилового эфира 2-хлорсульфонил-4-нитро-бензойной кислоты, полученного согласно примеру 2, в 1500мл этилацетата при температуре 0°С каплями добавляют 206г трет, бутиламина Затем реакционной смеси дают нагреваться до комнатной температуры, и размешивают при этой температуре в течение часа После промывки разбавленной соляной кислотой и водой органическую фазу сушат над сульфатом магния и сгущают Остаток тщательно размешивают с простым диизопропиловым эфиром Получают 377,6г целевого сульфонамида, точка плавления 122 -124°С Пример 4 г) М-третбутил-2-диметиламинокарбонил-5-нитро-бензолсульфонамид В 115г М-трет бутил-2-метоксикарбонил-5 48134 14 13 нитробензолсульфонамиду, полученному сокарбонил-бензолсульфонамида, полученного гласно примеру 3, в 1500мл метанола вводят согласно примеру 5, при температуре 0°С распримерно 200г газового диметиламина Получентворяют в 3,5мл диметилформамида, и добавную смесь размешивают при температуре приляют 0,28г хлорангидрида пропионовой кислоты мерно 35°С в течение недели Раствор сгущают и 0,50мл триэтиламина Размешивают в течение при пониженном давлении, остаток поглощают в часа при температуре 5°С каплями, затем смесь етилацетате, и последовательно промывают поглощают в этилацетате и последовательно разбавленной соляной кислотой, насыщенным промывают разбавленной соляной кислотой и раствором бикарбоната натрия и насыщенным водой В результате сушки над сульфатом маграствором хлористого натрия После сушки над ния и сгущения органической фазы получают сульфатом магния органическую фазу сгущают 0,60г высоковязкого вещества, которое без дальПолучают 92г М-трет бутил-2-диметиламинокарнейшей очистки используют для дальнейших бонил-5-ни-тро-бензолсульфонамида, точка реакций плавления 138-141 °С Пример 9 2-диметиламинокарбонил-5-метоксикарбониламино-бензолсульфонамид Пример 5 5-амино-М-трет бутил-2-диметиламинокарбонил-бензолсульфонамид 1,48г N-трет бутил-2-диметиламинокарбонил5-метоксикарбониамино-бензол-сульфонамида, К суспензии 22,0г N-трет бутил-2-диметилаполученного согласно примеру 6, размешивают в минокарбонил-5-нитро-бензолсуль-фонамида, 25мл трифторуксусной кислоты в течение 18 чаполученного согласно примеру 4, 18,2г хлорида сов После отгонки кислоты остаток суспендиаммония, 70мл воды и 150 мл метанола добавруют в толуоле В результате повторного сгущеляют 23,6г цинка в виде порошка Полученную ния получают 1,40г указанного сульфонамида, смесь размешивают при температуре 50°С По точка плавления 75 - 77°С завершении реакции отфильтровывают твердое вещество, которое промывают этилацетатом Пример 10 2-диметиламинокарбонил-5-форЗатем фильтрат сгущают, остаток поглощают в миламино-бензолсульфонамид этилацетате и промывают водой После сушки Аналогично примеру 9 0,85г N-трет б ути л-2над сульфатом магния органическую фазу сгудиметиламино-карбонил-5-фор-миламино-бенщают, и остаток промывают простым диизопрозолсульфонамида, полученного согласно припиловым эфиром Получают 17,5г целевого сомеру 7, подвергают взаимодействию с 10мл единения, точка плавления 205 - 208°С трифторуксусной кислоты Получают 0,88г высоковязкой массы, которую без дальнейшей очиПример 6 стки используют для осуществления реакции по N-трет бутил-2-диметиламинокарбонил-5-мепримеру 13 токсикарбониламино-бен-золсульфонамид К суспензии 1,50г 5-амино-М-трет бутил-2Пример 11 2-диметиламинокарбонил-5-продиметиламинокарбонил-бензолсуль- фонамида, пиониламино-бензолсульфонамид полученного согласно примеру 5, и 1,46г бикарАналогично примеру 9 0,80г N-трет б ути л-2боната натрия в 50мл ацетонитрила при темпедиметиламино-карбонил-5-пропио-ниламиноратуре 0°С каплями добавляют 0,47г сложного бензолсульфонамида подвергают взаимодейстметилового эфира хлормуравьиной кислоты По вию с 10 мл трифтор-уксусной кислоты Полузавершении реакции реакционную смесь поглочают 0,80г высоковязкой массы, которую без щают в этилацетате, промывают 1 н соляной дальнейшей очистки используют для осуществкислотой, сушат над сульфатом магния и сгуления реакции по примеру 14 щают Получают 1,48г N-трет бутил-2-диметилаПример 12 минокарбонил-5-метоксикарбониламино-бензол^[(4,6-диметоксипиримидин-2-ил)-аминосульфонамида, точка плавления 184 - 188°С карбонил]-2-диметиламино-карбонил-5-метоксикарбониламино-бензолсульфонамид Пример 7 N-трет бутил-2-диметиламинокарбонил-5К суспензии 1,40г 2-диметиламинокарбонилформиламино-бензолсуль-фонамид 5-метоксикарбониламино-бензол-сульфонамида, полученного согласно примеру 9, и 1,28 г 4,6-диСмесь 0,34мл муравьиной кислоты и 0,70мл метокси-2-фен-оксикарбониламино-пиримидина ангидрида уксусной кислоты в течение 2 часов в 30мл ацетонитрила при температуре 0°С капнагревают при температуре 50°С, после чего лями добавляют диазабициклоундекан Темпедобавляют раствор 0,85г 5-aMHHO-N-TpeT бутил-2ратуре дают медленно повышаться до комнатдиметиламинокарбонил-бензолсульфон-амида, ной После отгонки растворителя остаток полученного согласно примеру 5, и 3,5мл димепоглощают водой и промывают простым диэтитилформамида По истечении 4 часов смесь половым эфиром Водную фазу подкисляют конглощают в этилацетате и последовательно процентрированной соляной кислотой, и затем вымывают разбавленной соляной кислотой и делившуюся сульфонил мочевину промывают насыщенным раствором бикарбоната натрия В метанолом и простым диизопропиловым эфирезультате сушки над сульфатом магния и сгуром, после чего сушат Получают 1,45г целевого щения органической фазы получают 0,88г высосоединения в виде бесцветного твердого вещековязкого вещества, которое без дальнейшей ства, точка плавления 181 - 182°С (разложение) очистки используют для дальнейших реакций Пример 8 N-трет бутил-2-диметиламинокарбонил-5пропиониламино-бензол-сульфонамид 0,85г 5-aMHHO-N-TpeT бутил-2-диметиламино Пример 13 ^[(4,6-диметоксипиримидин-2-ил)-аминокарбонил]-2-диметиламино-карбонил-5-формиламино-бензолсульфонамид 15 Аналогично примеру 12 0,88г 2-диметиламинокарбонил-5-формил-амино-бен-золсульфонамида, полученного согласно примеру 10, подвергают взаимодействию с 0,89г 4,6-диметокси-2феноксикарбониламино-пиримидина и 0,98г диазабициклоундекана в 10мл ацетонитрила Получают 0,69г кристаллической сульфонил мочевины, точка плавления 126 127°С (разложение) Пример 14 г\І-[(4,6-диметоксипиримидин-2-ил)-аминокарбонил]-2-диметиламино-карбонил-5-пропиониламино-бензолсульфонамид Аналогично примеру 12 0,80г 2-диметиламинокарбонил-5-пропиониламино-бензолсульфонамида подвергают взаимодействию с 0,74г 4,6диметокси-2-феноксикарбониламино-пиримидина и 0,82г диазабициклоундекана в 10мл ацетонитрила Получают 0,68г кристаллической сульфонил мочевины, точка плавления 135 140°С (разложение) Пример 15 г\І-[(4,6-диметоксипиримидин-2-ил)-аминокарбонил]-2-диметиламино-карбонил-5-метоксикарбониламино-бензолсульфонамид в виде натриевой соли К смеси 0,93г І\І-[(4,6-диметоксипиримидин-2ил)-аминокарбонил]-2-диметил-аминокарбонил5-метоксикарбонил-амино-бензолсульфонамида в 20мл ацето-нитрила добавляют 1,85мл 1н натриевого щелока После образования прозрачного раствора смесь сгущают при пониженном давлении Остаток размешивают с небольшим количеством простого диизопропилового эфира Получают 0,82г целевой соли, точка плавления 187 -191 °С (разложение) Пример 16 г\І-[(4,6-диметоксипиримидин-2-ил)-аминокарбонил]-2-диметиламино-карбонил-5-формиламино-бензолсульфонамид в виде натриевой соли Аналогично примеру 15 взаимодействию подвергают 0,30г І\І-[(4,6-димет-оксипиримидин-2ил)-аминокарбонил]-2-диметиламинокарбонил-5формилами-но-бензолсульфонамида, полученного согласно примеру 13, и 0,65мл 1н натрового щелока в 4мл метанола и 4мл дихлорметана Получают 0,32г вышеуказанной натриевой соли, точка плавления 205°С (разложение) Пример 17 г\І-[(4,6-диметоксипиримидин-2-ил)-аминокарбонил]-2-диметиламино-карбонил-5-пропиониламино-бензолсульфонамид в виде натриевой соли Аналогично примеру 15 взаимодействию подвергают 0,30г І\І-[(4,6-димет-оксипиримидин-2ил)-аминокарбонил]-2-диметиламино-карбонил5-пропионил-амино-бензолсульфонамида, полученного согласно примеру 14, и 0,60мл 1н натрового щелока в 4мл метанола и 4мл дихлорметана Получают 0,31г вышеуказанной натриевой соли, точка плавления 212°С (разложение) Аналогично примерам 1 2 - 1 7 получают соединения формулы (I), сведенные в таблице 1 16 48134 Таблица 1 NH ^ - ^ SO 3 NC0—N 17 Возможные составы предлагаемого гербицидного состава иллюстрируются следующими приемами Примеры а) Пылевидный препарат получают за счет того, что 10вес частей соединения примера 12 смешивают с 90вес частями талька в качестве инертного вещества, и получаемую смесь измельчают в ударной мельнице б) Легкодиспергируемый в воде, смачивающийся порошок получают за счет того, что 25вес частей соединения примера 13 смешивают с 64вес частями содержащего каолин кварца в качестве инертного вещества, Ювес частями лигнинсульфокислого калия и 1 весовой частью олеоилметил-тауринокислого натрия в качестве смачивателя и диспергатора, и получаемую смесь измельчают в стержневой мельнице в) Легкодиспергируемый в воде дисперсионный концентрат получают за счет того, что 20вес частей соединения примера 45 смешивают с 6 вес частями простого алкилфенолполигликолевого эфира (торговый продукт Triton X 207), 3 вес частями простого изотридеканолполигликолевого эфира (содержащего 8 моль этиленоксида) и 71 вес частью парафиннового минерального масла (с пределами кипения около 255 - свыше 277°С), и получаемую смесь измельчают в шаровой мельнице до величины частиц ниже 5 микрон г) Эмульгируемый концентрат получают из 15вес частей соединения примера 47, 75вес частей циклогексанона в качестве растворителя и Ювес частей оксэтилированного нонилфенола в качестве эмульгатора д) Диспергируемый в воде гранулят получают за счет того, что 75вес частей соединения примера 56 смешивают с Ювес частями лигнинсульфокислого кальция, 5вес частями лаурилсульфата натрия, 3 вес частями поливинилового спирта и 7вес частями каолина, получаемую смесь измельчают при помощи стержневой мельницы, и порошок гранулируют в псевдоожиженном слое путем впрыскивания в него воды е) Диспергируемый в воде гранулят получают также за счет того, что в коллоидной мельнице гомогенизуют и предварительно измельчают смесь 25вес частей соединения примера 57, 13, 5вес частей 2,2'-динафтилме-тан-6,6'-дисульфокислого натрия, 2вес частей олеилметилтауринкислого натрия, 1 вес части поливинилового спирта, 17вес частей карбоната кальция и 50вес частей воды Затем осуществляют помол до заданной величины частиц, и получаемую суспензию распыляют и сушат в распылительной башне, снабженной одноканальным соплом Гербицидная активность предлагаемых соединений поясняется результатами следующих опытов Опыт А Действие на сорняки в результате довсходовой обработки Семена или ризомные куски моно- и дикотильных сорняков вносят в песчаную глинистую почву в пластмассовых горшках, и затем на почву наносят покровный слой той же земли Имею 48134 18 щиеся в виде смачивающегося порошка или эмульсионного концентрата активные вещества разбавляют водой, взятой в количестве 600 800г/га Получаемые при этом водные суспензии или эмульсии наносят на поверхность покровной почвы в различных дозах, указанных в таблицах 2, 3 После обработки горшки размещают в теплице и оставляют стоять там в условиях роста сорняков Оптическую оценку повреждения растений осуществляют после всхода подопытных растений через 3 - 4 недель по сравнению с необработанными контрольными растениями Активные вещества и их процентное гербицидное действие сведены в таблицах 2, 3 Опыт Б Действие на сорняки в результате послевсходовой обработки Семена или ризомные куски моно- и дикотильных сорняков вносят в песчаную глинистую почву в пластмассовых горшках, и затем на почву наносят покровный слой той же земли Горшки размещают в теплице в условиях роста сорняков Через три недели после высева подопытные растения, находящиеся в стадии развития трех листьев, обрабатывают гербицидами Имеющиеся в качестве смачивающегося порошка или эмульсионного концентрата активные вещества разбавляют водой, взятой в количестве 600 - 800г/га Получаемые при этом рабочие препараты наносят на зеленые части растений в различных дозах, указанных в таблицах 4 - 7 Через 3 - 4 недели выращивания подопытных растений в теплице в оптимальных уловиях оптически определяют активность препаратов по сравнению с необработанными контрольными растениями Активные вещества и процентное гербицидное действие сведены в таблицах 4 - 6 Опыт В Переносимость гербицидорв культурными растениями Для осуществления данных опытов семена ряда культурных и сорных растений высеивают в песчаную глинистую почву, которую покрывают слоем той же земли Часть горшков сразу обрабатывают согласно данным по вышеприведенному пункту 1, а остальные горшки размещают в теплице до равития двух или трех настоящих листьев у рстений, а затем растения обрабатывают гербицидами, применяемыми в различных дозах, указанных в таблице 7 Через 4 - 5 недель после обработки и пребывания в теплице оптически определяют гербицидную активность и переносимость Активные вещества и процентные данные по указанным двум показателям сведены в таблице 7 В опытах А - В используют известные из упомянутого ближайшего аналога соединения I - IV формулы 19 48134 20 где радикалы имеют следующие значения осн, {XVI), осн, № соединения I II III IV Ra ОСНз ОСНз ОСНз N(CH3)2 Rb СНО СООСНз СОСНз Н Re Н Н Н Н Таблица 2 Гербицидное действие в % при довсходовой обработке Норма расхода акСоединение притивного вещества, мера № г/га 13 AV 95 75 0 80 70 40 0 0 0 80 20 5 80 20 5 80 20 5 12 I Сорняки AL 100 100 97 95 85 70 99 98 60 CY 100 90 90 85 80 70 90 60 50 AM 97 95 95 90 80 70 97 95 80 Таблица 3 Гербицидное действие в % при довсходовой обработке Норма Соединение расхода примера № акт вещества, г/га 80 20 80 20 13 IV Сорняки AV 95 75 0 0 AL 99 99 90 75 SE 100 100 50 0 РО 98 98 98 0 LO 100 99 40 0 ЕС 98 80 85 40 CY 100 80 40 0 SI 98 97 85 20 GA 98 97 75 50 СН 100 97 85 70 МА 98 97 98 40 ST 97 95 85 80 AM 97 95 98 50 Таблица 4 Гербицидное действие в % при после всход о вой обработке Соединение примера № 13 I Норма расхода активного вещества, г/га 80 20 5 80 20 5 Сорняки AV 100 90 70 80 40 30 ЕС 100 80 50 50 40 30 CY 70 60 50 30 20 10 AM 100 90 80 60 50 40 21 22 48134 Таблица 5 Соединение примера № 1 12 1 12 » Гербицидное действие в % при после всход о вой обработке Сорняки Норма расхода активного вещеAV AL SE РО LO ЕС CY GA СН AM ства, г/га 2 3 4 5 6 7 8 9 10 11 12 80 99 99 95 98 99 92 92 94 100 99 продолжение таблицы 5 2 3 4 5 6 7 8 9 10 11 12 20 87 99 87 95 100 90 90 92 98 94 5 85 92 45 92 85 55 55 82 82 70 80 40 90 50 80 95 70 70 95 100 80 20 30 80 40 70 90 60 60 80 90 70 5 20 60 20 60 80 40 40 60 60 60 Таблица 6 Гербицидное действие в % при после всход о вой обработке Норма расхода активного вещества, г/га 80 20 5 80 20 5 Соединение примера № 13 • и AV AL РО LO ЕС CY SI GA СН МА ST AM 100 90 70 40 40 20 100 90 60 60 40 30 99 90 80 60 40 20 100 90 80 30 20 10 100 80 60 40 30 20 70 60 50 20 10 0 90 90 80 90 80 70 90 80 40 30 20 10 90 90 80 60 50 40 90 80 60 80 70 60 90 90 80 60 40 20 100 90 80 80 60 50 Таблица 7 Гербицидное действие и его селективность в % при после всход о вой обработке Соединение примера № 18 III Норма расхода активного вещества, г/га 80 20 80 20 В вышеприведенных таблицах 2-7 использованы следующие условные сокращения AV = Avena fatua AL = Alopecurus myosuroides SE = Setana lutescens PO = Poa annua LO = Lohum multiflorum EC = Echinochloa crus-galh CY = Cyperus esculentus SI = Smapis alba GA = Gahum aparme CH = Chrysantemum segetum Кукуруза Хлопок AV ЕС СУ 45 40 100 90 20 10 40 30 95 70 70 60 90 65 70 30 80 70 50 MA = Matncana modora ST = Stellana media AM = Amaranthus retroflexus PH = Pharbitis purpurea Сравнение результатов опытов А - В свидетельствует о том, что предлагаемые соединения формулы (I) проявляют лучшее гербицидное действие и избирательность действия, чем известные соединения аналогичной структуры Соединения примеров 1 4 - 6 9 проявляют аналогичные свойства 23 48134 ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71 24
ДивитисяДодаткова інформація
Назва патенту англійськоюAcylated aminophenylsulfonyl ureas and their salts, intermediate phenylsulfonyls, a herbicidal agent on the basis of acylated aminophenylsulfonyl ureas and a method for combating weed vegetation
Автори англійськоюSchnabel Gerhard, Willms Lothar, BAUER Klaus, BIRINGER Hermann
Назва патенту російськоюАцилированные аминофенилсульфонилмочевины и их соли, промежуточные фенилсульфонилы, гербицидное средство на основе ацилированных аминофенилсульфонилмочевин и способ борьбы с сорной растительностью
Автори російськоюШнабель Герхард, Вилльмс Лотар, БАУЭР Клаус, БИРИНГЕР Херманн
МПК / Мітки
МПК: C07D 251/16, C07C 327/00, C07D 251/52, A01N 47/36, C07D 239/46, C07C 311/16, C07D 521/00, C07D 251/46, C07D 239/42, C07C 311/39
Мітки: проміжні, солі, ацильованих, амінофенілсульфонілсечовин, засіб, фенілсульфоніли, гербіцидний, ацильовані, бур'яновою, боротьби, основі, амінофенілсульфонілсечовини, спосіб, рослинністю
Код посилання
<a href="https://ua.patents.su/12-48134-acilovani-aminofenilsulfonilsechovini-ta-kh-soli-promizhni-fenilsulfonili-gerbicidnijj-zasib-na-osnovi-acilovanikh-aminofenilsulfonilsechovin-ta-sposib-borotbi-z-buryanovoyu-roslin.html" target="_blank" rel="follow" title="База патентів України">Ацильовані амінофенілсульфонілсечовини та їх солі, проміжні фенілсульфоніли, гербіцидний засіб на основі ацильованих амінофенілсульфонілсечовин та спосіб боротьби з бур’яновою рослинністю</a>
Попередній патент: Спосіб виготовлення скла у флоат-печі
Наступний патент: Заміщені ароматичні аміди тіокарбонової кислоти та гербіцидний засіб, що їх містить
Випадковий патент: Спосіб визначення структурних змін в акрилових матеріалах












