Фармацевтична композиція елтромбопагу оламіну (варіанти) і спосіб її виготовлення (варіанти)
Формула / Реферат
1. Фармацевтична таблетка, що містить
а) 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько 95,7 мг, та близько 127,6 мг,
де
b) близько 90 % лікарських частинок мають розмір більший за 10 мікрон, але менший за 90 мікрон;
с) таблетка містить від близько 25 % до близько 89 % за вагою одного або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза, порошкоподібна целюлоза, пептизований крохмаль, крохмаль, лактитол, манітол, сорбітол, та мальтодекстрин, та
d) таблетка має плівкове покриття.
2. Фармацевтична таблетка за п. 1, яка відрізняється тим, що:
таблетка містить від близько 25 % до близько 89 % за вагою одного або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза та манітол.
3. Спосіб виготовлення фармацевтичних таблеток, що містять 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько 95,7 мг, та близько 127,6мг, згідно з яким виконують такі стадії:
а) змішують:
3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін), де близько 90 % лікарських частинок мають розмір більший за 10 мікрон, але менший за 90 мікрон,
один або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза, порошкоподібна целюлоза, пептизований крохмаль, крохмаль, лактитол, манітол, сорбітол, та мальтодекстрин, та
інші інгредієнти,
для утворення суміші,
b) спресовують суміш у таблетки, та
с) наносять на таблетки плівкове покриття,
за умови, що:
кожна таблетка містить: 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько 95,7 мг, та близько 127,6 мг, та
кожна таблетка містить від близько 25 % до близько 89 % одного або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза, порошкоподібна целюлоза, пептизований крохмаль, крохмаль, лактитол, манітол, сорбітол, та мальтодекстрин.
4. Спосіб за п. 3, який відрізняється тим, що:
кожна таблетка містить від близько 25 % до близько 89 % за вагою одного або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза та манітол.
5. Фармацевтична таблетка, що містить:
а) 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько 95,7 мг, та близько 127,6 мг, яка відрізняється тим, що
b) таблетка містить від близько 25% до близько 89% одного або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза, порошкоподібна целюлоза, пептизований крохмаль, крохмаль, лактитол, манітол, сорбітол, та мальтодекстрин, та
d) таблетка має плівкове покриття.
6. Фармацевтична таблетка за п. 5, яка відрізняється тим, що:
таблетка містить від близько 25 % до близько 89 % за вагою одного або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза та манітол.
7. Фармацевтична таблетка, що містить:
а) 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько 95,7 мг, та близько 127,6 мг,
яка відрізняється тим, що
b) близько 90 % лікарських частинок мають розмір більший за 10 мікрон, але менший за 90 мікрон
с) таблетка має плівкове покриття.
8. Спосіб виготовлення фармацевтичних таблеток, що містять 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько 95,7 мг, та близько 127,6мг, згідно з яким виконують такі стадії:
а) змішують:
3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін), де близько 90 % лікарських частинок мають розмір більший за 10 мікрон, але менший за 90 мікрон, та розріджувачі,
для утворення суміші,
b) спресовують суміш у таблетки, та
с) наносять на таблетки плівкове покриття,
за умови, що:
кожна таблетка містить: 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс-(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько 95,7 мг, та близько 127,6 мг.
9. Спосіб лікування тромбоцитопенії людини, що цього потребує, згідно з яким цій людині вводять терапевтичну кількість фармацевтичної таблетки за п.1.
10. Спосіб лікування тромбоцитопенії людини, що цього потребує, згідно з яким цій людині вводять терапевтичну кількість фармацевтичної таблетки за п.5.
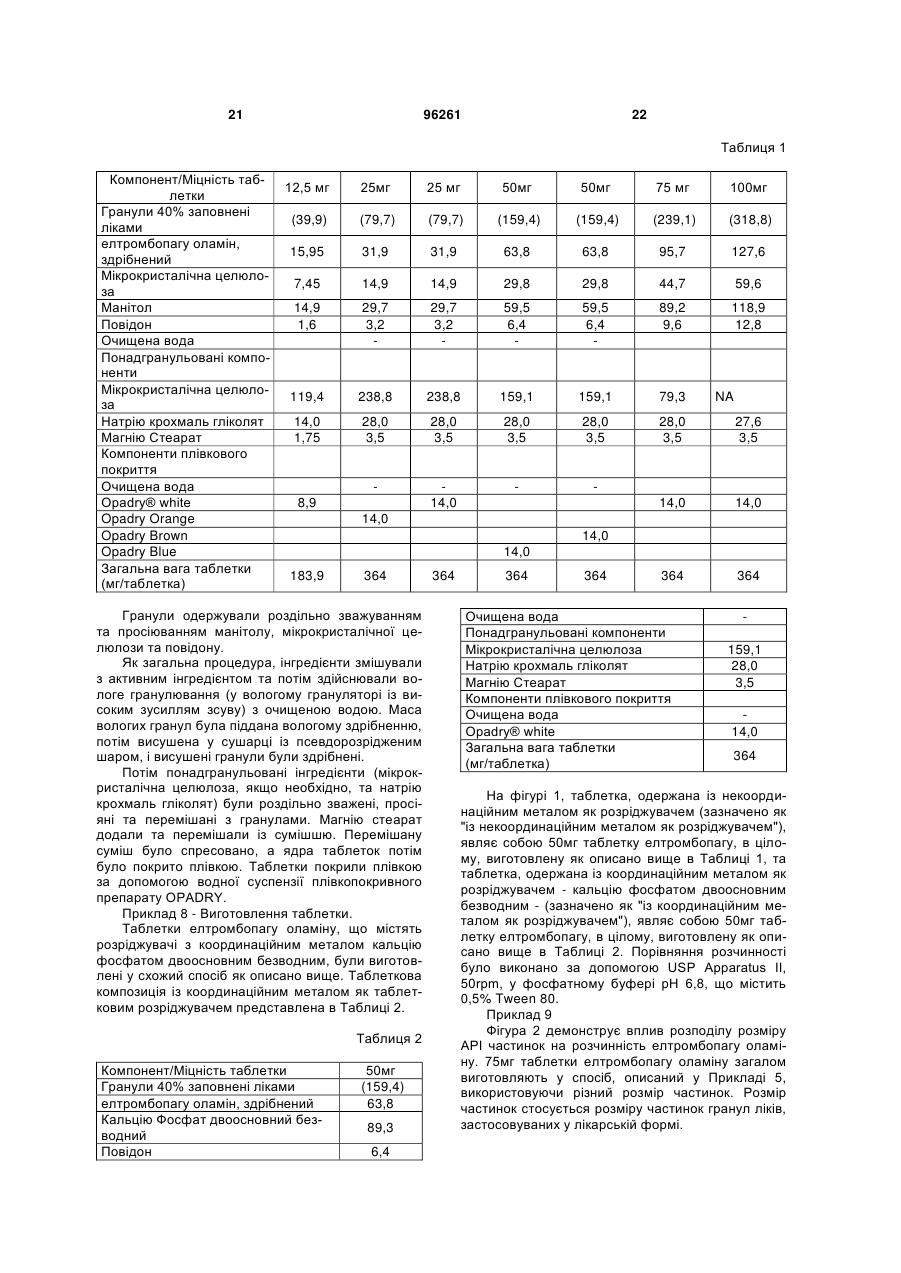
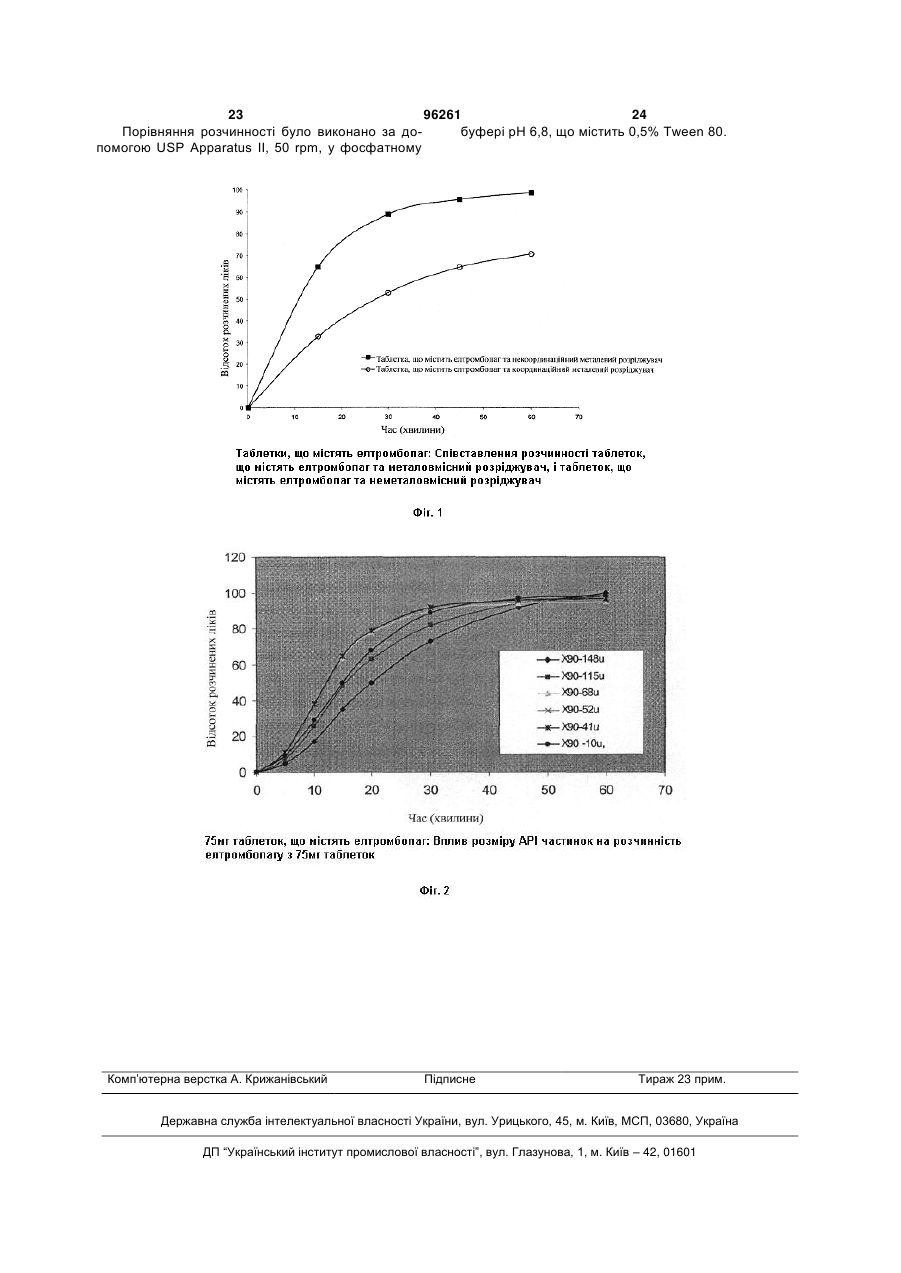
Текст
1. Фармацевтична таблетка, що містить а) 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'гідрокси-[1,1'-біфеніл]-3-карбонової кислоти біс(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько 95,7 мг, та близько 127,6 мг, де b) близько 90 % лікарських частинок мають розмір більший за 10 мікрон, але менший за 90 мікрон; с) таблетка містить від близько 25 % до близько 89 % за вагою одного або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза, порошкоподібна целюлоза, пептизований крохмаль, крохмаль, лактитол, манітол, сорбітол, та мальтодекстрин, та d) таблетка має плівкове покриття. 2. Фармацевтична таблетка за п. 1, яка відрізняється тим, що: таблетка містить від близько 25 % до близько 89 % за вагою одного або більше розріджувачів, вибраних з таких: мікрокристалічна целюлоза та манітол. 3. Спосіб виготовлення фармацевтичних таблеток, що містять 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5дигідро-3-метил-5-оксо-4H-піразол-4іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3карбонової кислоти біс-(моноетаноламін) у кількості, вибраній з: близько 15,95 мг, близько 31,9 мг, 2 (19) 1 3 96261 4 b) таблетка містить від близько 25% до близько близько 63,8 мг, близько 95,7 мг, та близько 89% одного або більше розріджувачів, вибраних з 127,6мг, згідно з яким виконують такі стадії: таких: мікрокристалічна целюлоза, порошкоподіба) змішують: на целюлоза, пептизований крохмаль, крохмаль, 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метиллактитол, манітол, сорбітол, та мальтодекстрин, та 5-оксо-4H-піразол-4-іліден]гідразино]-2'-гідроксиd) таблетка має плівкове покриття. [1,1'-біфеніл]-3-карбонової кислоти біс6. Фармацевтична таблетка за п. 5, яка відрізня(моноетаноламін), де близько 90 % лікарських ється тим, що: частинок мають розмір більший за 10 мікрон, але таблетка містить від близько 25 % до близько 89 менший за 90 мікрон, та розріджувачі, % за вагою одного або більше розріджувачів, вибдля утворення суміші, раних з таких: мікрокристалічна целюлоза та маніb) спресовують суміш у таблетки, та тол. с) наносять на таблетки плівкове покриття, 7. Фармацевтична таблетка, що містить: за умови, що: а) 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3кожна таблетка містить: 3'-[(2Z)-[1-(3,4метил-5-оксо-4H-піразол-4-іліден]гідразино]-2'диметилфеніл)-1,5-дигідро-3-метил-5-оксо-4Hгідрокси-[1,1'-біфеніл]-3-карбонової кислоти біспіразол-4-іліден]гідразино]-2'-гідрокси-[1,1'(моноетаноламін) у кількості, вибраній з: близько біфеніл]-3-карбонової кислоти біс15,95 мг, близько 31,9 мг, близько 63,8 мг, близько (моноетаноламін) у кількості, вибраній з: близько 95,7 мг, та близько 127,6 мг, 15,95 мг, близько 31,9 мг, близько 63,8 мг, близько яка відрізняється тим, що 95,7 мг, та близько 127,6 мг. b) близько 90 % лікарських частинок мають розмір 9. Спосіб лікування тромбоцитопенії людини, що більший за 10 мікрон, але менший за 90 мікрон цього потребує, згідно з яким цій людині вводять с) таблетка має плівкове покриття. терапевтичну кількість фармацевтичної таблетки 8. Спосіб виготовлення фармацевтичних таблеток, за п.1. що містять 3'-[(2Z)-[1-(3,4-диметилфеніл)-1,510. Спосіб лікування тромбоцитопенії людини, що дигідро-3-метил-5-оксо-4H-піразол-4цього потребує, згідно з яким цій людині вводять іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3терапевтичну кількість фармацевтичної таблетки карбонової кислоти біс-(моноетаноламін) у кількоза п.5. сті, вибраній з: близько 15,95 мг, близько 31,9 мг, Даний винахід стосується гранул та твердих оральних фармацевтичних дозованих форм, прийнятно таблеток, прийнятно капсул, що містять 3'[(2Z)-[1-(3,4-диметилфеніл)-1,5-дигідро-3-метил-5оксо-4Н-піразол-4-іліден]гідразино]-2'-гідрокси[1,1'-біфеніл]-3-карбонової кислоти біс(моноетаноламін), представлений наступною формулою (І) та називаний в подальшому як "елтромбопагу оламін" або Сполука В: CO2 H OH N NH O N HO NH2 2 N , (сполука В) 3'-{N'-[1-(3,4-диметилфеніл)-3-метил-5-оксо1,5-дигідропіразол-4-іліден]гідразино}-2'гідроксибіфеніл-3-карбонова кислота (далі Сполука А) є сполукою, яка розкрита та заявлена, разом з її фармацевтичне прийнятними солями, гідратами, сольватами та складними ефірами, як така, що є корисною як агоніст ТРО рецептора, особливо в підвищенні виробляння тромбоцитів та особливо в лікуванні тромбоцитопенії, в міжнародній заявці № PCT/USO 1/16863, яка має міжнародну дату подання травень 24, 2001; номер міжнародної публікації WO 01/89457 та міжнародну дату публікації листопад 29, 2001; яка має номер публікації в Сполучених Штатах US2004/0019190 А1, яка має дату публікації в Сполучених Штатах січень 29, 2004; тепер патент Сполучених Штатів № 7,160,870, виданий у січні 9, 2007, розкриття якої включено шляхом посилання. Біс-(моноетаноламін)-ова сіль цієї сполуки розкрита (розкрита як 3'-[(2Z)-[1-(3,4-диметилфеніл)1,5-дигідро-3-метил-5-оксо-4Н-піразол-4іліден]гідразино]-2'-гідрокси-[1,1'-біфеніл]-3карбонова кислота, яка також описує Сполуку А) в міжнародній заявці № PCT/US03/16255, яка має міжнародну дату подання травень 21, 2003; номер міжнародної публікації WO 03/098002 та міжнародну дату публікації грудень 4, 2003; яка має номер публікації в Сполучених Штатах US2006/0178518 А1, яка має дату публікації в Сполучених Штатах серпень 10, 2006; розкриття якої включено шляхом посилання. Сполука А розкрита для лікування дегенеративних захворювань/пошкоджень в міжнародній заявці № PCT/US04/013468, яка має міжнародну дату подання квітень 29, 2004; номер міжнародної публікації WO 04/096154 та міжнародну дату публікації листопад 11, 2004; яка має номер публікації в Сполучених Штатах US2007/0105824 А1, яка має 5 96261 6 дату публікації в Сполучених Штатах травень 10, цевтичних дозованих форм, що містять елтромбо2007; розкриття якої включено шляхом посилання. пагу оламін. Композиції, що можуть містити Сполуку А Інший аспект цього винаходу стосується грата/або Сполуку В розкриті в міжнародній заявці № нул та твердих оральних фармацевтичних дозоPCT/USO 1/16863, міжнародній заявці № ваних форм, прийнятно таблеток, прийнятно капPCT/US03/16255 та міжнародній заявці № сул, що містять елтромбопагу оламін, які PCT/US04/013468. виготовлені із розріджувачами, які, по суті, є вільТверді оральні фармацевтичні дозовані форними від відновлювальних цукрів, який, як викорими є широко відомими та корисними формами стано тут та у формулі, включає розріджувачі, які є препаратів для введення фармацевтичне активвільними від відновлювальних цукрів та які є, по них сполук. Варіанти таких форм відомі та вклюсуті, вільними від координаційних металів, який, як чають таблетки, капсули, пелеги, коржики та повикористано тут та у формулі, включає розріджурошки. вачі, які є вільними від координаційних металів. Однак виготовлення прийнятних твердих ораТакі гранули та тверді оральні фармацевтичні дольних фармацевтичних дозованих форм у промизовані форми демонструють поліпшені властивоссловому масштабі не завжди просте. Лікарська ті. Такі поліпшені властивості допомогають гаранформа та спосіб виробництва мають бути такими, тувати надійність та ефективність лікування. щоб забезпечити цілу тверду дозовану форму, яка Інший аспект цього винаходу стосується покзберігає свою цілісність, доки не використовуєтьритих плівкою фармацевтичних таблеток, які місся. Тверда дозована форма має також володіти тять елтромбопагу оламін, де плівкове покриття прийнятними розчинністю та розкладанням для містить некоординаційні метали або лише кількість того, щоб забезпечити бажаний профіль при викокоординаційного металу, яка приблизно дорівнює ристанні. Фармацевтичне активні компоненти з або менше ніж 0,025 частин Сполуки В. Такі табнизькою розчинністю та/або такі, що можуть реалетки демонструють поліпшені властивості. Такі гувати із загально використовуваними ексципієнполіпшені властивості допомогають гарантувати тами, можуть висувати окремі вимоги до приготунадійність та ефективність лікування. вання доброякісних твердих дозованих форм, Інший аспект цього винаходу стосується граоскільки фізичні властивості ліків впливають на нул та твердих оральних фармацевтичних дозовластивості твердої дозувальної форми. Розробваних форм, що містять елтромбопагу оламін, які ник рецептури має збалансувати специфічні власвиготовляють з визначеним діапазоном розміру тивості ліків із властивостями кожного ексципієнта частинок ліків, де близько 90% розміру частинок для одержання надійної, ефективної та зручної у ліків знаходиться в діапазоні від 10 до 90 мікронів. застосуванні твердої дозувальної форми. Такі таблетки демонструють поліпшені властивосЕлтромбопагу оламін підносить розробнику ті. Такі поліпшені властивості допомогають гаранрецептури специфічні турботи при спробі рецептутувати надійність та ефективність лікування. вати цю сполуку у прийнятну тверду оральну фаІнший аспект цього винаходу стосується грармацевтичну дозовану форму, прийнятно таблетнул та твердих оральних фармацевтичних дозоку, прийнятно капсулу, з бажаним ваних форм, що містять елтромбопагу оламін, які фармакокінетичним профілем, особливо в промимістять високу частку дезінтегранта, прийнятно словому масштабі. Такі турботи включають, але не кількість, рівну або більшу ніж 4%. Такі таблетки обмежуються: тенденцію сполуки утворювати недемонструють поліпшені властивості. Такі поліпрозчинніметалеві комплекси при контакті з ексцишені властивості допомогають гарантувати надійпієнтами, які містять координаційний метал, повіність та ефективність лікування. льне розчинення сполуки з твердих дозованих Інший аспект цього винаходу стосується споформ та тенденцію сполуки проходити реакцію собу лікування тромбоцитопенії, в якому спосіб Мілларда при контакті з ексципієнтами, які містять включає введення суб'єкту, який цього потребує, відновлювальні цукри. Значне втілення цих протерапевтично ефективної кількості гранул або блем буде мати несприятливий вплив на m vivo твердої оральної фармацевтичної дозованої форвведення елтромбопагу оламіну. ми за даним винаходом. Було б бажаним забезпечити елтромбопагу Інший аспект цього винаходу стосується спооламіном в твердій оральній дозованій формі в собу агонізації ТРО рецептора, в якому спосіб промисловому масштабі з бажаним фармакокіневключає введення суб'єкту, який цього потребує, тичним профілем. терапевтично ефективної кількості гранул або Даний винахід спрямований на гранули та твердої оральної фармацевтичної дозованої фортверді оральні фармацевтичні дозовані форми, що ми за даним винаходом. містять елтромбопагу оламін, прийнятно тверда Також включені в даний винахід способи сумідозована форма є таблеткою, прийнятно тверда сного введення гранул або твердої оральної фардозована форма є капсулою, прийнятно ці тверді мацевтичної дозованої форми за даним винаходозовані форми виготовляються в промисловому дом з іншими активними інгредієнтами. масштабі. Фігура 1 демонструє співставлення розчинносДаний винахід стосується гранул та твердих ті таблеток, що містять елтромбопаг та металовміоральних фармацевтичних дозованих форм, що сний розчинник, і таблеток, що містять елтромбомістять терапевтично ефективну кількість елтромпаг та неметаловмісний розчинник. бопагу оламіну. Винахід також стосується способу Фігура 2 демонструє вплив розміру АРІ частивиготовлення гранул та твердих оральних фарманок на розчинність елтромбопагу з 75мг таблеток. 7 96261 8 Під термінами "координаційний метал" та "конаційних металів та/або відновлювальних цукрів ординаційні метали" та їх похідними, як викорисможуть бути включені у розріджувальний компотано тут, розуміють метал або металовмісний екснент без шкідливого впливу на характеристики ципієнт, прийнятно розріджувач, або таблетки. металовмісний покривний матеріал таблетки, який Термін "ефективна кількість" та його похідні утворює комплекс, такий як хелатний комплекс, в означає ту кількість ліків або активного інгредієнта, присутності елтромбопагу оламіну. Приклади таяка буде викликати біологічну або медичну відпоких металів включають: алюміній, кальцій, мідь, відь тканини, системи, тварини або людини, яку кобальт, золото, залізо, магній, марганець та цинк. шукає, наприклад, дослідник або клініцист. Окрім Під терміном "відновлювальний цукор", як витого, термін "терапевтично ефективна кількість" користано тут, розуміють цукор або цукровмісний означає будь-яку кількість, яка порівняно із відпоексципієнт, прийнятно розріджувач, який реагує з відним суб'єктом, який не одержував такої кількоселтромбопагу оламіном з утворенням продукту ті, призводить до поліпшеного лікування, заживреакції Мілларда при змішуванні разом. Приклади лення, попередження або покращення перебігу таких відновлювальних цукрів включають: лактозу, хвороби, розладу або бічного ефекту, або зниженмальтозу, глюкозу, арабінозу та фруктозу. ня ступеня прогресування хвороби або розладу. Термін "реакція Мілларда" є добре відомим в Термін також включає в межах його границь кільгалузі та використаний тут стосовно її стандартнокості, ефективні, щоб посилити нормальну фізіолого значення. В цілому, термін "реакція Мілларда", гічну функцію. як використано тут, означає реакцію відновлюваЯк використано тут, термін "лікарська форма" льного цукру, як визначено тут, у лікарській формі, та його похідні, якщо не зазначено інше, стосуєтьприйнятно гранулах або твердих дозованих форся гранул та/або твердих оральних фармацевтичмах, з елтромбопагу оламіном, яка продукує пігних дозованих форм за винаходом, які містять мент або пігменти, прийнятно коричневий пігмент. елтромбопагу оламін. Пігменти згадані тут як продукти реакції Мілларда. Під терміном "сумісне введення" та його похіОдержання таких продуктів реакції Мілларда є дними, як використано тут, розуміють або спільне ознакою хімічної нестабільності. введення, або будь-який спосіб роздільного посліЯк використано тут, термін "поліпшені властидовного введення гранул та/або твердої оральної вості" та його похідні передбачає декілька переваг фармацевтичної дозованої форми за даним винащодо фармакокінетичного профілю m vivo вивільходом та додаткового активного інгредієнта або нення Сполуки В із лікарської форми, прийнятно інгредієнтів, відомих для лікування тромбоцитопегранул або твердої оральної фармацевтичної донії, включаючи тромбоцитопенію, викликану хіміозованої форми, яка використовує аспект даного терапією, та трансплантації кісткового мозку та винаходу, коли порівнювати із лікарською форінших станів із зниженим виробленням тромбоцимою, яка не використовує аспект даного винаходу, тів. Термін додатковий активний інгредієнт або прийнятно лікарська форма виробляється в проінгредієнти, як використано тут, включає будь-яку мисловому масштабі, та буде різнитися в залежсполуку або терапевтичний агент, відомий для або ності від окремого аспекту винаходу, що викорисякий демонструє корисні властивості, коли ввотовується. Приклади поліпшених властивостей диться із ТРО або ТРО мітетиками. Переважно, включають: підвищену оральну біодоступність, якщо введення не спільне, сполуки вводять в обзнижене утворення нерозчинних металевих коммеженій часом близькості одна від одної. Окрім плексів, поліпшену хімічну стабільність, стійкий того, не має значення чи вводять сполуки у тій фармакокінегичний профіль та стійкий ступінь росамій дозованій формі, наприклад одна сполука зчинення. може бути введена зовнішньо, а інша сполука моЯк використано тут, термін "ліки" або "активже бути введена орально. ний інгредієнт" та його похідні означає Сполуку В Приклади додаткового активного інгредієнта або елтромбопагу оламін. або інгредієнтів для використання в комбінації із Під терміном "промисловий масштаб" та його зараз винайденими лікарськими формами вклюпохідними, як використано тут, розуміють, виготочають, але не обмежуються: хіміозахисні або мієвлення партії масштабом більше ніж приблизно лозахисні агенти, такі як G-CSF, ВВІ 0010 (demons 20кг грануляційної суміші, прийнятно більше ніж et al., Breast Cancer Res. Treatment, 1999, 57, 127), 50кг, прийнятно більше ніж 75кг або партії розміаміфостин (Етіол) (Fetscher et al., Current Opinion ром, придатним для одержання принаймні прибin Hemat, 2000, 7, 255-60), SCF, IL-11, MCP-4, IL-1лизно 50,000 таблеток, прийнятно принаймні beta, AcSDKP (Gaudron et al. Stem Cells, 1999, 17, 75,000 таблеток, прийнятно принаймні 100,000 100-6), TNF-a, TGF-b, MIP-la (Egger et al. Bone таблеток. Marrow TranspL 1998, 22 (Suppl. 2), 34-35), та інші При зазначенні, що розріджувачі, при викорисмолекули, ідентифіковані як такі, що мають антиатанні тут та у формулі винаходу, є, по суті, вільнипоптичні, підвищують виживаність або проліферами від координаційних металів та/або що є, по суті, тивні властивості. вільними від відновлювальних цукрів, мається на Термін "гранули" та його похідні, як використаувазі, що незначні кількості, наприклад: но тут, стосується рецептованих частинок, що місприблизно 5% або менше, розріджувального тять елтромбопагу оламін, розріджувачі, які є, по компонента можуть містити координаційний метал суті, вільними від координаційних металів та/або або метали та/або відновлювальний цукор або які є, по суті, вільними від відновлювальних цукрів, відновлювальні цукри. В цьому аспекті винаходу, та прийнятно також зв'язуючі та/або змащувачі припускається, що дуже незначні кількості коордита/або дезінтегранти, таких, що частинки є прида 9 96261 10 тними для використання в твердих оральних фарГранули та тверді оральні фармацевтичні домацевтичних дозованих формах, що виготовлязовані форми за даним винаходом типово містять ються. Також є можливим вводити гранули безповід приблизно 25% до приблизно 89% одного або середньо суб'єкту, який їх потребує, як більше розріджувачів. медикамент. Однак, очікується, що гранули найОдин аспект даного винаходу включає гранубільш відповідно використовувати у виготовленні ли, де гранули виготовляють, використовуючи ротвердих оральних фармацевтичних дозованих зріджувач або розріджувачі, які є, по суті, вільними форм, як зазначено вище. від координаційних металів та/або які є, по суті, Термін "тверда оральна фармацевтична дозовільними від відновлювальних цукрів. вана форма" або "тверда дозована форма" та його Один аспект даного винаходу включає тверді похідні, як використано тут, стосується кінцевого оральні фармацевтичні дозовані форми, де тверді фармацевтичного препарату, що містить елтромдозовані форми виготовляють, використовуючи бопагу оламін, такого як таблетки, капсули, пелерозріджувач або розріджувачі, які є, по суті, вільти, коржики та порошки (включаючи покриті варіаними від координаційних металів та/або які є, по нти будь-яких таких препаратів), який є придатним суті, вільними від відновлювальних цукрів. для in vivo введення. Один аспект даного винаходу включає фарПрийнятно, гранули та тверді оральні фармамацевтичні таблетки, де таблетки виготовляють, цевтичні дозовані форми за даним винаходом місвикористовуючи розріджувач або розріджувачі, які тять елтромбопагу оламін, розріджувач (також є, по суті, вільними від координаційних металів відомий як наповнювач або агент для збільшення та/або які є, по суті, вільними від відновлювальних об'єму), та прийнятно також зв'язувач та/або змацукрів. щувач та/або дезінтегрант. Обізнані в галузі зроОдин аспект даного винаходу включає фарзуміють, що заданий матеріал може забезпечити мацевтичні капсули, де капсули виготовляють, одну або більше функцій в таблетованій лікарській використовуючи розріджувач або розріджувачі, які формі, хоча матеріал зазвичай включають для є, по суті, вільними від координаційних металів первинної функції. Процентний вміст розріджувата/або які є, по суті, вільними від відновлювальних ча, зв'язуючого, змащувача та дезінтегранта, нацукрів. даний тут та у формулі винаходу, представлений Зв'язуючі надають порошкоподібному матеріза вагою таблетки. алу властивостей до зчеплення. Приклади зв'язуРозріджувачі забезпечують об'єм, наприклад, ючих, придатних для використання в даному винащоб зробити таблетку зручного для обробки розході включають: міру. Розріджувачі можуть також сприяти обробці, крохмаль (наприклад, пасту, пептизований наприклад, забезпечуючи поліпшені фізичні власкрохмаль, рослинний клей), желатину, цукри (нативості, такі як плинність, стисливість та твердість приклад, сахарозу, глюкозу, декстрозу, мелясу, таблетки. Через відносно високі процентний вміст лактозу, декстрин, ксилітол, сорбітол), поліметакрозріджувача та ступінь прямого контакту між розрилати, природні та синтетичні смоли (наприклад, ріджувачем та активною сполукою в типовому фааравійська камедь, альгінові кислоти та їх солі такі рмацевтичному складі, взаємодія розріджувача з як натрію альгінат, трагакантову камедь, екстракт активною сполукою є окремою турботою розробІрландського моху, панварову смолу, камедь гатті, ника рецептур. Приклади розріджувачів, прийнятгуарову смолу, зеїн), похідні целюлози [такі як карних за загального використання включають: водобоксиметил целюлоза та її солі, метил целюлоза розчинні наповнювачі та водонерозчинні (МС), гідроксипропіл метил целюлоза (НРМС), наповнювачі, такі як кальцію фосфат (наприклад, гідроксипропіл целюлоза (НРС), гідроксіетил цеди- та триосновний, гідратований або безводний), люлоза (НЕС) та етил целюлоза (ЕС)], полівінілпікальцію сульфат, кальцію карбонат, магнію карборолідон, вігум, мординовий арабогалакган, поліенат, каолін, висушену розпиленням або безводну тиленгліколь, воски, воду, спирт, магнію алюмінію лактозу, целюлозу (наприклад, мікрокристалічну силікат та бентоніти. В одному з втілень даного целюлозу, порошкоподібну целюлозу), пептизовавинаходу, зв'язувач містить полівінілпіролідон ний крохмаль, крохмаль, лактитол, манітол, сорбі(PVP). тол, мальтодекстрин, цукрову пудру, стискуваний Гранули та тверді оральні фармацевтичні доцукор, сахарозу, декстрозу та іноситол. Розріджузовані форми за даним винаходом типово містять вачі, що не містять координаційних металів та роаж до приблизно 8% зв'язуючого. Лікарські форми зріджувачі, що являють собою невідновлювальні прийнятно містять аж до приблизно 5%, прийнятно цукри, є прийнятними для таблеток за даним виаж до приблизно 2% зв'язуючого. находом. Прийнятні розріджувачі для використанЗмащувачі широко використовують для покня в цьому винаході включають мікрокристалічну ращення обробки, наприклад, щоб попередити целюлозу, порошкоподібну целюлозу, пептизоваприлипання матеріалу лікарської форми до техноний крохмаль, крохмаль, лактитол, манітол, сорбілогічного обладнання, знизити тертя між частинтол та мальтодекстрин. Неприйнятні розріджувачі ками, поліпшити інтенсивність потоку складу включають кальцію фосфат (наприклад, ди- та та/або сприяти викиду лікарських форм з технолотриосновний, гідратований або безводний), кальгічного обладнання. Приклади змащувачів, прийнцію сульфат, кальцію карбонат, магнію карбонат, ятних для використання в даному винаході вклюкаолін та висушену розпиленням або безводну чають: тальк, стеарати (наприклад, магнію лактозу. В одному з втілень даного винаходу, розстеарат, кальцію стеарат, цинк стеарат, пальміторіджувач складається з одного або обох манітолу стеарат), стеаринову кислоту, гідрогенізовані роста мікрокристалічної целюлози. линні олії, гліцерил беханат, поліетиленгліколь, 11 96261 12 етилен оксид полімери (наприклад, CARBOWAXn), ляцію, гранулювання у псевдозрідженому шарі та рідкий парафін, натрію лаурил сульфат, магнію вологе гранулювання, та види використовуваних лаурил сульфат, натрію олеат, натрію стеарил ексципієнтів будуть варіюватися відповідно. Було фумарат, DL-лейцин та кремнеземні похідні (навиявлено, що вологе гранулювання особливо приприклад, колоїдний діоксид кремнію, колоїдний датне для забезпечення високої міцності, низької кремнезем, пірогенний кремнезем та гідратований ламкості таблеток, що містять відносно високі коннатрію кремнеалюмінат). В одному з втілень даноцентрації елтромбопагу оламіну (наприклад, прибго винаходу, змащувач містить магнію стеарат. лизно 40% або більше), в масштабі, придатному Гранули та тверді оральні фармацевтичні додля промислового виробництва. Прийнятні одерзовані форми за даним винаходом типово містять жані вологим гранулюванням таблетки за винахоаж до приблизно 2% змащувача. Лікарські форми дом містять гранули, що містять елтромбопагу прийнятно містять аж до приблизно 1,5%, прийняоламін та один або більше наповнювачів, зв'язуютно аж до приблизно 1% змащувача. чих та дезінтегрантів, де гранули змішують з додаДезінтегранти використовують, щоб полегшити тковим наповнювачем, зв'язуючим, дезінтегрантом руйнування або розпад лікарської форми після та/або змащувачем для одержання спресовуваної введення. Приклади дезінтегрантів, придатних для суміші, яку пресують для формування таблеток. використання в даному винаході, включають: кроВключеними в даний винахід є фармацевтичні хмалі, целюлози, смоли, поперечносшиті полімери композиції у таблетованій формі, прийнятно вигота шипучі агенти, такі як кукурудзяний крохмаль, товлені в промисловому масштабі, що містять елкартопляний крохмаль, пептизований крохмаль, тромбопагу оламін, де таблетку одержують шлямодифікований кукурудзяний крохмаль, кроскархом вологої грануляції, використовуючи мелоза натрію, кросповідон, натрію крохмаль глірозріджувач або розріджувачі, які є, по суті, вільколят, Вігум HV, метил целюлоза, мікрокристалічними від координаційних металів та/або які є, по на целюлоза, целюлоза, модифікована целюлозна суті, вільними від відновлювальних цукрів. Також камедь (наприклад, Ac-Di-Sol R), агар, бентоніт, включеними в даний винахід є такі фармацевтичні монтморилонітний клей, природна губка, катіоноокомпозиції, які містять плівкове покриття, де плівбмінні смоли, іонообмінні смоли (наприклад, поліакове покриття містить некоординаційні метали або крин калію), альгінова кислота та альгінати, гуаролише кількість координаційного металу, яка прибва смола, м'якоть цитруса, лизно дорівнює або менше ніж 0,025 частин Спокарбоксиметилцелюлоза та її солі, такі як натрію луки В. лаурил сульфат, магнію алюмінію силікат, воднеТакож включеними в даний винахід є фармавий алюмінію силікат, натрію бікарбонат у суміші з цевтичні композиції, що містять елтромбопагу підкислювачем, таким як винна кислота або лиоламін, де таблетку одержують шляхом вологої монна кислота. В одному з втілень даного винахогрануляції, прийнятно в промисловому масштабі, ду, дезінтегрант являє собою натрію крохмаль використовуючи розріджувач або розріджувачі, які гліколят. є, по суті, вільними від координаційних металів Гранули та тверді оральні фармацевтичні дота/або які є, по суті, вільними від відновлювальних зовані форми за даним винаходом типово містять цукрів, та приблизно 90% частинок елтромбопагу кількість від 4% до приблизно 12% дезінтегранта. оламіну мають розмір частинок більше ніж 10 мікЛікарські форми прийнятно містять від приблизно рон, але менше ніж 90 мікрон. 6% до приблизно 10%, прийнятно від приблизно Також включеними в даний винахід є фарма7% до 9%, дезінтегранта. цевтичні композиції, що містять елтромбопагу Тверді оральні фармацевтичні дозовані фороламін, де таблетку одержують шляхом вологої ми, прийнятно таблетки, прийнятно капсули, за грануляції, прийнятно в промисловому масштабі, даним винаходом будуть типово виконуватися використовуючи розріджувач або розріджувачі, які розміром до 1 грама, наприклад, від приблизно є, по суті, вільними від координаційних металів 0,01 грама до приблизно 0,8 грама. Такі тверді та/або які є, по суті, вільними від відновлювальних дозовані форми типово містять від приблизно 5мг цукрів, та приблизно 90% частинок елтромбопагу до приблизно 900мг елтромбопагу оламіну на дооламіну мають розмір частинок більше ніж 10 мікзовану форму. У прийнятних втіленнях, тверді дорон, але менше ніж 90 мікрон, прийнятно більше зовані форми містять від приблизно 5 до приблизніж 20 мікрон, але менше ніж 50 мікрон. но 200мг елтромбопагу оламіну (наприклад, у Також включеними в даний винахід є фармаприблизно 100-800мг дозованій формі). Таблетоцевтичні композиції, що містять елтромбопагу вані лікарські форми за винаходом можуть мати оламін, де таблетку одержують шляхом вологої різні конфігурації, включаючи ромбовидну, у вигрануляції, прийнятно в промисловому масштабі, гляді модифікованої капсули, модифікованого використовуючи розріджувач або розріджувачі, які овалу та шестикутну, та можуть необов'язково є, по суті, вільними від координаційних металів мати нахил. та/або які є, по суті, вільними від відновлювальних Таблетки. цукрів, та приблизно 50% частинок елтромбопагу Вибір окремих видів та кількостей ексципієнтів, оламіну мають розмір частинок більше ніж 5 мікта застосовуваних методів таблетування залежить рон, але менше ніж 50 мікрон, прийнятно більше від наступних властивостей елтромбопагу оламіну ніж 5 мікрон, але менше ніж 20 мікрон. та ексципієнтів, наприклад, стисливість, сипкість, В одному з втілень даного винаходу, таблетки розмір частинок, сумісність та щільність. Таблетки за даним винаходом містять: можуть бути виготовлені за методами, відомими в (і) від приблизно 2% до приблизно 65% елтрогалузі, включаючи пряме пресування, суху гранумбопагу оламіну; 13 96261 14 (іі) від приблизно 25% до приблизно 89% розфат, карбоксиметил целюлоза та подібні); полівіріджувача; нілпіролідон; зеїн; та акрилові полімери (напри(ііі) аж до приблизно 8% зв'язуючого, прийнятклад, співполімери естеру метакрилової кислоно аж до приблизно 5%, прийнятно аж до приблити/метакрилової кислоти, такі як співполімери зно 4%; метакрилової кислоти/метилметакрилату та подіб(iv) аж до приблизно 2% змащувача, прийнятні). Полімери на основі целюлози є переважними в но аж до приблизно 1,5%, прийнятно аж до прибданому винаході, особливо етери целюлози та лизно 1%; та більш особливо НРМС та НРС. Полімери типово (v) від 4% до приблизно 12% дезінтегранта, доставляють або у водному, або в органічному прийнятно від 6% до 10%, прийнятно від 7% до розчиннику на основі розчинів або водних диспер9%. сій. Однак, полімери можуть подаватися у сухій Прийнятні одержані вологим гранулюванням формі, окремо або у порошковій суміші із іншими таблетки містять, за вагою таблетки, від приблизкомпонентами (наприклад, пластифікатором но 10% до приблизно 95% активних інтрагранул та/або барвником), яку перетворює на розчин або елтромбопагу оламіну та від приблизно 5% до дисперсію користувач шляхом змішування із водприблизно 90% зовнішніх ексципієнтів; де активні ним носієм. інтрагранули елтромбопагу оламін містять, за ваВодна композиція для плівкового покриття догою інтрагранули: датково містить воду як носій для інших компонен(і) від приблизно 2% до приблизно 88% елтротів, для полегшення їх доставки до поверхні табмбопагу оламіну; летки. Носій може необов'язково додатково (іі) від приблизно 10% до приблизно 96% розмістити один або більше водорозчинних розчинниріджувача; ків, наприклад, спирти (наприклад, метанол, ізоп(ііі) від приблизно 2% до приблизно 5% зв'язуропанол, пропанол) та кетони (наприклад, ацетон). ючого; та Кваліфікований спеціаліст може вибрати придатні (iv) необов'язково від 0% до приблизно 4% компоненти носія для забезпечення гарної взаєдезінтегранта; модії між плівкотвірним полімером та носієм, щоб та, де зовнішні ексципієнти містять, за вагою забезпечити гарні властивості плівки. В цілому, таблетки: взаємодія полімер-носій призначена, щоб привес(і) від 0% до приблизно 70% розріджувача; ти до максимального подовження ланцюга полі(іі) від приблизно 0,25% до приблизно 2%, меру для одержання плівок, що мають найбільшу прийнятно від приблизно 0,25% до приблизно міцність зчеплення та відповідні механічні власти1,25%, змащувача; та вості. Компоненти також вибирають, щоб забезпе(ііі) від 4% до приблизно 10% дезінтегранта. чити гарне відкладення плівкотвірного полімера на У вищенаведених втіленнях, розріджувач явповерхню таблетки, виходячи з того, щоб досягти ляє собою прийнятно комбінацію манітолу та мікцільної та клейкої плівки. рокристалічної целюлози, невідновлювальний цуВодна композиція для плівкового покриття кор є прийнятно манітолом, зв'язувач є прийнятно може необов'язково містити один або більше полівінілпіролідоном, змащувач є прийнятно магад'ювантів, відомих в галузі, таких як пластифіканію стеаратом, та дезінтегрант є прийнятно натрію тори, барвники, речовини для зниження клейкості, крохмаль гліколят. Прийнятно, наповнювач інтрагвторинні плівкотвірні полімери, допоміжні речовиранул є сумішшю манітолу та мікрокристалічної ни, що підвищують плинність, поверхнево-активні целюлози та зовнішній наповнювач є мікрокристаречовини (наприклад, для сприяння розтіканню), лічною целюлозою. мальтодекстрин та полідекстроза. В одному з втілень даного винаходу, таблетки Пластифікатори забезпечують плівці пластичпокривають плівковим покриттям, одержуваним з ність, що може знизити розтріскування плівки, поводної композиції для плівкового покриття. Водні ліпшити прилипання до таблетки. Прийнятні пласкомпозиції для плівкового покриття, придатні для тифікатори будуть, в цілому, мати високий ступінь використання в даному винаході, містять плівкотсумісності з плівкотвірним полімером та достатню вірний полімер, воду як носій та необов'язково незмінність, виходячи з умови, що властивості один або більше ад'ювантів, таких як відомі з техпокриттів, в цілому, стабільні. Приклади прийнятнології плівкового покриття. Коли плівкове покритних пластифікаторів включають гліцерин, пропілен тя містить координаційний метал, як використано гліколь, поліетилен гліколі (наприклад, з молекутут, кількість координаційного металу приблизно лярною вагою від 200 до 20,000, включаючи Union дорівнює або менше ніж 0,025 частин сполуки В. Carbide's PEG 400, 4000, 6000, 8000, та 20,000), Плівкотвірний полімер вибирають для утвогліцерин триацетат (також відомий під назвою рення покриттів з механічними властивостями (натриацетин), ацетильований моногліцерид, естери приклад, механічна міцність, пластичність), прийнлимонної кислоти (наприклад, триетил цитрат, ятними, щоб відповідати вимогам до робочих ацетил триетил цитрат, трибутил цитрат, ацетил характеристик, наприклад таких, що вимагаються трибутил цитрат), фталат естери (наприклад, діенаміченим середовищем застосування (напритил фталат), мінеральне масло та гідрогенізоваклад, профіль розчинення в шлунковокишкових ний глюкозний сироп. В одному з втілень даного рідинах), та/або застосуванням (наприклад, в'язвинаходу, пластифікатор вибраний з поліетилен кість розчину). Приклади прийнятних плівкотвірних гліколів, триацетину, пропілен гліколю, гліцерину полімерів включають полімери на основі целюлози та їх сумішей. (наприклад, целюлозні етери, такі як НРМС, НРС, Водна композиція для плівкового покриття МС, ЕС, НЕС, CAP, натрію етил целюлоза сульприйнятно містить один або більше барвників. На 15 96261 16 додаток до підвищення естетичної привабливості, лизно 25% до приблизно 70%, прийнятно від прибарвник забезпечує ідентифікацію продукту. Приблизно 60% до приблизно 70%, плівкотвірного йнятні барвники включають ті, що апробовані та полімеру; від приблизно 5% до приблизно 10%, сертифіковані FDA, включаючи FD&C та D&C апприйнятно від приблизно 6% до приблизно 8%, робовані фарби, лаки та пігменти, та діоксид титапластифікатора; та від приблизно 20% до приблину, за умови, що плівкове покриття містить некоозно 35% барвника, за вагою. рдинаційні метали або лише кількість Прийнятні водні композиції для плівкового покоординаційного металу, яка приблизно дорівнює криття є комерційне доступними. Водна композиабо менше ніж 0,025 частин Сполуки В. ція для плівкового покриття може бути виконана у Прийнятно, барвник містить один або більше формі розчину або дисперсії. Альтернативно, комбарвних агентів, вибраних з групи, що містить окпозиція може бути виконана у сухій формі, що мосиди червого заліза, червоні фарби та лаки, оксиже комбінуватися із компонентами носія згідно з ди жовтого заліза, жовті фарби та лаки, діоксид інструкціями поставника до покривання таблетки. титану та індиго кармін. Наприклад, барвник може Прийнятно, водні композиції для плівкового покбути вибраний для забезпечення світло бежевого риття є комерційне доступними від Colorcon, Inc. of відтінку, наприклад, що складається, по суті, з а) West Point, PA, під торгівельним найменуванням оксиду червого заліза, червоної фарби та/або черOPADRY та OPADRY II (нелімітуючі приклади воного лаку, b) оксиду жовтого заліза, жовтої фарвключають Opadry YS-1-7706-G white, Opadry би та/або жовтого лаку, та с) діоксиду титану. АльYellow 03B92357, Opadry Blue 03B90842). Ці комтернативно, барвник може бути підібраний для позиції доступні у вигляді сухих композицій для забезпечення розового відтінку (наприклад, що плівкого покриття, які можуть швидко бути розчискладається, по суті, з діоксиду титану та оксиду нені у воді перед використанням. OPADRY та червого заліза, червоної фарби та/або червоного OPADRY II склади містять плівкотвірний полімер лаку); світло-зеленого відтінку (наприклад, що на основі целюлози (наприклад, НРМС та/або складається, по суті, з оксиду жовтого заліза, жовНРС) та можуть містити полідекстрозу, мальтодектої фабри та/або жовтого лаку, індиго карміну та стрин, пластифікатор (наприклад, триацетин, полідіоксиду титану); блакитного відтінку (наприклад, етиленгліколь), полісорбат 80, барвник (наприщо складається, по суті, з діоксиду титану та індиклад, діоксид титану, одну або більше фарб або го карміну); або помаранчевого відтінку (наприлаків), та/або інші прийнятні плівкотвірні полімери клад, що складається, по суті, з діоксиду титану та (наприклад, акрилат-метакрилат співполімери). кольору сонця, що заходить, жовтого). Прийнятні OPADRY або OPADRY II склади можуть Вищенаведені барвники, що містять коордимістити пластифікатор та один або більше з мальнаційний метал, прийнятні на рівні, який приблизтодекстрину та полідекстрози (включаючи, але не но дорівнює або менше ніж 0,025 частин Сполуки обмежуючи, а) триацетин та полідекстрозу або В. мальтодекстрин, або лактозу, або b) поліетиленгВ прийнятних альтернативних втіленнях, водліколь та полідекстрозу або мальтодекстрин). на композиція для плівкового покриття для викоТаблетки також прийнятно покривають, щоб ристання в даному винаході містить: забезпечити однакове покриття без вкраплень. (і) плівкотвірний полімер на основі целюлози; Таблетки типово покривають для забезпечення та збільшення ваги сухої таблетки від приблизно 2 до (іі) пластифікатор. приблизно 5%, прийнятно від приблизно 3 до 4%. Прийнятно, такі композиції додатково містять Непокриті ядра таблеток покривають водною барвник. Такі композиції можуть необов'язково композицією для плівкового покриття методами, додатково містити один або більше додаткових добре відомими в галузі, використовуючи комерад'ювантів, таких як речовина для зниження клейційне доступне обладнання (наприклад, Thomas кості, допоміжна речовина, що підвищує плинність, Accela-Cota, Vector Hi-Coater, Compu-Lab 36). В поверхнево-активна речовина, та вторинний плівцілому, процес зазвичай залучає качання або пекотвірний полімер. рекидання таблеток у чані або суспендування табПриклади необов'язкової речовини для знилеток на повітряній подушці (у псевдозрідженому ження клейкості включають лецитин, стеаринову шарі) та періодичне або постійне (переважно поскислоту, мінеральне масло, модифікований деритійне) напилювання тонкої дисперсії розпилених ватний крохмаль, тапіока декстрин та поліетиленкрапельок композиції для покриття на таблетки, гліколь. Приклади необов'язкових вторинних плівзволоження, розтікання та зрощення крапель із котвірних полімерів включають натрію альгінат, поверхнею таблеток для утворення липкого та пропілен гліколь альгінат та полівінілпіролідон. цільного плівкового покриття. Таблетки типово Приклади необов'язкових поверхнево-активних нагрівають до приблизно 40-50°C, прийнятно приречовин включають діокгил натрій сульфосукцинат близно 45-50°C, наприклад, повітрям, яке має тета полісорбат 80. Приклади необов'язкових допомпературу аж до приблизно 75°C, прийнятно приміжних речовин, що підвищують плинність, вклюблизно 65-70°C. чають тальк, пірогенний кремнезем, бентоніт, гідСпосіб виготовлення таблетки. рогенізовані рослинні олії, стеарини та воски. Вологогранульовані фармацевтичні таблетки Водна композиція для плівкового покриття буза винаходом можуть бути виготовлені способом, де типово містити від приблизно 5% до приблизно що включає кроки: 25%, прийнятно від приблизно 5% до приблизно І) виготовлення гранул, яке включає кроки: 20%, сухих речовин покриття в носії. У прийнятних а) змішування разом сухих матеріалів, що місвтіленнях, сухі речовини типово містять від прибтять елтромбопагу оламін, розріджувач, зв'язуюче 17 96261 18 та необов'язково дезінтегрант протягом часу, досПотім проводять вологе здрібнювання вологих татнього для гомогенізації матеріалів; гранул методами, такими як відомі в галузі для b) додавання гранулювальної рідини до суміші одержання, в цілому, однакової за розміром волосухих матеріалів, переважно в ході змішування; гої маси (таке, що гранули сушаться порівняно c) змішування гранулювальної рідини із сумірівномірно). Прийнятні технології вологого гранушшю сухих матеріалів протягом часу, достатнього лювання можуть задіювати просіювання (напридля, в цілому, рівномірного зволоження сухих маклад, ручне просіювання), подрібнювальні млини теріалів, щоб сформувати вологі гранули; (такі як Co-mil, включаючи але не обмежуючи, d) вологе здрібнювання вологих гранул; 0,375" сито) або екструдери. e) висушування волого-здрібнених гранул для Вологогранульовані гранули висушують метоутворення сухих гранул; та дами, такими як відомі в галузі за забезпечення, в f) сухе здрібнювання сухих гранул для утвоцілому, рівномірного висушування, для зниження рення гранул бажаного розміру; залишкової кількості гранулювальної рідини (переII) одержання таблетки, яке включає кроки: важно від приблизно 0,5% до приблизно 1,0%). a) змішування гранул, одержаних на кроці І) f), Сушарки із псевдозрідженим шаром є прийнятним із зовнішніми ексципієнтами, які включають наповдля висушування обладнанням. нювач, змащувач та дезінтегрант, протягом часу, Потім проводять сухе здрібнювання висушедостатнього для гомогенізації гранул та зовнішніх них гранул, використовуючи відомі методи для ексципієнтів; та одержання, в цілому, однакових за розміром граb) пресування суміші, що містить гранули та нул (унімодальний розподіл), прийнятно, що мазовнішні ексципієнти для утворення таблетки. ють значення діаметру частинок від менше ніж 240 Прийнятно, таблетки додатково покривають мікронів (виявлено, щоб забезпечити поліпшену плівкою, переважно покривають водною плівкою. однорідність вмісту). Прийнятно для волого грануВ процесі виготовлення волого-гранульованих лювання обладнання включає Co-mils, включаючи, гранул сухі матеріали можуть бути змішані за доале не обмежуючи, таке, що має 0,094" сито. помогою прийнятного обладнання, такого як відоПрийнятно гранули та сухі матеріали спресоме в галузі (наприклад, Niro-Fielder вуваної суміші є, в цілому, унімодальними в розBlender/Granulator, Bear Varimixer, Key High Shear поділі за розміром, для того, щоб полегшити утвоMixer/Granulator), протягом часу, достатнього для рення гомогенної суміші та стримувати можливе гомогенізації матеріалів, наприклад, протягом розшарування суміші після переметування. За приблизно 3 хвилин. необхідності, сухі матеріали можуть бути попередГранулювальну рідину потім додають до сухої ньо просіяні для забезпечення бажаного розподілу суміші, переважно в ході змішування. Гранулювачастинок за розміром. Просіювання змащувача льна рідина є прийнятно водою, хоча може альтеможе бути особливо корисним для деагломерації рнативно включати воду у суміші з одним або бізмащувача. льше зв'язуючими, такими як PVP та НРМС, В процесі одержання спресовуваної суміші прийнятно використовують від приблизно 10 гранули, наповнювач та дезінтегрант змішують об./ваг.% до приблизно 30 об./ваг.% гранулювальпротягом прийнятного періоду часу, приблизно 5ної рідини, виходячи з загальної вологості грану15 хвилин. Потім додають змащувач та змішують ляційної суміші. Гранулювальна рідина та сухі мапротягом прийнятного періоду часу, приблизно 1-4 теріали можуть бути змішані за допомогою хвилини. Суміш потім спресовують у таблетки, прийнятного обладнання, такого як відоме в галузі використовуючи преси, такі як відомі в галузі (на(наприклад, Niro-Fielder Blender/Granulator, Bear приклад, роторний таблетувальний прес). Varimixer, Key High Shear Mixer/Granulator), протяБуло виявлено, що вище наведені рівні гранугом загального часу, достатнього для, в цілому, лювальної рідини, час гранулювання та ексципієнрівномірного зволоження сухого матеріалу, щоб ти забезпечують поліпшену обробку. сформувати вологі гранули, прийнятно протягом Капсули. від приблизно 3 до приблизно 15 хвилин. Типово Вибір окремих типів та кількостей ексципієнтів, рідину додають до сухого матеріалу при змішуа також застосовуваних методів капсулювання ванні протягом від приблизно 1 до приблизно 15 залежить від наступних властивостей елтромбопахвилин, потім весь об'єм змішують протягом додагу оламіну та ексципієнтів, наприклад, стисливість, ткового часу (час грануляції після гранулювання із сипкість, розмір частинок, сумісність, та щільність. доданою рідиною) від приблизно 0,5 хвилин до Капсули можуть бути виготовлені за методами, приблизно 6 хвилин. відомими в галузі, прийнятно наповненням станВ прийнятному втіленні, застосовують від придартної двокомпонентної желатинової капсули близно 10 об./ваг.% до приблизно 30об./ваг.% граелтромбопагу оламіном, змішаним з ексципієнтанулювальної рідини і час грануляції після грануми, прийнятно наповненням стандартної двокомлювання із доданою рідиною від приблизно 6 понентної желатинової капсули гранулами, одерхвилин або менше. Прийнятно, застосовують прижаними згідно з цим винаходом, прийнятно в близно 24 об./ваг.% гранулювальної рідини і час масштабі, придатному для промислового виробгрануляції після гранулювання із доданою рідиною ництва. Прийнятні капсули за винаходом містять менше ніж 3 хвилин, наприклад, приблизно 2,5 гранули, що містять елтромбопагу оламін та один хвилини. Прийнятно, застосовують приблизно 16 або більше наповнювачів, зв'язуючих та дезінтегоб./ваг.% гранулювальної рідини і час грануляції рантів, де гранули змішують з додатковим наповпісля гранулювання із доданою рідиною більше нювачем, зв'язуючим, дезінтегрантом та/або зманіж 2,5 хвилини, наприклад, приблизно 4 хвилини. 19 96261 20 щувачем для утворення гранульованої суміші, Спосіб за цим винаходом індукування ТРО якою наповнюють капсули. агоністичної активності у людей включає введення Включеними в даний винахід є фармацевтичні суб'єкту, який потребує такої активності, терапевкомпозиції у формі капсули, прийнятно виготовлені тично ефективної кількості твердої оральної фарв промисловому масштабі, що містять елтромбомацевтичної дозованої форми за даним винахопагу оламін, де капсулу виготовляють, використодом. вуючи розріджувач або розріджувачі, які є, по суті, Винахід також передбачає використання елтвільними від координаційних металів та/або які є, ромбопагу оламіну у виробництві твердої оральної по суті, вільними від відновлювальних цукрів. фармацевтичної дозованої форми за даним винаТакож включеними в даний винахід є фармаходом. цевтичні композиції, що містять елтромбопагу Винахід також передбачає використання елтоламін, де капсулу виготовляють, прийнятно в ромбопагу оламіну у виробництві твердої оральної промисловому масштабі, використовуючи розріфармацевтичної дозованої форми за даним винаджувач або розріджувачі, які є, по суті, вільними ходом для застосування в підвищенні виробляння від координаційних металів та/або які є, по суті, тромбоцитів. вільними від відновлювальних цукрів, та приблизВинахід також передбачає використання елтно 90% частинок елтромбопагу оламіну мають ромбопагу оламіну у виробництві твердої оральної розмір частинок більше ніж 10 мікрон, але менше фармацевтичної дозованої форми за даним винаніж 90 мікрон. ходом для застосування в лікуванні тромбоцитоТакож включеними в даний винахід є фармапенії. цевтичні композиції, що містять елтромбопагу Винахід також передбачає тверду оральну оламін, де капсулу виготовляють, прийнятно в фармацевтичну дозовану форму для застосування промисловому масштабі, використовуючи розріяк ТРО міметика, яка містить елтромбопагу оламін джувач або розріджувачі, які є, по суті, вільними та фармацевтичне прийнятний носій за даним від координаційних металів та/або які є, по суті, винаходом. вільними від відновлювальних цукрів, та приблизВинахід також передбачає тверду оральну но 90% частинок елтромбопагу оламіну мають фармацевтичну дозовану форму для застосування розмір частинок більше ніж 10 мікрон, але менше в лікуванні тромбоцитопенії, яка містить елтромніж 90 мікрон, прийнятно більше ніж 20 мікрон, але бопагу оламін та фармацевтичне прийнятний номенше ніж 50 мікрон. сій за даним винаходом. Також включеними в даний винахід є фармаВинахід також передбачає тверду оральну цевтичні композиції, що містять елтромбопагу фармацевтичну дозовану форму для застосування оламін, де капсулу виготовляють, прийнятно в в підвищенні виробляння тромбоцитів, яка містить промисловому масштабі, використовуючи розріелтромбопагу оламін та фармацевтичне прийнятджувач або розріджувачі, які є, по суті, вільними ний носій за даним винаходом. від координаційних металів та/або які є, по суті, Винахід також передбачає спосіб виготовленвільними від відновлювальних цукрів, та приблизня твердих оральних фармацевтичних дозованих но 50% частинок елтромбопагу оламіну мають форм, що містять розріджувач або розріджувачі, розмір частинок більше ніж 5 мікрон, але менше які є, по суті, вільними від координаційних металів ніж 50 мікрон, прийнятно більше ніж 5 мікрон, але та/або які є, по суті, вільними від відновлювальних менше ніж 20 мікрон. цукрів та терапевтично ефективну кількість елтроВинайдені гранули та тверді оральні фармамбопагу оламіну, в якому спосіб включає об'єдцевтичні дозовані форми можуть вводитися в тенання елтромбопагу оламіну з розріджувачем або рапевтично ефективних кількостях для лікування розріджувачами. або попередження хворобливих станів, наприклад, Не очікуються неприпустимі токсикологічні як описано у вищенаведених Міжнародних заявках ефекти, коли сполуку за винаходом вводять у від№ PCT/US01/16863, № PCT/US03/16255 та № повідності до даного винаходу. PCT/US04/013468, розкриття яких включено сюди Без подальшого уточнення, припускається, що шляхом посилання. Обізнаному в галузі буде зрообізнаний в галузі фахівець може, використовуючи зуміло, що оптимальна кількість та періодичність попередній опис, використати даний винахід в йоіндивідуальних дозувань лікувальних форм елтго максимально повному обсязі. Наступні Прикларомбопагу оламіну за винаходом будуть визначади, відповідно, мають трактуватися лише як ілюсттись природою та об'ємом стану, який лікують, та ративні, а не обмеження обсягу даного винаходу. окремим пацієнтом, якого лікують, і що такі оптиВсі ексципієнти, використані тут, є стандартмуми можуть бути визначені стандартними метоними фармацевтичними якісними ексципієнтами, дами. Фахівцю в галузі також буде зрозуміло, що доступними у численних виробників, добре знаниоптимальний курс лікування, тобто кількість доз ми для цього в галузі. елтромбопагу оламіну, що дають на день протягом Приклади. визначеної кількості днів, може бути з'ясована таПриклади від 1 до 7 - Виготовлення таблеток. ким фахівцем, використовуючи звичайні тести з Таблетки, одержані вологою грануляцією, що визначення курсу лікування. містять елтромбопагу оламін та інгредієнти, представлені у Таблиці 1. 21 96261 22 Таблиця 1 Компонент/Міцність таблетки Гранули 40% заповнені ліками елтромбопагу оламін, здрібнений Мікрокристалічна целюлоза Манітол Повідон Очищена вода Понадгранульовані компоненти Мікрокристалічна целюлоза Натрію крохмаль гліколят Магнію Стеарат Компоненти плівкового покриття Очищена вода Opadry® white Opadry Orange Opadry Brown Opadry Blue Загальна вага таблетки (мг/таблетка) 12,5 мг 25мг 25 мг 50мг 50мг 75 мг 100мг (39,9) (79,7) (79,7) (159,4) (159,4) (239,1) (318,8) 15,95 31,9 31,9 63,8 63,8 95,7 127,6 7,45 14,9 14,9 29,8 29,8 44,7 59,6 14,9 1,6 29,7 3,2 29,7 3,2 59,5 6,4 59,5 6,4 89,2 9,6 118,9 12,8 119,4 238,8 238,8 159,1 159,1 79,3 14,0 1,75 28,0 3,5 28,0 3,5 28,0 3,5 28,0 3,5 28,0 3,5 27,6 3,5 14,0 14,0 14,0 364 364 8,9 NA 14,0 14,0 14,0 183,9 364 Гранули одержували роздільно зважуванням та просіюванням манітолу, мікрокристалічної целюлози та повідону. Як загальна процедура, інгредієнти змішували з активним інгредієнтом та потім здійснювали вологе гранулювання (у вологому грануляторі із високим зусиллям зсуву) з очищеною водою. Маса вологих гранул була піддана вологому здрібненню, потім висушена у сушарці із псевдорозрідженим шаром, і висушені гранули були здрібнені. Потім понадгранульовані інгредієнти (мікрокристалічна целюлоза, якщо необхідно, та натрію крохмаль гліколят) були роздільно зважені, просіяні та перемішані з гранулами. Магнію стеарат додали та перемішали із сумішшю. Перемішану суміш було спресовано, а ядра таблеток потім було покрито плівкою. Таблетки покрили плівкою за допомогою водної суспензії плівкопокривного препарату OPADRY. Приклад 8 - Виготовлення таблетки. Таблетки елтромбопагу оламіну, що містять розріджувачі з координаційним металом кальцію фосфатом двоосновним безводним, були виготовлені у схожий спосіб як описано вище. Таблеткова композиція із координаційним металом як таблетковим розріджувачем представлена в Таблиці 2. Таблиця 2 Компонент/Міцність таблетки Гранули 40% заповнені ліками елтромбопагу оламін, здрібнений Кальцію Фосфат двоосновний безводний Повідон 50мг (159,4) 63,8 89,3 6,4 364 364 364 Очищена вода Понадгранульовані компоненти Мікрокристалічна целюлоза Натрію крохмаль гліколят Магнію Стеарат Компоненти плівкового покриття Очищена вода Opadry® white Загальна вага таблетки (мг/таблетка) 159,1 28,0 3,5 14,0 364 На фігурі 1, таблетка, одержана із некоординаційним металом як розріджувачем (зазначено як "із некоординаційним металом як розріджувачем"), являє собою 50мг таблетку елтромбопагу, в цілому, виготовлену як описано вище в Таблиці 1, та таблетка, одержана із координаційним металом як розріджувачем - кальцію фосфатом двоосновним безводним - (зазначено як "із координаційним металом як розріджувачем"), являє собою 50мг таблетку елтромбопагу, в цілому, виготовлену як описано вище в Таблиці 2. Порівняння розчинності було виконано за допомогою USP Apparatus II, 50rpm, у фосфатному буфері рН 6,8, що містить 0,5% Tween 80. Приклад 9 Фігура 2 демонструє вплив розподілу розміру АРІ частинок на розчинність елтромбопагу оламіну. 75мг таблетки елтромбопагу оламіну загалом виготовляють у спосіб, описаний у Прикладі 5, використовуючи різний розмір частинок. Розмір частинок стосується розміру частинок гранул ліків, застосовуваних у лікарській формі. 23 96261 24 Порівняння розчинності було виконано за добуфері рН 6,8, що містить 0,5% Tween 80. помогою USP Apparatus II, 50 rpm, у фосфатному Комп’ютерна верстка А. Крижанівський Підписне Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical compositions containing eltrombopag olamine and processes for the preparation thereof
Автори англійськоюFransis X. Muller, Shivakumar G. Kapsi
Назва патенту російськоюФармацевтическая композиция элтромбопага оламина (варианты) и способ ее изготовления (варианты)
Автори російськоюФренсис Кс. Мюллер, Шивакумар Г. Капси
МПК / Мітки
МПК: A61P 7/06, A61K 31/4152, A61P 7/02
Мітки: варіанти, виготовлення, оламіну, композиція, елтромбопагу, фармацевтична, спосіб
Код посилання
<a href="https://ua.patents.su/12-96261-farmacevtichna-kompoziciya-eltrombopagu-olaminu-varianti-i-sposib-vigotovlennya-varianti.html" target="_blank" rel="follow" title="База патентів України">Фармацевтична композиція елтромбопагу оламіну (варіанти) і спосіб її виготовлення (варіанти)</a>
Попередній патент: Режим застосування кладрибіну для лікування розсіяного склерозу
Наступний патент: Вагон з відхиляючим пристроєм автозчіпки
Випадковий патент: Термічний клапан