Комбінація сполук, що містить інгібітори віл інтегрази з іншими терапевтичними агентами
Формула / Реферат
1. Комбінація, що містить сполуку формули (І)
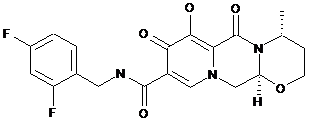 (І)
(І)
або її фармацевтично прийняту сіль, з одним або більше терапевтичними агентами, вибраними з групи, що складається з абакавіру та ефавіренцу.
2. Комбінація за п. 1, яка відрізняється тим, що терапевтичний агент являє собою абакавір.
3. Комбінація за п. 1 або 2, яка відрізняється тим, що фармацевтично прийнятною сіллю сполуки формули (І) є натрієва сіль.
4. Комбінація за п. 2, яка відрізняється тим, що додатково містить ламівудин.
5. Спосіб лікування ВІЛ інфекції, при якому вводять людині сполуку формули (І)
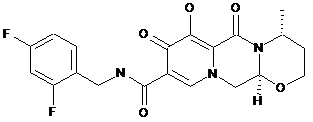 (І)
(І)
або її фармацевтично прийнятну сіль, з одним або більше терапевтичними агентами, вибраними з групи, що складається з абакавіру та ефавіренцу.
6. Спосіб за п. 5, який відрізняється тим, що терапевтичний агент являє собою абакавір.
7. Спосіб за п. 5 або 6, який відрізняється тим, що фармацевтично прийнятною сіллю сполуки формули (І) є натрієва сіль.
8. Спосіб за п 6, який відрізняється тим, що додатково вводять ламівудин.
9. Фармацевтична композиція, що містить сполуку формули (І) та один або більше терапевтичних агентів, вибраних з групи, що складається з абакавіру та ефавіренцу, разом з фармацевтично прийнятним носієм.
10. Фармацевтична композиція за п. 9, яка відрізняється тим, що терапевтичний агент являє собою абакавір.
11. Фармацевтична композиція за п. 9 або 10, яка відрізняється тим, що фармацевтично прийнятною сіллю сполуки формули (І) є натрієва сіль.
12. Фармацевтична композиція за п. 10, яка відрізняється тим, що додатково містить ламівудин.
13. Спосіб лікування за будь-яким з пп. 5-8, який відрізняється тим, що сполуку формули (І) та терапевтичний агент(и) вводять одночасно.
14. Спосіб лікування за будь-яким з пп. 5-8, який відрізняється тим, що сполуку формули (І) та терапевтичний агент(и) вводять послідовно.
15. Пакет пацієнта, що містить сполуку формули (І) та один або більше терапевтичних агентів, вибраних з групи, що складається з абакавіру, ефавіренцу і ламівудину.
Текст
Реферат: Даний винахід належить до комбінацій сполук, що містять інгібітори ВІЛ інтегрази та інші терапевтичні агенти. Такі комбінації корисні в інгібуванні ВІЛ реплікації, профілактиці та/або лікуванні ВІЛ інфікування і при лікуванні СНІД та/або ARC. UA 105556 C2 (12) UA 105556 C2 UA 105556 C2 5 10 15 20 25 30 35 40 45 50 55 60 Вірус імунодефіциту людини ("ВІЛ") є агентом, що викликає синдром набутого імунодефіциту ("СНІД"), захворювання, що характеризується руйнуванням імунної системи, + особливо CD4 Т-клітин, з супутньою сприйнятливістю до опортуністичних інфекцій, і його попередником, пов'язаним зі СНІД комплексом ("ARC"), синдром характеризується такими симптомами, як персистуюча генералізована лімфаденопатія, лихоманка і втрата ваги. ВІЛ є ретровірусом, перетворення його РНК на ДНК здійснюється через дію ферменту зворотної транскриптази. Сполуки, які пригнічують функцію зворотної транскриптази, пригнічують реплікацію ВІЛ в інфікованих клітинах. Такі сполуки є корисними в профілактиці і лікуванні інфекції ВІЛ у людей. На додаток до CD4, ВІЛ вимагає ко-рецептора для потрапляння в клітини-мішені. Рецептори хемокінів функціонують разом з CD4 в якості ко-рецепторів для ВІЛ. Рецептори хемокінів CXCR4 і CCR5 були визначені в якості основних ко-рецепторів для ВІЛ-1. CCR5 діє як основний ко-рецептор для синтезу і введення макрофаг-тропічного ВІЛ у клітини хазяїна. Ці рецептори хемокінів, як вважають, відіграють важливу роль у створенні та розповсюдженні ВІЛ інфекції. Таким чином, антагоністи CCR5 вважаються корисними в якості терапевтичних агентів, активних щодо ВІЛ. Як і у випадку декількох інших ретровірусів, ВІЛ кодує продукування протеази, що здійснює пост-трансляційне розщеплення поліпептидів попередників в процесі, необхідному для формування інфекційних віріонів. Ці продукти включають ген пол, який кодує віріон РНКзалежну ДНК-полімеразу (зворотну транскриптазу), ендонуклеазу, ВІЛ протеазу, і ген капсидних білків, який кодує ядра білків віріону. Одним з напрямків розробки противірусних лікарських препаратів полягає в тому, щоб створити сполуки, які інгібують утворення інфекційних віріонів, взаємодіючи з процесінгом вірусних прекурсорів поліпротеїну. Процесінг цих попередників білків потребує дію вірускодованих протеаз, які необхідні для реплікації. Антивірусний потенціал інгібування ВІЛ протеази був продемонстрований з використанням пептидил інгібіторів. Необхідна стадія ВІЛ реплікації в людських Т-клітинах являє собою введення віруснокодованою інтегразою провірусної ДНК в геном клітини-хазяїна. Інтеграція, як вважають, опосередкована інтегразою в процесі, що включає складання стабільного комплексу нуклеопротеїна з вірусними ДНК послідовностями, розщеплення двох нуклеотидів від 3'-кінців лінійної провірусної ДНК і ковалентних сполук, вбудованих на 3' ОН кінцях провірусної ДНК в шаховому відсіканні на сайті-мішені хазяїна. Відновлювальний синтез результуючого гепу може бути досягнутий за допомогою клітинних ферментів. Інгібітори ВІЛ інтегрази можуть бути ефективними в лікуванні СНІД та інгібуванні реплікації вірусу. Введення комбінації терапевтичних сполук при лікуванні ВІЛ інфекції та пов'язаних з ними станів може призвести до потенційованої противірусної активності, зниження токсичності, затримки прогресування резистентності та збільшення ефективності препарату. Комбінації вводять в стандартній одиничній дозі та це може призвести до збільшення дотримання пацієнтом, оскільки навантаження таблетками зменшується і дозування спрощуються. Однак, не всі сполуки придатні для введення в комбінаціях. Фактори, які впливають на можливості комбінацій, включають хімічну нестабільність сполук, розмір одинарної дози, можливість антагоністичних або просто додаткових активностей комбінаційних сполук, і труднощі в досягненні відповідного складання у композицію. Все ще існує необхідність знайти терапевтичні агенти, придатні для використання в комбінації і можливості фармацевтичних композицій для лікування ВІЛ інфекції. Завдяки своїй високій активності та фармакокінетичному профілю, деякі інгібітори ВІЛ інтегрази привабливі як компоненти комбінованої терапії. Стислий опис креслень Фігура 1: Інгібування ВІЛ-1IIIB сполукою формули (I), GSK1349572A, в комбінації з абакавіром (ABC). Фігура 2: Інгібування ВІЛ-1IIIB сполукою формули (I), GSK1349572A, в комбінації з ефавіренцом (EFV). Фігура 3: Інгібування ВІЛ-1IIIB сполукою формули (I), GSK1349572A, в комбінації з лопінавіром (LPV). Суть винаходу Даний винахід відноситься до комбінації сполук, що містять інгібітори ВІЛ інтегрази та інші лікарські препарати. Такі комбінації корисні в інгібуванні реплікації ВІЛ, запобіганні та/або лікуванні інфекції ВІЛ, і в лікуванні СНІД та/або ARC. Даний винахід також включає фармацевтичні композиції, що містять інгібітори ВІЛ інтегрази. Детальний опис винаходу 1 UA 105556 C2 Даний винахід відноситься до комбінацій, що містять сполуку наступної формули (I), (II) або (III): O F O O N N N O H O F O (I) O O N N O O H N F F (II) O O O H N N O N H N F 5 10 15 20 25 30 35 F (III) або їх фармацевтично прийнятної солі, і одного або більше терапевтичних агентів, вибраних з групи, що складається з нуклеотидних інгібіторів зворотної транскриптази, нуклеозидних інгібіторів зворотної транскриптази (NRTIs), ненуклеозидних інгібіторів зворотної транскриптази (NNRTIs), інгібіторів протеаз, CCR5 антагоністів, CXCR4 антагоністів, інгібіторів гибридизації, інгібіторів дозрівання і інгібіторів інтегрази. Даний винахід відноситься до способів лікування ВІЛ-інфекції, СНІД та пов’язаних зі СНІД станів шляхом введення суб'єкту сполуки формули (I), (II) або (III) і одного або більше терапевтичних агентів, вибраних з групи, що складається з нуклеотидних інгібіторів зворотної транскриптази, нуклеозидних інгібіторів зворотної транскриптази (NRTIS), ненуклеозидних інгібіторів зворотної транскриптази (NNRTIS), інгібіторів протеаз, CCR5 антагоністів, CXCR4 антагоністів, інгібіторів гибридизації, інгібіторів дозрівання і інгібіторів інтеграз. Сполука формули (I) також відома як GSK1349572. Хімічна назва сполуки формули (I) (4R,12aS)-N-[2,4-фторфеніл)метил]-3,4,6,8,12,12a-гексагідро-7-гідрокси-4-метил-6,8-діоксо-2Hпіридо[1’,2’:4,5]піразіно [2,1-b] [1,3] оксазин-9-карбоксамід. Хімічна назва сполуки формули (II) (3S, 11aR)-N-[(2,4-дифторфеніл)метил]-2,3,5,7,11,11aгексагідро-6-гідрокси-3-метил-5,7-діоксо-оксазоло[3,2-a]піридо[1,2-d]піразін-8-карбоксамід. Хімічна назва сполуки формули (III) (4aS,13aR)-N-[2,4-дифторфеніл)метил]-10-гідрокси-9,11діоксо-2,3,4a,5,9,11,13,13a-октагідро-1H-піридо[1,2-a]піроло[1’,2’:3,4,]імідазо[1,2-d]піразін-8карбоксамід. Термін "фармацевтично прийнятний носій або ад'ювант" відноситься до носія або ад'юванта, які можуть бути введені пацієнтові, а також сполук за даним винаходом, і який не руйнує їх фармакологічну активність і нетоксичних при введенні в дозах, достатніх для доставки терапевтичної кількості противірусного агента. Термін "лікування", який використовують у цій заявці, відноситься до полегшення симптомів, зокрема розладу у пацієнта, або полегшення, що встановлюється вимірюваннями, пов'язаного з певним розладом, і може включати пригнічення симптомів рецидиву у безсимптомних пацієнтів, таких, як пацієнти, у яких вірусна інфекція стала прихованою. Лікування може включати профілактику, яка відноситься до запобігання захворювання або станів, або запобігання появи симптомів такого захворювання або станів, у пацієнта. Використовуваний у цій заявці термін "пацієнт" відноситься до ссавців, включаючи людину. 2 UA 105556 C2 5 10 15 20 25 30 35 40 45 50 55 60 Використовуваний у цій заявці термін «суб'єкт» відноситься до пацієнта, тварини або біологічної проби. Фармацевтично прийнятні солі сполук за даним винаходом, включають одержані з фармацевтично прийнятних неорганічних і органічних кислот і основ. Прикладами відповідних кислот є соляна, бромистоводнева, сірчана, азотна, хлорна, фумарова, малеїнова, фосфорна, гліколева, молочна, саліцилова, янтарна, толуол-п-сульфонова, винна, оцтова, лимонна, метансульфонова, етансульфонова, мурашина, бензойна, малонова, нафталін-2сульфокислота і бензолсульфонова кислота. Інші кислоти, такі як щавлева, в той час як самі по собі не є фармацевтично прийнятними, можуть бути використані при одержанні солей, корисних в якості проміжних сполук при одержанні сполук за даним винаходом та їх фармацевтично прийнятних солей адитивних кислот. Солі, одержані з відповідних основ, включають солі лужних + металів (наприклад, натрію), лужноземельних металів (наприклад, магнію), амонію, NW 4 (де W являє собою C1-4 алкіл) та інших амінних солей. Переважною сіллю є натрієва сіль. Солі сполук за даним винаходом можуть бути одержані способами, відомими фахівцям в цій галузі. Наприклад, обробка сполуки за даним винаходом відповідною основою або кислотою у відповідному розчиннику може дати відповідну сіль. Даний винахід відноситься до способів лікування або профілактики вірусних інфекцій, наприклад ВІЛ інфекції, в організмі людини, що включають введення людині терапевтично ефективної кількості сполуки формули (I), (II) або (III) або фармацевтично прийнятної солі в комбінації з одним або більше терапевтичними агентами, вибраними з групи, що складається з нуклеотидних інгібіторів зворотної транскриптази, нуклеозидних інгібіторів зворотної транскриптази (NRTIS), ненуклеозидних інгібіторів зворотної транскриптази (NNRTIS), інгібіторів протеаз, CCR5 антагоністів, CXCR4 антагоністів, інгібіторів гібридизації, інгібіторів дозрівання і інгібіторів інтегрази. Комбінацію можна вводити одночасно або послідовно. Сполуки формули (I), (II) і (III) особливо придатні для лікування або профілактики ВІЛ інфекції і супутніх захворювань. Посилання у цій заявці на лікування можуть поширюватися на профілактику, а також лікування встановлених інфекцій, симптомів і асоційованих клінічних станів, таких як СНІД-повязаний комплекс (ARC), саркома Капоші, а також СНІД-деменції. Комбіновані терапії включають введення сполуки за даним винаходом або її фармацевтично прийнятної солі та іншого фармацевтично активного агента. Активний інгредієнт(и) і фармацевтично активні агенти можна вводити одночасно (тобто паралельно), або в одній або різних фармацевтичних композиціях, або послідовно в будь-якому порядку. Кількість активного інгредієнта(ів) і фармацевтично активного агента(ів) і відносні розрахунки часу введення обирають для того, щоб досягти бажаного комбінованого терапевтичного ефекту. Приклади таких терапевтичних агентів включають, але не обмежуючись цим, агенти, які є ефективними для лікування вірусних інфекцій та супутніх станів. Серед цих агентів є нуклеотидні інгібітори зворотної транскриптази, ациклічні нуклеозидні фосфонати, наприклад, (S)-1-(3-гідрокси-2-фосфонілметоксипропіл) цитозин (HPMPC), [[[2-(6-аміно-9H-пурин-9іл)етокси] метил]фосфініліден] біс(оксиметилен)-2,2-диметилпропаноєва кислота (біс-POM PMEA адефовір діпівоксіл), адефовір, [[(1R)-2-(6-аміно-9Н-пурин-9-іл)-1-метилметокси] метил] фосфонова кислота (тенофовір), тенофовір дізопроксіл фумарат та біс(ізопропоксикарбонілоксиметил)естер (R)-[[2-(6-аміно-9H-пурин-9-іл)-1метилетокси]метил]фосфонієвої кислоти (біс-POC-PMPA); нуклеозидні інгібітори зворотної транскриптази, наприклад 3'-азидо-3'-дезокситимидина (AZT, зидовудин), 2 ', 3'дидезоксицитидин (ddC, зальцитабін), 2',3'-дидезоксиаденозин, 2',3'-дидезоксиінозин (ddI, диданозин), 2',3'-дидегідротімідін (d4T, ставудин), (-)-цис-1-(2-гідроксиметил)-1,3-оксатіолан-5іл) цитозин (ламівудин), цис-1-(2-(гідроксиметил)-1,3-оксатіолан-5-іл)-5-фторцитозин (FTC, емтрицитабін), (-)-цис-4-[2-аміно-6-(циклопропіламіно)-9H-пурин-9-іл]-2-циклопентен-1-метанол (абакавір), фозівудин тидоксил, аловудин, амдоксовір, ельвуцитабін, априцитабін та фестинавір (OBP-601); інгібітори протеаз, наприклад, індинавір, ритонавір, нелфінавір, ампренавір, саквінавір, фосампренавір, лопінавір, атазанавір, тіпранавір, дарунавір, бреканавір, паланавір, лазінавір, TMC-310911, DG-17, PPL-100; ненуклеозидні інгібітори зворотної транскриптази (NNRTIS), наприклад, невірапін, делавірдін, ефавіренц, GSK2248761 (IDX-12899), лерсіверин (UK-453,061), рілпівірін (TMC-278), етравірин, ловірід, імманокал, олтіпарз, каправірін та RDEA806; інгібітори інтеграз, наприклад, ралтегравір, елвітегравір та JTK-656; CCR5 та/або CXCR4 антагоністи, наприклад, маравірок, вікрівірок (Sch-D), TBR-652 (TAK-779), TAK-449, PRO-140, GSK706769 та SCH-532706; інгібітори гибридизації, наприклад енфувіртід (T-20), T-1249, PRO542, ібалізумаб (TNX-355), BMS-378806 (BMS-806 ), BMS-488043, KD-247, 5-гелікс інгібітори та інгібітори ВІЛ приєднання та інгібітори дозрівання, наприклад, бевірімат (PA-344 і РА-457). Даний винахід включає комбінацію, що містить сполуку формули (I) 3 UA 105556 C2 O F O O N N N O H O F 5 10 15 20 25 (I) або її фармацевтично прийнятні солі, і одного або більше терапевтичних агентів, вибраних з групи, що складається з ламівудину, абакавіру, тенофовіру, ефавіренцу, GSK2248761, лерсівіріну, лопінавіру, фосампренавіру і атазанавіру. Даний винахід також охоплює комбінацію, що містить сполуку формули (I) або її фармацевтично прийнятну сіль, і одного або більше терапевтичних агентів, вибраних з абакавіру, ефавіренцу або лопінавіру. Даний винахід охоплює комбінацію, що складається із сполуки формули (I) або її фармацевтично прийнятної солі, і абакавіру. Даний винахід охоплює спосіб лікування ВІЛ інфекції, що включає введення суб'єкту сполуки формули (I), або її фармацевтично прийнятної солі, і одного або більше терапевтичних агентів, вибраних з групи, що складається з ламівудину, абакавіру, тенофовіру, ефавіренцу, GSK2248761, лерсівурину, лопінавіру, фосампренавіру і атазанавіру. Даний винахід охоплює спосіб лікування ВІЛ інфекції, що включає введення суб'єкту сполуки формули (I) або її фармацевтично прийнятної солі, з одним або більше терапевтичним агентом, вибраним з групи, що складається з абакавіру, ефавіренцу і лопінавіру. Даний винахід охоплює спосіб лікування ВІЛ інфекції, що включає введення суб'єкту сполуки формули (I) або її фармацевтично прийнятної солі, і абакавіру. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (I) або її фармацевтично прийнятну сіль, і один або більше терапевтичних агентів, вибраних з групи, що складається з: ламівудину, абакавіру, ефавіренцу, тенофовіру, GSK2248761, лерсівірину, лопінавіру, фосампренавіру і атазанавіру разом з фармацевтично прийнятним носієм. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (I) або її фармацевтично прийнятну сіль, і один або більше терапевтичних агентів, вибраних з групи, що складається з: абакавіру, ефавіренцу і лопінавіру, разом з фармацевтично прийнятним носієм. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (I) або її фармацевтично прийнятну сіль та абакавір разом з фармацевтично прийнятним носієм. Даний винахід охоплює комбінацію, що містить сполуку формули (II) O O O N N O O H N F 30 35 40 F (II) або її фармацевтично прийнятну сіль, і одного або більше терапевтичних агентів, вибраних з групи, що складається з ламівудину, абакавіру, тенофовіру, ефавіренцу, GSK2248761, лерсівирину, лопінавіру, фосампренавіру і атазанавіру. Даний винахід також охоплює комбінацію сполуки формули (II) або її фармацевтично прийнятної солі, і одного або більше терапевтичних агентів, вибраних з абакавіру, ефавіренцу і лопінавіру. Даний винахід охоплює комбінацію, що містить сполуку формули (II) або її фармацевтично прийнятну сіль, і абакавір. Даний винахід охоплює спосіб лікування ВІЛ інфекції, що включає введення суб'єкту сполуки формули (II) або її фармацевтично прийнятної солі, і одного або більше терапевтичних агентів, вибраних з групи, що складається з ламівудину, абакавіру, тенофовіру, ефавіренцу, GSK2248761, лерсивірину, лопінавіру, фосампренавіру і атазанавіру. Даний винахід охоплює спосіб лікування ВІЛ інфекції, що включає введення суб'єкту сполуки формули (II) або її фармацевтично прийнятної солі, з одним або більше терапевтичних агентів, вибраних з групи, що складається з абакавіру, ефавіренцу і лопінавіру. Даний винахід охоплює спосіб лікування ВІЛ інфекції, що включає введення суб'єкту сполуки формули (II) або її 4 UA 105556 C2 5 10 фармацевтично прийнятної солі, і абакавіру. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (II) або її фармацевтично прийнятну сіль, і один або більше терапевтичних агентів, вибраних з групи, що складається з: ламівудину, абакавіру, тенофовіру, ефавіренцу, GSK2248761, лерсівирину, лопінавіру, фосампренавіру і атазанавіру разом з фармацевтично прийнятним носієм. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (II) або її фармацевтично прийнятну сіль, і один або більше терапевтичних агентів, вибраних з групи, що складається з: абакавіру, ефавіренцу і лопінавіру разом з фармацевтично прийнятним носієм. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (II) або її фармацевтично прийнятну сіль і абакавір разом з фармацевтично прийнятним носієм. Даний винахід охоплює комбінацію, що містить сполуку формули (III) O O O H N N O N H N F F 15 20 25 30 35 40 45 50 (III) або її фармацевтично прийнятну сіль, і одного або більше терапевтичних агентів, вибраних з групи, що складається з ламівудину, абакавіру, тенофовіру, ефавіренцу, GSK2248761, лерсивірину, лопінавіру, фосампренавіру і атазанавіру. Даний винахід також охоплює комбінацію сполуки формули (III) або її фармацевтично прийнятної солі, і одного або більше терапевтичних агентів, вибраних з абакавіру, ефавіренцу і лопінавіру. Даний винахід також охоплює комбінацію сполуки формули (III) або її фармацевтично прийнятної солі, і абакавір. Даний винахід охоплює спосіб лікування ВІЛ інфекції, що включає введення суб'єкту сполуки формули (III) або її фармацевтично прийнятної солі, і одного або більше терапевтичних агентів, вибраних з групи, що складається з ламівудину, абакавіру, тенофовіру, ефавіренцу, GSK2248761, лерсивірину, лопінавіру, фосампренавіру і атазанавіру. Даний винахід охоплює спосіб лікування ВІЛ інфекції, що включає введення суб'єкту комбінації сполуки формули (III) або її фармацевтично прийнятної солі, з одним або більше терапевтичним агентом, вибраним з групи, що складається з абакавіру, ефавіренцу, і лопінавіру. Даний винахід охоплює спосіб лікування інфекції ВІЛ, що включає введення суб'єкту сполуки формули (III) або її фармацевтично прийнятної солі, і абакавіру. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (III) або її фармацевтично прийнятну сіль, і один або більше терапевтичних агентів, вибраних з групи, що складається з: ламівудину, абакавіру, тенофовіру, ефавіренцу, GSK2248761, лерсивірину, лопінавіру, фосампренавіру і атазанавіру разом з фармацевтично прийнятним носієм. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (III) або її фармацевтично прийнятну сіль, і один або більше терапевтичних агентів, вибраних з групи, що складається з: абакавіру, ефавіренцу і лопінавіру разом з фармацевтично прийнятним носієм. Даний винахід охоплює фармацевтичну композицію, що містить сполуку формули (III) або її фармацевтично прийнятну сіль і абакавір разом з фармацевтично прийнятним носієм. Даний винахід охоплює комбінації, способи лікування і фармацевтичні композиції, як описано вище, де фармацевтично прийнятною сіллю сполук формули (I), (II) або (III) є натрієва сіль. Даний винахід охоплює комбінації, способи лікування і фармацевтичні композиції, як описано вище, в яких один або більше терапевтичних агентів являє собою фармацевтично прийнятну сіль зазначених терапевтичних агентів, наприклад, абакавіра гемісульфат, фосампренавір кальцій, атазанавір сульфат, тенофовір дізопроксіл сульфат, вікрівірок малеат або бевірімат дімеглумін. Даний винахід охоплює способи лікування, як описано вище, де суб’єктом є людина. Даний винахід охоплює комбінації, способи лікування і фармацевтичні композиції, як описано вище, де комбінації вводять послідовно. Даний винахід охоплює комбінації, способи лікування і фармацевтичні композиції, як описано вище, де комбінації вводять одночасно або паралельно. 5 UA 105556 C2 5 10 15 20 25 30 35 40 45 50 55 60 Сполуки формули (I), (II) та (III) можуть бути одержані способами, описаними в WO 2006/116764, США 61/193, 634 (WO2010/068253) або 61/193,636 (WO2010/068262), що включені у цю заявку шляхом посилання. Абакавір може бути одержаний способами, описаними в патентах США №№ 5,034,394; 5,089,500; 6,294,540; 5,641,889; 5,840,990; 5,919,941; 5,808,147; 6,392,085; 6,448,403; 5,917,041; 6,087,501; 5,917,042; 6,555,687; 6,552,193; 6,870,053; 6,294,540; 6,340,587; або 6,646,125. Ламівудин може бути одержаний способами, описаними в патентах США №№ 5,047,407; 7,119,202; 5,905,082; 5,696,254; 5,663,320; 5,693,787; 6,051,709; або 6,329,522. Тенофовір може бути одержаний способами, описаними в патентах США №№ 5,922,695; 5,935,946; 5,977,089; 6,043,230, 6,069,249. Ефавіренц може бути одержаний способами, описаними в патентах США №№ 5,519.021; 5,663,169; 5,811,423; 6,555,133; 6,639,071; або 6,939,964. GSK2248761 може бути одержаний способами, описаними в патенті США № 7,534,809. Лерсівірін може бути одержаний способами, описаними в патенті США № 7,109,228. Лопінавір може бути одержаний способами, описаними в патенті США № 5,914,332. Фосампренавір може бути одержаний способами, описаними в патентах США №№ 6,436,989; 6,514,953; або 6,281,367. Атазанавір може бути одержаний способами, описаними в патентах США №№ 5,849,911 або 6,087,383. Терапевтичні агенти комбінацій можуть бути одержані відповідно до опублікованих способів або будь-яким способом, відомим фахівцям в цій галузі. В аспекті даного винаходу, сполуки формули (I), (II) або (III) або їх фармацевтично прийнятні солі можуть бути складені в композиції разом з одним або більше терапевтичними агентами. Композиція може бути фармацевтичною композицією, яка містить сполуку формули (I), (II) або (III), один або декілька терапевтичних агентів, і фармацевтично прийнятний носій, ад'ювант або основу. В одному варіанті виконання композиція включає кількість комбінації за даним винаходом, ефективних для лікування та профілактики вірусних інфекцій, наприклад ВІЛ інфекції, в біологічній пробі або у пацієнта. В іншому варіанті виконання комбінації за даним винаходом та їх фармацевтичні композиції, що містять кількість комбінації за даним винаходом, ефективні для інгібування реплікації вірусу або для лікування, або для профілактики вірусних інфекцій або хвороби або розладу, наприклад ВІЛ інфекції, і фармацевтично прийнятний носій, ад'ювант або основа, можуть бути складені у композицію для введення пацієнтові, наприклад, для перорального введення. Даний винахід охоплює комбінації за даним винаходом для застосування в медичній терапії, наприклад, для лікування або профілактики вірусних інфекцій, наприклад, ВІЛ інфекції та пов'язаних з нею станами. Сполуки за даним винаходом особливо корисні для лікування СНІДу та пов'язаних з ним клінічних станів, таких як СНІД-пов'язаний комплекс (ARC), прогресивна генералізована лімфаденопатія (PGL), саркома Капоші, тромбоцитопенічна пурпура, пов'язаних зі СНІД неврологічних захворювань, таких, як комплекс СНІД-деменція, розсіяний склероз або тропічний парапарез, анти-ВІЛ антитіло-позитивних і ВІЛ-позитивних станів, у тому числі таких станів у безсимптомних хворих. Згідно з іншим аспектом, даний винахід відноситься до способу лікування або профілактики симптомів або наслідків вірусної інфекції у інфікованих пацієнтів, наприклад, у ссавців, включаючи людину, яка включає введення вказаному пацієнтові фармацевтично ефективної кількості комбінації за даним винаходом. Відповідно до одного аспекту даного винаходу, вірусна інфекція являє собою ретровірусну інфекцію, зокрема ВІЛ інфекцію. Даний винахід також включає застосування комбінації за даним винаходом при одержанні лікарського засобу для одночасного (паралельного) або послідовного введення суб’єкту для лікування вірусних інфекцій, зокрема, ВІЛ інфекції. Даний винахід також відноситься до способу лікування клінічного стану у пацієнта, наприклад, ссавця, включаючи людину, клінічний стан якого включає такі, які були розглянуті вище, що включає лікування зазначеного пацієнта фармацевтично ефективною кількістю сполуки за даним винаходом. Даний винахід також включає спосіб лікування або профілактики будь-якого з зазначених вище захворювань або станів. Сполуки за даним винаходом можуть бути введені з агентом, який, як відомо, інгібує або зменшує метаболізм сполук, наприклад ритонавіром. Відповідно, даний винахід охоплює спосіб лікування або профілактики захворювання, як було описано, шляхом введення сполуки за даним винаходом в комбінації з метаболічним інгібітором. Таку комбінацію можна вводити одночасно або послідовно. Загалом придатна доза для кожного з вищезазначених станів буде знаходитися в діапазоні 6 UA 105556 C2 5 10 15 20 25 30 35 40 45 50 55 60 від 0,01 до 250 мг на кілограм маси тіла реципієнта (наприклад, людини) в день, в діапазоні від 0,1 до 100 мг на кілограм маси тіла в день, в діапазоні від 1 до 30 мг на кілограм маси тіла в день, в діапазоні від 0,5 до 20 мг на кілограм маси тіла в день. Якщо не вказано інше, всі маси активних інгредієнтів розраховують як батьківську сполуку формули (I), (II) або (III) та інші терапевтичні агенти. Для їх солей маса буде збільшуватися пропорційно. Бажана доза може бути представлена як одна, дві, три, чотири, п'ять, шість або більше суб-доз, які вводять через відповідні проміжки часу протягом дня. В деяких випадках бажана доза може бути надана через день. Ці суб-дози можуть бути введені у стандартній лікарській формі, наприклад, що містить від 1 до 2000 мг, від 5 до 500 мг, від 10 до 400 мг, від 20 до 300 мг кожного активного інгредієнта на одиницю стандартної лікарської форми. Комбінації можуть бути введені для досягнення піку концентрації в плазмі крові кожного активного інгредієнта. Хоча це можливо, щоб активні інгредієнти були введені окремо, переважно представляти їх у вигляді фармацевтичної композиції. Композиції за даним винаходом містять активний інгредієнт, як зазначено вище, разом з одним або більше прийнятними носіями і одним або більше додатковими терапевтичними агентами. Кожен носій повинен бути прийнятним в сенсі сумісності з іншими інгредієнтами композиції і не шкідливим для пацієнта. Фармацевтичні композиції включають придатні для перорального, ректального, назального, місцевого (в тому числі трансдермального, буккального та сублінгвального), вагінального або парентерального (включаючи підшкірне, внутрішньом'язове, внутрішньовенне, внутрішньошкірне, та інтравітреальне) введення. Композиції можуть бути зручно представлені у стандартній лікарській формі і можуть бути отримані будь-якими способами, добре відомими в галузі фармацевтики. Такі способи являють собою ще один аспект даного винаходу і включають стадію об'єднання активних інгредієнтів з носієм, який представляє собою один або декілька допоміжних інгредієнтів. Загалом, композиції одержують шляхом однорідного і ретельного об’єднання активних інгредієнтів з рідкими носіями або тонко подрібненими твердими носіями або обома, з наступним, якщо необхідно, формуванням продукту. Даний винахід також включає фармацевтичну композицію, як визначено вище, де сполука за даним винаходом або її фармацевтично прийнятне похідне, та інший терапевтичний агент представлені окремо один від одного у вигляді набору частин. Композиції, придатні для трансдермального введення можуть бути представлені у вигляді окремих пластирів, пристосованих для того, щоб залишатися в тісному контакті з епідермісом реципієнта протягом тривалого періоду часу. Такі пластирі придатним чином містять активну сполуку 1) у необов'язково буферному водному розчині або 2) розчинені та/або дисперговані в клею або 3) дисперговані у полімері. Відповідна концентрація активної сполуки становить приблизно від 1% до 25%, переважно приблизно від 3% до 15%. Як одна конкретна можливість, активна сполука може бути доставлена з пластирі електротранспортом або іонофорезом, як взагалі описано в Pharmaceutical Research 3 (6), 318 (1986). Фармацевтичні композиції за даним винаходом, придатні для перорального введення, можуть бути представлені у вигляді дискретних форм дозування, таких, як капсули, таблеткикапсули, саше або таблетки, кожна з яких містить певну кількість активних інгредієнтів, у вигляді порошку або гранул, у вигляді розчину або суспензії у водній або неводній рідині, або у вигляді рідкої емульсії типу олія-в-воді або рідкої емульсії типу вода-в-олії. Активний інгредієнт може бути також представлений у вигляді болюса, електуарія або пасти. Таблетка може бути одержана шляхом пресування або формування, необов'язково з одним або більше допоміжними інгредієнтами. Пресовані таблетки можуть бути одержані шляхом пресування у відповідному пристрої активних інгредієнтів у вільно текучій формі, такій, як порошок або гранули, необов'язково в суміші зі зв'язуючою речовиною (наприклад, повідон, желатин, гідроксипропілметилцелюлоза), мастилом, інертним розріджувачем, консервантом, розпушувачем (наприклад, натрій крохмаль гліколят, поперечно-зшитий повідон, поперечнозшита натрій карбоксиметилцелюлоза), поверхнево-активна речовина або диспергатор. Формовані таблетки можуть бути одержані шляхом формування суміші порошкоподібної сполуки, змоченої інертним рідким розріджувачем у відповідному пристрої. Таблетки можуть бути додатково покриті або на них можуть бути зроблені зарубки і можуть бути складені таким чином, щоб забезпечити повільне або контрольоване вивільнення активних інгредієнтів в них, використовуючи, наприклад, гідроксипропілметилцелюлозу в різних пропорціях для отримання бажаного профілю вивільнення. Таблетки можуть бути необов’язково забезпечені ентеросолюбільним покриттям, щоб забезпечити вивільнення в частинах кишечнику, крім шлунку. Фармацевтичні композиції, придатні для місцевого застосування у порожнині рота, 7 UA 105556 C2 5 10 15 20 25 30 35 40 45 50 55 60 включають лепішки, що містять активні інгредієнти в ароматній основі, зазвичай, сахарозу або трагакантову акацію, пастилки, що містять активний інгредієнт в інертній основі, такій, як желатин та гліцерин, або сахароза та акація, і рідини для полоскання рота включають активний інгредієнт у відповідному рідкому носії. Фармацевтичні композиції, придатні для вагінального введення, можуть бути представлені у вигляді свічок, тампонів, кремів, гелів, паст, піни або спрея. Фармацевтичні композиції можуть містити на додаток до активного інгредієнта такі носії, які відомі в цій галузі як придатні. Фармацевтичні композиції для ректального введення можуть бути представлені у вигляді свічок з відповідним носієм, що включає, наприклад, масло какао або саліцилат або інші матеріали, що широко використовуються в техніці. Свічки можуть бути зручно сформовані шляхом змішування активної комбінації з розм'якшеним або розплавленим носієм(ями) з подальшим охолодженням і формуванням в формах. Фармацевтичні композиції придатні для парентерального введення включають водні та неводні ізотонічні стерильні розчини для ін'єкцій, які можуть містити антиоксиданти, буфери, бактеріостатичні і розчинені речовини, які надають фармацевтичній композиції ізотонічності з кров'ю цільового реципієнта, а також водні та неводні стерильні суспензії, які можуть містити агенти суспендування та загусники, та ліпосоми або інші системи мікрочастинок, які призначені для влучення сполуки у компоненти крові або одного або декількох органів. Фармацевтичні композиції можуть бути представлені в герметичних контейнерах на стандартну дозу або множину доз, наприклад, ампулах і віалах, а також можуть бути збережені в ліофілізованому стані, що вимагає тільки додавання стерильного рідкого носія, наприклад, води для ін'єкцій, безпосередньо перед використанням. Розчини для ін'єкцій і суспензії, що не готують заздалегідь, можуть бути одержані зі стерильних порошків, гранул і таблеток типу, який було описано вище у цій заявці. Фармацевтичні композиції стандартної лікарської форми включають ті, які містять добову дозу або добову субдозу активних інгредієнтів, як зазначено вище, або їх відповідну фракцію. Фармацевтичні композиції за даним винаходом можуть бути представлені як пакети для пацієнтів, що містять один або більше курсів лікування в одній упаковці, наприклад, блістерна упаковка. Має бути зрозуміло, що введення комбінації за даним винаходом за допомогою одного пакета пацієнта, або пакетів пацієнта кожної композиції, являє собою додаткову ознаку даного винаходу. Має бути зрозуміло, що додатково до інгредієнтів, конкретно зазначених вище, фармацевтичні композиції за даним винаходом можуть містити інші агенти, традиційні в цій галузі, з урахуванням типу фармацевтичної композиції, що розглядається, наприклад, фармацевтичні композиції придатні для перорального введення можуть містити такі додаткові агенти як підсолоджувачі, загусники і ароматизатори. Приклади Приклад 1: Біологічна активність Аналізи Спосіб Противірусну ВІЛ активність вимірювали за допомогою колориметричної процедури на основі тетразолію в трансформованій клітинній лінії MT-4 людського Т-клітинного вірусу лейкемії (HTLV-1). Аліквоти тестової сполуки розводили вертикально поперек вихідної аналітичної планшети з глибокими лунками, в середовищі (RPMI 1640, 10% об./об. ембріональної телячої сироватки (FBS), і 10 мкг/мл гентаміцину) в концентраціях, які були приблизно в 40 разів вище, ніж в кінцевій аналітичній концентрації. Серійні розведення були зроблені у співвідношеннях 1:2 або 1:3,16. ВІЛ інгібітори розводили по горизонталі поперек вихідних аналітичних планшет, а також в концентраціях, які були приблизно в 40 разів вище, ніж в кінцевій аналітичній концентрації. Невеликі аліквоти обох вертикально-розведених і горизонтально-розведених сполук були об'єднані в дочірні планшети з використанням автоматизованої системи піпеток на 96-лунок (RapidPlate-96, Zymark Corp.) Шахові розведення були організовані таким чином, щоб кожна концентрація тестової сполуки була проаналізована в присутності і за відсутності кожної концентрації ВІЛ інгібіторів. Аналізи анти-ВІЛ активності проводили в трьох тестах, або більше, в кожній комбінації. Експоненціально зростаючі клітини МТ-4 збирали і центрифугували при 1000 об./хв. протягом 10 хвилин в центрифузі Жуан (модель CR 4 12). Дебрис повторно суспендeвали у свіжому середовищі (RPMI 1640, 20% 6 об./об. FBS, 20% об./об. IL-2, і 10 мкг/мл гентаміцину) до густини 1,25x10 клітин/мл. Аліквоти дебрису були інфіковані шляхом додавання ВІЛ-1 (штам IIIB), розведеного, щоб отримати 4 вірусну множинність зараження (MOI) у 73 БУО на 1x10 клітин. Аналогічну аліквоту дебрису розводили середовищем для забезпечення фальшиво-інфікованого контролю. Інфікування 8 UA 105556 C2 5 10 15 20 25 30 35 40 45 дебрису проводили протягом 1 години при 37°С в інкубаторі культур тканин зі зволоженою 5% CO2 атмосферою. Через 1 годину інкубації вірусну/клітинну суспензію додавали в кожну лунку планшет, що містили попередньо розведені сполуки. Планшети були потім поміщені в інкубатор культур тканин зі зволоженою 5% CO2 протягом 5 днів. Наприкінці інкубаційного періоду, 40 мкл CellTiter 96 MTS реагенту (Promega № G3581) було додано у кожну лунку інкубаційної планшети. Планшети інкубували при 37°С протягом 2-3 годин, щоб дозволити розвиток кольору. Оптичну густину вимірювали при 492 нм з використанням планшетного рідеру поглинання (Tecan № 20-300). Використаний вірус ВІЛ-1 штам IIIB, дикого типу лабораторний штам, титр вірусу = 6,896 Е4 TCID 50/мл. Аналіз даних Хоча деякі формати аналізів можуть теоретично пропустити антагонізм через комбінаційну цитотоксичність, підхід, описаний у цій заявці, не повинен пропустити антагоністичну дію. Зчитування в аналізі клітин МТ-4 використовує MTS, реагент забарвлення на основі тетразолію, де зміни оптичної густини (O.D.) реагенту використовують для оцінки загального числа клітин, що залишилися після лікування. Остаточні кількості МТ-4 клітин можуть зменшуватися за рахунок двох ефектів. По-перше, ВІЛ-індукована цитотоксичність може виникнути, коли ВІЛ вбиває більше ніж 75% МТ-4 клітин протягом 5 днів після зараження. По-друге, цитотоксичність, індукована сполуками, може мати місце, коли сполука або безпосередньо вбиває МТ-4 клітини, або запобігає росту клітин (стаз) протягом 5 днів у інфікованих або неінфікованих клітин. У будьякій з цих ситуацій оптична густина є низькою в порівнянні з інфікованими клітинами, захищеними анти-ВІЛ-1 сполуками або по відношенню до непролікованих і неінфікованих клітин контролю. Оскільки як цитотоксичні ефекти, так і антагонізм анти-ВІЛ активності призведе до зниження оптичної густини, ми не повинні пропустити антагоністичну дію через комбінаційну цитотоксичність, але можемо недооцінювати синергетичні комбінації. В рамках аналізу комбінаційну цитотоксичність оцінювали шляхом порівняння лунок, що містять неінфіковані клітини МТ-4 від аналітичних планшет, що містили найвищу концентрацію тестової сполуки або реперної сполуки, з лунками, що містили ВІЛ-1-інфіковані МТ-4 клітини при відповідних найвищих комбінаційних концентраціях. Для кожного з цих значень існує одна лунка на аналітичну пластину і, отже, не менше 3 лунок на комбінаційний аналіз. Незважаючи на те, що вони не включають формальний аналіз комбінаційної цитотоксичності, співвідношення сполук в комбінаціях з окремою сполукою забезпечує визначення комбінаційної цитотоксичності сполук в рамках досліджених концентрацій. Взаємодія кожної пари комбінацій сполук була проаналізована методами, описаними Selleseth, D.W. et al. (2003) Antimicrobial Agents and Chemotherapy 47:1468-71. Синергія і антагонізм визначали як відхилення від дозової адитивності, в результаті чого два препарати взаємодіють таким чином, якби вони були однаковими лікарськими засобами. Значення для середнього відхилення від адитивності в діапазоні від - 0,1 до - 0,2 вказують на слабку синергію та значення цього підходу - 0,5 вказує на сильну синергію взаємодії. З іншого боку, позитивні значення від 0,1 до 0,2 означатимуть, що існує слабкий антагонізм між процедурами лікування. Результати Як було встановлено, сполука формули (I) є добавкою до ралтегравіра, адефовіра і маравірока і на неї не впливає наявність рибавірину. Сполука формули (I), як було встановлено, має синергетичний ефект у комбінації з ставудином, абакавіром, ефавіренцом, невірапіном, лопінавіром, ампренавіром, енфувіртідом. ФОРМУЛА ВИНАХОДУ 1. Комбінація, що містить сполуку формули (І) 50 O F O O N N F N O H O (І) або її фармацевтично прийняту сіль, з одним або більше терапевтичними агентами, вибраними з групи, що складається з абакавіру та ефавіренцу. 9 UA 105556 C2 5 2. Комбінація за п. 1, яка відрізняється тим, що терапевтичний агент являє собою абакавір. 3. Комбінація за п. 1 або 2, яка відрізняється тим, що фармацевтично прийнятною сіллю сполуки формули (І) є натрієва сіль. 4. Комбінація за п. 2, яка відрізняється тим, що додатково містить ламівудин. 5. Спосіб лікування ВІЛ інфекції, при якому вводять людині сполуку формули (І) O F O O N N F 10 15 20 25 N O H O (І) або її фармацевтично прийнятну сіль, з одним або більше терапевтичними агентами, вибраними з групи, що складається з абакавіру та ефавіренцу. 6. Спосіб за п. 5, який відрізняється тим, що терапевтичний агент являє собою абакавір. 7. Спосіб за п. 5 або 6, який відрізняється тим, що фармацевтично прийнятною сіллю сполуки формули (І) є натрієва сіль. 8. Спосіб за п 6, який відрізняється тим, що додатково вводять ламівудин. 9. Фармацевтична композиція, що містить сполуку формули (І) та один або більше терапевтичних агентів, вибраних з групи, що складається з абакавіру та ефавіренцу, разом з фармацевтично прийнятним носієм. 10. Фармацевтична композиція за п. 9, яка відрізняється тим, що терапевтичний агент являє собою абакавір. 11. Фармацевтична композиція за п. 9 або 10, яка відрізняється тим, що фармацевтично прийнятною сіллю сполуки формули (І) є натрієва сіль. 12. Фармацевтична композиція за п. 10, яка відрізняється тим, що додатково містить ламівудин. 13. Спосіб лікування за будь-яким з пп. 5-8, який відрізняється тим, що сполуку формули (І) та терапевтичний агент(и) вводять одночасно. 14. Спосіб лікування за будь-яким з пп. 5-8, який відрізняється тим, що сполуку формули (І) та терапевтичний агент(и) вводять послідовно. 15. Пакет пацієнта, що містить сполуку формули (І) та один або більше терапевтичних агентів, вибраних з групи, що складається з абакавіру, ефавіренцу і ламівудину. 10 UA 105556 C2 Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 11
ДивитисяДодаткова інформація
Назва патенту англійськоюAntiviral therapy
Автори англійськоюUnderwood, Mark Richard
Автори російськоюУндервуд Марк Ричард
МПК / Мітки
МПК: A01N 43/00
Мітки: віл, комбінація, іншими, терапевтичними, агентами, містить, інгібітори, інтегрази, сполук
Код посилання
<a href="https://ua.patents.su/13-105556-kombinaciya-spoluk-shho-mistit-ingibitori-vil-integrazi-z-inshimi-terapevtichnimi-agentami.html" target="_blank" rel="follow" title="База патентів України">Комбінація сполук, що містить інгібітори віл інтегрази з іншими терапевтичними агентами</a>
Попередній патент: Стійкий до утворення задирок різьбовий трубний компонент і спосіб нанесення покриття на зазначений компонент
Наступний патент: Похідні 2,6-діарил-7-гідрокси-5-(2-гідроксифеніл)-4,5,6,7-тетрагідропіразоло[1,5-а]піримідин-7-карбонової кислоти та спосіб їх одержання
Випадковий патент: Дисковий кристалізатор












