1,4-дизаміщені аналоги піридазину та способи лікування пов’язаних з дефіцитом smn станів
Номер патенту: 114726
Опубліковано: 25.07.2017
Автори: Керріган Джон, Санг Му, Сан Роберт, Фазаль Алім, Цзінь Донован Ноель, Херлі Тімоті Брайєн, Дейлз Наталі, Чун Етвуд, Шу Лей, О'Браєн Гері
Формула / Реферат
1. Сполука або її сіль згідно з формулою (І):
 , (I)
, (I)
де
А являє собою 2-гідроксифеніл, який заміщений 0, 1, 2 або 3 замісниками, незалежно вибраними з С1-С4алкілу, де 2 С1-С4алкільні групи можуть бути з'єднані з атомами, з якими вони зв'язані, з утворенням 5-6-членного кільця, та заміщений 0 або 1 замісником, вибраним з оксо, оксиму та гідрокси, галоген-С1-С4алкілу, дигалоген-С1-С4алкілу, тригалоген-С1-С4алкілу, С1-С4алкокси, С1-С4алкокси-С3-С7циклоалкілу, галоген-С1-С4алкокси, дигалоген-С1-С4алкокси, тригалоген-С1-С4алкокси, гідрокси, ціано, галогену, аміно, моно- та ді-С1-С4алкіламіно, гетероарилу, С1-С4алкілу, заміщеного гідрокси, С1-С4алкокси, заміщеного арилом, аміно, -С(О)NHС1-С4алкілгетероарилом, -NHC(O)-С1-С4алкілгетероарилом, С1-С4алкілС(О)NН-гетероарилом, С1-С4алкілNHС(О)-гетероарилом, 3-7-членним циклоалкілом, 5-7-членним циклоалкенілом або 5-, 6- або 9-членним гетероциклом, що містить 1 або 2 гетероатоми, незалежно вибрані з S, О та N, де гетероарил містить 5, 6 або 9 кільцевих атомів, 1, 2 або 3 кільцеві гетероатоми, вибрані з N, О та S, та заміщений 0, 1 або 2 замісниками, незалежно вибраними з оксо, гідрокси, нітро, галогену, С1-С4алкілу, С1-С4алкенілу, С1-С4алкокси, С3-С7циклоалкілу, С1-С4алкіл-ОН, тригалоген-С1-С4алкілу, моно- та ді-С1-С4алкіламіно, -C(O)NH2, -NH2, -NO2, гідроксі-С1-С4алкіламіно, гідроксі-С1-С4алкілу, 4-7-членний гетероцикл-С1-С4алкілу, аміноС1-С4алкілу та моно- та ді-С1-С4алкіламіноС1-С4алкілу; або
де В вибирають з групи, що складається з
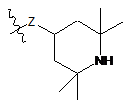 ,
, 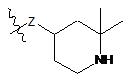 ,
, 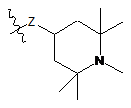 ,
, 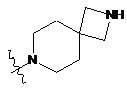 ,
,
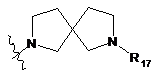 ,
, 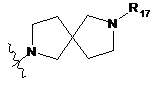 ,
, 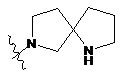 ,
,  та
та
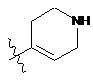 ,
,
де Z являє собою О або N(Me); та
R17 являє собою водень або метил.
2. Сполука за п. 1 або її сіль, де А являє собою 2-гідроксифеніл, який заміщений 0, 1, 2 або 3 замісниками, незалежно вибраними з С1-С4алкілу, галоген-С1-С4алкіл-С1-С4алкокси, гідрокси, ціано, галогену, аміно, моно- та ді-С1-С4алкіламіно, гетероарилу та С1-С4алкілу, заміщеного гідрокси або аміно, причому гетероарил містить 5 або 6 кільцевих атомів, 1 або 2 кільцеві гетероатоми, вибрані з N, О та S, та заміщений 0, 1 або 2 замісниками, незалежно вибраними з С1-С4алкілу, моно- та ді-С1-С4алкіламіно, гідроксі-С1-С4алкіламіно, гідроксі-С1-С4алкілу, 4-7-членний гетероцикл-С1-С4алкілу, аміно-С1-С4алкілу та моно- та ді-С1-С4алкіламіно-С1-С4алкілу.
3. Сполука за п. 1 або п. 2 або її сіль, де сполука представлена формулою (III):
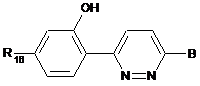 , (III)
, (III)
де R16 являє собою 5-членний гетероарил, який містить один кільцевий атом азоту та 0 або 1 додатковий кільцевий гетероатом, вибраний з N, О або S, де гетероарил необов'язково заміщений С1-С4алкілом.
4. Сполука або її сіль за будь-яким із пп. 1-3, де В являє собою:
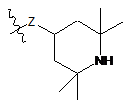 .
.
5. Сполука або її сіль за будь-яким із пп. 1, 2, 3 або 4, де R16 являє собою:
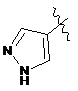 .
.
6. Сполука або її сіль за п. 1, де сполука має формулу (IV):
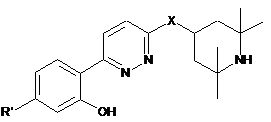 , (IV)
, (IV)
де X являє собою -О- або 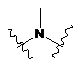 ;
;
R' являє собою 5-членний гетероарил, необов'язково заміщений 0, 1 або 2 групами, вибраними з оксо, гідрокси, нітро, галогену, С1-С4алкілу, С1-С4алкенілу, С1-С4алкокси, С3-С7циклоалкілу, С1-С4алкіл-ОН, тригалоген-С1-С4алкілу, моно- та ді-С1-С4алкіламіно, -C(O)NH2, -NH2, -NO2, гідроксі-С1-С4алкіламіно, гідроксі-С1-С4алкілу, 4-7-членний гетероцикл-С1-С4алкілу, аміно-С1-С4алкілу та моно- та ді-С1-С4алкіламіно-С1-С4алкілу.
7. Сполука або її сіль за п. 1, вибрана з групи, що складається з
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-хлор-2-(6-(метил(1,2,2,6,6-пентаметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
4-гідрокси-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)бензонітрилу;
2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}-4-трифторметилфенолу;
2-фтор-6-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу;
3,5-диметокси-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу;
4,5-диметокси-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу;
5-метокси-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу;
4,5-дифтор-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу;
5-фтор-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу;
3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)бензонітрилу;
N-аліл-3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)бензаміду;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу;
5-(5-метилоксазол-2-іл)-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу;
5-(4-гідроксиметил-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(1H-імідазол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(4-аміно-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(4-аміно-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(3-амінопіразол-1-іл)-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-(2-морфоліноетил)-1H-піразол-4-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-піразол-4-іл)фенолу;
5-(5-аміно-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-1-іл)фенолу;
2-(6-(піперидин-4-ілокси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу;
2-(6-(((2S,4R,6R)-2,6-диметилпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу;
5-(1H-піразол-1-іл)-2-(6-(піролідин-3-ілокси)піридазин-3-іл)фенолу;
2-(6-((-2-метилпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу;
(S)-5-(1H-піразол-1-іл)-2-(6-(піролідин-3-ілметокси)піридазин-3-іл)фенолу;
(R)-5-(1H-піразол-1-іл)-2-(6-(піролідин-3-ілметокси)піридазин-3-іл)фенолу;
2-(6-((3-фторпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу;
2-[6-(1,2,2,6,6-пентаметилпіперидин-4-ілокси)піридазин-3-іл]-5-піразол-1-ілфенолу;
5-піразол-1-іл-2-[6-(2,2,6,6-тетраметилпіперидин-4-ілокси)піридазин-3-іл]фенолу;
5-(1H-піразол-4-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4-іл)фенолу;
2-[6-(7-метил-2,7-діазаспіро[4.4]нон-2-іл)піридазин-3-іл]-5-піразол-1-ілфенолу;
2-[6-(2,7-діазаспіро[3.5]нон-7-іл)піридазин-3-іл]-5-піразол-1-ілфенолу;
2-[6-(1,7-діазаспіро[4.4]нон-7-іл)піридазин-3-іл]-5-піразол-1-ілфенолу;
2-(6-((3aR,6aS)-гексагідропіроло[3,4-c]пірол-2(1H)-іл)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу;
5-піразол-1-іл-2-[6-(1,2,3,6-тетрагідропіридин-4-іл)піридазин-3-іл]фенолу;
3-метокси-2-(6-(метил(2,2,6-триметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5-метилоксазол-2-іл)фенолу;
2-(6-((6S)-6-((S)-1-гідроксіетил)-2,2-диметилпіперидин-4-ілокси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4-іл)бензол-1,3-діолу;
3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-піразол-4-іл)-3-(трифторметокси)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4-іл)-3-(трифторметокси)фенолу;
4-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(трифторметокси)феніл)-1-метилпіридин-2(1H)-ону;
3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-піразол-4-іл)фенолу;
3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5,6,7,8-тетрагідроімідазо[1,2-a]піридин-3-іл)фенолу;
3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(піридин-3-іл)фенолу;
5-(1-циклопентил-1H-піразол-4-іл)-3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
3',5-диметокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-[1,1'-біфеніл]-3-олу;
3-(бензилокси)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5-метилоксазол-2-іл)фенолу;
3-етокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5-метилоксазол-2-іл)фенолу;
3-(циклопропілметокси)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5-метилоксазол-2-іл)фенолу;
2-метил-5-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-1H-бензо[d]імідазол-6-олу;
5-хлор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
2-(6-((2,2-диметилпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-4-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(4,5,6,7-тетрагідропіразоло[1,5-a]піразин-3-іл)фенолу;
4-(1H-індол-2-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
4-(циклопент-1-ен-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-3-іл)фенолу;
4-(4-гідрокси-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)піридин-2-олу;
4-(4-гідрокси-3-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону;
4-(4-гідрокси-3-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)феніл)піридин-2-олу;
5-(1H-індазол-7-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
4-хлор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4-іл)фенолу;
4-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4-іл)фенолу;
5-фтор-4-(1H-імідазол-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-4-іл)фенолу;
5-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-5-іл)фенолу;
гідрохлориду 9-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5,6-дигідроімідазо[5,1-a]ізохінолін-8-олу;
4-гідрокси-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-N-((1-метил-1H-піразол-4-іл)метил)бензаміду;
4-(4-(гідроксиметил)-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
гідрохлориду 3-фтор-5-(2-метоксипіридин-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
гідрохлориду 4-(3-фтор-5-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)піридин-2(1H)-ону;
гідрохлориду 4-(3-фтор-5-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону;
гідрохлориду 5-(3-фтор-5-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону;
гідрохлориду 3-фтор-5-(1H-піразол-4-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)фенолу;
гідрохлориду 5-хлор-3-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
гідрохлориду 3-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4-іл)фенолу;
гідрохлориду 3-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-піразол-4-іл)фенолу;
5-(5-метоксипіридин-3-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)піридин-2-олу;
4-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)піридин-2-олу;
5-(6-метоксипіридин-3-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-3-(трифторметил)піридин-2-олу;
5-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону;
4-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону;
5-(2-метоксипіридин-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
4-(3-гідрокси-4-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)феніл)піридин-2-олу;
5-(6-(диметиламіно)піридин-3-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
4-(3-гідрокси-4-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(піримідин-5-іл)фенолу;
5-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)піридин-3-олу;
1-циклопропіл-4-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)піридин-2(1H)-ону;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1,2,3,6-тетрагідропіридин-4-іл)фенолу;
5-(циклопент-1-ен-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(3,6-дигідро-2H-піран-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(імідазо[1,5-a]піридин-7-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(імідазо[1,2-a]піридин-7-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(2-метилпіридин-4-іл)фенолу;
5-(1H-імідазол-2-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(1H-імідазол-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
5-(імідазо[1,2-a]піразин-3-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5,6,7,8-тетрагідроімідазо[1,2-a]піразин-3-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(4-метил-1H-імідазол-2-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-імідазол-4-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-імідазол-5-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(4-нітро-1H-імідазол-2-іл)фенолу;
2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(2-метил-1H-імідазол-4-іл)фенолу;
5-(1,2-диметил-1H-імідазол-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу;
1-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-1H-піразол-4-карбоксаміду;
2-(6-((3aR,6aS)-5-метилгексагідропіроло[3,4-c]пірол-2(1H)-іл)піридазин-3-іл)-5-(1H-піразол-4-іл)фенолу;
4-(3-гідрокси-4-(6-(5-метилгексагідропіроло[3,4-c]пірол-2(1H)-іл)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону.
8. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за будь-яким з пп. 1-7 або її фармацевтично прийнятної солі та один або декілька фармацевтично прийнятних носіїв.
9. Комбінація, яка включає у себе терапевтично ефективну кількість сполуки за будь-яким з пп. 1-7 або її фармацевтично прийнятної солі та один або декілька фармацевтично активних співагентів.
10. Спосіб лікування, профілактики або зменшення інтенсивності пов'язаного з дефіцитом SMN стану, що включає введення суб'єкту, який цього потребує, ефективної кількості сполуки або її солі за будь-яким з пп. 1-7.
11. Спосіб за п. 10, де зазначений пов'язаний з дефіцитом SMN стан являє собою спінальну м'язову атрофію.
12. Сполука або її сіль 5-(1Н-піразол-4-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)фенол, яка представлена формулою:
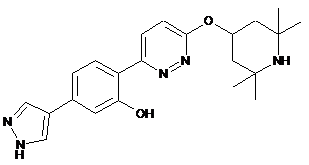 .
.
13. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за п. 12 або її фармацевтично прийнятної солі та один або декілька фармацевтично прийнятних носіїв.
14. Комбінація, яка включає у себе терапевтично ефективну кількість сполуки за п. 12 або її фармацевтично прийнятної солі та один або декілька фармацевтично активних співагентів.
15. Спосіб лікування, профілактики або зменшення інтенсивності пов'язаного з дефіцитом SMN стану, що включає введення суб'єкту, який цього потребує, ефективної кількості сполуки або її солі за п. 12.
16. Спосіб за п. 15, де зазначений пов'язаний з дефіцитом SMN стан являє собою спінальну м'язову атрофію.
17. Сполука або її сіль 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1Н-піразол-4-іл)фенол, яка представлена формулою:
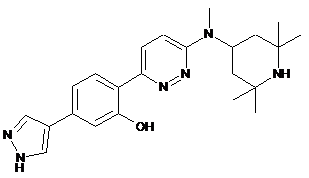 .
.
18. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за п. 17 або її фармацевтично прийнятної солі та один або декілька фармацевтично прийнятних носіїв.
19. Комбінація, яка включає у себе терапевтично ефективну кількість сполуки за п. 17 або її фармацевтично прийнятної солі та один або декілька фармацевтично активних співагентів.
20. Спосіб лікування, профілактики або зменшення інтенсивності пов'язаного з дефіцитом SMN стану, що включає введення суб'єкту, який цього потребує, ефективної кількості сполуки або її солі за п. 17.
21. Спосіб за п. 20, де зазначений пов'язаний з дефіцитом SMN стан являє собою спінальну м'язову атрофію.
Текст
УКРАЇНА (19) UA (51) МПК (11) 114726 (13) C2 (2017.01) C07D 401/14 (2006.01) C07D 405/14 (2006.01) C07D 413/14 (2006.01) C07D 401/12 (2006.01) C07D 403/14 (2006.01) C07D 409/14 (2006.01) C07D 417/14 (2006.01) C07D 471/14 (2006.01) C07D 471/04 (2006.01) C07D 471/08 (2006.01) C07D 487/04 (2006.01) C07D 487/10 (2006.01) A61K 31/501 (2006.01) A61P 21/00 МІНІСТЕРСТВО ЕКОНОМІЧНОГО РОЗВИТКУ І ТОРГІВЛІ УКРАЇНИ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (21) Номер заявки: a 2015 00562 (22) Дата подання заявки: 13.08.2013 (24) Дата, з якої є чинними 25.07.2017 права на винахід: (31) Номер попередньої 61/682,448 (32) Дата подання 13.08.2012 заявки відповідно до Паризької конвенції: попередньої заявки відповідно до Паризької конвенції: (33) Код держави-учасниці US Паризької конвенції, до якої подано попередню заявку: (41) Публікація відомостей 10.07.2015, Бюл.№ 13 про заявку: (46) Публікація відомостей 25.07.2017, Бюл.№ 14 про видачу патенту: (86) Номер та дата подання міжнародної заявки, поданої відповідно до Договору PCT PCT/US2013/054687, 13.08.2013 (72) Винахідник(и): Чун Етвуд (US/US), Цзінь Донован Ноель (US/US), Дейлз Наталі (US/US), Фазаль Алім (US/US), Херлі Тімоті Брайєн (US/US), Керріган Джон (US/US), О'Браєн Гері (CA/US), Шу Лей (CN/US), Сан Роберт (US/US), Санг Му (KR/US) (73) Власник(и): НОВАРТІС АГ, Lichtstrasse 35, CH-4056 Basel, Switzerland (CH) (74) Представник: Ошарова Iрина Олександрiвна, реєстр. №9 (56) Перелік документів, взятих до уваги експертизою: WO 2011/130515 A1, 20.10.2011 WO 2011/133882 A1, 27.10.2011 WO 2007/003604 A2, 11.01.2007 EP 2 014 656 A2, 14.01.2009 WO 2007/133561 A2, 22.11.2007 WO 2004/043960 A1, 27.05.2004 WO 2007/137030 A2, 29.11.2007 DATABASE REGISTRY, CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US, Database accession no. 1330184-80-9, XP002716119 [X] 1-2,5 * abstract * AKIO OHSAWA, YOSHIHITO ABE, HIROSHI IGETA, "Cross-Coupling Reaction of Chloropyridazines and Grignard Reagents with Nickel-phosphine Complexes: Alkylation and Arylation of Pyridazines", CHEMICAL AND PHARMACEUTICAL BULLETIN (1978), vol. 26, no. 8, pages 2550-2554 PETRENKO O. P. ET AL., "Effect of an intramolecular hydrogen bond on the rate of nucleophilic substitution in a series of haloazines", DATABASE CA, CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US, Database accession no. 1981:191211, URL: STN, XP002716255 [X] 1,3,6 * abstract * * Compound with the Registry Number 7758598-9 * UA 114726 C2 (12) UA 114726 C2 (54) 1,4-ДИЗАМІЩЕНІ АНАЛОГИ ПІРИДАЗИНУ ТА СПОСОБИ ЛІКУВАННЯ ПОВ'ЯЗАНИХ З ДЕФІЦИТОМ SMN СТАНІВ (57) Реферат: Даний винахід стосується сполуки формули І або її фармацевтично прийнятної солі: A B N N , (I) способу одержання сполук згідно з даним винаходом та їх застосувань у терапії. Даний винахід також стосується комбінації фармацевтично активних засобів та фармацевтичної композиції. UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 Передумови створення даного винаходу Проксимальна спінальна м'язова атрофія (SMA) являє собою спадкову, клінічно гетерогенну групу нейром'язових порушень, що характеризуються дегенерацією клітин переднього рогу спинного мозку. Пацієнти страждають від симетричної слабкості м'язів тулуба та кінцівок, причому ноги є ураженими більшою мірою, ніж руки, а проксимальні м'язи є більш слабкими, ніж дистальні; діафрагма, м'язи обличчя та ока не зачіпаються. Існують три форми SMA з початком у дитячому віці (типи I, II та III) та порівняно нещодавно виділена форма IV з початком у зрілому віці, які всі можуть бути диференційовані на підставі віку початку захворювання та важкості клінічного перебігу хвороби, оцінюваного за допомогою клінічного огляду, м'язової біопсії та електроміографії (EMG) (Munsat T. L., Davies K. E. (1992)). Тип I (хвороба Вердніга-Гофмана) являє собою найбільш гостру та важку форму з початком хвороби до досягнення 6 місяців та смертю, як правило, протягом двох років; діти ніколи не здатні сидіти без підтримки. Симптоми захворювання можуть відзначатися під час вагітності у вигляді зниження рухів плода; під час народження; або, найчастіше, протягом перших чотирьох місяців життя. Уражені захворюванням діти виражено пасивні, зазнають труднощів з харчуванням та діафрагмальним диханням та характеризуються загальною слабістю у міжреберних та додаткових респіраторних м'язах. Уражені захворюванням діти ніколи не сідають та не стоять, та звичайно гинуть до досягнення віку 2 років; смерть, як правило, пов'язана з респіраторною недостатністю. Тип II (проміжна, хронічна форма) починається у віці між шістьма та вісімнадцятьома місяцями; характерні м'язові фасцикуляції, та сухожильні рефлекси прогресивно знижуються. Діти не здатні стояти або ходити без підтримки. Проблеми з харчуванням та ковтанням не завжди присутні при SMA типу II, хоча деяким пацієнтам може бути необхідна живильна трубка. У більшості пацієнтів, як правило, розвивається прогресуючий м'язовий сколіоз, який може потребувати хірургічної корекції. Подібно пацієнтам із захворюванням I типу, очищення трахеальних виділень та кашель можуть стати утрудненими внаслідок слабкої бульбарної функції та слабких міжреберних м'язів. Такі пацієнти характеризуються вираженою гіпотонією, симетричним атонічним паралічем та відсутністю контролю рухів голови. Тип III (хвороба Кугельберга-Веландера або ювенільна спінальна м'язова атрофія) являє собою м'яку, хронічну форму з початком захворювання у віці старше 18 місяців; етапи розвитку моторних нейронів є нормальними, та ходіння може бути збережене до різного віку. У таких пацієнтів часто розвивається сколіоз, та часто спостерігаються симптоми перевантаження суглобів, звичайно викликані слабістю. Прогнозована тривалість життя практично відповідає нормальній, але якість життя суттєво знижена. Типи I, II та III прогресують із часом, супроводжуючись погіршенням стану пацієнта. Тип IV з початком у зрілому віці характеризується слабістю у другій або третій декаді життя з м'яким моторним порушенням, що не супроводжуються респіраторними проблемами або проблемами з харчуванням. SMA дорослих характеризується непомітним початком та дуже повільним прогресуванням. Бульбарні м'язи рідко уражуються при типі IV. Не з'ясовано, чи пов'язана етіологічно SMA типу IV з формами типу I-III. Інші форми спінальної м'язової атрофії містять у собі Х-хромосомне захворювання, спінальну м'язову атрофію з респіраторним дистрес-синдромом (SMARD), спінальну та бульбарну м'язову атрофію (хвороба Кеннеді або бульбо-спінальна м'язова атрофія) та дистальну спінальну м'язову атрофію. SMA обумовлена мутаціями у гені виживання рухового нейрону (SMN), який є присутнім у людей у двох формах (SMN1 та SMN2). Втрата SMN є руйнівною для рухових нейронів та приводить до нейром'язової недостатності, відмінної риси цього захворювання. З генетичної точки зору, SMA являє собою аутосомно-рецесивний стан, викликаний порушенням гену SMN1, розташованого у 5q13 (Lefebvre S., et al. (1995) Cell 80:155-165). Більше ніж у 98 % пацієнтів зі спінальною м'язовою атрофією присутнє гомозиготне порушення гену SMN1 за допомогою делеції, перебудови або мутації. Проте, усі ці пацієнти зберігають, щонайменше, одну копію гену SMN2. На геномному рівні було виявлено, що тільки п'ять нуклеотидів відрізняють ген SMN1 від гену SMN2. Крім того, ці два гени продукують ідентичні мРНК за винятком нуклеотидної заміни, що мовчить, у екзоні 7, тобто C→T заміна шести пар основ всередині екзону 7 у гені SMN2. Ця мутація модулює активність підсилювача сплайсингу екзонів (Lorson and Androphy (2000) Hum. Mol. Genet. 9:259-265). Результатом цього та інших нуклеотидних замін у інтронних та промоторних областях є те, що більшість генів SMN2 зазнають альтернативного сплайсингу, та у їх транскриптах не вистачає екзонів 3, 5 або 7. Навпаки, мРНК, що транскрибується з гену SMN1, як правило, являє собою повнорозмірну мРНК лише з невеликою фракцією її 1 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 транскриптів, сплайсованих з видаленням екзонів 3, 5 або 7 (Gennarelli et al. (1995) Biochem. Biophys. Res. Commun. 213:342-348; Jong et al. (2000) J. Neurol. Sci. 173:147-153). У всіх суб'єктів з SMA є, щонайменше, одна та, як правило, дві-чотири копії гену SMN2, який кодує той самий білок, що і ген SMN1; однак ген SMN2 продукує тільки низькі рівні повнорозмірного SMN білку. Білок SMN∆7 є нефункціональним та вважається швидко деградуючим. Приблизно 10 % пре-мРНК SMN2 сплайсується правильно та транслюється надалі у повнорозмірний білок SMN (FL-SMN), а частина, що залишилася, являє собою SMN∆7 копію. Ефективність сплайсингу SMN2 може залежати від важкості захворювання, та продукція повнорозмірного транскрипту SMN2 може варіюватися від 10 % до 50 %. Крім того, присутність або відсутність гену SMN1, приблизно 90 % якого стає FL-SMN продуктом гену або білком, впливає на важкість SMA залежно від того, чи може воно компенсувати обрізані копії SMN∆7. Низький рівень білку SMN уможливлює ембріональний розвиток, але не є достатнім для підтримки виживання рухових нейронів у спинному мозку. Клінічна важкість пацієнтів з SMA зворотно корелює із числом генів SMN2 та з рівнем продукованого функціонального білку SMN (Lorson C. L., et al. (1999) PNAS; 96:6307-6311)(Vitali T. et al. (1999) Hum Mol Genet; 8:2525-2532)(Brahe C. (2000) Neuromusc. Disord.; 10:274275)(Feldkotter M., et al. (2002) Am J Hum Genet; 70:358-368)(Lefebvre S., et al. (1997) Nature Genet; 16:265-269)(Coovert D. D., et al. (1997) Hum Mol Genet; 6:1205-1214)(Patrizi A. L., et al. (1999) Eur J Hum Genet; 7:301-309). Сучасні стратегії терапії SMA в основному зосереджені на збільшенні рівнів повнорозмірного білку SMN (білку дикого типу), модулюванні сплайсингу на користь включення екзону 7, стабілізації білку дикого типу та, меншою мірою, на відновленні м'язової функції при SMA шляхом забезпечення трофічної підтримки або шляхом інгібування атрофії скелетних м'язів. Механізм, що веде до втрати мотонейрону та м'язової атрофії, дотепер залишається неясним, хоча доступність моделей такого захворювання на тваринах сприяє швидкому збільшенню знань у цій області (Frugier T., et al. (2000) Hum Mol. Genet. 9:849-58; Monani U. R., et al. (2000) Hum Mol Genet 9:333-9; Hsieh-Li H. M., et al. (2000) Nat Genet 24:66-70; Jablonka S., et al. (2000) Hum Mol. Genet. 9:341-6). Функція білку SMN дотепер також частково не відома, та дослідження вказують на його можливе залучення у метаболізм мРНК (Meister G., et al. (2002). Trends Cell Biol. 12:472-8; Pellizzoni L., et al. (2002). Science. 298:1775-9), та, можливо, у транспорт білків/мРНК до нейром'язових синапсів (Ci-fuentes-Diaz C., et al. (2002) Hum Mol. Genet. 11:1439-47; Chan Y. B., et al. (2003) Hum Mol. Genet. 12:1367-76; McWhorter M. L., et al. (2003) J. Cell Biol. 162:919-31; Rossoll W., et al. (2003) J. Cell Biol. 163:801-812). На додаток до типів SMA, окремо повідомлялося про залучення делеції гену SMN1 у вроджений множинний артрогрипоз нейрогенного типу (вроджений AMC), наводячи на думку, що певний рівень патології у хворих, очевидно, пов'язаний з низькими рівнями SMN у рухових нейронах (L. Burgien et al., (1996) J. Clin. Invest. 98(5):1130-32). Вроджений AMC уражує людей та тварин, наприклад, коней, велику рогату худобу, овець, кіз, свиней, собак та кішок (M. Longeri et al., (2003) Genet. Sel. Evol. 35:S167-S175). Також було виявлено, що ризик розвитку або важкість бічного аміотрофічного склерозу (ALS) корелює з низькими рівнями SMN у рухових нейронах. На сьогоднішній день не існує доступного лікування SMA, а тому було б корисно надати нові способи модулювання SMN для лікування хворих, що страждають на SMA, вроджений нейрогенний AMC, ALS або інші пов'язані з дефіцитом SMN стани. Також було б корисно надати нові лікарські мішені, які могли б бути використані як основа для розробки ефективних терапевтичних або діагностичних засобів для таких нейрональних станів. Короткий опис даного винаходу Існує потреба у нових способах лікування та видах терапії спінальної м'язової атрофії. Даний винахід відноситься до сполук, їх солей, їх фармацевтичних лікарських форм та їх комбінацій, причому сполуки є модуляторами спінальної м'язової атрофії. Даний винахід також відноситься до способів лікування, профілактики або зменшення інтенсивності спінальної м'язової атрофії, що включають введення суб'єктові, який цього потребує, ефективної кількості модулятору SMN (наприклад, сполуки згідно із даним винаходом). Різні варіанти здійснення даного винаходу описані у даному документі. Слід розуміти, що характерні риси, визначені у кожному варіанті здійснення, можуть бути сполучені з іншими певними характерними рисами для одержання інших варіантів здійснення. У контексті певних аспектів, модулятори SMN, представлені у даному документі, являють собою сполуки формули I та їх солі: 2 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 (I) Згідно з іншим варіантом здійснення, даний винахід відноситься до фармацевтичної композиції, що містить терапевтично ефективну кількість сполуки згідно з визначенням формули (I) або її підформул та один або декілька фармацевтично прийнятних носіїв. Згідно з іншим варіантом здійснення, даний винахід відноситься до комбінації, зокрема до фармацевтичної комбінації, що включає у себе терапевтично ефективну кількість сполуки згідно з визначенням формули (I) або її субформул, та один або декілька терапевтично активних співагентів. Одним варіантом здійснення даного винаходу є надання способу лікування, профілактики або зменшення інтенсивності зв'язаного з дефіцитом SMN стану, який включає введення суб'єкту, який цього потребує, ефективної кількості модулятору SMN або фармацевтичної композиції, що містить його. Інший варіант здійснення даного винаходу являє собою спосіб модулювання SMN білку шляхом введення модулятору SMN. Згідно з іншим варіантом здійснення, згаданий модулятор SMN здатен збільшувати вмісти одного або декількох з FL-SMN або SMN∆7. Згідно з іншим варіантом здійснення, згаданий модулятор SMN здатен попереджати вирізання екзону 7 з транскрипту під час сплайсингу. Даний винахід оснований на відкриття, що модулятори SMN згідно з даним винаходом (наприклад, сполуки формули (I) та/або сполуки формули (I-A)) здатні модулювати білки SMN, наприклад, шляхом активації промотору SMN, модулювання сплайсингу (наприклад, попередження вирізання екзону 7 з гену SMN під час сплайсингу) та/або модулювання стабільності білку SMN. Детальний опис даного винаходу Як відмічено вище, даний винахід відноситься до сполук, які модулюють активність SMN. Такі сполуки можуть використовуватися in vitro або in vivo для модулювання (переважно, збільшення) продукції та активності SMN у цілому ряді випадків. Згідно з першим варіантом здійснення, даний винахід відноситься до сполук формули I та їх фармацевтично прийнятних солей, які модулюють SMN активність. Сполуки формули I представлені структурою: Згідно з першим варіантом здійснення, даний винахід відноситься до сполук або їх солей (переважно їх фармацевтично прийнятних солей) у відповідності з формулою (I). (I) A являє собою 2-гідроксифеніл, який заміщений 0, 1, 2 або 3 замісниками, незалежно вибраними з C1-C4алкілу, де 2 C1-C4алкільні групи можуть бути з'єднані з атомами, з якими вони зв'язані, з утворенням 5-6-членного кільця, та заміщений 0 або 1 замісником, вибраним з оксо, оксиму та гідрокси, галогенC1-C4алкілу, дигалогенC1-C4алкілу, тригалогенC1-C4алкілу, C1C4алкокси, C1-C4алкокси-C3-C7циклоалкілу, галогенC1-C4алкокси, дигалогенC1-C4алкокси, тригалогенC1-C4алкокси, гідрокси, ціано, галогену, аміно, моно- та ди-C1-C4алкіламіно, гетероарилу, C1-C4алкілу, заміщеного гідрокси, C1-C4алкокси, заміщеного арилом, аміно, C(O)NHC1-C4алкілгетероарилом, -NHC(O)-C1-C4алкілгетероарилом, C1-C4алкілC(O)NHгетероарилом, C1-C4алкілNHC(O)-гетероарилом, 3-7-членним циклоалкілом, 5-7-членним циклоалкенілом або 5-, 6- або 9-членним гетероциклом, що містить 1 або 2 гетероатоми, незалежно вибрані з S, O та N, де гетероарил містить 5, 6 або 9 кільцевих атомів, 1, 2 або 3 кільцеві гетероатоми, вибрані з N, O та S, та заміщений 0, 1 або 2 замісниками, незалежно вибраними з оксо, гідрокси, нітро, галогену, C1-C4алкілу, C1-C4алкенілу, C1-C4алкокси, C3C7циклоалкілу, C1-C4алкіл-OH, тригалогенC1-C4алкілу, моно- та ди-C1-C4алкіламіно, -C(O)NH2, NH2, -NO2, гідроксиC1-C4алкіламіно, гідроксиC1-C4алкілу, 4-7-членний гетероцикл-C1-C4алкілу, аміноC1-C4алкілу та моно- та ди-C1-C4алкіламіноC1-C4алкілу; або A являє собою 2-нафтил, необов'язково заміщений гідрокси по 3-положенню та додатково заміщений 0, 1 або 2 замісниками, вибраними з гідрокси, ціано, галогену, C1-C4алкілу, C2-C4алкенілу, C1-C5алкокси, де алкокси є незаміщеним або заміщеним гідрокси, C 1-C4алкокси, аміно, N(H)C(O)C1-C4алкілом, N(H)C(O)2-C1-C4алкілом, алкілен-4-7-членним гетероциклом, 4-7-членним гетероциклом та 3 UA 114726 C2 5 10 15 20 25 30 35 40 моно- та ди-C1-C4алкіламіно; або A являє собою 6-членний гетероарил, який містить 1-3 кільцеві атоми азоту, причому 6-членний гетероарил заміщений фенілом або гетероарилом, що містить 5 або 6 кільцевих атомів, 1 або 2 кільцеві гетероатоми, незалежно вибрані з N, O та S, та заміщений 0, 1 або 2 замісниками, незалежно вибраними з C 1-C4алкілу, моно- та ди-C1C4алкіламіно, гідроксиC1-C4алкіламіно, гідроксиC1-C4алкілу, аміноC1-C4алкілу та моно- та ди-C1C4алкіламіноC1-C4алкілу; або A являє собою біциклічний гетероарил, який містить від 9 до 10 кільцевих атомів та 1, 2 або 3 кільцеві гетероатоми, незалежно вибрані з N, O або S, де біциклічний гетероарил заміщений 0, 1 або 2 замісниками, незалежно вибраними з ціано, галогену, гідрокси, C1-C4алкілу, C2-C4алкенілу, C2-C4алкінілу, C1-C4алкокси та C1-C4алкокси, заміщеного гідрокси, C1-C4алкокси, аміно та моно- та ди-C1-C4алкіламіно; або A являє собою трициклічний гетероарил, який містить 12 або 13 кільцевих атомів та 1, 2 або 3 кільцеві гетероатоми, незалежно вибрані з N, O або S, причому трициклічний гетероарил заміщений 0, 1 або 2 замісниками, незалежно вибраними з ціано, галогену, гідрокси, C 1-C4алкілу, C2C4алкенілу, C2-C4алкінілу, C1-C4алкокси, C1-C4алкокси, заміщеного гідрокси, C1-C4алкокси, аміно, моно- та ди-C1-C4алкіламіно та гетероарилом, де зазначений гетероарил містить 5, 6 або 9 кільцевих атомів, 1, 2 або 3 кільцеві гетероатоми, вибрані з N, O та S, та заміщений 0, 1 або 2 замісниками, незалежно вибраними з оксо, гідрокси, нітро, галогену, C 1-C4алкілу, C1-C4алкенілу, C1-C4алкокси, C3-C7циклоалкілу, C1-C4алкіл-OH, тригалогенC1-C4алкілу, моно- та ди-C1C4алкіламіно, -C(O)NH2, -NH2, -NO2, гідроксиC1-C4алкіламіно, гідроксиC1-C4алкілу, 4-7-членний гетероцикл-C1-C4алкілу, аміноC1-C4алкілу та моно- та ди-C1-C4алкіламіноC1-C4алкілу; B являє собою групу формули: , де m, n та p незалежно вибирають з 0 або 1; R, R1, R2, R3 та R4 незалежно вибирають з групи, що складається з водню, C1-C4алкілу, причому алкіл необов'язково заміщений гідрокси, аміно або моно- та ди-C1-C4алкіламіно; R5 та R6 незалежно вибирають з водню та фтору; або R та R3 утворюють разом конденсоване 5- або 6-членне гетероциклічне кільце, яке містить 0 або 1 додатковий кільцевий гетероатом, вибраний з N, O або S; R 1 та R3 утворюють разом C1C3алкіленову групу; R1 та R5 утворюють разом C1-C3алкіленову групу; R3 та R4 утворюють разом з атомом вуглецю, до якого вони приєднані, спіроцикл-C3-C6циклоалкіл; X являє собою CRARB, O, NR7 або зв'язок; R7 являє собою водень або C1-C4алкіл; RA та RB незалежно вибирають з водню та C1-C4алкілу, або RA та RB утворюють разом двовалентну C2-C5алкіленову групу; Z являє собою CR8 або N; якщо Z являє собою N, тоді X являє собою зв'язок; R8 являє собою водень або утворює разом з R6 подвійний зв'язок; або B являє собою групу формули: , де p та q незалежно вибирають з групи, що містить 0, 1 та 2; R 9 та R13 незалежно вибирають з водню та C1-C4алкілу; R10 та R14 незалежно вибирають з водню, аміно, моно- та ди-C1C4алкіламіно та C1-C4алкілу, причому алкіл необов'язково заміщений гідрокси, аміно або монота ди-C1-C4алкіламіно; R11 являє собою водень, C1-C4алкіл, аміно або моно- та ди-C1C4алкіламіно; R12 являє собою водень або C1-C4алкіл; або R9 та R11 утворюють разом насичений азацикл, який містить від 4 до 7 кільцевих атомів, який необов'язково заміщений 1-3 C1C4алкільними групами; або R11 та R12 утворюють разом насичений азацикл, який містить від 4 до 7 кільцевих атомів, який необов'язково заміщений 1-3 C1-C4алкільними групами. 4 UA 114726 C2 5 10 15 20 25 30 35 40 Згідно з другим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим варіантом здійснення або її солі, де A являє собою 6-членний гетероарил, який містить 1-3 кільцеві атоми азоту, причому 6-членний гетероарил заміщений фенілом або гетероарилом, що містить 5 або 6 кільцевих атомів, 1 або 2 кільцеві гетероатоми, незалежно вибрані з N, O та S, та заміщений 0, 1 або 2 замісниками, незалежно вибраними з C1-C4алкілу, моно- та ди-C1-C4алкіламіно, гідроксиC1-C4алкіламіно, гідроксиC1-C4алкілу, аміноC1-C4алкілу та моно- та ди-C1-C4алкіламіноC1-C4алкілу; або A являє собою біциклічний гетероарил, який містить від 9 до 10 кільцевих атомів та 1, 2 або 3 кільцеві гетероатоми, незалежно вибрані з N, O або S, причому гетероарил заміщений 0, 1 або 2 замісниками, незалежно вибраними з ціано, галогену, гідрокси, C1-C4алкілу, C2-C4алкенілу, C2-C4алкінілу, C1-C4алкокси та C1-C4алкокси, заміщеного гідрокси, C1-C4алкокси, аміно та моно- та ди-C1-C4алкіламіно. Згідно з третім варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим варіантом здійснення або її солі, де A являє собою 2-гідроксифеніл, який заміщений 0, 1, 2 або 3 замісниками, незалежно вибраними з C1-C4алкілу, галогенC1-C4алкіл-C1-C4алкокси, гідрокси, ціано, галогену, аміно, моно- та ди-C1-C4алкіламіно, гетероарилу та C1-C4алкілу, заміщеного гідрокси або аміно, причому гетероарил містить 5 або 6 кільцевих атомів, 1 або 2 кільцеві гетероатоми, вибрані з N, O та S, та заміщений 0, 1 або 2 замісниками, незалежно вибраними з C1-C4алкілу, моно- та ди-C1-C4алкіламіно, гідроксиC1-C4алкіламіно, гідроксиC1C4алкілу, 4-7-членного гетероцикл-C1-C4алкілу, аміноC1-C4алкілу та моно- та ди-C1C4алкіламіноC1-C4алкілу. Згідно з четвертим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим варіантом здійснення або її солі, де A являє собою 2-нафтил, необов'язково заміщений при 3 положенні гідрокси та додатково заміщений 0, 1 або 2 замісниками, вибраними з гідрокси, ціано, галогену, C1-C4алкілу, C2-C4алкенілу, C1-C4алкокси, де алкокси є незаміщеним або заміщеним гідрокси, C 1-C4алкокси, аміно, N(H)C(O)C1-C4алкілом, N(H)C(O)2-C1-C4алкілом, 4-7-членним гетероциклом та моно- та ди-C1-C4алкіламіно; або згідно з п'ятим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим варіантом здійснення або її солі, де B являє собою групу формули: , де m, n та p незалежно вибирають з 0 або 1; R, R1, R2, R3 та R4 незалежно вибирають з групи, що складається з водню, C1-C4алкілу, причому алкіл необов'язково заміщений гідрокси, аміно або моно- та ди-C1-C4алкіламіно; R5 та R6 являють собою водень; або R та R3 утворюють разом конденсоване 5- або 6-членне гетероциклічне кільце, яке містить 0 або 1 додатковий кільцевий гетероатом, вибраний з N, O або S; R 1 та R3 утворюють разом C1-C3алкіленову групу; R1 та R5 утворюють разом C1-C3алкіленову групу; R3 та R4 утворюють разом з атомом вуглецю, до якого вони приєднані, спіроцикл-C3-C6циклоалкіл; X являє собою CRARB, O, NR7 або зв'язок; RA та RB незалежно вибирають з водню та C1-C4алкілу, або RA та RB утворюють разом двовалентну C2-C5алкіленову групу; Z являє собою CR8 або N; якщо Z являє собою N, тоді X являє собою зв'язок; R8 являє собою водень або утворює разом з R 6 подвійний зв'язок. Згідно з шостим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим-четвертим варіантами здійснення або її солі, де B являє собою групу формули: , де p та q незалежно вибирають з групи, що містить 0, 1 та 2; R 9 та R13 незалежно вибирають з водню та C1-C4алкілу; R10 та R14 незалежно вибирають з водню, аміно, моно- та ди-C1 5 UA 114726 C2 5 10 15 20 C4алкіламіно та C1-C4алкілу, причому алкіл необов'язково заміщений гідрокси, аміно або монота ди-C1-C4алкіламіно; R11 являє собою водень, C1-C4алкіл, аміно або моно- та ди-C1C4алкіламіно; R12 являє собою водень або C1-C4алкіл; або R9 та R11 утворюють разом насичений азацикл, який містить від 4 до 7 кільцевих атомів, який необов'язково заміщений 1-3 C1C4алкільними групами; або R11 та R12 утворюють разом насичений азацикл, який містить від 4 до 7 кільцевих атомів, який необов'язково заміщений 1-3 C1-C4алкільними групами. Згідно з сьомим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим або третім варіантами здійснення або її солі,де сполука представлена формулою (II): (II), де R15 являє собою водень, гідроксил, C1-C4алкокси, причому алкокси необов'язково заміщений гідрокси, метокси, аміно, моно- та диметиламіно або морфоліном. Згідно з восьмим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим або четвертим варіантами здійснення або її солі, де сполука представлена формулою (III): (III), де R16 являє собою 5-членний гетероарил, який містить один кільцевий атом азоту та 0 або 1 додатковий кільцевий гетероатом, вибраний з N, O або S, де гетероарил необов'язково заміщений C1-C4алкілом. Згідно з дев'ятим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим-четвертим, сьомим та восьмим варіантами здійснення або її солі, де B вибирають з групи, що включає у себе , , 25 30 , , , , , та , де Х являє собою O або N(Me); та R17 являє собою водень або метил. Згідно з десятим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим-п'ятим та сьомим-дев'ятим варіантами здійснення або її солі, де X являє собою -O-. Згідно з одинадцятим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим-п'ятим та сьомим-дев'ятим варіантами здійснення або її солі, де B являє собою: 6 UA 114726 C2 . Згідно з дванадцятим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з восьмим-одинадцатим варіантами здійснення або її солі, де R 16 являє собою: 5 . Згідно з тринадцятим варіантом здійснення, даний винахід відноситься до сполуки у відповідності з першим варіантом здійснення або її солі, де сполука являє собою сполука формули (IV): (IV), 10 15 20 25 30 35 де X являє собою -O- або ; R" являє собою 5-членний гетероарил, необов'язково заміщений 0, 1 або 2 групами, вибраними з оксо, гідрокси, нітро, галогену, C 1-C4алкілу, C1C4алкенілу, C1-C4алкокси, C3-C7циклоалкілу, C1-C4алкіл-OH, тригалогенC1-C4алкілу, моно- та диC1-C4алкіламіно, -C(O)NH2, -NH2, -NO2, гідроксиC1-C4алкіламіно, гідроксиC1-C4алкілу, 4-7членний гетероцикл-C1-C4алкілу, аміноC1-C4алкілу та моно- та ди-C1-C4алкіламіноC1-C4алкілу. Згідно з чотирнадцятим варіантом здійснення, даний винахід відноситься до сполуки або її солі, вибраним з групи, що складається з: 6-(нафталін-2-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 6-(бензо[b]тіофен-2-іл)-N-метил-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 2-(6-(2,2,6,6-тетраметилпіперидин-4-іламіно)піридазин-3-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)бензо[b]тіофен-5карбонітрилу; 6-(хінолін-3-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 3-(бензо[b]тіофен-2-іл)-6-(2,2,6,6-тетраметилпіперидин-4-ілокси)піридазину; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу; 6-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)нафталін-2-олу; 6-(бензо[b]тіофен-2-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 7-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)ізохіноліну; 6-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)ізохіноліну; N-метил-6-(хінолін-7-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; N-метил-6-(хінолін-6-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 6-(ізохінолін-7-іл)-N-метил-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 6-(ізохінолін-6-іл)-N-метил-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 6-(імідазо[1,2-a]піридин-6-ілпіридазин-3-іл)метил(2,2,6,6-тетраметилпіперидин-4-іл)аміну; метил[6-(6-фенілпіридин-3-іл)піридазин-3-іл]-(2,2,6,6-тетраметилпіперидин-4-іл)аміну; метил[6-(6-пірол-1-ілпіридин-3-іл)піридазин-3-іл]-(2,2,6,6-тетраметилпіперидин-4-іл)аміну; метил[6-(6-піразол-1-ілпіридин-3-іл)піридазин-3-іл]-(2,2,6,6-тетраметилпіперидин-4-іл)аміну; метил(6-хіноксалін-2-ілпіридазин-3-іл)-(2,2,6,6-тетраметилпіперидин-4-іл)аміну; метил(6-хінолін-3-ілпіридазин-3-іл)-(2,2,6,6-тетраметилпіперидин-4-іл)аміну; N-метил-6-(фталазин-6-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 6-(бензо[c][1,2,5]оксадіазол-5-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 7 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 6-(бензо[d]тіазол-5-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 6-(2-метилбензо[d]оксазол-6-іл)-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин-3-аміну; 3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)нафталін-2-олу; 5-хлор-2-(6-(метил(1,2,2,6,6-пентаметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу; 3-(6-(2,2,6,6-тетраметилпіперидин-4-іламіно)піридазин-3-іл)нафталін-2-олу; 5-хлор-2-(6-(1,2,2,6,6-пентаметилпіперидин-4-іламіно)піридазин-3-іл)фенолу; 4-гідрокси-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)бензонітрилу; 3-[6-(2,2,6,6-тетраметилпіперидин-4-ілокси)піридазин-3-іл]нафталін-2-олу; 2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}-4-трифторметилфенолу; 2-фтор-6-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу; 3,5-диметокси-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу; 4,5-диметокси-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу; 5-метокси-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу; 4,5-дифтор-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу; 5-фтор-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}фенолу; 3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)бензонітрилу; 1-аліл-6-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)нафталін-2-олу; 6-(бензо[b]тіофен-2-іл)-N-(1,2,2,6,6-пентаметилпіперидин-4-іл)піридазин-3-аміну; N-аліл-3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3іл)бензаміду; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-1іл)фенолу; 5-(5-метилоксазол-2-іл)-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3іл}фенолу; 5-(4-гідроксиметил)-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4іл)аміно)піридазин-3-іл)фенолу; 5-(1H-імідазол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 5-(4-аміно-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 5-(4-аміно-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 5-(3-амінопіразол-1-іл)-2-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)-аміно]піридазин-3іл}фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-(2-морфоліноетил)1H-піразол-4-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-піразол-4іл)фенолу; 5-(5-аміно-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-1іл)фенолу; 2-{6-[(2-гідроксиетил)-(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}-5-піразол-1ілфенолу; 2-(6-(піперидин-4-ілокси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу; 2-(6-(((2S, 4R, 6R)-2,6-диметилпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1іл)фенолу; 2-(6-((-2,6-диметилпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)-фенолу; 2-(6-((-2,6-диметилпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)-фенолу; 5-(1H-піразол-1-іл)-2-(6-(піролідин-3-ілокси)піридазин-3-іл)фенолу; 2-(6-((-2-метилпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу; (S)-5-(1H-піразол-1-іл)-2-(6-(піролідин-3-ілметокси)піридазин-3-іл)фенолу; (R)-5-(1H-піразол-1-іл)-2-(6-(піролідин-3-ілметокси)піридазин-3-іл)фенолу; 2-(6-((3-фторпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу; 2-[6-(1,2,2,6,6-пентаметилпіперидин-4-ілокси)піридазин-3-іл]-5-піразол-1-ілфенолу; 5-піразол-1-іл-2-[6-(2,2,6,6-тетраметилпіперидин-4-ілокси)піридазин-3-іл]фенолу; 5-(1H-піразол-4-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)фенолу; 2-(6-піперазин-1-ілпіридазин-3-іл)-5-піразол-1-ілфенолу; 3-[6-(азетидин-3-іламіно)піридазин-3-іл]нафталін-2-олу; 2-[6-(азетидин-3-іламіно)піридазин-3-іл]-5-піразол-1-ілфенолу; 8 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 2-[6-(3,5-диметилпіперазин-1-іл)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-[6-(7-метил-2,7-діазаспіро[4.4]нон-2-іл)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-(6-[1,4]діазепан-1-ілпіридазин-3-іл)-5-піразол-1-ілфенолу; 2-{6-[4-(2-гідроксиетил)-піперазин-1-іл]піридазин-3-іл}-5-піразол-1-ілфенолу; 2-[6-(3,6-діазабіцикло[3.2.1]окт-3-ил)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-[6-(2,7-діазаспіро[3.5]нон-7-іл)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-[6-(3-гідроксиметилпіперазин-1-іл)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-[6-(1,7-діазаспіро[4.4]нон-7-іл)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-[6-(4-аміно-4-метилпіперидин-1-іл)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-[6-(3-диметиламінопіперидин-1-іл)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-[6-(1,2,2,6,6-пентаметилпіперидин-4-іламіно)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-[6-(3,3-диметилпіперазин-1-іл)піридазин-3-іл]-5-піразол-1-ілфенолу; 2-(6-(7-(2-гідроксиетил)-2,7-діазаспіро[4.4]нонан-2-іл)піридазин-3-іл)-5-(1H-піразол-1іл)фенолу; 2-(6-((3aR, 6aS)-гексагідропіроло[3,4-c]пірол-2(1H)-іл)піридазин-3-іл)-5-(1H-піразол-1іл)фенолу; 3-(6-(піперазин-1-іл)піридазин-3-іл)нафталін-2,7-діолу; 5-піразол-1-іл-2-[6-(1,2,3,6-тетрагідропіридин-4-іл)піридазин-3-іл]фенолу; 2-(6-піперидин-4-ілпіридазин-3-іл)-5-піразол-1-ілфенолу; 3-(6-(1,2,3,6-тетрагідропіридин-4-іл)піридазин-3-іл)нафталін-2-олу; 3-(6-(1,2,3,6-тетрагідропіридин-4-іл)піридазин-3-іл)нафталін-2,7-діолу; 3-(6-(2,2,6,6-тетраметил-1,2,3,6-тетрагідропіридин-4-іл)піридазин-3-іл)нафталін-2,7-діолу; 3-(6-(1-метил-1,2,3,6-тетрагідропіридин-4-іл)піридазин-3-іл)нафталін-2,7-діолу; 3-(6-(піперидин-4-іл)піридазин-3-іл)нафталін-2,7-діолу; 3-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)нафталін-2,7-діолу; 3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)нафталін-2,7-діолу; 3-(6-((2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)нафталін-2,7-діолу; складного трет-бутилового ефіру [3-(7-гідрокси-6-{6-[метил(2,2,6,6-тетраметилпіперидин-4іл)аміно]піридазин-3-іл}нафталін-2-ілокси)пропіл]карбамінової кислоти; 7-(3-амінопропокси)-3-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3іл}нафталін-2-олу; N-[3-(7-гідрокси-6-{6-[метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно]піридазин-3-іл}нафталін2-ілокси)пропіл]ацетаміду; 7-(3-гідроксипропокси)-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)нафталін-2-олу; 7-(3-метоксипропокси)-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3іл)нафталін-2-олу; 7-(2-морфоліноетокси)-3-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3іл)нафталін-2-олу; 3-(6-(піперидин-4-ілметил)піридазин-3-іл)нафталін-2-олу; 5-(1H-піразол-1-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4-іл)метил)піридазин-3-іл)фенолу; 3-метокси-2-(6-(метил(2,2,6-триметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5метилоксазол-2-іл)фенолу; 2-(6-((6S)-6-((S)-1-гідроксиетил)-2,2-диметилпіперидин-4-ілокси)піридазин-3-іл)-5-(1Hпіразол-1-іл)фенолу; 7-гідрокси-6-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-2нафтонітрилу; 3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-7-(піперидин-1ілметил)нафталін-2-олу; 3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-7-(піролідин-1ілметил)нафталін-2-олу; 1-бром-6-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-нафталін-2,7діолу; 1-хлор-6-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-нафталін-2,7діолу; 7-метокси-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-нафталін-2олу; 7-метокси-3-(6-(метил(1,2,2,6,6-пентаметилпіперидин-4-іл)аміно)піридазин-3-іл)-нафталін-2олу; 9 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 7-(3,6-дигідро-2H-піран-4-іл)-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)-аміно)піридазин3-іл)нафталін-2-олу; 3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-7-(тетрагідро-2H-піран-4іл)нафталін-2-олу; 7-(дифторметил)-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3іл)нафталін-2-олу; 7-((4-гідрокси-2-метилбутан-2-іл)окси)-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4іл)аміно)піридазин-3-іл)нафталін-2-олу; 7-(3-гідрокси-3-метилбутокси)-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин3-іл)нафталін-2-олу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4іл)бензол-1,3-діолу; 3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол4-іл)фенолу; 5-(1H-піразол-4-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-3(трифторметокси)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-піразол-4іл)-3-(трифторметокси)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4-іл)-3(трифторметокси)фенолу; 4-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5(трифторметокси)феніл)-1-метилпіридин-2(1H)-ону; 3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил1H-піразол-4-іл)фенолу; 3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5,6,7,8тетрагідроімідазо[1,2-a]піридин-3-іл)фенолу; 3-метокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(піридин-3іл)фенолу; 5-(1-циклопентил-1H-піразол-4-іл)-3-метокси-2-(6-(метил(2,2,6,6-тетраметил-піперидин-4іл)аміно)піридазин-3-іл)фенолу; 3',5-диметокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-[1,1'біфеніл]-3-олу; 3-(бензилокси)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5метилоксазол-2-іл)фенолу; 3-етокси-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5метилоксазол-2-іл)фенолу; 3-(циклопропілметокси)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3-іл)5-(5-метилоксазол-2-іл)фенолу; 2-метил-5-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-1Hбензо[d]імідазол-6-олу; 5-хлор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-фенолу; 5-(1H-піразол-1-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу; 3-гідрокси-4-(6-((2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)бензонітрилу; 2-(6-((2,2-диметилпіперидин-4-іл)окси)піридазин-3-іл)-5-(1H-піразол-1-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-4іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(4,5,6,7тетрагідропіразоло[1,5-a]піридин-3-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(4,5,6,7тетрагідропіразоло[1,5-a]піразин-3-іл)фенолу; 4-(1H-індол-2-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу; 4-(циклопент-1-ен-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-3іл)фенолу; 4-(4-гідрокси-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3іл)феніл)піридин-2-олу; 4-(4-гідрокси-3-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)феніл)-1метилпіридин-2(1H)-ону; 10 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 4-(4-гідрокси-3-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)феніл)піридин-2олу; 5-(1H-індазол-7-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 4-хлор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4іл)фенолу; 4-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1H-піразол-4іл)фенолу; 5-фтор-4-(1H-імідазол-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин3-іл)фенолу; 5-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-4іл)фенолу; 5-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-4-(1H-піразол-5іл)фенолу; 6-гідрокси-5-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-2,3-дигідро1H-інден-1-ону; 6-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-1,4-дигідроіндено[1,2c]піразол-7-олу; гідрохлориду 6-гідрокси-5-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)2,3-дигідро-1H-інден-1-оноксиму; 5-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-2,3-дигідро-1H-інден-1,6діолу; гідрохлориду 2-аміно-6-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3-іл)8H-індено[1,2-d]тіазол-5-олу; гідрохлориду 9-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5,6дигідроімідазо[5,1-a]ізохінолін-8-олу; 4-гідрокси-3-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-N-((1-метил1H-піразол-4-іл)метил)бензаміду; 4-(4-(гідроксиметил)-1H-піразол-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4іл)аміно)піридазин-3-іл)фенолу; 5-(1H-піразол-4-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4-іл)метил)піридазин-3-іл)фенолу; 6-(3-(бензилокси)ізохінолін-6-іл)-N-метил-N-(2,2,6,6-тетраметилпіперидин-4-іл)-піридазин-3аміну; 6-(1-(бензилокси)ізохінолін-7-іл)-N-метил-N-(2,2,6,6-тетраметилпіперидин-4-іл)-піридазин-3аміну; гідрохлориду 3-фтор-5-(2-метоксипіридин-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4іл)аміно)піридазин-3-іл)фенолу; гідрохлориду 4-(3-фтор-5-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4іл)аміно)піридазин-3-іл)феніл)піридин-2(1H)-ону; гідрохлориду 4-(3-фтор-5-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4іл)аміно)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону; гідрохлориду 5-(3-фтор-5-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4іл)аміно)піридазин-3-іл)феніл)-1-метилпіридин-2(1H)-ону; гідрохлориду 3-фтор-5-(1H-піразол-4-іл)-2-(6-((2,2,6,6-тетраметилпіперидин-4іл)окси)піридазин-3-іл)фенолу; гідрохлориду 5-хлор-3-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин3-іл)фенолу; гідрохлориду 3-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3-іл)-5(1H-піразол-4-іл)фенолу; гідрохлориду 3-фтор-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3-іл)-5(1-метил-1H-піразол-4-іл)фенолу; 5-(5-метоксипіридин-3-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 5-(3-гідрокси-4-(6-метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)піридин-2-олу; 4-(3-гідрокси-4-(6-метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)піридин-2-олу; 5-(6-метоксипіридин-3-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 11 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 5-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-3(трифторметил)піридин-2-олу; 5-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-1метилпіридин-2(1H)-ону; 4-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-1метилпіридин-2(1H)-ону; 5-(2-метоксипіридин-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 4-(3-гідрокси-4-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)-феніл)піридин-2олу; 5-(6-(диметиламіно)піридин-3-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4іл)аміно)піридазин-3-іл)фенолу; 4-(3-гідрокси-4-(6-((2,2,6,6-тетраметилпіперидин-4-іл)окси)піридазин-3-іл)-феніл)-1метилпіридин-2(1H)-ону; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(піримідин-5іл)фенолу; 5-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3іл)феніл)піридин-3-олу; 1-циклопропіл-4-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)-аміно)піридазин3-іл)феніл)піридин-2(1H)-ону; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1,2,3,6тетрагідропіридин-4-іл)фенолу; 5-(циклопент-1-ен-1-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3іл)фенолу; 5-(3,6-дигідро-2H-піран-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин3-іл)фенолу; 5-(імідазо[1,5-a]піридин-7-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин3-іл)фенолу; 5-(імідазо[1,2-a]піридин-7-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин3-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(2-метилпіридин-4іл)фенолу; 5-(1H-імідазол-2-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 5-(1H-імідазол-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)-піридазин-3іл)фенолу; 5-(імідазо[1,2-a]піразин-3-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)-аміно)піридазин3-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(5,6,7,8тетрагідроімідазо[1,2-a]піразин-3-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(4-метил-1H-імідазол2-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-імідазол4-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(1-метил-1H-імідазол5-іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(4-нітро-1H-імідазол-2іл)фенолу; 2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)-5-(2-метил-1H-імідазол4-іл)фенолу; 5-(1,2-диметил-1H-імідазол-4-іл)-2-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)фенолу; 1-(3-гідрокси-4-(6-(метил(2,2,6,6-тетраметилпіперидин-4-іл)аміно)піридазин-3-іл)феніл)-1Hпіразол-4-карбоксаміду; 2-(6-((3aR, 6aS)-5-(2-гідроксиетил)гексагідропіроло[3,4-c]пірол-2(1H)-іл)піридазин-3-іл)-5-(1Hпіразол-4-іл)фенолу; 2-(6-((3aR, 6aS)-гексагідропіроло[3,4-c]пірол-2(1H)-іл)піридазин-3-іл)-5-(1H-піразол-4іл)фенолу; 2-(6-((3aR, 6aS)-5-метилгексагідропіроло[3,4-c]пірол-2(1H)-іл)піридазин-3-іл)-5-(1H-піразол-4іл)фенолу; 12 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 4-(3-гідрокси-4-(6-(5-метилгексагідропіроло[3,4-c]пірол-2(1H)-іл)піридазин-3-іл)феніл)-1метилпіридин-2(1H)-ону; 4-(3-гідрокси-4-(6-((3aR, 6aR)-1-метилгексагідропіроло[3,4-b]пірол-5(1H)-іл)піридазин-3іл)феніл)-1-метилпіридин-2(1H)-ону; 2-(6-(2,7-діазаспіро[4.5]декан-2-іл)піридазин-3-іл)-5-(1H-піразол-4-іл)фенолу; та 4-(4-(6-(2,7-діазаспіро[4.5]декан-2-іл)піридазин-3-іл)-3-гідроксифеніл)-1-метилпіридин-2(1H)ону. Згідно з п'ятнадцятим варіантом здійснення, даний винахід являє собою фармацевтичну композицію, що містить терапевтично ефективну кількість сполуки у відповідності з будь-яким з першого-чотирнадцятого варіантів здійснення або її фармацевтично прийнятної солі та один або декілька фармацевтично прийнятних носіїв. Згідно з шістнадцятим варіантом здійснення, даний винахід являє собою комбінацію, що включає терапевтично ефективну кількість сполуки у відповідності з будь-яким з першогочотирнадцятого варіантів здійснення або її фармацевтично прийнятної солі та один або декілька терапевтично активних співагентів. Згідно з сімнадцятим варіантом здійснення, даний винахід являє собою спосіб лікування, профілактики або зменшення інтенсивності зв'язаного з дефіцитом SMN стану, що включає введення суб'єкту, який цього потребує, ефективної кількості сполуки або її солі у відповідності з будь-яким з першого-чотирнадцятого варіантів здійснення. Згідно з вісімнадцятим варіантом здійснення, даний винахід являє собою спосіб згідно з сімнадцятим варіантом здійснення, у якому згаданий пов'язаний з дефіцитом SMN стан являє собою спінальну м'язову атрофію. Згідно з дев'ятнадцятим варіантом здійснення, даний винахід являє собою сполуку у відповідності з будь-яким з першого-чотирнадцятого варіантів здійснення або її фармацевтично прийнятну сіль для застосування як лікарський засіб. Згідно з двадцятим варіантом здійснення, даний винахід являє собою сполуку у відповідності з будь-яким з першого-чотирнадцятого варіантів здійснення або її фармацевтично прийнятну сіль для застосування при лікуванні зв'язаного з дефіцитом SMN стану. Згідно з двадцять першим варіантом здійснення, даний винахід являє собою сполуку у відповідності з двадцятим варіантом здійснення або її фармацевтично прийнятну сіль для застосування при лікуванні спінальної м'язової атрофії. Згідно з двадцять другим варіантом здійснення, даний винахід являє собою застосування сполуки у відповідності з будь-яким з першого-чотирнадцятого варіантів здійснення або її фармацевтично прийнятної солі для виробництва лікарського засобу для лікування спінальної м'язової атрофії. З метою інтерпретації даного опису будуть використовуватися наступні визначення, та у відповідних випадках терміни, використані у формі однини, також будуть включати у себе форму множини та навпаки. Використаний у даному документі термін "модулятор SMN" включає у себе засоби, такі як сполуки згідно з даним винаходом, які мають здатність модулювати, наприклад, збільшувати, рівні білку SMN шляхом, щонайменше, одного з множини можливих механізмів. Необмежуюча група механізмів включає у себе активацію промотору SMN, модулювання сплайсингу (наприклад, попередження вирізання екзону 7 при сплайсингу гену SMN) та модулювання стабільності білку SMN. Модулятори SMN можуть модулювати, наприклад, збільшувати, рівні FL-SMN та/або SMN∆7 шляхом будь-якого із згаданих механізмів та/або можуть попереджати деградацію SMN∆7. Використаний у даному документі термін "сполуки згідно з даним винаходом" включає у себе без обмеження сполуки формули (I) та сполуки формули (I-A). Використаний у даному документі термін "пов'язані з дефіцитом SMN стани" включає у себе без обмеження спінальну м'язову атрофію (SMA), вроджений множинний артрогрипоз нейрогенного типу (вроджений AMC) та бічний аміотрофічний склероз (ALS). Використаний у даному документі термін "спінальна м'язова атрофія" ("SMA") включає у себе три форми SMA з початком у дитячому віці: тип I (хвороба Верднига-Гофманна); тип II (проміжна, хронічна форма); тип III (хвороба Кугельберга-Веландера або ювенільна спінальна м'язова атрофія); тип IV з початком у зрілому віці; а також інші форми SMA, включаючи Ххромосомне захворювання, спінальну м'язову атрофію з респіраторним дистрес-синдромом (SMARD), спінальну та бульбарну м'язову атрофію (хвороба Кеннеді або бульбо-спінальна м'язова атрофія) та дистальну спінальну м'язову атрофію. 13 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 З метою інтерпретації даного опису будуть використовуватися наступні визначення, та у відповідних випадках терміни, використані у формі однини, також будуть включати у себе форму множини та навпаки. Використаний у даному документі термін "C1-10алкіл" відноситься до повністю насиченого розгалуженого або нерозгалуженого вуглеводневого фрагменту, який містить від 1 до 10 атомів вуглецю. Терміни "C1-6алкіл" та "C1-4алкіл" слід тлумачити відповідно. Типові приклади C 110алкілу включають у себе без обмеження метил, етил, н-пропіл, ізопропіл, н-бутил, втор-бутил, ізобутил, трет-бутил, н-пентил, ізопентил, неопентил, н-гексил, 3-метилгексил, 2,2диметилпентил, 2,3-диметилпентил, н-гептил, н-октил, н-ноніл та н-децил. Використаний у даному документі термін "C1-10алкілен" відноситься до двовалентної алкільної групи, визначеної вище у даному документі, що містить від 1 до 10 атомів вуглецю. Терміни "C1-6алкілен" та "C1-4алкілен" слід тлумачити відповідно. Типові приклади C 1-10алкілену включають у себе без обмеження метилен, етилен, н-пропілен, ізопропілен, н-бутилен, вторбутилен, ізобутилен, трет-бутилен, н-пентилен, ізопентилен, неопентилен, н-гексилен, 3метилгексилен, 2,2-диметилпентилен, 2,3-диметилпентилен, н-гептилен, н-октилен, н-нонілен та н-децилен. Використаний у даному документі термін "галогенC1-10алкіл" відноситься до C1-10алкільної групи, визначеної вище у даному документі, у якій, щонайменше, один з атомів водню замінений атомом галогену. ГалогенC1-10алкільна група може являти собою моногалогенC1-10алкіл, дигалогенC1-10алкіл або полігалогенC1-10алкіл, включаючи пергалогенC1-10алкіл. МоногалогенC110алкіл може містити у алкільній групі один атом йоду, брому, хлору або фтору. ДигалогенC 110алкільні та полігалогенC1-10алкільні групи можуть містити два або декілька однакових атоми галогену або поєднання різних галогенових груп у алкілі. Звичайно полігалогенC 1-10алкільна група містить до 12, або 10, або 8, або 6, або 4, або 3, або 2 галогенових груп. Необмежуючі приклади галогенC1-10алкілу включають у себе фторметил, дифторметил, трифторметил, хлорметил, дихлорметил, трихлорметил, пентафторетил, гептафторпропіл, дифторхлорметил, дихлорфторметил, дифторетил, дифторпропіл, дихлоретил та дихлорпропіл. ПергалогенC110алкільна група відноситься до C1-10алкільної групи, у якій всі атоми водню замінені атомами галогену. Термін "арил" відноситься до ароматичної вуглеводневої групи, що містить 6-20 атомів вуглецю у кільцевій частині. Звичайно арил являє собою моноциклічний, біциклічний або трициклічний арил, який містить 6-20 атомів вуглецю, та включає у себе одне або декілька ароматичних кілець, конденсованих з одним або декількома неароматичними вуглеводневими кільцями. Необмежуючі приклади включають у себе феніл, нафтил або тетрагідронафтил. Використаний у даному документі термін "C1-10алкокси" відноситься до C1-10алкіл-O-, де C1алкіл визначений вище у даному описі. Типові приклади C 1-10алкокси включають у себе без 10 обмеження метокси, етокси, пропокси, 2-пропокси, бутокси, трет-бутокси, пентилокси, гексилокси, гептилокси, октилокси та децилокси. Використаний у даному документі термін "гетероцикліл" або "гетероцикло" відноситься до насиченого або ненасиченого неароматичного кільця або кільцевої системи, які являють собою 4-, 5-, 6- або 7-членне моноциклічне кільце, яке містить 1, 2 або 3 гетероатоми, вибрані з O, S та N, 7-, 8-, 9-, 10-, 11- або 12-членну біциклічну кільцеву систему, яка містить 1, 2, 3, 4 або 5 гетероатомів, вибраних з O, S та N, або 10-, 11-, 12-, 13-, 14- або 15-членну трициклічну кільцеву систему, яка містить 1, 2, 3, 4, 5, 6 або 7 гетероатомів, вибраних з O, S та N, де N та S також можуть бути необов'язково окислені до різних степенів окислення. Гетероциклічна група може бути приєднана через гетероатом або атом вуглецю. Гетероцикліл може включати у себе конденсовані або з'єднані містковим зв'язком кільця, а також спіроциклічні кільця. Приклади гетероциклів включають у себе тетрагідрофуран (THF), дигідрофуран, 1,4-діоксан, морфолін, 1,4-дитіан, піперазин, піперидин, 1,3-діоксолан, імідазолідин, імідазолін, піролін, піролідин, тетрагідропіран, дигідропіран, оксатіолан, дитіолан, 1,3-діоксан, 1,3-дитіан, оксатіан та тіоморфолін. Використаний у даному документі термін "C3-12циклоалкіл" відноситься до насичених або ненасичених моноциклічних, біциклічних або трициклічних вуглеводневих груп, що містять 3-12 атомів вуглецю. Термін "C3-18циклоалкіл" відноситься до повністю насиченої або ненасиченої моноциклічної вуглеводневої групи, що складається з 3-8 атомів вуглецю. Типові моноциклічні вуглеводневі групи включають у себе без обмеження циклопропіл, циклобутил, циклопентил, циклопентеніл, циклогексил та циклогексеніл. Типові біциклічні вуглеводневі групи включають у себе борніл, індил, гексагідроіндил, тетрагідронафтил, декагідронафтил, біцикло[2.1.1]гексил, біцикло[2.2.1]гептил, біцикло[2.2.1]гептеніл, 6,6-диметилбіцикло[3.1.1]гептил, 2,6,6 14 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 триметилбіцикло[3.1.1]гептил, біцикло[2.2.2]октил. Типові трициклічні вуглеводневі групи включають у себе, наприклад, адамантил. Використаний у даному документі термін "C 3-12циклоалкілокси" відноситься до C3циклоалкіл-O-, де C3-12циклоалкіл визначений вище у даному описі. Типові приклади C 312 12циклоалкілокси включають у себе без обмеження моноциклічні групи, такі як циклопропокси, циклобутокси, циклопентилокси, циклопентенілокси, циклогексилокси та циклогексенілокси та т.п. Типові біциклічні вуглеводневі групи включають у себе борнілокси, індилокси, гексагідроіндилокси, тетрагідронафтилокси, декагідронафтилокси, біцикло[2.1.1]гексилокси, біцикло[2.2.1]гептилокси, біцикло[2.2.1]гептенілокси, 6,6-диметилбіцикло[3.1.1]гептилокси, 2,6,6триметилбіцикло[3.1.1]гептилокси, біцикло[2.2.2]октилокси та т.п. Типові трициклічні вуглеводневі групи включають у себе, наприклад, адамантилокси. Використаний у даному документі термін "арилокси" відноситься як до -O-арильної, так і до O-гетероарильної групи, де значення арилу та гетероарилу визначені у даному документі. Використаний у даному документі термін "гетероарил" відноситься до 5-, 6- або 7-членного моноциклічного ароматичного кільця, що містить 1, 2, 3 або 4 гетероатоми, вибрані з O, S та N, 8-, 9- або 10-членної конденсованої біциклічної кільцевої системи, що містить 1, 2, 3, 4 або 5 гетероатомів, вибраних з O, S та N, або 11-, 12-, 13- або 14-членної конденсованої трициклічної кільцевої системи, що містить 1, 2, 3, 4, 5 або 6 гетероатомів, вибраних з O, S та N, де, щонайменше, одне з кілець біциклічних або трициклічних кільцевих систем є повністю ароматичним. Типові гетероарильні групи включають у себе 2- або 3-тієніл, 2- або 3-фурил, 2або 3-піроліл, 2-, 4- або 5-імідазоліл, 3-, 4-, або 5-піразоліл, 2-, 4- або 5-тіазоліл, 3-, 4- або 5ізотіазоліл, 2-, 4- або 5-оксазоліл, 3-, 4- або 5-ізоксазоліл, 3- або 5-1,2,4-триазоліл, 4- або 51,2,3-триазоліл, тетразоліл, 2-, 3- або 4-піридил, 3- або 4-піридазиніл, 3-, 4- або 5-піразиніл, 2піразиніл, 2-, 4- або 5-піримідиніл, 1-, 2-, 3-, 5-, 6-, 7- або 8-індолізиніл, 1-, 3-, 4-, 5-, 6- або 7ізоіндоліл, 2-, 3-, 4-, 5-, 6- або 7-індоліл, 2-, 3-, 4-, 5-, 6- або 7-індазоліл, 2-, 4-, 5-, 6-, 7- або 8пуриніл, 1-, 2-, 3-, 4-, 6-, 7-, 8- або 9-хінолізиніл, 2-, 3-, 4-, 5-, 6-, 7- або 8-хінолініл, 1-, 3-, 4-, 5-, 6-, 7- або 8-ізохінолініл, 1-, 4-, 5-, 6-, 7- або 8-фталазиніл, 2-, 3-, 4-, 5- або 6-нафтиридиніл, 2-, 3-, 5-, 6-, 7- або 8-хіназолініл, 3-, 4-, 5-, 6-, 7- або 8-циннолініл, 2-, 4-, 6- або 7-птеридиніл, 1-, 2-, 3-, 4-, 5-, 6-, 7- або 8-4aH карбазоліл, 1-, 2-, 3-, 4-, 5-, 6-, 7- або 8-карбазоліл, 1-, 3-, 4-, 5-, 6-, 7-, 8- або 9-карболініл, 1-, 2-, 3-, 4-, 6-, 7-, 8-, 9- або 10-фенантридиніл, 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8- або 9акридиніл, 1-, 2-, 4-, 5-, 6-, 7-, 8- або 9-перимідиніл, 2-, 3-, 4-, 5-, 6-, 8-, 9- або 10-фенантролініл, 1-, 2-, 3-, 4-, 6-, 7-, 8- або 9-феназиніл, 1-, 2-, 3-, 4-, 6-, 7-, 8-, 9- або 10-фенотіазиніл, 1-, 2-, 3-, 4-, 6-, 7-, 8-, 9- або 10-феноксазиніл, 2-, 3-, 4-, 5-, 6- або 1-, 3-, 4-, 5-, 6-, 7-, 8-, 9- або 10безізохінолінил, 2-, 3-, 4- або тієно[2,3-b]фураніл, 2-, 3-, 5-, 6-, 7-, 8-, 9-, 10 або 11-7Hпіразино[2,3-c]карбазоліл, 2-, 3-, 5-, 6- або 7-2H-фуро[3,2-b]піраніл, 2-, 3-, 4-, 5-, 7- або 8-5Hпіридо[2,3-d]-орто-оксазиніл, 1-, 3- або 5-1H-піразоло[4,3-d]оксазоліл, 2-, 4- або 54H-імідазо[4,5d]тіазоліл, 3-, 5- або 8-піразино[2,3-d]піридазиніл, 2-, 3-, 5- або 6-імідазо[2,1-b]тіазоліл, 1-, 3-, 6-, 7-, 8- або 9-фуро[3,4-c]циннолініл, 1-, 2-, 3-, 4-, 5-, 6-, 8-, 9-, 10 або 11-4H-піридо[2,3c]карбазоліл, 2-, 3-, 6- або 7-імідазо[1,2-b][1,2,4]триазиніл, 7-бензо[b]тієніл, 2-, 4-, 5-, 6- або 7бензоксазоліл, 2-, 4-, 5-, 6- або 7-бензімідазоліл, 2-, 4-, 4-, 5-, 6- або 7-бензотіазоліл, 1-, 2-, 4-, 5-, 6-, 7-, 8- або 9- бензоксапініл, 2-, 4-, 5-, 6-, 7- або 8-бензоксазиніл, 1-, 2-, 3-, 5-, 6-, 7-, 8-, 9-, 10або 11-1H-піроло[1,2-b][2]бензазапініл, 2-, 3-, 4-, 5-, 6-, 7- або 8-хінолініл, 1-, 3-, 4-, 5-, 6-, 7- або 8-ізохінолініл, 2-, 3-, 4-, 5-, 6- або 7-індоліл, 2-, 3-, 4-, 5-, 6- або 7-бензо[b]тієніл, 2-, 4-, 5-, 6- або 7-бензоксазоліл, 2-, 4-, 5-, 6- або 7-бензімідазоліл та 2-, 4-, 5-, 6- або 7-бензотіазоліл. Використаний у даному документі термін "галоген" або "галоїд" відноситься до фтору, хлору, брому та йоду. Використаний у даному документі термін "ізомери" відноситься до різних сполук, які мають однакові молекулярні формули, але відрізняються розташуванням та конфігурацією атомів. Також у тому розумінні, як тут використаний, термін "оптичний ізомер" або "стереоізомер" відноситься до будь-якої з різних стереоізомерних конфігурацій, які можуть існувати для даної сполуки згідно з даним винаходом, та включають геометричні ізомери. Слід розуміти, що замісник може бути приєднаний до хірального центру атому вуглецю. Тому даний винахід включає енантіомери, діастереоізомери або рацемічні сполуки. "Енантіомери" являють собою пари стереоізомерів, які не є дзеркальними зображеннями один одного, що суміщаються. Суміш 1:1 пари енантіомерів являє собою "рацемічну" суміш. Термін використовують за необхідності для позначення рацемічної суміші. "Діастереоізомери" являють собою стереоізомери, у яких є щонайменше два асиметричні атоми, але які не є дзеркальними зображеннями один іншого. Абсолютну стереохімію визначають у відповідності з R-S системою Кана-Інгольда-Прелога. Якщо сполука являє собою чистий енантіомер, стереохімію кожного хірального вуглецю можна визначити або як R або як S. Розділені сполуки, абсолютна конфігурація яких невідома, можна 15 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 позначати як (+) або (-) залежно від напрямку (право- або лівообертальні), у якому вони обертають площину поляризації світла на довжині хвилі D лінії натрію. Розкриті у описі сполуки містять один або більше з асиметричних центрів або осей та тому можуть мати енантіомери, діастереоізомери та інші стереоізомерні форми, які можна розділити у термінах абсолютної стереохімії як (R)- або (S)-. Мається на увазі, що даний винахід включає всі такі можливі ізомери, включаючи рацемічні суміші, оптично чисті форми та проміжні суміші. Оптично активні (R)- та (S)- ізомери можна одержати, використовуючи хіральні синтони або хіральні реагенти, або розділити, використовуючи звичайні методики. Якщо сполука містить подвійний зв'язок, замісник може існувати у E або Z конфігурації. Якщо сполука містить дизаміщений циклоалкіл, такий циклоалкільний замісник може існувати у цис- або транс-конфігурації. Всі таутомерні форми також мають бути включені у даний документ. Використовувані у даному документі терміни "сіль" або "солі" відносяться до кислотноадитивної або основно-адитивної солі сполуки згідно з даним винаходом. Термін "солі" зокрема включає у себе термін "фармацевтично прийнятні солі". Термін "фармацевтично прийнятні солі" відноситься до солей, які зберігають біологічну ефективність та властивості сполук згідно з даним винаходом та, як правило, не є небажаними з біологічної або іншої точки зору. У багатьох випадках сполуки згідно з даним винаходом здатні утворювати кислотні та/або основні солі внаслідок наявності аміногруп та/або карбоксильних груп або груп, подібних до них. Фармацевтично прийнятні кислотно-адитивні солі можуть бути утворені з неорганічними кислотами та органічними кислотами, наприклад, ацетатні, аспартатні, банзоатні, безилатні, бромідні/гідробромідні, бікарбонатні/карбонатні, бісульфатні/сульфатні, камфорсульфонатні, хлоридні/гідрохлоридні, хлортіофілонатні, цитратні, етандисульфонатні, фумаратні, глюцептатні, глюконатні, глюкуронатні, гіпуратні, гідройодидні/йодидні, ізотіонатні, лактатні, лактобіонатні, лаурилсульфатні, малатні, малеатні, малонатні, манделатні, мезилатні, метилсульфатні, нафтоатні, напсилатні, нікотинатні, нітратні, октадеканоатні, олеатні, оксалатні, пальмітатні, памоатні, фосфатні/гідрофосфатні/дигідрофосфатні, полігалактуронатні, пропіонатні, стеаратні, сукцинатні, сульфосаліцилатні, тартратні, тозилатні та трифторацетатні солі. Неорганічні кислоти, з яких можуть бути отримані солі, включають у себе, наприклад, соляну кислоту, бромистоводневу кислоту, сірчану кислоту, азотну кислоту, фосфорну кислоту та т.п. Органічні кислоти, з яких можуть бути отримані солі, включають у себе, наприклад, оцтову кислоту, пропіонову кислоту, гліколеву кислоту, щавлеву кислоту, малеїнову кислоту, малонову кислоту, бурштинову кислоту, фумарову кислоту, винну кислоту, лимонну кислоту, бензойну кислоту, мигдальну кислоту, метансульфонову кислоту, етансульфонову кислоту, толуолсульфонову кислоту, сульфосаліцилову кислоту та т.п. Фармацевтично прийнятні основно-адитивні солі можуть бути утворені з неорганічними та органічними основами. Неорганічні основи, з яких можуть бути отримані солі, включають у себе, наприклад, солі амонію та металів I-XII груп періодичної таблиці. Згідно з певними варіантами здійснення, такі солі отримують з натрію, калію, амонію, кальцію, магнію, заліза, срібла, цинку та міді; особливо підходящі солі включають у себе солі амонію, калію, натрію, кальцію та магнію. Органічні основи, з яких можуть бути отримані солі, включають у себе, наприклад, первинні, вторинні та третинні аміни, заміщені аміни, включаючи заміщені аміни, що зустрічаються у природі циклічні аміни, основні іонообмінні смоли та т.п. Певні органічні аміни включають у себе ізопропіламін, бензатин, холінат, діетаноламін, діетиламін, лізин, меглумін, піперазин та трометамін. Фармацевтично прийнятні солі згідно з даним винаходом можуть бути синтезовані з вихідної сполуки, основного або кислотного фрагменту, шляхом загальноприйнятих хімічних способів. Як правило, такі солі можуть бути одержані шляхом здійснення взаємодії таких сполук у формі вільної кислоти із стехіометричною кількістю відповідної основи (такої як гідроксид, карбонат, бікарбонат Na, Ca, Mg або K, та т.п.) або шляхом здійснення взаємодії таких сполук у формі вільної основи із стехіометричною кількістю відповідної кислоти. Такі взаємодії звичайно проводять у воді або у органічному розчиннику, або у їх суміші. Як правило, використання неводного середовища, такого як простий ефір, етилацетат, етанол, ізопропанол або ацетонітрил, є бажаним за наявності такої можливості. Списки додаткових підходящих солей можна знайти, наприклад, у "Remington's Pharmaceutical Sciences", 20th ed., Mack Publishing Company, Easton, Pa., (1985); та у "Handbook of Pharmaceutical Salts: Properties, Selection, and Use" by Stahl and Wermuth (Wiley-VCH, Weinheim, Germany, 2002). Будь-яка формула, представлена у даному документі, також призначена для представлення немічених форм, а також мічених ізотопами форм сполук. Мічені ізотопами сполуки мають структури, відображені приведеними у даному документі формулами, за виключенням того, що 16 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 один або декілька атомів заміщені атомом, що має вибрану атомну масу або масовий номер. Приклади ізотопів, які можуть бути включені у склад сполук згідно з даним винаходом, 2 включають у себе ізотопи водню, вуглецю, азоту, кисню, фосфору, фтору та хлору, такі як H, 3 11 13 14 15 18 31 32 35 36 125 H, C, C, C, N, F, P, P, S, Cl, I, відповідно. Даний винахід включає у себе різні мічені ізотопами сполуки, визначені у даному документі, наприклад, сполуки, у яких присутні 3 13 14 радіоактивні ізотопи, такі як H, C та C. Такі мічені ізотопами сполуки застосовні у 14 2 3 дослідженнях метаболізму (з C), дослідженнях кінетики реакції (з, наприклад, H або H), методиках визначення або візуалізації, таких як позитронно-емісійна томографія (PET) або однофотонна емісійна комп'ютерна томографія (SPECT), включаючи методи аналізу розподілу ліків або субстрату у тканинах, або для радіоактивного лікування пацієнтів. Зокрема, для PET 18 або SPECT досліджень може бути особливо бажане використання F або міченої сполуки. Мічені ізотопами сполуки згідно з даним винаходом та їх проліки, як правило, можуть бути приготовлені шляхом здійснення методик, розкритих у схемах або у описаних нижче прикладах та підготовчих прикладах, шляхом заміни не міченого ізотопами реагенту легко доступним міченим ізотопами реагентом. 2 Крім того, заміна більш важкими ізотопами, зокрема дейтерієм (тобто H або D), дозволяє досягати певних терапевтичних переваг внаслідок більшої метаболічної стабільності, наприклад, збільшеного часу напівжиття in vivo або зниженого необхідного дозування або поліпшеного терапевтичного індексу. Слід розуміти, що у цьому контексті дейтерій розглядається як замісник сполук формули (I). Концентрація такого більш важкого ізотопу, зокрема дейтерію, може бути визначена фактором ізотопного збагачення. Використаний у даному документі термін "фактор ізотопного збагачення" означає співвідношення між ізотопною сполукою та поширеністю у природі конкретного ізотопу. Якщо замісник у сполуці згідно з даним винаходом позначений як дейтерій, тоді для кожного позначеного атому дейтерію така сполука характеризується фактором ізотопного збагачення, рівним, щонайменше, 3500 (52,5 % включення дейтерію у кожному позначеному атомі дейтерію), щонайменше, 4000 (60 % включення дейтерію), щонайменше, 4500 (67,5 % включення дейтерію), щонайменше, 5000 (75 % включення дейтерію), щонайменше, 5500 (82,5 % включення дейтерію), щонайменше, 6000 (90 % включення дейтерію), щонайменше, 6333,3 (95 % включення дейтерію), щонайменше, 6466,7 (97 % включення дейтерію), щонайменше, 6600 (99 % включення дейтерію) або, щонайменше, 6633,3 (99,5 % включення дейтерію). Мічені ізотопами сполуки формули (I), як правило, можуть бути отримані шляхом загальноприйнятих методик, відомих фахівцям у даній галузі техніки, або способами, аналогічними описаним у прикладених прикладах та підготовчих прикладах, з використанням підходящих мічених ізотопами реагентів замість раніше використаного неміченого реагенту. Фармацевтично прийнятні сольвати згідно з даним винаходом включають у себе сольвати, у яких розчинник кристалізації може бути заміщений ізотопами, наприклад, D 2O, d6-ацетон, d6ДМСО. Сполуки згідно з даним винаходом, тобто сполуки формули (I), які містять групи, здатні виступати як донори та/або акцептори водневих зв'язків, можуть бути здатні формувати співкристали з підходящими утворювачами співкристалів. Такі співкристали можуть бути приготовлені зі сполук формули (I) шляхом відомих методик формування співкристалів. Такі методики включають здрібнювання, нагрівання, спільне сублімування, спільне плавлення або приведення у контакт у розчині сполук формули (I) з утворювачем співкристалу в умовах проведення кристалізації та виділення отриманих у такий спосіб співкристалів. Підходящі утворювачі співкристалів включають у себе такі, описані у WO 2004/078163. Отже, даний винахід також відноситься до співкристалів, що містять сполуку формули (I). Термін "терапевтично ефективна кількість" сполуки згідно з даним винаходом відноситься до кількості сполуки згідно з даним винаходом, яка буде викликати у пацієнта біологічну або медичну відповідь, наприклад, зниження або інгібування активності ферменту або білку, або зменшення інтенсивності симптомів, полегшення станів, уповільнення або відстрочку прогресії захворювання, або попередження захворювання та т.п. Відповідно до одного необмежуючого варіанту здійснення, термін "терапевтично ефективна кількість" відноситься до кількості сполуки згідно з даним винаходом, яка при введенні суб'єктові є ефективною (1) щонайменше, для часткового полегшення, інгібування, профілактики та/або зменшення інтенсивності стану або порушення або захворювання, (i) опосередкованого геном виживання рухового нейрону (SMN) або продуктом цього гену, або деградацією SMN∆7 або відносними рівнями FL-SMN та SMN∆7, (ii) асоційованого з активністю SMN, або (iii) що характеризується активністю (нормальною або аномальною) SMN; або (2) для зниження або інгібування активності SMN; або (3) для зниження або інгібування експресії SMN1 або SMN2. 17 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 Відповідно до іншого необмежуючого варіанту здійснення, термін "терапевтично ефективна кількість" відноситься до кількості сполуки згідно з даним винаходом, яка при введенні у клітину, або у тканину, або у неклітинний біологічний матеріал, або у середовище є ефективною, щонайменше, для часткового зниження або інгібування активності SMN; або, щонайменше, часткового зниження або інгібування експресії SMN, у обох випадках шляхом модулювання відносних рівнів FL-SMN та SMN∆7. Використовувані у даному документі вирази "терапевтично ефективна кількість" та "ефективна кількість" означають кількість, достатню для зниження, щонайменше, приблизно на 15 відсотків, переважно, щонайменше, на 50 відсотків, більш переважно, щонайменше, на 90 відсотків, та найбільше переважно для запобігання клінічно значимого дефіциту активності, функції та відповіді хазяїна. У якості альтернативи, терапевтично ефективної кількості досить для забезпечення поліпшення клінічно значимого стану/симптому у хазяїна. Ефективна кількість може варіюватися залежно від таких факторів, як розмір та маса суб'єкта, тип захворювання або конкретна сполука згідно з даним винаходом. Наприклад, вибір сполуки згідно з даним винаходом може впливати на визначення розміру "ефективної кількості". Фахівець у даній галузі техніки зможе вивчити фактори, що містяться у даному документі, та дати визначення ефективній кількості сполук згідно з даним винаходом без додаткових експериментів. Схема введення може впливати на визначення розміру ефективної кількості. Сполука згідно з даним винаходом може бути введена суб'єктові як до, так і після початку зв'язаного з дефіцитом SMN стану. Крім того, декілька роздільних дозувань, а також східчасті дозування, можуть вводитися щодоби або послідовно, або доза може бути тривало введена шляхом інфузії або може являти собою болюсну ін'єкцію. Крім того, залежно від гостроти терапевтичної або профілактичної ситуації, дозування сполуки(сполук) згідно з даним винаходом можуть бути пропорційно збільшені або знижені. Використаний у даному документі термін "суб'єкт" відноситься до тварині. Звичайно тварина являє собою ссавця. Термін суб'єкт також відноситься, наприклад, до приматів (наприклад, до людей, чоловічої або жіночої статі), корів, овець, кіз, коней, собак, кішок, кролів, щурів, мишей, риб, птахів та т.п. Згідно з певними варіантами здійснення, суб'єкт являє собою примата. Згідно ще іншими варіантами здійснення, суб'єкт являє собою людину. Використаний у даному документі термін "інгібувати", "інгібування" або "інгібуючий" відноситься до зниженню або супресії даного стану, симптому, порушення або захворювання, або до значимого зниження фонової активності біологічної активності або процесу. Відповідно до одного варіанту здійснення, використаний у даному документі термін "лікувати", "проведення лікування" або "лікування" будь-якого захворювання або порушення відноситься до зменшення інтенсивності захворювання або порушення (тобто до уповільнення або зупинки або зниження розвитку захворювання або, щонайменше, одного з його клінічних симптомів). Згідно з іншим варіантом здійснення, термін "лікувати", "проведення лікування" або "лікування" відноситься до поліпшення або зменшення інтенсивності, щонайменше, одного фізичного параметру, включаючи параметри, які можуть бути неочевидні для пацієнта. Згідно ще з одним варіантом здійснення, термін "лікувати", "проведення лікування" або "лікування" відноситься до модулювання захворювання або порушення, як до фізичного (наприклад, шляхом стабілізації очевидного симптому) або фізіологічного (наприклад, шляхом стабілізації фізичного параметру), так і до обох. Згідно з ще одним варіантом здійснення, термін "лікувати", "проведення лікування" або "лікування" відноситься до запобігання або відстрочення початку, розвитку або прогресії захворювання або порушення. Згідно із даним документом, суб'єкт є "таким, що потребує" лікування, якщо внаслідок такого лікування такий суб'єкт міг би отримати біологічну, медичну користь або користь, що визначає якість життя. Використовувані у даному документі невизначені артиклі та аналогічні терміни, використовувані у контексті даного винаходу (особливо у контексті формули винаходу), слід витлумачувати як такі, що включають у себе як однину, так і множину, якщо інше не зазначене у даному документі або очевидно не суперечить контексту. Усі способи, описані у даному документі, можуть бути здійснені у будь-якому підходящому порядку, якщо інше не зазначене у даному документі або очевидно не суперечить контексту. Використання всіляких прикладів, або використовувані у даному документі типові вирази (наприклад, "такий як"), призначені лише для кращого висвітлення даного винаходу та не ставить обмеження на обсяг даного винаходу, зазначеного іншим способом. Будь-який асиметричний атом (наприклад, атом вуглецю та т.п.) сполуки(сполук) згідно з даним винаходом може бути присутнім у рацемічно або енантіомерно збагаченій конфігурації, 18 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 наприклад (R)-, (S)- або (R, S)-конфігурації. Згідно з певними варіантами здійснення, кожен асиметричний атом у (R)- або (S)-конфігурації характеризується, щонайменше, 50 % енантіомерною чистотою, щонайменше, 60 % енантіомерною чистотою, щонайменше, 70 % енантіомерною чистотою, щонайменше, 80 % енантіомерною чистотою, щонайменше, 90 % енантіомерною чистотою, щонайменше, 95 % енантіомерною чистотою або, щонайменше, 99 % енантіомерною чистотою. Замісники на атомах з ненасиченими зв'язками можуть, якщо це можливо, бути у цис- (Z)- або транс-(E)-формі. Відповідно, використовувана у даному документі сполука згідно з даним винаходом може бути у формі одного з можливих ізомерів, ротамерів, атропізомерів, таутомерів або їх сумішей, наприклад, у вигляді по суті чистих геометричних (цис- або транс-) ізомерів, діастереоізомерів, оптичних ізомерів (антиподи), рацематів або їх сумішей. На підставі фізико-хімічних відмінностей складових частин, будь-які кінцеві суміші ізомерів можуть бути розділені до чистих або по суті чистих геометричних або оптичних ізомерів, діастереоізомерів, рацематів, наприклад, шляхом хроматографії та/або фракційної кристалізації. Будь-які отримані рацемати кінцевих продуктів або проміжних продуктів можуть бути розділені на оптичні антиподи шляхом відомих способів, наприклад, шляхом розділення їх діастереоізомерних солей, отриманих з оптично активною кислотою або основою, та вивільнення оптично активної сполуки у вигляді кислоти або основи. Зокрема, тому фрагмент основи може бути використаний для розділення сполук згідно з даним винаходом на їхні оптичні антиподи, наприклад, шляхом фракційної кристалізації солі, утвореної з оптично активною кислотою, наприклад, винною кислотою, дибензоїлвинною кислотою, діацетилвинною кислотою, ди-O, O'-паратолуоїлвинною кислотою, мигдальною кислотою, яблучною кислотою або камфор10-сульфоновою кислотою. Рацемічні продукти також можуть бути розділені шляхом хіральної хроматографії, наприклад, високоефективної рідинної хроматографії (ВЕРХ) з використанням хірального адсорбенту. Сполуки згідно з даним винаходом одержують як у вільній формі, у вигляді її солі, так і у вигляді їх пролікарських похідних. Якщо у одній і тій же молекулі присутня як основна група, так і кислотна група, тоді сполуки згідно з даним винаходом також можуть формувати внутрішні солі, наприклад, цвіттеріонні молекули. Крім того, сполуки згідно з даним винаходом, включаючи їх солі, також можуть бути отримані у формі їх гідратів, або включають у собі інші розчинники, використовувані для їхньої кристалізації. Сполуки згідно з даним винаходом можуть самі по собі або навмисно формувати сольвати з фармацевтично прийнятними розчинниками (включаючи воду); тому передбачається, що даний винахід охоплює як сольватовані, так і несольватовані форми. Термін "сольват" відноситься до молекулярного комплексу сполуки згідно з даним винаходом (включаючи її фармацевтично прийнятні солі) з однією або декількома молекулами розчинника. Такі розчинники являють собою звичайно використовувані у галузі фармацевтики розчинники, відомі як нешкідливі для реципієнта, наприклад, вода, етанол та т.п. Термін "гідрат" відноситься до комплексу, у якому молекулою розчиннику є вода. Сполуки згідно з даним винаходом, включаючи їх солі, гідрати та сольвати, можуть самі по собі або навмисно формувати поліморфи. Даний винахід також включає у собі будь-який варіант способу згідно з даним винаходом, при якому у якості вихідної речовини використовують проміжний продукт, отриманий на будьякій його стадії, та проводяться етапи, що залишилися, при яких в умовах проведення реакції вихідні речовини утворюються in situ, або у якому компоненти реакції використовуються у формі їх солей або оптично чистої речовини. Сполуки згідно з даним винаходом та проміжні продукти також можуть бути перетворені один у інший у відповідності зі способами, як правило, відомими фахівцям у даній галузі техніки. Згідно з іншим аспектом, даний винахід відноситься до фармацевтичної композиції, що містить сполуку згідно з даним винаходом або її фармацевтично прийнятну сіль та фармацевтично прийнятний носій. Фармацевтична композиція може бути приготовлена для конкретних шляхів введення, таких як пероральне введення, парентеральне введення та ректальне введення, та т.п. На додаток, фармацевтичні композиції згідно з даним винаходом можуть бути приготовлені у твердій формі (включаючи без обмеження капсули, таблетки, пігулки, гранули, порошки або супозиторії) або у рідкій формі (включаючи без обмеження розчини, суспензії або емульсії). Фармацевтичні композиції можуть бути піддані загальноприйнятим фармацевтичним процедурам, таким як стерилізація, та/або можуть містити 19 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 загальноприйняті інертні розріджувачі, змащення або буферні засоби, а також ад'юванти, такі як консерванти, стабілізатори, зволожувачі, емульгатори та буфери, та т.п. Звичайно фармацевтичні композиції являють собою таблетки або желатинові капсули, що містять активний інгредієнт разом з розріджувачами, наприклад, з лактозою, декстрозою, сахарозою, манітом, сорбітом, целюлозою та/гліцином; зі змащеннями, наприклад, із кремнієм, тальком, стеариновою кислотою, її магнієвої або кальцієвою сіллю та/або поліетиленгліколем; для таблеток також зі зв'язувальними речовинами, наприклад, з алюмосилікатом магнію, крохмальною пастою, желатином, трагакантом, метилцелюлозою, карбоксиметилцелюлозою натрію та/або полівінілпіролідоном; при бажанні з розпушувачами, наприклад, із крохмалями, агаром, альгіновою кислотою та її натрієвою сіллю, або шипучими сумішами; та/або з абсорбентами, барвниками, смакоароматизаторами та підсолоджувачами. Таблетки можуть бути забезпечені плівковим покриттям або кишково-розчинним покриттям у відповідності зі способами, відомими у даній галузі техніки. Підходящі композиції для перорального введення містять ефективну кількість сполуки згідно з даним винаходом у формі таблеток, льодяників, водних або масляних суспензій, дисперсних порошків або гранул, емульсії, твердих або м'яких капсул або сиропів або еліксирів. Композиції, призначені для перорального застосування, готують у відповідності з будь-яким способом, відомим у даній галузі приготування фармацевтичних композицій, та такі композиції можуть містити один або декілька засобів, вибраних з групи, що складається з підсолоджувачів, смакоароматизаторів, барвників та консервантів, з метою забезпечення фармацевтично елегантних та привабливих препаратів. Таблетки можуть містити активний інгредієнт у суміші з нетоксичними фармацевтично прийнятними наповнювачами, які підходять для виробництва таблеток. Такі наповнювачі являють собою, наприклад, інертні розріджувачі, такі як карбонат кальцію, карбонат натрію, лактоза, фосфат кальцію та фосфат натрію; гранулюючі засоби та розпушувачі, наприклад, кукурудзяний крохмаль або альгінова кислота; зв'язувальні речовини, наприклад, крохмаль, желатин або акація; та змащення, наприклад, стеарат магнію, стеаринова кислота або тальк. Таблетки готують без покриття або забезпечують покриттям шляхом відомих методик для відстрочення розпушення та всмоктування у шлунково-кишковому тракті, та забезпечують тим самим безперервну дію протягом тривалого періоду часу. Наприклад, може бути використана речовина із затримкою розпаду у часі, така як гліцерилмоностеарат або гліцерилдистеарат. Лікарські форми для перорального застосування можуть бути представлені у вигляді твердих желатинових капсул, у яких активний інгредієнт змішаний з інертним твердим розріджувачем, наприклад, з карбонатом кальцію, фосфатом кальцію або каоліном, або у вигляді м'яких желатинових капсул, у яких активний інгредієнт змішаний з водою або масляним середовищем, наприклад, з арахісовим маслом, рідким парафіном або оливковим маслом. Певні ін'єкційні композиції являють собою водні ізотонічні розчини або суспензії, та супозиторії переважно готують з жирних емульсій або суспензій. Згадані композиції можуть бути стерилізовані та/або містити ад'юванти, такі як консерванти, стабілізатори, зволожувачі або емульгатори, підсилювачі розчинення, солі для регулювання осмотичного тиску та/або буфери. Крім того, вони можуть також містити інші терапевтично цінні речовини. Згадані композиції готують у відповідності із загальноприйнятими способами змішування, гранулювання або нанесення покриття, відповідно, та містять приблизно 0,1-75 %, або містять приблизно 1-50 % активного інгредієнту. Підходящі композиції для крізьшкірного застосування містять ефективну кількість сполуки згідно з даним винаходом з підходящим носієм. Носії, підходящі для крізьшкірної доставки, включають усмоктувані фармакологічно прийнятні розчинники для полегшення проходження через шкіру пацієнта. Наприклад, крізьшкірні обладнання представлені у формі бандажа, який включає у себе підкладкову частину, резервуар, який містить сполуку необов'язково з носіями, необов'язково бар'єр, що контролює швидкість доставки сполуки у шкіру хазяїна з контрольованою та визначеною швидкістю протягом пролонгованого періоду часу, та засобу для кріплення обладнання на шкірі. Підходящі композиції для місцевих аплікацій, наприклад, на шкіру та око, включають у себе водні розчини, суспензії, мазі, креми, гелі та лікарські форми у вигляді спреїв, наприклад, для доставки шляхом аерозолю та т.п. Такі системи місцевої доставки будуть, зокрема, підходящими для аплікацій на шкіру, наприклад, для лікування раку шкіри, наприклад, для 20 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 профілактичного застосування у кремах від засмаги, лосьйонах, спреях та т.п. Тому вони особливо підходять для застосування у місцевих (включаючи косметичні) лікарських формах, добре відомих у даній галузі техніки. Такі композиції можуть містити солюбілізатори, стабілізатори, підсилювачі тонічності, буфери та консерванти. Використаний у даному документі термін "місцева аплікація" може також відноситися до інгаляції або до інтраназального застосуванню. Вони можуть бути підходящим чином доставлені у формі сухого порошку (як окремо, у вигляді суміші, наприклад, сухої суміші з лактозою, так і у вигляді частки зі змішаних компонентів, наприклад з фосфоліпідами) з порошкового інгалятору або подачі аерозольного спрею з контейнера під тиском, помпи, спрею, атомайзеру або небулайзеру, із застосуванням підходящого пропеленту або без нього. Даний винахід також відноситься до безводних фармацевтичних композицій та лікарських форм, що містить сполуки згідно з даним винаходом у якості активних інгредієнтів, оскільки вода може сприяти деградації певних сполук. Безводні фармацевтичні композиції та лікарські форми згідно з даним винаходом можуть бути приготовлені з використанням безводних інгредієнтів або інгредієнтів з низьким вмістом вологи та в умовах низької вологості або низького зволоження. Безводну фармацевтичну композицію можна приготувати та зберігати таким чином, щоб її безводна природа зберігалася. Отже, безводні композиції упаковують із використанням матеріалів, відомих як такі, що запобігають впливу води, таким чином, що вони можуть бути включені у підходящі лікарські набори. Приклади підходящого упакування включають у себе без обмеження герметично запаяну фольгу, пластмаси, контейнери одноразових доз (наприклад, ампули), блістерні упакування та контурні упакування. Даний винахід також відноситься до фармацевтичних композицій та лікарських форм, які містять один або декілька засобів, що знижують швидкість, з якою розпадається використовувана як активний інгредієнт сполука згідно з даним винаходом. Такі засоби, що називаються у даному документі "стабілізаторами", включають у себе без обмеження антиоксиданти, такі як аскорбінова кислота, рН-буфери або сольові буфери та т.п. Сполуки формули I у вільній формі або формі солі демонструють цінні фармакологічні властивості, наприклад, властивості модулювання продукції повнорозмірного білку SMN, наприклад, як зазначено у представлені у наступних розділах тестах in vitro та in vivo, а тому запропоновані для терапії або для застосування як речовини для досліджень, наприклад, як аналітичні сполуки. Тому, як наступний варіант здійснення, даний винахід відноситься до застосування сполуки формули (I) або її солі у терапії. Згідно з ще одним варіантом здійснення, таку терапію вибирають виходячи із захворювання, яке може піддаватися лікуванню шляхом модулювання продукції повнорозмірного білку SMN. Згідно з іншим варіантом здійснення, таке захворювання вибирають з вище перерахованого переліку, відповідно, спінальної м'язової атрофії. Згідно з іншим варіантом здійснення, даний винахід відноситься до способу лікування захворювання, яке піддають лікуванню шляхом модулювання продукції повнорозмірного білку SMN, що включає у себе введення терапевтично прийнятної кількості сполуки формули (I) або її солі пацієнту, який потребує такої терапії. Згідно з ще одним варіантом здійснення, таке захворювання вибирають з вище перерахованого списку, відповідно, спінальної м'язової атрофії. Тому, як наступний варіант здійснення, даний винахід відноситься до застосування сполуки формули (I) або її солі для виробництва лікарського засобу. Згідно з ще одним варіантом здійснення, лікарський засіб призначений для лікування захворювання, яке може піддаватися лікуванню шляхом модулювання продукції білку SMN. Згідно з іншим варіантом здійснення, таке захворювання вибирають з вище перерахованого переліку, відповідно, спінальної м'язової атрофії. Фармацевтична композиція або комбінація згідно з даним винаходом може являти собою стандартну лікарську форму, що містить приблизно 0,01-1000 мг активного(их) інгредієнту(ів) для суб'єкта з масою приблизно 0,5-70 кг або приблизно 1-20 кг, або що містить приблизно 1500 мг, або приблизно 1-250 мг, або приблизно 1-150 мг, або приблизно 0,5-100 мг, або приблизно 0,01-1 мг, або приблизно 0,01-0,1 мг, або приблизно 1-50 мг активних інгредієнтів. Терапевтично ефективне дозування сполуки, фармацевтичної композиції або їх комбінацій залежить від виду суб'єкта, маси тіла, віку або індивідуального стану, порушення або захворювання, що піддають лікуванню, або його важкості. Середній лікар, клініцист або ветеринар зможе легко визначити ефективну кількість кожного з активних інгредієнтів, необхідну для профілактики, лікування або інгібування прогресування порушення або захворювання. 21 UA 114726 C2 5 10 15 20 25 30 35 40 45 50 55 60 Вищенаведені особливості дозування показові у тестах in vitro та in vivo з використанням переважно ссавців, наприклад, мишей, щурів, собак, мавп або виділених органів, тканин та їх препаратів. Сполуки згідно з даним винаходом можуть застосовуватися in vitro у формі розчинів, наприклад, водних розчинів, та in vivo ентерально або парентерально, переважно внутрішньовенно, наприклад, у вигляді суспензії або водного розчину. Дозування in vitro може -3 -9 варіюватися приблизно між 10 M та 10 M концентраціями. Залежно від шляху введення, терапевтично ефективна in vivo кількість може варіюватися приблизно між 0,1-500 мг/кг або приблизно між 1-100 мг/кг. Сполука згідно з даним винаходом може вводитися як одночасно з одним або декількома іншими терапевтичними засобами, так і до або після них. Сполуку згідно з даним винаходом можна вводити окремо шляхом того ж або іншого шляху введення, або разом з іншими засобами у тій же фармацевтичній композиції. Відповідно до одного варіанту здійснення, даний винахід відноситься до продукту, що містить сполуку формули (I) та, щонайменше, один інший терапевтичний засіб у вигляді комбінованого препарату для одночасного, роздільного або послідовного застосування у терапії. Відповідно до одного варіанту здійснення, така терапія являє собою лікування спінальної м'язової атрофії. Продукти, представлені у вигляді комбінованого препарату, включають у себе композицію, що містить разом сполуку формули (I) та інший(і) терапевтичний(і) засіб(засоби) у складі однієї і тієї ж фармацевтичної композиції, або сполуку формули (I) та інший(і) терапевтичний(і) засіб(засоби) у окремих формах, наприклад, у вигляді набору. Відповідно до одного варіанту здійснення, даний винахід відноситься до фармацевтичної композиції, що містить сполуку формули (I) та інший(і) терапевтичний(і) засіб(засоби). Фармацевтична композиція може необов'язково містити описаний вище фармацевтично прийнятний носій. Відповідно до одного варіанту здійснення, даний винахід відноситься до набору, що включає у себе дві або декілька окремих фармацевтичних композицій, щонайменше, одна з яких містить сполуку формули (I). Відповідно до одного варіанту здійснення, такий набір включає у себе засоби для окремого зберігання згаданих композицій, такі як контейнер, розділений на секції флакон або розділений на секції пакет з фольги. Приклад такого набору являє собою блістерне упакування, яке звичайно використовується для упакування таблеток, капсул та т.п. Набір згідно з даним винаходом може бути використаний для введення різних лікарських форм, наприклад, пероральних та парентеральних, для введення окремих композицій через різні інтервали часу, або для титрування окремих композицій один іншим. Для полегшення дотримання режиму, такий набір згідно з даним винаходом звичайно містить інструкції із введення. При комбінованих видах терапії згідно з даним винаходом сполука згідно з даним винаходом та інший терапевтичний засіб можуть бути зроблені та/або приготовлено одним і тим же або різними виробниками. Більше того, сполука згідно з даним винаходом та інший терапевтичний засіб можуть бути об'єднані для комбінованої терапії: (i) до одержання комбінованого продукту лікарем (наприклад, у випадку набору, що містить сполуку згідно з даним винаходом та інший терапевтичний засіб); (ii) безпосередньо самим лікарем (або під керівництвом лікаря) прямо перед введенням; (iii) у організмі самих пацієнтів, наприклад, у процесі послідовного введення сполуки згідно з даним винаходом та іншого терапевтичного засобу. Наступні приклади призначені для ілюстрації даного винаходу та не повинні тлумачитися як обмежуючі його. Значення температури представлені у градусах Цельсію. Якщо не зазначене інше, всі випарювання проводять в умовах зниженого тиску, переважно при значеннях тиску приблизно між 15 мм рт.ст. та 100 мм рт.ст. (=20-133 мбар). Структуру кінцевих продуктів, проміжних продуктів та вихідних речовин підтверджували за стандартними аналітичними методами, наприклад, мікрохімічним аналізом та одержанням спектроскопічних характеристик, наприклад, методами МС, ІЧ, ЯМР. Використані скорочення є загальноприйнятими у даній галузі техніки. Усі вихідні речовини, структурні елементи, реагенти, кислоти, основи, осушувачі, розчинники, каталізатори та уловлювачі, використані для синтезу сполук згідно з даним винаходом, є або комерційно доступними, або можуть бути отримані за способами органічного синтезу, відомими середньому фахівцеві у даній галузі техніки (Houben-Weyl 4th Ed. 1952, Methods of Organic Synthesis, Thieme, Volume 21). Крім того, сполуки згідно з даним винаходом можуть бути отримані за способами органічного синтезу, відомими середньому фахівцеві у даній галузі техніки, як представлено у наступних прикладах. Одержання сполук 22 UA 114726 C2 5 10 15 20 25 30 35 40 45 Розуміється, що у наступному описі комбінації замісників та/або змінних у описаних формулах є припустимими, якщо тільки такі фактори приводять до стабільних сполук. Фахівцям у даній галузі техніки також слід враховувати, що у описаних нижче процесах функціональні групи проміжних сполук можуть потребувати захисту підходящими захисними групами. Такі функціональні групи включають у себе гідрокси, фенол, аміно та карбокси. Підходящі захисні групи для гідрокси або фенолу включають у себе триалкілсиліл або діарилалкілсиліл (наприклад, трет-бутилдиметилсиліл, трет-бутилдифенілсиліл або триметилсиліл), тетрагідропіраніл, бензил, заміщений бензил, метил та т.п. Підходящі захисні групи для аміно, амідино та гуанідино включають у себе трет-бутоксикарбоніл, бензилоксикарбоніл та т.п. Підходящі захисні групи для карбокси включають у себе алкільні, арильні або арилалкільні складні ефіри. Захисні групи можуть вводитися або видалятися у відповідності зі стандартними методиками, які добре відомі фахівцям у даній галузі техніки та які описані у даному винаході. Застосування захисних груп докладно описане у Green, T.W. and P.G.M. Wutz, Protective Groups in Organic Synthesis (1999), 3rd Ed., Wiley. Захисна група також може являти собою полімерну смолу, наприклад, смолу Ванга або 2-хлортритилхлоридну смолу. Фахівцями у даній галузі техніки також слід враховувати, що хоча такі захищені похідні сполук згідно з даним винаходом не можуть мати фармакологічну активність як такі, вони можуть бути введені суб'єктові, а після цього метаболізуватися у організмі з утворенням сполук згідно з даним винаходом, які є фармакологічно активними. Отже, такі похідні можуть бути описані як "проліки". Усі проліки сполук згідно з даним винаходом включені у обсяг даного винаходу. У наступних реакційних схемах представлені способи одержання сполук згідно з даним винаходом. Розуміється, що фахівець у даній галузі техніки буде здатний одержати зазначені сполуки за аналогічними способами або способами, добре відомими фахівцеві у даній галузі техніки. У загальному випадку, вихідні компоненти та реагенти можуть бути отримані з таких джерел, як Sigma Aldrich, Lancaster Synthesis, Inc., Maybridge, Matrix Scientific, TCI, Fluorochem USA, Strem та інших комерційних постачальників, або синтезовані у відповідності з джерелами, відомими фахівцям у даній галузі техніки, або отримані за способами, описаними у даному винаході. Якщо не зазначене конкретно, значення A, B, X, R, R 1, R2, R3, R4 визначені у розділі "Опис". У загальному випадку, піридазинові сполуки формули (I) відповідно до даного винаходу можуть бути синтезовані за наступним загальним способом, описаним на схемі 1. Вихідні речовини для зазначеної вище реакційної схеми є комерційно доступними або можуть бути отримані за способами, відомими спеціалісту у даній галузі техніки, або за способами, розкритими у даному документі. У загальному випадку, сполуки згідно з даним винаходом отримували, як представлено вище на реакційній схемі 1, наступним чином: У реакції заміщення або опосередкованої металом реакції крос-сполучення (реакція Бухвальда) здійснювали взаємодію дигалогенпіридазину (1) зі спиртом або аміном (B) з одержанням піридазинового проміжного продукту (2). У опосередкованій металом перехідної валентності реакції крос-сполучення, такій як реакція за Судзукі, між галоїдною сполукою (2) та заміщеною арильною або гетероарильною сполукою A, такою як боронова кислота або складний ефір боронової кислоти, отримували сполуку (3) формули (I) згідно з даним винаходом. 23 UA 114726 C2 На додаток, сполуки формули (I) можуть бути синтезовані наступним загальним способом, описаним на схемі 2. Загальна схема 2 5 10 15 20 25 30 35 40 45 Вихідні речовини для зазначеної вище реакційної схеми є комерційно доступними або можуть бути отримані за способами, відомими спеціалісту у даній галузі техніки, або способами, розкритими у даному документі. У загальному випадку, сполуки згідно з даним винаходом отримували, як представлено вище на реакційній схемі 2, наступним чином: У опосередкованій металом перехідної валентності реакції крос-сполучення, такій як реакція за Судзукі, здійснювали взаємодію дигалогенпіридазину (1) із заміщеною арильною або гетероарильною сполукою A, такою як боронова кислота або складний ефір боронової кислоти, з одержанням піридазинового проміжного продукту (4). У реакції заміщення здійснювали взаємодію піридазинового проміжного продукту (4) зі спиртом або аміном (B) з одержанням піридазину (3) формули (I) згідно з даним винаходом. Сполуки формули (I) також можуть бути отримані наступним загальним способом, описаним на схемі 3. Загальна схема 3 Вихідні речовини для зазначеної вище реакційної схеми є комерційно доступними або можуть бути отримані за способами, відомими спеціалісту у даній галузі техніки, або способами, розкритими у даному документі. У загальному випадку, сполуки згідно з даним винаходом отримували, як представлено вище на реакційній схемі 3, наступним чином: У опосередкованій металом перехідної валентності реакції крос-сполучення, такій як реакція за Судзукі, здійснювали взаємодію дигалогенпіридазину (1) із заміщеною арильною або гетероарильною сполукою A, такою як боронова кислота або складний ефір боронової кислоти, з одержанням піридазинового проміжного продукту (4). У другому опосередкованому металом крос-сполученні, такому як реакція за Судзукі, здійснювали взаємодію піридазинового проміжного продукту (4) з одержанням піридазину (3) формули (I) згідно з даним винаходом. Для одержання сполук формули (I) згідно з даним винаходом, загальних схем 1, 2 та 3 можна дотримуватися для цілого ряду ароматичних A груп, таких як заміщені феноли, нафтили, гетероарили тощо, та різних амінових або спиртових B груп, таких як заміщені амінопіперидини, піперазини, гомопіперазини, 4-гідроксипіперидини тощо. Для одержання кінцевих сполук формули (I) можуть бути потрібні загальноприйняті для захисних груп алгоритми дій. Всі вихідні речовини, структурні елементи, реагенти, кислоти, основи, осушувачі, розчинники, каталізатори та уловлювачі, використані для синтезу сполук згідно з даним винаходом, є або комерційно доступними, або можуть бути отримані за способами органічного синтезу, відомими середньому спеціалісту у даній галузі техніки. Крім того, сполуки згідно з даним винаходом можуть бути отримані за способами органічного синтезу, відомими середньому спеціалісту у даній галузі техніки, як представлено у наступних прикладах. Наступні приклади призначені для ілюстрації даного винаходу та не повинні тлумачитися як обмежуючі його. Значення температури представлені у градусах Цельсію. Якщо не зазначено інше, всі упарювання проводять в умовах зниженого тиску, переважно при значеннях тиску приблизно між 15 мм рт.ст. та 100 мм рт.ст. (=20-133 мбар). Структуру кінцевих продукті, проміжних продуктів та вихідних речовин підтверджували стандартними аналітичними методами, наприклад, мікрохімічним аналізом та одержанням спектроскопічних характеристик, наприклад, методами РХ/МС, ЯМР, елементного аналізу. Використані скорочення є 24 UA 114726 C2 5 10 15 20 25 30 35 40 загальноприйнятими у даній галузі техніки, та їх перелік представлений у кінці розділу "Експериментальна частина". Підготовчий приклад 1 Проміжний продукт 1-1: Синтез 6-хлор-N-метил-N-(2,2,6,6-тетраметилпіперидин-4іл)піридазин-3-аміну: У круглодонній колбі ємкістю 300 мл до 3,6-дихлорпіридазину (4 г, 26,8 ммоль) та N, 2,2,6,6пентаметилпіперидин-4-аміну (7,32 г, 43,0 ммоль) додавали бутан-1-ол (67 мл) з одержанням безбарвного розчину. Суміш нагрівали до 120 °C впродовж 72 год. Бутан-1-ол видаляли з використанням роторного випарнику. Залишок розподіляли між водою та DCM, та додатково екстрагували водний шар DCM. Об'єднані органічні шари промивали водою та сольовим розчином, сушили над MgSO4 та концентрували в умовах вакууму. Чорну неочищену речовину перемішували у невеликій кількості EtOAc впродовж ночі, та збирали отриману не зовсім білу тверду речовину з одержанням 6-хлор-N-метил-N-(2,2,6,6-тетраметилпіперидин-4-іл)піридазин3-аміну (проміжний продукт 1-1, 4,18 г, 14,78 ммоль, вихід 55,0 %). РХ/МС Rt=0,8 хвил. (умови 1 проведення B), МС (M+1)=283,5, H ЯМР (400 МГц, МЕТАНОЛ-d4) δ м.ч. 7,40 (д, J=9,60 Гц, 1H), 7,14 (д, J=9,60 Гц, 1H), 4,96-5,13 (м, 1H), 2,93 (c, 3H), 1,59-1,68 (м, 2H), 1,51 (т, J=12,38 Гц, 2H), 1,20 (c, 6H), 1,33 (c, 6H). Підготовчий приклад 2 Проміжний продукт 1-2: Синтез 6-хлор-N-(2,2,6,6-тетраметилпіперидин-4-іл)-піридазин-3аміну: Суміш 3,6-дихлорпіридазину (6,26 г, 42 ммоль) та 2,2,6,6-тетраметилпіперидин-4-аміну (14,7 мл, 84 ммоль) перемішували нерозведеною при 120 °C впродовж 1 год. До цієї неочищеної суміші додавали н-бутанол (40 мл) та перемішували реакційну суміш при 120 °C впродовж 1 год. Неочищену реакційну суміш охолоджували до кімнатної температури та розводили водою та CH2Cl2. Органічний шар сушили над MgSO4, фільтрували та концентрували. Неочищену речовину перекристалізовували з CH 3CN з одержанням 6-хлор-N-(2,2,6,6-тетраметилпіперидин4-іл)піридазин-3-аміну (проміжний продукт 1-2, 7,3 г) у вигляді не зовсім білої твердої речовини. 1 РХ/МС Rt=1,10 хвил. (умови проведення B), МС (M+1)=269,2, H ЯМР (400 МГц, ХЛОРОФОРМd) δ м.ч. 7,08 (д, J=9,3 Гц, 1H), 6,54 (д, J=9,3 Гц, 1H), 4,53 (д, J=7,6 Гц, 1H), 4,05-4,26 (м, 1H), 1,98 (дд, J=12,6, 3,8 Гц, 2H), 1,22 (c, 6H), 1,08 (c, 6H), 0,93 (уявний т, J=12,1 Гц, 2H). Підготовчий приклад 3 Проміжний продукт 1-3: Синтез 3-хлор-6-(2,2,6,6-тетраметилпіперидин-4-ілокси)-піридазину: До розчину 2,2,6,6-тетраметилпіперидин-4-олу (106 мг, 0,67 ммоль) у DMF (6,7 мл) додавали 60 мас. % NaH (35 мг, 0,87 ммоль). Розчин перемішували при к.т. впродовж 30 хвил., а потім додавали 3,6-дихлорпіридазин (100 мг, 0,67 ммоль) та перемішували реакційну суміш впродовж 1 год. Неочищену реакційну суміш розводили EtOAc. Органічний шар промивали водою (5), сольовим розчином, сушили над Na2SO4, фільтрували та концентрували в умовах зниженого тиску з одержанням 3-хлор-6-(2,2,6,6-тетраметилпіперидин-4-ілокси)піридазину (проміжний продукт 1-3, 135 мг). Неочищену речовину використовували без додаткового очищення. РХ/МС 1 Rt=1,22 хвил. (умови проведення B); МС (M+1)=270,2, H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ м.ч. 25 UA 114726 C2 5 10 15 20 25 30 35 40 7,53 (c, 1H), 7,37 (д, J=9,1 Гц, 1H), 6,91 (д, J=9,1 Гц, 1H), 5,68-5,78 (м, 1H), 2,20 (дд, J=12,4, 4,0 Гц, 2H), 1,32 (c, 6H), 1,27-1,29 (м, 2H), 1,20 (c, 6H). Підготовчий приклад 4 Проміжний продукт 1-4: Синтез 6-хлор-N-метил-N-(1,2,2,6,6-пентаметилпіперидин-4іл)піридазин-3-аміну: До охолодженої до 0 °C суспензії 6-хлор-N-(1,2,2,6,6-пентаметилпіперидин-4-іл)піридазин-3аміну (проміжний продукт 1-5, 4,0 г, 14,1 ммоль) у DMF (140 мл) порціями додавали 60 мас. % NaH (735 мг, 18,39 ммоль). Реакційну суміш нагрівали до к.т. та перемішували впродовж 60 хвилин. Через 60 хвилин додавали метилйодид (0,88 мл, 14,1 ммоль) та додатково перемішували реакційну суміш впродовж 3 год., а потім повільно гасили додаванням води при кімнатній температурі. Неочищену реакційну суміш розводили EtOAc. Органічний шар промивали водою (5), сольовим розчином, сушили над MgSO 4, фільтрували та концентрували в умовах зниженого тиску з одержанням 6-хлор-N-метил-N-(1,2,2,6,6-пентаметилпіперидин-4іл)піридазин-3-аміну (проміжний продукт 1-4, 3,98 г). Неочищену речовину використовували далі 1 без додаткового очищення. РХ/МС Rt=1,16 хвил. (умови проведення B), МС (M+1)=297,0, H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ м.ч. 7,10 (д, J=9,6 Гц, 1H), 6,69 (д, J=9,6 Гц, 1H), 4,79-5,00 (м, 1H), 2,86 (c, 3H), 2,22 (c, 3H), 1,61-1,73 (м, 2H), 1,48-1,57 (м, 2H), 1,14 (c, 6H), 1,10 (c, 6H). Проміжний продукт 1-5: Синтез 6-хлор-N-(1,2,2,6,6-пентаметилпіперидин-4-іл)піридазин-3аміну: Цю речовину отримували двома партіями. Партія 1: Суміш 1,2,2,6,6-пентаметилпіперидин-4-аміну (15,1 г, 89,0 ммоль) та 3,6дихлорпіридазину (6,6 г, 44,3 ммоль) нагрівали нерозведеними при 120 °C впродовж 30 хвил. Неочищену речовину отвердівали та повторно суспендували у н-бутанолі (45 мл). Неочищену суміш додатково перемішували при 120 °C впродовж 2 год., потім нагрівали до 160 °C впродовж 1 год., а потім охолоджували та об'єднували з партією 2 для виділення продукту. Партія 2: Суміш 1,2,2,6,6-пентаметилпіперидин-4-аміну (14,2 г, 83 ммоль) та 3,6дихлорпіридазину (6,2 г, 41,6 ммоль) у н-бутанолі (10 мл) нагрівали при 120 °C впродовж 120 хвил. Неочищену речовину отвердівали та повторно суспендували у н-бутанолі (15 мл) та нагрівали при 120 °C впродовж 1 год. Цю неочищену речовину об'єднували з партією 1 для виділення та очищення продукту. До об'єднаної неочищеної речовини додавали воду та CH 2Cl2, органічний шар розділяли, промивали водою та сольовим розчином, сушили над MgSO 4, фільтрували та концентрували. Неочищену речовину перекристалізовували з CH 3CN (400 мл) з одержанням 6-хлор-N-(1,2,2,6,6-пентаметилпіперидин-4-іл)піридазин-3-аміну (проміжний продукт 1-5, 15,5 г, перший збір). Повторювали перекристалізацію з використанням CH 3CN з одержанням другого збору 6-хлор-N-(1,2,2,6,6-пентаметилпіперидин-4-іл)піридазин-3-аміну 1 (проміжний продукт 1-5, 3,98 г). РХ/МС Rt=1,10 хвил. (умови проведення B); МС (M+1)=283,0, H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ м.ч. 7,15 (д, J=9,3 Гц, 1H), 6,65 (д, J=9,3 Гц, 1H), 4,70 (д, J=7,3 Гц, 1H), 4,08-4,26 (м, 1H), 2,31 (c, 3H), 1,89-2,09 (м, 2H), 1,42 (уявний т, J=12,1 Гц, 2H), 1,21 (c, 6H), 1,15 (c, 6H). Підготовчий приклад 5 Проміжний продукт 2-1: Синтез 3-хлор-6-(2-метокси-4-(1H-піразол-1-іл)-феніл)піридазину: 26 UA 114726 C2 5 10 15 20 25 30 35 40 45 Стадія 1: (4-бром-3-метоксифеніл)гідразин 4-Бром-3-метоксианілін (3,0 г, 14,85 ммоль) суспендували у концентрованій HCl (50 мл) та охолоджували суміш до 0 °C на бані з льодом/водою. До реакційної суміші дуже повільно додавали розчин нітриту натрію (1,23 г, 17,82 ммоль) у 10 мл води. Суміш ставала жовтою, а потім коричневою з жовтою замутненістю, що вказує на діазотування. Сіль діазонію підтримували при 0 °C впродовж 1 години, а потім дуже повільно (увага, надзвичайно екзотермічний процес) додавали розчин дигідрату хлориду олова(II) (10,05 г, 44,5 ммоль) у концентрованій HCl (20 мл). Реакційну суміш перемішували впродовж 2 год. при 0 °C, а потім при к.т. впродовж ночі. Реакційну суміш фільтрували, та промивали осад на фільтрі холодною H2O з одержанням (4-бром-3-метоксифеніл)гідразину у вигляді рудуватої твердої речовини (3,1 + г, МС: 218 [M+H ]). Стадія 2: 1-(4-бром-3-метоксифеніл)-1H-піразол До розчину (4-бром-3-метоксифеніл)гідразину (62 г, 245 ммоль) у етанолі (310 мл) впродовж декількох хвилин додавали тетраметоксипропан (40,2 г, 245 ммоль), та нагрівали суміш до внутрішньої температури 70 °C. Суміш перемішували при 70 °C впродовж 1,5 год., а потім повільно охолоджували до к.т. Етанол видаляли в умовах вакууму, та суспендували залишок у EtOAc. Залишок нейтралізували додаванням 1 M водного гідроксиду натрію (~700 мл) з індукцією преципітації. Двофазну суміш фільтрували, фільтрат екстрагували EtOAC, сушили над сульфатом натрію та концентрували з одержанням 30 г 1-(4-бром-3-метоксифеніл)-1H+ піразолу у вигляді чорної твердої речовини (30 г, МС: 254 [M+H ]). Стадія 3: 1-(3-метокси-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)феніл)-1H-піразол У круглодонну колбу ємкістю 2 л додавали 1-(4-бром-3-метоксифеніл)-1H-піразол (28,5 г, 113 ммоль), біс(пінаколато)дибор (42,9 г, 169 ммоль), карбонат калію (15,56 г, 113 ммоль) та адукт PdCl2(dppf)·CH2Cl2 (9,20 г, 11,26 ммоль), а потім додавали діоксан (700 мл). Реакційну суміш продували N2 та перемішували впродовж ночі у атмосфері N2 при внутрішній температурі 84 °C. Реакційну суміш фільтрували через лійку з одноразовим фільтром та концентрували на силікагелі. Суміш очищали методом колонкової хроматографії (20 % EtOAc у гептанах). Цільові фракції збирали та концентрували з одержанням 13,5 г 1-(3-метокси-4-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)феніл)-1H-піразолу. Стадія 4: 3-хлор-6-(2-метокси-4-(1H-піразол-1-іл)феніл)піридазин У 3-горлу круглодонну колбу ємкістю 250 мл, оснащену магнітною мішалкою та впуском азоту, завантажували 3,6-дихлорпіридизин (11,99 г, 80 ммоль), 1-(3-метокси-4-(4,4,5,5тетраметил-1,3,2-діоксаборолан-2-іл)феніл)-1H-піразол (16,1 г, 53,6 ммоль), карбонат натрію (17,06 г, 161 ммоль) та адукт дихлориду 1,1′-біс(дифенілфосфіно)фероценпаладію та дихлорметану (3,07 г, 3,75 ммоль). Додавали 1,4-діоксан (274 мл) та деіонізовану воду (46 мл), та тричі дегазували/заповнювали азотом реакційну суміш. Реакційну суміш нагрівали у тефлоновому нагрівачі до 85 °C впродовж 16 год. Після видалення 1,4-діоксану в умовах вакууму залишок суспендували у етилацетаті та фільтрували через заповнену целітом лійку з фритованого скла. Фільтрат концентрували на силікагелі та очищали на колонці з 330 г силікагелю, елююючи 10-35 % етилацетатом у гептанах. Фракції, що містять продукт, концентрували до 10 % об'єму, суспендували у суміші етилацетат/гептани (3/1, 100 мл), перемішували при к.т. впродовж 1 год., а потім фільтрували з одержанням 7 г (46 %) 3-хлор-61 (2-метокси-4-(1H-піразол-1-іл)феніл)піридазину у вигляді твердої речовини. H ЯМР (600 МГц, ХЛОРОФОРМ-d) δ 8,12 (дд, J=8,80, 11,30 Гц, 2H), 8,05 (д, J=1,88 Гц, 1H), 7,80 (c, 1H), 7,61 (д, J=1,25 Гц, 1H), 7,54 (д, J=9,03 Гц, 1H), 7,35 (дд, J=1,44, 8,22 Гц, 1H), 6,55 (c, 1H), 4,00 (c, 3H). Підготовчий приклад 6 Проміжний продукт 2-2: Синтез 2-(6-хлорпіридазин-3-іл)-5-(1H-піразол-1-іл)-фенолу: 27 UA 114726 C2 5 10 15 20 25 30 35 40 До розчину 3-хлор-6-(2-метокси-4-(1H-піразол-1-іл)феніл)піридазину (проміжний продукт 2-1, 8,6 г, 30 ммоль) у DCM (150 мл) при 0 °C додавали BCl3 (1 M у DCM, 91 мл, 91 ммоль) та перемішували реакційну суміш впродовж 5 год. при к.т. До реакційної суміші при 0 °C додавали MeOH (50 мл), потім нагрівали реакційну суміш до к.т., та випарювали розчинник в умовах зниженого тиску. Неочищену речовину обробляли гарячим CH 3CN, а потім охолоджували до 5 °C. Суміш фільтрували та отримували 2-(6-хлорпіридазин-3-іл)-5-(1H-піразол-1-іл)фенол 1 (проміжний продукт 2-2, 7,6 г, 86 %) у вигляді жовтої твердої речовини. МС [M+H]: 273,2; H ЯМР (400 МГц, ДМСО-d6) δ 11,95 (c, 1H), 8,59 (д, J=2,0 Гц, 1H), 8,49 (д, J=9,0 Гц, 1H), 8,09 (д, J=8,5 Гц, 1H), 8,04 (д, J=9,0 Гц, 1H), 7,80 (д, J=2,0 Гц, 1H), 7,56 (д, J=2,0 Гц, 1H), 7,51 (дд, J=8,5, 2,0 Гц, 1H), 6,59 (т, J=2,0 Гц, 1H). Підготовчий приклад 7 Проміжний продукт 3-1: Синтез 7-(бензилокси)-6-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)нафталін-2-олу: У колбу ємкістю 250 мл з 7-(бензилокси)-6-бромнафталін-2-олом (2,03 г, 6,17 ммоль) додавали біс(пінаколато)дибор (3,13 г, 12,33 ммоль), KOAc (3,63 г, 37,0 ммоль) та адукт PdCl2(dppf)·CH2Cl2 (0,504 г, 0,617 ммоль). Потім додавали ДМСО (30,8 мл), та приєднували зворотний холодильник. Реакційну суміш дегазували/заповнювали N 2 (2), а потім нагрівали при 100 °C впродовж ночі. Реакційну суміш охолоджували до кімнатної температури, фільтрували через целіт (заповнена фільтр-лійка) з використанням EtOAc та концентрували в умовах вакууму до неочищеного масла. Методом флеш-хроматографії, елююючи 5-30 % EtOAc у гептані, отримували 7-(бензилокси)-6-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)нафталін-2ол (вихід 58 %) у вигляді безбарвного масла. РХ/МС Rt=1,72 хвил. (умови проведення C). МС 1 (M+1)=377,6, HЯМР (400 МГц, МЕТАНОЛ-d4) δ м.ч. 8,07 (c, 1H), 7,68 (т, J=8,91 Гц, 3H), 7,367,43 (м, 2H), 7,28-7,34 (м, 1H), 7,09 (c, 1H), 7,02 (д, J=2,51 Гц, 1H), 6,92 (дд, J=8,78, 2,51 Гц, 1H), 5,21 (c, 2H), 1,40 (c, 12H). Підготовчий приклад 8 Проміжний продукт 4-1: Синтез (6S)-6-((S)-1-(трет-бутилдиметилсилілокси)-етил)-2,2диметилпіперидин-4-олу: Стадія 1. (S)-етил-2-(трет-бутилдиметилсилілокси)пропаноат До розчину (S)-етиллактату (11,8 г, 100 ммоль) у DMF (50 мл) додавали імідазол (10,2 г, 150 ммоль). Суміш охолоджували на бані з льодом, та трьома порціями додавали третбутилдиметилсилілхлорид (15,8 г, 105 ммоль) з інтервалами у 30 хвил. між кожним додаванням. Реакційну суміш перемішували впродовж ночі. Реакційну суміш розводили водою (30 мл) та екстрагували Et2O (250 мл). Об'єднані екстракти промивали сольовим розчином, сушили над MgSO4 та концентрували в умовах вакууму. Залишок піддавали дистиляції в умовах вакууму (т.кип. 70-78 °C, 0,5 мм рт.ст.) з одержанням 22,07 г (95 %) (S)-етил-2-(трет1 бутилдиметилсилілокси)пропаноату: H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ 4,32 (кв., J=6,6 Гц, 28
ДивитисяДодаткова інформація
Назва патенту англійською1,4-disubstituted pyridazine analogs and methods for treating smn-deficiency-related conditions
Автори англійськоюCheung, Atwood, Chin, Donovan Noel, Dales, Natalie, Fazal, Aleem, Hurley, Timothy Brian, Kerrigan, John, O'Brien, Gary, Shu, Lei, Sun, Robert, Sung, Moo
Автори російськоюЧун Этвуд, Цзинь Донован Ноель, Дэйлз Натали, Фазаль Алим, Хэрли Тимоти Брайен, Кэрриган Джон, О'Браен Гэри, Шу Лэй,Сан Роберт, Санг Му
МПК / Мітки
МПК: C07D 401/14, C07D 403/14, C07D 471/14, C07D 401/12, C07D 417/14, C07D 471/08, C07D 487/10, C07D 409/14, C07D 487/04, A61K 31/501, C07D 471/04, C07D 413/14, C07D 405/14
Мітки: дефіцитом, лікування, станів, 1,4-дизаміщені, способи, аналоги, пов'язаних, піридазину
Код посилання
<a href="https://ua.patents.su/137-114726-14-dizamishheni-analogi-piridazinu-ta-sposobi-likuvannya-povyazanikh-z-deficitom-smn-staniv.html" target="_blank" rel="follow" title="База патентів України">1,4-дизаміщені аналоги піридазину та способи лікування пов’язаних з дефіцитом smn станів</a>
Попередній патент: Курильний виріб, призначений для використання з внутрішнім нагрівальним елементом
Наступний патент: Бронежилет
Випадковий патент: Формувач періодичної послідовності триімпульсних кодових серій з програмованою тривалістю паузи між імпульсами у серії













































































































































