Антивірусні фосфінатні сполуки
Номер патенту: 96295
Опубліковано: 25.10.2011
Автори: Кім Чоунг У., Шенг Ксіаонінг К., Чо Езоп, Кларк Майкл, Ванг Джіанйїнг, Піун Хіунгджунг, Доерффлер Едвард, Кесейріз Ентоні, Чодгарі Клім, Фердіс Мерайя
Формула / Реферат
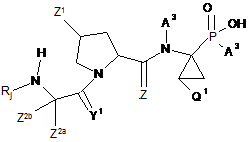
1. Сполука формули (II):
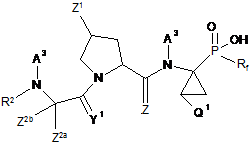 (II)
(II)
або її фармацевтично прийнятна сіль, у якій:
R2 вибирають з
a) -C(Y1)(A3),
b) (С2-10)алкілу, (С3-7)циклоалкілу або (С1-4)алкіл-(С3-7)циклоалкілу, де зазначений циклоалкіл та алкілциклоалкіл можуть бути необов'язково одно-, ди- або тризаміщеними (С1-3)алкілом, або
де зазначений алкіл, циклоалкіл та алкілциклоалкіл може бути необов'язково заміщений одним або двома замісниками, вибраними з гідроксигрупи та О-(С1-4)алкілу, або
де кожна з зазначених алкільних груп може бути необов'язково заміщена одним, двома або трьома галогенами, або
де кожна з зазначених циклоалкільних груп є п'ятичленною, шестичленною або семичленною, причому одна або дві -СН2-групи, що не є безпосередньо зв'язаними одна з іншою, можуть бути необов'язково заміщеними, заміненими -О-, таким чином, що атом О зв'язаний з атомом N, до якого приєднаний R2 за допомогою щонайменше двох атомів С,
c) фенілу, (С1-3)алкілфенілу, гетероарилу або (С1-3)алкілгетероарилу,
де гетероарильні групи є п'ятичленними або шестичленними, що мають від одного до трьох гетероатомів, вибраних з N, О та S, де зазначені фенільні та гетероарильні групи можуть бути необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, -ОН, (С1-4)алкілу, О-(С1-4)алкілу, S-(С1-4)алкілу, -NH2, -CF3, -NH(С1-4)алкілу та -N((С1-4)алкіл)2, -CONH2 та -СОNН-(С1-4)алкілу; та де зазначений (С1-3)алкіл може бути необов'язково заміщеним одним або більшою кількістю атомів галогену; або
d) -S(O)2(A3);
R3 являє собою Н або (С1-6)алкіл;
Y1 незалежно являє собою О, S, N(A3), N(O)(A3), N(OA3), N(O)(OA3) або N(N(A3)(A3));
Z являє собою О, S або NR3;
Z1 являє собою:
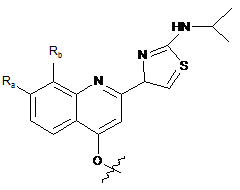 ,
,
Ra являє собою Н або (С1-6)алкоксигрупу;
Rb являє собою Н, F, Сl, Вr, І або (С1-6)алкіл;
Z2b являє собою Н, (С1-6)алкіл, (С2-8)алкеніл, (С2-8)алкініл;
Z2a являє собою (С1-10)алкіл, (С2-10)алкеніл, (С2-10)алкініл, де будь-який атом вуглецю може бути необов'язково замінений гетероатомом, вибраним з О, S або N;
Q1 являє собою (С1-8)алкіл, (С2-8)алкеніл або (С2-8)алкініл, за умови, що Q1 та Z2а разом з атомами, до яких вони приєднані, утворюють гетероцикл, який може бути необов'язково заміщеним одним або більшою кількістю оксо (=О) груп або А3;
А3 незалежно вибирають з алкілу, алкенілу, алкінілу, амідогрупи, імідогрупи, іміногрупи, CF3, CH2CF3, циклоалкілу, арилу, аралкілу, алкоксигрупи, арилоксигрупи, гетероциклу, -(СН2)m-гетероциклу, -(СН2)mС(О)Оалкілу, -О-(СН2)m-О-С(О)-Оалкілу, -О-(СН2)m-О-С(О)-(СН2)m-алкілу, -(СН2)mО-С(О)-О-алкілу, -(СН2)mО-С(О)-О-циклоалкілу, -N(Н)С(Ме)С(О)О-алкілу або алкоксіарилсульфонаміду,
необов'язково кожен незалежно А3 та Q1 разом з одним або більшою кількістю А3 або Q1 груп утворює кільце;
А2 незалежно вибирають з PRT, Н, алкілу, алкенілу, алкінілу, аміногрупи, амінокислоти, алкоксигрупи, арилоксигрупи, ціаногрупи, галоалкілу, циклоалкілу, арилу, гетероарилу, алкілсульфонаміду або арилсульфонаміду, необов'язково заміщених за допомогою А3,
m являє собою 0-6; та
Rf являє собою Н, алкіл, алкеніл, алкініл, арил, гетероарил або циклоалкіл, причому Rf необов'язково заміщений одним або більшою кількістю Rg;
кожен Rg незалежно являє собою галогрупу, гідроксигрупу, ціаногрупу, арилтіогрупу, циклоалкіл, арил, гетероарил, алкоксигрупу, NRhRi, -C(=O)NRhRi, де кожен арил та гетероарил необов'язково заміщений одним або більшою кількістю алкілів, галогруп, гідроксигруп, ціаногруп, нітрогруп, аміногруп, алкоксигруп, алкоксикарбонілів, алканоїлоксигруп, галоалкілів або галоалкоксигруп, та
кожен Rh та Ri незалежно являє собою Н, алкіл або галоалкіл.
2. Сполука або її фармацевтично прийнятна сіль за п. 1, у якій Z1 вибраний з наступних структур:
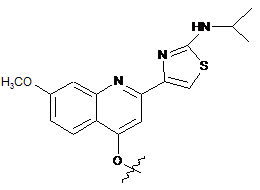 ,
, 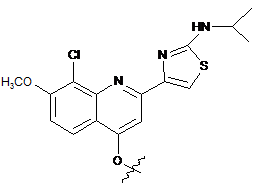 ,
,
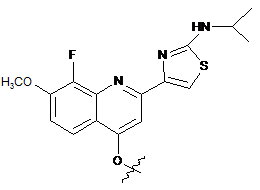 ,
, 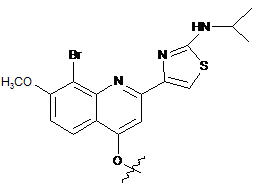 ,
,
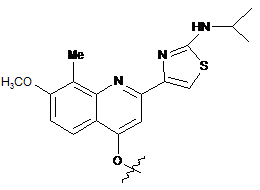 .
.
3. Сполука або її фармацевтично прийнятна сіль за п. 1 або п. 2, у якій Rf являє собою алкіл, алкеніл або алкініл, причому Rf заміщений арилом, який необов'язково заміщений одним або більшою кількістю алкілів, галогруп, гідроксигруп, ціаногруп, нітрогруп, аміногруп, алкоксигруп, алкоксикарбонілів, алканоїлоксигруп, галоалкілів або галоалкоксигруп.
4. Сполука або її фармацевтично прийнятна сіль за п. 3, у якій Rf являє собою алкіл, який заміщений арилом, який необов'язково заміщений одним або більшою кількістю алкілів, галогруп, гідроксигруп, ціаногруп, нітрогруп, аміногруп, алкоксигруп, алкоксикарбонілів, алканоїлоксигруп, галоалкілів або галоалкоксигруп.
5. Сполука або її фармацевтично прийнятна сіль за п. 4, у якій Rf являє собою (С1-6)алкіл, заміщений фенільним кільцем, яке необов'язково заміщене 1, 2 або 3 алкілами, галогрупами, гідроксигрупами, ціаногрупами, нітрогрупами, аміногрупами, алкоксигрупами, алкоксикарбонілами, алканоїлоксигрупами, галоалкілами або галоалкоксигрупами.
6. Сполука або її фармацевтично прийнятна сіль за п. 4, у якій Rf являє собою бензил або фенетил, який необов'язково заміщений 1, 2 або 3 алкілами, галогрупами, гідроксигрупами, ціаногрупами, нітрогрупами, аміногрупами, алкоксигрупами, алкоксикарбонілами, алканоїлоксигрупами, галоалкілами або галоалкоксигрупами.
7. Сполука або її фармацевтично прийнятна сіль за п. 4, у якій Rf являє собою бензил, 4-фторбензил, 3-фторбензил, 2-фторбензил, 4-ціанобензил, 3-ціанобензил, 2-ціанобензил, 4-метоксибензил, 3-метоксибензил, 2-метоксибензил, 2-бромбензил, 2-трифторметоксибензил, 2-ізопропоксибензил, 2-метилбензил, 3-метилбензил, 4-метилбензил, 2-етилбензил, 4-трифторметилбензил, 3-трифторметилбензил, 2-трифторметилбензил, 4-хлорбензил, 3-хлорбензил, 2-хлорбензил, 2,6-дифторбензил, 2-хлор-6-фторбензил, 2,6-дихлорбензил, 2-метокси-6-фторбензил, 2,6-диметилбензил, 2,6-дифтор-3-хлорбензил, 2,6-дифтор-4-хлорбензил, 2-хлор-3,6-дифторбензил, 2,3,6-трифторбензил, 3-хлор-2,4-дифторбензил, 2-хлор-3,6-дифторбензил, 2,3-дихлор-6-фторбензил, 2-нітробензил, 2-амінобензил, 2-тієнілметил, 2-фурилметил, 3-фурилметил, 5-трифторметилфур-2-илметил, 5-піразолілметил, 2-оксазолілметил, 4-метилтіазол-2-ілметил, 3-піридил, 2-піридилметил, 3-гідрокси-2-піридилметил, 6-хлор-2-піридилметил, 2-піразинілметил, 5-піримідинілметил, 2-піримідинілметил, 4-піримідинілметил, феніл, 2-тіазоліл, N,N-диметиламінокарбонілметил, N-метиламінокарбонілметил, амінокарбонілметил, 1-пропініл або 2-метилтіазол-4-ілметил.
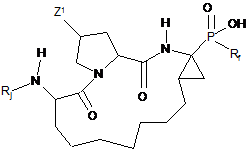
8. Сполука або її фармацевтично прийнятна сіль за п. 1, яка являє собою сполуку формули (III):
 , (ІІІ)
, (ІІІ)
у якій:
Rj являє собою циклопентилоксикарбоніл, 1-[N-(2,2,2-трифторетил)іміно]етил, a,a-дифторфенетил, циклопентилацетил, бутаноїл, 4,4,4-трифторбутаноїл, 3,3,3-трифторпропілсульфоніл, 3,3-диметилбутаноїл, циклопентиламінокарбоніл, 2-норборнанілацетил, 2-аміно-3,3-диметилбутаноїл, 4-метилфеніл, 4-трифторметилфеніл, 3-трифторметилфеніл, 2-трифторметилфеніл, 3,3,3-трифторпропаноїл, 5,5,5-трифторпентаноїл, тpeт-бутиламінокарбоніл, 2,2-диметилпропоксикарбоніл або 4-трет-бутилтіазол-2-іл.
9. Сполука або її фармацевтично прийнятна сіль за п. 8, у якій Z1 вибраний з наступних структур:
 ,
,  ,
,
 ,
,  ,
,
 .
.
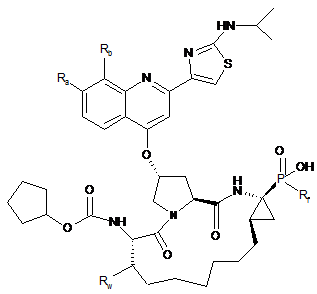
10. Сполука або її фармацевтично прийнятна сіль за п. 9, яка являє собою сполуку формули (VII):
 . (VII)
. (VII)
11. Сполука за п. 1, яка являє собою сполуку формули (XIX):
 , (XIX)
, (XIX)
або її фармацевтично прийнятна сіль; у якій
Ra являє собою Н або (С1-6)алкоксигрупу;
Rb являє собою Н, F, Сl, Вr, І або (С1-6)алкіл;
Rf являє собою алкіл, заміщений арилом, який необов'язково заміщений одним або більшою кількістю алкілів, галогруп, гідроксигруп, ціаногруп, нітрогруп, аміногруп, алкоксигруп, алкоксикарбонілів, алканоїлоксигруп, галоалкілів або галоалкоксигруп, та
Rw являє собою Н або (С1-6)алкіл.
12. Сполука або її фармацевтично прийнятна сіль за п. 11, у якій Rw являє собою Н.
13. Сполука або її фармацевтично прийнятна сіль за п. 11 або п. 12, у якій Ra являє собою (С1-6)алкоксигрупу.
14. Сполука або її фармацевтично прийнятна сіль за п. 13, у якій Ra являє собою метоксигрупу.
15. Сполука або її фармацевтично прийнятна сіль за будь-яким з пп. 11-14, у якій Rb являє собою F, Сl, Вr або І.
16. Сполука або її фармацевтично прийнятна сіль за п. 5 у якій Rf являє собою 2,6-дифторбензил.
17. Сполука або її фармацевтично прийнятна сіль за п. 16, яка являє собою сполуку формули (XXI):
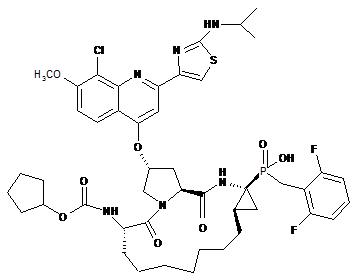 . (XXI)
. (XXI)
18. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-17 або її фармацевтично прийнятну сіль та щонайменше один фармацевтично прийнятний носій.
19. Фармацевтична композиція за п. 18, яка додатково містить аналог нуклеозиду.
20. Фармацевтична композиція за п. 18 або п. 19, яка додатково містить інтерферон або пегильований інтерферон.
21. Фармацевтична композиція за п. 20, у якій зазначений аналог нуклеозиду вибирають з рибавірину, вірамідину, левовірину, L-нуклеозиду та ізаторибіну, та зазначений інтерферон являє собою a-інтерферон або пегильований інтерферон.
Текст
1. Сполука формули (II): Z1 3 96295 4 HN Rb Ra N HN N S N R H3CO O , Ra являє собою Н або (С1-6)алкоксигрупу; Rb являє собою Н, F, Сl, Вr, І або (С1-6)алкіл; 2b Z являє собою Н, (С1-6)алкіл, (С2-8)алкеніл, (С28)алкініл; 2a Z являє собою (С1-10)алкіл, (С2-10)алкеніл, (С210)алкініл, де будь-який атом вуглецю може бути необов'язково замінений гетероатомом, вибраним з О, S або N; 1 Q являє собою (С1-8)алкіл, (С2-8)алкеніл або (С21 2а разом з атомами, 8)алкініл, за умови, що Q та Z до яких вони приєднані, утворюють гетероцикл, який може бути необов'язково заміщеним одним 3 або більшою кількістю оксо (=О) груп або А ; 3 А незалежно вибирають з алкілу, алкенілу, алкінілу, амідогрупи, імідогрупи, іміногрупи, CF3, CH2CF3, циклоалкілу, арилу, аралкілу, алкоксигрупи, арилоксигрупи, гетероциклу, -(СН2)mгетероциклу, -(СН2)mС(О)Оалкілу, -О-(СН2)m-ОС(О)-Оалкілу, -О-(СН2)m-О-С(О)-(СН2)m-алкілу, (СН2)mО-С(О)-О-алкілу, -(СН2)mО-С(О)-Оциклоалкілу, -N(Н)С(Ме)С(О)О-алкілу або алкоксіарилсульфонаміду, 3 1 необов'язково кожен незалежно А та Q разом з 3 1 одним або більшою кількістю А або Q груп утворює кільце; 2 А незалежно вибирають з PRT, Н, алкілу, алкенілу, алкінілу, аміногрупи, амінокислоти, алкоксигрупи, арилоксигрупи, ціаногрупи, галоалкілу, циклоалкілу, арилу, гетероарилу, алкілсульфонаміду або арилсульфонаміду, необов'язково заміщених за 3 допомогою А , m являє собою 0-6; та Rf являє собою Н, алкіл, алкеніл, алкініл, арил, гетероарил або циклоалкіл, причому Rf необов'язково заміщений одним або більшою кількістю Rg; кожен Rg незалежно являє собою галогрупу, гідроксигрупу, ціаногрупу, арилтіогрупу, циклоалкіл, арил, гетероарил, алкоксигрупу, NRhRi, C(=O)NRhRi, де кожен арил та гетероарил необов'язково заміщений одним або більшою кількістю алкілів, галогруп, гідроксигруп, ціаногруп, нітрогруп, аміногруп, алкоксигруп, алкоксикарбонілів, алканоїлоксигруп, галоалкілів або галоалкоксигруп, та кожен Rh та Ri незалежно являє собою Н, алкіл або галоалкіл. 2. Сполука або її фармацевтично прийнятна сіль 1 за п. 1, у якій Z вибраний з наступних структур: S N O , HN Cl R H3CO N S N O , HN F R H3CO N S N O , HN Br R H3CO N S N O , 5 96295 HN Me R H3CO N S N O . 3. Сполука або її фармацевтично прийнятна сіль за п. 1 або п. 2, у якій Rf являє собою алкіл, алкеніл або алкініл, причому Rf заміщений арилом, який необов'язково заміщений одним або більшою кількістю алкілів, галогруп, гідроксигруп, ціаногруп, нітрогруп, аміногруп, алкоксигруп, алкоксикарбонілів, алканоїлоксигруп, галоалкілів або галоалкоксигруп. 4. Сполука або її фармацевтично прийнятна сіль за п. 3, у якій Rf являє собою алкіл, який заміщений арилом, який необов'язково заміщений одним або більшою кількістю алкілів, галогруп, гідроксигруп, ціаногруп, нітрогруп, аміногруп, алкоксигруп, алкоксикарбонілів, алканоїлоксигруп, галоалкілів або галоалкоксигруп. 5. Сполука або її фармацевтично прийнятна сіль за п. 4, у якій Rf являє собою (С1-6)алкіл, заміщений фенільним кільцем, яке необов'язково заміщене 1, 2 або 3 алкілами, галогрупами, гідроксигрупами, ціаногрупами, нітрогрупами, аміногрупами, алкоксигрупами, алкоксикарбонілами, алканоїлоксигрупами, галоалкілами або галоалкоксигрупами. 6. Сполука або її фармацевтично прийнятна сіль за п. 4, у якій Rf являє собою бензил або фенетил, який необов'язково заміщений 1, 2 або 3 алкілами, галогрупами, гідроксигрупами, ціаногрупами, нітрогрупами, аміногрупами, алкоксигрупами, алкоксикарбонілами, алканоїлоксигрупами, галоалкілами або галоалкоксигрупами. 7. Сполука або її фармацевтично прийнятна сіль за п. 4, у якій Rf являє собою бензил, 4фторбензил, 3-фторбензил, 2-фторбензил, 4ціанобензил, 3-ціанобензил, 2-ціанобензил, 4метоксибензил, 3-метоксибензил, 2метоксибензил, 2-бромбензил, 2трифторметоксибензил, 2-ізопропоксибензил, 2метилбензил, 3-метилбензил, 4-метилбензил, 2етилбензил, 4-трифторметилбензил, 3трифторметилбензил, 2-трифторметилбензил, 4хлорбензил, 3-хлорбензил, 2-хлорбензил, 2,6дифторбензил, 2-хлор-6-фторбензил, 2,6дихлорбензил, 2-метокси-6-фторбензил, 2,6диметилбензил, 2,6-дифтор-3-хлорбензил, 2,6дифтор-4-хлорбензил, 2-хлор-3,6-дифторбензил, 2,3,6-трифторбензил, 3-хлор-2,4-дифторбензил, 2хлор-3,6-дифторбензил, 2,3-дихлор-6-фторбензил, 2-нітробензил, 2-амінобензил, 2-тієнілметил, 2фурилметил, 3-фурилметил, 5-трифторметилфур2-илметил, 5-піразолілметил, 2-оксазолілметил, 4метилтіазол-2-ілметил, 3-піридил, 2-піридилметил, 6 3-гідрокси-2-піридилметил, 6-хлор-2-піридилметил, 2-піразинілметил, 5-піримідинілметил, 2піримідинілметил, 4-піримідинілметил, феніл, 2тіазоліл, N,N-диметиламінокарбонілметил, Nметиламінокарбонілметил, амінокарбонілметил, 1пропініл або 2-метилтіазол-4-ілметил. 8. Сполука або її фармацевтично прийнятна сіль за п. 1, яка являє собою сполуку формули (III): O Z1 3 A OH P 3 N A H Rj N N Z Y Z2b Q 1 1 Z2a , (ІІІ) у якій: Rj являє собою циклопентилоксикарбоніл, 1-[N(2,2,2-трифторетил)іміно]етил, ,дифторфенетил, циклопентилацетил, бутаноїл, 4,4,4-трифторбутаноїл, 3,3,3трифторпропілсульфоніл, 3,3-диметилбутаноїл, циклопентиламінокарбоніл, 2-норборнанілацетил, 2-аміно-3,3-диметилбутаноїл, 4-метилфеніл, 4трифторметилфеніл, 3-трифторметилфеніл, 2трифторметилфеніл, 3,3,3-трифторпропаноїл, 5,5,5-трифторпентаноїл, тpeт-бутиламінокарбоніл, 2,2-диметилпропоксикарбоніл або 4-третбутилтіазол-2-іл. 9. Сполука або її фармацевтично прийнятна сіль 1 за п. 8, у якій Z вибраний з наступних структур: HN N R H3CO S N O , HN Cl R H3CO N S N O , 7 96295 8 HN HN F N R H3CO Rb S Ra N N S N O O O H N O , O NH N R H3CO , HN R H3CO S N O . 10. Сполука або її фармацевтично прийнятна сіль за п. 9, яка являє собою сполуку формули (VII): O Z1 H OH P N H Rf Rj N N Rw S O N Rf O N Me OH O HN Br P N O O . (VII) 11. Сполука за п. 1, яка являє собою сполуку формули (XIX): , (XIX) або її фармацевтично прийнятна сіль; у якій Ra являє собою Н або (С1-6)алкоксигрупу; Rb являє собою Н, F, Сl, Вr, І або (С1-6)алкіл; Rf являє собою алкіл, заміщений арилом, який необов'язково заміщений одним або більшою кількістю алкілів, галогруп, гідроксигруп, ціаногруп, нітрогруп, аміногруп, алкоксигруп, алкоксикарбонілів, алканоїлоксигруп, галоалкілів або галоалкоксигруп, та Rw являє собою Н або (С1-6)алкіл. 12. Сполука або її фармацевтично прийнятна сіль за п. 11, у якій Rw являє собою Н. 13. Сполука або її фармацевтично прийнятна сіль за п. 11 або п. 12, у якій Ra являє собою (С16)алкоксигрупу. 14. Сполука або її фармацевтично прийнятна сіль за п. 13, у якій Ra являє собою метоксигрупу. 15. Сполука або її фармацевтично прийнятна сіль за будь-яким з пп. 11-14, у якій Rb являє собою F, Сl, Вr або І. 16. Сполука або її фармацевтично прийнятна сіль за п. 5 у якій Rf являє собою 2,6-дифторбензил. 17. Сполука або її фармацевтично прийнятна сіль за п. 16, яка являє собою сполуку формули (XXI): 9 96295 10 HN Cl H3CO R N S N O O O P H N O NH OH F N O F O 18. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-17 або її фармацевтично прийнятну сіль та щонайменше один фармацевтично прийнятний носій. 19. Фармацевтична композиція за п. 18, яка додатково містить аналог нуклеозиду. 20. Фармацевтична композиція за п. 18 або п. 19, яка додатково містить інтерферон або пегильований інтерферон. Галузь винаходу Винахід відноситься в основному до фосфінатних сполук з активністю інгібування ВІЛ. Рівень техніки, що передує винаходу Гепатит С вважають хронічною вірусною хворобою печінки, яка характеризується захворюванням печінки. Хоча лікарські препарати, направлені на печінку, широко застосовують та демонструють ефективність, токсичність та інші побічні ефекти обмежують їх застосування. Інгібітори ВГС (вірусу гепатиту С) використовують для обмеження появи та розвитку інфекції ВГС, а також в діагностичних аналізах на ВГС. Існує необхідність в нових факторах лікування ВГС. Розкриття винаходу В одному варіанті здійснення винахід передбачає сполуку, що відповідає винаходу, яка являє собою сполуку формули I: або її фармацевтично прийнятну сіль або пролікарську форму, де: . (XXI) 21. Фармацевтична композиція за п. 20, у якій зазначений аналог нуклеозиду вибирають з рибавірину, вірамідину, левовірину, L-нуклеозиду та ізаторибіну, та зазначений інтерферон являє собою -інтерферон або пегильований інтерферон. 1 R незалежно вибирають з H, алкілу, алкенілу, алкінілу, арилу, циклоалкілу, гетероциклу, галогену, галоалкілу, алкілсульфонамідо групи, арилсульфонамідо групи, -C(O)NHS(O)2-, або -S(O)2-, 3 необов’язково заміщених одним або більше A ; 2 R вибирають з 1 3 a) -C(Y )(A ), b) (C2-10)алкілу, (C3-7)циклоалкілу або (C14)алкіл-(C3-7)циклоалкілу, де зазначений циклоалкіл та алкіл-циклоалкіл можуть бути необов’язково одно-, дво- або три-заміщеними (C1-3)алкілом, або де зазначений алкіл, циклоалкіл та алкілциклоалкіл може бути необов’язково заміщений одним або двома замісниками, вибраними з гідрокси групи та O-(C1-4)алкілу, або де кожна з зазначених алкільних груп може бути необов’язково одно-, дво- або тризаміщеною галогеном або де кожна з зазначених циклоалкільних груп є 5-, 6або 7-членною, причому одна або дві -CH2-групи, що не є безпосередньо зв’язаними одна з іншою, можуть бути необов’язково заміщеними, заміненими -O-, таким чином, що атом O зв’язаний з 2 атомом N, до якого приєднаний R за допомогою щонайменше двох атомів C, c) фенілу, (C1-3)алкіл-фенілу, гетероарилу або (C1-3)алкіл-гетероарилу, де гетероарильні групи є 5- або 6-членними, що мають від 1 до 3 гетероатомів, вибраних з N, O та S, де зазначені фенільні та гетероарильні групи можуть бути необов’язково одно-, дво- або тризаміщеними замісниками, вибраними з галогену, -OH, (C1-4)алкілу, O-(C1-4)алкілу, 11 96295 12 3 S-(C1-4)алкілу, -NH2, -CF3,-NH(C1-4)алкілу та -N((C14)алкіл)2, -CONH2 та -CONH-(C1-4)алкілу; та де зазначений (C1-3)алкіл може бути необов’язково заміщеним одним або більшою кількістю атомів галогену; або 3 d) -S(O)2(A ); R являє собою H або (C1-6)алкіл; 1 3 Y незалежно являє собою O, S, N(A ), 3 3 3 3 3 N(O)(A ), N(OA ), N(O)(OA ) або N(N(A )(A )); 3 Z являє собою O, S або NR ; 1 Z вибирають з наступних структур: Ra являє собою H або (C1-6)алкокси групу; Rb являє собою H, F, Cl, Br, I або (C1-6)алкіл; Rc являє собою H, ціано групу, F, Cl, Br, I, C(=O)NRdRe, (C1-6)алкокси групу або феніл, який є необов’язково заміщеним одним або більшою кількістю F, Cl, Br, I, (C1-6)алкілів або (C1-6)алкокси груп; кожен з Rd та Re незалежно один від іншого являють собою H або (C1-6)алкіл; кожен L незалежно один від іншого являє собою CH або N; 2a Z являє собою H, (C1-10)алкіл, (C2-10)алкеніл, (C2-10)алкініл, де будь-який атом вуглецю може бути необов’язково заміщений гетероатомом, 2a вибраним з O, S або N, або Z необов’язково утворює гетероцикл з одним або більшою кількіс1 2 1 3 тю R , R , Q або A ; 2b Z являє собою H, (C1-6)алкіл, (C2-8)алкеніл, (C2-8)алкініл; 1 Q являє собою (C1-8)алкіл, (C2-8)алкеніл або 1 2a (C2-8)алкініл, або Q та Z , взяті разом з атомами, до яких вони приєднані, утворюють гетероцикл, причому даний гетероцикл може бути необов’язково заміщеним однією або більшою кількі3 стю оксо (=O) груп або A ; 3 A незалежно вибирають з PRT, H, -OH, C(O)OH, ціано групи, алкілу, алкенілу, алкінілу, аміно групи, амідо групи, імідо групи, іміно групи, галогену, CF3, CH2CF3, циклоалкілу, нітро групи, арилу, аралкілу, алкокси групи, арилокси групи, 2 2 2 2 гетероциклу, -C(A )3, -C(A )2-C(O)A , -C(O)A , 2 2 2 2 C(O)OA , -O(A ), -N(A )2, -S(A ), 1 2 2 1 2 2 CH2P(Y )(A )(OA ), -CH2P(Y )(A )(N(A )2), 1 2 2 1 2 2 CH2P(Y )(OA )(OA ), -OCH2P(Y )(OA )(OA ), 1 2 2 1 2 2 OCH2P(Y )(A )(OA ), -OCH2P(Y )(A )(N(A )2), 1 2 2 C(O)OCH2P(Y )(OA )(OA ), 1 2 2 C(O)OCH2P(Y )(A )(OA ), 1 2 2 C(O)OCH2P(Y )(A )(N(A )2), 1 2 2 1 2 2 CH2P(Y )(OA )(N(A )2), -OCH2P(Y )(OA )(N(A )2), 1 2 2 C(O)OCH2P(Y )(OA )(N(A )2), CH2P(Y )(N(A )2)(N(A )2), 1 2 2 C(O)OCH2P(Y )(N(A )2)(N(A )2), 1 2 2 OCH2P(Y )(N(A )2)(N(A )2), -(CH2)m-гетероциклу, (CH2)mC(O)Oалкілу, -O-(CH2)m-O-C(O)-Oалкілу, O-(CH2)m-O- C(O)-(CH2)m-алкілу, -(CH2)mO-C(O)-Oалкілу, -(CH2)mO-C(O)-O-циклоалкілу, N(H)C(Me)C(O)O-алкілу або алкоксиарилсульфонаміду, 3 де кожен A може бути необов’язково заміщеним за допомогою 1 – 4 замісників, що вибирають з групи, яка включає: 1 1 2 2 1 2 2 -R , -P(Y )(OA )(OA ), -P(Y )(OA )(N(A )2), 1 2 2 1 2 2 P(Y )(A )(OA ), -P(Y )(A )(N(A )2) або 1 2 2 2 P(Y )(N(A )2)(N(A )2), -C(=O)N(A )2), галоген, алкіл, алкеніл, алкініл, арил, карбоцикл, гетероцикл, аралкіл, арилсульфонамід, арилалкілсульфонамід, арилоксисульфонамід, арилоксиалкілсульфонамід, арилоксиарилсульфонамід, алкілсульфонамід, алкілоксисульфонамід, алкілоксиалкілсульфонамід, арилтіо групу, (CH2)mгетероцикл, -(CH2)m-C(O)O-алкіл, O(CH2)mOC(O)Oалкіл, -O-(CH2)m-O-C(O)-(CH2)mалкіл, -(CH2)m-O-C(O)-O-алкіл, -(CH2)m-O-C(O)-Oциклоалкіл, -N(H)C(CH3)C(O)O-алкіл або алкокси1 арилсульфонамід, необов’язково заміщені R ; Необов’язково кожен незалежний окремий 3 1 випадок A та Q можна взяти разом з однією або 3 1 більшою кількістю груп A або Q для утворення циклу; 2 A незалежно вибирають з PRT, H, алкілу, алкенілу, алкінілу, аміно групи, амінокислоти, алкокси групи, арилокси групи, ціано групи, галоалкілу, циклоалкілу, арилу, гетероарилу, алкілсульфонаміду або арилсульфонаміду, нео3 бов’язково заміщених A , та m являє собою 0-6. Даний винахід передбачає також фармацевтичну композицію, що включає сполуку, яка відповідає винаходу, та щонайменше один фармацевтично прийнятний носій. 1 2 2 13 Даний винахід передбачає також фармацевтичну композицію, призначену для застосування при лікуванні порушень, асоційованих з ВГС. Даний винахід передбачає також фармацевтичну композицію, що додатково включає аналог нуклеозиду. Даний винахід передбачає також фармацевтичну композицію, що додатково включає інтерферон або пегільований інтерферон. Даний винахід передбачає також фармацевтичну композицію, в якій зазначений аналог нуклеозиду вибраний з рибавірину, вірамідину, леворину, L-нуклеозиду та ізаторибіну, та зазначений інтерферон являє собою інтерферон або пегільований інтерферон. Даний винахід передбачає також спосіб лікування порушень, асоційованих з гепатитом C, причому зазначений спосіб включає введення пацієнту фармацевтичної композиції, яка включає в себе терапевтично ефективну кількість сполуки, що відповідає винаходу. Даний винахід передбачає також спосіб інгібування ВГС, що включає введення ссавцю, ураженому станом, пов’язаним з активністю ВГС, кількості сполуки, що відповідає винаходу, ефективної для того, щоб інгібувати ВГС. Даний винахід передбачає також сполуку, що відповідає винаходу, призначену для лікування (переважно для застосування при інгібуванні ВГС або лікування стану, асоційованого з активністю ВГС), а також застосування сполуки, що відповідає винаходу, для виготовлення лікарського засобу, що використовують для інгібування ВГС або лікування стану, асоційованого з активністю ВГС у ссавця. Даний винахід передбачає також способи синтезу та нові проміжні продукти, розкриті в даному контексті, які використовують для одержання сполук, що відповідають винаходу. Деякі зі сполук, що відповідають винаходу, використовують для одержання інших сполук, що відповідають винаходу. В іншому аспекті винахід передбачає спосіб інгібування активності ВГС у зразку, що включає обробку зразку сполукою, що відповідає винаходу. В одному варіанті здійснення винахід передбачає сполуку, що має покращенні інгібуючі або фармакокінетичні властивості, включаючи підвищену активність у відношенні розвинення стійкості вірусу, покращену біодоступність при пероральному застосуванні, більш високу активність або пролонгований ефективний період напіврозкладу in vivo. Деякі сполуки, по винаходу, можуть мати менше побічних ефектів, менш складні схеми дозування або є активними при пероральному введенні. Детальний опис винаходу Тут будуть в деталях описувати ряд варіантів здійснення винаходу, приклади яких проілюстровані в супровідних структурах та формулах. Хоча винахід буде описано у взаємозв’язку з багаточисельними варіантами здійснення, слід мати на увазі, що вони не призначені для обмеження винаходу даними варіантами здійснення. Навпаки, 96295 14 винахід призначено для того, щоб охопити всі альтернативні варіанти, модифікації та еквівалентні рішення, які можуть бути включені в обсяг даного винаходу, як визначено у варіантах здійснення. Сполуки, що відповідають винаходу Сполуки, що відповідають винаходу, виключають сполуки, відомі раніше. Однак у винахід входить застосування сполук, про які раніше не було відомо, що вони мають противірусні властивості, для противірусних цілей (наприклад, для одержання противірусного ефекту у тварини). Стосовно Сполучених Штатів Америки сполуки або композиції, приведені в даному контексті, виключають сполуки, які передбачають за 35 USC (Зведення законів США) 102 або які очевидні за 35 USC 103. Коли сполука, описана в даному контексті, є заміщеною більше ніж однією з тих же зазначе1 3 них груп, наприклад, "R " або "A ", то слід мати на увазі, що групи можуть бути однаковими або різними, тобто кожну групу вибирають незалежно. "Алкіл" являє собою C1-C18вуглеводень, що включає нормальні, вторинні, третинні або циклічні атоми вуглецю. Прикладами є метил (Me, CH3), етил (Et, -CH2CH3), 1-пропіл (н-Pr, н-пропіл, -CH2CH2CH3), 2-пропіл (ізо-Pr, ізо-пропіл, CH(CH3)2), 1-бутил (н-Bu, н-бутил, CH2CH2CH2CH3), 2-метил-1-пропіл (ізо-Bu, ізобутил, -CH2CH(CH3)2), 2-бутил (втор-Bu, вторбутил, -CH(CH3)CH2CH3), 2-метил-2-пропіл (третBu, трет-бутил, -C(CH3)3), 1-пентил (н-пентил, CH2CH2CH2CH2CH3), 2-пентил (CH(CH3)CH2CH2CH3), 3-пентил (-CH(CH2CH3)2), 2метил-2-бутил (-C(CH3)2CH2CH3), 3-метил-2бутил (-CH(CH3)CH(CH3)2), 3-метил-1-бутил (CH2CH2CH(CH3)2), 2-метил-1-бутил (CH2CH(CH3)CH2CH3), 1-гексил (CH2CH2CH2CH2CH2CH3), 2-гексил (CH(CH3)CH2CH2CH2CH3), 3-гексил (CH(CH2CH3)(CH2CH2CH3)), 2-метил-2-пентил (C(CH3)2CH2CH2CH3), 3-метил-2-пентил (CH(CH3)CH(CH3)CH2CH3), 4-метил-2-пентил (CH(CH3)CH2CH(CH3)2), 3-метил-3-пентил (C(CH3)(CH2CH3)2), 2-метил-3-пентил (CH(CH2CH3)CH(CH3)2), 2,3-диметил-2-бутил (C(CH3)2CH(CH3)2), 3,3-диметил-2-бутил (CH(CH3)C(CH3)3. "Алкеніл" являє собою C2-C18вуглеводень, що включає нормальні, вторинні, третинні або циклічні атоми вуглецю з щонайменше одним центром 2 ненасиченості, тобто вуглець-вуглецевим sp подвійним зв’язком. Приклади включають, але без обмеження перерахованим, етилен або вініл (-CH=CH2), аліл (-CH2CH=CH2), циклопентеніл (C5H7) та 5-гексеніл (-CH2CH2CH2CH2CH=CH2). "Алкініл" являє собою C2-C18вуглеводень, що містить нормальні, вторинні, третинні або циклічні атоми вуглецю з щонайменше одним центром ненасиченості, тобто вуглець-вуглецевим spпотрійним зв’язком. Приклади включають, але без обмеження перерахованим, ацетилен (CCH) та пропаргіл (-CH2CCH). Термін "алкілен" відноситься до насиченого або циклічного вуглеводневого радикалу, що має 15 розгалужений або нерозгалужений ланцюг, що складається з 1-18 атомів вуглецю, та що має два одновалентних центри радикалу, отримані шляхом видалення двох атомів водню від одного та того ж або двох різних атомів вуглецю вихідного алкану. Типові алкіленові радикали включають, але без обмеження перерахованим, метилен (CH2-) 1,2-етил (-CH2CH2-), 1,3-пропіл (CH2CH2CH2-), 1,4-бутил (-CH2CH2CH2CH2-) тощо. Термін "алкенілен" відноситься до насиченого або циклічного вуглеводневого радикалу, що має розгалужений або нерозгалужений ланцюг, що складається з 2-18 атомів вуглецю, та що має два одновалентних центри радикалу, отриманого шляхом видалення двох атомів водню від одного та того ж або двох різних атомів вуглецю вихідного алкену. Типові алкеніленові радикали включають, але без обмеження перерахованим, 1,2етилен (-CH=CH-). Термін "алкінілен" відноситься до насиченого або циклічного вуглеводневого радикалу, що має розгалужений або нерозгалужений ланцюг, що складається з 2-18 атомів вуглецю, та що має два одновалентних центри радикалу, отриманого шляхом видалення двох атомів водню від одного та того ж або двох різних атомів вуглецю вихідного алкіну. Типові алкініленові радикали включають, але без обмеження перерахованим, ацетилен (-CC-), пропаргіл (-CH2C=C-) та 4-пентиніл (CH2CH2CH2CCH-). "Арил" означає одновалентний ароматичний вуглеводневий радикал, що складається з 6-20 атомів вуглецю, отриманий шляхом видалення одного атому водню від одного атому вуглецю вихідної ароматичної циклічної системи. Типові арильні групи включають, але без обмеження перерахованим, радикали, отримані з бензолу, заміщеного бензолу, нафталіну, антрацену, біфенілу тощо. Термін "арилалкіл" відноситься до нециклічного алкільного радикалу, в якому один з атомів водню, зв’язаний з атомом вуглецю, як правило, 3 кінцевим або sp атомом вуглецю, заміщений арильним радикалом. Типові арилалкільні групи включають, але без обмеження перерахованим, бензил, 2-фенілетан-1-іл, нафтилметил, 2нафтилетан-1-іл, нафтобензил, 2нафтофенілетан-1-іл тощо. Арилалкільна група включає 6-20 атомів вуглецю, наприклад, алкільну частину, що включає алканільну, алкенільну або алкінільну групи арилалкільної групи з 1-6 атомів вуглецю та арильну частину з 5-14 атомів вуглецю. Терміни "заміщений алкіл", "заміщений арил" та "заміщений арилалкіл" означають алкіл, арил та арилалкіл відповідно, у яких кожен з одного або більшої кількості атомів водню незалежно один від іншого заміщені неводневим замісником. Типові замісники включають, але без обмеження перерахованим, -X, -R, -O , -OR, -SR, -S , -NR2, NR3, =NR, -CX3, -CN, -OCN, -SCN, -N=C=O, -NCS, -NO, -NO2, =N2, -N3, NC(=O)R, -C(=O)R, C(=O)NRR, -S(=O)2O , -S(=O)2OH, -S(=O)2R, OS(=O)2OR, -S(=O)2NR, -SC=O)R, -OP(=O)O2RR, P(=O)O2RR, -P(=O)(O )2, -P(=O)(OH)2, -C(=O)R, 96295 16 C(=O)X, -C(S)R, -C(O)OR, -C(O)O , -C(S)OR, C(O)SR, -C(S)SR, -C(O)NRR, -C(S)NRR, C(NR)NRR, де кожен X незалежно один від іншого являє собою галоген: F, Cl, Br або I та кожен R незалежно один від іншого являє собою галоген H, алкіл, арил, гетероцикл, захисну групу або структуру пролікарської форми. Алкіленова, алкеніленова та алкініленова групи можуть бути також аналогічним чином заміщеними. "Гетероцикл", як використовують в даному контексті, включає як приклад, а не обмеження, ті гетероцикли, які описані в монографіях Paquette, Leo A.; Principles of Modern Heterocyclic Chemistry (Принципи сучасної хімії гетероциклів) CW.A. Benjamin, New York, 1968), особливо глави 1, 3, 4, 6, 7 та 9; The Chemistry of Heterocyclic Compounds. A Series of Monographs (Хімія гетероциклічних сполук. Серія монографій) (John Wiley & Sons, New York, 1950 до даного часу), зокрема, т.т. 13, 14, 16, 19 та 28, та J. Am. Chem. Soc. (1960) 82:5566. В одному спеціальному варіанті здійснення винаходу термін "гетероцикл" включає "вуглецевий цикл", як визначено в даному контексті, в якому один або більша кількість (наприклад, 1, 2, 3 або 4) атомів вуглецю заміщені гетероатомом (наприклад O, N або S). Приклади гетероциклів включають як приклад, а не обмеження, піридил, дигідропіридил, тетрагідропіридил (піперидил), тіазоліл, тетрагідротіофеніл, тетрагідротіофеніл з окисленою сіркою, піримідиніл, фураніл, тієніл, піроліл, піразоліл, імідазоліл, тетразоліл, бензофураніл, тіонафталеніл, індоліл, індоленіл, хінолініл, ізохінолініл, бензімідазоліл, піперидиніл, 4піперидоніл, піролідиніл, 2-піролідоніл, піролініл, тетрагідрофураніл, тетрагідрохінолініл, тетрагідроізохінолініл, декагідрохінолініл, октагідроізохінолініл, азоциніл, триазиніл, 6H-1,2,5триадіазиніл, 2H,6H-1,5,2-дитіазиніл, тієніл, тіантреніл, піраніл, ізобензофураніл, хроменіл, ксантеніл, феноксатиніл, 2H-піроліл, ізотіазоліл, ізоксазоліл, піразиніл, піридазиніл, індолізиніл, ізоіндоліл, 3H-індоліл, 1H-індазоліл, пуриніл, 4Hхінолізиніл, фталазиніл, нафтиридиніл, хіноксалініл, хіназолініл, циннолініл, птеридиніл, 4Hкарбазоліл, карбазоліл, β-карболініл, фенантридиніл, акридиніл, піримідиніл, фенантролініл, феназиніл, фенотіазиніл, фуразаніл, феноксазиніл, ізохроманіл, хроманіл, імідазолідиніл, імідазолініл, піразолідиніл, піразолініл, піперазиніл, індолініл, ізоіндолініл, хінуклідиніл, морфолініл, оксазолідиніл, бензотриазоліл, бензізоксазоліл, оксіндоліл, бензоксазолініл, ізатіноїл та бістетрагідрофураніл: Як приклад, а не обмеження, вуглець-зв’язані гетероцикли зв’язані в положенні 2, 3, 4, 5 або 6 піридину, в положенні 3, 4, 5 або 6 піридазину, в положенні 2, 4, 5 або 6 піримідину, в положенні 2, 3, 5 або 6 піразину, в положенні 2, 3, 4 або 5 фу 17 рану, тетрагідрофурану, тіофурану, тіофену, піролу або тетрагідропіролу, в положенні 2, 4 або 5 оксазолу, імідазолу або тіазолу, в положенні 3, 4 або 5 ізоксазолу, піразолу або ізотіазолу, в положенні 2 або 3 азиридину, в положенні 2, 3 або 4 азетидину, в положенні 2, 3, 4, 5, 6, 7 або 8 хіноліну або в положенні 1, 3, 4, 5, 6, 7 або 8 ізохіноліну. Ще більш типово, коли вуглець-зв’язані гетероцикли включають 2-піридил, 3-піридил, 4піридил, 5-піридил, 6-піридил, 3-піридазиніл, 4піридазиніл, 5-піридазиніл, 6-піридазиніл, 2піримідиніл, 4-піримідиніл, 5-піримідиніл, 6піримідиніл, 2-піразиніл, 3-піразиніл, 5-піразиніл, 6-піразиніл, 2-тіазоліл, 4-тіазоліл або 5-тіазоліл. Як приклад, а не обмеження, азот-зв’язані гетероцикли зв’язані в положенні 1 азиридину, азетидину, піролу, піролідину, 2-піроліну, 3-піроліну, імідазолу, імідазолідину, 2-імідазоліну, 3імідазоліну, піразолу, піразолону, 2-піразоліну, 3піразоліну, піперидину, піперазину, індолу, індоліну, 1H-індазолу, в положенні 2 ізоіндолу або ізоіндоліну, в положенні 4 морфоліну та положенні 9 карбазолу або -карболіну. Ще більш типово азот-зв’язані гетероцикли включають 1азиридил, 1-азетедил, 1-піроліл, 1-імідазоліл, 1піразоліл та 1-піперидиніл. Термін "вуглецевий цикл" відноситься до насиченого, ненасиченого або ароматичного циклу, що має до приблизно 25 атомів вуглецю. Як правило, вуглецевий цикл має приблизно 3-7 атомів вуглецю як моноцикл, приблизно 7-12 атомів вуглецю як біцикл та до приблизно 25 атомів вуглецю як поліцикл. Моноциклічні вуглецеві цикли, як правило, мають 3-6 атомів циклу, ще більш типово 5-6 атомів циклу. Біциклічні вуглецеві цикли, як правило, мають 7-12 атомів циклу, наприклад, організовані як біцикло [4,5], [5,5], [5,6] або [6,6] система або 9 або 10 атомів циклу, організовані як біцикло [5,6] або [6,6] система. Термін вуглецевий цикл включає "циклоалкіл", що є насиченим або ненасиченим вуглецевим циклом. Приклади моноциклічних вуглецевих циклів включають циклопропіл, циклобутил, циклопентил, 1-циклопент-1-еніл, 1-циклопент-2-еніл, 1циклопент-3-еніл, циклогексил, 1-циклогекс-1еніл, 1-циклогекс-2-еніл, 1-циклогекс-3-еніл, фе1 2a ніл, спірил та нафтил. Коли Q та Z , взяті разом з атомами, до яких вони приєднані, утворюють 1 2a гетероцикл, гетероцикл, утворений Q та Z , взятими разом з атомами, до яких вони приєднані, може, як правило, включати приблизно 25 атомів. Термін "хіральний" відноситься до молекул, які мають властивість ненакладання дзеркального партнера, тоді як термін "нехіральний" відноситься до молекул, які накладаються на свого дзеркального партнера. Термін "стереоізомери" відноситься до сполук, які мають ідентичну хімічну будову, але відрізняються розташуванням атомів або груп у просторі. Термін "діастереомер" відноситься до стереоізомера із двома або більше центрами хіральності, та чиї молекули не є дзеркальними зображеннями один одного. Діастереомери мають різні фізичні властивості, наприклад, температури плавлення, температури кипіння, спект 96295 18 ральні властивості та реакційну здатність. Суміші діастереомерів можна розділити аналітичними способами високого розділення, такими як електрофорез та хроматографія. Термін "енантіомери" відноситься до двох стереоізомерів сполуки, які являють собою дзеркальні зображення, що не накладаються, одне інше. Термін "лікування" або "курс лікування" у тому ступені, у якій він відноситься до захворювання або стану, включає попередження виникнення захворювання або стану, пригнічення захворювання або стану, усунення захворювання або стану та/або полегшення одного або більше симптомів захворювання або стану. Термін "PRT" вибраний з термінів "структура пролікарської форми" та "захисна група", як визначено в даному контексті. Стереохімічні визначення та умовні позначки, використовувані в даному контексті, в основному відповідають наведеним у словнику під ред. S.P. Parker, McGraw-Hill Dictionary of Chemical Terms (Словник хімічних термінів) (1984) McGraw-Hill Book Company, New York; та монографії Eliel, E. and Wilen, S., Stereochemistry of Organic Compounds (Стереохімія органічних сполук), (1994) John Wiley & Sons, Inc., New York. Багато органічних сполук знаходяться в оптично активних формах, тобто вони мають здатність обертати площину плоскополяризованого світла. В описі оптично активної сполуки використовують приставки D та L або R та S для позначення абсолютної конфігурації молекули у відношенні її хірального центру(ів). Приставки d та l або (+) та (-) використовують для позначення знаку обертання сполукою плоскополяризованого світла, при цьому (-) або l означають, що сполука є лівообертальною. Сполука, позначувана приставкою (+) або d є правообертальною. Для заданої хімічної структури дані стереоізомери є ідентичними за винятком того, що вони є дзеркальними зображеннями один одного. Специфічний стереоізомер можна також позначити як енантіомер, та суміш даних ізомерів часто називають енантіомерною сумішшю. Суміш 50:50 енантіомерів називають рацемічною сумішшю або рацематом, вона може існувати за відсутності стереоселективності або стереоспецифічності хімічної реакції або процесу. Терміни "рацемічна суміш" та "рацемат" відносяться до еквімолярної суміші двох енантіомерних структур, позбавленої оптичної активності. Винахід включає всі стереоізомери сполук, описаних у даному контексті. Пролікарські форми Термін "пролікарська форма", як використовують у даному контексті, відноситься до будьякої сполуки, яка при введенні в біологічну систему генерує лікарську субстанцію, тобто активний інгредієнт як результат спонтанної хімічної реакції(ій), хімічної реакції(ій), що каталізується ферментом, фотолізу та/або метаболічної хімічної реакції(ій). Пролікарська форма, таким чином, являє собою ковалентно модифікований аналог або сховану форму терапевтично активної сполуки. 19 Термін "структура пролікарської форми" відноситься до лабільної функціонального групи, що відокремлюється від активної інгібуючої сполуки в процесі метаболізму, системно, всередині клітини, за допомогою гідролізу, ферментного розщеплення або шляхом якого-небудь іншого процесу (див. роботи Bundgaard, Hans, "Design and Application of Prodrugs" (Створення та застосування пролікарських форм" в A Textbook of Drug Design and Development (Посібник зі створення та розробки лікарських препаратів), (1991), під ред. P. Krogsgaard-Larsen та H. Bundgaard, Harwood Academic Publishers, стор. 113-191). Ферменти, які здатні здійснювати ферментативну активацію фосфонатних пролікарських форм сполук, що відповідають винаходу, включають, але без обмеження перерахованим, амідази, естерази, мікробні ферменти, фосфоліпази, холінестерази та фосфази. Пролікарські структури можуть слугувати для підвищення розчинності, всмоктування та ліпофільності з метою оптимізації доставки лікарських препаратів, біодоступності та ефективності. Пролікарська структура може включати активний метаболіт або сам лікарський препарат. Приклади пролікарських структур включають гідролітично чутливі або лабільні ацилоксимети9 лові складні ефіри -CH2OC(=O)R та ацилоксиме9 9 тилові карбонати -CH2OC(=O)OR , де R являє собою C1-C6 алкіл, C1-C6 заміщений алкіл, C6-C20 арил або C6-C20 заміщений арил. Ацилоксиалкіловий складний ефір вперше використаний як стратегія пролікарської форми для карбонових кислот та потім застосований до фосфатів та фосфонатів у роботі Farquhaf et al. (1983) J. Pharm. Sci 72: 324; див. також патенти США №№ 4816570, 4968788, 5663159 та 5792756. Згодом ацилоксиалкіловий складний ефір був використаний для доставки фосфонових кислот через клітинні мембрани та для підвищення біодоступності при пероральному введенні. Близький варіант ацилоксиалкілового складного ефіру, алкоксикарбонілоксиалкіловий складний ефір (карбонат), також може підвищувати біодоступність при пероральному введенні як пролікарську структуру в сполуках комбінацій, що відповідають винаходу. Прикладом ацилоксиметилового складного ефіру є півалоїлоксиметокси, (POM) CH2OC(=O)C(CH3)3. Прикладом пролікарської структури ацилоксиметилкарбонату є півалоїлоксиметилкарбонат (POC) -CH2OC(=O)OC(CH3)3. Показано, що арилові складні ефіри фосфорних груп, особливо фенілові складні ефіри, підвищують пероральну біодоступність (див. статтю De Lombaert et al. (1994) J. Med. Chem. 37:498). Описані також фенілові складні ефіри, що включають складний ефір карбонової кислоти в ортоположенні по відношенню до фосфату (див. статтю Khamnei and Torrence, (1996) J. Med. Chem. 39: 4109-4115). Показано, що бензилові складні ефіри генерують вихідні фосфонові кислоти. У ряді випадків замісники в орто- або парі-положенні можуть прискорювати гідроліз. Бензильні аналоги з ацильованим фенолом або алкільованим фенолом можуть генерувати фенольну сполуку за допомо 96295 20 гою дії ферментів, наприклад, естераз, оксидів та т.п., що, у свою чергу, піддається розщепленню бензильного зв'язку C-O з генерацією фосфорної кислоти та хінонметидної проміжної сполуки. Приклади даного класу пролікарських форм описані в статті Mitchell et al. (1992) J. Chem. Soc. Perkin Trans. II 2345; заявці Glazier WO 91/019721. Описані ще одні бензильні пролікарські форми, що включають групу, що містить складний ефір карбонової кислоти, приєднаний до бензильного метилену (див. заявку Glazier WO 91/019721). Показані пролікарські форми, що містять тіо групу, призначені для використання з метою внутрішньоклітинної доставки фосфонатних лікарських препаратів. Дані проефіри включають етилтіогрупу, у якій тіолова група або естерифікована ацильною групою, або скомбінована з іншою тіоловою групою з утворенням дисульфіду. Деестерифікація або відновлення дисульфіду генерує вільну проміжну тіосполуку, що згодом розкладається на фосфорну кислоту та епісульфід (див. статті Puech et al. (1993) Antiviral Res., 22: 155-174; Benzaria et al. (1996) J. Med. Chem. 39: 4958). Захисні групи У контексті даного винаходу захисні групи включають пролікарські структури та хімічні захисні групи. Термін "захисна група" відноситься до структури сполуки, що маскує або змінює властивості функціональної групи або властивості сполуки в цілому. Хімічні захисні групи та стратегії захисту/зняття захисту добре відомі в галузі техніки. Див., наприклад, монографію Protective Groups in Organic Chemistry (Захисні групи в органічній хімії), Theodora W. Greene, John Wiley & Sons, Inc., New York, 1991. Захисні групи часто використовують, щоб маскувати реакційність ряду функціональних груп, підвищувати ефективність необхідних хімічних реакцій, наприклад, створення та розриву хімічних зв'язків впорядкованим та попередньо заданим чином. Захист функціональних груп сполуки змінює, крім реакційності, інші фізичні властивості захищеної функціональної групи, такі як полярність, ліпофільність (гідрофобність) та інші властивості, які можна виміряти за допомогою звичайних аналітичних приладів. Хімічні захищені проміжні продукти самі по собі можуть бути біологічно активними або неактивними. Захищені сполуки також можуть проявляти змінені, та в ряді випадків, оптимізовані властивості in vitro та in vivo, такі як проникнення через клітинні мембрани та стійкість до ферментного розкладання або до виведення. У даній ролі захищені сполуки із планованими терапевтичними ефектами можна назвати пролікарськими формами. Іншою функцією захисної групи є перетворення вихідного лікарського препарату в пролікарську форму, причому вихідний лікарський препарат вивільняється при перетворенні пролікарської форми in vivo. Оскільки активні пролікарські форми можуть всмоктуватися більш ефективно, ніж вихідний лікарський препарат, пролікарські форми можуть мати більшу активність in vivo, ніж вихідний лікарський препарат. 21 96295 22 Захисні групи видаляють або in vitro у випадку хімічних проміжних продуктів, або in vivo, у випадку пролікарських форм. При використанні хімічних проміжних продуктів не є особливо важливим, щоб отримані продукти після зняття захисту, наприклад, спирти були фізіологічно прийнятними, хоча, як правило, більш бажано, коли продукти є фармакологічні нешкідливими. Захисні групи доступні, загальновідомі, та їх при необхідності використовують для попередження побічних реакцій із захищеною групою під час процедур синтезу, тобто шляхів або способів одержання сполук, що відповідають винаходу. У більшості випадків рішення щодо того, які групи захистити, коли це зробити та природи хімічної захисної групи "PG", буде залежати від хімії реакції, у якій передбачають захист (наприклад, кислих, основних, окисних, відновлювальних або інших умов) та планованого напрямку синтезу. PG-групи не обов'язково повинні бути та, як правило, не є однаковими, якщо сполуку заміщено безліччю PG. В основному PG будуть використовувати для захисту функціональних груп, таких як карбоксил, гідроксил, тіо або аміногрупи та, таким чином, для того, щоб попередити побічні реакції або іншим способом підвищити ефективність синтезу. Порядок зняття захисту з метою одержання вільних груп зі знятим захистом залежить від планованого напрямку синтезу та умов реакції, з якими стикаються, та може здійснюватися в будьякому порядку, який визначає фахівець. Можна захистити різні функціональні групи сполуки, що відповідає винаходу . Наприклад, захисні групи для -OH-груп (гідроксильної чи, карбонової кислоти, фосфонової кислоти або інших функцій) включають "групи, що утворюють прос тий або складний ефір". Групи, що утворюють простий або складний ефір, здатні функціонувати як хімічні захисні групи в схемах синтезу, наведених у даному контексті. Однак ряд захисних груп гідроксилу або тіо групи, не є групами, що утворюють простий або складний ефір, як будуть мати на увазі компетентні фахівці в галузі техніки, та включені з обговорюваними нижче амідами. Дуже велика кількість захисних груп гідроксилу та амід-утворюючих груп та відповідних хімічних реакцій розщеплення описано в монографії Захисні групи в органічному синтезі. Theodora W. Greene (John Wiley & Sons, Inc., New York, 1991, ISBN 0-471-62301-6) ("Greene"). Див. також монографію Kocienski, Philip J.; Protecting groups (Захисні групи) (Georg Thieme Verlag Stuttgart, New York, 1994), що включена в даному контексті у вигляді у своїй повноті. Див., зокрема, гл. 1, Protecting groups: An Overview (Захисні групи: Огляд), стор. 1-20, гл. 2, Hydroxyl Protecting groups (Захисні групи гідроксилу), стор. 21-94, гл. 3, Diol Protecting groups (Захисні групи діолу), стор. 95-117, гл. 4, Carboxyl Protecting groups (Захисні групи карбоксилу), стор. 118-154, гл. 5, Carbonyl Protecting groups (Захисні групи карбонілу), стор. 155-184. Щодо захисних груп карбонової кислоти, фосфонової кислоти, фосфонату, сульфонової кислоти та інших захисних груп кислот див. Greene, як наведено нижче. 3 2 A та A можуть являти собою H, алкіл або простий або складний ефір-утворюючу групу. Вираз "група, що утворює простий ефір", означає групу, що здатна до утворення стабільного ковалентного зв'язку між вихідною молекулою та групою, що має формулу: де Va являє собою чотиривалентний атом, як правило, вибраний з C та Si; Vb являє собою тривалентний атом, як правило, вибраний з B, Al, N та P, більш типово - N та P; Vc являє собою двовалентний атом, як правило, вибраний з O, S та Se, більш типово S; V1 являє собою групу, пов'язану з Va, Vb або Vc за допомогою стабільного простого ковалентного зв'язку, як правило, V1 2 являє собою групи A ; V2 являє собою групу, поa b в'язану з V або V за допомогою стабільного подвійного ковалентного зв'язку, за умови, що V2 не є =O, =S або =N-, як правило, V2 являє собою =C(V1)2, де V1 таке, як описано вище, та V3 являє собою групу, зв'язану з Va за допомогою стабільного потрійного ковалентного зв'язку, як правило, V3 являє собою V∫C(V1), де V1 таке, як описано вище. Вираз "група, що утворює складний ефір" означає групу, що здатна до утворення стабільного ковалентного зв'язку між вихідною молекулою та групою, що має формулу: де Va, Vb та V1 такі, як описано вище, Vd являє собою п’ятивалентний атом, як правило, вибраний з P та N; Ve являє собою шестивалентний атом, як правило, S, та V4 є групою, зв'язаною з Va, Vb, Vd або Ve за допомогою подвійного ковалентного зв'язку за умови, що щонайменше одне 23 96295 24 з V4 являє собою =O, =S або =N-V1, як правило V4, коли воно відмінно від =O, =S або =N-, являє собою =C(V1)2, де V1 таке, як описано вище. Захисні групи для функцій -OH (гідрокси чи, кислотна або інша функції) являють собою варіанти здійснення "груп, що утворюють простий або складний ефір". Особливий інтерес являють собою групи, що утворюють простий або складний ефір, які здатні діяти як захисні групи в схемах синтезу, наведених у даному контексті. Однак, деякі захисні групи гідроксилу та тіо групи не є групами, що утворюють ні простий, ні складний ефір, як буде зрозуміло компетентним фахівцям в галузі техніки, та вони включені з амідами, обговорюваними нижче та здатні захищати гідроксильні або тіогрупи, таким чином, що гідроліз із вихідної молекули забезпечує одержання гідроксилу або тіо групи. 3 У своїй складний ефір-утворюючій ролі A 2 або A , як правило, пов'язані з якою-небудь кислотною групою, такою як приклад, а не обмеження, група -CO2H або -C(S)OH, у такий спосіб при3 2 водячи в результаті до -CO2A2 або -CO2A . A , наприклад, виводять із численних складноефірних груп, представлених в WO 95/007920. 2 Приклади A включають C3-C12гетероцикл (описаний вище) або арил. Дані ароматичні групи необов’язково є поліциклічними або моноциклічними. Приклади включають феніл, спірил, 2- та 3піроліл, 2- та 3-тієніл, 2- та 4-імідазоліл, 2-, 4- та 5-оксазоліл, 3- та 4-ізоксазоліл, 2-, 4- та 5тіазоліл, 3-, 4- та 5-ізотіазоліл, 3- та 4- піразоліл, 1-, 2-, 3- та 4-піридиніл, та 1-, 2-, 4- та 5піримідиніл, C3-C12 гетероцикл або арил, заміще1 1 ний гало, R , R -O-C1-C12алкілен, C1-C12алкокси групу, CN, NO2, OH, карбокси групу, складний ефір карбокси групу, тіол, тіоефір, C1C12галоалкіл (1-6 атомів галогену), C2-C12алкеніл або C2-C12алкініл. Дані групи включають 2-, 3- та 4-алкоксифеніл(C1-C12алкіл), 2-, 3- та 4метоксифеніл, 2-, 3- та 4- етоксифеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- та 3,5-диетоксифеніл, 2- та 3- карбокcиетокси-4-гідроксифеніл, 2- та 3-етокси-4гідроксифеніл, 2- та 3-етокси-5-гідроксифеніл, 2та 3-етокси-6-гідроксифеніл, 2-, 3- та 4-Oацетилфеніл, 2-, 3- та 4-диметиламінофеніл, 2-, 3- та 4- метилмеркаптофеніл, 2-, 3- та 4галофеніл (включаючи 2-, 3- та 4- фторфеніл та 2-, 3- та 4-хлорфеніл), 2,3-, 2,4-, 2,5-, 2,6-, 3,4- та 3,5-диметилфеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- та 3,5біскарбоксиетилфеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- та 3,5-диметоксифеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- та 3,5-дигалофеніл (включаючи 2,4-дифторфеніл та 3,5-дифторфеніл), 2-, 3- та 4-галоалкілфеніл (1-5 атомів галогену, C1-C12алкіл, включаючи 4трифторметилфеніл), 2-, 3- та 4-ціанофеніл, 2-, 3та 4-нітрофеніл, 2-, 3- та 4-галоалкілбензил (1-5 атомів галогену, C1-C12алкіл, включаючи 4трифторметилбензил та 2-, 3та 4трихлорметилфеніл та 2-, 3та 4трихлорметилфеніл), 4-N-метилпіперидиніл, 3-Nметилпіперидиніл, 1-етилпіперазиніл, бензил, алкілсаліцилфеніл (C1-C4 алкіл, включаючи 2-, 3та 4-етилсаліцилфеніл), 2-,3- та 4-ацетилфеніл, 1,8-дигідроксинафтил (-C10H6-OH) та арилоксиетил [C6-C9арил (включаючи феноксиетил)], 2,2дигідроксибіфеніл, 2-, 3та 4-N,Nдіалкіламінофенол, -C6H4CH2-N(CH3)2, триметоксибензил, триетоксибензил, 2-алкілпіридиніл (C14алкіл); Складні ефіри 2-карбоксифенілу та C1C4алкілен-C3-C6арил (включаючи бензил, -CH2піроліл, -CH2-тієніл, -CH2-імідазоліл, -CH2оксазоліл, -CH2-ізоксазоліл, -CH2-тіазоліл, -CH2ізотіазоліл, -CH2-піразоліл, -CH2-піридиніл та CH2-піримідиніл), заміщений в арильній частині 35 атомами галогену, 1-2 атомами або групами, вибраними з галогену, C1-C12алкокси (включаючи метокси та етокси), ціано, нітро, OH, C1C12галоалкілу (1-6 атомів галогену, включаючи СH2-CCl3), C1-C12 алкілу (включаючи метил та етил), C2-C12 алкенілу або C2-C12 алкінілу; алкоксиетил [C1-C6алкіл, включаючи -CH2CH2-O-CH3 (метокси етил)]; алкіл, заміщений будь-якою з груп, приведених вище для арилу, зокрема, OH або 1-3 атомами гало (включаючи -CH3, -CH(CH3)2, -C(CH3)3, CH2CH3, -(CH2)2CH3, -(CH2)3CH3, -(CH2)4CH3, (CH2)5CH3, -CH2CH2F, -CH2CH2Cl, -CH2CF3 та CH2(OC(O)CH2R ), холестерил, енолпіруват (HOOC-C(=CH2)-), гліцерин, моносахарид з 5-6 атомів вуглецю, дисахарид або олігосахарид (3-9 моносахаридних залишків); тригліцериди, такі як -D--дигліцериди (де жирні кислоти, що складають ліпіди гліцеринів, в основному являють собою природні насичені або ненасичені C6-26, C6-18 або C6-10жирні кислоти, такі як ліноленова, лаврова, міристинова, пальмітинова, стеаринова, олеїнова, пальмітолеїнова, ліноленова та т.п. жирні кислоти), зв’язані з ацилом вихідних сполук в даному контексті за допомогою гліцерильного кисню тригліцериду; фосфоліпіди, зв’язані з карбоксильною групою за допомогою фосфату фосфоліпіду; фталідил (показаний на фіг. 1 статті Clayton et al., Antimicrob. Agents Chemo. 5(6):670671 [1974]); циклічні карбонати, такі як (5-Rd-2оксо-1,3-діоксолен-4-іл)метилові складні ефіри (див. статтю Sakamoto et al., Chem. Pharm. Bull. 1 4 32(6)2241-2248 [1984]), де Rd являє собою R , R CH2CCl3); -N-2-пропілморфоліно, 2,3-дигідро-6-гідроксиінден, сезамол, катехоло1 1 вий моноефір, -CH2-C(O)-N(R )2, -CH2-S(O)(R ), 1 CH2-S(O)2(R1), -CH2CH(OC(O)CH2R ) 1 або арил; та Гідроксильні групи сполук, що відповідають даному винаходу, необов’язково заміщені однією 25 з груп III, IV або V, описаних в заявці WO 94/021604 або ізопропілом. Як варіанти здійснення в таблиці A перера2 ховані приклади складноефірних частин A , які, наприклад, можуть бути зв’язані за допомогою кисню з групами -C(O)O- та -P(O)(R)(O-). Показаний також ряд амідатів, які зв’язані безпосередньо з -C(O)- або -P(O)2-. Складні ефіри структур 1-5, 8-10 та 16, 17, 19-22 синтезують шляхом реакції сполуки, описаної в даному матеріалі, що має вільний гідроксил, з відповідним галідом (хлоридом або ацилхлоридом та т.п.) та N,N 96295 26 дициклогексил-N-морфолінкарбоксамідином (або іншою основою, такою як DBU, триетиламін, CsCO3, N,N-диметиланілін та т.п.) в ДМФА (диметилформаміді) (або іншому розчиннику, такому як 3 ацетонітрил або N-метилпіролідон). Коли A являє собою фосфонат, складні ефіри структур 5-7, 11, 12, 21 та 23-26 синтезують реакцією спирту або солі алкоксиду (або відповідних амінів у випадку таких сполук, як 13, 14 та 15), з монохлорфосфонатом або дихлорфосфонатом (або іншим активованим фосфонатом). Таблиця А 1. -CH2-C(O)-N(R1)2* 2. -CH2-S(O)(R1) 3. -CH2-S(O)2(R1) 4. -CH2-O-C(O)-CH2-C6H5 5. 3-хлорестерил 6. 3-піридил 7. N-етилморфоліно 8. -CH2-O-C(O)-C6H5 9. -CH2-O-C(O)-CH2CH3 10. -CH2-O-C(O)-C(CH3)3 11. -CH2-CCl3 12. -C6H5 13. -NH-CH2-C(O)O-CH2CH3 14. -N(CH3)-CH2-C(O)O-CH2CH3 15. -NHR1 16. -CH2-O-C(O)-C10H15 17. -CH2-O-C(O)-CH(CH3)2 18. -CH2-C#H(OC(O)CH2R1)-CH2-(OC(O)CH2R1)* # - хіральним центром є (R), (S) або рацемат. Інші складні ефіри, які підходять для застосування в даному контексті, описані в європейському патенті № 632048. 2 A також включає "подвійний складний ефір", що формує профункціональності, такі як CH2ОC(O)OCH3, -CH2SCOCH3, CH2ОCON(CH3)2 або алкілабо арилацилоксиалкільна групи структури 1 1 CH(R )O((CO)R37) або -CH(R )((CO)OR38) (зв’язані з киснем кислотної групи), де R37 та R38 являють собою алкільну, арильну або алкіларильну групи (див. патент США № 4968788). Часто R37 та R38 являють собою об’ємисті групи, такі як розгалужений алкіл, орто-заміщений арил, метазаміщений арил або їх комбінації, включаючи нормальний, вторинний, ізо- та третинний алкіли з 1-6 атомів вуглецю. Прикладом є півалоїлоксиметильна група. Вони особливо застосовні з пролікарськими формами для перорального застосування. Прикладами даних використовуваних груп 2 A є алкілацилоксиметилові складні ефіри та їх похідні, включаючи CH(CH2CH2OCH3)OC(O)C(CH3)3, CH2OC(O)C10H15, -CH2ОC(O)C(CH3)3, CH(CH2OCH3)OC(O)C(CH3)3, CH(CH(CH3)2)OC(O)C(CH3)3, CH2OC(O)CH2CH(CH3)2, -CH2OC(O)C6H11, CH2OC(O)C6H5, -CH2OC(O)C10H15, CH2OC(O)CH2CH3, -CH2OC(O)CH(CH3)2, CH2OC(O)C(CH3)3 та -CH2OC(O)CH2C6H5. Для цілей пролікарських форм складний ефір, як правило, вибирають із одного з раніше використовуваних для противірусних лікарських препаратів, зокрема, циклічних карбонатів, подвійних складних ефірів або фталідилових, арилових або алкілових складних ефірів. 3 2 Як відзначено, групи A або A необов'язково використовують для попередження побічних реакцій із захищеною групою у процесі процедур синтезу, тому вони діють як захисні групи (PRT) 27 під час синтезу. Головним чином рішення відносно того, які групи захищати, коли це робити та природи PRT буде залежати від хімії реакції, у відношенні якої здійснюють захист (наприклад, кислих, лужних, окисних, відновлювальних або інших умов) та планованого напрямку синтезу. Не потрібно, щоб групи PRT були, та вони, як правило, не є однаковими, якщо сполуку заміщено багатьма PRT. У загальному PRT будуть використовувати для захисту карбоксильної, гідроксильної або аміногруп. Порядок зняття захисту для одержання вільних груп залежить від планованого напрямку синтезу та умов реакції, з якими стикаються, та може відбуватися в будьякому порядку, який встановлює дослідник. У ряді варіантів здійснення захищена за до2 помогою A кислотна група являє собою склад2 ний ефір кислотної групи та A є залишком гідроксил-вмісної функціональності. В інших варіантах здійснення використовують аміносполуку для захисту кислотної функціональності. Залишки підходящих гідроксил- або аміно-вмісних функціональностей наведені вище або їх можна знайти в заявці WO 95/007920. Особливий інтерес представляють залишки амінокислот, складних ефірів амінокислот, поліпептидів або арилових спиртів. Типові залишки амінокислот, поліпептидів та карбоніл-естерифікованих амінокислот описані на стор. 11-18 та у відповідному матеріалі WO 95/007920 як групи L1 або L2. У заявці WO 95/007920 ясно описані амідати фосфонових кислот, але слід мати на увазі, що дані амідати утворені з будь-який з кислотних груп, наведених у даному контексті, та залишків амінокислот, наведених у заявці WO 95/007920. 2 Типові складні ефіри A для захисту кислот3 них функціональностей A описані також у заявці WO 95/007920, знову маючи на увазі, що такі ж складні ефіри можуть бути утворені з кислотними групами, описаними в даному контексті, як з фосфонатами, представленими в публікації '920. Типові складноефірні групи визначені щонайме31 нше в WO 95/007920, див. стор. 89-93 (під R або 35 1 R ), таблицю на стор. 105 та стор. 21-23 (як R ). Особливий інтерес представляють складні ефіри незаміщеного арилу, такого як феніл, або арилалкілу, такого як бензил або гідрокси-, гало-, алкокси-, карбокси- та/або алкіловий складний ефір карбокси-заміщений арил або алкіларил, особливо феніл, орто-етоксифеніл або C1-C4алкіловий складний ефір карбоксифеніл (саліцилатC1C12алкілові складні ефіри). 3 Захищені кислотні групи A , особливо при використанні складних ефірів або амідів, представлених в WO 95/007920, використовують як пролікарські форми для перорального застосування. Однак для ефективного введення сполук, що відповідають винаходу, пероральним шляхом не 3 є важливим, щоб кислотна група А була захищеною. Коли сполуки, що відповідають винаходу, що мають захисні групи, зокрема, амідати амінокислот або заміщені та незаміщені арилові складні ефіри вводять системно або перорально, вони здатні до гідролітичного розщеплення in vivo з утворенням вільної кислоти. 96295 28 Захищають один або більше кислотних гідроксилів. Якщо захищають більше одного кислотного гідроксилу, то використовують однакові або різні захисні групи, наприклад, складні ефіри можуть бути різними або однаковими, або можна використовувати комбінацію амідату та складного ефіру. 2 Типові захисні групи гідрокси А , описані в Green (див. стор. 14-118) включають прості ефіри (метиловий); заміщені прості метилові ефіри (метоксиметиловий, метилтіометиловий, третбутилтіометиловий, (фенілдиметилсиліл)метоксиметиловий, бензилоксиметиловий, пметоксибензилоксиметиловий, (4метоксифенокси)-метиловий, гваяколметиловий, трет-бутоксиметиловий, 4пентенілоксиметиловий, сілоксиметиловий, 2метоксиетоксиметиловий, 2,2,2трихлоретоксиметиловий, біс(2хлоретокси)метиловий, 2(триметилсиліл)етоксиметиловий, тетрагідропіраніловий, 3-бромтетрагідропіраніловий, тетрагідротіопіраніловий, 1-метоксициклогексиловий, 4метокситетрагідропіраніловий, 4метокситетрагідротіопіраніловий, 4метокситетра-гідротіопіраніл-S,S-діоксидо, 1-[(2хлор-4-метил)феніл]-4-метоксипіперидин-4іловий, 3,5,1,4-діоксан-2-іловий, тетрагідрофураніловий, тетрагідротіофураніловий, 2,3,3a,4,5,6,7,7a-октагідро-7,8,8-триметил-4,7метанoбензофуран-2-іловий)); заміщені прості етилові ефіри (1-етоксиетиловий, 1-(2хлоретокси)етиловий, 1-метил-1метоксиетиловий, 1-метил-1бензилоксиетиловий, 1-метил-1-бензилокси-2фторетиловий, 2,2,2-трихлоретиловий, 2триметилсилілетиловий, 2(фенілселеніл)етиловий, трет-бутиловий, аліловий, п-хлорфеніловий, п-метоксифеніловий, 2,4динітрофеніловий, бензиловий); заміщені прості бензилові ефіри (п-метоксибензиловий, 3,4диметоксибензиловий, o-нітробензиловий, пнітробензиловий, п-галобензиловий, 2,6дихлорбензиловий, п-ціанобензиловий, пфенілбензиловий, 2- та 4-піколіловий, 3-метил-2піколіл-N-оксидо, дифенілметиловий, п,п'динітробензгідриловий, 5-дибензосубериловий, трифенілметиловий, нафтилдифенілметиловий, пметоксифенілдифенілметиловий, ди(пметоксифеніл)фенілметиловий, три(пметоксифеніл)метиловий, 4-(4'бромфенацилокси)фенілдифенілметиловий, 4,4',4"-тріс(4,5-дихлорфталімідофеніл)метиловий, 4,4',4"тріс(левуліноїлоксифеніл)метиловий, 4,4',4"тріс(бензоїлокси-феніл)метиловий, 3-(імідазол-1ілметил)біс(4',4"диметоксифеніл)метиловий, 1,1-біс(4-метоксифеніл)-1'-піренілметиловий, 9антриловий, 9-(9-феніл)ксантеніловий, 9-(9феніл-10-оксо)антриловий, 1,3-бензодитіолан-2іловий, бензізотіазоліл S,S-діоксидо); прості силілові ефіри (триметилсиліловий, триетилсиліловий, триізопропілсиліловий, диметилізопропілсиліловий, діетилізопропілсиліловий, 29 96295 30 диметилтексилсиліловий, третбутилдиметилсиліловий, третбутилдифенілсиліловий, трибензилсиліловий, три-п-ксилілсиліловий, трифенілсиліловий, дифенілметилсиліловий, третбутилметоксифенілсиліловий); складні ефіри (форміат, бензоїлформіат, ацетат, хлорацетат, дихлорацетат, трихлорацетат, трифторацетат, метоксиацетат, трифенілметоксиацетат, феноксиацетат, п-хлорфеноксиацетат, пполіфенілацетат, 3-фенілпропіонат, 4оксопентаноат (левулінат), 4,4(етилендитіо)пентаноат, півалоат, адамантоат, кротонат, 4-метоксикротонат, бензоат, пфенілбензоат, 2,4,6-триметилбензоат (мезитоат)); карбонати (метил, 9-флуоренілметил, етил, 2,2,2-трихлоретил, 2-(триетилсиліл)етил, 2(фенілсульфоніл)етил, 2(трифенілфосфоніо)етил, ізобутил, вініл, аліл, пнітрофеніл, бензил, п-метоксибензил, 3,4диметоксибензил, o-нітробензил, п-нітробензил, S-бензилтіокарбонат, 4-етокси-1-нафтил, метилдитіокарбонат); групи з допоміжним розщепленням (2-йодобензоат, 4-азидобутират, 4-нітро-4метилпентаноат, o-(дибромметил)бензоат, 2формілбензолсульфонат, 2(метилтіометокси)етилкарбонат, 4(метилтіометокси)-бутират, 2(метилтіометоксиметил)бензоат); інші складні ефіри (2,6-дихлор-4-метилфеноксиацетат, 2,6дихлор-4-(1,1,3,3-тетраметилбутил)феноксиацетат, 2,4-біс(1,1диметилпропіл)феноксиацетат, хлордифенілацетат, ізобутират, моносукциноат, (E)-2-метил-2бутеноат (тиглоат), o-(метоксикарбоніл)бензоат, п-полібензоат, -нафтоат, нітрат, алкіл N,N,N',N,тетраметилфосфородіамідат, N-фенілкарбамат, борат, диметилфосфінотіоїл, 2,4 динітрофенілсульфенат) та сульфонати (сульфат, метансульфонат (мезилат), бензилсульфонат, тозилат). 2 Більш типово, коли захисні групи гідрокси А включають заміщені метилові прості ефіри, заміщені бензилові прості ефіри, силілові прості ефіри та складні ефіри, включаючи складні ефіри сульфонових кислот, ще більш типово триалкілсилілові прості ефіри, тозилати та ацетати. Типові захисні групи 1,2-діолу (відповідно, як правило, коли дві групи OH беруть разом з захи2 сною функціональністю A ) описані в роботі Greene на стор. 118-142 та включають циклічні ацеталі та кеталі (метилен, етиліден, 1-третбутилетиліден, 1-фенілетиліден, (4метоксифеніл)етиліден, 2,2,2-трихлоретиліден, ацетонід (ізопропіліден), циклопентиліден, циклогексиліден, циклогептиліден, бензиліден, пметоксибензиліден, 2,4-диметоксибензиліден, 3,4-диметоксибензиліден, 2-нітробензиліден); циклічні складні орто-ефіри (метоксиметилен, етоксиметилен, диметоксиметилен, 1метоксиетиліден, 1-етоксиетиліден, 1,2диметоксиетиліден, α-метоксибензиліден, 1-(N,Nдиметиламіно)етиліденову похідну, -(N,Nдиметиламіно)бензиліденову похідну, 2оксациклопентиліден); силілові похідні (ди-третбутилсиліленова група, 1,3-(1,1,3,3тетраізопропілдисилілоксаніліден) та тетра-третбутоксидисилоксан-1,3-дііліден), циклічні карбонати, циклічні боронати, етилборонат та фенілборонат. Більш типово, коли захисні групи 1,2-діолу включають представлені в таблиці B, ще більш типово епоксиди, ацетоніди, циклічні кеталі та арилкеталі. Таблиця B 9 де R являє собою C1-C6алкіл. 2 A також являє собою H, захисну групу для аміно або сполуки, що містить залишок карбоксилу, зокрема, H, -C(O)R4, амінокислоту, поліпептид або захисну групу, відмінну від -C(O)R4, аміноки2 слоти або поліпептиду. Амід-формуюче A знахо3 2 диться, наприклад, в групі A . Коли A являє собою амінокислоту або поліпептид, воно має структуру R15NHCH(R16)C(O)-, де R15 являє собою H, залишок амінокислоти або поліпептиду, або R15 та R16 визначені нижче. R16 являє собою нижчий алкіл або нижчий алкіл (C1-C6), заміщений аміно, карбоксилом, амідом, складним ефіром карбонової кислоти, гідроксилом, C6-C7арилом, гуанідинілом, імідазолілом, індолом, сульфгідрилом, сульфоксидом та/або алкілфосфатом. R10 також беруть разом з амінокислотою αN для формування залишку проліну (R10 = -(CH2)3-). Однак, R10 являє собою, як правило, бічну групу природної амінокислоти, таку як H, -CH3, -CH(CH3)2, -CH2-CH(CH3)2, CHCH3-CH2-CH3, -CH2-C6H5, -CH2CH2-S-CH3, CH2OH, -CH(OH)-CH3, -CH2-SH, -CH2-C6H4OH, CH2-CO-NH2, -CH2-CH2-CO-NH2, -CH2-COOH, CH2-CH2-COOH, -(CH2)4NH2 та -(CH2)3-NH-C(NH2) 31 NH2. R10 також включає 1-гуанідинопроп-3-іл, бензил, 4- гідроксибензил, імідазол-4-іл, індол-3-іл, 2 метоксифеніл та етоксифеніл. A являють собою здебільшого залишки карбонових кислот, але використовують будь-яку з типових захисних груп аміно, описаних в роботі Greene на стор. 315-385. Вони включають карбамати (метил та етил, 9флуоренілметил, 9(2-сульфо)флуоренілметил, 9(2,7-дибром)фторметил, 2,7-ди-трет-бутил-[9(10,10-діоксо-10,10,10,10-тетрагідротіоксантил)]метил, 4-метоксифенацил); заміщений етил (2,2,2-трихлоретил, 2триметилсилілетил, 2-фенілетил, 1-(1адамантил)-1-метилетил, 1,1-диметил-2галоетил, 1,1-диметил-2,2-диброметил, 1,1диметил-2,2,2-трихлоретил, 1-метил-1-(4біфеніліл)етил, 1-(3,5-ди-трет-бутилфеніл)-1метилетил, 2-(2'- та 4'-піридил)етил, 2-(N,Nдициклогексилкарбоксамідо)етил, трет-бутил, 1адамантил, вініл, аліл, 1-ізопропілаліл, циннаміл, 4-нітроциннаміл, 8-хіноліл, N-гідроксипіперидиніл, алкілдитіо, бензил, п-метоксибензил, пнітробензил, п-бромбензил, п-хлорбензил, 2,4дихлорбензил, 4-метилсульфінілбензил, 9антрилметил, дифенілметил); групи з допоміжним розщепленням (2-метилтіоетил, 2метилсульфонілетил, 2-(п-толуолсульфоніл)етил, [2-(1,3-дитіаніл)]метил, 4-метилтіофеніл, 2,4диметилтіофеніл, 2-фосфоніоетил, 2трифенілфосфоніоізопропіл, 1,1-диметил-2ціаноетил, м-хлор-п-ацилоксибензил, п(дигідроксиборил)бензил, 5бензізоксазолілметил, 2-(трифторметил)-6хромонілметил); групи, здатні до фотолітичного розщеплення (м-нітрофеніл, 3,5диметоксибензил, o-нітробензил, 3,4-диметокси6-нітробензил, феніл(о-нітрофеніл)метил); похідні типу сечовини (фенотіазиніл-(10)-карбоніл, N'-птолуолсульфоніламінокарбоніл, N'феніламінотіокарбоніл); інші карбамати (третаміл, S-бензилтіокарбамат, п-ціанобензил, циклобутил, циклогексил, циклопентил, циклопропілметил, п-децилоксибензил, діізопропілметил, 2,2-диметоксикарбонілвініл, o-(N,Nдиметилкарбоксамідо)бензил, 1,1-диметил-3(N,N-диметилкарбоксамідо)пропіл, 1,1диметилпропініл, ди(2-піридил)метил, 2фуранілметил, 2-йодоетил, ізоборніл, ізобутил, ізонікотиніл, п-(п'-метоксифенілазо)бензил, 1метилциклобутил, 1-метилциклогексил, 1-метил1-циклопропілметил, 1-метил-1-(3,5диметоксифеніл)етил, 1-метил-1-(п- фенілазофеніл)етил, 1-метил-1-фенілетил, 1-метил-1-(4піридил)етил, феніл, п-(фенілазо)бензил, 2,4,6три-трет-бутилфеніл, 4-(триметиламоній)бензил, 2,4,6-триметилбензил); аміди (N-форміл, Nацетил, N-хлорацетил, N-трихлорацетил, Nтрифторацетил, N-фенілацетил, N-3фенілпропіоніл, N-піколіноїл, N-3піридилкарбоксамід, N-бензоїлфенілаланіл, Nбензоїл, N-п-фенілбензоїл); аміди з допоміжним розщепленням (N-o-нітрофенілацетил, N-oнітрофеноксиацетил, N-ацетоацетил, (N'дитіобензилоксикарбоніламіно)ацетил, N-3-(пгідроксифеніл)-пропіоніл, N-3-(o 96295 32 нітрофеніл)пропіоніл, N-2-метил-2-(oнітрофенокси)-пропіоніл, N-2-метил-2-(αфенілазофенокси)пропіоніл, N-4-хлорбутирил, N3-метил-3-нітро-бутирил, N-o-нітроциннамоїл, Nацетилметіонін, N-o-нітробензоїл, N-o(бензоїлоксиметил)бензоїл, 4,5-дифеніл-3оксазолін-2-он); похідні циклічних імідів (Nфталімід, N-дитіасукциноїл, N-2,3дифенілмалеоїл, N-2,5-диметилпіроліл, адукт N1,1,4,4-тетраметилдисилілазациклопентану, 5заміщений 1,3-диметил-1,3,5-триазациклогексан2-он, 5-заміщений 1,3-дибензил-1,3-5триазациклогексан-2-он, 1-заміщений 3,5динітро-4-піридоніл); N-алкіл та N-ариламіни (Nметил, N-аліл, N-[2-(триметилсиліл)етокси]метил, N-3-ацетоксипропіл, N-(1-ізопропіл-4-нітро-2-оксо3-піролин-3-іл), солі четвертинного амонію, Nбензил, N-ди(4-метоксифеніл)метил, N-5дибензосуберил, N-трифенілметил, N-(4метоксифеніл)дифенілметил, N-9фенілфлуореніл, N-2,7-дихлор-9флуоренілметилен, N-фероценілметил, N-2піколіламін N'-оксид), похідні іміну (N-1,1диметилтіометилен, N-бензиліден, N-пметоксибензиліден, N-дифенілметилен, N-[(2піридил)мезитил]метилен, N,(N',N'диметиламінометилен, N,N'-ізопропілиден, N-пнітробензиліден, N-саліциліден, N-5хлорсаліциліден, N-(5-хлор-2гідроксифеніл)фенілметилен, N-циклогексиліден); похідні енаміну (N-(5,5-диметил-3-оксо-1циклогексеніл)); похідні N-металів (похідні Nборану, похідні N-дифенілборинової кислоти, N[феніл(пентакарбонілхром або -вольфрам)] карбеніл, хелат N-міді або N-цинку); N-N-похідні (Nнітро, N-нітрозо, N-оксид); N-P-похідні (Nдифенілфосфініл, N-диметилтіофосфініл, Nдифенілтіофосфініл, N-діалкілфосфорил, Nдибензилфосфорил, N-дифенілфосфорил); N-Siпохідні; N-S-похідні; N-сульфенілові похідні (Nбензолсульфеніл, N-o-нітробензолсульфеніл, N2,4-динітробензолсульфеніл, Nпентахлорбензолсульфеніл, N-2-нітро-4метоксибензолсульфеніл, Nтрифенілметилсульфеніл, N-3нітропіридинсульфеніл) та N-сульфонілові похідні (N-п-толуолсульфоніл, N-бензолсульфоніл, N2,3,6-триметил-4-метоксибензолсульфоніл, N2,4,6-триметоксибензолсульфоніл, N-2,6диметил-4-метоксибензолсульфоніл, Nпентаметилбензолсульфоніл, N-2,3,5,6,тетраметил-4-метоксибензолсульфоніл, N-4метоксибензолсульфоніл, N-2,4,6триметилбензолсульфоніл, N-2,6-диметокси-4метилбензолсульфоніл, N-2,2,5,7,8пентаметилхроман-6-сульфоніл, Nметансульфоніл, N-Dтриметилсилілетансульфоніл, N-9антраценсульфоніл, N-4-(4',8'диметоксинафтилметил)бензолсульфоніл, Nбензилсульфоніл, N-трифторметилсульфоніл, Nфенацилсульфоніл). Більш типово, коли захищені аміногрупи включають карбамати та аміди, ще більш типово 1 1 1 - -NHC(O)R або -N=CR N(R )2. Інша захисна гру 33 па, що також використовують як пролікарську 3 форму в центрі A , зокрема, для аміно або NH(R5), являє собою: див., наприклад, статтю Alexander, J. et al.; J. Med. Chem. 1996, 39, 480-486. 2 A являє собою також H або залишок аміновмісної сполуки, зокрема, амінокислоти, поліпептиду, захисної групи, -NHSO2R4, NHC(O)R4, N(R4)2, NH2 або -NH(R4)(H), де, наприклад, проводять реакцію групи карбоксилу або фосфоно3 вої кислоти A з аміном з утворенням аміду, як у 2 2 2 C(O)A , -P(O)(A )2 або -P(O)(OH)(A ). Як правило, 2 A має структуру R17C(O)CH(R16)NH-, де R17 яв2 ляє собою OH, OA , OR5, залишок амінокислоти або поліпептиду. Амінокислоти являють собою низькомолекулярні сполуки молекулярної маси порядку менше ніж приблизно 1000, які включають щонайменше одну аміно або іміногрупу та щонайменше одну карбоксильну групу. Як правило, амінокислоти будуть виявляти в природних умовах, тобто їх можна виявити в біологічному матеріалі, такому як бактерії або інші мікроорганізми, рослини, тварини або людина. Підходящі амінокислоти, як правило, являють собою -амінокислоти, тобто сполуки, що характеризуються одним аміно- або іміно-атомом азоту, відділеним від атому вуглецю карбоксильної групи одним заміщеним або незаміщеним -атомом вуглецю. Особливий інтерес представляють гідрофобні залишки, такі як моноабо діалкіл- або ариламінокислоти, циклоалкіламінокислоти тощо. Дані залишки вносять вклад в проникність клітин шляхом підвищення коефіцієнту розподілення вихідного лікарського препарату. Як правило, залишок не включає сульфгідрильний або гуанідино-замісник. Залишками природних амінокислот є такі залишки, як виявлені в природних умовах в рослинах, тваринах або мікроорганізмах, особливо в їх білках. Найбільш типово, коли поліпептиди будуть в основному складатися з даних залишків природних амінокислот. Дані амінокислоти являють собою гліцин, аланін, валін, лейцин, ізолейцин, серін, треонін, цистеїн, метіонін, глутамінову кислоту, аспарагінову кислоту, лізин, гідроксилізин, аргінін, гістидин, фенілаланін, тирозин, триптофан, пролін, аспарагін, глутамін та гідроксипролін. 2 Коли A являють собою окремі залишки амінокислот або поліпептиди, вони звичайно замі3 щені в положенні A . Дані кон’югати отримують шляхом утворення амідного зв’язку між карбоксильною групою амінокислоти (або, наприклад, C-кінцевою амінокислотою поліпептиду) та амінним азотом. Аналогічно формують кон’югати між 3 A та аміногрупою амінокислоти або поліпептиду. Як правило, тільки один з яких-небудь центрів 96295 34 вихідної молекули амідований амінокислотою, як описано в даному контексті, хоча в обсяг даного винаходу входить інтродукція амінокислот в більш, ніж один допустимий центр. Звичайно кар3 боксильну групу A амідують амінокислотою. Як правило, -аміно або -карбоксильна група амінокислоти або кінцева аміно або карбоксильна група поліпептиду зв’язані з вихідними функціональностями, тобто карбоксильну або аміногрупи в бічних ланцюгах амінокислот звичайно не використовують для утворення амідних зв’язків з вихідною сполукою (хоча може знадобитися, щоб дані групи були захищені під час синтезу кон’югатів, як далі описано нижче). У відношенні карбоксил-вмісних бічних ланцюгів амінокислот або поліпептидів слід мати на увазі, що карбоксильна група необов’язково буде блокувати, на2 приклад, за допомогою A , естерифікована за 2 2 допомогою A або амідована за допомогою A . Аналогічно амінобічні ланцюги R16 необов’язково 2 будуть блоковані A або заміщені R5. Дані складно-ефірні або амідні зв’язки з аміно або карбоксильною групами бічних ланцюгів, подібно складним ефірам або амідам вихідної молекули, необов’язково гідролізуються in vivo або in vitro в кислих (pH10) умовах. Альтернативно вони є в суттєвому степені стабільними в шлунково-кишковому тракті людини, але ферментативно гідролізуються в крови або внутріклітинних умовах. Складні ефіри або амідати амінокислот або поліпептидів також використовують як проміжні продукти для одержання вихідної молекули, що включає вільні аміно або карбоксильні групи. Вільна кислота або основа вихідної сполуки, наприклад, легко утворюються зі складних ефірів або кон’югатів амінокислот або поліпептидів, що відповідають даному винаходу, за допомогою прийнятих способів гідролізу. Коли залишок амінокислоти включає один або більше хіральних центрів, можуть бути використані будь-який з D-, L-, мезо-, трео- або еритро- (відповідно) рацематів, скалематів або їх сумішей. Як правило, якщо проміжні продукти повинні бути гідролізовані неферментативно (як було б у випадку, коли аміди використовують як хімічні проміжні продукти для одержання вільних кислот або вільних амінів), використовують Dізомери. З іншого боку, L-ізомери є більш універсальними, оскільки вони можуть бути чутливими як до неферментативного, так і до ферментативного гідролізу та більш ефективно транспортуються системами транспорту амінокислот або дипептидилів в шлунково-кишковому тракті. Прикладами підходящих амінокислот, залиш2 ки яких представлені в A , включають наступні: гліцин; амінополікарбонові кислоти, наприклад, аспарагінову кислоту, -гідроксиаспарагінову кислоту, глутамінову кислоту, -гідроксиглутамінову кислоту, -метиласпарагінову кислоту, метилглутамінову кислоту, ,диметиласпарагінову кислоту, гідроксиглутамінову кислоту, ,дигідроксиглутамінову кислоту, 35 фенілглутамінову кислоту, -метиленглутамінову кислоту, 3-аміноадипінову кислоту, 2амінопімелінову кислоту, 2-аміносуберінову кислоту та 2-аміносебацинову кислоту; аміди амінокислот, такі як глутамін та аспарагін; поліаміно- або поліосновні монокарбонові кислоти, такі як аргінін, лізин, -аміноаланін, амінобутирин, орнітин, цитруллін, гомоаргінін, гомоцитруллін, гідроксилізин, аллогідроксилізин та діаміномасляна кислота; інші залишки основних амінокислот, такі як гістидин; діамінодикарбонові кислоти, такі як ,'діаміноянтарна кислота, ,'-діаміноглутарова кислота, ,'-діаміноадипінова кислота, ,'діамінопімелінова кислота, ,'-діаміно-гідроксипімелінова кислота, ,'діаміносуберинова кислота, ,'діаміноазелаїнова кислота та ,'діаміносебацинова кислота; імінокислоти, такі як пролін, гідроксипролін, аллогідроксипролін, γ-метилпролін, піпеколінова кислота, 5-гідроксипіпеколінова кислота та азетидин-2-карбонова кислота; моно або діалкіл (як правило, C1-C8 розгалужений або нормальний) амінокислота, така як аланін, валін, лейцин, алілгліцин, бутирин, норвалін, норлейцин, гептилін, -метилсерін, аміно--метил--гідроксивалеріанова кислота, аміно--метил--гідроксивалеріанова кислота, аміно--метил--гідроксикапронова кислота, ізовалін, -метилглутамінова кислота, аміноізомасляна кислота, -амінодіетилоцтова кислота, -амінодіізопропілоцтова кислота, аміноди-н-пропілоцтова кислота, амінодіізобутилоцтова кислота, -аміноди-нбутилоцтова кислота, аміноетилізопропілоцтова кислота, -аміно-нпропілоцтова кислота, -амінодіізоамінооцтова кислота, -метиласпарагінова кислота, метилглутамінова кислота, 1-аміноциклопропан1-карбонова кислота, ізолейцин, алоізолейцин, трет-лейцин, -метилтриптофан та -аміно-етил--фенілпропіонова кислота; -фенілсерініл; аліфатичні -аміно--гідроксикислоти, такі як серін, -гідроксилейцин, -гідроксинорлейцин, гідроксинорвалін та -аміно--гідроксистеаринова кислота; -аміно, -, -, - або -гідроксикислоти, такі як залишки гомосеріну, -гідроксинорваліну, гідроксинорваліну та -гідроксинорлейцину; канаванін та канавалін; -гідроксиорнітин; 2-гексозамінові кислоти, такі як Dглюкозамінова кислота або D-галактозамінова кислота; -аміно--тіоли, такі як пеніцилламін, тіолнорвалін або -тіолбутирин; інші залишки сірковмісних амінокислот, що включають цистеїн; гомоцистин, -фенілметіонін, метіонін, S-аліл-1-цистеїнсульфоксид, 2 96295 36 тіолгістидин, цистатіонін та тіолові складні ефіри цистеїну або гомоцистеїну; фенілаланін, триптофан та цикл-заміщені амінокислоти, такі як феніл- або циклогексиламінокислоти, -амінофенілоцтова кислота, аміноциклогексилоцтова кислота та -аміно-циклогексилпропіонова кислота; аналоги фенілаланіну та похідні, що включають арил, нижчий алкіл, гідрокси, гуанідино, оксиалкілефір, нітро, сірка або гало-заміщений феніл (наприклад, тирозин, метилтирозин та o-хлор-, п-хлор-, 3,4дихлор, o-, м- або п-метил-, 2,4,6-триметил-, 2етокси-5-нітро-, 2-гідрокси-5-нітро- та п-нітрофенілаланін); фурил-, тієніл-, піридил-, піримідиніл-, пуринніл- або нафтил-аланіни, та аналоги та похідні триптофану, включаючи кінуренін, 3гідроксикінуренін, 2-гідрокситриптофан та 4карбоксyтриптофан; -амінозаміщені амінокислоти, включаючи саркозин (N-метилгліцин), N-бензилгліцин, Nметилаланін, N-бензилаланін, Nметилфенілаланін, N-бензилфенілаланін, Nметилвалін та N-бензилвалін; та -гідрокси та заміщені -гідрокси амінокислоти, включаючи серін, треонін, аллотреонін, фосфосерін та фосфотреонін. Поліпептиди являють собою полімери амінокислот, в яких карбоксильна група одного амінокислотного мономеру зв’язана з аміно- або іміногрупою наступного амінокислотного мономеру амідним зв’язком. Поліпептиди включають дипептиди, низькомолекулярні поліпептиди (молекулярної маси приблизно 1500-5000) та білки. Білки необов’язково включають 3, 5, 10, 50, 75, 100 або більше залишків та, відповідно, мають в суттєвому ступені гомологічну послідовність з білками людини, тварини, рослини або мікроорганізму. Вони включають ферменти (наприклад, пероксидазу), а також імуногени, такі як KLH (гемоціанін блюдечка), або антитіла чи білки будь-якого типу, у відношенні яких потрібно отримати імунну відповідь. Природа та ідентичність поліпептиду можуть широко варіювати. Амідати поліпептидів використовують як імуногени при утворенні антитіл у відношенні або поліпептиду (якщо він не є імуногенним у тварини, якій його вводять) або у відношенні епітопів на частині сполуки, що залишилася, що відповідає даному винаходу. Антибіотики, здатні до зв’язування з вихідною непептидильною сполукою, використовують для виділення вихідної сполуки з сумішей, наприклад, при діагностиці або одержанні вихідної сполуки. Кон’югати вихідної сполуки та поліпептиду, як правило, більш імуногенні, ніж поліпептиди у тварин з близькою гомологією, та внаслідок цього роблять поліпептид більш імуногенним, сприяючи утворенню антитіл до нього. Відповідно, необов’язково, щоб поліпептид або білок були імуногенними у тварини, що, як правило, використовують для утворення антитіл, наприклад, кролика, миші, коня або щура, але кінцевий продукт кон’югат повинен бути імуногенним у щонайменше одного з даних тварин. Поліпептид нео 37 бов’язково включає центр розщеплення пептидолітичним ферментом на пептидному зв’язку між першим та другим залишками, прилеглими до кислотного гетероатому. Дані центри розщеплення фланкіровані структурами розпізнавання ферменту, наприклад, визначеною послідовністю залишків, що розпізнається пептидолітичним ферментом. Пептидолітичні ферменти для розщеплення кон’югатів поліпептидів, що відповідають даному винаходу, добре відомі та, зокрема включають карбоксипептидази. Карбоксипептидази розщеплюють поліпептиди шляхом видалення Cкінцевих залишків та є специфічними у багатьох випадках у відношенні певних С-кінцевих послідовностей. Дані ферменти та їх вимоги до субстратів загалом добре відомі. Наприклад, дипептид (що має задану пару залишків та вільний карбоксильний кінець), ковалентно зв’язаний через свою α-аміногрупу з атомами фосфору або вуглецю сполук, описаних в даному контексті. В варіантах здійснення, де A3 являє собою фосфонат, очікують, що даний пептид буде розщеплюватися відповідним пептидолітичним ферментом, що видаляє карбоксил проксимального залишку амінокислоти, щоб аутокаталітично розщепити фосфоноамідатний зв’язок. Підходящі дипептидильні групи (позначені однобуквеним кодом) являють собою AA, AR, AN, AD, AC, AE, AQ, AG, AH, AI, AL, AK, AM, AF, AP, AS, AT, AW, AY, AV, RA, RR, RN, RD, RC, RE, RQ, RG, RH, RI, RL, RK, RM, RF, RP, RS, RT, RW, RY, RV, NA, NR, NN, ND, NC, NE, NQ, NG, NH, NI, NL, NK, NM, NF, NP, NS, NT, NW, NY, NV, DA, DR, DN, DD, DC, DE, DQ, DG, DH, DI, DL, DK, DM, DF, DP, DS, DT, DW, DY, DV, CA, CR, CN, CD, CC, CE, CQ, CG, CH, CI, CL, CK, CM, CF, CP, CS, CT, CW, CY, CV, EA, ER, EN, ED, EC, EE, EQ, EG, EH, EI, EL, EK, EM, EF, EP, ES, ET, EW, EY, EV, QA, QR, QN, QD, QC, QE, QQ, QG, QH, QI, QL, QK, QM, QF, QP, QS, QT, QW, QY, QV, GA, GR, GN, GD, GC, GE, GQ, GG, GH, GI, GL, GK, GM, GF, GP. GS, GT, GW, GY, GV, HA, HR, HN, HD, HC, HE, HQ, HG, HH, HI, HL, HK, HM, HF, HP, HS, HT, HW, HY, HV, IA, IR, IN, ID, IC, IE, IQ, IG, IH, II, IL, IK, IM, IF, IP, IS, IT, IW, IY, IV, LA, LR, LN, LD, LC, LE, LQ, LG, LH, LI, LL, LK, LM, LF, LP, LS, LT, LW, LY, LV, KA, KR, KN, KD, KC, KE, KQ, KG, KH, KI, KL, KK, KM, KF, KP, KS, KT, KW, KY, KV, MA, MR, MN, MD, MC, ME, MQ, MG, MH, MI, ML, MK, MM, MF, MP, MS, MT, MW, MY, MV, FA, FR, FN, FD, FC, FE, FQ, FG, FH, FI, FL, FK, FM, FF, FP, FS, FT, FW, FY, FV, PA, PR, PN, PD, PC, PE, PQ, PG, PH, PI, PL, PK, PM, PF, PP, PS, PT, PW, PY, PV, SA, SR, SN, SD, SC, SE, SQ, SG, SH, SI, SL, SK, SM, SF, SP, SS, ST, SW, SY, SV, TA, TR, TN, TD, TC, TE, TQ, TG, TH, TI, TL, TK, TM, TF, TP, TS, TT, TW, TY, TV, WA, WR, WN, WD, WC, WE, WQ, WG, WH, WI, WL, WK, WM, WF, WP, WS, WT, WW, WY, WV, YA, YR, YN, YD, YC, YE, YQ, YG, YH, YI, YL,YK, YM, YF, YP, YS, YT, YW, YY, YV, VA, VR, VN, VD, VC, VE, VQ, VG, VH, VI, VL, VK, VM, VF, VP, VS, VT, VW, VY та VV. 2 Як А використовують також залишки трипеп3 тидів. Коли A являє собою фосфонат, послідов 96295 38 4 5 4 ність -X -pro-X - (де X являє собою залишок 5 будь-якої амінокислоти та X являє собою залишок амінокислоти, карбоксил-складний ефір проліну або водень) буде розщеплюватися карбок4 сипептидазою просвіту кишки з утворенням X з вільним карбоксилом, який, у свою чергу, як очікують, аутокаталітично розщеплює фосфоноамі5 датний зв’язок. Карбоксигрупа X необов’язково естерифікована бензилом. Дипептидні або трипептидні елементи можна вибрати на підставі відомих властивостей транспорту та/або чутливості до пептидаз, які можуть впливати на транспорт у слизову оболонку кишки або інші типи клітин. Дипептиди та трипептиди з відсутністю α-аміногрупи являють собою транспортні субстрати для пептидного транспортера, що виявляються в мембрані щіткової облямівки клітин слизової оболонки кишки (див. статтю Bai, J.P.F., "PharmRes." 9:969-978 (1992)). Транспортно-компетентні пептиди можна у такий спосіб використати для підвищення біодоступності амідатних сполук. Ди- або трипептиди, що мають одну або більше амінокислот в D-конфігурації, також сумісні із транспортом пептидів та можуть бути використані в амідатних сполуках, що відповідають даному винаходу. Амінокислоти в Dконфігурації можна використовувати для зниження чутливості ди- або трипептиду до гідролізу протеазами, звичайними для щіткової облямівки, такими як амінопептидаза N (EC 3.4.11.2). Крім того, ди- або трипептиди альтернативно вибирають на основі їх відносної стійкості до гідролізу протеазами, що виявляють у просвіті кишки. Наприклад, трипептиди або поліпептиди, у яких відсутніми asp та/або glu, є недостатніми субстратами для амінопептидази A (EC 3.4.11.7), ди- або трипептиди, у яких відсутні залишки гідрофобних амінокислот з боку N-кінця (leu, tyr, phe, val, tip), є недостатніми субстратами для ендопептидази 24.11 (EC 3.4.24.11), та пептиди з відсутністю залишку pro у передостанньому положенні на вільному карбоксильному кінці є недостатніми субстратами для карбоксипептидази P (EC 3.4.17). Аналогічні міркування можна також застосувати до вибору пептидів, які або відносно стійкі, або відносно чутливі до гідролізу цитозольними, нирковими, печіночними, сироватковими або іншими пептидазами. Дані слабко розщеплювані амідати поліпептидів є імуногенами, або їх використовують для зв'язування з білками з метою одержання імуногенів. Сполуки, що інгібують ВГС Сполуки, що відповідають винаходу, включають ті, що мають інгібуючу ВГС активність, а також проміжні сполуки, які використовують для одержання активних сполук. Термін "сполука, що інгібує ВГС" включає ті сполуки, які інгібують ВГС. Як правило, сполуки, що відповідають винаходу, мають молекулярну масу від приблизно 200 аом (атомних одиниць маси) до приблизно 10000 аом; в окремому варіанті здійснення винаходу сполуки мають молекулярну масу менше ніж приблизно 5000 аом; в іншому окремому варіанті здійснення винаходу сполуки мають молекулярну масу менше ніж приблизно 2500 аом; в іншому 39 окремому варіанті здійснення винаходу сполуки мають молекулярну масу менше ніж приблизно 1000 аом; в іншому окремому варіанті здійснення винаходу сполуки мають молекулярну масу менше ніж приблизно 800 аом; в іншому окремому варіанті здійснення винаходу сполуки мають молекулярну масу менше ніж приблизно 600 аом та в іншому окремому варіанті здійснення винаходу сполуки мають молекулярну масу менше ніж приблизно 600 аом та молекулярну масу більше ніж приблизно 400 аом. Сполуки, що відповідають винаходу, також, як правило, мають logD (полярність) менше ніж приблизно 5. В одному варіанті здійснення винахід передбачає сполуки, що мають logD менше ніж приблизно 4; в іншому варіанті здійснення винахід передбачає сполуки, що мають logD менше ніж приблизно 3; в іншому варіанті здійснення винахід передбачає сполуки, що мають logD більше ніж приблизно -5; в іншому варіанті здійснення винахід передбачає сполуки, що мають logD більше ніж приблизно -3, та в іншому варіанті здійснення винахід передбачає сполуки, що мають logD більше ніж приблизно 0 та менше ніж приблизно 3. Вибрані замісники в сполуках, що відповідають винаходу, присутні рекурсивно. В даному контексті термін "рекурсивний замісник" означає, що замісник може представляти свій інший варіант. Теоретично внаслідок рекурсивної природи даних замісників в будь-якому даному варіанті здійснення може бути присутня велика кількість x y [замісників]. Наприклад, R включає замісник R . y 2 R може являти собою R , який, у свою чергу, 3 3 може являти собою R . Якщо вибирають, що R 3c являє собою R , то можна вибрати другий варіx ант R . Звичайний спеціаліст в галузі медичної хімії розуміє, що загальне число даних замісників розумно обмежено необхідними властивостями передбачуваної сполуки. Дані властивості включають як приклад, а не обмеження, фізичні властивості, такі як молекулярна маса, розчинність або log P, властивості, пов’язані з застосуванням, такі як активність у відношенні передбачуваної мішені, та практичні властивості, такі як простота синтезу. 3 2 1 Як приклад, а не обмеження, всі, A , A та R , являють собою рекурсивні замісники в ряді варіантів здійснення. Як правило, кожен з них незалежно один від іншого може бути включений 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1 або 0 раз в даному варіанті здійснення. Більш типово, коли кожен з них незалежно один від іншого може бути включений 12 або менше разів в даному варіанті здійснення. Усякий раз, коли сполука, описана в даному контексті, заміщена більше ніж однією з однаково позначених 1 3 груп, наприклад, "R " або "A ", буде зрозуміло, що групи можуть бути однаковими або різними, тобто, кожна група вибрана незалежно [від другої]. Хвилясті лінії вказують центр приєднання ковалентного зв’язку до прилеглих груп, структур або атомів. В одному варіанті здійснення винаходу сполука знаходиться у виділеній або очищеній фор 96295 40 мі. Як правило, термін "виділений та очищений" означає, що сполука в істотному ступені вільна від біологічних матеріалів (наприклад, крові, тканини, клітин, т.п.). В одній частині варіанті здійснення винаходу, термін означає, що сполука або кон’югат, що відповідають винаходу, щонайменше приблизно на 50 мас. % вільні від біологічних матеріалів; в іншому окремому варіанті здійснення термін означає, що сполука або кон’югат, що відповідають винаходу, щонайменше приблизно на 75 мас. % вільні від біологічних матеріалів; в іншому окремому варіанті здійснення термін означає, що сполука або кон’югат, що відповідають винаходу, щонайменше приблизно на 90 мас. % вільні від біологічних матеріалів; в іншому окремому варіанті здійснення термін означає, що сполука або кон’югат, що відповідають винаходу, щонайменше приблизно на 98 мас. % вільні від біологічних матеріалів, та в іншому окремому варіанті здійснення термін означає, що сполука або кон’югат, що відповідають винаходу, щонайменше приблизно на 99 мас. % вільні від біологічних матеріалів. В іншому окремому варіанті здійснення винахід передбачає сполуку або кон’югат, що відповідають винаходу, які отримані синтетичним шляхом (наприклад, ex vivo). Накопичення в клітині В одному варіанті здійснення винахід передбачає сполуки, здатні накопичуватися в людських PBMC (мононуклеарних клітинах периферичної крові). PBMC відносяться до клітин крові, що мають округлі лімфоцити та моноцити. Фізіологічна роль PBMC полягає в тому, що вони являють собою важливі компоненти механізму, що діє проти інфекції. PBMC можна виділити з гепаринізованої цільної крові нормальних здорових донорів або лейкоцитних плівок за допомогою стандартного центрифугування в градієнті щільності та зібрати з границі поділу, промити (наприклад забуференим фосфатом сольовим розчином) та зберігати в середовищі, що заморожують. PBMC можна культивувати в багатолункових планшетах. У різні періоди культивування або можна видалити супернатант для оцінки, або можна зібрати та аналізувати клітини (див. статтю Smith R. et al (2003) Blood 102(7): 2532-2540). Сполуки, що відповідають даному варіанту здійснення, можуть далі включати фосфонат або фосфонатну пролікарську форму. Більш типово, коли фосфонат або фосфонатна пролікарська форма мо3 же мати структуру A , як описано у даному контексті. Стереоізомери Сполуки, що відповідають винаходу, можуть мати хіральні центри, наприклад, хіральні атоми вуглецю або фосфору. Сполуки, що відповідають винаходу, таким чином, включають суміші всіх стереоізомерів, у тому числі енантіомерів, діастереомерів та атропоізомерів. Крім того, сполуки, що відповідають винаходу, включають збагачені або розділені оптичні ізомери в будь-якому із всіх асиметричних хіральних атомів. Інакше кажучи, хіральні центри, очевидні з опису, представлені як хіральні ізомери або рацемічні суміші. Всі, як рацемічні, так і діастереомерні суміші, а також 41 окремі оптичні ізомери, виділені або синтезовані, в істотному ступені вільні від своїх енантіомерних або діастереомерних партнерів, входять в обсяг винаходу. Рацемічні суміші розділяють на їх окремі в істотному ступені оптично чисті ізомери за допомогою добре відомих способів, таких як, наприклад, розділення діастереомерних солей, утворених з оптично активними додатковими сполуками, наприклад, кислотами або основами, з наступним перетворенням назад в оптично активні субстанції. У більшості випадків потрібний оптичний ізомер синтезують за допомогою стереоспецифічних реакцій, починаючи з підходящого стереоізомера потрібного вихідного матеріалу. Сполуки, що відповідають винаходу, у ряді випадків можуть також існувати як таутомерні ізомери. Хоча може бути описана тільки одна делокалізована резонансна структура, передбачають, що всі дані форми входять в обсяг винаходу. Наприклад, можуть існувати ен-амінні таутомери для пуринової, піримідинової, імідазолової, гуанідинової, амідинової та тетразолової систем, та всі їх можливі таутомерні форми входять в обсяг винаходу. Солі та гідрати Приклади фізіологічно прийнятних солей сполук, що відповідають винаходу, включають солі, отримані з відповідної основи, такі як [солі] лужного металу (наприклад, натрію), [солі] лужноземельного [металу] (наприклад, магнію), амо+ нію та NX4 (де X означає C1-C4алкіл). Фізіологічно прийнятні солі атому водню або аміногрупи включають солі органічних карбонових кислот, таких як оцтова, бензойна, молочна, фумарова, винна, малеїнова, малонова, яблучна, ізетіонова, лактобіонова та бурштинова кислоти; органічних сульфонових кислот, таких як метансульфонова, етансульфонова, бензолсульфонова та птолуолсульфонова кислоти, та неорганічних кислот, таких як соляна, сірчана, фосфорна та сульфамінова кислоти. Фізіологічно прийнятні солі сполуки гідроксигрупи включають аніон зазначеної сполуки в сполученні з підходящим катіоном, + + таким як Na та NX4 (де X незалежно вибирають з H або C1-C4алкільної групи). Для терапевтичного застосування солі активних інгредієнтів сполук, що відповідають винаходу, будуть, як правило, фізіологічно прийнятними, тобто вони будуть являти собою солі, отримані з фізіологічно прийнятної кислоти або основи. Однак солі кислоти або основи, які не є фізіологічно прийнятними, також можуть знайти застосування, наприклад, при одержанні або очищенні фізіологічно прийнятного сполуки. Всі солі, отримані вони чи ні, з фізіологічно прийнятної кислоти або основи, входять в обсяг даного винаходу. Солі металів, як правило, отримують реакцією гідроксиду металу зі сполукою, що відповідає даному винаходу. Прикладами солей металів, які + отримують даним шляхом, є солі, що містять Li , + + Na та K . Менш розчинну сіль металу можна осадити з розчину більш розчинної солі за допомогою додавання сполуки підходящого металу. Крім того, солі можуть бути утворені за допомогою введення кислоти з ряду органічних та неор 96295 42 ганічних кислот, наприклад, HCl, HBr, H2SO4, H3PO4, або органічних сульфонових кислот, в основні центри, як правило, аміни, або в кислотні групи. Нарешті, слід мати на увазі, що композиції, представлені в даному контексті, включають сполуки, що відповідають винаходу, у їх неіонізованій, а також цвіттеріонній формі, та комбінації зі стехіометричними кількостями води як у гідратах. Крім того, в обсяг даного винаходу включають солі вихідних сполук із однієї або більше амінокислот. Підходять будь-які із природних або неприродних амінокислот, особливо природні амінокислоти, що виявляють у вигляді білкових компонентів, хоча амінокислота, як правило, являє собою несучий бічний ланцюг з основною або кислотною групою, наприклад, лізин, аргінін або глутамінову кислоту, або нейтральною групою, наприкоал, гліцин, серін, треонін, аланін, ізолейцин або лейцин. Способи інгібування ВГС Інший аспект винаходу відноситься до способів інгібування активності ВГС, що включає стадію обробки зразка, що можливо містить ВГС, сполуки або композицію, що відповідають винаходу. Сполуки, що відповідають винаходу, можуть діяти як інгібітори ВГС, як проміжні продукти для даних інгібіторів або мати інші застосування, як описано нижче. Інгібітори будуть, як правило, зв'язуватися з положеннями на поверхні або в порожнині печінки. Сполуки, що зв'язуються в печінці, можуть зв'язуватися з різним ступенем оборотності. Ті сполуки, які зв'язуються в істотному ступені необоротно, є найкращими кандидатами для застосування в даному способі, що відповідає винаходу. Після введення мітки в істотному ступені необоротно єднальні сполуки використовують як зонди для детекції ВГС. Відповідно винахід відноситься до способів детекції NS3 у зразку, що можливо містить ВГС, що включає стадії: обробки зразку, що можливо містить ВГС, композицію, що включає сполуку, що відповідає винаходу, пов'язану з міткою, та спостереження ефекту зразку на активність мітки. Підходящі мітки добре відомі в галузі діагностики та включають стабільні вільні радикали, флуорофори, радіоізотопи, ферменти, хемілюмінесцентні групи та хромогени. У сполуки, представлені в даному контексті, вводять мітку прийнятим чином, використовуючи функціональні групи, такі як гідроксил або аміно група. В одному варіанті здійснення винахід передбачає сполуку формули (I), що включає або яка приєднана або пов'язана з однієї або більше обумовлених міток. У контексті винаходу зразки, що можливо містять ВГС, включають природні або штучні матеріали, такі як живі організми, тканеві або клітинні культури; біологічні зразки, такі як зразки біологічних матеріалів (кров, сироватку, сечу, спинномозкову рідину, слізну рідину, мокротиння, слину, зразки тканин та т.п.), лабораторні зразки, зразки продуктів харчування, води або повітря, зразки біопродуктів, такі як клітинні екстракти, особливо рекомбінантні клітини, що синтезують потрібний глікопротеїн та т.п. Як правило, зразок буде мож 43 ливо містити ВГС. Зразки можуть міститися в будь-якому середовищі, включаючи воду та суміші органічних розчинників/води. Зразки включають живі організми, такі як люди, та штучні матеріали, такі як клітинні культури. Стадія обробки, що відповідає винаходу, включає додавання сполуки, що відповідає винаходу, до зразка або вона включає додавання попередника композиції до зразка. Стадія додавання включає будь-який спосіб застосування, як описано вище. При необхідності активність ВГС після застосування сполуки можна реєструвати будь-яким способом, включаючи прямі та непрямі способи визначення активності ВГС. Передбачають всі кількісні, якісні та напівкількісні способи визначення активності ВГС. Як правило, застосовують один з вищеописаних способів скринінгу, однак застосовний також будь-який інший спосіб, такий як спостереження за фізіологічними показниками живого організму. Багато організмів містять ВГС. Сполуки, що відповідають даному винаходу, використовують для лікування або профілактики станів, пов’язаних з активацією ВГС у тварини або людини. Однак при скринінгу сполук, здатних інгібувати ВГС, слід мати на увазі, що результати ферментних аналізів не завжди можуть корелювати з аналізами на клітинних культурах. У такий спосіб аналіз на основі клітин повинен, як правило, бути основним інструментом скринінгу. Способи скринінгу інгібіторів ВГС Сполуки, що відповідають винаходу, піддають скринінгу на інгібуючу активність у відношенні ВГС за допомогою кожного із прийнятих способів оцінки активності ферментів. У контексті винаходу, як правило, сполуки спочатку піддають скринінгу на інгібування ВГС in vitro, та сполуки, що демонструють інгібуючу активність, потім піддають скринінгу на активність in vivo. Сполуки, що мають in vitro Ki (константи інгібування) менше -6 ніж приблизно 5 X 10 M, як правило, менше ніж -7 приблизно 1 X 10 M та переважно менше ніж -8 приблизно 5 X 10 M є кращими для використання in vivo. Використовувані способи скринінгу in vitro описані детально. Фармацевтичні препарати Сполуки, що відповідають даному винаходу, отримують із прийнятими носіями та наповнювачами, які будуть вибирати відповідно до звичайної практики. Таблетки будуть включати наповнювачі, ковзкі компоненти, інертні наповнювачі, зв’язуючі компоненти та т.п. Водні препарати готовлять у стерильній формі та, якщо вони призначені для доставки шляхом, відмінним від перорального введення, вони будуть ізотонічними. Всі препарати будуть необов'язково включати наповнювачі, такі як наведені в Handbook of Pharmaceutical Excipients (Довідник по фармацевтичних наповнювачах) (1986). Наповнювачі включають аскорбінову кислоту та інші антіоксиданти, хелатуючі агенти, такі як ЕДТА (етилендіамінтетраоцтова кислота), вуглеводи, такі як декстрин, гідроксиалкілцелюлоза, 96295 44 гідроксиалкілметилцелюлоза, стеаринова кислота та т.п. pН препаратів знаходиться в інтервалі від приблизно 3 до приблизно 11, але звичайно становить приблизно 7-10. Хоча можливе введення активних інгредієнтів у вигляді монокомпоненту, може бути кращим представляти їх у вигляді фармацевтичних препаратів. Препарати як для ветеринарного, так та для медичного застосування, що відповідають винаходу, включають щонайменше один активний інгредієнт, як визначено вище, разом з одним або більшою кількістю прийнятних носіїв та необов'язково з іншими терапевтичними інгредієнтами. Носій(ії) повинен бути "прийнятним" у розумінні сумісності з іншими інгредієнтами препарату та фізіологічно нешкідливим для свого реципієнта. Препарати включають підходящі для вищеописаних шляхів введення. Препарати можуть бути зручно представлені в уніфікованій лікарській формі та можуть бути отримані будь-яким зі способів, добре відомих в галузі фармації. Способи та препарати в основному розкриті в довіднику Remington's pharmaceutical Sciences (Довідник по фармацевтичних науках Ремінгтона) (Mack Publishing Co., Easton, PA). Дані способи включають стадію контактування активного інгредієнта з носієм, який включає один або більше допоміжних інгредієнтів. Як правило, препарати отримують шляхом однорідного та тісного контактування активного інгредієнта з рідкими носіями або тонко здрібненими твердими носіями або обома з наступним (при необхідності) формуванням продукту. Препарати, що відповідають даному винаходу, що підходять для перорального введення, можуть бути у вигляді окремих одиниць, таких як капсули, крохмальні капсули або таблетки, кожна з яких включає попередньо задану кількість активного інгредієнта, у вигляді порошку або гранул, у вигляді розчину або суспензії у водній або неводній рідини або у вигляді рідкої емульсії типу масло-у-воді або рідкій емульсії типу вода-у-маслі. Активний інгредієнт можна також вводити у вигляді болюсу, електуарію або пасти. Таблетку отримують шляхом пресування або формування, необов'язково з одним або більшою кількістю допоміжних інгредієнтів. Пресовані таблетки можна виготовити пресуванням у підходящому пристрої активного інгредієнта в сипучій формі, такій як порошок або гранули, необов'язково змішаній зі сполучним компонентом, змащуючою речовиною, інертним розріджувачем, консервантом, поверхнево-активним агентом або розпушуючим агентом. Формовані таблетки можна виготовити формуванням у підходящому пристрої суміші порошкового активного інгредієнта, зволоженого інертним рідким розріджувачем. Таблетки можуть бути необов'язково покритими або можуть мати насічки, та вони необов'язково виготовлені таким чином, щоб забезпечувати уповільнене або контрольоване вивільнення з них активного інгредієнта. Для введення в око або інші зовнішні тканини, наприклад, рот та шкіру, переважно, коли 45 препарати наносять у вигляді зовнішньої мазі або крему, що включають активний інгредієнт(и) у кількості, наприклад, 0,075-20% мас./мас. (включаючи активний інгредієнт(и) в інтервалі від 0,1% до 20% зі зростанням 0,1% мас./мас., наприклад, 0,6% мас./мас., 0,7% мас./мас. та т.п.), переважно 0,2-15% мас./мас. та найбільш переважно 0,510% мас./мас. При одержанні у вигляді мазі активні інгредієнти можна використовувати або з вазеліновою, або з мазевою основою, що змішується з водою. Альтернативно активні інгредієнти можна одержати в кремі із кремовою основою типу масло-у-воді. При необхідності водна фаза кремової основи може включати, наприклад, щонайменше 30% мас./мас. багатоатомного спирту, тобто спирту, що має дві або більше гідроксильних груп, таких як пропіленгліколь, бутан 1,3-діол, манітол, сорбітол, гліцерин та поліетиленгліколь (включаючи ПЕГ 400) та їх суміші. При необхідності місцеві препарати можуть включати сполуку, що підвищує всмоктування або проникнення активного інгредієнта через шкіру або інші ушкоджені області. Приклади даних підсилювачів проникнення через шкіру включають диметилсульфоксид та споріднені аналоги. Масляна фаза емульсій, що відповідають даному винаходу, може бути складена з відомих інгредієнтів відомим чином. Хоча фаза може включати тільки емульгатор (який інакше називають емульгуючою речовиною), бажано, щоб вона включала суміш щонайменше одного емульгатора з жиром або маслом або обома, жиром та маслом. Переважно, коли гідрофільний емульгатор включають разом з ліпофільним емульгатором, який діє як стабілізатор. Переважно також включення як масла, так і жиру. Спільно емульгатор(и) зі стабілізатором або без нього утворюють так званий емульгуючий віск, та віск разом з маслом та жиром утворюють так звану емульгуючу мазеву основу, що утворює масляну дисперсну фазу кремових препаратів. Емульгатори та стабілізатори емульсії, що підходять для використання в препараті, що відповідає винаходу, включають Tween 60, Span 80, цетостеариловий спирт, бензиловий спирт, міристиловий спирт, гліцерилмоностеарат та лаурилсульфат натрію. Вибір підходящих масел або жирів для препарату оснований на досягненні необхідних косметичних властивостей. Крем переважно повинен бути нежирним, незабарвлюючим та змиваним продуктом з підходящою консистенцією, щоб уникнути витікання з тюбиків або інших контейнерів. Можна використати одно- або двоосновні складні алкілефіри з нерозгалуженим або розгалуженим ланцюгом, такі як ди-ізоадипат, ізоцетилстеарат, діефір пропіленгліколю та жирних кислот кокосу, ізопропілміристат, децилолеат, ізопропілпальмітат, бутилстеарат, 2етилгексилпальмітат або суміш складних ефірів з розгалуженим ланцюгом, відому як Crodamol CAP, останні три є кращими складними ефірами. Вони можуть бути використані як монокомпонент або в комбінації залежно від необхідних власти 96295 46 востей. Альтернативно використовують ліпіди з високою температурою плавлення, такі як безбарвний м'який парафін та/або вазелінове масло або інші мінеральні масла. Фармацевтичні препарати, що відповідають даному винаходу, включають одну або більше сполук, що відповідають винаходу, разом з одним або більшою кількістю фармацевтично прийнятних носіїв або наповнювачів та необов'язково іншими терапевтичними агентами. Фармацевтичні препарати, що включають активний інгредієнт, можуть бути у формі, що підходить для наміченого способу введення. При використанні для перорального введення, можна одержати, наприклад, таблетки, пастилки, коржі, водні або масляні суспензії, порошки або гранули, що диспергуються, тверді або м'які капсули, сиропи або еліксири. Композиції, призначені для перорального застосування, можна одержати відповідно до будьякому способу, відомого в галузі виготовлення фармацевтичних композицій, та дані композиції можуть включати один або більше агентів, у тому числі підсолоджувачі, смакові добавки, барвники та консерванти, щоб одержати приємний на смак препарат. Прийнятні таблетки, що містять активні інгредієнти в суміші з нетоксичними фармацевтично прийнятними наповнювачами, які підходять для виготовлення таблеток. Дані наповнювачі можуть являти собою, наприклад, інертні розріджувачі, такі як карбонат кальцію або натрію, лактоза, лактози моногідрат, натрій кроскармелоза, повідон, фосфат кальцію або натрію; гранулюючі або розпушуючі агенти, такі як кукурудзяний крохмаль або альгінова кислота, зв’язуючі агенти, такі як целюлоза, мікрокристалічна целюлоза, крохмаль, желатин або акація, та змащуючі агенти, такі як стеарат магнію, стеаринова кислота або тальк. Таблетки можуть бути непокритими або можуть бути покритими за допомогою відомих способів, включаючи мікроінкапсуляцію, з метою уповільнення розпаду та всмоктування в шлунково-кишковий тракт і, таким чином, одержання уповільненої дії протягом більш тривалого періоду. Наприклад, можна використати матеріал для затримки в часі, такий як гліцерилмоностеарат або гліцерилдистеарат у вигляді монокомпоненту або з воском. Препарати для перорального застосування можуть бути також представлені у вигляді твердих желатинових капсул, у яких активний інгредієнт змішують з інертним твердим розріджувачем, наприклад, фосфатом кальцію або каоліном, або у вигляді м'яких желатинових капсул, у яких активний інгредієнт змішують з водою або масляним середовищем, такий як арахісове масло, вазелінове масло або маслинове масло. Водні суспензії, що відповідають винаходу, включають активні матеріали в суміші з наповнювачами, що підходять для виготовлення водних суспензій. Дані наповнювачі включають суспендуючий агент, такий як натрій карбоксиметилцелюлоза, метилцелюлоза, гідроксипропілметилцелюлоза, альгінат натрію, поливінілпіролідон, трагакантова камедь та камедь акації, та розпушуючі або змочувальні агенти, такі як природний 47 фосфатид (наприклад, лецитин), продукт конденсації алкіленоксиду з жирною кислотою (наприклад, поліоксиетиленстеарат), продукт конденсації етиленоксиду з аліфатичним спиртом з довгим ланцюгом (наприклад, гептадекаетиленоксицетанол), продукт конденсації етиленоксиду із частковим складним ефіром, отриманим з жирної кислоти та гекситоловим ангідридом (наприклад, поліоксиетиленсорбіт моноолеат). Водна суспензія може також включати один або більше консервантів, таких як етил або н-пропіл пгідроксибензоат, один або більше барвників, один або більше смакових компонентів та один або більше підсолоджувачів, таких як сахароза або сахарин. Масляні суспензії можна одержати суспендуванням активного інгредієнта в рослинному маслі, такому як арахісове масло, маслинове масло, кунжутне масло або кокосове масло, або в мінеральному маслі, такому як вазелінове масло. Пероральні суспензії можуть включати згущувач, такий як бджолиний віск, твердий парафін або цетиловий спирт. Підсолоджувачі, такі як приведені вище, та смакові компоненти можна додати, щоб одержати приємний на смак пероральний препарат. Дані композиції можна законсервувати додаванням антіоксиданту, такого як аскорбінова кислота. Порошки та гранули, що диспергуються, які відповідають винаходу, що підходять для одержання водної суспензії шляхом додавання води, дають активний інгредієнт у суміші із розпушуючим або змочувальним агентом, суспендуючим агентом та одним або більшою кількістю консервантів. Підходящі розпушуючі або змочувальні агенти та суспендуючі агенти проілюстровані приведеними вище. Можуть також бути присутнім додаткові наповнювачі, наприклад, підсолоджувачі, смакові компоненти та барвники. Фармацевтичні композиції, що відповідають винаходу, можуть бути також у формі емульсій типу масло у воді. Масляна фаза може являти собою рослинне масло, таке як маслинове масло або арахісове масло, мінеральне масло, таке як вазелінове масло, або їх суміш. Підходящі емульгатори включають природні камеді, такі як камедь акації та камедь трагаканту, природні фосфатиди, такі як соєвий лецитин, складні ефіри або часткові складні ефіри, отримані з жирних кислот, та гекситолові ангідриди, такі як сорбітмоноолеат, продукти конденсації даних часткових складних ефірів з етиленоксидом, такі як поліоксиетиленсорбітмоноолеат. Емульсія може також включати підсолоджувачі та смакові компоненти. Сиропи та еліксири можна приготувати з підсолоджувачами, такими як гліцерин, сорбіт або сахароза. Дані препарати можуть також включати засіб, що зменшує подразнення, консервант, смаковий компонент або барвник. Фармацевтичні композиції, що відповідають винаходу, можуть бути у формі стерильного ін'єкційного препарату, такого як стерильна ін'єкційна водна або масляна суспензія. Дану суспензію можна виготовити відповідно до відомого рівня техніки з використанням тих підходящих диспер 96295 48 гуючих або змочувальних агентів та суспендуючих агентів, які згадані вище. Стерильний ін'єкційний препарат може також являти собою стерильний ін'єкційний розчин або суспензію в нетоксичному прийнятному для парентерального введення розріджувачі або розчиннику, такий як розчин в 1,3-бутандіолі, або може бути отриманий як ліофілізований порошок. Із прийнятних носіїв або розчинників можна використати воду, розчин Рінгера та ізотонічний розчин хлориду натрію. Крім того, стерильні нелеткі масла можна традиційно використовувати як розчинник або суспендуюче середовище. Для даної мети можна використати будь-яке м'яке нелетке масло, включаючи синтетичні моно- або дигліцериди. Крім того, жирні кислоти, такі як олеїнова кислота, можуть бути аналогічним чином використані при одержанні ін’єкційних препаратів. Кількість активного інгредієнта, яку можна комбінувати з носієм для одержання одноразової лікарської форми, буде варіюватися залежно від хазяїна, якого лікують, та конкретного способу введення. Наприклад, препарат із пролонгованою дією, призначений для перорального введення людині, може включати приблизно 1-1000 мг активного матеріалу, змішаного з відповідною та зручною кількістю матеріалу носія, що може варіюватися від приблизно 5 до приблизно 95% від композицій у цілому (маса:маса). Можна приготувати фармацевтичну композицію, що забезпечує легко вимірювані кількості для введення. Наприклад, водний розчин, призначений для внутрішньовенної інфузії, може включати від приблизно 3 до 500 мкг активного інгредієнта/мл розчину, щоб відбувалася інфузія підходящого об’єму зі швидкістю приблизно 30 мл/годину. Препарати, що підходять для введення в око, включають очні краплі, у яких активний інгредієнт розчинений або суспендований у підходящому носії, зокрема, у водному розчиннику для активного інгредієнта. Переважно, коли активний інгредієнт знаходиться в даних препаратах у концентрації 0,5-20%, переважно 0,5-10%, зокрема, приблизно 1,5% мас./мас. Препарати, що підходять для місцевого застосування в порожнині рота, включають коржі, що містять активний інгредієнт в основі зі смаковою добавкою, звичайно сахарозою, та акацієву камедь або трагакант, пастилки, що містять активний інгредієнт в інертній основі, такій як желатин та гліцерин, або сахарозу та акацієву камедь, та полоскання для рота, що містять активний інгредієнт у підходящому рідкому носії. Препарати для ректального застосування можуть бути представлені у вигляді супозиторіїв з підходящою основою, що містить, наприклад, масло какао або саліцилат. Препарати, що підходять для внутрішньолегеневого або назального застосування мають розмір часток, наприклад, в інтервалі від 0,1 до 500 мікронів (включаючи розміри часток в інтервалі від 0,1 до 500 мікронів при збільшенні в мікронах, такому як 0,5, 1, 30 мікрон, 35 мікрон та т.п.), які вводять швидкою інгаляцією через носовий прохід або інгаляцією через рот, щоб досягти 49 альвеолярних мішечків. Підходящі препарати включають водні або масляні розчини активного інгредієнта. Препарати, що підходять для введення аерозолем або сухим порошком, можна одержати згідно прийнятим способом та можна доставити з іншими терапевтичними агентами, такими як сполуки, раніше використовувані для лікування або профілактики станів, пов’язаних з активністю ВГС. Препарати, що підходять для вагінального застосування, можуть бути у вигляді песарієв, тампонів, кремів, гелів, паст, пін або препаратів спреїв, що містять крім активного інгредієнта такі носії, які відомі як підходящі в галузі техніки. Препарати, що підходять для парентерального застосування, включають водні та неводні стерильні ін'єкційні розчини, які можуть включати антиоксиданти, буфери, бактеріостатики та розчинені речовини, які роблять препарат ізотонічним із кров'ю передбачуваного реципієнта, та водні та неводні стерильні суспензії, які можуть включати суспендуючі агенти та згущувачі. Препарати представлені в однодозних або багатодозних контейнерах, наприклад, запаяних ампулах та флаконах, та їх можна зберігати в отриманому сублімаційним сушінням (ліофілізованому) стані, що вимагає тільки додавання стерильного рідкого носія, наприклад, води для ін'єкцій, безпосередньо перед використанням. Ін'єкційні розчини для неповільного застосування отримують зі стерильних порошків, гранул та таблеток раніше описаного типу. Кращими уніфікованими лікарськими препаратами є ті, які містять добову дозу або уніфіковану добову субдозу, як представлено вище в даному контексті, або її відповідну фракцію активного інгредієнта. Слід мати на увазі, що крім інгредієнтів, особливо відмічених вище, препарати, що відповідають даному винаходу, можуть включати інші агенти, прийняті в галузі техніки, що мають відношення до типу обговорюваного препарату, наприклад, ті, які підходять для перорального введення, можуть включати смакові добавки. Крім того, винахід передбачає ветеринарні композиції, що включають, щонайменше, один активний інгредієнт, як визначено вище, разом з ветеринарним носієм для нього. Ветеринарні носії являють собою матеріали, використовувані для мети введення композиції, та можуть бути твердими, рідкими або газоподібними матеріалами, які в інших відношеннях інертні або прийнятні в галузі ветеринарії та сумісні з активним інгредієнтом. Дані ветеринарні композиції можна вводити перорально, парентерально або іншим необхідним шляхом. Сполуки, що відповідають винаходу, можна також одержати, щоб забезпечити контрольоване вивільнення активного інгредієнта для одержання можливості менш частого дозування або для поліпшення фармакокінетичного профілю або профілю токсичності активного інгредієнта. Відповідно, винахід також передбачає композиції, що включають одну або більше сполук, що відповідають винаходу, виготовлені для уповільненого або контрольованого вивільнення. 96295 50 Ефективна доза активного інгредієнта залежить щонайменше від природи стану, що лікують, токсичності, від того, чи використовують сполуку профілактично (більш низькі дози), від способу доставки та фармацевтичного препарату та буде визначена лікарем з використанням прийнятих досліджень підвищення дози. Можна чекати, що вона буде становити від приблизно 0,0001 до приблизно 100 мг/кг маси тіла/день. Як правило, від приблизно 0,01 до приблизно 10 мг/кг маси тіла/день. Більш типово від приблизно 0,01 до приблизно 5 мг/кг маси тіла/день. Більш типово від приблизно 0,05 до приблизно 0,5 мг/кг маси тіла/день. Наприклад, добова потенційна доза для дорослої людини маси тіла приблизно 70 кг буде лежати в інтервалі від 1 мг до 1000 мг, переважно від 5 мг до 500 мг та може мати форму одноразової або багаторазової доз. Шляхи введення Одну або більше сполук, що відповідають винаходу (у даному контексті позначають як активні інгредієнти), вводять будь-яким шляхом, що відповідає стану, що лікують. Підходящі шляхи включають пероральний, ректальний, назальний, місцевий (включаючи защічний та під'язичний), вагінальний та парентеральний (включаючи підшкірний, внутрім'язовий, внутрішньовенний, внутрішкірний, інтратекальний та епідуральний) тощо. Слід мати на увазі, що кращий шлях може змінюватися в залежності,наприклад, від стану реципієнта. Перевага сполук, що відповідають даному винаходу, полягає в тому, що вони біодоступні при пероральному введенні та їх можна дозувати перорально. Комбінована терапія Активні інгредієнти, що відповідають винаходу, можна також використовувати в комбінації з іншими активними інгредієнтами. Дані комбінації вибирають на основі стану, що лікують, з урахуванням перехресної реактивності інгредієнтів та фармакологічних властивостей комбінації. Можливо також об'єднати будь-яку сполуку, що відповідає винаходу, з одним або більшою кількістю інших активних інгредієнтів в одиничній лікарській формі для одночасного або послідовного введення пацієнту. Комбіновану терапію можна застосовувати як схему одночасного або послідовного введення. При послідовному введенні комбінацію можна застосовувати у вигляді двох або більше введень. Комбінована терапія може давати "синергію" та "синергічний ефект", тобто ефект, що досягається, коли активні інгредієнти використовують разом, більше ніж сума ефектів, які є результатом окремого використання сполук. Синергічний ефект може досягатися, коли активні інгредієнти: (1) отримують разом та вводять одночасно в комбінованому препараті, (2) доставляють по черзі або паралельно у вигляді окремих препаратів, або (3) за допомогою якої-небудь іншої схеми. При доставці в терапії, що чергується, синергічний ефект може досягатися, коли сполуки вводять або доставляють послідовно, наприклад, в окремих таблетках, пігулках або капсулах або за допомогою різних ін'єкцій в окремих шприцах. 51 Як правило, під час терапії, що чергується, ефективну дозу кожного активного інгредієнта вводять послідовно, тобто серійно, тоді як при комбінованій терапії ефективні дози двох або більше активних інгредієнтів вводять спільно. Метаболіти сполук, що відповідають винаходу Крім того, в обсяг даного винаходу входять продукти метаболізму in vivo сполук, описаних у даному контексті. Дані продукти можуть бути результатом, наприклад, окислювання, відновлення, гідролізу, амідування, естерифікації та т.п. введеної сполуки, в основному внаслідок ферментативних процесів. Відповідно винахід включає сполуки, отримані способом, що включає контактування сполуки, що відповідає даному винаходу, зі ссавцем у період часу, достатній для одержання продукту його метаболізму. Дані продукти, як правило, ідентифікують шляхом одержання спо14 луки, що несе радіоактивну мітку (наприклад, C 3 або H ), що відповідає винаходу, її парентерального введення в обумовленій дозі (наприклад, більше ніж приблизно 0,5 мг/кг) тварині, такій як щур, миша, морська свинка, мавпа або людина, надання достатнього часу для протікання метаболізму [метаболічного перетворення] (як правило, приблизно від 30 секунд до 30 часів) та виділення продуктів її перетворення із сечі, крові або інших біологічних зразків. Дані продукти легко виділити, оскільки вони позначені (інші виділяють з використанням антитіл, здатних зв'язувати епітопи, що зберігаються в метаболіті). Структури метаболітів визначають прийнятим способом, наприклад, за допомогою МС або ЯМР-аналізу. Як правило, аналіз метаболітів проводять тим же шляхом, що і прийняті дослідження метаболізму лікарських препаратів, добре відомі компетентним фахівцям в області техніки. Продукти перетворення, за умови, що їх іншим способом не виявляють in vivo, використовують у діагностичних аналізах терапевтичного дозування сполук, що відповідають винаходу, навіть якщо вони самі по собі не мають активності інгібування ВГС. Відомі способи визначення стабільності сполук в штучних шлунково-кишкових виділеннях. Сполуки визначають у даному контексті як стабільні в шлунково-кишковому тракті, коли менше ніж приблизно 50 моль% захищених груп втрачають захист у штучному кишковому або шлунковому соку при інкубуванні протягом 1 години при 37°C. Тільки те, що сполуки стабільні в шлунковокишковому тракті, не означає, що вони не можуть гідролізуватися in vivo. Фосфонатні пролікарські форми, що відповідають винаходу, як правило, будуть стабільні в травній системі, але вони в істотному ступені гідролізуються до вихідного лікарського препарату в просвіті травного тракту, печінки або іншому метаболічному органі або в клітинах у цілому. Ілюстративні способи одержання сполук, що відповідають винаходу. Винахід також відноситься до способів одержання композицій, що відповідають винаходу. Композиції [прим. перекл. - сполуки] отримують кожним із застосовних способів органічного син 96295 52 тезу. Багато з даних способів добре відомі в галузі техніки. Однак багато з відомих способів розроблені в роботі Compendium of Organic Synthetic Methods (Збірник методів органічного синтезу) (John Wiley & Sons, New York), т. 1, Ian T. Harrison and Shuyen Harrison, 1971; т. 2, Ian T. Harrison and Shuyen Harrison, 1974; т. 3, Louis S. Hegedus and Leroy Wade, 1977; т. 4, Leroy G. Wade, Jr., 1980; т. 5, Leroy G. Wade, Jr., 1984 та т. 6, Michael B. Smith; а також у монографії March, J., Advanced Organic Chemistry, Third Edition (Сучасна органічна хімія, 3 вид.) (John Wiley & Sons, New York, 1985), Comprehensive Organic Synthesis. Selectivity, Strategy & Efficiency in Modern Organic Chemistry (Повний органічний синтез. Вибірковість, стратегія та ефективність у сучасній органічний хімії) в 9 томах, гол. ред. Barry M. Trost, (Pergamon Press, New York, вид. 1993). Інші способи, що підходять для одержання сполук, що відповідають винаходу, описані в публікації міжнародної патентної заявки WO 2006/020276. Ряд ілюстративних способів одержання композицій, що відповідають винаходу, представлений нижче. Дані способи призначені для ілюстрації природи даних препаратів та не призначені для обмеження обсягу застосовних способів. Як правило, умови реакції, такі як температура, час реакції, розчинники, процедури обробки та т.п., будуть тими, які загальновідомі в рівні техніки для певної проведеної реакції. Наведений посилальний матеріал разом з матеріалом, що цитується у даному контексті, включає детальні описи даних умов. Як правило, температури будуть становити -100°C - 200°C, розчинники будуть непротонними або протонними, час реакції буде становити від 10 секунд до 10 днів. Обробка, як правило, включає в себе гасіння якихнебудь реагентів, що не прореагували, з наступним розподілом між системою водного/органічного шару (екстракцією) та виділенням шару, що включає продукт. Реакції окислювання та відновлення, як правило, проводять при температурах, близьких до кімнатній температурі (приблизно 20°C), хоча для відновлення гідридів металів часто температуру знижують до 0°C - -100°C, розчинники, як правило, є непротонними для відновлень та можуть бути або протонними, або непротонними для окислювань. Час реакцій підбирають таким чином, щоб досягти необхідних перетворень. Реакції конденсації, як правило, проводять при температурах, близьких до кімнатній температурі, хоча для нерівноважних кінетично контрольованих конденсацій поширені також знижені температури (від 0°C до -100°C). Розчинники можуть бути або протонними (звичайно в рівноважних реакціях) або непротонними (звичайно в кінетично контрольованих реакціях). Стандартні способи синтезу, такі як азеотропне видалення побічних продуктів реакції та використання безводних умов реакції (наприклад, середовища інертного газу) загальноприйняті в галузі техніки та будуть використовуватися, коли вони застосовні. 53 Терміни "оброблений", "процес обробки", "обробка", та т.п. при використанні у зв'язку з операцією хімічного синтезу означають контактування, змішування, проведення реакції, створення можливості реакції, приведення в контакт та інші терміни, звичайні для галузі техніки, призначені для того, щоб показати, що одну або більше хімічних структур обробляють таким чином, щоб перетворити її в одну або більше інших хімічних структур. Це означає, що вираз "обробка сполуки один сполукою два" є синонімом виразу "створення можливості для сполуки один вступити у реакцію зі сполукою два", "контактування сполуки один зі сполукою два", "проведення реакції сполуки один зі сполукою два" та інші вирази, прийняті в області органічного синтезу для коректного позначення того, що сполуку один "обробляють", "вступає в реакцію", "дають можливість реагувати" та т.п. зі сполукою два. Наприклад, термін обробка вказує на раціональний та ефективний спосіб, у якому дають можливість вступати в реакцію органічним хімічним сполукам. Поки не зазначено інше, передбачають нормальні концентрації (0,01 M - 10 M, як правило, 0,1 M - 1 M), температури (-100°C - 250°C, як правило, від 78°C до 150°C, більш типово від -78°C до 100°C, ще більш типово від 0°C до 100°C), реакційні ємності (як правило, скляні, пластикові, металеві), розчинники, тиски, атмосфери (як правило, повітря для реакцій, нечутливих до кисню та води, або азот або аргон для чутливих до кисню або воді) та т.д. Відомості про подібні реакції, відомі в галузі органічного синтезу, використовують при виборі умов та встаткування для "обробки" у заданому способі. Зокрема, звичайний фахівець в галузі органічного синтезу вибирає умови та встаткування, що, як обґрунтовано очікують, дозволяє успішно проводити хімічні реакції, що відповідають описаним процесам, на основі знань в галузі техніки. Модифікації кожної з ілюстративних схем та в прикладах (далі "ілюстративні схеми") приводять до одержання різних аналогів специфічних ілюстративних матеріалів. Вищеприведені посилання, що описують підходящі способи органічного синтезу, застосовні до даних модифікацій. У кожній з ілюстративних схем може бути корисним відокремити продукти реакції один від іншого та/або від вихідних матеріалів. Необхідні продукти кожної стадії або серії стадій відокремлюють та/або очищують (далі відокремлюють) до необхідного ступеня гомогенності способами, прийнятими в галузі техніки. Як правило, дані розділення включають багатофазну екстракцію, кристалізацію з розчиннику або суміші розчинників, відгін, сублімацію або хроматографію. Хроматографія може включати будь-яке число способів у тому числі, наприклад, способи та встаткування для обернено-фазової та нормально-фазової, ексклюзійної по розміру, іонообмінної, рідинної хроматографії високого, середнього та низького тиску, лабораторної аналітичної, зі штучним рухливим шаром (SMB) та препаративної тонко- або товстошарової хроматографії, а також способи лабораторної тонкошарової та експрес-хроматографії. 96295 54 Інший клас способів розділення включає обробку суміші реагентом, вибраним для того, щоб зв'язувати або іншим способом робити відокремлюваним потрібний продукт, вихідний матеріал, що не прореагував, побічний продукт реакції тощо. Дані реагенти включають адсорбенти або абсорбенти, такі як активоване вугілля, молекулярні сита, іонообмінні середовища та т.п. Альтернативно реагенти можуть являти собою кислоти у випадку основного матеріалу, основи у випадку кислотного матеріалу, що зв'язують реагенти, такі як антитіла, що зв'язують білки, виборчі хелатори, такі як краун-ефіри, рідкі/рідкі іонні екстракційні реагенти (LIX) або подібні їм. Вибір відповідних способів розділення залежить від природи включених матеріалів. Наприклад, температура кипіння та молекулярна маса при відгоні та сублімації, наявність або відсутність функціональних груп у хроматографії, стабільність матеріалів у кислому та лужному середовищі в багатофазній екстракції та т.п. Компетентний фахівець в галузі техніки буде застосовувати способи, які з найбільшою ймовірністю дозволяють досягти потрібного розділення. Окремий стереоізомер, наприклад, енантіомер, в істотному ступені вільний від свого стереоізомера, можна одержати шляхом розділення рацемічної суміші з використанням такого способу, як формування діастереомерів за допомогою оптично активних поділяючих агентів (див. статтю Stereochemistry of Carbon Compounds (Стереохімія вуглецевих сполук), (1962) E. L. Eliel, McGraw Hill; Lochmuller, C. H., (1975) J. Chromatogr., 113:(3) 283-302). Рацемічні суміші хіральних сполук, що відповідають винаходу, можна розділити та виділити підходящим способом, включаючи: (1) утворення іонних діастереомерних солей з хіральними сполуками та поділ фракційною кристалізацією або іншими способами, (2) утворення діастереомерних сполук із хіральними дериватизуючими реагентами, поділ діастереомерів та перетворення в чисті стереоізомери та (3) поділ в істотному ступені чистих або збагачених стереоізомерів безпосередньо в хіральних умовах. У межах способу (1) діастереомерні солі можна одержати шляхом реакції енантіомерно чистих хіральних основ, таких як бруцин, хінін, ефедрин, стрихнін, -метил--фенілетиламін (амфетамін) та т.п., з асиметричними сполуками, що несуть кислотну функціональність, таку як карбонова кислота та сульфонова кислота. Можна викликати розділення діастереомерних солей фракційною кристалізацією або іонною хроматографією. Для розділення оптичних ізомерів аміносполук додавання хіральних карбонових або сульфонових кислот, таких як камфорсульфонова кислота, винна кислота, мигдальна кислота або молочна кислота, може привести в результаті до утворення діастереомерних солей. Альтернативно згідно способу (2) субстрат, що розділюють, реагує з одним енантіомером хіральної сполуки з утворенням діастереомерної пари (див. монографію Eliel, E. and Wilen, S. (1994) Stereochemistry of Organic Compounnds (Стереохімія органічних сполук). John Wiley & 55 Sons, Inc., стор. 322). Діастереомерні сполуки можна одержати шляхом реакції асиметричних сполук із енантіомерно чистими хіральними дериватизуючими реагентами, такими як ментильні похідні, з наступним розділенням діастереомерів та гідролізом з одержанням вільного енантіомерно чистого ксантену. Спосіб визначення оптичної чистоти включає одержання хіральних складних ефірів, таких як ментиловий складний ефір, наприклад, (-)ментилхлорформіат, у присутності основи або складного ефіру Мошера, -метокси-(трифторметил)-фенілацетату (див. статтю Jacob III. (1982) J. Org. Chem. 47:4165), рацемічної суміші та аналіз ЯМР-спектру на присутність двох атропізомерних діастереомерів. Стабільні діастереомери атропізомерних сполук можна розділити та виділити нормально- та оберненофазовою хроматографією, слідуючи способам розділення атропізомерних нафтил-ізохінолінів 96295 56 (дів. Hoye T., WO 96/15111). Способом (3) рацемічну суміш двох енантіомерів можна розділити хроматографією з використанням хіральної стаціонарної фази (див. монографію Chiral Liquid Chromatography (Хіральна рідинна хроматографія), (1989), під ред. W. J. Lough, Chapman and Hall, New York; статтю Okamoto, (1990) J. of Chromatogr. 513:375-378). Збагачені або очищені енантіомери можна розділити способами, використовуваними для розділення інших хіральних молекул з асиметричними атомами вуглецю, такими як оптичне обертання та хіральний дихроїзм. Окремі варіанти здійснення публікації міжнародної патентної заявки № WO 2006/020276 відносяться до ряду конкретних сполук. В одному окремому варіанті здійснення винаходу сполуки, що відповідають винаходу, виключають наступні сполуки: 57 96295 58 В іншому варіанті здійснення винаходу сполуки, що відповідають винаходу, виключають наступну сполуку: В іншому варіанті здійснення винаходу сполуки, що відповідають винаходу, виключають сполуку формули (X): 59 96295 60 або її фармацевтично прийнятну сіль чи пролікарську форму, де: Rp являє собою циклопентил або трет-бутил; 1 Z вибирають з наступних структур: Ra являє собою метокси групу; Rb являє собою H; Rс являє собою феніл, який необов’язково заміщений одним або більшою кількістю F, Cl, Br, I, (C1-6)алкілів або (C1-6)алкокси груп; та 3 A приймає будь-яке зі значень, визначених в даному контексті. В іншому варіанті здійснення винаходу сполуки, що відповідають винаходу, виключають сполуку формули (X): або її фармацевтично прийнятну сіль або пролікарську форму, де: Rp являє собою (C1-6)алкіл або (C36)циклоалкіл; 1 Z вибирають з наступних структур: a R являє собою метокси групу; Rb являє собою H; Rc являє собою феніл, який необов’язково заміщений одним або більшою кількістю F, Cl, Br, I, (C1-6)алкілів або (C1-6)алкокси груп; та 3 A приймає будь-яке зі значень, визначених в даному контексті. В іншому варіанті здійснення винаходу сполуки, що відповідають винаходу, виключають сполуку формули (X): або її фармацевтично прийнятну сіль або пролікарську форму, де: Rp являє собою циклопентил або трет-бутил; 1 Z вибирають з наступних структур:
ДивитисяДодаткова інформація
Назва патенту англійськоюAntiviral phosphinate compounds
Автори англійськоюCasarez Anthony, Chaudhary Kleem, Cho, Aesop, Clarke Michael, Doerffler Edward, Fardis Maria, Kim, Choung, U., Kim Choung U., Pyun Hyungjung, Sheng, Xiaoning, C., Wang Jianying
Назва патенту російськоюАнтивирусные фосфинатные соединения
Автори російськоюКесейриз Энтони, Чодгари Клим, Чо Эзоп, Кларк Майкл, Доэрффлер Эдвард, Фердис Мерайя, Ким Чоунг У., Пиун Хиунгджунг, Шенг Ксиаонинг К., Ванг Джианиинг
МПК / Мітки
МПК: C07F 9/572, A61P 31/12, C07F 9/6558, A61K 31/662
Мітки: антивірусні, сполуки, фосфінатні
Код посилання
<a href="https://ua.patents.su/139-96295-antivirusni-fosfinatni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Антивірусні фосфінатні сполуки</a>
Попередній патент: Застосування сполуки, що містить кремній, як осушувача поліолефінових композицій
Наступний патент: Піридазинові сполуки і їх застосування
Випадковий патент: Сонячний водонагрівач