7-азаіндоли, їх застосування як інгібіторів фосфодіестерази 4 та спосіб їх одержання
Номер патенту: 76432
Опубліковано: 15.08.2006
Автори: Гьофген Норберт, Полімеропулос Еммануель, Зелений Штефан, Егерланд Уте, Кронбах Томас, Маркс Дегенхард, Кусс Хільдегард
Формула / Реферат
1. 7-азаіндоли формули 1
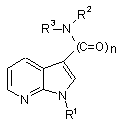 , 1
, 1
де
n може дорівнювати 1 або 2, і
R1 може означати
-(С1-С10)-алкіл лінійної або розгалуженої будови, незаміщений або заміщений одним або кількома замісниками, вибраними із групи, до якої входять -OH, -SH, -NH2, -NH(С1-С6)-алкіл, -N(С1-С6-алкіл)2, -NH(С6-С14)-арил, -N(С6-С14-арил)2, -N(С1-С6-алкіл)(С6-С14-арил), -NO2, -CN, -F, -Cl, -Br, -I, -O-(С1-С6)-алкіл, -O-(С6-С14)-арил, -S-(С1-С6)-алкіл, -S-(С6-С14)-арил, -SO3H, -SO2(С1-С6)-алкіл, -SO2(С6-С14)-арил, -OSO2(С1-С6)-алкіл, -OSO2(С6-С14)-арил, -COOH, -(CO)(С1-С5)-алкіл, моно-, ди- або трициклічні карбоцикли з кількістю членів у циклах від 3 до 14, насичені або з одним або кількома ненасиченими зв’язками, моно-, ди- або трициклічні гетероцикли з числом членів у циклах від 5 до 15, насичені або з одним або кількома ненасиченими зв’язками, що містять від 1 до 6 гетероатомів, у варіанті, якому віддається перевага, N, O та S, причому (С6-С14)-арильні групи та карбоциклічні й гетероциклічні замісники можуть бути у свою чергу незаміщеними або заміщеними одним або кількома замісниками R4,
-(С2-С10)-алкеніл з одним або кількома ненасиченими зв’язками лінійної або розгалуженої будови, незаміщений або заміщений одним або кількома замісниками, вибраними із групи, до якої входять -OH, -SH, -NH2, -NH(С1-С6)-алкіл, -N(С1-С6-алкіл)2, -NH(С6-С14)-арил, -N(С6-С14-арил)2, -N(С1-С6-алкіл)(С6-С14-арил), -NO2, -CN, -F, -Cl, -Br, -I, -O-(С1-С6)-алкіл, -O-(С6-С14)-арил, -S-(С1-С6)-алкіл, -S-(С6-С14)-арил, -SO3H, -SO2(С1-С6)-алкіл, -SO2(С6-С14)-арил, -OSO2(С1-С6)-алкіл, -OSO2(С6-С14)-арил, -COOH, -(CO)(С1-С5)-алкіл, моно-, ди- або трициклічні карбоцикли з кількістю членів у циклах від 3 до 14, насичені або з одним або кількома ненасиченими зв’язками, моно-, ди- або трициклічні гетероцикли з кількістю членів у циклах від 5 до 15, насичені або з одним або кількома ненасиченими зв’язками, що містять від 1 до 6 гетероатомів, у варіанті, якому віддається перевага, N, O та S, причому (С6-С14)-арильні групи та карбоциклічні й гетероциклічні замісники можуть бути у свою чергу незаміщеними або заміщеними одним або кількома замісниками R4,
R2 та R3 можуть бути однаковими або різними, при цьому лише один із них може бути атомом водню; крім того, R2 та R3 можуть означати
-(С1-С5)-алкіл, незаміщений або заміщений одним або кількома замісниками, вибраними із групи, до якої входять -OH, -SH, -NH2, -NH(С1-С6)-алкіл, -N(С1-С6-алкіл)2, -NO2, -CN, -F, -Cl, -Br, -I, -O-(С1-С6)-алкіл, -S-(С1-С6)-алкіл, -феніл, -піридил,
-феніл, незаміщений або заміщений одним або кількома замісниками, вибраними із групи, до якої входять -OH, -SH, -NH2, -NH(С1-С3)-алкіл, -N(С1-С3-алкіл)2, -NO2, -CN, -COOH, -COO(С1-С3)-алкіл, -F, -Cl, -Br, -O-(С1-С3)-алкіл, -S-(С1-С3)-алкіл,
-піридил, незаміщений або заміщений одним або кількома замісниками, вибраними із групи, до якої входять -NO2, -CN, -COOH, -COO(С1-С3)-алкіл, -Cl, -Br, -O-(С1-С3)-алкіл, -S-(С1-С3)-алкіл, а також
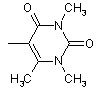 ,
,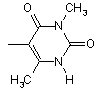 ,
,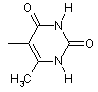 ,
,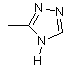 ,
,
і, крім того, група -NR2R3 у цілому може являти собою
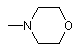 ,
,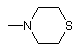 ,
,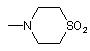 ,
,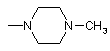 ,
,
і R4 може означати
-Н, -OH, -SH, -NH2, -NH(С1-С6)-алкіл, -N(С1-С6-алкіл)2, -NH(С6-С14)-арил, -N(С6-С14-арил)2, -N(С1-С6-алкіл)(С6-С14-арил), -NHCO(С1-С6)-алкіл, -NO2, -CN, -COOH, -COO(С1-С6)-алкіл, -(CO)(С1-С6)-алкіл, -(CS)(С1-С6)-алкіл, -F, -Cl, -Br, -I, -O-(С1-С6)-алкіл, -O-(С6-С14)-арил, -S-(С1-С6)-алкіл, -S-(С6-С14)-арил, -SO(С1-С6)-алкіл, -SO2(С1-С6)-алкіл,
за умови, що якщо n=1, R1, R2, R3 не є в той же час
R1=(С1-С6)-алкіл,
R2=-Н або (С1-С6)-алкіл, і
R3=
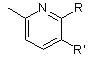 ,
,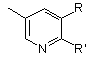 ,
,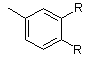 ,
,
причому R, R¢ незалежно один від одного є -(С1-С6)-алкіл, факультативно заміщений одним або кількома атомами галоїду, -(С2-С6)-алкеніл, -(С3-С6)-циклоалкоксигрупа, -(С3-С6)-циклоалкіл-(С1-С6)-алкоксигрупа, -(С2-С6)-алкініл, -(С3-С6)-циклоалкіл, -(С3-С6)-циклоалкіл-(С1-С6)-алкіл, -(С1-С6)-алкілтіогрупа, -(С3-С6)-циклоалкілтіогрупа, -(С3-С6)-циклоалкіл-(С1-С6)-алкілтіогрупа, -(С1-С6)-алкоксигрупа, гідроксил, галоїд, нітрогрупа, -CF3, -C2F5, -OCF3, -SCF3, -SO2CF3, -SO2F, форміл, -(С2-С6)-алканоїл, ціан, факультативно заміщений феніл або тієніл, -NR¢¢2, -CONR¢¢2, -COOR”,
або
R+R¢ спільно утворюють 5-членний карбоцикл або гетероцикл, і
R¢¢ є -H або -(С1-С6)-алкіл.
2. Фізіологічно толерантні солі сполук формули 1 за п. 1, де основні групи нейтралізовані неорганічними або органічними кислотами або кислотні групи нейтралізовані неорганічними або органічними основами, або третинні аміногрупи перетворені у четвертинні амонієві солі.
3. Сполуки формули 1 за пп. 1 або 2 з асиметричними вуглецевими атомами в D-формі, L-формі або у формі D,L-сумішей, або, в разі кількох асиметричних вуглецевих атомів, у діастереомерних формах.
4. Сполука формули 1 за пп. 1-3, де n=1, вибрана з перелічених нижче сполук:
(1) амід N-(4-піридилметил)-1-циклопропілметил-7-азаіндол-3-карбонової кислоти;
(2) амід N-(3,5-дихлорпіридин-4-іл)-1-ізобутил-7-азаіндол-3-карбонової кислоти;
(3) амід N-(3,5-дихлорпіридин-4-іл)-1-гексил-7-азаіндол-3-карбонової кислоти;
(4) амід N-(3,5-дихлорпіридин-4-іл)-1-циклопропілметил-7-азаіндол-3-карбонової кислоти;
(5) амід N-(4-піридилметил)-1-(4-фторбензил)-7-азаіндол-3-карбонової кислоти;
(6) амід N-(3,5-дихлорпіридин-4-іл)-1-(4-фторбензил)-7-азаіндол-3-карбонової кислоти;
(7) амід N-(3,5-дихлорпіридин-4-іл)-1-(4-метоксибензил)-7-азаіндол-3-карбонової кислоти;
(8) амід N-(4-піридилметил)-1-(4-хлорбензил)-7-азаіндол-3-карбонової кислоти;
(9) морфолід 1-(4-фторбензил)-7-азаіндол-3-карбонової кислоти;
(10) амід N-(2,6-дихлорфеніл)-1-(2-метилпропен-3-іл)-7-азаіндол-3-карбонової кислоти і
(11) амід N-(3,5-дихлорпіридин-4-іл)-1-(4-піридилметил)-7-азаіндол-3-карбонової кислоти.
5. Сполука формули 1 за пп. 1-3, де n=2, вибрана з перелічених нижче сполук:
(12) амід N-(3,5-дихлорпіридин-4-іл)-[1-(3-метоксибензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(13) гідрохлорид аміду N-(4-піридил)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(14) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(15) гідрохлорид аміду N-(4-піридил)-[1-(4-хлорбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(16) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4-хлорбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(17) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4-метоксибензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(18) амід N-(2,6-дихлорфеніл)-[1-(4-хлорбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(19) амід N-(4-карбоксифеніл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(20) амід N-(4-етоксикарбонілфеніл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(21) амід N-(3,4-диметоксифеніл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(22) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4-метилбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(23) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4-гідроксибензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(24) амід N-(3,5-дихлорпіридин-4-іл)-[1-(3-гідроксибензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(25) амід N-(3,5-дихлорпіридин-4-іл)-(1-циклопропілметил-7-азаіндол-3-іл)-гліоксилової кислоти;
(26) амід N-(3,5-дихлорпіридин-4-іл)-(1-гексил-7-азаіндол-3-іл)-гліоксилової кислоти;
(27) амід N-(3,5-дихлорпіридин-4-іл)-(1-ізобутил-7-азаіндол-3-іл)-гліоксилової кислоти;
(28) амід N-(3,5-дихлорпіридин-4-іл)-[1-(2-метилпропен-3-іл)-7-азаіндол-3-іл]-гліоксилової кислоти;
(29) амід N-(3,5-дихлорпіридин-4-іл)-[1-(2-метоксіетил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(30) амід N-(3,5-дихлорпіридин-4-іл)-[1-(1-нафтилметил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(31) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4-піридилметил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(32) амід N-(3,5-дихлорпіридин-4-іл)-[1-(3,5-диметилізоксазол-4-ілметил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(33) амід N,N-біс(2-метоксіетил)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(34) морфолід [1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(35) S,S-діоксотіоморфолід [1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(36) 4-метилпіперазид [1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(37) амід N-(6-метилурацил-5-іл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(38) амід N-(3,6-диметилурацил-5-іл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти;
(39) амід N-(1,3,6-триметилурацил-5-іл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти і
(40) амід N-(1,2,4-4H-триазол-3-іл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти.
6. Спосіб одержання сполук формули 1 за одним із пп. 1-4, де n=1, який відрізняється тим, що 7-азаіндол-3-карбонові кислоти дією хлорангідридів кислот перетворюють в аналогічні хлорангідриди 7-азаіндол-3-карбонових кислот, після чого шляхом реакції з первинними або вторинними амінами одержують сполуки формули 1 згідно з винаходом, де n=1.
7. Одержання сполук формули 1 за способом п. 6, яке відрізняється тим, що для синтезу хлорангідридів 7-азаіндол-3-карбонових кислот як згадані хлорангідриди кислот використовують тіонілхлорид або оксалілхлорид.
8. Одержання сполук формули 1 за способом пп. 6 або 7, яке відрізняється тим, що реакцію хлорангідридів 7-азаіндол-3-карбонових кислот із первинними або вторинними амінами виконують у присутності допоміжної основи, у варіанті, якому віддається перевага, у присутності надлишку аміну, використовуваного як реагент, третинного аміну, наприклад, піридину або триетиламіну, а також неорганічних основ, у варіанті, якому віддається перевага, гідроксидів лужних металів або гідридів лужних металів.
9. Спосіб одержання сполук формули 1 за одним із пп. 1-3 та 5, де n=2, який відрізняється тим, що 7-азаіндоли дією оксалілхлориду перетворюють в аналогічні хлорангідриди 7-азаіндол-3-ілгліоксилових кислот, після чого шляхом реакції з первинними або вторинними амінами одержують сполуки формули 1, де n=2.
10. Одержання сполук формули 1 за способом п. 9, яке відрізняється тим, що реакцію хлорангідридів 7-азаіндол-3-ілгліоксилових кислот із первинними або вторинними амінами виконують у присутності допоміжної основи, у варіанті, якому віддається перевага, у присутності надлишку аміну, використовуваного як реагент, третинного аміну, наприклад, піридину або триетиламіну, а також неорганічних основ, у варіанті, якому віддається перевага, гідроксидів лужних металів або гідридів лужних металів.
11. Сполуки формули 1 за одним із пп. 1-5 для застосування як терапевтичних активних речовин для виготовлення лікарських засобів для лікування захворювань, при яких терапевтично корисним є інгібування TNFa.
12. Сполуки формули 1 за одним із пп. 1-5 для застосування як терапевтичних активних речовин для виготовлення лікарських засобів для лікування захворювань, при яких терапевтично корисним є інгібування фосфодіестерази 4.
13. Сполуки формули 1 за одним із пп. 1-5 для застосування як терапевтичних активних речовин для виготовлення лікарських засобів для лікування захворювань, пов’язаних із впливом еозинофілів.
14. Сполуки формули 1 за одним із пп. 1-5 для застосування як терапевтичних активних речовин для виготовлення лікарських засобів для лікування захворювань, пов’язаних із впливом нейтрофілів.
15. Сполуки формули 1 за одним із пп. 1-5 для застосування як активних речовин для виготовлення лікарського засобу для лікування та/або профілактики захворювань, при яких корисним є інгібування TNFa, зокрема, запалення суглобів, артриту, ревматоїдного артриту, захворювань типу артритів, ревматоїдного спондиліту, остеоартриту, остеопорозу, сепсису, септичного шоку, грам-негативного сепсису, синдрому токсичного шоку, синдрому дихальної недостатності, астми, хронічних легеневих захворювань, резорбції кісток, реакції відторгнення трансплантатів; автоімунних захворювань, системного червоного вовчака, розсіяного склерозу, гломерулонефриту, увеїту, інсулінозалежного цукрового діабету, хронічної демієлінізації; вірусних захворювань, вірусних інфекцій, паразитарних інфекцій, малярії, лейшманіозу, лихоманки інфекційного походження, болю в м’язах інфекційного походження, СНІДу, кахексії; захворювань, які можна лікувати шляхом інгібування фосфодіестерази 4, астми; захворювань, при яких певну роль відіграють еозинофіли, бронхіальної астми, алергічного риніту, алергічного кон’юнктивіту, атопічного дерматиту, екземи, алергічного ангіїту, опосередкованих еозинофілами запалень, еозинофільного фасциту, еозинофільної пневмонії, синдрому PIE (легенева інфільтрація з еозинофілією), уртикарії, виразкового коліту, хвороби Крона, проліферативних захворювань шкіри, псоріазу, кератозу; хронічних обструктивних захворювань легенів; захворювань, які можна лікувати шляхом нейропротекції, сенільної деменції, хвороби Альцгеймера, втрати пам’яті, хвороби Паркінсона, депресій, нападів (ударів), переміжної кульгавості, захворювань простати, доброякісного розростання простати, частого сечовипускання, нічної поліурії, нетримання сечі, колік, колік, спричинених каменями в сечовому міхурі, статевих дисфункцій у чоловіків та жінок; а також як бронходилататорів, для інгібування виникнення залежності від лікарських засобів, а також для обмеження розвитку звикання до лікарських засобів.
16. Лікарський засіб, який містить одну або кілька сполук за пп. 1-5, а також звичайні фізіологічно толерантні носії та/або розріджувачі або допоміжні речовини.
17. Спосіб виготовлення лікарського засобу за п. 16, який відрізняється тим, що одну або кілька сполук за одним із пп. 1-5 перероблюють у фармацевтичний препарат спільно зі звичайними фармацевтичними носіями та/або розріджувачами або іншими допоміжними речовинами та/або в терапевтично застосовувані лікарські форми.
18. Сполука формули 1 за одним із пп. 1-3, яка являє собою амід N-(3,5-дихлорпіридин-4-іл)-[1-(4-фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти.
Текст
1. 7-азаіндоли формули 1 2 (19) 1 3 76432 4 -піридил, незаміщений або заміщений одним або 3. Сполуки формули 1 за пп. 1 або 2 з асиметричкількома замісниками, вибраними із групи, до якої ними вуглецевими атомами в D-формі, L-формі входять -NO2, -CN, -COOH, -COO(С1-С3)-алкіл, -Cl, або у формі D,L-сумішей, або, в разі кількох аси-Br, -O-(С1-С3)-алкіл, -S-(С1-С3)-алкіл, а також метричних вуглецевих атомів, у діастереомерних формах. O CH3 O CH3 4. Сполука формули 1 за пп. 1-3, де n=1, вибрана з N N перелічених нижче сполук: O O (1) амід N-(4-піридилметил)-1-циклопропілметил-7N азаіндол-3-карбонової кислоти; N (2) амід N-(3,5-дихлорпіридин-4-іл)-1-ізобутил-7H3C H H3C CH3 , , азаіндол-3-карбонової кислоти; O H (3) амід N-(3,5-дихлорпіридин-4-іл)-1-гексил-7азаіндол-3-карбонової кислоти; N N N (4) амід N-(3,5-дихлорпіридин-4-іл)-1O циклопропілметил-7-азаіндол-3-карбонової кислоN N ти; (5) амід N-(4-піридилметил)-1-(4-фторбензил)-7H3C H H , , азаіндол-3-карбонової кислоти; 2 3 і, крім того, група -NR R у цілому може являти (6) амід N-(3,5-дихлорпіридин-4-іл)-1-(4собою фторбензил)-7-азаіндол-3-карбонової кислоти; (7) амід N-(3,5-дихлорпіридин-4-іл)-1-(4метоксибензил)-7-азаіндол-3-карбонової кислоти; N O N S N SO2 (8) амід N-(4-піридилметил)-1-(4-хлорбензил)-7, , , азаіндол-3-карбонової кислоти; (9) морфолід 1-(4-фторбензил)-7-азаіндол-3N N CH3 карбонової кислоти; (10) амід N-(2,6-дихлорфеніл)-1-(2-метилпропен-3, іл)-7-азаіндол-3-карбонової кислоти і 4 і R може означати (11) амід N-(3,5-дихлорпіридин-4-іл)-1-(4-Н, -OH, -SH, -NH2, -NH(С1-С6)-алкіл, -N(С1-С6піридилметил)-7-азаіндол-3-карбонової кислоти. алкіл)2, -NH(С6-С14)-арил, -N(С6-С14-арил)2, -N(С15. Сполука формули 1 за пп. 1-3, де n=2, вибрана з С6-алкіл)(С6-С14-арил), -NHCO(С1-С6)-алкіл, -NO2, перелічених нижче сполук: CN, -COOH, -COO(С1-С6)-алкіл, -(CO)(С1-С6)-алкіл, (12) амід N-(3,5-дихлорпіридин-4-іл)-[1-(3-(CS)(С1-С6)-алкіл, -F, -Cl, -Br, -I, -O-(С1-С6)-алкіл, метоксибензил)-7-азаіндол-3-іл]-гліоксилової кисO-(С6-С14)-арил, -S-(С1-С6)-алкіл, -S-(С6-С14)-арил, лоти; -SO(С1-С6)-алкіл, -SO2(С1-С6)-алкіл, (13) гідрохлорид аміду N-(4-піридил)-[1-(4за умови, що якщо n=1, R1, R2, R3 не є в той же час фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти; R1=(С1-С6)-алкіл, (14) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4R2=-Н або (С1-С6)-алкіл, і фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти; R3= (15) гідрохлорид аміду N-(4-піридил)-[1-(4R N R R хлорбензил)-7-азаіндол-3-іл]-гліоксилової кислоти; (16) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4хлорбензил)-7-азаіндол-3-іл]-гліоксилової кислоти; N R, R' , R' , (17) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4метоксибензил)-7-азаіндол-3-іл]-гліоксилової киспричому R, R незалежно один від одного є -(С1лоти; С6)-алкіл, факультативно заміщений одним або (18) амід N-(2,6-дихлорфеніл)-[1-(4-хлорбензил)-7кількома атомами галоїду, -(С2-С6)-алкеніл, -(С3азаіндол-3-іл]-гліоксилової кислоти; С6)-циклоалкоксигрупа, -(С3-С6)-циклоалкіл-(С1(19) амід N-(4-карбоксифеніл)-[1-(4-фторбензил)-7С6)-алкоксигрупа, -(С2-С6)-алкініл, -(С3-С6)азаіндол-3-іл]-гліоксилової кислоти; циклоалкіл, -(С3-С6)-циклоалкіл-(С1-С6)-алкіл, -(С1(20) амід N-(4-етоксикарбонілфеніл)-[1-(4С6)-алкілтіогрупа, -(С3-С6)-циклоалкілтіогрупа, -(С3фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти; С6)-циклоалкіл-(С1-С6)-алкілтіогрупа, -(С1-С6)(21) амід N-(3,4-диметоксифеніл)-[1-(4алкоксигрупа, гідроксил, галоїд, нітрогрупа, -CF3, фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти; C2F5, -OCF3, -SCF3, -SO2CF3, -SO2F, форміл, -(С2(22) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4С6)-алканоїл, ціан, факультативно заміщений феметилбензил)-7-азаіндол-3-іл]-гліоксилової кислоніл або тієніл, -NR 2, -CONR 2, -COOR”, ти; або (23) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4R+R спільно утворюють 5-членний карбоцикл або гідроксибензил)-7-азаіндол-3-іл]-гліоксилової кисгетероцикл, і лоти; R є -H або -(С1-С6)-алкіл. (24) амід N-(3,5-дихлорпіридин-4-іл)-[1-(32. Фізіологічно толерантні солі сполук формули 1 гідроксибензил)-7-азаіндол-3-іл]-гліоксилової кисза п. 1, де основні групи нейтралізовані неорганічлоти; ними або органічними кислотами або кислотні гру(25) амід N-(3,5-дихлорпіридин-4-іл)-(1пи нейтралізовані неорганічними або органічними циклопропілметил-7-азаіндол-3-іл)-гліоксилової основами, або третинні аміногрупи перетворені у кислоти; четвертинні амонієві солі. 5 76432 6 (26) амід N-(3,5-дихлорпіридин-4-іл)-(1-гексил-710. Одержання сполук формули 1 за способом азаіндол-3-іл)-гліоксилової кислоти; п. 9, яке відрізняється тим, що реакцію хлорангід(27) амід N-(3,5-дихлорпіридин-4-іл)-(1-ізобутил-7ридів 7-азаіндол-3-ілгліоксилових кислот із перазаіндол-3-іл)-гліоксилової кислоти; винними або вторинними амінами виконують у (28) амід N-(3,5-дихлорпіридин-4-іл)-[1-(2присутності допоміжної основи, у варіанті, якому метилпропен-3-іл)-7-азаіндол-3-іл]-гліоксилової віддається перевага, у присутності надлишку амікислоти; ну, використовуваного як реагент, третинного амі(29) амід N-(3,5-дихлорпіридин-4-іл)-[1-(2ну, наприклад, піридину або триетиламіну, а також метоксіетил)-7-азаіндол-3-іл]-гліоксилової кислоти; неорганічних основ, у варіанті, якому віддається (30) амід N-(3,5-дихлорпіридин-4-іл)-[1-(1перевага, гідроксидів лужних металів або гідридів нафтилметил)-7-азаіндол-3-іл]-гліоксилової кислолужних металів. ти; 11. Сполуки формули 1 за одним із пп. 1-5 для (31) амід N-(3,5-дихлорпіридин-4-іл)-[1-(4застосування як терапевтичних активних речовин піридилметил)-7-азаіндол-3-іл]-гліоксилової кислодля виготовлення лікарських засобів для лікування ти; захворювань, при яких терапевтично корисним є (32) амід N-(3,5-дихлорпіридин-4-іл)-[1-(3,5інгібування TNF . диметилізоксазол-4-ілметил)-7-азаіндол-3-іл]12. Сполуки формули 1 за одним із пп. 1-5 для гліоксилової кислоти; застосування як терапевтичних активних речовин (33) амід N,N-біс(2-метоксіетил)-[1-(4-фторбензил)для виготовлення лікарських засобів для лікування 7-азаіндол-3-іл]-гліоксилової кислоти; захворювань, при яких терапевтично корисним є (34) морфолід [1-(4-фторбензил)-7-азаіндол-3-іл]інгібування фосфодіестерази 4. гліоксилової кислоти; 13. Сполуки формули 1 за одним із пп. 1-5 для (35) S,S-діоксотіоморфолід [1-(4-фторбензил)-7застосування як терапевтичних активних речовин азаіндол-3-іл]-гліоксилової кислоти; для виготовлення лікарських засобів для лікування (36) 4-метилпіперазид [1-(4-фторбензил)-7захворювань, пов’язаних із впливом еозинофілів. азаіндол-3-іл]-гліоксилової кислоти; 14. Сполуки формули 1 за одним із пп. 1-5 для (37) амід N-(6-метилурацил-5-іл)-[1-(4застосування як терапевтичних активних речовин фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти; для виготовлення лікарських засобів для лікування (38) амід N-(3,6-диметилурацил-5-іл)-[1-(4захворювань, пов’язаних із впливом нейтрофілів. фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти; 15. Сполуки формули 1 за одним із пп. 1-5 для (39) амід N-(1,3,6-триметилурацил-5-іл)-[1-(4застосування як активних речовин для виготовфторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти лення лікарського засобу для лікування та/або і профілактики захворювань, при яких корисним є (40) амід N-(1,2,4-4H-триазол-3-іл)-[1-(4інгібування TNF , зокрема, запалення суглобів, фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти. артриту, ревматоїдного артриту, захворювань типу 6. Спосіб одержання сполук формули 1 за одним із артритів, ревматоїдного спондиліту, остеоартриту, пп. 1-4, де n=1, який відрізняється тим, що 7остеопорозу, сепсису, септичного шоку, грамазаіндол-3-карбонові кислоти дією хлорангідридів негативного сепсису, синдрому токсичного шоку, кислот перетворюють в аналогічні хлорангідриди синдрому дихальної недостатності, астми, хроніч7-азаіндол-3-карбонових кислот, після чого шляних легеневих захворювань, резорбції кісток, реахом реакції з первинними або вторинними амінами кції відторгнення трансплантатів; автоімунних заодержують сполуки формули 1 згідно з винаходом, хворювань, системного червоного вовчака, де n=1. розсіяного склерозу, гломерулонефриту, увеїту, 7. Одержання сполук формули 1 за способом п. 6, інсулінозалежного цукрового діабету, хронічної яке відрізняється тим, що для синтезу хлорангіддемієлінізації; вірусних захворювань, вірусних інридів 7-азаіндол-3-карбонових кислот як згадані фекцій, паразитарних інфекцій, малярії, лейшмахлорангідриди кислот використовують тіонілхлоніозу, лихоманки інфекційного походження, болю в рид або оксалілхлорид. м’язах інфекційного походження, СНІДу, кахексії; 8. Одержання сполук формули 1 за способом пп. 6 захворювань, які можна лікувати шляхом інгібуабо 7, яке відрізняється тим, що реакцію хлорангівання фосфодіестерази 4, астми; захворювань, дридів 7-азаіндол-3-карбонових кислот із первинпри яких певну роль відіграють еозинофіли, бронними або вторинними амінами виконують у присухіальної астми, алергічного риніту, алергічного тності допоміжної основи, у варіанті, якому кон’юнктивіту, атопічного дерматиту, екземи, алервіддається перевага, у присутності надлишку амігічного ангіїту, опосередкованих еозинофілами ну, використовуваного як реагент, третинного амізапалень, еозинофільного фасциту, еозинофільної ну, наприклад, піридину або триетиламіну, а також пневмонії, синдрому PIE (легенева інфільтрація з неорганічних основ, у варіанті, якому віддається еозинофілією), уртикарії, виразкового коліту, хвоперевага, гідроксидів лужних металів або гідридів роби Крона, проліферативних захворювань шкіри, лужних металів. псоріазу, кератозу; хронічних обструктивних за9. Спосіб одержання сполук формули 1 за одним із хворювань легенів; захворювань, які можна лікупп. 1-3 та 5, де n=2, який відрізняється тим, що 7вати шляхом нейропротекції, сенільної деменції, азаіндоли дією оксалілхлориду перетворюють в хвороби Альцгеймера, втрати пам’яті, хвороби аналогічні хлорангідриди 7-азаіндол-3Паркінсона, депресій, нападів (ударів), переміжної ілгліоксилових кислот, після чого шляхом реакції з кульгавості, захворювань простати, доброякісного первинними або вторинними амінами одержують розростання простати, частого сечовипускання, сполуки формули 1, де n=2. нічної поліурії, нетримання сечі, колік, колік, спри 7 76432 8 чинених каменями в сечовому міхурі, статевих 17. Спосіб виготовлення лікарського засобу за дисфункцій у чоловіків та жінок; а також як бронп. 16, який відрізняється тим, що одну або кілька ходилататорів, для інгібування виникнення залежсполук за одним із пп. 1-5 перероблюють у фарності від лікарських засобів, а також для обмеженмацевтичний препарат спільно зі звичайними фаня розвитку звикання до лікарських засобів. рмацевтичними носіями та/або розріджувачами 16. Лікарський засіб, який містить одну або кілька або іншими допоміжними речовинами та/або в сполук за пп. 1-5, а також звичайні фізіологічно терапевтично застосовувані лікарські форми. толерантні носії та/або розріджувачі або допоміжні 18. Сполука формули 1 за одним із пп. 1-3, яка речовини. являє собою амід N-(3,5-дихлорпіридин-4-іл)-[1-(4фторбензил)-7-азаіндол-3-іл]-гліоксилової кислоти. Цей винахід стосується азаіндолів загальної формули 1 заміщених 7 способу їх одержання, фармацевтичних препаратів, які містять ці сполуки, а також фармацевтичного застосування цих сполук, які є інгібіторами фосфодіестерази 4, як активних речовин для лікування захворювань, при яких виникає потреба пригнічення активності фосфодіестерази 4 в імунокомпетентних клітинах (наприклад, макрофагах та лімфоцитах) дією сполук, що відповідають цьому винаходу. Активація рецепторів клітинних мембран трансмітерами спричиняє активацію системи "вторинних месенджерів". Аденілатциклаза синтезує з аденозинмонофосфату (AMP) та іуанозин-3',5'монофосфату (GMP) активні сполуки - відповідно циклічний AMP (cAMP) та циклічний GMP (cGMP). Ці речовини викликають, наприклад, релаксацію у клітинах гладеньких м'язів або пригнічення виділення або синтезу медіатора в запалених клітинах. Розклад "вторинних месенджерів" сАМР та cGMP відбувається під впливом фосфодіестераз (PDE). На цей час відомі 11 сімейств ензимів PDE (PDE1-PDE11), які відрізняються одне від одного специфічністю до субстратів (сАМР, cGMP або до обох) та залежністю від інших субстратів (наприклад, калмодуліну). Ці ізоензими виконують в організмі різні функції і виражені в окремих видах клітин у різному ступені [дивись Бево, Конті та Хейсліп, "Множинні фосфодіестерази циклічних нуклеотидів" - Beavo J.A., Conti M., Heaslip R.J., Multiple cyclic nucleotide phosphodiesterases. Моl. Pharmacol. 1994, 46:399-405; Холл, "Ізоензими селективні інгібітори фосфодіестераз: потенціальне клінічне застосування" - Hall I.P., Isoenzyme selective phosphodiesterase inhibitors: potential clinical uses, Br. J. Clin. Pharmacol. 1993, 35:1-7]. Шляхом інгібування різних ізоензимних типів PDE досягається нагромадження сАМР або cGMP у клітинах, яке можна використати для лікувальних цілей [дивись Торфі, Ліві, Крістенсен, "Нові інгібітори фосфодіестераз для терапії астми" TorphyT.J., Livi G.P., Christensen S.B., Novel Phosphodiesterase Inhibitors for the Therapy of Asthma, Drug News and Perspectives 1993, 6:203214]. У клітинах, які відіграють важливу роль при алергічних запаленнях (лімфоцитах, мастоцитах, еозинофільних гранулоцитах, макрофагах) переважним ізоензимом PDE є ізоензим типу 4 [дивись Торфі та Ундем, "Інгібітори фосфодіестераз: нові можливості лікування астми" - Torphy T.J., Undem В. J., Phosphodiesterase inhibitors: new opportunities for the treatment of astma. Thorax 1991, 46:512-523]. Тому пригнічення PDE 4 відповідними інгібіторами розглядається як важливий підхід до лікування численних захворювань, викликаних алергією [дивись Шудт, Дент, Рабе, "Інгібітори фосфодіестераз" - Schudt Ch., Dent G., Rabe К., Phosphodiesterase Inhibitors, Acad. Press, London 1996]. Важливою властивістю інгібіторів фосфодіестерази 4 є інгібування виділення -фактора некрозу пухлин (TNF ) із запалених клітин. TNF є сильнодіючим запальним цитокіном, який впливає на численні біологічні процеси. TNF вивільнюється, наприклад, з активованих макрофагів, активованих Т-лімфоцитів, мастоцитів, базофілів, фібробластів, клітин ендотелію та астроцитів у мозку. У свою чергу, він спричиняє активацію нейтрофілів, еозинофілів, фібробластів та клітин ендотелію, причому виділяються різноманітні медіатори, які сприяють руйнуванню тканин. У моноцитах, макрофагах та Т-лімфоцитах TNF викликає посилене продукування інших запальних цитокінів, таких як фактор стимуляції колонієутворення гранулоцитарних макрофагів (GM-CSF) або інтерлейкін-8. Унаслідок свого стимулювального впливу на запалення та катаболічного ефекту TNF відіграє головну роль при численних захворюваннях, наприклад, при запаленнях дихальних шляхів, запаленнях суглобів, ендотоксичному шоку, відторгненні тканин, СНІДі та багатьох імунологічних захворюваннях. Отже, інгібітори фосфодіестерази 4 придатні також для лікування таких захворювань, пов'язаних із впливом TNF . Хронічні обструктивні захворювання легенів (COPD) широко розповсюджені серед населення і мають також велике економічне значення. Так, наприклад, захворювання типу COPD є причиною 9 76432 10 приблизно 10-15% загальних витрат на лікування у ється незадовільною, особливо з точки зору посрозвинутих країнах, і в США на рахунок цих захвотійного погіршення функції легенів. Нові терапеврювань можна віднести приблизно 25% всіх смертичні підходи, базовані на застосуванні медіаторів тних випадків [дивись Норман, "COPD: нові розрозапалення, протеаз або адгезивних молекул, мобки та терапевтичні можливості" - Norman P., жуть бути дуже перспективними [Барнс, "Хронічні CORD: New developments and therapeutic обструктивні захворювання: нові можливості розopportunities, Drug News Perspect. 11(7), 431-437, робки лікарських засобів" - Barnes P.J. Chronic 1998]; проте вік більшості пацієнтів на момент obstructive disease: new opportunities for drug смерті перевищує 55 років [Нольте, "Хронічний development, TiPS 10(19), 415-423, 1998]. бронхіт - загальнонаціональне захворювання баНезалежно від бактеріальних інфекцій, які гатофакторного походження" - Nolte D., Chronic ускладнюють захворювання, у бронхах виявляєтьBronchitis - a National Disease of Multifactorial Origin. ся хронічне запалення, при якому домінують нейтAtemw.-Lungenkrkh. 20(5), 260-267, 1994]. За оцінрофільні гранулоцити. Вважається, що за структуками ВООЗ, у найближчі 20 років COPD стануть рні зміни в дихальних шляхах (емфізему), які третьою за частотою причиною смерті. спостерігаються, несуть відповідальність, поряд з Загальна картина захворювання на хронічні іншими чинниками, медіатори та ензими, які вивіобструктивні хвороби легенів (COPD) охоплює льнюються з нейтрофільних гранулоцитів. Таким різноманітні синдроми хронічних захворювань типу чином, інгібування активності нейтрофільних грабронхітів із симптомами кашлю та виділення мокнулоцитів є раціональним прийомом для запобіротиння, а також прогресуючого та необоротного гання подальшому розвиткові COPD (погіршенню погіршення функції легенів (особливо утруднюєтьфункціональних параметрів легенів) або для спося видих). Перебіг захворювання нерівномірний і вільнення такого розвитку. Важливим чинником часто ускладнюється бактеріальними інфекціями активації гранулоцитів є запальний цитокін TNF [Реннард, "COPD: огляд визначень, епідеміологія (фактор некрозу пухлин). Відомо, наприклад, що та чинники, що впливають на розвиток захворюTNF стимулює утворення вільних кисневих радивання" - Rennard S. I., CORD: Overview of калів у гранулоцитах [Йєрсман, Ратьєн, Ферранте, definitions, Epidemiology, and factors influencing its "Посилення індукованого ліпополісахаридами проdevelopment. Chest 113(4) Suppl., 235S-241S, дукування кисневих радикалів нейтрофілами під 1998]. У процесі захворювання функція легенів впливом TNF " -Jersmann Η.Ρ.Α., D.A. Rathien and постійно погіршується, розвивається емфізема A. Ferrante: Enhancement of LPS-induced neutrophil легенів, і дихальна недостатність у пацієнтів стає oxygen radical production by TNF , Infection and очевидною. Це захворювання явно погіршує якість Immunity, 4, 1744-1747, 1998]. Інгібітори PDE4 здажиття пацієнтів (задишка, низька витривалість при тні дуже ефективно інгібувати вивільнення TNF із фізичних навантаженнях) і значно скорочує очікурізноманітних клітин і пригнічувати таким чином вану тривалість життя. Головним фактором ризиактивність нейтрофільних гранулоцитів. Неспецику, окрім чинників навколишнього середовища, є фічний інгібітор PDE - пентоксифілін - може інгібупаління [Куммер, "Астма та COPD" - KummerF. вати як утворення кисневих радикалів, так і фагоAstma and CORD, Atemw.-Lungenkrkh. 20(5), 299цитозну здатність нейтрофільних гранулоцитів 302, 1994; Rennard S. I., CORD: Overview of [Веніш та інші, "Вплив пентоксифіліну in vitro на definitions, Epidemiology, and factors influencing its продукування реакційноздатного кисню та фагоциdevelopment. Chest 113(4) Suppl., 235S-241S, тарну здатність нейтрофілів за даними цитометрії 1998], отже, у чоловіків захворювання зустрічаєтьв потоці" - С. Wenish, К. Zedtwitz-Liebenstein, В. ся явно частіше, ніж серед жінок. Однак у майбутParschalk, W. Graninger: Effect of pentoxifylline in ньому слід очікувати зміну цієї закономірності під vitro on neutrophil reactive oxygen production and впливом зміни життєвих звичок і збільшення кільphagocytic ability, assessed by flow cytometry, Clin. кості жінок, які палять. Drug Invest., 13(2):99-104, 1997]. Сучасна терапія спрямована тільки на полегУже відомі різноманітні інгібітори PDE4. Мова шення симптомів і не втручається в причини розйде переважно про похідні ксантину, аналоги ролівитку захворювання. Застосування бета-2праму або похідні нітраквазону [огляд дивись Карагоністів тривалої дії (наприклад, сальметеролу), лсон, Альдос, "Інгібітори фосфодіестерази 4 для можливо в комбінації з мускаринергічними агоніслікування астми" - J.-A. Karlsson, D. Aldos, тами (наприклад, іпратопіумом) поліпшує функцію Phocphodiesterase 4 inhibitors for the treatment of легенів шляхом розширення бронхів і широко заastma, Exp. Opin. Ther. Patents 1997, 7:989-1003]. стосовується в практиці [дивись Norman P., CORD: Жодна з цих сполук досі не була доведена до кліNew developments and therapeutic opportunities, нічного застосування. Доводилося констатувати, Drug News Perspect. 11(7), 431-437, 1998]. Значну що відомі інгібітори PDE4 спричиняють різноманітроль при загостреннях COPD відіграють бактеріані побічні ефекти, наприклад, нудоту та блювання, льні інфекції, які слід лікувати антибіотиками [Уїлякі до цього часу не вдавалося достатньою мірою сон, "Роль інфекції при COPD" - Wilson R., The role усувати. Тому існує потреба в віднайденні нових of infections in CORD, Chest 113(4) Suppl., 242Sінгібіторів PDE4 із покращеним терапевтичним 248S, 1998; Гросман, "Значення антибіотиків та діапазоном. наслідки терапії антибіотиками при загостреннях Застосування 7-азаіндолів при розробленні COPD" - Grossman R.F. The value of antibiotics and нових активних речовин для різних цілей до цього the outcomes of antibiotic therapy in exacerbations of часу згадувалося лише зрідка. CORD, Chest 113(4) Suppl., 249S-255S, 1998]. ТеВ патенті Японії №10120681 [Fujisawa Pharm. рапія цього захворювання до цього часу залишаCo. Ltd.] заявлені 5- та 7-азаіндоли загальної фор 11 76432 12 мули де R1 - водень або нижчий алкіл, R2 може означати водень, галоїд, нижчі алкіли, циклоалкіли, алкілкарбоніли або алканоїли, R3 означає алканоїли, захищені карбоксили, ціан або заміщені карбамоїли. L означає короткий алкіленовий місточок. Q означає заміщені ароматичні та гетероциклічні групи. Одна із груп А1 та А2 означає N, а друга СН. Ці сполуки відрізняються від сполук згідно з цим винаходом, зокрема, замісниками R2 та R3, частково групами R1 та А2. Описані сполуки заявлені як інгібітори фосфодіестерази, специфічної для cGMP (PDE5). Як показання до застосування вказані різноманітні захворювання серця та системи кровообігу, бронхіт, астма, риніт, імпотенція, ускладнення діабету та глаукома. [Л.Н. Яхонтов, С.С. Ліберман, Д.М. Краснокутська та інші (Хим.-Фарм. Журнал 8(11), 1974, 5-9)] описали синтези різноманітних 3-аміноалкіл-4азаіндолів та 3-аміноалкіл-7-азаіндолів. Описано депресивну або антидепресивну дію 3-(2аміноетил)-7-азаіндолу. Виявлено ефект зниження кров'яного тиску під впливом 3-амінометил-7азаіндолу. [Вербіскар (A. J. Verbiscar, J. Med. Chem. 15(2), 1972, 149-152)] описав сполуку формули у якої виявлено протималярійну дію. У патенті США 650223 [Sterling Drug Inc.] описано синтез різноманітних 2-(імідазолін-2-іл)-алкіл7-азаіндолів та 3-(імідазолін-2-іл)-алкіл-7азаіндолів із відповідних 2- або 3-ціаноалкіл-7азаіндолів і заявлено застосування цих сполук як судинозвужувачів. Як інгібітори PDE4 7-азаіндоли до цього часу зовсім невідомі. Цей винахід стосується заміщених 7азаіндолів загальної формули 1 ви, де n може дорівнювати 1 або 2, і R1 означає -(С1-С10)-алкіл лінійної або розгалуженої будо факультативно заміщений одним або кількома замісниками, вибраними із групи, до якої входять ОН, -SH, -NH2, -NН(С1-С6)-алкіл, -N(С1-С6-алкіл)2, NH(C6-C14)-aptui, -N(С6-С14-арил)2, -N(С1-С6алкіл)(С6-С14-арил), -NO2, -CN, -F, -Cl, -Br, -І, -О(С1-С6)-алкіл, -О-(С6-С14)-арил, -S-(С1-С6)-алкіл, -S(C6-C14)-арил, -SO3H, -SО2(С1-С6)-алкіл, -SО2(С6С14)-арил, -ОSО2(СгС6)-алкіл, -ОSО2(С6-С14)-арил, СООН, -(СО)(С1-С5)-алкіл, моно-, ди- або трициклічні карбоцикли з кількістю членів у циклах від 3 до 14, насичені або з одним або кількома ненасиченими зв'язками, моно-, ди- або трициклічні гетероцикли з кількістю членів у циклах від 5 до 15, насичені або з одним або кількома ненасиченими зв'язками, що містять від 1 до 6 гетероатомів, переважно Ν, Ο та S, причому (С6-С14)-арильні групи та карбоциклічні й гетероциклічні замісники можуть бути у свою чергу заміщені одним або кількома замісниками R4, -(С2-С10)-алкеніл з одним або кількома ненасиченими зв'язками лінійної або розгалуженої будови, факультативно заміщений одним або кількома замісниками, вибраними з групи, до якої входять ОН, -SH, -NH2, -NH(C1-С6)-алкіл, -N(С1-С6-алкіл)2, NН(С6-С14)-арил, -N(С6-С14-арил)2, -N(С1-С6алкіл)(С6-С14-арил), -NO2, -CN, -F, -СІ, -Вr, -І, -О(С1-С6)-алкіл, -О-(С6-С14)-арил, -S-(С1-С6)-алкіл, -S(C6-C14)-арил, -SO3H, -SO2(С1-С6)-алкіл, -SО2(С6С14)-арил, -ОSО2(С1-С6)-алкіл, -OSO2(C6-C14)-арил, -СООН, -(СО)(С1-С5)-алкіл, моно-, ди- або трициклічні карбоцикли з кількістю членів у циклах від 3 до 14, насичені або з одним або кількома ненасиченими зв'язками, моно-, ди- або трициклічнігетероцикли з кількістю членів у циклах від 5 до 15, насичені або з одним або кількома ненасиченими зв'язками, що містять від 1 до 6 гетероатомів, переважно Ν, Ο та S, причому (С6-С14)-арильні групи та карбоциклічні й гетероциклічні замісники можуть бути у свою чергу заміщені одним або кількома замісниками R4, R2 та R3 можуть бути однаковими або різними, при цьому лише один із них може бути атомом водню; крім того, R2 та R3 можуть означати -(С1-С5)-алкіл, факультативно заміщений одним або кількома замісниками, вибраними із групи, до якої входять -ОН, -SH, -NH2, -NH(С1-С6)-алкіл, N(С1-С6-алкіл)2, -NO2, -CN, -F, -СІ, -Вr, -І, -О-(С1С6)-алкіл, -S-(С1-С6)-алкіл, -феніл, -піридил, феніл, факультативно заміщений одним або кіль 13 76432 14 кома замісниками, вибраними із групи, до якої У варіантах, яким віддається особлива перевходять -ОН, -SH, -NH2, -NH(С1-С3)-алкіл, -N(С1-С3вага, R1 є група, яка містить циклічний вуглевоалкіл)2, -NO2, -CN, -COOH, -СОО(С1-С3)-алкіл, -F, день, наприклад, циклопропілметил, лінійний вугСІ, -Вr, -О-(С1-С3)-алкіл, -S-(С1-С3)-алкіл, -піридил, леводень, наприклад, н-гексил, лінійний факультативно заміщений одним або кількома вуглеводень, заміщений алкоксигрупою, напризамісниками, вибраними із групи, до якої входять клад, 2-метоксіетил, розгалужений вуглеводень, NO2, -CN, -СООН, -СОО(С1-С3)-алкіл, -СІ, -Вr, -Онаприклад, ізобутил, ненасичений вуглеводень, (С1-С3)-алкіл, -S-(С1-С3)-алкіл, а також наприклад, 2-метилпропен-3-іл, або вуглеводневий радикал, який містить ароматичну групу, факультативно заміщену, наприклад, 4-фторбензил, 3-метоксибензил, 4-метоксибензил, 4-хлорбензил, 4-метилбензил, 3-гідроксибензил або 4гідроксибензил, група, яка містить гетероароматичний вуглеводень, наприклад, 4-піридилметил або 3,5-диметилізоксазол-4-метил, або група, яка місГрупа -NR2R3 у цілому може являти собою тить конденсований ароматичний вуглеводень, наприклад, 1-нафтилметил. Замісники при атомі азоту, R2 та R3, у варіанті, якому віддається перевага, можуть бути факультативно заміщеними (С1-С5)-алкілами, зокрема, R4 може означати (С1-С3)-алкілами, а особлива перевага віддається -Н, -ОН, -SH, -NH2, -NH(С1-С6)-алкіл, -N(С1-С6С1-алкілу (тобто, метилу). алкіл)2, -NH(C6-C14)-арил, -N(C6-C14-арил)2, -N(С1У варіантах здійснення винаходу, яким віддаС6-алкіл)(С6-С14-арил), -NHCO(С1-С6)-алкіл, -NO2, ється перевага, один із замісників R2 та/або R3 є CN, -COOH, -СОО(С1-С6)-алкіл, -(СО)(С1-С6)-алкіл, радикал, який включає гетероароматичний вугле-(CS)(С1-С6)-алкіл, -F, -СІ, -Вr, -І, -О-(С1-С6)-алкіл, водень, наприклад, 4-піридилметил, причому згаО-(С6-С14)-арил, -S-(С1-С6)-алкіл, -S-(C6-C14)-арил, даний гетеароматичний вуглеводень може бути, в -SО(С1-С6)-алкіл, -SО2(С1-С6)-алкіл. свою чергу, заміщеним, у варіанті, якому віддаєтьВ 7-азаівдолах формули 1 згідно з цим вина1 ся перевага, галоїдом, таким як 3,5-дихлор-4ходом замісник R є переважно (С1-С10)-алкіл. Тапіридил. В іншому варіанті, якому віддається пекий алкільний радикал може мати лінійну, розгаревага, R2 та/або R3 є радикал морфоліно. Далі, лужену або циклічну будову, причому перевага перевага віддається замісникам R2 та R3, які вклювіддається лінійній будові. Особлива перевага чають ароматичний вуглеводень, який у варіанті, віддається алкільним радикалам із кількістю вугякому віддається перевага, є заміщеним, зокрема, лецевих атомів від 1 до 6, ще більша перевага галоїдом або карбоксилом, наприклад, 2,6радикалам із кількістю вуглецевих атомів від 1 до дихлорфеніл, 4-карбоксифеніл, 44. В іншому варіанті здійснення винаходу, якому етоксикарбонілфеніл, 3,4-диметоксифеніл. Ще віддається перевага, R1 є (С2-С10)-алкеніл, у варіакраще, якщо як R2, так і R3 означають метоксіетил. нті, якому віддається більша перевага, (С2-С6)В інших варіантах здійснення винаходу, яким відалкеніл, у варіанті, якому віддається найбільша дається перевага, R2 або R3 означає радикал перевага, (С -С )-алкеніл. Цей алкенільний ради2 4 кал може містити один або кілька ненасичених зв'язків, наприклад, два або три таких зв'язки. Алкенільний радикал може мати лінійну, розгалужену або циклічну будову. Особлива перевага віддається замісникам R1, де алкільний або алкенільний радикал має один або кілька замісників, наприклад, два, три, чотири або п'ять. У варіантах, яким віддається особлива перевага, замісник R1 є заміщений C1-алкіл (тобто, метил). Серед вищезгаданих замісників при алкільній або алкенільній групі R1 перевага віддається, зокрема, -ОН, -F, -СІ, -Вr, І, (С1-С4)-алкоксигрупам. Далі, перевага віддається замісникам, де алкіл (у разі його присутності) містить від 1 атому до 4 атомів вуглецю, а арил (у разі його присутності) містить від 6 атомів до 10 атомів вуглецю. Серед карбоциклів перевага віддається фенілу, зокрема, заміщеному фенілу, який заміщенийу варіанті, якому віддається перевага, F, -СІ, -Br, -I, (С1-С6)-алкоксигрупою або гідроксилом. Серед гетероциклів перевага віддається таким, які містять щонайменше один гетероатом, вибраний із групи, до якої входять Ν, Ο та S. Особлива перевага серед гетероциклів віддається піридилу, а також ізоксазолілу, зокрема, 3,5диметилізоксазолілу. Прикладом конденсованого карбоциклічного замісника є нафтил. або група -NR2R3 у цілому являє собою Далі, цей винахід стосується фізіологічно толерантних солей сполук формули 1. Фізіологічно толерантні солі одержують звичайним способом шляхом нейтралізації основ неорганічними або органічними кислотами або шляхом нейтралізації кислот неорганічними або органічними основами. Як неорганічні кислоти можуть бути використані, наприклад, хлористоводнева кислота, сірчана кислота, фосфорна кислота або бромистоводнева кислота; як органічні кислоти, наприклад, карбонові, сульфокислоти або сульфонові кислоти, наприклад, оцтова кислота, винна кислота, молочна кислота, пропіонова кислота, гліколева кислота, малонова кислота, малеїнова кислота, фумарова кислота, дубильна кисло 15 76432 16 та, бурштинова кислота, альгінова кислота, бенбет, а також хронічну демієлінізацію. зойна кислота, 2-феноксибензойна кислота, 2Крім того, сполуки згідно з винаходом можна ацетоксибензойна кислота, корична кислота, мигзастосовувати для терапії інфекційних захворюдалева кислота, лимонна кислота, яблучна кисловань, наприклад, вірусних та паразитарних інфекта, саліцилова кислота, 3-аміносаліцилова кислоцій, наприклад, для лікування малярії, лейшманіота, аскорбінова кислота, ембонова кислота, зу, лихоманки інфекційного походження, болю в нікотинова кислота, ізонікотинова кислота, щавлем'язах інфекційного походження, СНІДу та кахексії. ва кислота, амінокислоти, метансульфокислота, Сполуки згідно з винаходом є інгібіторами фоетансульфокислота, 2-гідроксіетансульфокислота, сфодіестерази 4. етан-1,2-дисульфокислота, бензолсульфокислота, Отже, ці сполуки можна застосувати для інгі4-метилбензолсульфокислота або нафталін-2бування фосфодіестерази 4. сульфокислота. Як неорганічні основи можуть бути Таким чином, предметом цього винаходу є те, використані, наприклад, гідроксид натрію, гідрокщо сполуки формули 1 та їхні солі, а також фарсид калію, аміак, як органічні основи - аміни, примацевтичні препарати, які містять ці сполуки або чому перевага віддається третинним амінам, наїхні солі, можна застосувати для лікування захвоприклад, триметиламін, триетиламін, піридин, Ν,Νрювань, при яких корисним є інгібування фосфодіестерази 4. диметиланілін, хінолін, ізохінолін, -піколін, Отже, сполуки згідно з цим винаходом можна піколін, -піколін, хінальдин або піримідин. застосовувати як бронхорозширювачі та для проКрім того, фізіологічно толерантні солі сполук філактики астми. Крім того, сполуки формули 1 є формули 1 можна одержати шляхом перетворення інгібіторами нагромадження еозинофілів, а також відомим способом похідних, які містять третинні їхньої активності. Таким чином, сполуки згідно з аміногрупи, у четвертинні амонієві солі дією відповинаходом можна застосовувати також при захвовідних агентів. Такими агентами можуть бути галорюваннях, в яких певну роль відіграють еозинофіїдні алкіли, наприклад, метилйодид, етилбромід та ли. До таких захворювань належать, наприклад, н-пропілхлорид, а також галоїдні арилалкіли, назапальні захворювання дихальних шляхів, наприприклад, бензилхлорид або 2-фенілетилбромід. клад, бронхіальна астма, алергічний риніт, алергіКрім того, цей винахід стосується D-форм, Lчний кон'юнктивіт, атопічний дерматит, екзема, форм та D,L-сумішей сполук формули 1, які місалергічний ангіїт, опосередковані еозинофілами тять асиметричний атом вуглецю, а також, в разі запалення, наприклад, еозинофільний фасцит, наявності кількох асиметричних вуглецевих атоеозинофільна пневмонія та синдром PIE (легенева мів, діастереомерних форм. Ті сполуки формули 1, інфільтрація з еозинофілією), уртикарія, виразкоякі містять асиметричні атоми вуглецю й одержувий коліт, хвороба Крона та проліферативні захвоються, як правило, у формі рацемічних сумішей, рювання шкіри, наприклад, псоріаз або кератоз. можна розділити на оптично активні ізомери відоПредметом цього винаходу є те, що сполуки мими способами, наприклад, із застосуванням формули 1 та їхні солі можуть інгібувати як вивільоптично активної кислоти. Можливо також із самонення TNF in vitro, так і індуковану ліпополісахаго початку синтезу використовувати оптично актиридами легеневу інфільтрацію нейтрофілів у павну вихідну речовину, при цьому кінцевий продукт цюків in vivo. Сукупність цих виявлених утворюється у формі відповідної оптично активної фармакологічно важливих властивостей підтверабо діастереомерної сполуки. джує, що сполуки формули 1 та їхні солі, а також У сполук згідно з винаходом виявлено фармафармацевтичні препарати, які містять ці сполуки кологічно важливі властивості, які можна викорисабо їхні солі, можна терапевтично застосувати для тати з терапевтичною метою. лікування хронічних обструктивних захворювань Сполуки згідно з винаходом є інгібіторами вилегенів. вільнення TNF . Крім того, сполуки згідно з цим винаходом маОтже, ці сполуки можна застосувати для інгіють нейропротекторні властивості і можуть бути бування вивільнення TNF . застосовані для лікування захворювань, при яких Таким чином, предметом цього винаходу є те, корисною є нейропротекція. До таких захворювань що сполуки формули 1 та їхні солі, а також фарналежать, наприклад, сенільна деменція (хвороба мацевтичні препарати, які містять ці сполуки або Альцгеймера), втрата пам'яті, хвороба Паркінсона, їхні солі, можна застосувати для лікування захводепресії, напади (удари) та переміжна кульгавість. рювань, при яких корисним є інгібування TNF . Іншими можливостями застосування сполук До таких захворювань належать, наприклад, згідно з винаходом є профілактика та лікування запалення суглобів, в тому числі артрит та ревмазахворювань простати, наприклад, доброякісного тоїдний артрит, а також інші захворювання типу розростання простати, частого сечовипускання, артритів, наприклад, ревматоїдний спондиліт та нічної поліурії, а також лікування нетримання сечі, остеоартрит. Подальшими можливостями застоколік, спричинених каменями в сечовому міхурі, та сування є лікування пацієнтів, які страждають на статевих дисфункцій у чоловіків та жінок. остеопороз, сепсис, септичний шок, грамНарешті, сполуки згідно з винаходом можна негативний сепсис, синдром токсичного шоку, синзастосовувати також для інгібування виникнення дром дихальної недостатності, астму або інші хрозалежності від лікарських засобів при систематичнічні легеневі захворювання, резорбцію кісток або ному вживанні аналгетиків, наприклад, морфіну, а реакцію відторгнення трансплантата або на інші також для обмеження розвитку звикання до цих автоімунні захворювання, наприклад, системний аналгетиків при їх систематичному вживанні. червоний вовчак, розсіяний склероз, гломерулоДля виготовлення лікарських засобів, крім нефрит та увеїт, інсулінозалежний цукровий діа 17 76432 18 звичайних допоміжних речовин, носіїв та домішок, лінолевої, елаїдинової, брасидинової, ерукової використовують ефективну дозу сполуки згідно з або олеїнової кислот з одно-, дво- або триатомницим винаходом. ми спиртами з кількістю вуглецевих атомів від 1 до Доза активної речовини може варіювати зале6, наприклад, метанолом, етанолом, пропанолом, жно від шляху введення в організм, віку та маси бутанолом, пентанолом або їхніми ізомерами, глітіла пацієнта, виду та тяжкості захворювання, що колем або гліцерином. Такими складними ефірами підлягає лікуванню, та аналогічних чинників. жирних кислот є, наприклад, комерційно доступні Добову дозу можна вводити в організм у формігліоли (Miglyols), ізопропілміристат, ізопропілпамі однієї дози, що вводиться одноразово, або дільмітат, ізопропілстеарат, ПЕГ-6-капринова кислолити на дві або більше доз; добова доза станота, складний ефір каприлової та капринової кислот вить, як правило, від 0,001мг до 100мг. із насиченими жирними спиртами, поліоксіетиленСеред способів уведення в організм перевага гліцеринтриолеат, етилолеат, воскоподібні складні віддається пероральним, парентеральним, внутефіри жирних кислот, наприклад, штучний жир рішньовенним, черезшкірним, місцевим, інгаляційкуприкової залози качок, ізопропіловий ефір жирним та назальним способам і відповідним лікарсьних кислот кокосової олії, олеїловий ефір олеїноким формам. вої кислоти, децилолеат, етиловий ефір молочної Для застосування придатні звичайні форми кислоти, дибутифталат, діізопропіладипінат, склафармацевтичних препаратів, наприклад, таблетки, дний ефір поліолів із жирними кислотами тощо. таблетки, вкриті оболонкою, капсули, порошки для Придатні також силіконові масла різної в'язкості диспергування, грануляти, водні розчини, водні або жирні спирти, наприклад, ізотридециловий або масляні суспензії, сиропи, еліксири або краплі. спирт, 2-октилдодеканол, цетилстеариловий спирт Тверді лікарські форми можуть містити інертні або олеїловий спирт; жирні кислоти, наприклад, наповнювачі та носії, наприклад, карбонат кальолеїнова кислота. Крім того, можуть застосовувацію, фосфат кальцію, фосфат натрію, лактозу, тися рослинні олії, наприклад, рицинова олія, мигкрохмаль, маніт, альгінати, желатин, гуарову кадалева олія, оливкова олія, кунжутна олія, бавовмедь, стеарат магнію або алюмінію, метилцелюняна олія, арахісова олія або соєва олія. лозу, тальк, високодисперсну кремнієву кислоту, Як розчинники, гелеутворювачі та солюбілізасиліконове масло, високомолекулярні жирні кислотори можуть бути застосовані вода або розчиннити (наприклад, стеаринову кислоту), агар-агар, ки, що змішуються з водою. Придатними є, наприрослинні або тваринні жири й олії, тверді висококлад, спирти, наприклад, етанол або ізопропіловий молекулярні полімери (наприклад, поліетиленгліспирт, бензиловий спирт, 2-октилдодеканол, поліколь); препарати для перорального застосування етиленгліколі, фталати, адипінати, пропіленгліможуть в разі потреби містити додаткові смакові коль, гліцерин, ди- або трипропіленгліколь, воски, домішки та/або підсолоджувачі. метилцелозольв, целозольв, складні ефіри, морРідкі лікарські форми можуть бути стерилізофоліни, діоксан, диметил сульфоксид, диметилваними та/або містити факультативні допоміжні формамід, тетрагідрофуран, циклогексанон тощо. речовини, наприклад, консерванти, стабілізатори, Як плівкотвірні агенти можуть бути застосовані змочувальні агенти, пенетранти, емульгатори, прості ефіри целюлози, які розчиняються або наагенти, що сприяють розтіканню, солюбілізатори, бухають як у воді, так і в органічних розчинниках, солі, цукри або цукроспирти для регулювання оснаприклад, гідроксипропілметилцелюлоза, метилмотичного тиску або для буферного ефекту, целюлоза, етилцелюлоза або розчинні крохмалі. та/або регулятори в'язкості. Можливі також змішані форми геле- та плівкоДо таких домішок належать, наприклад, тарттвірних агентів. В цьому разі можуть бути застосоратні та цитратні буфери, етанол, комплексотвірні вані, насамперед, іонні макромолекули, наприречовини (наприклад, етилендіамінтетраоцтова клад, натрієва сіль карбоксиметилцелюлози, кислота та її нетоксичні солі). Для регулювання поліакрилова кислота, поліметакрилова кислота та в'язкості можуть використовуватися високомолеїхні солі, натрієвий амілопектиннапівгліколят, алькулярні полімери, такі як рідкий поліетиленоксид, гінова кислота або пропіленглікольальгінат у формікрокристалічні целюлози, такі як карбоксиметилмі натрієвої солі, гуміарабік, ксантанова камедь, целюлози, полівінілпіролідони, декстрани або жегуарова камедь або караген. латини. До твердих носіїв належать, наприклад, Як додаткові допоміжні речовини в композицірізновиди крохмалю, лактоза, маніт, метилцелюях можуть бути застосовані: гліцерин, парафіни лоза, тальк, високодисперсні кремнієві кислоти, різної в'язкості, триетаноламін, колаген, алантоїн, високомолекулярні жирні кислоти (наприклад, стеновантизолова кислота. При виготовленні компоаринова кислота), желатин, агар-агар, фосфат зицій може виявитися необхідним також застосукальцію, стеарат магнію, рослинні та тваринні живання поверхнево-активних речовин, емульгаторів ри, тверді високомолекулярні полімери, такі як або змочувальних агентів, прикладами яких є лауполіетиленгліколь. рилсульфат натрію, сульфати простих ефірів жирМасляні суспензії для парентерального або них спиртів, динатрій-N-лаурил- місцевого застосування можуть містити рослинні, імінодипропіонат, поліоксіетилована рицинова олія синтетичні або напівсинтетичні масла, такі як рідкі або сорбітан-моноолеат, сорбітан-моностеарат, складні ефіри жирних кислот із кількістю вуглецеполісорбати (наприклад, твін), цетиловий спирт, вих атомів у ланцюгу жирної кислоти від 8 до 22, лецитин, гліцеринмоностеарат, поліоксіетиленстетакі як складні ефіри пальмітинової, лауринової, арат, простий ефір полігліколю з алкіл фенолами, тридецилової, маргаринової, стеаринової, арахіхлорид цетилтриметиламонію або солі моноетанової, міристинової, бегенової, пентадецилової, ноламіну з моно/діалкілполігліколевими простими 19 76432 20 ефірами ортофосфорної кислоти. Для одержання композицій з бажаними властивостями можуть виявитися необхідними також стабілізатори, наприклад, монтморилоніт або колоїдні різновиди кремнієвої кислоти, для стабілізації емульсій, або антиоксиданти, наприклад, токоферол або бутилгідроксіанізол, для запобігання розкладу активних речовин, або консерванти, наприклад, складні ефіри п-гідроксибензойної кислоти. З виділених хлорангідридів 7-азаіндол-3Препарати для парентерального застосування карбонових кислот формули 3 потім одержують можуть виготовлятися у окремих дозованих одисполуки загальної формули 1 згідно з винаходом із ничних формах, наприклад, в ампулах або пляшевищезгаданими значеннями R1, R2, R3 та n=1 шлячках. Переважно використовуються розчини актихом реакції з первинним або вторинним аміном. вних речовин, краще водні розчини, найкраще Реакцію доцільно виконувати у присутності допоізотонічні розчини, а також суспензії. Ці ін'єкційні міжної основи. Як допоміжну основу можна застолікарські форми можуть виготовлятися як готові совувати надлишок аміну, використовуваного як препарати або постачатися у формі активної ререагент, третинний амін, у варіанті, якому віддачовини, наприклад, ліофілізату, в разі потреби з ється перевага, піридин або триетиламін, а також додатковими твердими носіями, який безпосереднеорганічні основи, у варіанті, якому віддається ньо перед уведенням змішують із бажаним розперевага, гідроксиди лужних металів або гідриди чинником або суспендувальною речовиною. лужних металів. Назальні композиції можуть мати форму водЗгідно з цим винаходом, сполуки загальної них або масляних розчинів або водних або масляформули 1 із вищезгаданими значеннями R1, R2, них суспензій. Вони можуть постачатися також у R3 та n=2 формі ліофілізатів, які перед застосуванням змішують із відповідним розчинником або суспендувальною речовиною. Виготовлення, фасування та герметизацію препаратів виконують у звичайних стерильних та асептичних умовах. Крім того, цей винахід стосується способу одержання сполук згідно з винаходом. Згідно з цим винаходом, сполуки загальної формули 1 із вищезгаданими значеннями R1, R2, R3 та n=1 одержують шляхом перетворення 7-азаіндолів формули 4 із тими ж значеннями R1 одержують шляхом перетворення 7-азаіндол3-карбонових кислот формули 2 із тими ж значеннями R1 відомим способом із використанням хлорангідридів кислот, у варіанті, якому віддається перевага, тіонілхлориду або оксалілхлориду, спочатку в аналогічні хлорангідриди 7-азаіндол-3-карбонових кислот формули 3 відомим способом шляхом ацилювання оксалілхлоридом спочатку в аналогічні хлорангідриди 7-азаіндол-3-ілгліоксилових кислот формули 5 З виділених хлорангідридів 7-азаіндол-3ілгліоксилових кислот формули 5 потім одержують сполуки загальної формули 1 згідно з винаходом із вищезгаданими значеннями R1, R2, R3 та n=2 шляхом реакції з первинним або вторинним аміном. Реакцію доцільно виконувати у присутності допоміжної основи. Як допоміжну основу можна застосовувати надлишок аміну, використовуваного як реагент, третинний амін, у варіанті, якому відда 21 76432 22 ється перевага, піридин або триетиламін, а також 1,14г гідриду натрію (60%-ного) суспендують в неорганічні основи, у варіанті, якому віддається 21мл ТГФ. При перемішуванні додають крапля за перевага, гідроксиди лужних металів або гідриди краплею при температурі приблизно 10°С розчин лужних металів. 0,93г 4-амінометилпіридину (8,6ммоль) у 21мл Приклади здійснення винаходу ТГФ. Приблизно через 15хв до реакційної суміші Приклади способу одержання сполук формули додають крапля за краплею вищезазначений роз1 згідно з винаходом, де n=1: чин хлорангідриду 1-циклопропілметил-7-азаіндолПриклад 1: Амід N-(4-піридилметил)-13-карбонової кислоти. Нагрівають одержану суміш циклопропілметил-7-азаіндол-3-карбонової кисіз зворотним холодильником протягом 3год. Після лоти охолодження додають до суміші 36мл етилацетату 1,87г 1-циклопропілметил-7-азаіндол-3та 36мл води. Розділяють фази і промивають оркарбонової кислоти (8,6ммоль) суспендують в ганічну фазу водою. Видаляють розчинник дисти15мл дихлорметану. При охолодженні водою доляцією і перекристалізовують залишок з етанолу. дають 1,8мл оксалілхлориду (17,4ммоль). ПереВихід: 1,3г (50% теоретичного). мішують реакційну суміш протягом 8год. При цьоТемпература плавлення: 187-189°С. му кристалізується й випадає в осад хлорангідрид Із застосуванням вищеописаного способу син1-циклопропілметил-7-азаіндол-3-карбонової кистезу можна одержати численні інші сполуки форлоти. Продукт відділяють і розчиняють в 18мл тетмули 1 із n=1; деякі з них наведено нижче як прикрагідрофурану (ТГФ). лади: Приклад 1 2 3 4 5 6 7 8 9 10 11 R1 циклопропілметилізобутилн-гексилциклопропілметил4-фторбензил4-фторбензил4-метоксибензил4-хлорбензил4-фторбензил2-метилпропен-3-іл4-піридилметил -NR2R3 4-піридилметил-аміно3,5-дихлор-4-піридиламіно3,5-дихлор-4-піридиламіно3,5-дихлор-4-піридиламіно4-піридилметил-аміно3,5-дихлор-4-піридиламіно3,5-дихлор-4-піридиламіно4-піридиламіноМорфоліно2,6-дихлорфеніл-аміно3,5-дихлор-4-піридиламіно n 1 1 1 1 1 1 1 1 1 1 1 Т.пл., °С*) 187-189 етанол 168-170 етанол 136-137 метанол 186-187 етанол 189-191 етанол 232-233 етанол 193-195 етанол 192-194 метанол 182-184 етанол 171-174 етанол 190-192 метанол *) Указано розчинник, застосований для перекристалізації Приклади способу одержання сполук формули 1 згідно з винаходом, де n=2: Приклад 12 Амід N-(3,5-дихлорпіридин-4-іл)-[1-(3метоксибензил)-7-азаіндол-3-іл]-гліоксилової кислоти 3,57г 1-(3-метоксибензил)-7-азаіндолу (15ммоль) розчиняють в 50мл третбутилметилового простого ефіру. При температурі 0°С додають крапля за краплею при перемішуванні розчин 1,54г оксалілхлориду (18ммоль) в 10мл трет-бутилметилового простого ефіру. Після цього суміш нагрівають із зворотним холодильником протягом 2год, а потім видаляють розчинник дистиляцією у вакуумі. Одержують хлорангідрид 1-(3метоксибензил)-7-азаіндол-3-ілгліоксилової кислоти у формі твердого залишку, який суспендують у 50мл тетрагідрофурану (ТГФ). До суспензії 2г гідриду натрію в 20мл ТГФ додають крапля за краплею при температурі -5°С розчин 2,4г 4-аміно-3,5-дихлорпіридину (15ммоль) у 30мл ТГФ. Після цього суміш витримують протягом 1год при 20°С при перемішуванні. Потім крапля за краплею додають вищезазначену суспензію хлорангідриду 1-(3-метоксибензил)-7-азаіндол-3ілгліоксилової кислоти при температурі приблизно 0°С. Нагрівають одержану суміш із зворотним холодильником протягом 4год. Видаляють розчинник у вакуумі. Залишок розмішують із 50мл етилацетату та 50мл води. Розділяють фази і промивають органічну фазу водою. Видаляють розчинник дистиляцією у вакуумі і перекристалізують залишок з ізопропанолу. Вихід: 3,5г (51,5% теоретичного). Температура плавлення: 165-167°С. Із застосуванням вищеописаного способу синтезу можна одержати численні інші сполуки формули 1 із n=2; деякі з них наведено нижче як приклади: 23 76432 24 ється in vivo, наприклад, інгібуванням астматичної реакції пізньої фази (еозинофіли), а також впливом на індуковану алергеном проникність судин в активно сенсибілізованих пацюків лінії BrownNorway. Інгібування фосфодіестераз Активність PDE4 визначають у препаратах ензиму з поліморфно-ядерних лімфоцитів (PMNL) людини, активність PDE2, 3 і 5 - із застосуванням PDE із тромбоцитів людини. Запобігали згортанню людської крові за допомогою цитрату. Шляхом центрифугування при 700 g протягом 20хв при кімнатній температурі відділяли збагачену тромбоцитами плазму (надосадову рідину) від еритроцитів та лейкоцитів. Тромбоцити руйнували обробкою ультразвуком і застосовували для визначення PDE3 та PDE5. Для визначення активності PDE2 цитозольну фракцію тромбоцитів очищали пропусканням через аніонообмінну колонку з елююванням градієнтом NaCl і відбирали для випробування фракцію (пік) PDE 2. PMNL для визначення PDE4 виділяли шляхом наступного осадження декстраном, після якого виконували градієнтним центрифугуванням із застосуванням Ficoll-Paque. Після дворазового промивання клітин залишкові еритроцити руйнували шляхом додавання 10мл гіпотонічного буфера (155мМ NH4Cl, 10мМ NaHCO3, 0,1мМ ЕДТА, рН=7,4) протягом 6хв при 4°С. PMNL, які ще залишалися непошкодженими, промивали ще двічі сольовим розчином із фосфатним буфером (PBS) і руйнували ультразвуком. Надосадова рідина після центрифугування протягом 1год при 48000 g при температурі 4°С містила цитозольну фракцію PDE4 і застосовувалася для вимірювання кількості PDE4. Активність фосфодіестераз визначали за модифікованою методикою, описаною Томпсоном та іншими [WJ. Thompson, Μ. Μ. Appleman, Assay of cyclic nucleotide phosphodiesterase and resolution of multiple molecular forms of the enzyme, Adv. Cycl. Nucl. Res. 1979, 10, 69-92]. Реакційні суміші містили 50мМ Трис-НСІ (рН 7,4), 5мМ MgCl2, інгібітори у різних концентраціях, відповідні препарати ензимів, а також додаткові компоненти, необхідні для визначення індивідуальних ізоензимів (дивись нижче). Реакцію ініціювали доданням субстрату 0,5мкМ [3Н]-сАМР або [3H]-cGMP (приблизно 6000 відліків за хвилину на пробу). Кінцевий об'єм проб становив 100мл. Випробовувані речовини додавали у формі вихідних розчинів у ДМСО (диметилсульфоксиді). Концентрація ДМСО в реакційній суміші становила 1% (об'єми.). ДМСО в такій концентрації не впливає на активність PDE. Після ініціювання реакції доданням субстрату проби інкубували протягом 30хв при 37°С. Реакцію припиняли нагріванням пробірки із пробою при 110°С протягом 2хв. Проби витримували на льоду протягом додаткових 10хв. Після додання 30мкл 5'-нуклеотидази (мг/мл, одержано із суспензії отрути змії Crotalus adamanteus) інкубували проби протягом 10хв при 37°С. Реакцію *) Указано розчинник, застосований для переприпиняли вміщенням проб у лід, додавали в кожкристалізації ну пробу 400мкл суміші смоли "Дауекс" із водою та Сполуки згідно з цим винаходом є сильними етанолом (1+1+1), ретельно перемішували і знову інгібіторами фосфодіестерази 4 та вивільнення витримували на льоду протягом 15хв. Пробірки із TNF . Їхній терапевтичний потенціал підтверджупробами центрифугували протягом 20хв при 25 76432 26 промивали шляхом кількаразового центрифугу3000 g. Аліквотні частки надосадової рідини об'євання з живильним розчином, пасивно сенсибілімом по 200мкл переносили безпосередньо в посузували доданням людського імуноглобуліну Ε (IgE) дини для підраховування сцинтиляцій. Після доі розводили суспензію клітин до концентрації 2млн. дання 3мл сцинтилятора проводили вимірювання клітин на 1мл середовищем RPMI 1640 (із домішв бета-лічильнику. ками антибіотиків, 10% сироватки плоду корови, Для визначення активності PDE4, 3 та 2 як 2мМ глутаміну та 25мМ HEPES). Цю суспензію субстрат застосовували [3Н]-сАМР, для визначенрозподіляли по 6-лунковому планшету для культиня активності PDE5 - [3H]-cGMP. Показники неспевування клітин (по 1мл у лунку). Клітини попередцифічної активності ензимів вимірювали в присутньо інкубували протягом 30хв із випробовуваними ності 100мкМ роліпраму (Rolipram) при визначенні речовинами в різних кінцевих концентраціях, після PDE4 і в присутності 100мкМ ІВМХ при визначенні PDE3 та 5 і віднімали від одержаних в експеримечого подразнювали для вивільнення TNF доданнтах значень. Інкубаційні суміші у випробуваннях ням анти-IgE (7,2мкг/мл). Максимальне вивільненна PDE3 містили 10мкМ роліпраму для інгібування ня у вказаному живильному середовищі має місце можливої домішки PDE4. Випробування на PDE2 приблизно через 18год. Протягом цього часу клівиконували із застосуванням проби SPA фірми тини інкубували при 37°С в атмосфері 5%-ного "Амершам" (Amersham). Випробування проводили СО2. Відділяли живильне середовище (надосадову у присутності активатора PDE2 (5мкМ cGMP). рідину) шляхом центрифугування (5хв, 4000об/хв) Для сполук згідно з винаходом визначені знаі зберігали при -70°С до визначення цитокіну. Вичення ІС50 стосовно до інгібування фосфодіестезначення TNF у надосадовій рідині виконували рази 4 лежать у межах від 10-9Μ до 10-5М. Селектак званим методом сендвіч-ELISA (варіант імутивність відносно типів PDE2, 3 та 5 має значення ноферментного твердофазного аналізу) (основний коефіцієнта від 100 до 10000. матеріал фірми Pharmingen), який дозволяє виУ поданій нижче таблиці наведено як приклазначати цитокін у концентраціях від 30пг/мл до ди результати випробувань інгібування PDE4 де1000пг/мл. якими сполуками: Клітини, не стимульовані анти-IgE, практично не продукують TNF ; навпаки, стимульовані клітиПриклад Інгібування PDE4, ІС50 (мкмоль/л) ни вивільнюють значні кількості TNF , які можна 1 0,710 зменшити, наприклад, дією інгібіторів PDE4, при цьому ступень зменшення залежить від дози. Зі 2 1,400 значень процента інгібування (вивільнення TNF 12 0,005 клітинами, стимульованими анти-IgE, приймали за 13 0,058 100%) під дією випробовуваних речовин у різних 14 0,004 концентраціях обчислювали значення ІС50 (конце15 0,031 нтрації, що відповідає 50%-ному інгібуванню). 16 0,002 Для сполук згідно з винаходом визначені пока17 0,008 зники ІС50 лежать у межах від 10-7Μ до 10-5Μ. 18 0,031 У поданій нижче таблиці наведено як прикла22 0,002 ди результати випробувань інгібування вивільнен23 0,001 ня TNF деякими сполуками: 24 0,003 25 0,004 Інгібування вивільнення TNF Приклад 26 0,021 Концентрація, мкмоль/л Інгібування, % 27 0,002 14 0,3 92 28 0,003 16 1,0 90 32 0,113 17 1,0 91 37 0,987 27 1,0 91 Інгібування вивільнення TNF із клітин назальних поліпів Процедура випробування в цілому відповідає методиці, описаній Кемпбелом та Буске [А.М. Campbell, J. Bousquet, Anti-allergic activity of Hr blockers, Int. Arch. Allergy Immunol., 1993, 101, 308310]. Вихідним матеріалом були назальні поліпи (матеріал ОР) пацієнтів, яких піддавали хірургічному лікуванню. Тканину промивали середовищем RPMI 1640, а потім обробляли протеазою (2,0мг/мл), колагеназою (1,5мг/мл), гіалуронідазою (0,75мг/мл) і ДНКазою (0,05мг/мл) протягом 2год при 37°С (1г тканини на 4мл RPMI 1640 з ензимами). Одержані клітини, що являли собою суміш епітеліальних клітин, моноцитів, макрофагів, лімфоцитів, фібробластів та гранулоцитів, відділяли фільтруванням і Інгібування еозинофіли у пізній фазі через 48год після овальбумінової провокації в активно сенсибілізованих пацюків лінії Brown-Norway Інгібування інфільтрації еозинофілів у легенях під впливом сполук згідно з цим винаходом випробовували на активно сенсибілізованих до яєчного альбуміну (OVA) самцях пацюків лінії BrownNorway (маса тіла 200-250г). Сенсибілізацію здійснювали шляхом підшкірного введення кожній тварині суспензії 10мкг OVA разом із 20мг гідроксиду алюмінію як допоміжної речовини в 0,5мл фізіологічного сольового розчину в 1-й, 14-й та 21-й дні досліду. Крім того, тварини одержували в ті ж моменти часу розведену вакцину Bordetella pertussis у кількості 0,25мл для кожної тварини шляхом внутрішньоочеревинної ін'єкції. На 28-й день досліду тварин уміщували поодинці у відкриті плексигла 27 76432 28 сові бокси місткістю 1л, приєднані до приладу для 10мг/кг, р.о. 70 експозиції голови та носа. Тварин піддавали дії 10мг/кг, і.р. 75 17 аерозолю 1%-ної суспензії яєчного альбуміну 10мг/кг, р.о. 32 (провокація алергеном). Аерозоль одержували за 10мг/кг, і.р. 50 27 допомогою розпилювача, що працював на стисне10мг/кг, р.о. 70 ному повітрі під тиском 0,2МПа (фірми Bird Micronebulizer, Palm Springs, CA, USA). Тривалість *) і.р. - внутрішньоочеревинно; р.о. - перораекспозиції була 1год, при цьому нормальних контльно рольних тварин піддавали експозиції аерозолем 0,9%-ного сольового розчину. Інгібування індукованої ліпополісахаридами Через 48год після провокації алергеном роз(LPS) легеневої нейтрофіли у пацюків Льюїса вивалася масована міграція еозинофільних грануІнгібування інфільтрації нейтрофілів у легені лоцитів у легені тварин. В цей момент тварин анепід впливом сполук згідно з цим винаходом випростезували надлишковою дозою етилуретану бовували на самцях пацюків Льюїса (маса тіла (1,5г/кг маси тіла внутрішньоочеревинно) і тричі 250-350г). У день проведення досліду тварин умівиконували бронхоальвеолярне промивання (BAL) щували поодинці у відкриті плексигласові бокси дозами по 4мл збалансованого розчину Хенка. місткістю 1л, приєднані до приладу для експозиції Після цього визначали загальну кількість клітин та голови та носа. Тварин піддавали дії аерозолю кількість еозинофільних гранулоцитів у зібраній суспензії ліпополісахаридів (100мкг LPS/мл 0,1%рідині після BAL за допомогою автоматизованого ного розчину гідроксиламіну) у сольовому розчині приладу для диференціації клітин (Technicon HIE з фосфатним буфером (PBS) (LPS-провокація). фірми Bayer Diagnostics). Для кожної тварини розАерозоль LPS та гідроксиламіну одержували за раховували кількість еозинофілів (EOS) у рідині допомогою розпилювача, що працював на стиснепісля BAL у мільйонах на тварину за формулою ному повітрі під тиском 0,2МПа (фірми Bird EOS/мкл вихід BAL (мл) = EOS/тварину. Micronebulizer, Palm Springs, CA, USA). Тривалість При кожному випробуванні використовували експозиції була 40хв, при цьому нормальні контдві контрольні групи (обприскування аерозолем рольні групи піддавали експозиції аерозолем фізіологічного сольового розчину та обприскуван0,1%-ного розчину гідроксиламіну в PBS також ня аерозолем розчину OVA). протягом 40хв. Процент інгібування еозинофілів для дослідної Через 6год після LPS-провокації розвивалася групи тварин, які одержували випробовувані речомаксимальна масована міграція нейтрофільних вини, розраховували за формулою: гранулоцитів у легені тварин. В цей момент тварин {[(OVAC-SC)-(OVAD-SC)]/(OVACанестезували надлишковою дозою етилуретану SC)} 100%=% інгібування (1,5г/кг маси тіла внутрішньоочеревинно) і тричі (SC - показник для контрольної групи, обробвиконували бронхоальвеолярне промивання (BAL) леної носієм і провокованої 0,9%-ним сольовим дозами по 4мл збалансованого розчину Хенка. розчином; OVAC - показник для контрольної групи, Після цього визначали загальну кількість клітин та обробленої носієм і провокованої 1%-ною суспенкількість нейтрофільних гранулоцитів у зібраній зією яєчного альбуміну; OVAD - показник для досрідині після BAL за допомогою автоматизованого лідної групи, обробленої випробовуваною речовиприладу для диференціації клітин (Technicon HIE ною і провокованої 1%-ною суспензією яєчного фірми Bayer Diagnostics). Для кожної тварини обальбуміну). числювали кількість нейтрофілів (NEUTRO) у рідиВипробовувані речовини вводили в організм ні після BAL у мільйонах на тварину за формулою тварин внутрішньоочеревинно або перорально у NEUTRO/мкл вихід BAL (мл) = NEUTRO/тварину. формі суспензії в 10% поліетиленгліколю-300 та При кожному випробуванні використовували 5% 5-гідроксіетилцелюлози за 2год до провокації дві контрольні групи (обприскування аерозолем алергеном. Контрольні групи одержували носій за 0,1%-ного розчину гідроксиламіну в PBS та обпритим же способом уведення. скування аерозолем розчину 100мкг LPS/мл 0,1%Сполуки згідно з винаходом інгібують еозиноного розчину гідроксиламіну в PBS). філію пізньої фази після внутрішньоочеревинного Процент інгібування нейтрофілів для дослідної введення в дозі 10мг/кг на 30-100% і після перорагрупи тварин, які одержували випробовувані речольного введення в дозі 30мг/кг на 30-75%. вини, розраховували за формулою: Таким чином, сполуки згідно з винаходом осо{[(LPSC-SC)-(LPSD-SC)]/(LPSC-SC)} 100%=% бливо придатні для виготовлення лікарських засоінгібування бів для лікування захворювань, які пов'язані із (SC - показник для контрольної групи, обробвпливом еозинофілів. леної носієм і провокованої 0,1%-ним розчином У поданій нижче таблиці наведено як приклагідроксиламіну; LPSC - показник для контрольної ди результати випробувань інгібування еозинофігрупи, обробленої носієм і провокованої LPS лії деякими сполуками: (100мкг/мл 0,1%-ного розчину гідроксиламіну); LPSD - показник для дослідної групи, обробленої Інгібування еозинофілії випробовуваною речовиною і провокованої LPS Приклад Доза/спосіб введення*) Інгібування, % (100мкг/мл 0,1%-ного розчину гідроксиламіну)). 10мг/кг, і.р. 62 Випробовувані речовини вводили в організм 14 10мг/кг, р.о. 59 тварин перорально у формі суспензії в 10% поліе16 10мг/кг, і.р. 100 тиленгліколю-300 та 5% 5-гідроксіетилцелюлози за 29 76432 30 2год до LPS-провокації. Контрольні групи одержували носій за тим же способом уведення. Інгібування нейтрофілії Приклад Сполуки згідно з винаходом інгібують нейтроДоза/спосіб введення*) Інгібування, % філію після перорального введення в дозі 1мг/кг 14 1мг/кг, р.о. 80 на 40-90% і, таким чином, є особливо придатними 22 1мг/кг, р.о. 64 для виготовлення лікарських засобів для лікування 27 1мг/кг, р.о. 52 захворювань, які пов'язані із впливом нейтрофілів. У поданій нижче таблиці наведено як прикла*) р.о. - перорально ди результати випробувань інгібування нейтpофілії деякими сполуками: Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською7-azaindoles, the use thereof as phosphodiesterase 4 inhibitors and a method for producing the same
Автори англійськоюEgerland, Ute, Marx Degenhard, KUSS HILDEGARD
Назва патенту російською7-азаиндолы, их применение как ингибиторов фосфодиэстеразы 4 и способ их получения
Автори російськоюМаркс Дегенхард, Кусс Хильдегард
МПК / Мітки
МПК: C07D 471/04, A61K 31/40, A61P 11/00
Мітки: інгібіторів, спосіб, фосфодіестерази, 7-азаіндоли, застосування, одержання
Код посилання
<a href="https://ua.patents.su/15-76432-7-azaindoli-kh-zastosuvannya-yak-ingibitoriv-fosfodiesterazi-4-ta-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">7-азаіндоли, їх застосування як інгібіторів фосфодіестерази 4 та спосіб їх одержання</a>
Попередній патент: Спосіб струминного здрібнювання матеріалів
Наступний патент: Охолоджувальна батарея для шахтних печей
Випадковий патент: Полімерна композиція












